Películas nanotubas de TiO2 sensibilizadas Bi2Se3 para proteção catódica fotogerada de aço inoxidável 304 sob luz visível
Resumo
Dióxido de titânio (TiO 2 ) arranjos de nanotubos acoplados a um semicondutor de gap estreito - seleneto de bismuto (Bi 2 Se 3 ) - aprimoramento notável exibido na propriedade de proteção fotocatódica para aço inoxidável 304 sob luz visível. Bi 2 Se 3 / TiO 2 nanocompósitos foram sintetizados com sucesso usando um método simples de duas etapas, incluindo um método de anodização eletroquímica para a preparação de TiO puro 2 e um método de deposição em banho químico para sintetizar Bi 2 Se 3 nanoflores. A morfologia e a estrutura dos filmes compostos foram estudadas por microscopia eletrônica de varredura, espectroscopia de dispersão de energia, espectroscopia de fotoelétrons de raios-X e difração de raios-X. Além disso, a influência do Bi 2 Se 3 o conteúdo sobre as propriedades fotoeletroquímicas e de proteção fotocatódica dos filmes compostos também foi estudado. A densidade de fotocorrente do Bi 2 Se 3 / TiO 2 nanocompósitos era significativamente maior do que o TiO puro 2 sob luz visível. O sensibilizador Bi 2 Se 3 melhorou a separação eficiente dos pares elétron-buraco fotogerados e as propriedades de proteção fotocatódica do TiO 2 . Sob iluminação de luz visível, Bi 2 Se 3 / TiO 2 nanocompósitos sintetizados pelo método de deposição em banho químico com Bi 3+ (0,5 mmol / L) exibiu o desempenho ideal de proteção catódica fotogerada para aço inoxidável 304.
Histórico
Como importantes materiais de engenharia, os aços inoxidáveis têm sido amplamente aplicados em projetos significativos em vários campos devido à sua excelente resistência à corrosão. No entanto, os aços inoxidáveis podem sofrer corrosão grave quando usados em ambientes agressivos específicos, como ambientes ácidos, bem como sob condições contendo cloreto ou de alta temperatura [1,2,3,4]. Extensas pesquisas e aplicações do método anticorrosivo tradicional, incluindo revestimentos [5, 6], uso de um ânodo de sacrifício [7] e proteção catódica de corrente impressa [8, 9], foram desenvolvidas durante as últimas décadas. No entanto, a tecnologia anticorrosiva ecologicamente correta e de longa duração ainda continua sendo um objetivo principal. Como uma nova tecnologia anticorrosiva, a proteção fotocatódica foi proposta pela primeira vez por Yuan e Tsujikawa em 1995 [10] antes de receber a atenção dos pesquisadores de corrosão [11,12,13,14].
Dióxido de titânio (TiO 2 ) é um importante material fotoelétrico com boa conversão fotoelétrica e propriedades de fotocatálise e é amplamente utilizado em catalisadores [15], células solares [16] e sensores de gás [17] devido ao seu baixo custo, não toxicidade e propriedades químicas estáveis. TiO 2 e TiO 2 Compósitos à base de fotogeração são usados para proteção catódica fotogerada:uma técnica promissora para prevenção de corrosão que sofreu um rápido desenvolvimento nos últimos anos [18,19,20,21,22,23]. No entanto, o bandgap (3,2 eV) do TiO 2 restringe a fotorresposta apenas à região ultravioleta, o que diminui significativamente a taxa de utilização da energia solar. Além disso, portadores de carga induzida por foto em TiO vazio 2 nanopartículas mostram uma vida útil muito curta devido à rápida recombinação de pares de elétron-buraco fotoexcitados, o que reduz o efeito de proteção fotocatódica do TiO puro 2 filmes. Assim, como superar as deficiências acima do TiO 2 tornou-se um tópico amplamente estudado. Muitos estudos foram conduzidos sobre a composição de TiO 2 com elementos não metálicos (F, N e S) [12, 24, 25], átomos de metal (Fe, Co, Cu e Ce) [26,27,28,29] e alguns nano-semicondutores de bandgap estreito (Ag 2 O, ZnSe, WO 3 , CdS, Ag 2 S, CdSe e Bi 2 S 3 ) [30,31,32,33,34,35,36] para melhorar a separação do portador e a utilização da luz de TiO 2 .
Seleneto de bismuto (Bi 2 Se 3 ) é um semicondutor em camadas de bandgap direto e membro importante da V 2 VI 3 família composta. Ele tem um alto coeficiente de absorção nas regiões de luz visível e infravermelho próximo com um estreito bandgap (0,35 eV) [37]. Como um importante calcogeneto de tipo n, Bi 2 Se 3 possui muitas características importantes, como alta condutividade elétrica [38], propriedade termoelétrica apreciável [39], fotossensibilidade [40], propriedade eletroquímica [41] e fotocondutividade [42]. Além disso, Bi 2 Se 3 é um isolante topológico popular [43,44,45] e tem a propriedade única de estados superficiais condutores e estados volumosos isolados. Bi 2 de alta qualidade Se 3 nanoestruturas foram preparadas usando um método de deposição física de alto vácuo, deposição de vapor químico, deposição de camada atômica, deposição de laser pulsado e uma técnica de vapor-líquido-sólido em alta temperatura [44,45,46,47,48,49]. Esses métodos sintéticos para Bi 2 Se 3 requerem uma fabricação difícil, levando a um alto custo de produção. Neste artigo, os problemas acima são superados pelo emprego de um método de deposição em banho químico simples e de baixo custo para Bi 2 Se 3 deposição de nanoflores em TiO 2 . A combinação de um n-Bi 2 Se 3 / n-TiO 2 heterojunção como um fotoanodo eficiente foi aplicada à proteção catódica fotogerada de 304ss pela primeira vez. A morfologia, estrutura e propriedade de absorção óptica de Bi 2 Se 3 / TiO 2 nanocompósitos foram estudados por microscopia eletrônica de varredura (SEM), difração de raios-X (XRD), espectroscopia de energia dispersiva de raios-X (EDS), espectroscopia de fotoelétrons de raios-X (XPS) e espectros de refletância difusa de UV-visível (UV-Vis) , respectivamente.
Métodos
Todos os produtos químicos usados neste estudo eram de grau analítico e usados como recebidos sem purificação adicional. Todas as soluções aquosas foram preparadas com água desionizada.
Preparação do TiO 2 Filme
Folhas de Ti (20 mm × 10 mm × 0,3 mm;> 99,9% de pureza) foram polidas usando uma mistura contendo NH 4 F (2,25 g), H 2 O (12,5 mL), H 2 O 2 (30% em peso, 30 mL) e HNO 3 (68% em peso, 30 mL) e, em seguida, os pedaços de Ti foram limpos com água desionizada e etanol. TiO 2 filme foi preparado em folha de Ti pelo método de oxidação anódica relatado na literatura [50]. A placa de Pt foi escolhida como o cátodo, e a folha de Ti foi o ânodo a 20 V por 1 h em uma solução de etilenoglicol contendo NH 4 F (0,22 g), H 2 O (4 mL) e etilenoglicol (40 mL) à temperatura ambiente. Em seguida, as amostras foram enxaguadas com água deionizada e etanol. Finalmente, as amostras foram recozidas a 450 ° C por 2 h e resfriadas ao ar ambiente para obter TiO 2 filme.
Síntese de Bi 2 Se 3 no TiO 2 Filme
O Bi 2 Se 3 foi preparado pelo método de deposição em banho químico. No procedimento experimental, 8 mmol de ácido nitrilotriacético (H 3 NTA) e 0,4 mmol de Bi (NO 3 ) 3 · 5H 2 O foram adicionados a água desionizada (400 mL) para formar o quelato de bismuto, com um Bi 3+ concentração de 1,0 mmol / L na solução misturada. Dois milimoles de ácido ascórbico como o reagente de redução foram adicionados à solução acima e, em seguida, hidróxido de amônio foi adicionado com cautela, gota a gota, até que o pH da mistura foi ajustado para aproximadamente 8,6 ~ 8,9 e a solução mista apareceu incolor e transparente. Finalmente, Na 2 SeSO 3 (20 mL, 30 mmol / L) foi injetado na solução acima. Em todas as experiências anteriores, as soluções aquosas foram cuidadosamente agitadas com um agitador magnético para obter uma solução homogénea. Em seguida, um TiO 2 o substrato foi imerso na solução final (40 mL) em um béquer (100 mL). O copo coberto com película aderente foi então transferido para um forno aquecido a uma temperatura de 80 ° C por 200 min para obter o Bi 2 Se 3 nanoflores no TiO 2 substrato. Finalmente, a amostra foi removida do copo e lavada várias vezes com água desionizada e etanol e, em seguida, deixada secar ao ar ambiente. Desta forma, Bi 2 Se 3 -sensibilizado TiO 2 filmes foram obtidos e rotulados com Bi 2 Se 3 / TiO 2 -1,0. Para simplificar, diferentes quantidades de Bi 2 Se 3 no TiO 2 substratos são designados como Bi 2 Se 3 / TiO 2 -γ neste artigo, onde γ denota a concentração de Bi 3+ no H 3 NTA e Bi (NÃO 3 ) 3 · 5H 2 Ó solução. Com as quantidades dos outros reagentes constantes, Bi 2 Se 3 / TiO 2 -0,5 e Bi 2 Se 3 / TiO 2 -0,25 foram obtidos para Bi 3+ concentrações de 0,5 mmol / L e 0,25 mmol / L, respectivamente. A influência de diferentes quantidades de Bi 2 Se 3 sobre as propriedades fotoeletroquímicas e de proteção fotocatódica dos filmes compostos foi investigado neste trabalho.
Morfologia e análise de composição
Microscopia eletrônica de varredura (SEM, Hitachi S-4800, Japão) foi usada para investigar as morfologias dos filmes preparados. Espectroscopia de energia dispersiva de raios-X (EDS, Oxford Energy 350 analisador de espectro de energia de raios-X) e espectroscopia de fotoelétrons de raios-X (XPS, Thermo Scientific ESCALAB 250Xi) foram empregadas para determinar a composição química do Bi 2 Se 3 / TiO 2 nanocompósitos. UV-Vis DRS (Japan Hitachi UH4150) foi usado para determinar a absorbância de luz das amostras. A composição da fase cristalina das amostras foi caracterizada por um difratômetro de raios-X (XRD, Germany Bruker AXSD8) usando Cu K α radiação (γ =1,54056 Å) de 10 ° a 80 °.
Medições fotoeletroquímicas
Como mostrado na Fig. 1, um sistema de acoplamento compreendendo fotólise e células eletrolíticas foi usado para as medições fotoeletroquímicas, e uma membrana de troca de prótons foi usada para ligar as duas células. A célula de fotólise continha 0,1 mol / L Na 2 Solução mista de NaOH S e 0,2 mol / L, que desempenhou o papel de agente sacrificial para promover a separação de elétrons e lacunas [33, 51], enquanto uma solução de NaCl 0,5 mol / L foi usada como eletrólito para a célula eletrolítica. Na célula eletrolítica, foi adotado um sistema de três eletrodos com uma folha de Pt como contra-eletrodo (CE), eletrodo de calomelano saturado como eletrodo de referência (RE) e 304ss como eletrodo de trabalho (WE). Bi 2 Se 3 / TiO 2 amostras nanocompósitos colocadas na célula de fotólise foram conectadas a um eletrodo 304ss imerso na célula eletrolítica por um fio de cobre. A fonte de luz na faixa de luz visível foi irradiada por uma lâmpada de xenônio de alta pressão (PLS-SXE 300 C, Beijing Perfectlight Company, China). As mudanças no potencial de circuito aberto (OCP) e nas curvas de fotocorrente foram medidas usando um potenciostato / galvanostato / sistema ZRA Gamry (GAMRY 3000, Gamry Instruments, EUA) antes e durante a irradiação de luz.
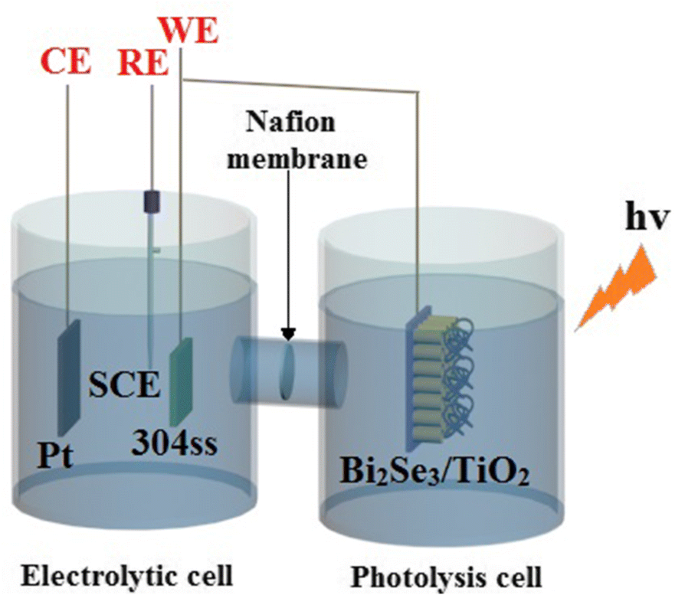
Esboços esquemáticos da configuração experimental usada para análise fotoeletroquímica
Resultados e discussão
Caracterização de TiO2 puro e Bi2Se3 / TiO2
A Figura 2a mostra uma vista superior típica e topografias em corte transversal para TiO 2 filmes preparados pelo método de anodização. O TiO 2 arranjos de nanotubos mostram uma estrutura nanoporosa composta de nanotubos bem ordenados e de alta densidade com um diâmetro interno médio e comprimento de aproximadamente 55 nm e 680 nm, respectivamente. Conforme mostrado na Fig. 2b – d, o TiO 2 as superfícies dos nanotubos foram modificadas com sucesso por Bi 2 Se 3 através do método de deposição em banho químico para diferentes concentrações de Bi 3+ . Para Bi 2 Se 3 / TiO 2 -0,25, o Bi 2 Se 3 nanoflakes foram esporadicamente distribuídos e agregados de forma desigual no TiO 2 nanotubos (Fig. 2b). Quando a concentração de Bi 3+ era 0,5 mmol / L, Bi 2 Se 3 foi composto quase inteiramente de padrões semelhantes a flores de nanoflocos ultrafinos flexíveis com um diâmetro de aproximadamente 800 nm, sem bloquear o bocal do TiO 2 nanotubos ou danificá-los (Fig. 2c). Bi 2 Se 3 nanoflores que foram observadas distribuídas uniformemente na superfície do TiO 2 mostraram uma estrutura interna reticulada para os nanoflocos ultrafinos, o que efetivamente evitou a agregação da lamela e manteve uma vida útil de longa duração das arquiteturas, como mostrado na Fig. 2c. Após a concentração de Bi 3+ foi aumentado para 1,0 mmol / L, a quantidade e o diâmetro do Bi 2 Se 3 nanoflores aumentaram significativamente, e a aglomeração de nanoflores bloqueou os nanotubos, como mostrado na Fig. 2d. O espectro EDS correspondente do Bi 2 Se 3 / TiO 2 Os filmes de -0,5 mostrados na Fig. 2e revelaram que os picos característicos para Ti, O, Bi e Se foram marcados com porcentagens atômicas de Bi e Se de 0,9% e 1,3%, respectivamente. É bem conhecido que o erro de medição do teste EDS aumenta com a diminuição do conteúdo do elemento de teste. Portanto, é aceitável que a razão atômica de Bi e Se seja próxima de 2:3.

Imagens SEM para a TiO puro 2 , b Bi 2 Se 3 / TiO 2 -0,25, c Bi 2 Se 3 / TiO 2 -0,5 e d Bi 2 Se 3 / TiO 2 -1,0; e Espectro EDS para Bi 2 Se 3 / TiO 2 -0,5 filmes
A Figura 3a mostra os espectros de XRD para TiO puro 2 (curva a) e Bi 2 Se 3 / TiO 2 -1,0 nanocompósitos (curva b). Além dos picos do substrato de Ti, os picos de difração a 25,38 °, 38,03 °, 48,01 °, 54,05 °, 55,17 °, 62,71 ° e 70,44 ° foram bem combinados com os planos de rede (101), (004), (200), (105), (211), (204) e (220) de anatase TiO 2 , respectivamente (JCPDS 21-1272). Exceto para o TiO 2 picos, os picos de difração distintos em 29,35 ° e 74,90 ° foram indexados aos planos de rede (015) e (0216) do cristal romboédrico Bi 2 Se 3 (JCPDS 33-0214). No entanto, não há pico óbvio de Bi 2 Se 3 / TiO 2 -1,0 devido ao baixo conteúdo Bi 2 Se 3 depositado no TiO 2 e os espectros de XRD em conformidade com os resultados de SEM e EDS. A espectroscopia de fotoelétrons de raios-X (XPS) foi usada para determinar as composições químicas e os estados do Bi 2 Se 3 / TiO 2 nanocompósitos. Conforme mostrado na Fig. 3b, o XPS revelou a existência de componentes Bi, Se, Ti e O além de contaminantes C devido à contaminação por hidrocarbonetos adventícios. A Figura 3c mostra as posições de pico para Ti 2p em 458,7 e 464,5 eV, indicando que os óxidos de titânio consistiam principalmente em TiO 2 [52]. Conforme ilustrado na Fig. 3d, os semáforos O 1s combinados com dois picos Gaussianos:o máximo na energia de ligação inferior (530,0 eV) foi atribuído ao oxigênio da rede (O L ) em Bi 2 Se 3 / TiO 2 nanocompósitos e o segundo na maior energia de ligação (531,5 eV) foi derivado do oxigênio adsorvido (O A ), incluindo oxigênio de ligação fraca ou grupos hidroxila. A existência de O A foi devido à geração de vacâncias de oxigênio na superfície dos nanocompósitos, o que pode melhorar as propriedades de conversão fotoelétrica de Bi 2 Se 3 / TiO 2 nanocompósitos em proteção fotocatódica [53]. A Figura 3e mostra que o 4f 7/2 pico assimétrico para Bi resolvido em dois picos (157,5 e 159,4 eV), com o Bi 4f 5/2 espectro similarmente dividido em duas bandas em 162,8 e 164,7 eV, respectivamente. As posições dos picos inferiores (157,5 eV e 162,8 eV) estavam de acordo com as de Bi 2 Se 3 , com os picos mais altos correspondendo ao óxido de bismuto em 159,4 eV e 164,7 eV [54, 55]. Pode-se concluir que um punhado de metal bismuto foi oxidado durante o processo de síntese com Bi 2 Se 3 modificar TiO puro 2 . Conforme mostrado na Fig. 3f, os dois picos foram atribuídos ao 3d 3/2 e 3d 5/2 níveis centrais de Se em 55,1 e 54,2 eV, respectivamente, indicando que Se existia na forma de Se 2- [56].
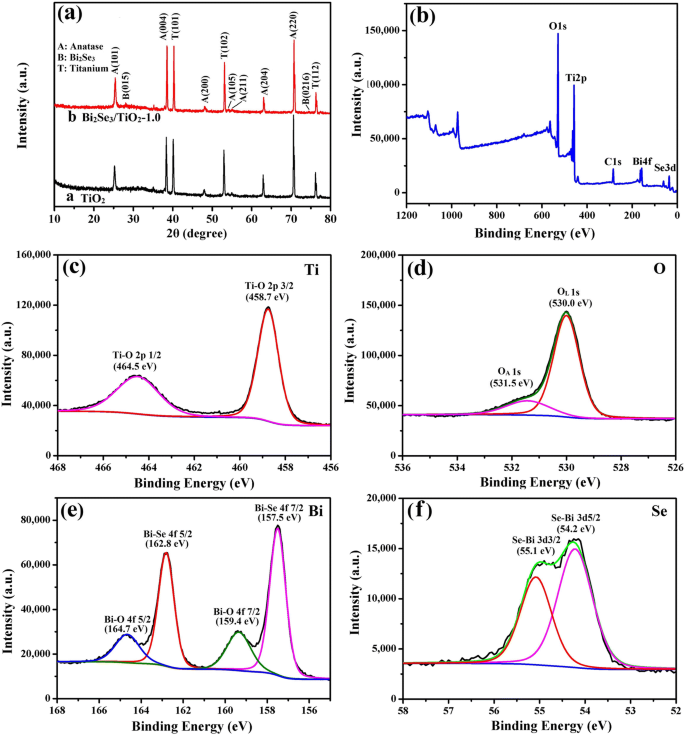
a Padrões de XRD para TiO puro 2 e Bi 2 Se 3 / TiO 2 -1,0 nanocompósitos; b o espectro total da pesquisa, c Ti 2p, d O 1s, e Bi 4f e f Espectro Se 3d XPS para Bi 2 Se 3 / TiO 2 -1,0 nanocompósitos
A Figura 4 mostra as habilidades de absorção de luz do TiO 2 puro e Bi 2 Se 3 / TiO 2 -1,0 nanocompósitos. A borda de absorção característica para TiO puro 2 era de aproximadamente 380 nm dentro da região UV devido ao bandgap de energia de anatase TiO 2 (3,2 eV) (curva a). Adsorção pronunciada foi observada para Bi 2 Se 3 / TiO 2 nanocompósitos na região de luz visível (350-800 nm) (curva b), com habilidades de absorção de luz visível maiores do que aquelas de TiO puro 2 devido à incorporação do Bi 2 Se 3 nanoflower. Este fenômeno pode ser atribuído ao fato de que Bi 2 Se 3 é excitado sob a luz visível devido ao seu estreito bandgap (0,35 eV), com elétrons e buracos produzidos em sua banda de condução (CB) e banda de valência (VB). Portanto, a adição de Bi 2 Se 3 aumenta efetivamente a capacidade de absorção de luz visível de Bi 2 Se 3 / TiO 2 nanocompósitos.
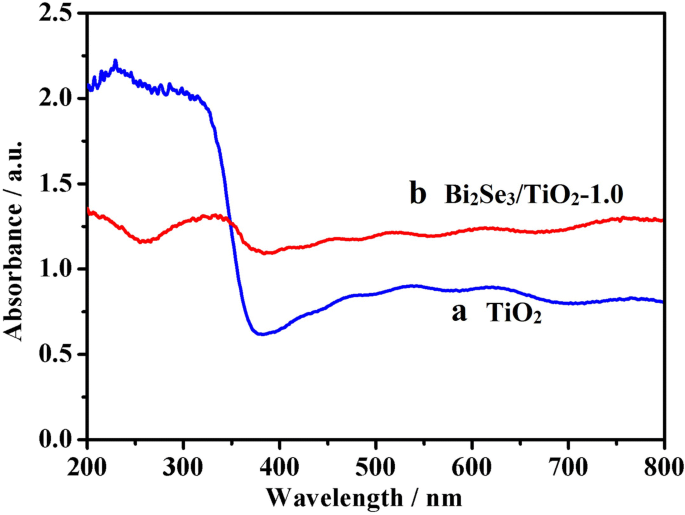
Espectro de absorção UV-visível para TiO 2 (a) e Bi 2 Se 3 / TiO 2 -1,0 (b)
Desempenho da proteção fotocatódica de TiO2 puro e Bi2Se3 / TiO2
Conforme mostrado na Fig. 5, as curvas OCP para 304ss acoplado com TiO puro 2 e Bi 2 Se 3 / TiO 2 fotoanodos nanocompósitos foram medidos sob luz visível intermitente, com a resposta do OCP à iluminação solicitada e alterada para um potencial negativo para todos os eletrodos acoplados. Na fase inicial de luz acesa, o OCP para todos os eletrodos acoplados mostrou um deslocamento negativo em um curto período de tempo, que foi devido à transferência dos fotoelétrons excitados do TiO puro 2 e Bi 2 Se 3 / TiO 2 nanocompósito para o eletrodo 304ss [1, 57]. Posteriormente, os valores de OCP relativamente estáveis podem ser atribuídos à taxa de equilíbrio entre a criação e recombinação dos elétrons fotogerados [32]. Após desligar a irradiação, os valores de OCP para o Bi 2 Se 3 / TiO 2 nanocompósitos voltaram aos seus valores originais em uma velocidade mais lenta em comparação com TiO puro 2 . Este fenômeno pode ser atribuído ao efeito do pool de elétrons de Bi 2 Se 3 / TiO 2 nanocompósitos, que podem armazenar elétrons fotoinduzidos sob irradiação de luz e liberar lentamente esses elétrons sem irradiação de luz. Sob irradiação de luz visível, o valor de OCP para 304ss foi de aproximadamente - 450 mV quando acoplado com TiO 2 (curva a), e os valores de OCP para 304ss juntamente com Bi 2 Se 3 / TiO 2 -0,25 (curva b), Bi 2 Se 3 / TiO 2 -0,5 (curva d) e Bi 2 Se 3 / TiO 2 -1,0 (curva c) atingiu - 905 mV, - 996 mV e - 958 mV, respectivamente. Estes resultados indicaram que 304ss foi catodicamente polarizado uma vez acoplado com Bi 2 Se 3 / TiO 2 nanocompósitos e que uma boa proteção catódica para 304ss pode ser fornecida pelo Bi 2 Se 3 / TiO 2 fotoanodos. Conforme mostrado na Fig. 5 d, o 304ss acoplado a Bi 2 Se 3 / TiO 2 -0,5 possuía potencial mais negativo indicava que o melhor desempenho de proteção fotocatódica para 304ss. Este resultado pode ser porque os locais ativos e a coleta de luz aumentaram com o aumento de Bi 2 Se 3 contente. No entanto, uma quantidade excessiva de Bi 2 Se 3 partículas serviam como locais de recombinação para elétrons e lacunas, o que impedia a transferência de carga do Bi 2 Se 3 / TiO 2 nanocompósitos a 304ss.
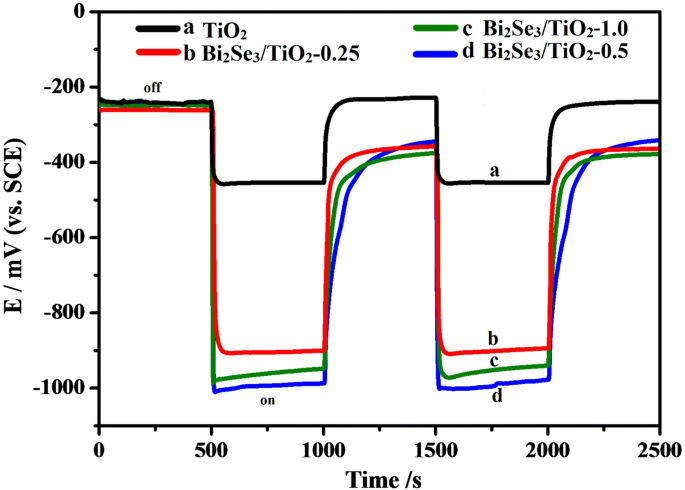
OCP para 304ss acoplado com TiO puro 2 e Bi 2 Se 3 / TiO 2 nanocompósitos em uma solução de NaCl 0,5 mol
Como mostrado na Fig. 6, as curvas de densidade de fotocorrente vs. tempo para TiO 2 e Bi 2 Se 3 / TiO 2 nanocompósitos mostraram uma fotorresposta rápida e reproduzível sob iluminação intermitente de luz visível, o que refletiu o desempenho de conversão fotoelétrica dos materiais. A corrente fotogerada era relativamente pequena sob luz visível devido à fraca absorção de luz visível (curva a). No entanto, a corrente fotogerada aumentou notavelmente sob iluminação de luz visível após a sensibilização de TiO 2 pelo Bi 2 Se 3 nanoflores (curvas b a d). Os dados implicam que o Bi 2 Se 3 / TiO 2 nanocompósitos foram capazes de utilizar luz visível e que a heterojunção entre TiO 2 e Bi 2 Se 3 promoveu a separação de elétrons fotogerados e lacunas [58]. Além disso, os fotoelétrons produzidos na banda de condução do Bi 2 Se 3 nanoflores podem ser facilmente transferidos para a banda de condução mais positiva do TiO 2 nanotubos sob iluminação de luz visível. Após três intervalos de irradiação, a fotocorrente manteve um valor relativamente estável e nenhuma degradação de fotocorrente foi detectada, ilustrando a boa estabilidade fotoquímica do Bi 2 Se 3 / TiO 2 filmes nanocompósitos. Para diferentes concentrações de Bi 3+ , o Bi 2 Se 3 / TiO 2 nanocompósitos apresentaram intensidades diferentes para a resposta da fotocorrente. Em particular, a densidade de fotocorrente transiente para Bi 2 Se 3 / TiO 2 -0,5 (415 μA / cm 2 ) foi maior do que para Bi 2 Se 3 / TiO 2 -0,25 (85 μA / cm 2 ) e Bi 2 Se 3 / TiO 2 -1,0 (160 μA / cm 2 ), indicando que Bi 2 Se 3 / TiO 2 -0,5 possuía uma eficiência de separação ideal para os pares elétron-buraco fotogerados. Os locais ativos e a coleta de luz diminuíram devido à deficiência de Bi 2 Se 3 nanoflores no Bi 2 Se 3 / TiO 2 filmes nanocompósitos, enquanto os locais de recombinação para elétrons e lacunas aumentaram na presença de uma quantidade excessiva de Bi 2 Se 3 nanoflores. Sob iluminação de luz visível, a maior densidade de corrente fotoinduzida do Bi 2 Se 3 / TiO 2 -0,5 fotoanodo foi consistente com as maiores quedas potenciais fotoinduzidas ilustradas na Fig. 5, validando ainda mais o desempenho de proteção fotocatódica ideal de Bi 2 Se 3 / TiO 2 -0,5 para 304ss.
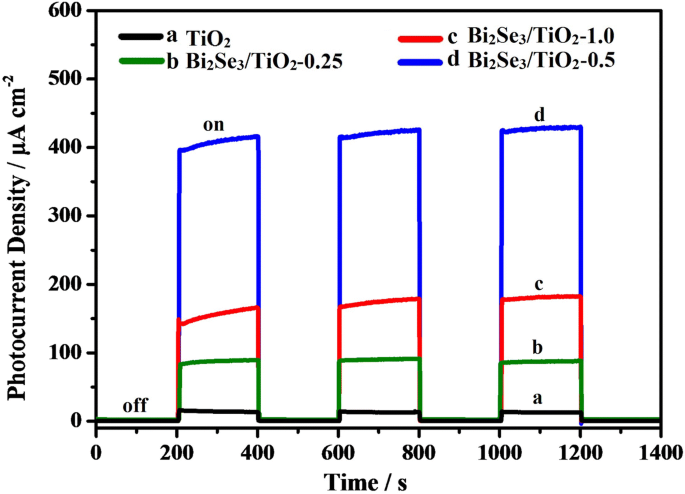
Curvas de densidade x tempo de fotocorrente para TiO puro 2 e Bi 2 Se 3 / TiO 2 nanocompósitos em 0,1 mol / L Na 2 S e solução mista de NaOH 0,2 mol / L
A Figura 7 mostra os processos de conversão e transporte fotoelétricos para o Bi 2 Se 3 / TiO 2 nanocompósitos. Sob luz visível, Bi 2 Se 3 nanoflores podem absorver prontamente fótons, pois contêm oxigênio adsorvido (O A ) e têm uma largura de banda estreita (0,35 eV). Quando os fótons são absorvidos pelo Bi 2 Se 3 nanoflores, elétrons fotoexcitados serão gerados por excitação da banda de valência (VB) de Bi 2 Se 3 para a banda de condução (CB) de Bi 2 Se 3 . Os elétrons fotoexcitados no CB de Bi 2 Se 3 são deslocados para o CB do TiO 2 , enquanto os orifícios fotogerados no VB do TiO 2 são transferidos para o VB de Bi 2 Se 3 , e então são capturados por S 2− no eletrólito para se transformar em S na superfície do filme de fotoanodo. Quando os elétrons fotoexcitados saem do fotoanodo e são transferidos para 304ss, eles vão reagir com o gás oxigênio e a água para converter OH - . Além disso, Na + é transportado da célula eletrolítica para a célula de fotólise pela membrana de troca de prótons, de modo que o sistema de acoplamento é eletricamente neutro como um todo. Como consequência, as cargas fotogeradas são efetivamente separadas e a probabilidade de recombinação para pares elétron-buraco fotogerados é reduzida. Assim que 304ss recebe elétrons fotoexcitados do Bi 2 Se 3 / TiO 2 nanocompósito através do fio, o potencial de 304ss muda negativamente. Sob iluminação de luz visível, o Bi 2 Se 3 / TiO 2 nanocompósitos podem reduzir a taxa de corrosão de 304ss. Portanto, a separação eficiente de pares de elétron-lacunas fotoexcitados em Bi 2 Se 3 / TiO 2 nanocompósitos irão acelerar a reação redox e gerar proteção fotocatódica efetiva para 304ss.
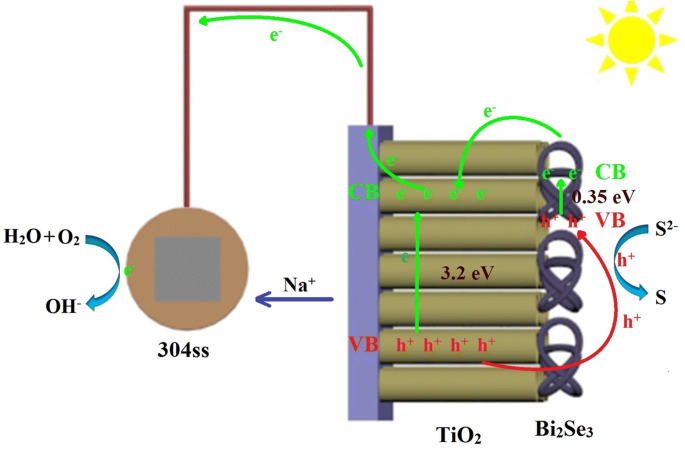
Representação esquemática dos processos de transferência de elétrons em Bi 2 Se 3 / TiO 2
Conclusões
Neste artigo, TiO 2 arranjos de nanotubos foram preparados pelo método de anodização e Bi 2 Se 3 nanoflores foram cultivadas em TiO 2 nanotubos por deposição em banho químico. O Bi 2 Se 3 / TiO 2 os nanocompósitos apresentaram distribuição homogênea e características ordenadas. Testes eletroquímicos para os nanocompósitos e TiO puro 2 acoplado com 304ss mostrou que o desempenho da proteção catódica fotogerada do Bi 2 Se 3 / TiO 2 os nanocompósitos foram superiores aos do TiO puro 2 . O valor OCP para 304ss juntamente com Bi 2 Se 3 / TiO 2 -0,5 mostrou uma mudança negativa para - 996 mV sob iluminação de luz visível devido aos locais ativos e coleta de luz de TiO 2 sensibilizado por Bi 2 Se 3 . Comparando os resultados dos testes eletroquímicos para três Bi 2 Se 3 / TiO 2 nanocompósitos, o nanocompósito preparado usando 0,5 mmol / L Bi 3+ no eletrólito exibiu um desempenho ideal.
Abreviações
- 304ss:
-
Aço inoxidável 304
- CB:
-
Banda de condução
- CE:
-
O contra eletrodo
- EDS:
-
Espectroscopia de raios-X de dispersão de energia
- H 3 NTA:
-
Ácido nitrilotriacético
- OA:
-
Oxigênio adsorvido
- OCP:
-
Potencial de circuito aberto
- OL:
-
Oxigênio reticular
- RE:
-
O eletrodo de referência
- SCE:
-
Eletrodo de calomelano saturado
- SEM:
-
Microscopia eletrônica de varredura
- UV-Vis:
-
Espectro de refletância difusa UV-visível
- VB:
-
Banda valence
- NÓS:
-
O eletrodo de trabalho
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- XRD:
-
Difração de raios X
Nanomateriais
- Seleção de aço inoxidável para aplicações de alta temperatura
- Diferenciando aço inoxidável 304 e 316
- Atividades fotocatalíticas aprimoradas por nanopartículas de Au-plasmônica em fotoeletrodo nanotubo de TiO2 revestido com MoO3
- Propriedades ópticas estruturais e de infravermelho próximo visível de TiO2 dopado com Cr para pigmentos frios coloridos
- Um método fácil para carregar nanopartículas de CeO2 em arranjos de nanotubos de TiO2 anódicos
- Matrizes de nanotubos de TiO2 bem alinhadas com nanopartículas de Ag para detecção altamente eficiente de íon Fe3 +
- Modificação Cu2-xSe em BiVO4 monoclínico para atividade fotocatalítica aprimorada sob luz visível
- Passivação para peças e invólucros de aço inoxidável
- Aplicações mais comuns para aço inoxidável
- Metais de precisão para fabricantes



