Modificação Cu2-xSe em BiVO4 monoclínico para atividade fotocatalítica aprimorada sob luz visível
Resumo
A rápida recombinação de pares de elétron-buraco em BiVO 4 limitou seu desempenho como fotocatálise. Neste artigo, BiVO 4 é combinado com Cu 2− x Se semicondutor para retardar o processo de recombinação e, assim, melhorar sua atividade fotocatalítica. Isso é possibilitado por um projeto cuidadoso da estrutura da banda. A função de trabalho de Cu 2− x Se é maior do que BiVO 4 . Portanto, os elétrons fluem para Cu 2− x Ver do BiVO 4 após a composição. Assim, um campo interno poderia ser construído, o que facilita a separação de elétrons e lacunas. O resultado experimental mostra que a eficiência fotocatalítica de 3% em peso Cu 2− x Se / BiVO 4 composto é 15,8 vezes o do BiVO 4 puro .
Introdução
Com o desenvolvimento da indústria moderna, a poluição ambiental tornou-se cada vez mais severa. Utilizando a energia solar, a decomposição fotocatalítica da matéria orgânica é uma tecnologia ecologicamente correta e eficiente para resolver a poluição [1,2,3,4,5,6]. O material fotocatalítico semicondutor de base dupla tem um gap adequado, o que lhe permite absorver luz visível suficientemente e possuir desempenho fotocatalítico superior [7,8,9,10]. Entre eles, BiVO monoclínico 4 tem um gap estreito de 2,4 eV e boa atividade fotocatalítica, que tem sido apontado como um material eficiente para decompor poluições orgânicas [11,12,13,14,15]. A rápida taxa de recombinação elétron-buraco, no entanto, leva a uma baixa atividade fotocatalítica para BiVO 4 puro [16,17,18]. Uma abordagem eficaz para desacelerar a recombinação de elétrons e lacunas é combinar dois materiais semicondutores diferentes, uma vez que as estruturas de banda dos dois materiais combinados correspondem a uma condição específica.
Como um semicondutor do tipo p, Cu 2− x O Se possui um bandgap indireto de 1,4 eV, que é benéfico para absorver a luz visível [19,20,21]. Quando BiVO 4 semicondutor é composto por Cu 2− x Se, a redistribuição de encargos é causada. A função de trabalho de Cu 2− x Se é maior do que BiVO 4 , e a energia Fermi é menor do que BiVO 4 [22, 23]. Portanto, os elétrons fluem para Cu 2− x Ver do BiVO 4 enquanto os buracos fluem ao contrário. Da mesma forma, um campo interno poderia ser construído apontando de BiVO 4 para Cu 2− x Se, o que facilita a separação de elétrons e lacunas. Quando sob iluminação, os elétrons gerados por foto no BiVO 4 e buracos gerados por foto em Cu 2− x Se irá se recombinar preferencialmente, devido à curvatura da banda e ao campo interno, deixando buracos úteis no BiVO 4 . Os furos úteis possuem maior nível de energia, o que pode beneficiar a geração de espécies • OH. Essas espécies • OH podem quebrar longas cadeias de matéria orgânica em pequenas moléculas. Portanto, o Cu 2− x Se / BiVO 4 espera-se que os compósitos tenham alta atividade fotocatalítica na luz visível.
Neste trabalho, nós fabricamos Cu 2− x Se / BiVO 4 compósitos e fez uso dele para a degradação de RhB sob irradiação de luz visível (> 420 nm) pela primeira vez. Depois de combinar com Cu 2− x Se, a atividade fotocatalítica se torna muito maior do que BiVO 4 puro . Especificamente, a eficiência fotocatalítica de 3% em peso de Cu 2− x Se / BiVO 4 composto é 15,8 vezes maior que o BiVO 4 puro . Além disso, após adicionar baixa concentração de H 2 O 2 na solução orgânica, o RhB degradou-se completamente em 50 min. Este trabalho fornece evidências de que Cu 2− x O Se é uma cocatálise eficaz para o desenvolvimento de novos fotocatalisadores semicondutores compostos.
Métodos
Preparação de Cu 2− x Se / BiVO 4 Compósitos
BiVO 4 foi sintetizado através de um método de precipitação química [24, 25]. O método de preparação de Cu 2− x Se pode ser encontrado em nosso artigo relatado anteriormente [26]. Então Cu 2− x Se / BiVO 4 os compósitos foram fabricados por uma abordagem de co-precipitação. A ilustração esquemática do progresso da preparação é mostrada na Fig. 1. Em primeiro lugar, o Cu 2− x pré-preparado Se e BiVO 4 os pós foram dispersos em etanol com agitação constante durante 4 h sob 60 ° C. Em segundo lugar, a suspensão da mistura foi agitada continuamente a 80 ° C para remover o solvente etanol. Finalmente, a amostra pulverulenta obtida foi aquecida a 160 ° C por 6 h sob uma atmosfera de fluxo de nitrogênio para formar o Cu 2− x Se / BiVO 4 composto.
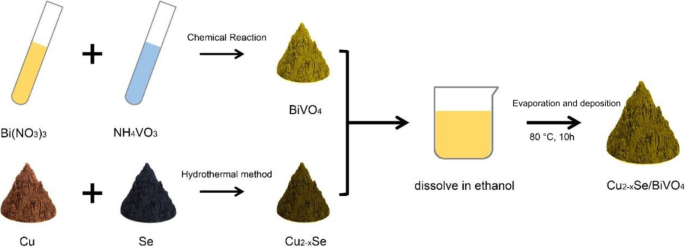
O diagrama esquemático de formação para Cu 2− x Se / BiVO 4 composto
Caracterização
A medição de XRD (difração de raios-X) das amostras preparadas foi realizada por um difratômetro PANalytical X’pert Pro com radiação Cu Kα. A morfologia da amostra foi obtida por MEV (microscópio eletrônico de varredura) Hitachi S-4800. XPS (espectroscopia de fotoelétrons de raios-X) das amostras foi caracterizada em um instrumento Pekin Elmer PHI-5300. Os espectros de emissão fotoluminescente das amostras foram confirmados em espectrofotômetro de fluorescência Cary Eclipse.
Reação fotocatalítica
O desempenho fotocatalítico foi caracterizado por um reator fotoquímico XPA. Além disso, uma lâmpada Xe com uma potência de 500 W e um comprimento de onda de corte de 420 nm é utilizada para simular a luz natural, enquanto uma solução de corante de teste RhB é usada para simular soluções orgânicas. Durante o processo de degradação, 60 mg de Cu 2− x O pó do compósito de Se foi colocado em uma solução de RhB de 60 mL. A suspensão foi agitada em um ambiente escuro por 2 h antes da irradiação de luz para realizar um equilíbrio de adsorção-dessorção. Em seguida, a iluminação de luz é adicionada com agitação remanescente e cerca de 6 mL da suspensão foram retirados em intervalos de 10 min. Posteriormente, a suspensão foi centrifugada duas vezes. O espectro de absorbância da solução foi caracterizado em um espectrômetro Shimadzu UV-2450.
Medições fotoeletroquímicas
A fotocorrente é medida por uma estação de trabalho eletroquímica CHI 660E. Para tornar a iluminação consistente com a do processo de degradação, a fonte de luz ainda é selecionada como uma lâmpada Xe com uma potência de 500 W e um comprimento de onda de corte de 420 nm. A medição fotoeletroquímica é detalhada a seguir. Primeiramente, 10 mg do fotocatalisador e 20 μL da solução de Nafion foram dispersos por ultrassom em 2 mL de álcool etílico. Em seguida, 40 μL da solução acima foram depositados em um vidro condutor ITO com 0,196 cm 2 , que foi aquecido sequencialmente a 200 ° C por 1 h para obter o eletrodo de trabalho. Além disso, a folha de Pt é escolhida como o contra-eletrodo. Uma solução saturada de mercúrio e cloreto de mercúrio em uma solução aquosa de cloreto de potássio como eletrodo de referência e 0,5 M de Na 2 SO 4 solução é usada para o eletrólito.
Resultados e discussão
Usamos a fotodegradação de RhB para examinar as propriedades fotocatalíticas das amostras. A Figura 2a mostra a degradação fotocatalítica de RhB sobre Cu 2− x Se / BiVO 4 . Quando BiVO 4 é combinado com Cu 2− x Se, seu desempenho fotocatalítico é significativamente melhorado. A proporção ótima do composto é de 3% e a eficiência fotocatalítica nessa proporção atinge o máximo. A Figura 2b mostra a taxa de degradação do Cu 2− x Se / BiVO 4 compósitos, correspondendo à concentração de Cu 2− x Se com 0, 2, 3 e 4% em peso, respectivamente. Na Fig. 2b, o valor do declive das linhas de degradação é 0,0011, 0,0118, 0,0174 e 0,0045 min −1 , respectivamente. Portanto, a eficiência fotocatalítica de 3% em peso Cu 2− x Se / BiVO 4 composto é 15,8 vezes o do BiVO 4 puro . A Figura 2c mostra as execuções de reciclagem da degradação fotocatalítica de RhB ao longo de 3% em peso de Cu 2− x Se / BiVO 4 composto com H 2 adicionado O 2 sob irradiação de luz visível. Quando uma pequena quantidade de H 2 O 2 é adicionado (103 μL / 100 mL), a 3% em peso de Cu 2− x Se / BiVO 4 compósitos podem degradar RhB completamente em 50 min sob excitação de luz visível. Também pode ser visto na Fig. 2c que a eficiência de degradação não é atenuada após 3 ciclos.
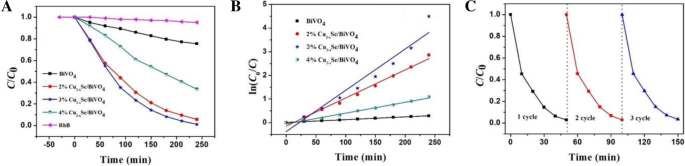
a Degradação fotocatalítica de RhB sobre Cu 2− x Se / BiVO 4 . b Constante de taxa de degradação fotocatalítica de RhB para Cu 2− x Se / BiVO 4 . c Ciclo de execuções de degradação fotocatalítica de RhB acima de 3% em peso de Cu 2− x Se / BiVO 4 composto com H 2 O 2 sob irradiação de luz visível
Com o objetivo de analisar a morfologia microscópica e o tamanho de grão das amostras, as amostras foram caracterizadas por MEV. Conforme mostrado na Fig. 3a, BiVO 4 é uma massa hexagonal com tamanho de partícula de 0,2–1 μm. Na Fig. 3b, a área circundada pela linha sólida vermelha exibe um Cu 2− x Folha de aço com espessura de 300 nm e comprimento de 4 μm. Após a composição, o Cu 2− x As folhas de páginas são distribuídas aleatoriamente na superfície do BiVO 4 volume. Os resultados do XPS também revelam a presença de Cu 2− x Veja (mostrado abaixo).

A fotografia SEM do BiVO 4 ( a ) e Cu 2− x Se / BiVO 4 ( b )
A Figura 4a mostra os dados de XRD para BiVO 4 e 3% em peso de Cu 2− x Se / BiVO 4 composto, que exibe que o BiVO 4 tem uma estrutura de cristal monoclínica. Pode ser visto que a estrutura cristalina do BiVO 4 não muda quando BiVO 4 é combinado com Cu 2− x Se. Isso pode ser devido ao fato de que o conteúdo de Cu é relativamente pequeno para ser detectado por XRD. A medição por fotoluminescência é uma forma geral de explorar a separação e combinação de elétrons e lacunas. A intensidade de luminescência relativamente baixa significa uma alta eficiência de separação elétron-buraco [27, 28]. A Figura 4b mostra os espectros PL para BiVO 4 e Cu 2− x Se / BiVO 4 compósitos. Após BiVO 4 é combinado com Cu 2− x Se, a intensidade de luminescência relativa do Cu 2− x Se / BiVO 4 composto é inferior ao de BiVO 4 , que indica que o Cu 2− x Se / BiVO 4 compósito tem maior eficiência de separação elétron-buraco após a combinação de BiVO 4 e Cu 2− x Se.
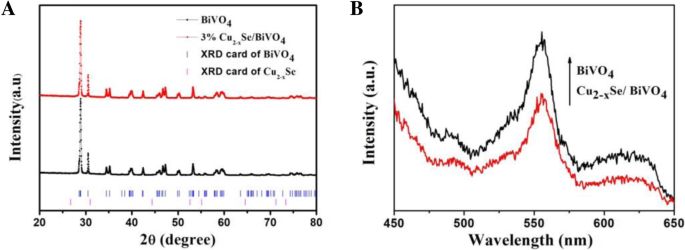
Os dados XRD para BiVO 4 e 3% Cu 2− x Se / BiVO 4 ( a ), o espectro PL para BiVO 4 e Cu 2− x Se / BiVO 4 compostos ( b )
O estado químico da superfície desempenha um papel importante na determinação do desempenho fotocatalítico. Assim, XPS é usado para analisar a valência do elemento de superfície do Cu 2− x Se / BiVO 4 composto. A Figura 5a é o espectro de pesquisa XPS do Cu 2− x Se / BiVO 4 BiVO composto e puro 4 , a partir da qual a energia característica de Bi, V, O, Cu e Se pode ser observada para Cu 2− x Se / BiVO 4 , e a energia característica de Bi, V e O pode ser observada para BiVO 4 . Os picos de 159,1 e 164,1 eV podem ser atribuídos às energias de ligação de Bi 4f 7/2 e Bi 4f 5/2 , respectivamente (Fig. 5b), que são derivados de Bi 3+ no BiVO 4 [29]. Os picos de 517,0 eV e 525,0 eV correspondem a V 2p 3/2 e V 2p 1/2 banda respectivamente (Fig. 5c), que são derivados do V 5+ de BiVO 4 . O pico de 530,2 eV pode ser atribuído a O 1 s em BiVO 4 (Fig. 5d) [30, 31]. Os dois picos de 58,6 eV e 53,8 eV correspondem a Se 3d 3/2 e Se 3d 5/2 , respectivamente (Fig. 5e) [32]. O Cu 2p 3/2 pico localizado em 931,9 eV corresponde a Cu 0 ou Cu I (Fig. 5f) [33].
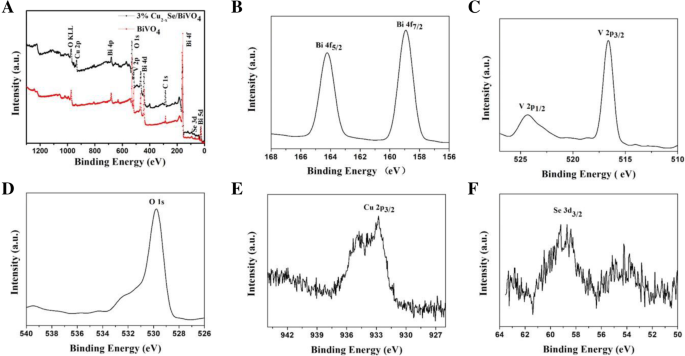
Os espectros XPS de Cu 2− x Se / BiVO 4 composto. a Pesquisa, b Bi, c V, d O, e Cu e f Se
Para ilustrar ainda mais a eficiência de separação de elétrons fotogerados e lacunas, a amostra foi submetida à análise EIS. Conforme mostrado na Fig. 6, o diagrama EIS Nyquist de Cu 2− x Se / BiVO 4 tem um raio de arco menor que Cu 2− x Se, indicando que Cu 2− x Se / BiVO 4 os compósitos têm menor resistência de transferência de carga e transferência de elétrons de interface mais rápida. [34, 35]
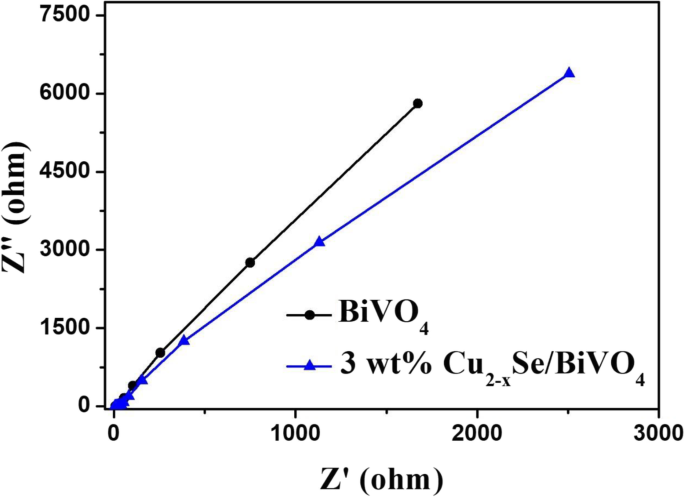
O EIS para BiVO 4 e Cu 2− x Se / BiVO 4 sob irradiação de luz visível em 0,5 M de Na 2 SO 4 solução
A razão pela qual Cu 2− x Se / BiVO 4 o composto apresenta alta eficiência é explicado a seguir. Conforme ilustrado na Fig. 7, o nível de Fermi de Cu 2− x Se e BiVO 4 discorda um do outro. Como resultado, após o BiVO 4 a superfície do semicondutor é composta com CuSe, as cargas serão redistribuídas. Cu 2− x Se tem função de trabalho maior e energia de Fermi mais baixa, então os elétrons fluem para Cu 2− x Ver do BiVO 4 enquanto os buracos fluem ao contrário. Como resultado, o Cu 2− x Se está carregado negativamente e BiVO 4 é carregado positivamente até que o nível de Fermi seja igual. Enquanto isso, a estrutura da banda de ambos os materiais se dobrará correspondendo ao movimento dos níveis de Fermi. Outro efeito da redistribuição de portadores é a construção de um campo interno apontando para BiVO 4 para Cu 2− x Se. Tanto o movimento do nível de Fermi quanto o campo interno formam a chamada heterojunção do esquema S entre Cu 2− x Se e BiVO 4 [36]. Sob iluminação, elétrons e lacunas são excitados em ambos os materiais. Neste tipo de heterojunção, entretanto, os elétrons fotogerados no BiVO 4 e buracos gerados por foto em Cu 2− x Se irá se recombinar preferencialmente, devido à curvatura da banda e ao campo interno, deixando buracos úteis no BiVO 4 . Os furos úteis possuem maior nível de energia, o que pode beneficiar a geração de espécies • OH. Essas espécies • OH podem quebrar longas cadeias de matéria orgânica em pequenas moléculas. Os resultados acima indicam que o carregamento de Cu 2− x Veja na superfície do BiVO 4 pode aumentar a atividade fotocatalítica da luz visível.
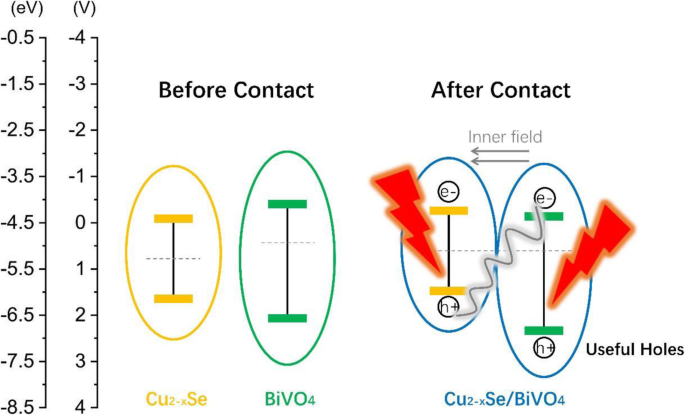
O diagrama esquemático do mecanismo fotocatalítico
Conclusão
Em resumo, o Cu 2− x Se / BiVO 4 os compósitos foram preparados e examinados com sucesso quanto à degradação de poluições orgânicas. Dados experimentais mostram que a atividade fotocatalítica é amplamente melhorada após a combinação. A eficiência fotocatalítica de 3% em peso de Cu 2− x Se / BiVO 4 composto é 15,8 vezes maior que o BiVO 4 puro . Além disso, após adicionar baixa concentração de H 2 O 2 , RhB pode ser completamente degradado em 50 min. Os resultados de SEM e XPS confirmam a presença de Cu 2− x Ver no Cu 2− x Se / BiVO 4 compósitos. Os resultados da fotoluminescência indicam que o Cu 2− x Se / BiVO 4 compósitos têm maior eficiência de separação elétron-buraco. Os resultados do EIS indicam que Cu 2− x Se / BiVO 4 os compósitos têm menor resistência de transferência de carga e transferência de elétrons de interface mais rápida. Este trabalho mostra que Cu 2− x O Se é uma cocatálise eficaz para o desenvolvimento de novos fotocatalisadores semicondutores compostos.
Abreviações
- RhB:
-
Rodamina B
- SEM:
-
Microscópio eletrônico de varredura
- XRD:
-
Difração de raios X
Nanomateriais
- Nanofibras e filamentos para entrega aprimorada de drogas
- Síntese hidrotérmica de nanopartículas de In2O3 híbridos gêmeos heteroestruturas de ZnO de disco hexagonal para atividades fotocatalíticas aprimoradas e estabilidade
- Efeitos sinérgicos de nanopartículas de Ag / BiV1-xMoxO4 com atividade fotocatalítica aprimorada
- Modificação do cocatalisador da liga PtNi do híbrido g-C3N4 / GO sensibilizado com Eosina Y para evolução eficiente do hidrogênio fotocatalítico com luz visível
- Evolução de hidrogênio fotocatalítico aprimorada carregando Cd0.5Zn0.5S QDs em nanofolhas Ni2P porosas
- Atividade fotocatalítica do nanocompósito ternário de atapulgita-TiO2-Ag3PO4 para degradação de Rodamina B sob irradiação solar simulada
- Nanotubos de titânia preparados por anodização de decomposição rápida para descoloração fotocatalítica de corantes orgânicos sob UV e luz solar natural
- Síntese fácil e atividade fotocatalítica de luz visível aprimorada de novos compostos de heterojunção p-Ag3PO4 / n-BiFeO3 para degradação de corante
- Influência de Mg Doping em Nanopartículas de ZnO para Avaliação Fotocatalítica Aprimorada e Análise Antibacteriana
- Películas nanotubas de TiO2 sensibilizadas Bi2Se3 para proteção catódica fotogerada de aço inoxidável 304 sob luz visível



