Pontos fluorescentes de nano-biomassa:extração assistida por ultrassom e sua aplicação como nanossonda para detecção de Fe3 +
Resumo
A biomassa como recurso sustentável e renovável tem sido uma das fontes de energia importantes para a vida humana. Aqui, pontos luminescentes de nano-biomassa (NBDs) foram extraídos da soja por meio do método ultrassônico, que confere à biomassa a propriedade de fluorescência. Os NBDs como preparados são amorfos na estrutura com um diâmetro médio de 2,4 nm e mostram fluorescência azul brilhante com um rendimento quântico de 16,7%. Beneficiando-se das matérias-primas comestíveis e do processo de síntese sem aquecimento, o teste de citotoxicidade mostra que a viabilidade celular ainda se mantém em 100% mesmo que a concentração dos NBDs atinja 800 μg / ml, indicando a boa biocompatibilidade dos NBDs. Além disso, a fluorescência dos NBDs é muito sensível ao Fe 3+ , que pode ser usado para Fe 3+ detecção em termos de sua superioridade em saúde. O limite de detecção (LOD) do sensor proposto foi determinado como 2,9 μM, que é inferior ao nível máximo permitido de Fe 3+ (5,37 μM) em água potável.
Histórico
Os nanomateriais luminescentes alcançaram uma ampla variedade de aplicações devido às suas propriedades ópticas únicas, especialmente em diodos emissores de luz, detectores, bioimagem e detecção de íons metálicos [1,2,3,4,5,6]. Vários nanomateriais luminescentes foram relatados até agora, como pontos quânticos semicondutores (QDs), nano-pontos de carbono e QDs de enxofre, que levaram a muitos avanços em muitos campos [7,8,9,10,11,12] . Os QDs como um excelente representante de nanomateriais luminescentes têm sido usados em muitos campos devido às suas excelentes propriedades ópticas e elétricas. Apesar de tudo isso, a toxicidade dos QDs ainda limita muito suas aplicações [13, 14]. É sempre de grande importância encontrar nanomateriais mais verdes e sustentáveis com luminescência. A biomassa é uma matéria orgânica original que pode ser produzida via fotossíntese, e se destaca por suas propriedades sustentáveis e renováveis. Especificamente, a biomassa é definida como a fração biodegradável de produtos, resíduos e resíduos de um organismo [15, 16]. No contexto da nanotecnologia, a biomassa é normalmente usada como um precursor e pode ser transformada em nanopontos com algumas propriedades ópticas após um tratamento especial. Em comparação com os precursores químicos, os principais componentes da biomassa, especialmente a biomassa comestível, são açúcares e proteínas, que são inofensivos em tratamentos subsequentes. Portanto, os pontos de nano-biomassa (NBDs) devem ser de alta biocompatibilidade, o que garante suas aplicações nos campos biológico e ambiental sem produzir substâncias nocivas.
Até agora, apenas nanopontos de carbono fluorescentes derivados de biomassa foram relatados. Basicamente, algumas biomassas naturais como folhas, clara de ovo e suco de limão foram tratadas por método hidrotérmico para sintetizar nanopartículas de carbono por fluorescência [17,18,19]. Há também outro tipo de nanopontos de carbono que existem em alimentos comestíveis, que são produzidos no processamento posterior de biomassa natural [20, 21]. Sem exceção, todos eles envolveram processos típicos de carbonização em alta temperatura. Este processo pode envolver muito tempo e alta temperatura, e é difícil alcançar a produção de lotes em larga escala [22]. Em comparação com altas temperaturas, a temperatura ambiente ou as condições de baixa temperatura são fáceis de serem realizadas e mantêm as propriedades originais da própria biomassa.
Nanossonda é uma das aplicações importantes de nanomateriais luminescentes [23]. Tendo em vista a fluorescência brilhante e a alta biocompatibilidade, os NBDs podem ser usados como uma espécie de nanossonda na área de biologia e meio ambiente. Fe 3+ é um importante íon metálico no corpo humano, para o qual desempenham um papel significativo na síntese de hemoglobina e mioglobina [24]. Mas excesso de Fe 3+ o acúmulo no corpo pode causar danos aos tecidos e falência de órgãos. Desenvolvimento de sistemas de detecção eficazes e mais ecológicos para a determinação qualitativa e quantitativa de Fe 3+ é de grande importância para questões clínicas, médicas e ambientais. Isso nos permite considerar se a biomassa pode ser adaptada em nanopontos com propriedades desejáveis diretamente da biomassa comestível natural, sem qualquer processamento. No entanto, nenhum desses NBDs luminescentes foi relatado até onde sabemos. Portanto, procurar precursores de biomassa mais naturais para obter NBDs com propriedades desejáveis e alta biocompatibilidade pode dar um passo em direção a nanomateriais luminescentes mais verdes e Fe 3+ detecção.
Aqui, pontos de nano-biomassa luminescentes (NBDs) foram demonstrados por meio de estratégia de extração ultrassônica (UES) de soja pela primeira vez. O rendimento quântico de fotoluminescência (PL) (QY) dos NBDs como preparados pode chegar a 16,7%, e os NBDs mostram emissão de brilho no estado sólido. O teste de citotoxicidade mostra que os NBDs apresentam alta biocompatibilidade. Além disso, os NBDs foram empregados para Fe 3+ detecção de sua dependência de intensidade de fluorescência linearmente no Fe 3+ concentração e o limite de detecção (LOD) pode chegar a 2,9 μM.
Métodos
Materiais
Variedades de soja do nordeste de acordo com o Padrão Nacional da República Popular da China ( GB1352-2009 ) foram adquiridos no supermercado local e lavados várias vezes com água destilada antes do uso. Cloreto de cálcio (CaCl 2 ), cloreto de manganês (MnCl 2 ), cloreto cúprico (CuCl 2 ), cloreto de cobalto (CoCl 2 ), nitrato de chumbo (Pb (NO 3 ) 2 ) e nitrato de cromo (Cr (NO 3 ) 3 ) foram adquiridos da Aladdin Ltd. (Shanghai, China). Cloreto férrico (FeCl 3 ), cloreto ferroso (FeCl 2 ), cloreto de cádmio (CdCl 2 ), dicloreto de mercúrio (HgCl 2 ), cloreto de sódio (NaCl) e cloreto de zinco (ZnCl 2 ) foram obtidos da Sinopharm Chemical Reagent Co., Ltd. (Shanghai, China). Todos os produtos químicos são de reagente analítico (pureza> 99,0%) e usados como recebidos sem purificação adicional.
Síntese de NBDs
Primeiramente, 100 peças de soja foram lavadas com uma mistura de álcool e água destilada por 3 vezes para remover as impurezas. Em seguida, os grãos de soja foram colocados em um béquer com 50 ml de água destilada seguida de ultrassom por 2 h. Durante este processo, a cor da solução mudou de transparente para amarelo escuro, indicando que a casca da soja foi adaptada em tamanho nanométrico para formar NBDs. Em seguida, a solução amarela escura foi transferida para tubos de centrífuga e centrifugada a 7000 rpm por 3 minutos duas vezes para remover partículas de grande porte, após o que o sobrenadante foi filtrado através de uma membrana de 0,22 μM para remover partículas grandes ou aglomeradas ainda mais. Posteriormente, a solução foi colocada em um refrigerador seguido por tratamento congelado a - 5 ° C por 6 h. Em seguida, foi transferido para um liofilizador a - 50 ° C por 12 h para obtenção dos pós. Os pós congelados foram dispersos em água para formar NBDs para posterior aplicação.
Caracterização
O padrão de difração de raios X (XRD) dos NBDs foi registrado usando um difratômetro X ′ Pert Pro, no qual os raios X foram gerados por uma fonte de Cu-Kα. Um microscópio eletrônico de transmissão (TEM) JEM-2010 foi empregado para caracterizar o tamanho e a cristalinidade dos NBDs. Os espectros de fluorescência dos NBDs foram obtidos com um espectrofotômetro de fluorescência F-7000. Os espectros de absorção de UV-Vis dos NBDs foram obtidos usando um espectrofotômetro UH4150. Os espectros de infravermelho com transformada de Fourier (FTIR) das amostras foram registrados por um espectrômetro Thermo Scientific Nicolet iS10 FTIR. Os espectros de espectroscopia de fotoelétrons de raios-X (XPS) das amostras foram coletados usando um espectrômetro Thermo Fisher Scientific ESCALAB 250Xi equipado com uma fonte de radiação de raios-X Al-Kα.
Medição de rendimento quântico por fotoluminescência
O PL QY foi testado em um espectrofluorômetro F-9000 com esfera integradora. Em primeiro lugar, a solução aquosa de NBD foi diluída para uma intensidade de absorção abaixo de 0,1. Em seguida, essa solução aquosa foi adicionada a uma cubeta de fluorescência, colocada na esfera integradora e excitada com luz monocromática de 370 nm. Os espectros de fluorescência foram coletados nas faixas de 430–450 nm. Enquanto isso, os mesmos espectros de fluorescência para água pura também foram registrados em condições idênticas. Finalmente, o PL QY foi calculado usando software de fluorescência com base nos espectros de PL da amostra e da água.
Teste de toxicidade celular
A citotoxicidade de NBDs é avaliada por métodos de MTT (3- (4,5) -dimetiltiahiazo (-z-y1) -3,5-di-fenitetra-zoliu-mrometo). As células foram cultivadas em RPMI-1640 normal com 10% de soro fetal bovino em 5% de CO 2 e 95% de ar a 37 ° C em uma incubadora umidificada. Para medições de viabilidade celular, células HeLa foram colocadas em placas de 96 poços e, em seguida, incubadas por 72 h. Após a incubação das células Hela com várias concentrações de NBDs e CDs por 72 h, a viabilidade celular foi registrada.
Detecção de Fe 3+
1 ml de solução com diferentes concentrações de Fe 3+ foi adicionado em 1 ml de NBDs com solução de 3 g / l antes das medições de PL. As soluções foram misturadas completamente e deixadas reagir por 1 min em temperatura ambiente, e então registrados os espectros de fluorescência associados. As medidas de PL foram realizadas sob excitação de 370 nm.
Resultados e discussão
Morfologia e composição química
Os NBDs foram preparados por meio de métodos UES; todos os processos são ilustrados no Esquema 1. Os tamanhos e morfologia dos NBDs foram caracterizados por microscopia eletrônica de transmissão (TEM), conforme mostrado nas Fig. 1a e b. As imagens TEM mostram que os NBDs eram quase esféricos em forma. Os diâmetros dos NBDs variam de 1 a 3 nm, com um diâmetro médio de 2,4 nm, e a distribuição de tamanho correspondente está listada na Fig. 1c. Franjas reticuladas dos NBDs não podem ser observadas a partir da imagem TEM de alta resolução (inserção da Fig. 1b), indicando a natureza amorfa dos NBDs. As imagens da microscopia eletrônica de transmissão de varredura de campo escuro anular de alto ângulo (HAADF-STEM) e o mapeamento elementar correspondente (carbono, nitrogênio e oxigênio) dos NBDs são mostrados na Fig. 1d – g. Pode-se observar que os elementos dominantes dos NBDs são carbono, nitrogênio e oxigênio. Além disso, estado sólido 13 As medições de ressonância magnética nuclear (NMR) C dos NBDs são mostradas na Fig. 1h. Os sinais variam de 160-180 ppm, e os picos em 164 ppm e 170 ppm correspondem a ligações C =O, que são indicativas de sp 2 átomos de carbono [25, 26].
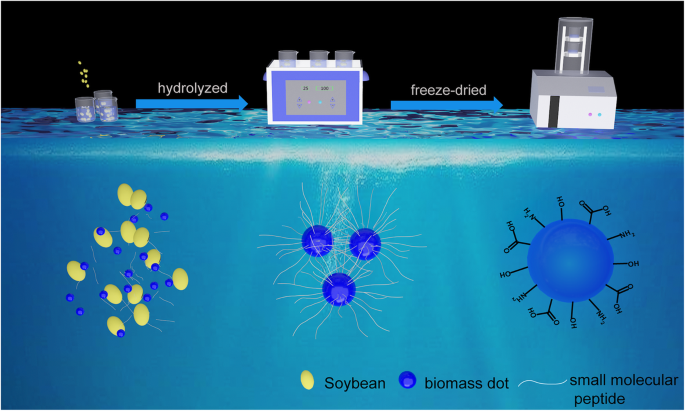
Ilustração esquemática do processo de preparação dos NBDs de soja
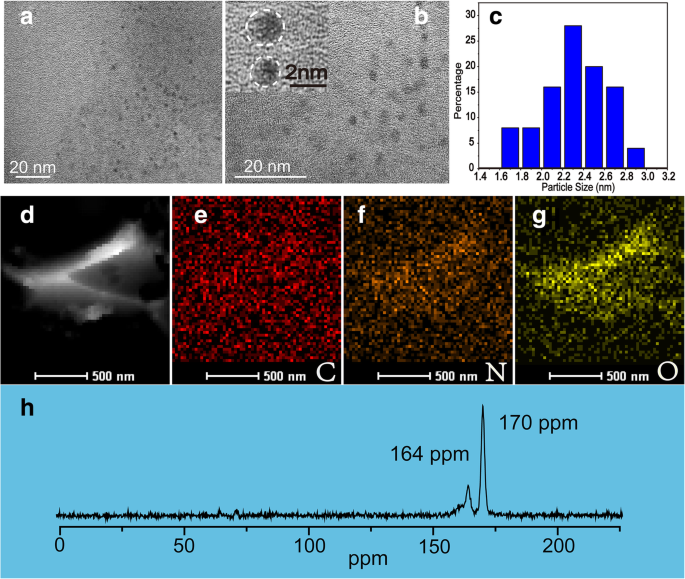
Imagens TEM dos NBDs ( a ) e ( b ) c A distribuição do tamanho de partícula dos NBDs. Imagem HAADF ( d ) e mapeamento de distribuição elementar correspondente de carbono ( e ), nitrogênio ( f ) e oxigênio ( g )
Para estudar mais as características estruturais dos NBDs, o padrão de difração de raios-X (XRD) foi registrado. Conforme mostrado na Fig. 2a, o padrão de XRD típico exibe um pico amplo localizado em torno de 21,5 o e um ombro pico em cerca de 41,0 o , que pode ser atribuído à fase de carbono amorfo [27]. Além disso, os picos de absorção característicos da soja e NBDs foram investigados por espectroscopia de infravermelho com transformada de Fourier (FTIR), conforme mostrado na Fig. 2 (b). As bandas de absorção em torno de 3380 cm −1 pode ser atribuído às vibrações de alongamento de O – H / –N – H, a banda em torno de 2906 cm −1 às vibrações de alongamento C – H e a banda em cerca de 1650 cm −1 às vibrações de alongamento C =O. Os picos em 1400 cm −1 e 1071 cm −1 são correspondentes às vibrações de flexão C – H e C – O, respectivamente [28]. Há uma diferença óbvia entre o espectro da soja e NBDs em torno de 1750 cm −1 , que pertence às vibrações de alongamento das ligações C =O dos lipídios na soja [29, 30]. Os lipídios insolúveis em solução aquosa foram separados da amostra ao serem imersos em água, levando ao desaparecimento das ligações no espectro de FTIR dos NBDs. As ligações C =O reduzidas na amostra vêm do grupo carboxila na proteína. O pico centrado em cerca de 1543 cm −1 também desapareceu, o que pode ser atribuído à proteólise no processo de embebição da soja. Ao comparar todos os picos antes e depois do processo de ultrassom, a formação de grupos –OH, –C =O (amida I) e –NH na superfície dos NBDs pode ser vista [31]. Os resultados acima demonstram a existência de grupos hidroxila, amidogênio e carboxílicos na superfície dos NBDs, e esses grupos funcionais desempenham um papel importante na hidrofilicidade e estabilidade dos NBDs em solução aquosa. Os espectros de espectroscopia de fotoelétrons de raios-X (XPS) foram realizados para elucidar ainda mais os componentes dos NBDs, como mostrado na Fig. 2c. O espectro XPS mostra três picos fortes em 532,0, 401,1 e 286,1 eV, que podem ser atribuídos a O 1s, N 1s (Fig. 2d) e C 1s (Fig. 2e), respectivamente [32]. Esses resultados indicam que os NBDs contêm principalmente C (64,33%), O (32,34%) e N (2,72%), bem como uma quantidade limitada de P, e o elemento P pode vir do fosfolipídeo da soja [33] . No espectro XPS de alta resolução, o espectro C 1s exibe três picos em 287,6, 285,8 e 284,6 eV, que podem ser atribuídos a C =O, C – O / C – N e C – C / C =C grupos, como mostrado na Fig. 2c. A ligação C =O é dos grupos carboxila solúveis [24]. O C – O / C =N e C – C / C =C são dos carbonos nitrosos e sp 2 / sp 3 carbonos, respectivamente [34]. O espectro de N 1s mostrado na Fig. 2d confirma duas bandas principais em 399,5 eV e 401,6 eV, revelando a existência de N piridínico e N pirrólico, o que é consistente com a análise de FTIR. O espectro de O 1s apresentado na Fig. 2f tem dois picos em 531,4 eV e 533,0 eV, que podem ser atribuídos aos grupos C – OH / C – O – C e C =O, respectivamente [9].
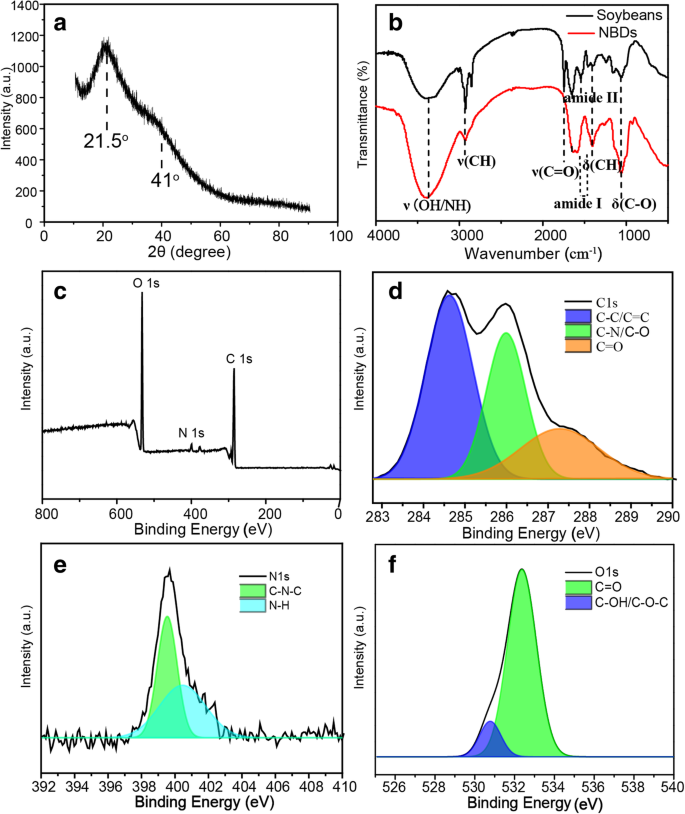
a Padrão de XRD dos NBDs. b Espectros de FTIR da soja e NBDs. c Espectro de pesquisa XPS dos NBDs. Espectros XPS de alta resolução de C 1s ( d ), N 1s ( e ), e O 1s ( f )
Um possível mecanismo para a formação de NBDs a partir da soja foi proposto com base na análise acima. Primeiro, algumas grandes partículas de biomassa suspensas na solução são quebradas em nanômetros pela concussão ultrassônica. As mudanças na solução antes e depois do tratamento de extração ultrassônica são mostradas no arquivo adicional 1:Figura S1. Em seguida, a proteína na soja foi hidrolisada em pequenos peptídeos moleculares e aminoácidos no processo acima, e muitas cadeias de peptídeos de moléculas pequenas são anexadas à biomassa de tamanho nanométrico para formar os pontos de biomassa altamente funcionalizados na superfície. Os grupos funcionais na superfície dos pontos de biomassa são os principais contribuintes para a fluorescência. De acordo com o mecanismo, o feijão mungo também foi utilizado como precursor, e NBDs fluorescentes azuis também foram obtidos, conforme mostrado no Arquivo Adicional 1:Figura S2.
Propriedades ópticas
Os NBDs mostram propriedades fluorescentes dependentes de excitação, e quando o comprimento de onda de excitação varia de 320 a 520 nm, o pico de emissão muda para o vermelho gradualmente, indicando que a emissão dos NBDs pode ser ajustada mudando o comprimento de onda de excitação, como mostrado na Fig. 3a. A solução aquosa NBD é transparente sob iluminação interna e mostra fluorescência azul sob iluminação UV, conforme mostrado no detalhe da Fig. 3b. O espectro de excitação de fotoluminescência (PLE) dos NBDs é mostrado no arquivo adicional 1:Figura S3, e o comprimento de onda de excitação óptica está na faixa de 360 a 420 nm. Para explorar a origem do PL dos NBDs, os espectros de absorção de UV-Vis dos NBDs com diferentes concentrações foram registrados à temperatura ambiente (a concentração de NBDs de baixo para cima é 0,03, 0,06, 0,13, 0,25, 0,25, 0,50, 0,50 , 0,75, 1,00 e 1,50 g / l), como mostrado na Fig. 3b. Os espectros de absorção de UV-Vis dos NBDs exibem dois picos de absorção claros em 270 nm e 330 nm, respectivamente. O primeiro pode ser atribuído ao π-π * transição de ligações C – C / C =C, enquanto a última para n-π * transição de ligações C =O / N [35, 36]. Esses grupos funcionais são os principais grupos cromogênicos que contribuem para a fluorescência dos NBDs [37, 38]. Os espectros de PL dos grãos de soja durante a extração ultrassônica são mostrados no Arquivo adicional 1:Figura S4, e a intensidade de PL aumenta com o tempo e atinge o máximo. A Figura 3c mostra os espectros de PL dos NBDs medidos de 80 a 300 K. Os NBDs exibem um comportamento típico de extinção térmica, em que todos os picos diminuem monotonicamente em intensidade com o aumento da temperatura. Este comportamento da PL pode ser atribuído ao aumento da recombinação não radiativa e à redução da recombinação da radiação com o aumento das temperaturas [39, 40]. Para avaliar a estabilidade dos NBDs, a fotoestabilidade e a termoestabilidade dos NBDs foram caracterizadas, conforme mostrado na Fig. 3d. Para fotoestabilidade, a imagem de configuração de medição é mostrada no arquivo adicional 1:Figura S5. Os valores de intensidade de fluorescência são mostrados no arquivo adicional 1:Figura S6 e S7. A intensidade de emissão dos NBDs permanece acima de 90% sob a iluminação da lâmpada UV por 6 h, indicando sua boa fotoestabilidade. Para termoestabilidade, as intensidades de fluorescência dos NBDs diminuem pouco quando a temperatura varia de 20 a 80 ° C, revelando sua alta estabilidade térmica.
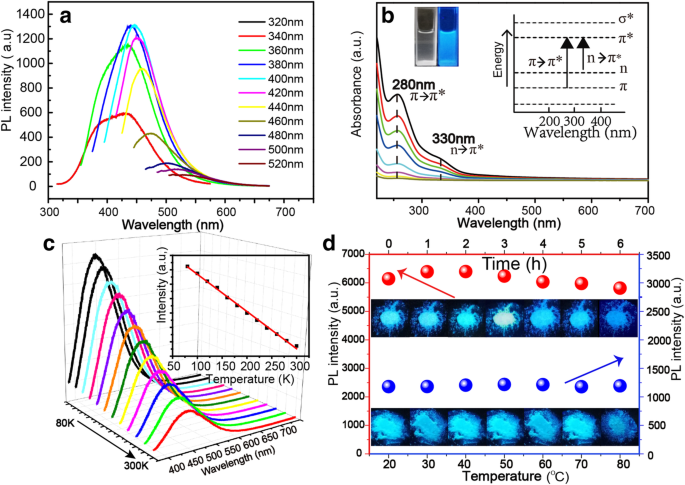
a Os espectros de fluorescência dos NBDs com alterações de comprimento de onda de excitação de 320 a 520 nm. b Espectros de absorção de UV-Vis dos NBDs. c Espectros de fluorescência dos NBDs em diferentes temperaturas, a inserção é o gráfico da intensidade de fluorescência dos NBDs em função da temperatura. d Intensidade de fluorescência e imagens dos pós NBD sob a iluminação de uma lâmpada de 365 nm para durações diferentes e as dos pós NBD em diferentes temperaturas de medição
Avaliação de citotoxicidade
Os ensaios de MTT foram usados para avaliar a citotoxicidade dos NBDs. As viabilidades das células HeLa incubadas com os NBDs e dois outros tipos de CDs sintetizados via método hidrotérmico, como mostrado na Fig. 4. Conforme indicado na figura, as viabilidades das células diminuem pouco quando a solução de NBD é introduzida, mesmo quando a concentração de NBDs atinge 800 μg / ml. A taxa de sobrevivência celular foi de 70% e 67% quando as células HeLa foram incubadas com os outros dois tipos de CDs na concentração de 800 μg / ml. Obviamente, os NBDs exibem biocompatibilidade superior do que os CDs preparados a partir de reagentes químicos.
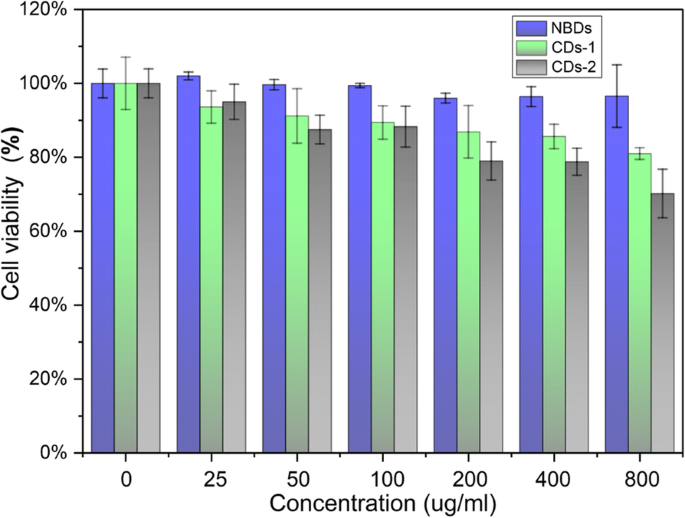
Viabilidade de células HeLa após 72 h de incubação com diferentes concentrações de NBDs e CDs
Propriedades de detecção dos NBDs em direção a Fe 3+
Curiosamente, a fluorescência dos NBDs pode ser efetivamente extinta por Fe 3+ , como mostrado na Fig. 5a, e a intensidade de PL dos NBDs diminui significativamente com o aumento de Fe 3+ concentração. Além disso, uma boa relação linear pode ser traçada entre F 0 / F e o Fe 3+ concentração variando de 0 a 30 μM ( R 2 =0,99), onde F 0 e F foram a intensidade PL dos NBDs no ex / em de 370/445 nm na ausência e presença de Fe 3+ , conforme mostrado na Fig. 5b. A eficiência de têmpera foi ajustada pela Stern-Volmer Eq:
$$ \ frac {{\ mathrm {F}} _ 0} {\ mathrm {F}} =1+ {K} _ {\ mathrm {SV}} \ left [Q \ right] $$ (1)
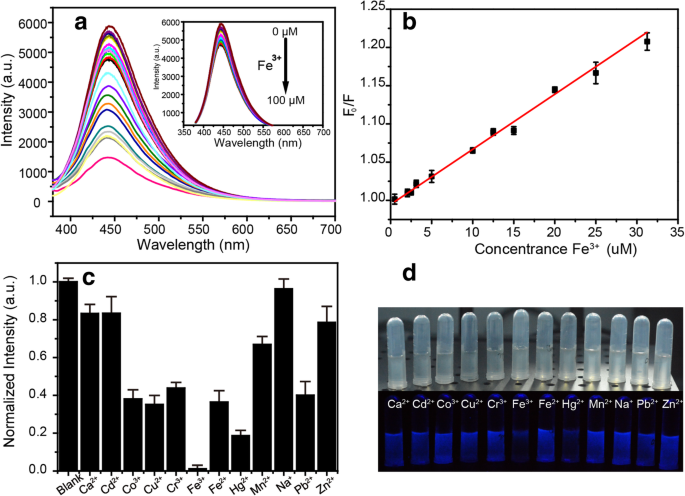
a Espectros PL dos NBDs na presença de diferentes concentrações de Fe 3 + . b Curva de calibração do sensor em função de Fe 3 + concentração. c Intensidades de fluorescência dos NBDs na presença de íons diferentes. d Imagens fotográficas da solução NBDs com diferentes íons metálicos sob iluminação interna e UV
onde K sv é a constante de têmpera de Stern-Volmer e [ Q ] é o Fe 3+ concentração. A equação de regressão linear é Y =0,0072 X + 0,99479, R 2 =0,99. O limite de detecção (LOD) do sensor proposto foi determinado como 2,9 μM, que é inferior ao nível máximo permitido de Fe 3+ (5,37 μM) em água potável estabelecida pela Agência de Proteção Ambiental dos Estados Unidos (USEPA) [24]. A seletividade é outro parâmetro crítico para sensores químicos. Portanto, a resposta de fluorescência do sensor em relação a vários íons metálicos interferentes foi investigada, incluindo Ca 2+ , Cd 2+ , Co 2+ , Cu 2+ , Cr 3+ , Fe 3+ , Fe 2+ , Hg 2+ , Mn 2+ , Na + , Pb 2+ e Zn 2+ . Íons metálicos, cada um a uma concentração de 10 −2 M foram adicionados a 1 ml de solução de NBDs com uma concentração de 3 g / l. Na Fig. 5c, pode ser visto que a intensidade de fluorescência dos NBDs responde de forma mais sensível ao Fe 3+ do que outros íons de metal. As fotografias na Fig. 5d são as imagens dos NBDs com vários íons sob iluminação interna e UV, e a concentração de íons metálicos foi de 100 μM. Obviamente, os NBDs estão se extinguindo na presença de Fe 3+ , indicando que eles podem ser usados para detecção visual.
Mecanismo de têmpera
O mecanismo de extinção dos NBDs na presença de Fe 3+ foi discutido com base nos espectros de absorção de UV-Vis e tempo de vida de fluorescência dos NBDs. A partir dos espectros de absorção de UV-Vis mostrados no arquivo adicional 1:Figura S8, não há alteração dos picos de absorção em 270 nm e 340 nm com a introdução de Fe 3+ , indicando que o Fe 3+ não influencia a estrutura dos NBDs [41]. Além do espectro de absorção de UV-Vis, o efeito do Fe 3+ sobre o tempo de vida do NBD também foi estudado. Na Fig. 6a, o tempo de vida da fluorescência torna-se mais curto após a adição de Fe 3+ , que pode envolver a transferência parcial de elétrons dos NBDs para o d orbital de Fe 3+ , diminuindo assim a recombinação radiativa dos NBDs [42]. O mecanismo de extinção de fluorescência dos NBDs causados por Fe 3+ é mostrado na Fig. 6b. O efeito de supressão de fluorescência sensível dos NBDs na presença de Fe 3+ pode originar-se da forte interação entre Fe 3+ e os grupos de superfície dos NBDs. Fe 3+ tem uma afinidade de ligação mais forte e cinética de quelação mais rápida com grupos amino e carboxílicos nas superfícies de NBDs. A coordenação especial entre o Fe 3+ íons e os grupos hidroxila / amina fenólicos de NBDs têm sido amplamente usados para a detecção de Fe 3+ íons ou reações coloridas na química orgânica tradicional [43, 44]. Além disso, os potenciais redox de Fe 3+ / Fe 2+ ( Ф =0,77) estão localizados entre o orbital molecular mais baixo desocupado (LUMO) e o orbital molecular mais ocupado (HOMO) dos NBDs, causando transferência de elétrons fotoinduzida de LUMO para os estados complexos de Fe 3+ [45]. Estes resultados demonstram que os NBDs são altamente sensíveis ao Fe 3+ sobre os outros íons de metal.
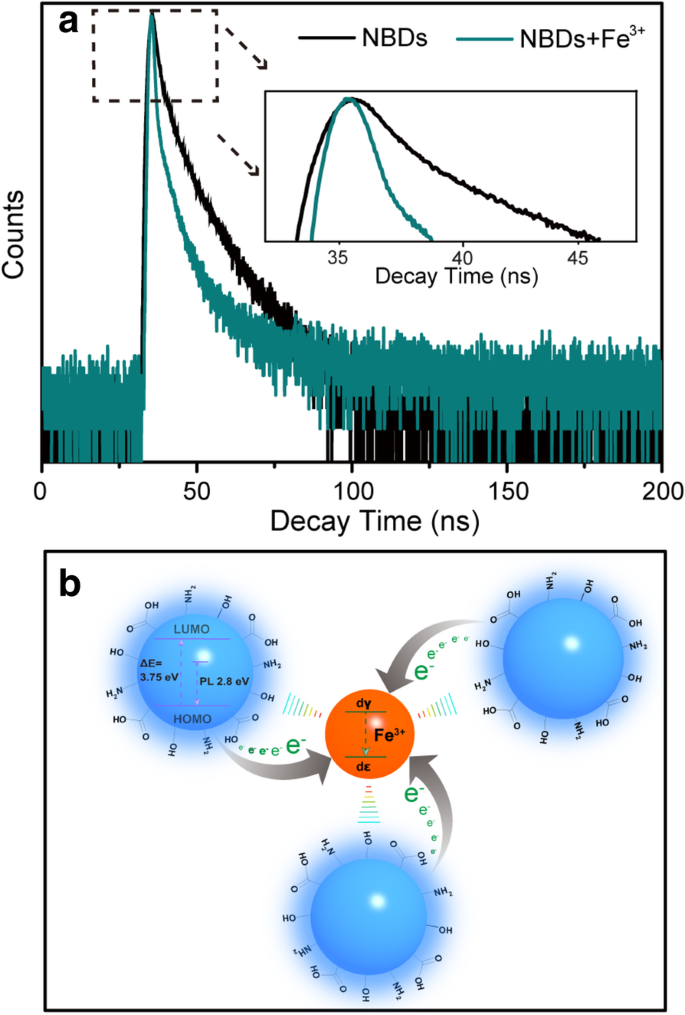
a Traços de decaimento de fluorescência de NCDs na ausência e presença de Fe 3 + sob excitação a 370 nm e emissão a 445 nm. b Ilustração esquemática para o possível mecanismo de extinção de fluorescência dos NBDs na presença de Fe 3 + íons
Conclusão
Em resumo, NBDs luminescentes foram preparados a partir de soja por meio de uma abordagem UES sem aquecimento. Os NBDs apresentam fluorescência azul brilhante com PL QY de 16,7% e, beneficiando-se da biomassa comestível e do processo de síntese sem aquecimento, a viabilidade celular ainda se mantém 100% mesmo que a concentração dos NBDs atinja 800 μg / ml. Além disso, a fluorescência dos NBDs exibe sensibilidade específica ao Fe 3+ , e o LOD pode chegar a 2,9 μM. A baixa toxicidade e o alto limite de detecção indicam que os NBDs devem encontrar aplicações potenciais em sistemas biológicos e ambientais.
Abreviações
- FTIR:
-
Transformada de Fourier Infra-vermelho
- HAADF-STEM:
-
Microscopia eletrônica de transmissão de varredura de campo escuro anular de alto ângulo
- LOD:
-
Limite de detecção
- NBDs:
-
Pontos de nanobiomassa
- NMR:
-
Ressonância magnética nuclear
- PL:
-
Fotoluminescência
- QDs:
-
Pontos quânticos
- QY:
-
Rendimento quântico
- TEM:
-
Microscopia eletrônica de transmissão
- UES:
-
Estratégia de extração ultrassônica
- USEPA:
-
Agência de Proteção Ambiental dos Estados Unidos
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- XRD:
-
Difração de raios X
Nanomateriais
- Demonstração de um biossensor flexível à base de grafeno para detecção sensível e rápida de células cancerosas do ovário
- Nanopartículas multifuncionais de ouro para aplicações diagnósticas e terapêuticas aprimoradas:uma revisão
- Avanços e desafios dos nanomateriais fluorescentes para aplicações biomédicas e de síntese
- N, N-Dimetilformamida regulando a fluorescência de pontos quânticos MXene para a determinação sensível de Fe3 +
- Síntese de pontos quânticos do tipo II / tipo I suprimida por reabsorção / CdS / ZnS Core / Shell Quantum Dots e sua aplicação para ensaio de imunossorvente
- Uma abordagem simples para sintetizar pontos quânticos de carbono fluorescentes de águas residuais de Tofu
- Síntese de pontos quânticos de sulfeto de antimônio solúvel em água e suas propriedades fotoelétricas
- Uma Sonda Fluorescente Resumível BHN-Fe3O4 @ SiO2 Híbrida Nanoestrutura para Fe3 + e sua Aplicação em Bioimagem
- Síntese fácil e ecológica de nanofios de Co3O4 e sua aplicação promissora com grafeno em baterias de íon-lítio
- Razões para o Warpage PCB e suas medidas preventivas



