Uma abordagem simples para sintetizar pontos quânticos de carbono fluorescentes de águas residuais de Tofu
Resumo
Apresentamos uma investigação sobre pontos quânticos de carbono (CQDs) sintetizados a partir de águas residuais induzidas durante a produção de tofu. Descobrimos que as águas residuais de tofu são uma boa fonte de matéria-prima para a produção de CQDs fluorescentes. Os CQDs correspondentes podem ser fabricados simplesmente por meio de reação hidrotérmica para carbonizar a matéria orgânica no serofluido amarelo das águas residuais de tofu. Dois tipos de CQDs podem ser obtidos na água desionizada e na solução de NaOH, respectivamente, onde os CQDs em água (solução de NaOH) podem emitir luz azul (verde) sob a irradiação UV. A partir da espectroscopia de fotoelétrons de raios-X (XPS), foi descoberto que a diferença básica entre esses dois tipos de CQDs é o conteúdo das ligações C – O e C =O na superfície dos CQDs. Essa diferença pode causar diferentes características dos espectros de fotoluminescência (PL) dos CQDs. Com base nos resultados obtidos nas medidas de XPS e PL, propomos um mecanismo para entender e explicar a emissão de luz induzida por fótons por CQDs. Este estudo é relevante para a fabricação e aplicação de CQDs fluorescentes como, por exemplo, materiais de exibição de luz.
Histórico
Tofu, feito de soja, é o alimento diário na China e na comunidade asiática. No passado, o tofu e produtos relacionados eram feitos principalmente por famílias e pequenas fábricas em quantidades relativamente pequenas. Com o vegetariano sendo cada vez mais popular em todo o mundo, a demanda por produtos de tofu tem aumentado rapidamente nas últimas duas décadas, desde que os grandes supermercados internacionais, como WalMart e Carrefour, os venderam como alimentos saudáveis. Hoje em dia, o tofu e produtos relacionados são produzidos principalmente em massa por grandes fábricas no parque industrial da China. No entanto, uma das questões ambientais da produção em massa de tofu no parque industrial são as águas residuais. A produção de produtos de soja resultaria em águas residuais misturadas com serofluido amarelo de soja. Essas águas residuais podem causar poluição ambiental. Por outro lado, o serofluido amarelo de tofu é altamente concentrado em matéria orgânica e contém carboidratos, proteínas, ácidos orgânicos, oligossacarídeos funcionais, nitrogênio não proteico solúvel em água e vitaminas, lipídios e outras substâncias pigmentares. Portanto, é uma boa fonte de matéria-prima na fabricação de pontos quânticos de carbono (CQDs) para óptica, biomedicina e outras aplicações. Assim, a aplicação de águas residuais de tofu para fazer CQDs pode reutilizar os resíduos da produção em massa de tofu e reduzir em grande parte a poluição ambiental. Essas se tornam a principal motivação de nosso presente estudo.
Os pontos quânticos de carbono são uma nova classe de nanomateriais à base de carbono, normalmente com tamanho espacial de 20 nm ou menos [1, 2]. Foi descoberto que os CQDs são de boa solubilidade em água, alta inércia química, baixa toxicidade e excelente biocompatibilidade [3, 4]. Do ponto de vista da física, o espectro de energia eletrônica para um CQD é semelhante a um semicondutor de gap direto. Assim, os CQDs têm sido propostos como materiais fluorescentes para dispositivos ópticos e optoeletrônicos avançados [5, 6]. Nos últimos anos, os CQDs têm sido investigados de forma bastante intensiva. Uma variedade de métodos de fabricação e diferentes fontes de matérias-primas foram aplicadas para realizar os CQDs para aplicações ópticas [5,6,7]. Em geral, a síntese de CQDs pode ser realizada por meio de abordagens top-down e bottom-up [8]. O método top-down é principalmente uma abordagem física na formação de pontos de carbono quebrando ou descascando estruturas maiores de material de carbono, incluindo descarga de arco [9], oxidação eletroquímica [10], oxidação química [11], ablação a laser [12], etc. O método ascendente consiste em empregar pequenas moléculas como precursores para obter CQDs por meio de reações químicas, incluindo combustão [13], microondas [14] e abordagens ultrassônicas [15] junto com síntese de solução química [16], reação hidrotérmica [17 ], etc.
Nos últimos anos, biomassa como palha de trigo [18] e folhas de plantas [19] tem sido amplamente utilizada como fontes de carbono para a síntese de CQDs. Além disso, CQDs fluorescentes solúveis em água foram preparados por tratamentos hidrotérmicos de suco de laranja [20] e bergamota Jinhua [21], que são considerados fontes de carbono. Essa abordagem simples foi aplicada para a síntese em larga escala de CQDs solúveis em água de muitos tipos de fontes derivadas de resíduos de alimentos [22].
Neste estudo, tomamos o serofluido amarelo de tofu como fonte de carbono para sintetizar os CQDs através do emprego do método hidrotérmico para carbonizar a matéria orgânica no serofluido amarelo. Foi apontado [17] que o método hidrotérmico é uma abordagem fácil e de baixo custo que pode ser aplicada à síntese em larga escala e em uma etapa de CQDs fluorescentes solúveis em água. Para aplicação óptica dos CQDs, especialmente como materiais de exibição de luz, é desejável ser capaz de produzir os CQDs fluorescentes que podem emitir radiação azul, verde e vermelha. Nosso atual trabalho de pesquisa está sendo conduzido nessa direção. No presente estudo, preparamos uma série de CQDs fluorescentes para investigação. A microscopia eletrônica de transmissão e a espectroscopia de fotoelétrons de raios-X são aplicadas para a caracterização dos CQDs fabricados. O experimento de fotoluminescência é empregado para medir as propriedades ópticas dos CQDs.
Métodos
Neste estudo, as águas residuais da produção de tofu são retiradas do Parque Industrial de Tofu no Condado de Shi Ping, Yunnan, China. Os processos gerais para sintetizar os CQDs do serofluido amarelo em águas residuais de tofu podem ser descritos como segue:(i) Preparamos os materiais precursores de carbono por meio da pirólise da polpa amarela de tofu em águas residuais. Aqui, 300 ml de xarope de tofu amarelo são colocados no copo de 500 ml e colocados na plataforma de aquecimento para aquecimento constante. Descobrimos que quando a temperatura de aquecimento está em cerca de 93 ° C e o tempo de aquecimento é de 3 a 5 h, o serofluido amarelo de tofu no copo pode ficar completamente seco. (ii) Deixamos o material no copo esfriar naturalmente até a temperatura ambiente e adicionamos 50–200 ml de água desionizada ao copo. (iii) A mistura é agitada magneticamente por 4 min para obter uma mistura uniforme e completa dos materiais e água. (iv) A mistura é levada a um choque ultrassônico de 5 min para quebrar os aglomerados soltos. Assim, podemos obter o sobrenadante que contém pontos de carbono. (v) O sobrenadante é posteriormente centrifugado a uma velocidade de 12.000 r / min durante 20 min, e o sobrenadante adicional pode ser obtido. Como resultado, os CQDs podem ser finalmente adquiridos em água desionizada. Verificou-se que a temperatura de aquecimento, o tempo de aquecimento e o valor do pH da água da polpa amarela no processo de síntese podem afetar fortemente o crescimento dos CQDs. Portanto, os CQDs podem ser fabricados com certas características fluorescentes por meio da variação das condições de síntese acima. Notamos, pela observação a olho nu com a luz do dia, que o sobrenadante com CQDs preparados sob as condições experimentais acima mencionadas parece amarelo. No entanto, pode parecer azul sob a irradiação UV. Chamamos esse tipo de CQDs fluorescentes de CQDs-1 neste artigo.
Ao adotar a abordagem de síntese semelhante, podemos produzir os CQDs usando NaOH como solução para queimar serofluido amarelo de tofu seco após a pirolisação, em vez de usar água desionizada discutida acima. Adicionamos 100 ml de solução de NaOH com um valor de pH de cerca de 12,4. Seguindo os mesmos processos de agitação magnética, choque ultrassônico e centrifugação conforme declarado acima, também podemos adquirir os CQDs dentro da solução de NaOH. Esses CQDs também parecem amarelos quando observados à luz do dia. No entanto, eles podem parecer verdes sob a irradiação UV. Chamamos esse tipo de CQDs fluorescentes de CQDs-2 neste artigo.
Neste trabalho, fizemos dois tipos de CQDs que podem emitir luzes verdes e azuis sob a irradiação UV. A investigação adicional do presente trabalho é conduzida principalmente para esses dois tipos de CQDs realizados a partir de águas residuais de tofu.
Resultados e discussões
Para a caracterização dos CQDs sintetizados a partir de águas residuais de tofu, primeiro realizamos a análise morfológica para esses CQDs. Na Fig. 1, mostramos a imagem típica dos CQDs em água deionizada e solução de NaOH (CQDs-1 e CQDs-2), obtida em microscopia eletrônica de transmissão de alta resolução (TEM). Como podemos ver, os CQDs preparados são esféricos e mono-dispersivos dentro da água desionizada (para CQDs-1) ou solução de NaOH (para CQDs-2). Por meio de uma média estatística da imagem TEM, o tamanho de partícula desses CQDs está na faixa de 2 a 10 nm. Descobrimos que esses CQDs são altamente cristalizados com estrutura típica de rede de carbono. As franjas da rede são claras e o espaçamento da rede correspondente é de cerca de 0,22 e 0,21 nm, respectivamente. Gostaríamos de notar que os resultados mostrados na Fig. 1 são muito semelhantes aos relatados anteriormente para o conteúdo de dopagem N e S em N- e S-CQDs com alto rendimento [23, 24]. Além disso, descobrimos que a distribuição de tamanho dos CQDs em água desionizada (CQDs-1) ou em solução de NaOH (CQDs-2) está localizada principalmente em torno de 3,5-5,5 nm e a espessura desses CQDs é de cerca de 3,5 nm.

a Imagens TEM para CQDs em água deionizada (CQDs-1) e b Imagens TEM para CQDs em solução de NaOH (CQDs-2). c , d Imagem ampliada de um único CQD de a e b , respectivamente
Como sabemos, a espectroscopia de fotoelétrons de raios-X (XPS) é uma ferramenta poderosa para a medição e compreensão das composições elementares e do conteúdo dos CQDs, especialmente para o exame das características de superfície modificada dos CQDs, como os grupos funcionais na superfície dos CQDs [25]. Na Fig. 2, os espectros completos de XPS para CQDs-1 e CQDs-2 são apresentados e os resultados correspondentes são indicados. Notamos que os CQDs medidos aqui contêm principalmente C (com uma energia de ligação típica C ls =284,8 eV), N (com uma energia de ligação típica N ls =400 eV) e O (com uma energia de ligação típica O ls =532 eV ) Os outros elementos como S e P (Na e Cl) também podem ser encontrados em CQDs-1 (CQDs-2). Como resultado, vemos que CQDs-1 é composto principalmente de elementos C, N, O, S e P, em que a razão atômica desses elementos é C1s:O1s:N1s:S2p:P2p =61,0:29,6:8,5 :0,5:0,4. Também vemos que CQDs-2 é composto principalmente de elementos C, O, N, Na e Cl. A razão atômica desses elementos é C1s:O1s:N1s:Na1s:Cl2p =66,7:26,2:6,8:0,1:0,1. Como a água residual de tofu em si contém cloreto e sulfato induzido pelo processo de fabricação de tofu, há espectros bastante amplos de sinais S e Cl na Fig. 2. Além disso, porque CQDs-2 é para CQDs em solução de NaOH em que NaOH pode desempenhar um papel como passivação dos CQDs, há um sinal de Na no painel inferior da Fig. 2.
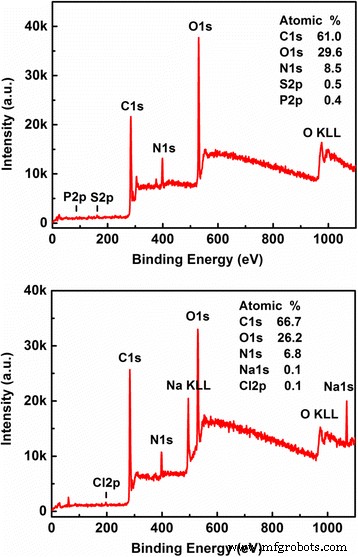
O espectro completo de XPS para CQDs-1 (painel superior) e CQDs-2 (painel inferior), respectivamente, onde os conteúdos obtidos dos elementos são indicados
Na Fig. 3, mostramos os espectros de C1s de alta resolução para CQDs-1 e CQDs-2, respectivamente, ajustados por uma energia de ligação Cls. Pode ser visto a partir do espectro de C1s no painel superior da Fig. 3 que três ligações químicas C – C / C =C em 284,7 eV, C – O em 286,08 eV e C =O em 287,86 eV presentes em CQDs-1 . Existem quatro ligações químicas C – C em 284,8 eV, C – O em 286,16 eV, C =O em 288 eV e COOH em 289,14 eV presentes em CQDs-2, conforme mostrado no painel inferior da Fig. 3. Do Os resultados de XPS mostrados na Fig. 3, aprendemos que a diferença básica entre CQDs-1 e CQDs-2 é o conteúdo das ligações C – O e C =O na superfície dos CQDs em água e solução de NaOH, respectivamente. Sabe-se que o OH - em solução de NaOH pode se acoplar com ligações C – O e C =O na superfície dos CQDs para formar COOH e o grupo carboxila e, assim, reduzir o conteúdo dos grupos C – O e C =O em CQDs-2. Esta é a principal razão pela qual os conteúdos das ligações C – O e C =O em CQDs-1 são marcadamente maiores do que aqueles em CQDs-2.
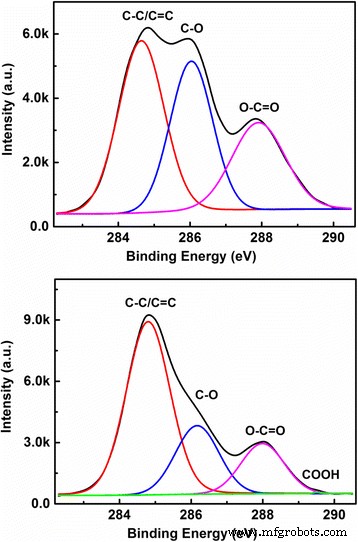
O espectro de C1s de alta resolução para CQDs-1 (painel superior) e CQDs-2 (painel inferior), respectivamente, ajustado por uma energia de ligação C1s
Neste estudo, tomamos uma configuração experimental padrão para medir a emissão de fotoluminescência (PL) de CQDs realizada a partir de águas residuais de tofu na largura de banda visível. O sistema de fluorescência HORIBA (EUA) é aplicado para a medição, onde uma lâmpada de xenônio é considerada como fonte de luz de excitação de banda larga, o monocromador GEMIMI 180 é usado para escolher o comprimento de onda de bombeamento óptico e o espectrômetro de grade iHR320 junto com um multiplicador fotoelétrico O detector de tubo (PMT) é usado para registrar o espectro da emissão de luz das amostras. As medições são realizadas à temperatura ambiente. Na Fig. 4, mostramos os espectros de emissão PL para CQDs-1 no painel superior e CQDs-2 no painel inferior em diferentes comprimentos de onda de excitação λ ex . Para a medição PL, o registro da intensidade da luz de emissão geralmente começa após o comprimento de onda de excitação para anular o dano do detector PMT. Assim, houve cortes nas curvas dos espectros de PL na Fig. 4. Notamos as seguintes características:(i) A intensidade da emissão de PL primeiro aumenta e depois diminui com o aumento do comprimento de onda de excitação. A emissão de PL mais forte pode ser observada em cerca de λ ex ~ 410 nm para CQDs-1 e 480 nm para CQDs-2, respectivamente. (ii) A posição do comprimento de onda de pico λ em no espectro PL varia com a alteração do comprimento de onda de excitação para ambos CQDs-1 e CQDs-2. Nas inserções da Fig. 4, mostramos λ em como uma função de λ ex então podemos ver mais claramente como os picos PL mudam com o comprimento de onda de excitação. Conforme mostrado na Fig. 4, λ em aumenta monotonamente com λ ex para CQDs-1 e CQDs-2. (iii) Em regime de comprimento de onda de excitação relativamente mais curto, dois picos PL podem ser observados para CQDs-1, enquanto apenas um pico PL pode ser visto para CQDs-2 ao longo do regime de comprimento de onda de 420-510 nm. (iv) CQDs-1 pode resultar em um espectro de PL mais amplo do que CQDs-2. (v) O comprimento de onda de pico PL induzido por CQDs-1 é mais curto do que aquele induzido por CQDs-2. Em comprimento de onda de excitação de 410 nm, a fluorescência azul pode ser alcançada por CQDs-1, enquanto em comprimento de onda de excitação de 480 nm, a fluorescência verde pode ser vista para CQDs-2. (vi) A fluorescência dos CQDs-1 com 8,5% de conteúdo de N-dopagem é maior do que a dos CQDs-2 com 6,8% de conteúdo de N-dopagem. A razão pela qual a emissão de PL aumenta com o conteúdo de N-dopagem dos CQDs é que a N-dopagem pode introduzir um novo tipo de estado de superfície. Elétrons aprisionados pelos novos estados de superfície formados são capazes de facilitar um alto rendimento de recombinação da radiação [24]. Os resultados de PL obtidos neste estudo indicam que a emissão de luz azul e verde pode ser obtida por CQDs-1 e CQDs-2, respectivamente, sob bombeamento óptico.
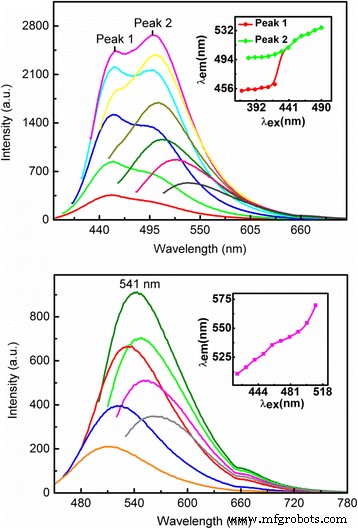
O espectro PL para CQDs-1 no painel superior e CQDs-2 no painel inferior em diferentes comprimentos de onda de excitação λ ex . No painel superior, λ ex são 370 nm (vermelho), 380 nm (verde), 390 nm (azul), 400 nm (azul claro), 410 nm (rosa escuro), 420 nm (amarelo), 430 nm (verde claro), 440 nm (escuro verde), 450 nm (vermelho claro) e 490 nm (verde oliva escuro). No painel inferior, λ ex são 420 nm (laranja), 440 nm (azul), 460 nm (amarelo), 480 nm (vermelho), 490 nm (verde), 500 nm (rosa) e 510 nm (verde oliva escuro). As inserções mostram o comprimento de onda de pico no espectro PL, λ em, como a função do comprimento de onda de excitação
No momento, o mecanismo físico para a emissão de luz induzida por fótons de CQDs ainda não está claro. No entanto, os resultados obtidos em investigações relacionadas [12, 26, 27] mostraram que a modificação da superfície dos CQDs por grupos funcionais amino e carboxila pode desempenhar um papel importante para a emissão de PL dos CQDs. As características do espectro de PL dos CQDs são determinadas não apenas pelo tamanho de partícula dos CQDs [1], mas também pelas propriedades de superfície dos CQDs [26, 27]. Com base em nossos resultados de XPS e PL obtidos no presente estudo, agora discutimos o mecanismo físico por trás dos resultados experimentais mostrados na Fig. 4 para CQDs realizados a partir de águas residuais de tofu. Sabemos que a estrutura de banda eletrônica dos CQDs é muito semelhante à de um semicondutor de gap direto. No entanto, para CQDs sintetizados a partir de águas residuais de tofu em diferentes soluções, como água e NaOH, existem grupos funcionais baseados em ligações C – O, C =O e COOH na superfície dos CQDs, conforme mostrado pelos resultados de XPS na Fig. 3. Os estados de energia desses grupos funcionais são estados de superfície que estão localizados entre as bandas de condução e valência dos CQDs. Eles desempenham um papel como estados intermediários, muito semelhantes aos estados de impureza em um semicondutor de gap direto. Na presença de campo de luz de excitação, os elétrons na banda de valência dos CQDs são bombeados para a banda de condução por meio do mecanismo de absorção óptica. Como a posição do pico de PL no espectro depende do comprimento de onda de excitação, a emissão de PL via mecanismo excitônico [28] não é o caso para esses CQDs. A emissão de luz induzida por fótons de CQDs é, portanto, uma consequência da fotoemissão direta induzida por transições eletrônicas de níveis de energia mais altos para estados de energia mais baixos. Como sabemos, os elétrons normalmente têm um tempo de relaxamento mais rápido ou menor nos estados de energia mais alta do que nos estados de energia mais baixa. Os resultados de nossas medições XPS e PL sugerem que a transição eletrônica radiativa em CQDs é obtida principalmente por meio do relaxamento de elétrons dos estados de superfície para a banda de valência dos CQDs. Os resultados experimentais obtidos mostram que a intensidade da emissão de PL dos CQDs preparados por KOH é muito mais forte do que aquela preparada por NaOH. Com o mesmo comprimento de onda de excitação, descobrimos que o íon alcalino em soluções alcalinas não afeta significativamente a posição do comprimento de onda de emissão PL.
Para o caso em que os CQDs estão na água (CDQs-1), existem dois estados intermediários induzidos pelos estados de superfície das ligações C – O e C =O e grupos funcionais relacionados. Esses dois estados de superfície estão com diferentes níveis de energia e regras de seleção correspondentes para transições eletrônicas radiativas, que são responsáveis pela emissão de PL com dois comprimentos de onda de emissão sob excitação de luz de comprimento de onda relativamente curto. Os elétrons fotoexcitados nos estados de energia mais alta na banda de condução dos CQDs primeiro relaxam rapidamente nos estados de superfície por meio do mecanismo de relaxamento não radiativo, como o espalhamento elétron-fônon e a interação elétron-elétron. Quando o tempo de relaxamento eletrônico não radiativo para elétrons nos estados de superfície é maior ou maior do que o tempo de relaxamento eletrônico radiativo, esses elétrons podem voltar para a banda de valência e emitir fótons. Com a diminuição do comprimento de onda de bombeamento, mais estados na banda de valência e especialmente na banda de condução podem tomar parte neste processo de bombeamento, relaxamento e emissão de luz e, assim, o comprimento de onda de pico no espectro de emissão de luz diminui com o comprimento de onda de excitação. Portanto, o comprimento de onda da emissão de luz depende do comprimento de onda da luz de excitação. O aumento no comprimento de onda de pico da emissão de luz com comprimento de onda de excitação implica que o tempo de relaxamento eletrônico não radiativo aumenta com a redução dos níveis de energia nos estados de superfície. Para excitação de luz de comprimento de onda relativamente longo, os elétrons fotoexcitados em CQDs são rapidamente relaxados da banda de condução para os níveis de energia mais baixos dos estados de superfície e emitem fótons. A possibilidade de emissão de fótons de níveis de energia mais elevados dos estados de superfície torna-se baixa o suficiente para que o efeito não possa ser medido de forma marcante.
Para o caso em que os CQDs estão em solução de NaOH (CDQs-2), existe apenas um estado intermediário para as transições eletrônicas radiativas. Como os conteúdos das ligações C – O e C =O e do grupo funcional relacionado são relativamente baixos neste caso, os estados de superfície radiativa são principalmente grupos baseados em COOH induzidos para CQDs-2. Como resultado, apenas um pico de emissão de PL pode ser observado. Uma vez que os níveis de energia dos estados de superfície induzidos por ligações C – O e C =O e grupos funcionais relacionados são normalmente maiores do que aqueles induzidos por grupos COOH, a emissão de PL de comprimento de onda mais curto pode ser observada para CQDs-1. Esta é a principal razão pela qual os CQDs-1 podem emitir luz azul, enquanto os CQDs-2 podem emitir luz verde sob excitação óptica.
A eficiência quântica Q da fluorescência para CQDs-1 pode ser avaliada a partir dos dados experimentais via [29, 30]
$$ Q ={Q} _ {\ mathrm {s}} \ times \ frac {I _ {\ mathrm {s}}} {I} \ times \ frac {A} {A _ {\ mathrm {s}}} \ vezes \ frac {\ eta ^ 2} {{\ eta _ {\ mathrm {s}}} ^ 2} $$ (1)
Aqui Q s é a eficiência quântica da fluorescência de uma amostra padrão para referência. Sob um comprimento de onda de excitação fixo em, por exemplo, 364 nm, I e eu s são as intensidades de emissão integradas da amostra CQDs-1 e da amostra padrão, respectivamente. A e A s são, respectivamente, a absorbância da amostra preparada e da amostra padrão no mesmo comprimento de onda de excitação. η e η s são, respectivamente, a refratividade da amostra preparada e da amostra padrão. Verificou-se que a eficiência quântica fluorescente de CQDs-1 é de cerca de 54,49%. Como não conseguimos encontrar a amostra de referência para CQDs-2, a eficiência quântica fluorescente de CQDs-2 não foi avaliada no presente estudo.
Conclusões
Neste estudo, fabricamos os pontos quânticos de carbono (CQDs) a partir de águas residuais induzidas durante a produção de tofu. Demonstramos que as águas residuais de tofu são uma boa fonte de matéria-prima para a produção de CQDs. Os CQDs fluorescentes podem ser fabricados simplesmente por meio de reação hidrotérmica para carbonizar a matéria orgânica no serofluido amarelo das águas residuais de tofu. O tamanho médio dos CQDs sintetizados a partir de águas residuais de tofu pode ser de até 3,5 nm. Obtivemos dois tipos de CQDs na água desionizada e na solução de NaOH, respectivamente. Eles podem emitir luzes azuis e verdes, respectivamente, sob a irradiação UV. A partir da espectroscopia de fotoelétrons de raios-X (XPS), foi descoberto que a diferença básica entre esses dois tipos de CQDs é o conteúdo das ligações C – O e C =O na superfície dos CQDs. Essa diferença pode causar diferentes características do espectro de fotoluminescência (PL) dos CQDs. Com base nos resultados obtidos nas medições de XPS e PL, propusemos um mecanismo para entender e explicar a emissão de luz induzida por fótons por CQDs. Uma das conclusões mais significativas obtidas neste estudo é que o uso de águas residuais de tofu para sintetizar os CQDs pode ser não apenas útil para fornecer uma solução para o problema ambiental causado pelas águas residuais, mas também promissor para a produção em massa simples e de baixo custo de CQDs para aplicações bio e ópticas. Até agora, obtivemos com sucesso os CQDs fluorescentes azul e verde de águas residuais de tofu. O desafio do nosso trabalho atual é obter os CQDs que possam emitir luz vermelha sob bombeamento óptico.
Nanomateriais
- N, N-Dimetilformamida regulando a fluorescência de pontos quânticos MXene para a determinação sensível de Fe3 +
- Fibras de carbono ativado com nanoestrutura hierárquica derivada de luvas de algodão como eletrodos de alto desempenho para supercondensadores
- Síntese de pontos quânticos de carbono co-dopados com N, S ricos em piridínicos como imitações de enzimas eficazes
- Nanopartículas de sílica para entrega de proteína intracelular:uma nova abordagem de síntese usando proteína fluorescente verde
- Síntese verde de pontos quânticos InP / ZnS Core / Shell para aplicação em diodos emissores de luz livres de metais pesados
- Microesferas de carbono magnético como um adsorvente reutilizável para remoção de sulfonamida da água
- Eliminação do tamanho bimodal em pontos quânticos InAs / GaAs para preparação de lasers de pontos quânticos de 1,3 μm
- Material e propriedades ópticas de pontos quânticos de carbono fluorescente fabricados a partir de suco de limão via reação hidrotérmica
- Projeto de pontos quânticos GeSn / GeSiSn com engenharia de tensão para emissão de bandgap direta de infravermelho médio no substrato de Si
- Síntese fácil em um vaso de pontos de carbono de polidopamina para terapia fototérmica



