Nanopartícula de sílica decorada com membrana de células cancerosas carregada com miR495 e doxorrubicina para superar a resistência aos medicamentos para uma terapia eficaz contra o câncer de pulmão
Resumo
A terapia atual do câncer geralmente sucumbe a muitas barreiras extracelulares e intracelulares, entre as quais a distribuição não direcionada e a resistência a múltiplas drogas (MDR) são duas dificuldades importantes responsáveis pelo mau resultado de muitos sistemas de distribuição de drogas (DDS). Aqui, em nosso estudo, o dilema foi abordado pelo desenvolvimento de nanopartículas de sílica revestida com membrana de células cancerosas (CCM) (SLI) para co-entregar miR495 com doxorrubicina (DOX) para terapia eficaz de câncer de pulmão (CCM / SLI / R-D). Supunha-se que o CCM homólogo de células de câncer de pulmão MDR (A549 / DOX) aumentava a propriedade de homing do DDS para contornar as barreiras extracelulares. Além disso, o MDR das células cancerosas foi conquistado através da regulação negativa da expressão da glicoproteína P (P-gp) usando miR495. Foi provado que miR495 pode diminuir significativamente a expressão de P-gp, que eleva o acúmulo de droga intracelular em A549 / DOX. Os resultados in vitro e in vivo exibiram que CCM / SLI / R-D mostrou um efeito terapêutico muito melhorado em A549 / DOX, que foi superior à aplicação de miR495 ou DOX sozinho. O efeito preferível de CCM / SLI / R-D em conquistar o MDR no câncer de pulmão fornece uma nova alternativa para a quimioterapia eficaz de cânceres MDR.
Introdução
Estudos recentes estão oferecendo evidências acumuladas para as correlações positivas entre a multirresistência (MDR) e o fracasso da quimioterapia [1, 2]. Um dos mecanismos mais amplamente reconhecidos para MDR é o transportador de cassete de ligação de ATP (ABC), entre o qual a glicoproteína P (gp-P) é a mais estudada [1, 3]. Verificou-se que a P-gp pode efetivamente bombear quimioterápicos intracelulares para fora das células, levando ao acúmulo de droga intracelular reduzido, como resultado seguido pela eficácia reduzida [4, 5]. A inibição da gp-P tem mostrado efeitos benéficos na superação da MDR, o que pode ser um alvo potencial para combater a MDR.
MicroRNAs (miRNA) são um tipo de RNA não codificante de ocorrência natural. No entanto, miRNA mostra papéis importantes na regulação da transfecção celular e expressão de proteínas [6]. Como resultado, foi relatado que a expressão da P-gp é afetada por vários miRNAs que dependem dos tipos de tumor [7]. Estudo anterior revelou que miR495 poderia efetivamente diminuir a expressão da P-gp em células de câncer ovariano e gástrico MDR [8]. Aqui, neste estudo, miR495 foi empregado para explorar ainda mais seu papel na regulação da P-gp em células de câncer de pulmão MDR.
Devido às vantagens incomparáveis, como efeitos colaterais muito reduzidos juntamente com aumento da biodisponibilidade, os sistemas de entrega de medicamentos (DDS) cresceram nas últimas décadas e foram reconhecidos como a alternativa aos medicamentos gratuitos na entrega de medicamentos, especialmente na terapia do câncer [9,10 , 11,12]. Como resultado, o desenvolvimento de DDS multifuncional capaz de vencer as complicadas barreiras extracelulares e intracelulares da terapia do câncer e, ao mesmo tempo, adequado para o carregamento de vários tipos de drogas está se tornando o foco de pesquisa [13,14,15,16]. Nanopartículas de sílica (SLI), como um dos candidatos mais amplamente adotados, têm virtudes versáteis, como fácil preparação, alta capacidade de carga de fármaco e boa biocompatibilidade e são nanocarreadores preferíveis. Naturalmente, o SLI tem sido usado por muitos DDS como o nanocarreador para alcançar eficácia satisfatória [17, 18].
No entanto, estudos pré-clínicos revelaram que a entrega direcionada de DDS também é vital para o sucesso da terapia do câncer. Para alcançar um melhor efeito de direcionamento, a abordagem mais comumente adotada é modificar os ligantes de direcionamento na superfície do DDS, que podem se ligar aos receptores correspondentes na superfície das células cancerosas [16, 19, 20]. De pequenas moléculas (peso molecular abaixo de 1000 Da) a anticorpos monoclonais (peso molecular acima de 10 kDa), foi relatado que esses ligantes de direcionamento foram aplicados com sucesso ao DDS [21,22,23]. No entanto, devido à natureza ectogênica de alguns ligantes ou outros motivos, ocorreram efeitos adversos como imunorreação e citotoxicidade. Nos últimos anos, as membranas plasmáticas celulares estão se tornando outro material promissor não apenas para modificar a superfície das nanopartículas, mas também para servir como um componente de direcionamento biocompatível. Com base na interação entre a membrana da célula cancerosa homóloga (CCM) com as células cancerosas, foi demonstrado que o CCM aumenta muito a capacidade de homing do DDS [24, 25].
A fim de combinar a propriedade de homing tumor de CCM e P-gp visando miR495 em um DDS para terapia de coquetel de câncer de pulmão (selecionado como um câncer modelo em nosso estudo), a amina SLI carregada positivamente foi fabricada e pré-carregada com doxorrubicina (DOX ) A amina SLI carregada com DOX foi subsequentemente carregada com miR495 para formar o núcleo de co-entrega (SLI / R-D). Finalmente, o SLI / R-D foi decorado com CCM carregado negativamente (adquirido de células A549 / DOX) para preparar um DDS de co-entrega e direcionamento a tumor (CCM / SLI / R-D). Esperava-se que o CCM pudesse guiar especificamente o CCM / SLI / R-D para a célula A549 / DOX homogênea para aumentar seu efeito de direcionamento ao tumor e aumentar a absorção intracelular. Enquanto isso, o miR495 lançado pode superar o MDR de A549 / DOX e atingir o efeito anticâncer sinérgico com DOX.
Materiais e métodos
Materiais
Metiltiazolil tetrazólio (MTT), N - (2-aminoetil) -3-aminopropiltrimetoxissilano (AEAPS), tetraetil ortossilicato (TEOS), doxorrubicina (DOX) e Triton X-100 foram obtidos da Sigma-Aldrich (St. Louis, MO, EUA). O miR495 foi fornecido pela Cell Biolabs Inc. (San Diego, CA, EUA). Outros produtos químicos e reagentes foram obtidos na Aladdin Co., Ltd (Shanghai, China) e de pureza analítica.
Cultura de células e modelo animal
As linhas celulares A549 (carcinoma de pulmão humano), A549 / DOX (linha celular resistente a DOX) e NIH3T3 (fibroblasto embrionário de camundongo) foram cultivadas em DMEM suplementado com 10% (v / v) de soro fetal bovino (FBS), penicilina (100 U / mL) e estreptomicina (100 U / mL) em uma incubadora de temperatura constante a 37 ° C contendo 5% de CO 2 . O A549 / DOX (linha de células resistentes a DOX) foi estabelecido incubando células A549 com concentração gradualmente aumentada de DOX como relatado [26]. Todas as linhas de células foram cultivadas em protocolo padrão, conforme relatado anteriormente [27]. Ratinhos nus Balb / c machos (~ 20 g) foram obtidos do Institute of Model Animal, Wuhan University (Wuhan, China), e foram criados com protocolos padrão. O modelo de xenoenxerto de tumor A549 / DOX foi estabelecido com base no artigo anterior [28]. Todos os experimentos relacionados a animais foram aprovados pelo Comitê de Ética institucional do Terceiro Hospital Afiliado da Sun Yet-sen University.
Modelo esferóide de tumor multicelular
O tumor esferóide multicelular (MCTS) foi estabelecido com base em relatório anterior [29]. Em resumo, uma placa de 96 poços (Corning, EUA) foi coberta com solução de agarose autoclavada para criar uma almofada de gel. Posteriormente, células A549 / DOX e NIH3T3 (1:1) misturadas foram semeadas na placa e incubadas para formar MCTS. A formação de MCTS foi monitorada por microscópio óptico (CX 23, Olympus, Japão).
Preparação de CCM / SLI / R-D
A fabricação da amina SLI foi realizada em uma microemulsão de água em óleo com base no relatório anterior [30]. Resumidamente, uma microemulsão de água em óleo contendo DOX foi fabricada em temperatura ambiente. Depois, AEAPS, TEOS e NH 4 OH foram adicionados sucessivamente para desencadear a reação. Após reagir por 24 h, a amina SLI carregada com DOX foi precipitada usando uma quantidade em excesso de etanol e coletada por centrifugação (3000 rpm, 10 min).
O miR495 foi dissolvido em tampão HEPES e adicionado gota a gota à solução aquosa de amina SLI carregada com DOX em várias relações peso / peso (p / p) com vórtice para obter complexos binários SLI / R-D [31].
O isolamento de CCM de células A549 / DOX foi realizado com base em relatório anterior [32]. Em resumo, as células A549 / DOX foram coletadas e concentradas por centrifugação. Posteriormente, as células foram dispersas em tampão de extração e posteriormente centrifugadas (10.000 g , 10 min), seguido por uma segunda ultracentrifugação (100.000 g , 60 min) para finalmente obter o CCM. Todos os procedimentos foram realizados a 4 ° C. A concentração de proteína de CCM foi quantificada usando um kit BCA (Beyotime, Shanghai, China).
O revestimento de CCM em SLI / R-D usou protocolo semelhante ao de ligação miR495. Em resumo, diferentes volumes de solução de CCM foram adicionados a SLI / R-D (1 mg / mL) sob vórtice. Finalmente, a mistura foi tratada com sonicação do tipo de sonda (100 W, 5 min) e, em seguida, foi centrifugada (10.000 g , 10 min) para obter o CCM / SLI / R-D.
Caracterização
A distribuição de tamanho e o potencial zeta de CCM / SLI / R-D foram avaliados por um Zetasizer (ZS90, Malvern, Reino Unido). Além disso, o microscópio eletrônico de transmissão (TEM, JEM1230, JEOL, Japão) foi aplicado para observar a morfologia dos nanocarreadores.
A capacidade de ligação de SLI a miR495 foi estudada por ensaio de retardamento em gel com miR495 nu como controle. O SLI / RD formulado em várias razões p / p (0,2-25, SLI para miR495) foi carregado em gel de agarose a 2% contendo Goldview (Solarbio Science &Technology Co., Ltd., Pequim) e eletroforese em 0,5 × Tris-Borato Tampão -EDTA (90 V, 60 min). A visualização do miR495 foi realizada com o analisador Gel-Pro (Genegenius, Syngene, UK).
O tampão de lise (Beyotime, Shanghai) foi usado para extrair a proteína total do CCM, após o qual o kit BCA foi usado para quantificação da concentração. Em seguida, as amostras foram transferidas para membrana de poli (fluoreto de vinilideno) (PVDF). Finalmente, a membrana foi corada com os primeiros anticorpos correspondentes (Abcam, EUA) e segundos anticorpos (Abcam, EUA). O densitômetro (E-Gel Imager, Thermo-Fisher, EUA) foi usado para a visualização.
O conteúdo de carga de droga (DLC) de CCM / SLI / R-D foi determinado emergindo os nanocarreadores como preparados em metanol por 48 h. As amostras foram centrifugadas (10.000 rpm, 30 min), e os sobrenadantes coletados para a determinação da DOX por cromatografia líquida de alta eficiência (CLAE) [33]. O carregamento de miR495 foi determinado por absorvância de UV a 260 nm (UV5Nano, METTLER TOLEDO, Suíça).
As mudanças de tamanho de partícula de CCM / SLI / R-D em PBS e plasma de camundongo foram registradas em cada ponto de tempo dentro de 48 h. O perfil de liberação de DOX de CCM / SLI / R-D foi investigado de acordo com relatório anterior [34].
Transfecção intracelular
As células A549 / DOX foram semeadas em placas de 6 poços por 24 h e, em seguida, cultivadas com CCM / SLI / miR495 (concentrações de miR495, 1-25 ng / mL) por 48 h. Posteriormente, as células foram destacadas, colhidas e submetidas à análise de Western blot da expressão de P-gp.
A concentração intracelular do fármaco foi determinada de acordo com relatório anterior [23]. Em resumo, depois de tratadas com CCM / SLI / miR495 por diferentes intervalos de tempo, as células A549 / DOX foram incubadas com DOX. Em intervalos de tempo predeterminados (4 e 8 h), as células foram destacadas, coletadas e dispersas em 5 mL de solução extratora de DOX (etanol 0,6 M HCl, 1:1, v / v), seguido por ultrassonicação a 400 W em banho de gelo por 40 vezes. A mistura foi deixada a 4 ° C durante 24 h e centrifugada a 12.000 rpm (4 ° C) durante 10 min. O sobrenadante foi coletado e submetido à medição do conteúdo de DOX conforme descrito acima.
Viabilidade celular
O efeito de citotoxicidade de nanocarreadores livres de drogas (10–200 μg / mL) e CCM / SLI / RD (concentração de DOX, 2-50 μM; a concentração de miR495, 10–250 nM; a razão molar entre DOX e miR495 foi fixada em 200) em células A549 / DOX por 48 h foi determinado por ensaio de brometo de 3- (4,5-dimetiltiazol-2-il) -2,5-difeniltetrazólio (MTT). As variações de nível de proteínas relacionadas à apoptose também foram determinadas usando o ensaio de Western blot.
MCTS com diâmetros de 300-400 μm foi incubado com o meio contendo diferentes formulações (concentração de DOX, 25 μM) a 37 ° C por 5 dias. Um microscópio óptico foi usado para registrar as mudanças de diâmetro do MCTS.
Segmentação In Vitro e In Vivo de CCM / SLI / R-D
O siRNA marcado com FAM foi adotado para construir o DDS. As células A549 / DOX foram semeadas em placas de 6 poços por 24 h. Em seguida, as células foram incubadas com CCM excessivo por 2 h, e SLC / siRNA e CCM / SLC / siRNA foram adicionados. Nos intervalos de tempo definidos, as células foram coletadas e determinadas por citômetro de fluxo (FCM, FC500MCL, Beckman Coulter) para quantificação.
O miR495 marcado com Cy5 foi adotado para construir o DDS. Os ratinhos com tumor A549 / DOX foram i.v. injetado com SLI / miR495 e CCM / SLI / miR495, e a distribuição de miR495 foi monitorada em intervalos de tempo predeterminados usando sistema de imagem em tempo real (ZEWTON 7.0, Vilber, França). Após a administração por 12 h, os tumores e os órgãos principais foram obtidos dos camundongos sacrificados e fotografados usando o mesmo sistema para análise analítica.
Ensaio anticâncer In Vivo
O ensaio anticâncer in vivo de CCM / SLI / R-D foi avaliado usando camundongos com tumor A549 / DOX. Em detalhes, os ratos foram divididos aleatoriamente em 5 grupos ( n =6):(1) solução salina (como controle), (2) DOX livre, (3) CCM / SLI / DOX, (4) CCM / SLI / miR495 e (5) CCM / SLI / R-D. Posteriormente, os camundongos foram administrados por via intratumoral com as formulações na dosagem de 5 mg / kg de DOX e 0,25 mg / kg de miR495 por 7 vezes em 14 dias. Os volumes do tumor e os pesos corporais dos camundongos em cada grupo foram determinados a cada 2 dias.
Resultados e discussão
Preparação de CCM / SLI / R-D
Para alcançar boa capacidade de carga de droga e biocompatibilidade em um DDS, a hidrólise síncrona de TEOS e AEAPS na microemulsão de água em óleo foi usada para a fabricação de SLI. DOX foi pré-aprisionado na matriz de SLI durante a fabricação. Como mostrado na Fig. 1a, o resultado de espalhamento dinâmico de luz (DLS) demonstrou que a amina SLI carregada com DOX tinha um diâmetro de ~ 100 nm. A imagem TEM revelou ainda que as nanopartículas eram de formato esférico com distribuição estreita, o que estava de acordo com os resultados obtidos por DLS.
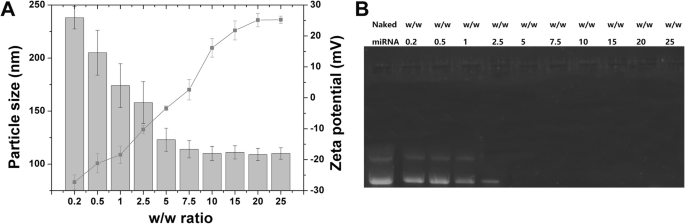
a Mudanças de tamanho e potencial zeta de SLI / R-D em diferentes proporções de peso / peso. b O ensaio de ligação de miRNA de complexos binários SLI / R-D em várias razões de peso / peso. Os dados foram apresentados como média ± DP ( n =3)
A amina SLI carregada com DOX tinha um potencial de superfície de 26,83 mV, que foi benéfico para servir como transportador miR495. De acordo com relatório anterior [31], a montagem de miR495 e SLI para formar complexos binários foi conduzida por interação eletrostática. O w / w SLI para miR495 nos complexos binários exerce impacto significativo na eficiência de transfecção final. Conforme exibido na Fig. 1a, devido ao fato de que miR495 é uma macromolécula carregada negativamente, em baixa razão p / p de SLI para miR495, os complexos binários mostraram uma carga superficial negativa com tamanho de partícula significativamente aumentado, o que pode ser devido a a adesão de nanopartículas vizinhas. No entanto, com o incremento da relação peso / peso, a carga superficial dos complexos binários tornou-se gradualmente positiva com um tamanho de partícula estável observado em torno de 100 nm. Foi mostrado que quando a razão p / p atingiu 20, tanto o tamanho da partícula quanto o potencial de superfície dos complexos binários permaneceram estáveis sem mudança significativa com o aumento da razão p / p.
As capacidades de ligação e proteção dos nanocarreadores para miR495 são vitais para a entrega do gene. A capacidade de ligação ao miR495 de SLI foi avaliada por ensaio de retardamento em gel. Como mostrado na Fig. 1b, miR495 nu não mostrou nenhum retardo enquanto a adição de SLI mudou significativamente o comportamento de miR495. Foi observado que o SLI mostrou capacidade crescente de ligação ao miR495 com o incremento da razão p / p, que alcançou o retardo completo de miR495 na razão p / p de 5.
Resumindo, inferiu-se que os complexos binários na razão w / w de 20 com tamanho de partícula adequado e carga superficial desejável, bem como ligação de miR495 eficaz e propriedade de proteção, foram a formulação ideal que foi selecionada como o modelo a ser executado os seguintes experimentos.
Em seguida, exploramos a proporção ideal de proteína CCM para os complexos binários, misturando CCM com complexos binários em diferentes proporções de massa (SLI para proteína CCM, p / p). A proporção ótima foi determinada pelo tamanho de partícula resultante e carga superficial em diferentes condições. Como mostrado na Fig. 2a, a adição de CCM (carga negativa) resultou em uma flutuação significativa no tamanho do produto, mas diminuição contínua na carga superficial. Os resultados indicaram que o CCM foi ancorado com sucesso na superfície de complexos binários. Mais importante ainda, foi observado que tanto o tamanho de partícula quanto a carga superficial de CCM / SLI / R-D atingiram um patamar na razão de massa de 7,5 e que o CCM adicional mostrou impacto insignificante nas cargas superficiais e apenas um ligeiro aumento no tamanho. Para ser específico, o diâmetro da nanopartícula atingiu 121,28 ± 3,36 nm e o potencial zeta mudou para - 28,04 ± 2,64 mV, que foi semelhante à carga superficial do CCM livre (- 27,95 ± 3,06 mV), sugerindo que a decoração do CCM atingiu a saturação nesta condição. Como resultado, o CCM / SLI / R-D na razão de massa de 7,5 foi selecionado como a formulação do modelo para realizar os seguintes experimentos.
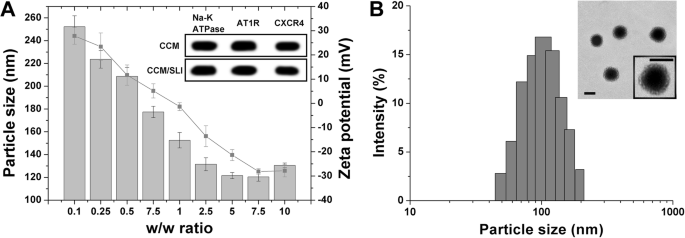
a Mudanças de tamanho e potencial zeta de CCM SLC / R-D em diferentes proporções de peso / peso. A imagem inserida foi uma análise de bolt ocidental das três proteínas representativas em CCM e CCM / SLI / R-D. b A distribuição de tamanho e TEM de CCM / SLI / R-D. Os dados foram apresentados como média ± DP ( n =3). Barras de escala 100 nm
Caracterização de CCM / SLI / R-D
Relatórios anteriores mostraram que proteínas em CCM são capazes de homing células tumorais homólogas quando adotadas para modificar nanopartículas [35, 36]. Portanto, três proteínas de membrana (Na-K ATPase, AT1R e CXCR4) foram selecionadas e seus níveis de expressão em CCM foram comparados com CCM / SLI / R-D. Como mostrado na imagem inserida da Fig. 2a, a quantidade de todas as três proteínas em CCM mostrou intensidade semelhante à de CCM / SLI / RD, o que demonstrou que proteínas integradas em CCM foram herdadas de CCM / SLI / RD após o revestimento e o perda ou degradação foi insignificante durante este processo. Este resultado também forneceu evidências sólidas para confirmar a construção bem-sucedida de CCM / SLI / R-D, que foi benéfica para o aumento do homing tumoral de CCM / SLI / R-D.
A distribuição de tamanho e morfologia de CCM / SLI / R-D também foram estudadas usando DLS e TEM. Como mostrado na Fig. 2b, DLS revelou que CCM / SLI / RD foi estreitamente distribuído em cerca de 120 nm, enquanto TEM mostrou que CCM / SLI / RD foi caracterizado como uma estrutura de concha central esférica e uma bicamada lipídica pode ser claramente observada na superfície camada.
O DLC de DOX em CM / SLI / R-D (determinado por HPLC) pode ser tão alto quanto 17,96%, e o carregamento de miR495 (determinado por espectrofotômetro UV) pode ser tão alto quanto 1,64%.
Estudos anteriores concluíram vários requisitos preliminares para a entrega segura de moléculas de drogas. Em primeiro lugar, o DDS adotado deve ser mantido estável sem variações dramáticas de tamanho em ambientes fisiológicos, uma vez que o tamanho das partículas contribuiu com significância crítica para o destino in vivo do sistema [10, 37]. Como resultado, a estabilidade dependente do tempo de CCM / SLI / R-D foi investigada. A fim de determinar a estabilidade coloidal de CCM / SLI / R-D em ambientes fisiológicos, as mudanças de tamanho de DDS em PBS (pH 7,4) e plasma de camundongo foram registradas até 48 h. Conforme exibido na Fig. 3a, CM / SLN / Ce6 poderia efetivamente manter seu tamanho durante toda a faixa de teste sem variações significativas. Portanto, concluiu-se que o CCM / SLI / R-D foi capaz de se manter estável em condição fisiológica. Conforme mostrado na Fig. 3b, o CCM / SLI / RD poderia preservar a estabilidade na condição extracelular (32,76% dos medicamentos sendo liberados após 120 h de incubação), indicando que durante o processo de entrega, o CCM / SLI / RD poderia encapsular com segurança o molécula de droga carregada sem induzir efeitos adversos potenciais. Mais importante ainda, ao entrar nas células e serem submetidos ao ambiente ácido das células cancerosas, os medicamentos foram prontamente liberados (75,93%), o que pode ser atribuído à alta concentração de hidrogênio que enfraquece a combinação de medicamentos e transportadores [6, 38].
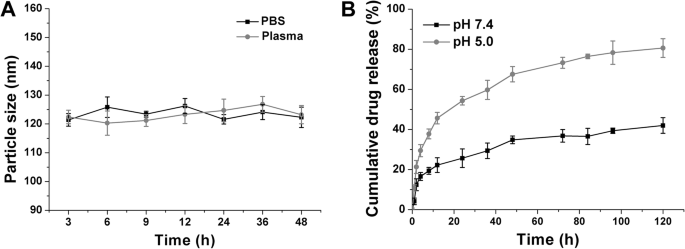
a Estabilidade coloidal de LCC / R-A em PBS (pH 7,4) e plasma de camundongo a 37 ° C por até 48 h. b Perfis de liberação de drogas de DOX do LCC / R-A em meios de liberação sob condições extracelulares e intracelulares de pHs (7,4 e 5,5). Os dados foram apresentados como média ± DP ( n =3)
Transfecção intracelular
Para revelar a relação entre a transfecção de miR495 e a expressão de P-gp, as células A549 / DOX foram transfectadas com diferentes concentrações de miR495. Posteriormente, o nível de expressão de P-gp nessas células foi determinado usando o ensaio de Western blot. Conforme mostrado na Fig. 4a, a expressão de P-gp mostrou uma relação negativa com a concentração de miR495, sugerindo que o CCM / SLI poderia ser aplicado como uma ferramenta útil para a entrega de miR495, o que é benéfico para CCM / SLI / RD para reverter o MDR em células A549 / DOX. Como uma prova de conceito, o efeito da transfecção de miR495 na variação do acúmulo de DOX intracelular foi estudado posteriormente. Após serem tratadas com CCM / SLC / siRNA por 48 ou 72 h (Fig. 4b), as células A549 / DOX foram tratadas com DOX por intervalos de tempo variados. Como mostrado na Fig. 5d, com pré-tratamento CCM / SLC / siRNA por 48 h, a fluorescência celular de DOX em células A549 / DOX aumentou 1,49 vezes (4 h pós-incubação) e 1,47 vezes (8 h pós-incubação) , respectivamente. Com pré-tratamento CCM / SLC / siRNA por 72 h, a fluorescência DOX intracelular em células A549 / DOX aumentou 1,63 vezes (4 h pós-incubação) e 1,85 vezes (8 h pós-incubação). Como resultado, concluiu-se que CCM / SLC / siRNA pode superar o MDR em A549 / DOX, aumentando o acúmulo de DOX intracelular em comparação com células não tratadas.
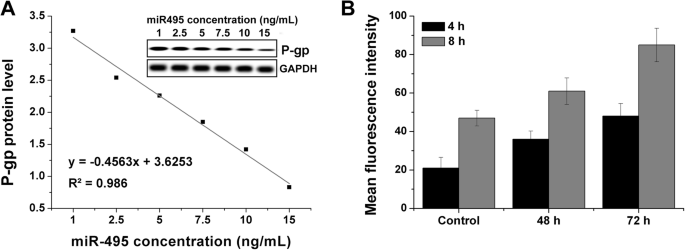
a A relação entre a concentração de miR495 e a expressão de proteínas P-gp em células A549 / DOX após serem tratadas com CCM / SLI / miR495 por 48 h. b O acúmulo de DOX intracelular em células A549 / DOX após serem tratadas com LCC / miR495 por diferentes intervalos de tempo. Os dados foram apresentados como média ± DP ( n =3)
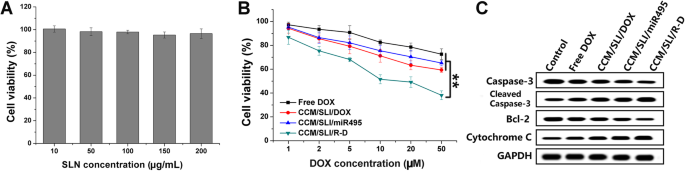
Viabilidade de células A549 / DOX tratadas com transportador livre de drogas ( a ) ou medicamentos contendo ( b ) diferentes formulações em diferentes concentrações de nanopartículas / fármaco por 48 h. c Ensaios de Western blot da expressão das proteínas caspase-3, citocromo C e bcl-2 após diferentes tratamentos. Os dados foram apresentados como média ± DP ( n =3). ** P <0,01
Ensaio Anticâncer In Vitro
A citotoxicidade do transportador livre de drogas (CCM / SLI) foi estudada para revelar ainda mais a biocompatibilidade do DDS. Conforme mostrado na Fig. 5a, após incubar com CCM / SLI por 48 h na concentração mais alta de 200 μg / mL, o A549 / DOX ainda mostrou mais de 90% de viabilidade, o que sugeriu que CCM / SLI era biocompatível com tóxico insignificante às células.
Posteriormente, o ensaio anticâncer in vitro foi avaliado. Como mostrado na Fig. 5b, os efeitos anticâncer de todas as formulações foram positivamente relacionados às concentrações do fármaco. Em detalhes, a viabilidade das células A549 / DOX ainda era de 72,6% na concentração mais alta de DOX (50 μM). O CCM / SLI / DOX e o CCM / SLI / miR495 na mesma condição obtiveram viabilidade celular semelhante, sendo 59,4% e 63,3%, respectivamente, superior ao DOX. No entanto, notou-se que a viabilidade celular para o tratamento com CCM / SLI / R-D diminuiu significativamente para 38,5%. Além disso, o índice CI em CCM / SLI / R-D foi determinado como 0,84, sugerindo um forte efeito sinérgico de miR495 e DOX na morte de células A549 / DOX.
Para verificar novamente a conclusão, as proteínas reguladoras da apoptose comumente adotadas (caspase-3, bcl-2 e citocromo-3) foram avaliadas em diferentes formulações. Conforme demonstrado na Fig. 5c, a quantidade de caspase-3 clivada foi a mais alta em células tratadas com CCM / SLI / RD e o nível de bcl-2 (supressor de apoptose) foi o mais baixo entre todos os grupos de teste, o que confirma ainda mais o anticâncer preferível eficácia de CCM / SLI / RD. Além disso, o CCM / SLI / R-D mostrou expressão muito elevada de citocromo-3, o que sugeriu que a apoptose neste grupo estava relacionada a danos mitocondriais.
O MCTS foi adotado para simular tumor sólido e para avaliar o efeito anticâncer de diferentes formulações. Como mostrado na Fig. 6a, o volume de MCTS no grupo DOX livre cresce persistentemente em todo o período do experimento, sugerindo que o MDR em A549 / DOX poderia diminuir significativamente a citotoxicidade do DOX. Os sistemas de entrega única (SLI / DOX e SLI / miR495) mostraram certo efeito de supressão com crescimento ligeiramente reduzido. Mais importante ainda, a combinação de miR495 e DOX em CCM / SLI / R-D mostrou eficácia muito elevada com um crescimento de volume negativo observado no final do teste. A imagem óptica na Fig. 6b também chegou a conclusões semelhantes.
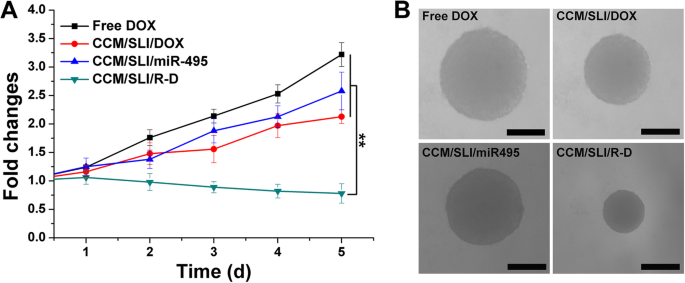
O volume muda ( a ) e imagens ópticas correspondentes ( b ) de MCTS após diferentes tratamentos. Os dados foram apresentados como média ± DP ( n =3). ** P <0,01
Segmentação In Vitro e In Vivo
Para revelar as possíveis razões para o efeito antitumor discriminativo de várias formulações, a absorção celular foi avaliada para investigar se a modificação de CCM poderia aumentar positivamente a capacidade de internalização de nanopartículas em células A549 / DOX, uma vez que muitos estudos demonstraram que a modificação de superfície de CCM pode aumentar o tumor -capacidade de direcionamento de nanocarriers [39, 40]. Conforme exibido na Fig. 7a, a intensidade da fluorescência intracelular aumentou no grupo CCM / SLI / miR49 e SLI / miR495 em função do tempo, sugerindo a relação positiva entre o tempo e a captação celular em ambas as nanopartículas. Além disso, observou-se que sinais de fluorescência mais elevados foram observados no grupo CCM / SLI / miR495, que foi 1,58 vezes maior do que no grupo SLI / miR495 no ponto de tempo de 6 h. Para verificar se a captação de CCM / SLI / miR495 foi via endocitose mediada por CCM, as células foram incubadas com CCM em excesso antes da adição de nanocarreadores. Observou-se que a intensidade de fluorescência no grupo CCM / SLI / miR495 continuou diminuindo, enquanto a intensidade de fluorescência no grupo SLI / miR495 permaneceu quase no mesmo nível. Esses resultados demonstraram que CCM / SLI / miR495 foi absorvido pelas células por meio de endocitose relacionada à CCM.
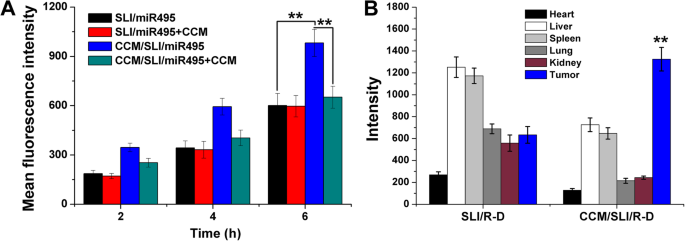
a Análise quantitativa da absorção dependente do tempo intracelular de diferentes formulações em células A549 / DOX (pré-tratadas com / sem CCM). b Intensidade de fluorescência média de tumores dissecados e órgãos principais de camundongos tratados com SLI / R-A e CCM / SLI / R-A 48 h após a injeção. Os dados foram expressos como média ± DP ( n =3). ** P <0,01
Esperava-se que o CCM de A549 / DOX aumentasse a capacidade de direcionamento de tumor de CCM / SLI / R-D para células A549 / DOX isógenas para aumentar o acúmulo de nanocarreadores no tumor. Para verificar nosso conceito, a distribuição de SLI / R-D e CCM / SLI / R-D foi monitorada por um sistema de imagem em tempo real. Como mostrado na Fig. 7b, como esperado, CCM / SLI / R-D mostrou mais acumulação dentro do tumor em comparação com SLI / R-D. Além disso, concluiu-se que o SLI / R-D estava distribuído em quase todos os órgãos (exceto o coração) com foco no fígado e baço, o que pode ser devido a sua fraca capacidade de homing tumoral. Pelo contrário, a modificação de CCM pode aliviar significativamente a captura do fígado para auxiliar o direcionamento aprimorado da carga carregada para o tecido tumoral.
Eficácia antitumoral in vivo
A eficácia antitumoral in vivo de CCM / SLI / R-D foi realizada. Após o tratamento com DOX ou SLI / DOX, o crescimento do tumor em camundongos foi retardado. No entanto, CCM / SLI / R-D teve a melhor eficácia antitumoral e resultou em um volume tumoral obviamente reduzido de 303 ± 25 mm 3 . Além disso, o resultado da variação do peso corporal de camundongos em grupos diferentes também exibiu resultados interessantes (Fig. 8). Ele mostrou que não houve declínio óbvio de peso corporal em camundongos tratados com CCM / SLI / R-D, sugerindo que a capacidade de direcionamento de tumor de CCM / SLI / R-D poderia aumentar a eficácia antitumoral com efeitos adversos reduzidos. Em contraste, a distribuição não direcionada de DOX livre causou toxicidade sistemática aos camundongos, o que foi refletido pela diminuição gradual do peso corporal em função do tempo. Em resumo, o CCM / SLI / R-D foi um DDS de localização de tumor superior para terapia de tumor de pulmão.
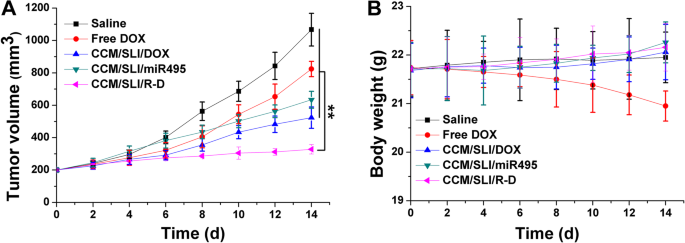
O volume do tumor ( a ) e peso corporal ( b ) of tumor tissue analysis of A549/DOX tumor-bearing Balb/c nude mice after intratumoral administration of different formulations. Data were expressed as mean ± SD (n = 6). ** P < 0.01
Conclusão
In summary, we successfully constructed a CCM-coated SLI nanoparticle as a DDS to co-delivery miR495 and DOX (CCM/SLI/R-D). The characterization demonstrated that CCM/SLI/R-D showed well distribution with a diameter of 120 nm, which showed high stability as well as pH-responsive drug release. Cellular experiments revealed that CCM/SLI/R-D could realize preferable miR495 delivery which achieved the significant downregulation of P-gp, which finally overcome the MDR in A549/DOX by increasing the intracellular DOX accumulation compared to untreated cells. The CCM/SLI/R-D showed promising tumor-homing capability. Most importantly, the synergetic effect of miR495 and DOX achieved much more potent anticancer effect to mono-delivery DDS or free DOX both in vitro and in vivo.
Disponibilidade de dados e materiais
The data and the analysis in the current work are available from the corresponding authors on reasonable request.
Abreviações
- AEAPS:
-
N -(2-Aminoethyl)-3-aminopropyltrimethoxysilane
- CCM:
-
Cancer cell membrane
- DDS:
-
Drug delivery systems
- DLC:
-
Drug loading content
- DOX:
-
Doxorubicin
- HPLC:
-
Cromatografia líquida de alta performance
- MCTS:
-
Multicellular tumor spheroid
- MDR:
-
Multidrug resistance
- miRNA:
-
MicroRNAs
- MTT:
-
Methyl thiazolyl tetrazolium
- P-gp:
-
P-glycoprotein
- SLI:
-
Sílica
- TEOS:
-
Ortosilicato de tetraetilo
Nanomateriais
- Nanofibras e filamentos para entrega aprimorada de drogas
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Administração de medicamentos baseados em células para solicitações de câncer
- Nanopartículas de albumina carregadas de resveratrol com circulação sanguínea prolongada e biocompatibilidade aprimorada para terapia de tumor pancreático direcionada altamente eficaz
- Nanomontagens de ácido 5-aminolevulínico-esqualeno para fotodetecção e terapia de tumor:estudos in vitro
- Cascas de diatomáceas de sílica adaptadas com nanopartículas de Au permitem a análise sensível de moléculas para aplicações biológicas, de segurança e ambientais
- Inibidor de autofagia (LY294002) e 5-fluorouracil (5-FU) Nanolipossoma baseado em combinação para eficácia aprimorada contra carcinoma de células escamosas de esôfago
- CeO2 nanoporoso semelhante a bastão modificado por nanopartículas de PdO para oxidação de CO e combustão de metano com alta atividade catalítica e resistência à água
- Entrega de siRNA à base de micela catiônica para terapia gênica eficiente do câncer de cólon
- Nanopartículas compostas à base de polidopamina com cascas de polímero redox-lábil para liberação controlada de drogas e terapia quimio-fototérmica aprimorada



