Fotoluminescência estável e reversível de nanofios GaN em ajuste de solução por concentração iônica
Resumo
Nós relatamos a resposta de fotoluminescência (PL) de nanofios de GaN sem proteção em soluções. A resposta distinta não é apenas para o pH, mas para a concentração iônica sob o mesmo pH. Os nanofios parecem ser altamente estáveis em solução aquosa com alta concentração iônica e baixo valor de pH até 1. Mostramos que o PL tem uma interação reversível com vários tipos de soluções ácidas e salinas. Os estados quânticos dos nanofios são expostos ao ambiente externo e possuem uma interação física direta que depende dos ânions dos ácidos. Conforme a concentração iônica aumenta, a intensidade da PL aumenta ou diminui dependendo da espécie química. A resposta resulta de uma competição de mudança na curvatura da banda de superfície e transferência de carga para o nível redox na solução. O dos filmes de GaN é relatado para comparação, já que o efeito da curvatura da banda de superfície pode ser desprezado, de modo que há apenas pequenas variações na intensidade de PL para os filmes de GaN. Além disso, essa interação física não impacta nos picos de PL em ácidos e sais, ao passo que há um desvio para o vermelho em PL quando os nanofios estão em solução básica, digamos NH4OH, devido à corrosão química ocorrida nos nanofios.
Introdução
O GaN cristalino foi escolhido como um material semicondutor promissor com um amplo gap direto de 3,39 eV. Tem muitas boas propriedades de materiais que foram aplicadas a aplicações extensas, como diodos de emissão de luz azul / ultravioleta [1, 2], optoeletrônica [3, 4], dispositivos de alta temperatura / alta potência [5, 6] e transistor de efeito de campo [7, 8]. Comparado ao material a granel, nanoestruturas unidimensionais existem relaxação de rede intrinsecamente eficiente [9]. Assim, eles podem ser cultivados com menos defeitos de cristal [10], e isso constitui o principal benefício onde a emissão de fotoluminescência (PL) e as propriedades elétricas são afetadas por esses defeitos. Nanofios longos fornecem superfícies maiores para serem utilizadas, o que poderia ser um grande uso em aplicações de sensor e química [11, 12]. Além disso, o GaN é estável e não se restringe ao vácuo, o que viabiliza as aplicações em ambientes químicos.
A fotoluminescência é uma das propriedades mais comumente usadas para estudar os estados quânticos de um material [13, 14], já que PL vem do decaimento radiativo dos estados excitados. Para materiais de estado sólido, a interação de PL com as condições químicas circundantes fornece uma maneira de sondar os estados excitados. Essa interação de superfície também pode ser usada para sensores químicos e imagens [15, 16]. No entanto, para a maioria dos materiais, o PL é degradado sob um ambiente reativo porque é facilmente extinto pelos estados de defeito de superfície ou pela transferência de portadores fotogerados para as espécies iônicas na solução [17, 18]. Em particular, PL é instável para a maioria dos semicondutores orgânicos e inorgânicos na solução aquosa [19,20,21]. Consequentemente, para os pontos quânticos semicondutores inorgânicos fluorescentes, uma estrutura núcleo-casca é freqüentemente necessária para proteger os estados quânticos emissores de luz [21,22,23,24,25]. Assim, a interação entre os produtos químicos em solução e o estado quântico torna-se fraca devido à proteção.
Sensores ópticos de pH foram propostos que superaram problemas como desvio de sinal, efeitos de fotocorrente parasita e estabilidade de contato elétrico encapsulado em líquidos quimicamente agressivos, embora não pudessem cobrir uma ampla faixa de pH [26]. As propriedades de luminescência de nanopartículas inorgânicas revestidas e não revestidas podem responder a variações de pH em uma faixa mais ampla [27, 28], mas o potencial elétrico de nanopartículas livres não pode ser controlado, proibindo uma análise quantitativa da resposta de pH. As excelentes propriedades ópticas dos nanofios de nitreto do grupo III [29, 30] permitem o uso do pH e da resposta de polarização à intensidade do PL como sinal de detecção [31]. A posição das bordas da banda em materiais de nitreto do grupo III com relação aos níveis redox de água atrai atenção para a aplicação em separação fotocatalítica de água por transferência de carga através da interface nitreto-material / eletrólito do grupo III [32,33,34]. A eficiência desse processo mostrou ser aumentada se nanofios em vez de eletrodos planares forem usados [35].
Até agora, a maior parte do estudo de PL em nanofios de GaN é feito no ar. Existem poucos relatórios discutindo PL em solução. Os íons podem alterar o processo de recombinação do foto-portador. A excitação óptica de nanofios em solução está relacionada a aplicações potenciais, como divisão de água e sensor de íons.
Neste trabalho, estudamos a resposta de PL a partir de nanofios de GaN, que contêm uma superfície de GaN altamente sensível [35,36,37,38], imersa em água incluindo ácido, base e sais sem qualquer proteção. A configuração, diferente da configuração típica para a reação eletroquímica [39,40,41,42,43], é menos complicada sem o revestimento dos terminais eletroquímicos. A resposta PL é medida e correlacionada com a concentração de íons. Os estados quânticos dos nanofios são expostos ao ambiente externo e têm uma interação física direta. Descobrimos que o PL aumenta principalmente com a concentração iônica para nanofios, mas diminui para filmes. Mostramos que a dependência da PL de íons tem uma interação reversível com vários tipos de soluções ácidas e salinas. Anteriormente, havia um relatório que usava a solução salina tamponada com fosfato padrão com uma concentração de fosfato de 0,01 M para mantê-la em alta concentração iônica constante, de modo que apenas os valores de pH fossem alterados nas medições e o PL dos nanofios dependesse apenas do valor de pH [ 31]. Em nosso trabalho, não há solução tampão de fundo e a concentração iônica é variável. O PL responde aos íons em vez de meramente aos valores de pH. Acontece que o PL não é controlado apenas pelo valor do pH, mas também depende da concentração de ânions dos ácidos. O mecanismo de reação relatado aqui é diferente da eletroquímica, que requer eletrodos para medições, e a concentração de íons em nossa configuração experimental muda com o pH, o que contribui principalmente para a PL. As tendências podem ser interpretadas pela competição de dois efeitos dos íons:a transferência do portador para o nível redox e a mudança da região de depleção.
Do ponto de vista da aplicação, uma resposta PL estável sob ambiente químico agressivo pode ser aplicada para monitorar o desperdício ou água poluída por um longo tempo. Se um pedaço de nanofios de GaN é imerso em tal água, sua resposta PL pode ser obtida a partir de excitação óptica externa e coleta de fluorescência. A vantagem dos nanofios de GaN é que ele tem apenas interação física, mas nenhuma interação química devido à sua estabilidade superior em condições extremas. O papel de teste convencional ou o sensor eletroquímico não podem funcionar nessas condições por um longo período. Além disso, os três terminais eletroquímicos não são necessários em nossa configuração experimental para manter o potencial eletrolítico. Isso torna a configuração muito mais simples. Não há reação química; uma imagem clara do processo de relaxamento do foto-portador é estabelecida para o importante material dos nanofios de GaN em solução eletrolítica. Essa imagem pode beneficiar o desenvolvimento futuro de novas aplicações de GaN, como sensor de íons ou divisão de água.
Métodos
Síntese de nanofios e filmes de GaN
O crescimento de nanofios de GaN via mecanismo VSS e filmes de GaN foram fabricados em um sistema de epitaxia de fase de vapor de hidreto (HVPE) [44, 45], onde o nível de vácuo é de 1 atmosfera. Os gases precursores foram amônia (NH 3 ) e cloreto de gálio (GaCl) formado pelo fluxo de gás HCl diluído com nitrogênio através de Ga fundido a 850 ° C. Para o crescimento do nanofio, Ni foi selecionado como o catalisador e o crescimento ocorreu a 880 ° C com V / III =20 e gás transportador N 2 de 400 sccm. Nanofios de GaN então cresceram quando os dois gases precursores, GaCl (como a fonte de Ga) e NH 3 (como a fonte de N), encontrou-se e reagiu perto das amostras a 650–950 ° C. Os nanofios de GaN foram orientados ao eixo m [45]. Observe que os catalisadores Ni-Ga foram atacados pelo HCl do fluxo e do produto secundário das reações durante o crescimento [46]. O filme espesso de GaN com orientação c foi cultivado em safira no sistema HVPE a uma temperatura de crescimento de 1050 ° C. A espessura dos filmes de GaN é 300 ± 10 μm.
Preparação da amostra
As amostras de GaN foram armazenadas em baixo vácuo (~ 10–1 Torr) após o crescimento e foram tratadas com vapor de HF para remover possível óxido antes das medições de PL.
Medição PL
A configuração das medidas da propriedade PL é mostrada no arquivo Adicional 1:Figura S1. O laser de hélio-cádmio (He-Ca) é usado como fonte de luz de excitação para saída de onda contínua em um comprimento de onda de 325 nm. A função da fibra era coletar a emissão de fótons de PL e conectar ao iHR 550 Imaging Spectrometer projetado para medições espectrais. O iHR 550 era um espectrômetro de grade tripla automatizado.
As fendas de entrada e saída do sistema desempenharam um papel fundamental. Particularmente, quanto mais amplos fossem, menor seria a resolução do espectro PL. No entanto, se as fendas forem muito estreitas, os ruídos podem afetar significativamente os sinais. Nessa medição, utilizou-se uma grade de 1200 ranhuras / mm e a fenda foi de 0,2 mm com o objetivo de obter excelente resolução. O tubo fotomultiplicador foi o detector com a fonte de alimentação (950 V). Para permitir que o laser focalizasse a amostra, as medições tiveram que usar três espelhos dicróicos e duas lentes de foco. Após a concentração, o diâmetro do ponto era de cerca de 0,3 mm e a densidade de potência atingiu 21 W / cm 2 na superfície da amostra. A fotografia da configuração experimental é mostrada no Arquivo Adicional 1:Figura S2.
Observação da morfologia
A morfologia dos nanofios de GaN foi examinada usando um microscópio eletrônico de varredura (SEM; JEOL-6700F SEM).
Resultados e discussão
Resposta de PL de GaN em direção à concentração de íons em soluções ácidas e de sal
A Figura 1a, b ilustra a influência dos valores de pH variando de 1 a 7, usando soluções ácidas e água DI, em nanofios de GaN e filmes de GaN. Eles mostram que a intensidade de PL com diferentes valores de pH tem duas tendências notáveis para diferentes soluções ácidas. Em particular, a intensidade PL de nanofios de GaN em ácidos clorídricos (HCl) aumenta significativamente com pH variando de 7 a 1 e em ácido fosfórico (H 3 PO 4 ) aumenta ligeiramente, enquanto a intensidade diminui drasticamente quando os nanofios de GaN são de ácido nítrico (HNO 3 ) e ácido acético (CH 3 COOH) com valores de pH diminuindo de 7 para 1, conforme mostrado na Fig. 1a. Da mesma forma, na Fig. 1b, são apresentados os resultados da intensidade PL das mudanças dos filmes de GaN nessas soluções ácidas. A resposta PL experimenta uma diminuição em CH 3 COOH de pH neutro para baixo e tendência suave para baixo ou estável no resto das soluções ácidas. A diferença mais marcante em comparação com o efeito em nanofios de GaN e filmes espessos é que a intensidade PL dos nanofios de GaN permanece aumentando ou diminuindo de forma consistente, mas a dos filmes de GaN é relativamente estável conforme eles diminuem ou a variação permanece dentro de uma faixa. Observe que as concentrações de íons de soluções ácidas são diferentes correspondendo aos valores de pH. Os testes das amostras em soluções salinas para os quais o pH é 7 mas com diferentes concentrações de íons são realizados para verificar a resposta aos íons em pH constante.
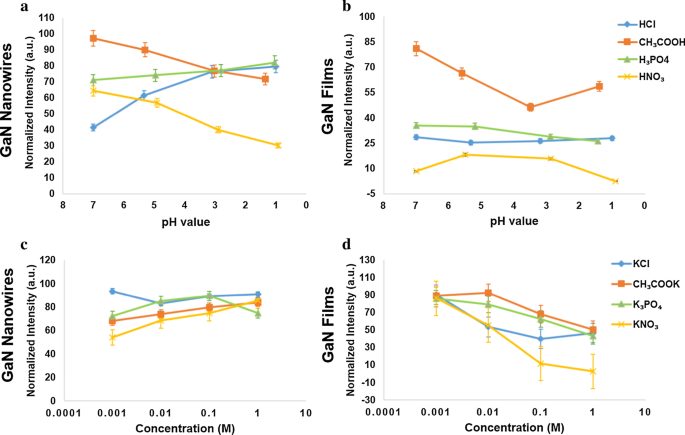
A distribuição da intensidade de PL em diferentes valores de pH de soluções ácidas e soluções salinas em diferentes concentrações. O laser He-Ca é usado aqui e abaixo como fonte de luz de excitação para saída de onda contínua em um comprimento de onda de 325 nm. a A resposta PL de nanofios de GaN com diâmetros variando entre 60 e 80 nm em soluções ácidas. b A resposta PL de filmes de GaN com ~ 300 μm de espessura em soluções ácidas. c A resposta PL de nanofios de GaN em soluções de sal com diferentes concentrações. d A resposta PL de filmes de GaN em soluções de sal com diferentes concentrações
Para confirmar a tendência com a concentração de íons, investigamos os efeitos de soluções de sal com diferentes concentrações na intensidade de PL em termos de dois tipos de materiais:nanofios de GaN e filmes de GaN como mostrado pelos gráficos de linha na Fig. 1c, d. A intensidade PL dos nanofios GaN testemunha um aumento constante no acetato de potássio (CH 3 COOK) e nitrato de potássio (KNO 3 ) junto com o aumento na concentração de sal de 0,001 para 1 M. Em contraste, o do cloreto de potássio (KCl) desce de 0,001 para 0,01 M, mas sobe gradualmente de 0,01 para 1 M. O do fosfato tripotássico (K 3 PO 4 ) tem um aumento significativo de 0,001 e 0,1 M, enquanto a inclinação diminui de 0,01 para 0,1 M. A intensidade diminui quando a concentração sobe para 1 M. Considerando a Fig. 1d para filmes de GaN, todas as inclinações mostram tendências descendentes no quatro tipos de sais com aumento na concentração de sal, que é diferente dos nanofios de GaN. Os resultados são consistentes com os de soluções ácidas em que os filmes de GaN têm tendências descendentes na intensidade de PL, mas a intensidade pode ser tanto para cima quanto para baixo com a mudança de pH. Conforme a concentração iônica aumenta, o PL dos nanofios sobe ou desce com inclinações dependendo da espécie química. Assim, as espécies e concentrações iônicas desempenham papéis críticos na PL.
As tendências provavelmente resultam da combinação de dois fatores que afetam o PL. O primeiro é a redução da região de depleção pela fixação iônica na superfície. O segundo é a transferência de elétrons para os níveis redox dos íons. Para entender as duas tendências não idênticas de intensidade de PL em diferentes soluções ácidas e soluções de sal para nanofios de GaN e filmes de GaN, a Fig. 2 mostra esquematicamente dois mecanismos pelos quais a concentração de íons controla a intensidade de PL:(A) redução da região de depleção e ( B) transferência de carga para o nível redox [31, 47].
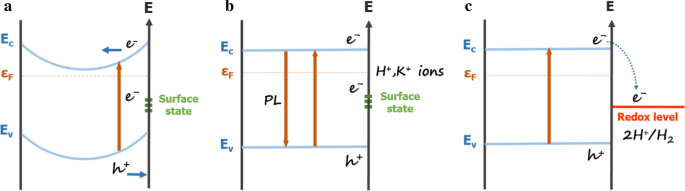
Ilustração esquemática do efeito da concentração de íons na intensidade da fotoluminescência. E é energia. E c , E v e ε F são a borda da banda de condução, a borda da banda de sanefa e o nível de Fermi, respectivamente. a Região de depleção da superfície causada pelos elétrons presos nos estados de superfície. b Região de depleção neutralizada pela ligação de íons positivos H + ou K + . c Transferência de elétrons para o nível redox de H +
A partir da modelagem da interface do semicondutor e solução eletrolítica [47], entendemos que os íons são distribuídos apenas entre a solução e a superfície do sólido, ou seja, existem camadas carregadas tanto no GaN quanto nas soluções. O potencial na interface foi então ajustado, o que causou a curvatura da banda. A separação da água fotocatalítica do GaN em pó sob irradiação de luz resulta do esquema de energia da banda de GaN, onde a borda da banda de condução de GaN está posicionada 0,5 V mais alta do que o potencial redox de H + / H 2 [30]. Nanofios de GaN exibem melhor atividade fotocatalítica por causa da grande área de superfície que aumenta a atividade fotocatalítica na região de pH ácido [38]. Por causa dos estados de superfície no intervalo de banda, os elétrons preencherão o estado de intervalo e o nível de Fermi é fixado ali [34, 43, 48]. A curvatura da banda é mostrada na Fig. 2a. Perto da superfície, existe uma região de depleção. Por causa do forte campo elétrico na região de depleção, os elétrons e buracos fotogerados serão direcionados para direções opostas e a recombinação será evitada. Quando há uma alta concentração de íons na solução, os íons podem se anexar à superfície para neutralizar a densidade de carga superficial e o esgotamento é reduzido. Tal ligação e desprendimento de íons altera a distribuição de carga no bandgap em sensores de pH [49]. Uma vez que a banda de energia se torna quase plana, a recombinação elétron-buraco é restaurada e a PL é aumentada, como também mostrado na Fig. 2a.
Por causa da grande área de superfície dos nanofios, o mecanismo da região de depleção é mais importante nos nanofios do que nos filmes. Na verdade, os pequenos nanofios estão totalmente esgotados [34]. No mecanismo (B), os íons desempenham um papel diferente para afetar o PL, conforme mostrado na Fig. 2b. Para nanofios GaN, os níveis redox de H + e OH - estão dentro do bandgap [36, 50,51,52]. A portadora foto-gerada pode, portanto, transferir para o nível redox em vez de se recombinar. Por exemplo, a reação entre prótons e os fotocondutores 2H + + 2e - → H 2 pode ocorrer. Como a região de depleção leva apenas uma pequena fração dos filmes, onde a maior parte do filme não está esgotada, o mecanismo (A) é relativamente sem importância. Conseqüentemente, o mecanismo de transferência de carga domina para os filmes. Observe que à medida que a concentração iônica aumenta, para o mecanismo (A) a PL é aumentada, enquanto que para o mecanismo (B) a PL é reduzida. Para nanofios de GaN, o PL é determinado pela competição de (A) e (B). Para filmes de GaN, o PL é determinado por (B) principalmente por causa da pequena fração da região de depleção de sua superfície limitada. Isso explica porque os nanofios de GaN têm tendências de PL crescentes ou decrescentes com o aumento da concentração de íons, mas os filmes de GaN têm apenas PL decrescente ou quase constante.
Além da condição de solução, a orientação plana e a polaridade das duas formas de GaN são diferentes. Os filmes de GaN são planos c com polaridade Ga, mas a frente de crescimento dos nanofios é plano m não polar. A área de superfície (a parede lateral) é maior em nanofios, que exibem uma variedade de conjuntos de planos cristalográficos, se assumindo que a seção transversal é quase circular. A polaridade pode contribuir parcialmente para o PL dependente do pH de nanofios e filmes de GaN.
Efeito da área de superfície na resposta de PL
Em relação à morfologia de GaN, por exemplo, nanofio e filme, também investigamos o PL de nanofios maiores para comparação. Os diâmetros de tais nanofios são ~ 200 nm, enquanto os nanofios típicos são ~ 60-80 nm. A Figura 3a mostra como HNO 3 e HCl afetam a intensidade PL de nanofios GaN maiores sob variação de pH de 7 a 1. Quando eles estão imersos em HNO 3 , A intensidade de PL atinge um pico em pH =5,27. Ao contrário, tem um salto notável de intensidade de PL em pH =5,27 de HCl e aumenta constantemente quando o pH desce. Na Fig. 3b, fazemos uma comparação da intensidade PL de três tipos de amostras (nanofios, filmes e nanofios maiores) em soluções de ácido nítrico e clorídrico. A distribuição de intensidade PL de nanofios com tamanhos típicos e nanofios maiores tem padrões descendentes com diminuição do pH em HNO 3 mas para cima em HCl. Em outras palavras, os dois tamanhos de nanofios têm desempenho semelhante na resposta de PL em soluções ácidas e segue os mecanismos discutidos na Fig. 2. Aparentemente, a intensidade de PL dos filmes de GaN em HCl e HNO 3 é relativamente estável e que em HCl é aproximadamente constante.
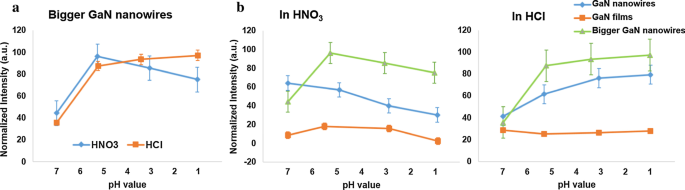
Comparação da intensidade PL de diferentes tamanhos e dimensões de GaN. a A distribuição da intensidade PL em vários valores de pH de soluções ácidas em nanofios GaN maiores com diâmetros de ~ 200 nm. b Uma comparação da intensidade PL para nanofios GaN, filmes GaN e nanofios GaN maiores em HNO 3 e HCl
Além disso, a intensidade PL de nanofios de GaN em ácidos hidro-hálicos, por exemplo, ácido bromídrico (HBr), ácido clorídrico (HCl) e ácido iodídrico (HI), flutua gradualmente com um movimento ascendente ao diminuir os valores de pH de 7 para 1, conforme mostrado em Fig. 4.
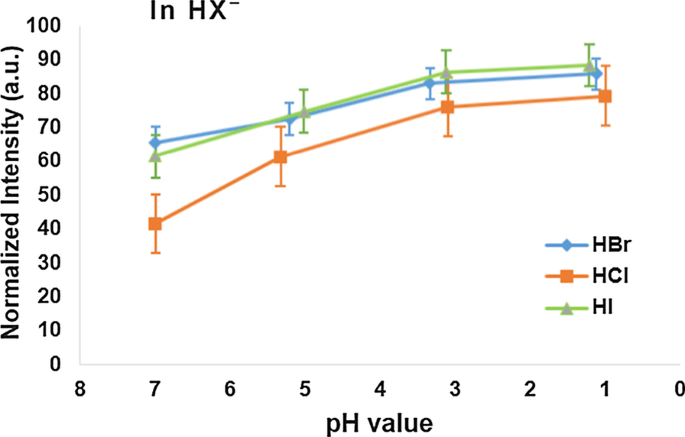
A distribuição da intensidade PL de nanofios de GaN sob variações de pH em três soluções de ácido hidrohálico
Interação de reversibilidade
Para avaliar o uso repetido para aplicações, os testes foram repetidos com nanofios em soluções de pH neutro a pH baixo. As amostras foram renovadas com água DI entre cada teste, conforme observado pelo pH 7 na Fig. 5. A intensidade do PL desceu quando o pH baixou, mas foi restaurada após a limpeza das amostras com água DI. Essa reversibilidade da intensidade PL sob mudança de pH de nanofios de GaN em soluções ácidas permite aplicações de longo prazo em ambientes químicos ácidos. Além disso, os picos de PL em que os nanofios foram imersos em soluções ácidas e após a remoção das soluções mantêm-se em ~ 3,4 eV (Arquivo adicional 1:Fig. S1-S4). Ele confirmou que as microestruturas dos nanofios de GaN não foram danificadas durante os tratamentos da solução.
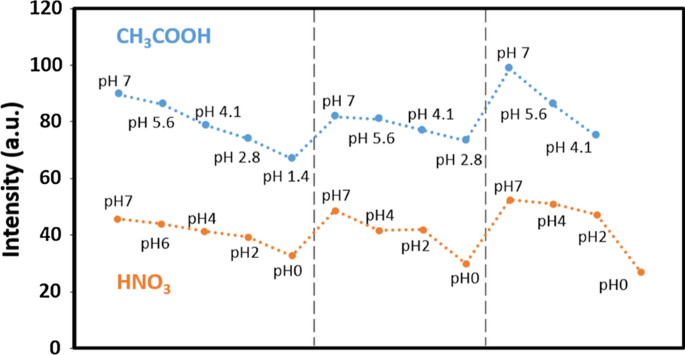
Reversibilidade da intensidade PL de nanofios de GaN em CH 3 COOH e HNO 3 com vários valores de pH
Efeito na qualidade do cristal
A Figura 6 fornece os detalhes dos espectros PL sobre a imersão de nanofios de GaN nas quatro soluções ácidas (Fig. 6a) e soluções de sal (Fig. 6b). Ele representa a variação da intensidade da PL com valores de pH ou concentrações iônicas, mas os picos principais ainda estão em ~ 3,4 eV. O largo bandgap direto de 3,4 eV de GaN [46, 53] mantém-se nessas soluções ácidas, o que sugere que ele exibe interação física em vez de reações químicas. As tendências de intensidade com valores de pH são discutidas na Fig. 1. O pico principal estável em ~ 3,4 eV (Fig. 6 e arquivo adicional 1:Fig. S3-S7) indica que a microestrutura dos nanofios de GaN mantém após a imersão em solução ácida.
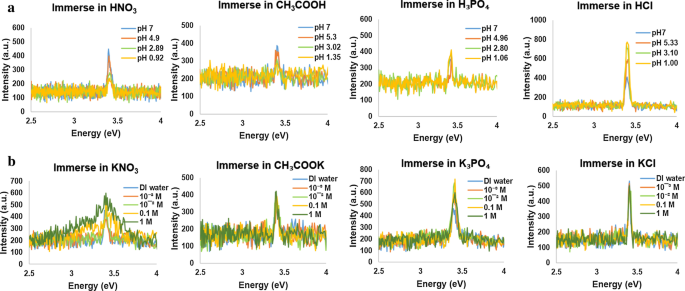
Espectros de PL quando nanofios de GaN imersos em soluções de diferentes pH ou concentrações. a Espectros PL de nanofios de GaN em soluções ácidas e b Espectros PL de nanofios de GaN em soluções de sal
Observe que o óxido de superfície pode contribuir para a luminescência amarela (YL), que é emitida a partir dos estados de superfície associados ao óxido de gálio [54] que decora a superfície livre e, possivelmente, também a interface do substrato e os limites internos dos grãos. De nossos espectros de PL, o YL não é significativo, o que indica que o óxido de Ga foi removido principalmente pelo tratamento com vapor de HF antes da medição. Além disso, o HCl pode gravar a camada de óxido de superfície também para eliminar a contribuição do óxido para PL.
Apesar dos ácidos, também investigamos o impacto da solução básica, por exemplo, solução de hidróxido de amônio (NH 4 OH), em nanofios de GaN para comparação por meio da resposta PL. Os picos de PL de nanofios GaN crescidos foram localizados em ~ 3,4 eV, enquanto os picos mudaram quando os submergiram em NH 4 Solução OH. Os espectros de PL para pH =11,24 (Fig. 7a) e 14,02 (Fig. 7b) mostraram desvios para o vermelho nos picos de ~ 3,10 eV. A mudança sugeriu a degradação em microestruturas GaN. A reação irreversível (arquivo adicional 1:Fig. S6) pode ser causada por reações químicas nas estruturas de GaN onde os nanofios de GaN foram danificados (Fig. 7c, d). Defeitos estruturais foram gerados na superfície dos nanofios de GaN que podem alterar a densidade de estados da superfície, daí a emissão de PL. Após a remoção de tais soluções, os picos permaneceram em 3,10 eV (arquivo adicional 1:Fig. S6) o que implica que a mudança foi permanente e os testes foram irreversíveis em NH 4 Solução OH. Em comparação, a morfologia dos nanofios permaneceu sem corrosão de superfície visível em soluções ácidas, digamos HCl, como mostrado na Fig. 7e, f.
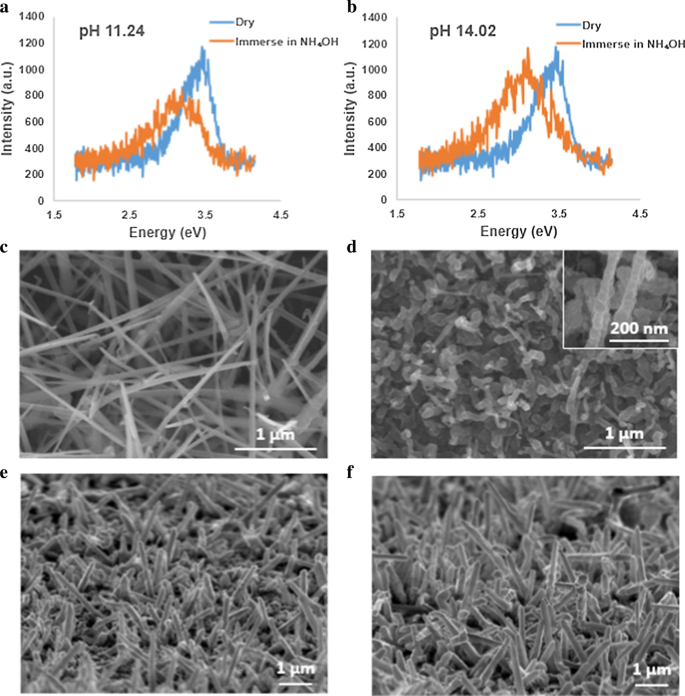
Os espectros PL de nanofios de GaN em NH 4 OH e as imagens SEM correspondentes. a Sinais quando os nanofios estão em NH 4 OH a pH =11,24. b Sinais quando os nanofios estão em NH 4 OH a pH =14,02. c Imagem SEM dos nanofios GaN conforme crescidos. d Os nanofios de GaN após imersão em NH 4 Solução OH por 20 min. e Imagem SEM dos nanofios GaN crescidos. f Os nanofios após os testes de imersão na solução ácida, HCl, por 20 min
Moléculas de oxigênio são conhecidas por afetar o PL das moléculas orgânicas. O PL vem principalmente do exciton de spin singlet. O exciton singleto poderia ser reduzido a exciton tripleto não emissivo pela excitação das moléculas de oxigênio do estado de tripleto de spin para o estado excitado singleto [55, 56]. No GaN, há pouca diferença de energia entre o par elétron-buraco singleto e tripleto. Não se espera que a presença de moléculas de oxigênio forme um canal de decaimento não radiativo e afete o PL. Em todas as nossas condições experimentais, existe um nível de oxigênio saturado na solução. A tendência da variação do PL para várias concentrações de íons não é, portanto, devido ao nível de oxigênio.
Conclusão
Demonstramos a estabilidade e a resposta ao PL de nanofios de GaN imersos em diferentes tipos de soluções ácidas em pH variável correspondente a diferentes concentrações de íons, e em soluções salinas com pH fixo, mas em concentrações diferentes. A resposta PL foi medida e correlacionada com a concentração de íons. Em ambos os tipos de soluções, as respostas PL dos nanofios de GaN foram aumentando ou diminuindo. Em comparação, as respostas de PL foram relativamente estáveis ou diminuíram ligeiramente em relação aos filmes de GaN. As respostas de PL foram distintas de nanofios e filmes de GaN que resultaram das diferentes estruturas de bandas deles. A competição de mudança na curvatura da banda de superfície e transferência de carga para o nível redox na solução foi considerada, onde o nanofio poderia ser totalmente esgotado de suas grandes áreas de superfície, mas a fração de depleção era pequena e insignificante para filmes onde havia apenas pequenas variações na intensidade de PL . Descobriu-se que o PL responde aos íons em vez de meramente aos valores de pH como a resposta da intensidade do PL em soluções de sal e HX - soluções confirmaram os resultados. Essa interação física não impactou nos picos de PL em ácidos e sais, ao passo que houve um desvio para o vermelho em PL quando os nanofios estavam em solução básica, digamos NH 4 OH, devido à corrosão química ocorrida nos nanofios. Mostramos que o PL teve uma interação reversível com essas soluções ácidas e salinas. A resposta PL estável e reversível de nanofios de GaN nessas soluções ácidas permite a aplicação potencial em tais ambientes químicos agressivos.
Disponibilidade de dados e materiais
Todos os dados gerados ou analisados durante este estudo estão incluídos neste artigo publicado.
Abreviações
- PL:
-
Fotoluminescência
- HVPE:
-
Epitaxia de fase de vapor de hidreto
- NH 3 :
-
Amônia
- GaCl:
-
Cloreto de gálio
- He – Ca:
-
Hélio-cádmio
- HCl:
-
Ácidos clorídricos
- H 3 PO 4 :
-
Ácido fosfórico
- HNO 3 :
-
Ácido nítrico
- CH 3 COOH:
-
Ácido acético
- CH 3 COZINHEIRO:
-
Acetato de potássio
- KNO 3 :
-
Nitrato de potássio
- KCl:
-
Cloreto de Potássio
- K 3 PO 4 :
-
Fosfato Tripotássico
- HBr:
-
Ácido bromídrico
- HI:
-
Ácido hidriódico
- YL:
-
Luminescência amarela
- NH 4 OH:
-
Solução de hidróxido de amônio
Nanomateriais
- 5G e GaN:a mudança de LDMOS para GaN
- 5G e GaN:inovações futuras
- Remoção adsortiva de íons de cobre (II) de solução aquosa usando um nanoadsorvente de magnetita de resíduos de escala de moinho:Síntese, caracterização, adsorção e modelagem cinética Estud…
- Características ópticas e elétricas de nanofios de silício preparados por corrosão eletrolítica
- Ajuste da química da superfície de polieteretercetona por revestimento de ouro e tratamento com plasma
- (La0.97RE0.01Yb0.02) Nanofosforos 2O2S convertidos de sulfato de hidroxila em camadas e investigação de fotoluminescência de conversão ascendente (RE =Ho, Er)
- Ajustando as morfologias de superfície e propriedades dos filmes ZnO pelo projeto da camada interfacial
- Um Projeto Eficiente e Eficaz de Nanofios InP para Captação Máxima de Energia Solar
- Preparação de nanoesferas poliméricas impressas com íons de paládio (II) e sua remoção de paládio (II) da solução aquosa
- Síntese e caracterização de BiOCl modificado e sua aplicação na adsorção de corantes de baixa concentração de solução aquosa



