Síntese verde e econômica de nanopartículas de óxido de estanho:uma revisão sobre as metodologias de síntese, mecanismo de formação e suas aplicações potenciais
Resumo
A nanotecnologia se tornou a área de pesquisa mais promissora com sua aplicação importante em todos os campos da ciência. Nos últimos anos, o óxido de estanho tem recebido grande atenção devido às suas propriedades fascinantes, que foram aprimoradas com a síntese desse material na faixa nanométrica. Numerosos métodos físicos e químicos estão sendo usados atualmente para produzir nanopartículas de óxido de estanho. No entanto, esses métodos são caros, requerem alta energia e também utilizam vários produtos químicos tóxicos durante a síntese. As crescentes preocupações relacionadas à saúde humana e ao impacto ambiental levaram ao desenvolvimento de um processo econômico e ambientalmente benigno para sua produção. Recentemente, nanopartículas de óxido de estanho foram sintetizadas com sucesso por métodos verdes usando diferentes entidades biológicas, como extrato de planta, bactérias e biomoléculas naturais. Porém, a produção em escala industrial utilizando abordagens de síntese verde permanece um desafio devido à complexidade dos substratos biológicos que dificultam a elucidação das reações e mecanismo de formações que ocorrem durante a síntese. Portanto, a presente revisão resume as diferentes fontes de entidades biológicas e metodologias utilizadas para a síntese verde de nanopartículas de óxido de estanho e o impacto em suas propriedades. Este trabalho também descreve os avanços na compreensão do mecanismo de formação relatados na literatura e as diferentes técnicas analíticas utilizadas para caracterizar essas nanopartículas.
Introdução
Nas últimas décadas, a nanotecnologia surgiu como uma nova área de pesquisa lidando com a síntese, caracterização, modificação e utilização de nanomateriais para sua tremenda aplicação em áreas como farmacêutica, indústria alimentícia, cosmética, indústria têxtil, medicina, ótica, eletrônica, ciências da energia e aplicações eletroquímicas [1,2,3,4]. Nanomateriais são materiais com uma dimensão em uma faixa de tamanho de 1–100 nm. A relação área de superfície muito grande para o volume e o tamanho extremamente pequeno desses materiais podem resultar em atividades elétricas, ópticas, magnéticas, catalíticas e antimicrobianas completamente novas ou aprimoradas em comparação com seus materiais a granel [5,6,7]. Por causa dessas propriedades únicas, as nanopartículas encontram aplicação em vários campos da ciência e engenharia modernas, como nanomedicina, fotocatálise, biossensores, agentes de limpeza e indústria têxtil [1, 8]. Entre as nanopartículas, óxido de estanho (IV) (SnO 2 ), em particular, ganhou imensa atenção devido às suas aplicações versáteis, como dispositivos optoeletrônicos [9], sensores de gás de estado sólido [10], eletrodos para baterias de íon-lítio [11], visores de emissão de campo [12], diodos emissores de luz [13], catálise [14], células solares baseadas em corantes [15], medicamentos [16], fotossensores e revestimentos antiestáticos [17].
Em ciência de materiais, SnO 2 é considerado um semicondutor do tipo n deficiente em oxigênio, que se cristaliza como a estrutura tetragonal do rutilo com constantes de rede a = b =4,7374 Å e c =3,1864 Å. A célula unitária consiste de dois átomos de estanho coordenados seis vezes e quatro átomos de oxigênio coordenados de três vezes [18, 19]. Uma grande lacuna de energia (3,6 a 3,8 eV), forte estabilidade térmica (até 500 ° C), um alto grau de transparência no espectro visível, fortes interações químicas e físicas com as espécies adsorvidas tornam SnO 2 um candidato promissor para uma aplicação potencial em baterias de íon-lítio, sensores, catálise, armazenamento de energia, revestimentos de vidro, medicamentos e remediação ambiental [20,21,22,23]. SnO 2 é utilizado como sensor para melhorar o tempo de resposta e a sensibilidade devido à sua alta área específica, alta estabilidade química, baixa resistência elétrica e baixa densidade [24]. Nos últimos anos, SnO 2 foi exaustivamente explorado para suas aplicações em células solares [25] e sensores de gás para detectar os gases combustíveis como CO, NO, NO 2 , H 2 S e C 2 H 5 OH [26,27,28,29]. Devido às propriedades físico-químicas únicas e às aplicações potenciais das nanopartículas (NPs), a comunidade científica vem desenvolvendo diversos métodos para a produção de nanopartículas. No entanto, os métodos químicos e físicos usados para a síntese de nanopartículas de metal e óxido de metal são bastante caros e usam substâncias tóxicas que são prejudiciais ao meio ambiente e à saúde humana [30]. Nos últimos anos, a maioria dos pesquisadores mudou seu interesse de pesquisa em direção à síntese verde de NPs porque ela tem muitas vantagens, como custo-benefício, procedimento de fabricação simples, reprodutibilidade na produção e frequentemente resulta em nanopartículas mais estáveis [31]. Durante a última década, vários estudos sobre a síntese verde de SnO 2 NPs foram relatados. No entanto, nenhum artigo de revisão está disponível na literatura que demonstre a metodologia de síntese e o mecanismo de formação. Portanto, este artigo descreve a síntese verde, mecanismo de formação, técnicas de caracterização e aplicações potenciais de SnO 2 NPs.
Síntese Verde de Nanopartículas de Óxido de Estanho
SnO 2 NPs são sintetizados por vários métodos físicos, químicos e verdes. Os métodos químicos incluem sol-gel, hidrotérmico, precipitação, método mecanoquímico, microemulsão e assim por diante [31,32,33,34,35,36,37]. Dentre os métodos químicos, a técnica mais utilizada é a síntese sol-gel, que utiliza sal precursor de estanho e reagentes químicos que regulam a formação do gel contendo estanho. Depois disso, o gel é exposto a um tratamento térmico em temperaturas de até 800 ° C para obter SnO 2 NPs [32, 38]. Estabilizadores químicos e agentes de proteção, como ácido oxálico ou etilenoglicóis, podem ser adicionados durante a síntese de SnO 2 NPs para controlar o tamanho e proibir a aglomeração das nanopartículas [32, 39]. O pH da solução, a concentração de produtos químicos, o tempo de reação e a temperatura de calcinação também podem influenciar o tamanho e a morfologia das nanopartículas [31, 34,35,36,37]. Os métodos acima mencionados de síntese de SnO 2 NPs utilizam vários reagentes químicos perigosos, solventes e surfactantes, que criam uma séria ameaça ao meio ambiente e à saúde humana [4, 30].
SnO 2 NPs também podem ser sintetizados por técnicas físicas, como spray pirólise, oxidação térmica, deposição química de vapor, ablação a laser e ultrassonicação [40,41,42,43,44]. Entre esses métodos, a ablação a laser é considerada um método simples e de baixo custo para sintetizar nanopartículas de metal e óxido de metal em líquido [44, 45]. Em contraste com os outros métodos convencionais, este método não requer agentes de cobertura / redução, alta temperatura ou alta pressão, e nos permite produzir nanopartículas de alta pureza [44, 45]. A variação nos parâmetros dos pulsos aplicados do feixe de laser e o tempo de ablação são parâmetros importantes que definem o tamanho de partícula, morfologia e química de superfície das nanopartículas [44]. No entanto, a maioria dos métodos físicos requer equipamentos complexos, alta energia e mão de obra qualificada [46]. Portanto, é muito importante desenvolver métodos de síntese que sejam ecologicamente corretos, baratos, eficientes e que funcionem em condições ambientais. Uma dessas soluções é a síntese verde, e muitos pesquisadores desenvolveram uma abordagem de química verde para sintetizar nanopartículas de óxido de estanho. Na estratégia de síntese verde, entidades biológicas como extrato de planta, microrganismos ou outras fontes verdes podem ser usadas como uma alternativa aos métodos físicos e químicos convencionais [47]. Hoje em dia, os métodos de síntese inspirados biologicamente também são conhecidos como síntese verde porque estão de acordo com os doze princípios da química verde [48]. Algumas das vantagens distintas que a síntese biológica tem sobre os métodos físicos e químicos são (a) método limpo e ecologicamente correto, pois são usados produtos químicos não tóxicos, (b) o uso de fontes renováveis, (c) os componentes biológicos ativos como a própria enzima como bem como os fitoquímicos atuam como agente redutor e capeador, minimizando assim o custo geral do processo de síntese, (d) condições experimentais externas como alta pressão e temperatura não são necessárias, causando economia de energia significativa [49, 50].
Na última década, o interesse em sintetizar SnO 2 As NPs por meio do método biológico aumentaram consideravelmente, porque o processo é mais confiável, ecológico, econômico, com baixo rendimento e alto rendimento e procedimentos simples, sem causar nenhum efeito adverso ao meio ambiente. Uma variedade de substratos biológicos, como extratos de plantas, bactérias e biomoléculas naturais, foram empregados com sucesso para a síntese verde de SnO 2 NPs. Os fitoquímicos de várias plantas e enzimas de bactérias são os principais responsáveis pela síntese verde. Os compostos ativos presentes nas fontes verdes também atuam como agentes redutores, limitadores e estabilizadores durante a síntese. Os NPs desejados são freqüentemente obtidos após calcinação ou recozimento em temperaturas especificadas [51,52,53,54].
Síntese de nanopartículas de óxido de estanho mediada por plantas
A síntese mediada por plantas tornou-se a melhor plataforma de síntese em relação aos métodos físico-químicos convencionais, porque é livre de produtos químicos tóxicos e fornece cobertura natural, bem como agentes redutores. Além disso, é fácil e ecológico e fornece produtos enriquecidos em quantidade e isentos de impurezas. Nesse método, não há necessidade de usar equipamentos de alta temperatura, alta pressão e caros. Além disso, a síntese mediada por plantas leva à produção em grande escala de nanopartículas mais estáveis com formas e tamanhos variados [55, 56]. Extratos de um grande número de partes de diferentes espécies de plantas têm sido utilizados para a síntese verde de SnO 2 NPs. Em geral, a síntese de SnO mediada por plantas 2 NPs é um processo muito simples em que um sal fino é adicionado ao extrato previamente preparado. Após a reação, a solução é submetida a centrifugação. Por fim, os pellets são submetidos a tratamento térmico seguido de caracterização por meio de diversas técnicas analíticas, como espectroscopia de infravermelho por transformada de Fourier (FTIR), difratômetro de raios X (XRD), análise de energia dispersiva de raios X (EDS), microscopia eletrônica de varredura ( SEM), microscopia eletrônica de transmissão (TEM), analisador de tamanho de partícula (PSA) e espalhamento dinâmico de luz (DLS). A espectroscopia UV-visível (UV-Vis) é usada para monitorar a formação de nanopartículas. O protocolo detalhado para a síntese mediada por plantas de SnO 2 NPs é esquematicamente ilustrado na Figura 1. Diallo et al. relatou a síntese verde de SnO 2 NPs usando Aspalathus linearis e cloreto de estanho pentahidratado (SnCl 4 · 5H 2 O) como um precursor [51]. O sal foi dissolvido no extrato da planta, e a formação de um depósito branco foi observada após 10 min. O depósito branco foi recolhido após o processo de centrifugação e foi seco a cerca de 80 ° C. O pó foi recozido em várias temperaturas por cerca de 4 he submetido a várias técnicas analíticas, como microscopia eletrônica de transmissão de alta resolução (HR-TEM), EDS, XRD e espectroscopia de fotoemissão de raios-X (XPS). Os NPs eram quase esféricos em forma, com um tamanho médio na faixa de 2,5-11,40 nm. Observou-se que o tamanho de partícula e a natureza cristalina das NPs aumentam com o aumento da temperatura de anelamento. Além disso, os componentes bioativos como aspalatina, notofagina e aspalalinina presentes no extrato da planta atuam como agentes quelantes e redutores. Camellia sinensis extrato de folha também foi usado para sintetizar SnO 2 NPs [53]. Os polifenóis presentes no extrato das folhas atuam tanto como estabilizadores quanto como agentes de cobertura. A microscopia eletrônica de varredura de alta resolução (HR-SEM) e a análise de XRD revelaram a forma esférica SnO 2 NPs com tamanho na faixa de 5–30 nm. Além disso, o bandgap dos NPs diminuiu com o aumento da temperatura de anelamento. O Catunaregam spinosa - SnO sintetizado verde mediado 2 NPs mostraram excelente atividade fotocatalítica contra o corante vermelho do Congo [57]. Os NPs biossintetizados são de forma esférica e tamanho médio de 47 nm.
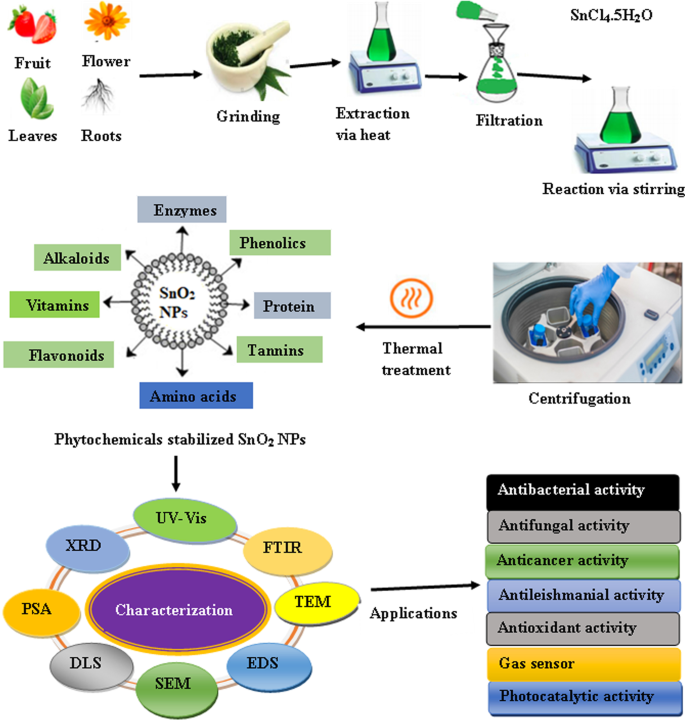
Um diagrama esquemático da síntese mediada por extrato vegetal de SnO 2 NPs
O extrato da folha de Aloe barbadensis miller foi usado para sintetizar SnO 2 NPs de SnCl 2 · 2H 2 O como um precursor [58]. Os NPs resultantes foram esféricos com um tamanho médio variando de 50 a 100 nm. Além disso, as nanopartículas sintetizadas exibiram excelente atividade antibacteriana contra S. aureus e E. coli.
Em outro estudo, a síntese verde de SnO 2 NPs foi feito por um método eficiente e barato usando Plectranthus amboinicus extrato de folha e SnCl 2 · 2H 2 O como material de partida [59]. O extrato vegetal atua como agente redutor e estabilizador. Os NPs resultantes foram caracterizados por SEM, EDX, XRD e PSA. Os NPs eram de forma tetragonal com um tamanho médio de partícula de 63 nm. Além disso, os autores revelaram que os NPs biossintetizados exibiram maior atividade fotocatalítica contra a Rodamina B em comparação com o SnO comercial 2 . Síntese verde de SnO 2 NPs foram relatados usando Nyctanthes arbor-tristis (Parijataka) extrato de flor [60]. Como é evidente a partir da análise de SEM e PSA, as nanopartículas sintetizadas exibiram a morfologia de grânulos finos com minúsculo estágio de aglomeração e tamanho médio de grão de 2-8 nm. O estudo também explorou a hidrólise e o potencial de proteção do extrato da planta.
A síntese verde de SnO 2 NPs foi realizado por um processo de baixo custo e ecológico usando Psidium guajava extrato de folha [61]. O resultado de UV-Vis revelou um pico de ressonância plasmônica de superfície em 314 nm, confirmando a formação de SnO 2 NPs. Além disso, os NPs eram esféricos com tamanho variando de 8 a 10 nm. O estudo também mostrou que as NPs exibem 90% de degradação do amarelo reativo 186 em 180 minutos sob irradiação de luz solar. Bhosale et al. [62] identificou o extrato da folha de Calotropis gigantea como uma fonte natural para a síntese de SnO 2 NPs. Os metabólitos secundários do extrato atuam como agente estabilizador e capeador na conversão de cloreto de estanho em SnO 2 NPs. Os autores sugeriram que os NPs eram esféricos e um tamanho médio entre 30 e 40 nm. Os NPs sintetizados degradam o corante laranja de metila em até 80%, em 120 min. Singh et al. [63] relatou a biossíntese de SnO 2 NPs usando Piper betle extrato de folha. A análise de SEM e TEM revelou a formação de NPs esféricos com um tamanho médio de 8,4 nm. As NPs degradam o amarelo reativo 186 em uma pseudo-primeira ordem com uma eficiência de 92,17%. Além disso, os NPs mostraram excelente seletividade para a remoção do amarelo reativo 186 em comparação com o vermelho reativo 120 e o verde reativo 119. Na literatura, diferentes plantas e extratos de plantas têm sido usados para a preparação de SnO 2 (Tabela 1). Da tabela, pode-se ver que a natureza das espécies de plantas e as condições de reação afetam o tamanho e a forma do SnO 2 NPs.
Síntese mediada por bactérias de nanopartículas de óxido de estanho
Micróbios são importantes nanofábricas que ganham imenso potencial como ferramentas ecológicas e econômicas, evitando produtos químicos tóxicos e a alta energia necessária para a síntese físico-química. Vários micróbios, como bactérias, fungos e leveduras, têm sido usados para a síntese de nanopartículas de metal e óxido de metal, tanto intracelularmente quanto extracelularmente. A síntese intracelular envolve o transporte dos íons metálicos para a célula microbiana e a formação dos NPs na presença da enzima, coenzimas e outras biomoléculas dentro da célula. Na síntese extracelular, os íons metálicos são aprisionados na superfície da célula microbiana. As enzimas e proteínas disponíveis na superfície reduzem os íons metálicos e são responsáveis por fornecer estabilização aos NPs [73]. No entanto, a síntese extracelular é mais vantajosa em comparação com a via intracelular, pois pode ser usada para fabricar grandes quantidades de NPs e elimina várias etapas de síntese necessárias para a recuperação de NPs [74].
A síntese biológica utilizando bactérias é uma abordagem ecológica e econômica em comparação com a síntese química. No entanto, este método tem várias desvantagens:(a) a triagem de micróbios é um processo demorado, (b) requer monitoramento cuidadoso do caldo de cultura e de todo o processo, e (c) é difícil controlar o tamanho e a morfologia de os NPs. Nem todas as bactérias podem sintetizar NPs devido ao seu processo metabólico intrínseco e atividades enzimáticas. Portanto, a seleção cuidadosa de uma bactéria apropriada é necessária para produzir NPs com tamanho e morfologia bem definidos [74]. Por exemplo, um estudo conduzido por Srivastava e Mukhopadhyay [54] relatou um procedimento de baixo custo, verde e mais simples para a síntese de SnO 2 NPs usando Erwinia herbicola fresca e limpa células bacterianas e uma solução aquosa de cloreto de estanho (II). O SnO sintetizado 2 NPs eram principalmente esféricos com tamanho na faixa de 10 a 42 nm. Foi relatado que a proteína bacteriana e outras biomoléculas atuam como um agente redutor e estabilizador durante a síntese de SnO 2 NPs. Essas biomoléculas também ajudaram no controle do tamanho e agregação de SnO 2 NPs.
Biomoléculas e outras sínteses mediadas por fontes verdes de nanopartículas de óxido de estanho
Além da síntese mediada por plantas e bactérias de SnO 2 NPs, os pesquisadores desenvolveram uma abordagem de química verde, ambientalmente benigna e não tóxica, utilizando outras biomoléculas, como aminoácidos, vitaminas, enzimas e açúcares (Tabela 2). Yang et al. [75] SnO sintetizado 2 NPs usando um método de baixo custo e ecologicamente correto usando vitamina C (ácido ascórbico), uma biomolécula naturalmente disponível. A análise TEM mostrou a formação de NPs esféricos com um tamanho médio em torno de 30 nm. A vitamina C atua como um agente limitador e redutor durante a síntese. O estudo sugeriu a vitamina C limitada à superfície do SnO 2 NPs diminuíram o estresse oxidativo causado por SnO 2 NPs nas células, levando a uma redução da perda de peso em camundongos neonatais. SnO esférico 2 NPs com tamanho médio de partícula de 13 nm foram preparados usando carboidratos (amido) [76]. Foi sugerido que o carboidrato atua como um molde, que pode ligar vários cátions metálicos através de seus grupos funcionais e, portanto, uma dispersão uniforme dos cátions foi observada. Em outro estudo, água remanescente coletada de feijões-de-bengala embebidos ( Cicer arietnum L.) foi empregada para sintetizar SnO não dopado 2 e SnO dopado com Ni, Fe e Au 2 NPs [77,78,79]. Os autores sugeriram que a pectina no extrato foi responsável pela síntese do SnO 2 NPs. O tamanho médio do cristalito do SnO não dopado de forma esférica 2 , SnO dopado com Ni 2 e SnO dopado com Au 2 Verificou-se que NPs eram de 11 nm, 6 nm e 25 nm, respectivamente.
Outro estudo mostrou uma abordagem verde para sintetizar SnO 2 NPs usando uma membrana de casca de ovo (ESM) [80], um bio-resíduo natural da casca do ovo da galinha. Foi sugerido que ESM constituintes biomoléculas como ácido urônico e sacarídeos contendo as porções aldeído, que atuam como um agente redutor durante a síntese. A análise morfológica mostrou a formação de forma de bastonete hexagonal e esférica de SnO 2 NPs com tamanho de partícula na faixa de 13–40 nm.
Diferentes aminoácidos como glicina, arginina, ácido aspártico, lisina e tirosina [81,82,83,84,85] foram usados para a síntese verde de SnO 2 NPs devido a seus bons agentes de cobertura ou complexantes. A síntese mediada por aminoácidos elimina o uso de produtos químicos tóxicos durante a síntese. SnO esférico 2 NPs foram sintetizados usando arginina [81]. Os estudos morfológicos sugerem que o SnO sintetizado 2 NPs eram esféricos com um tamanho médio na faixa de 4-5 nm. Bhattacharjee et al. [83] usou glicina para produzir SnO 2 NPs de cloreto estanoso. Foi sugerido que os NPs formados a 200 ° C, 400 ° C e 600 ° C são esféricos, policristalinos e monodispersos na natureza com um tamanho médio de 6, 16 e 33 nm, respectivamente. Além disso, a nanopartícula obtida a 400 ° C era luminescente. Da mesma forma, Begum et al. [84] demonstraram a síntese da estrutura tetragonal rutilo SnO 2 NPs usando L-lisina com tamanho na faixa de 4–17 nm.
Mecanismo de formação de nanopartículas de óxido de estanho por meio da síntese verde
Nos últimos anos, diferentes extratos de plantas, microrganismos e outros derivados biológicos têm sido usados na síntese verde de NPs de metal e óxido de metal. Estudos sugeriram que os metabólitos secundários, como fenóis, flavonóides, taninos, saponinas, terpenóides e carboidratos presentes no extrato da planta, desempenham um papel significativo, agindo como agentes redutores e estabilizadores na síntese de NPs de metal ou óxido de metal [87]. Além disso, a síntese mediada por micróbios pode ser obtida tanto intracelularmente quanto extracelularmente, de acordo com o local onde os NPs são formados. Na síntese extracelular, a biorredução ocorre na superfície das células microbianas na presença das enzimas disponíveis na superfície. Além disso, na biossíntese intracelular, os íons metálicos são transportados para a célula microbiana, e os NPs se formam facilmente lá na presença de enzimas dentro da célula [73]. Selvakumari et al. [53] utilizou Camellia sinensis extrato para a biossíntese de SnO 2 NPs. Eles demonstraram a partir de seus estudos que os compostos polifenólicos (epicatequina, epigalocatequina, galato de epicatequina e galato de epigalocatequina) presentes no extrato atuam tanto como agentes niveladores quanto estabilizadores. O SnO 2 NPs formados por este método consistem em algumas etapas principais, incluindo (i) redução de Sn 2+ para Sn 0 , (ii) o efeito redutor de compostos fenólicos (-OH) do extrato para formar espécies de Sn, e (iii) transformação térmica das espécies de Sn em SnO 2 NPs. No SnO 2 NPs sintetizados usando Calotropis gigantean extrato de folhas, compostos polifenólicos são responsáveis pelas transformações bioquímicas dos íons de estanho [62]. SnO esférico 2 NPs de tamanho no intervalo 3,62-6,34 nm foram sintetizados usando extrato de couve-flor [52]. Foi sugerido que os polifenóis e os flavonóides do extrato se coordenam com os íons metálicos, resultando na formação de Sn (OH) 2 intermediários, que após calcinação levam à formação de SnO 2 NPs. Em outro estudo, Srivastava e Mukhopadhyay [54] relataram a síntese intracelular e extracelular de SnO esférico 2 NPs pelas enzimas secretadas pela bactéria E. herbicola . Neste método, o Sn 2+ Os íons são capturados pelas enzimas extracelulares secretadas pela célula bacteriana ou por proteínas associadas à membrana na superfície celular, e a redução foi iniciada pelas enzimas desidrogenase. O Sn 2+ os íons são reduzidos ganhando dois elétrons e uma molécula de NAD + é oxidado para formar NADH, que finalmente resulta na produção de Sn NPs extracelulares. As nanopartículas de Sn biossintetizadas são então oxidadas pelo oxigênio presente na solução, o que leva à formação de SnO 2 NPs. A análise de FTIR revelou a presença de moléculas semelhantes a proteínas na superfície, que fornecem suporte natural e estabilidade do SnO 2 NPs. Além disso, os aminoácidos atuam como agentes de limitação ou complexação, minimizando assim o uso de produtos químicos tóxicos durante a síntese. O possível mecanismo para a síntese verde de SnO 2 NPs é mostrado na Fig. 2:
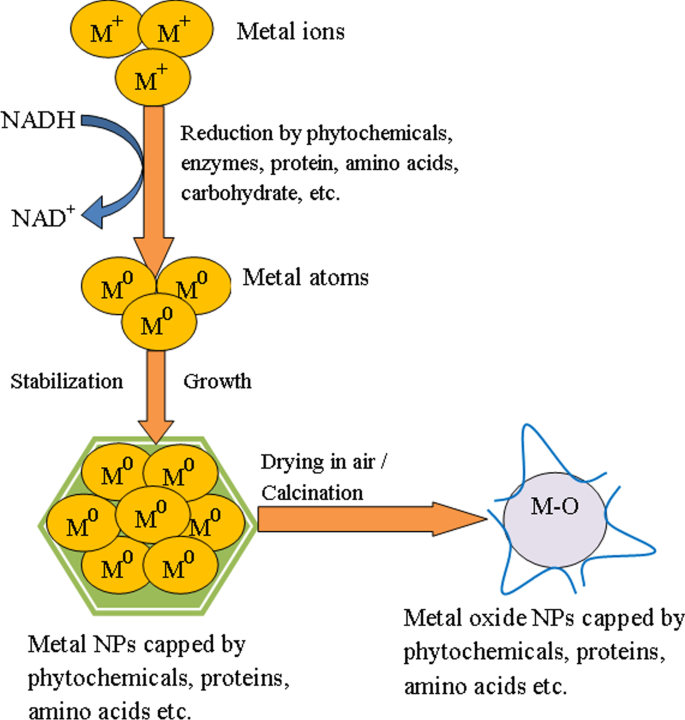
Diagrama mostrando o possível mecanismo para a síntese mediada biologicamente de óxido de metal (SnO 2 ) NPs
Caracterização de nanopartículas de óxido de estanho
A caracterização de NPs é muito importante para conhecer e controlar o procedimento de síntese e a aplicação. A morfologia da superfície e detalhes conformacionais sobre tamanho, forma, cristalinidade e área de superfície dos NPs sintetizados são estudados utilizando várias técnicas. Algumas das técnicas usadas para caracterizar SnO sintetizado em verde 2 NPs são UV – Vis, FTIR, XRD, EDS, SEM e TEM. A espectroscopia UV-Vis é usada para monitorar a formação de nanopartículas estudando suas propriedades ópticas. Espectros de UV-Vis do SnO 2 NPs sintetizados usando Catunaregam spinosa extrato exibiu o pico de absorção mais alto de 223 nm devido à sua ressonância de plasma de superfície [57]. XRD é uma técnica poderosa usada para estudar a estrutura cristalina de materiais. Bhattacharjee et al. [81] caracterizou SnO 2 NPs com picos de XRD em ângulos de difração (2 θ ) de 26,7, 34,2, 38,07, 51,9, 54,9, 58,1, 62,1, 64,9, 66,08, 71,6 e 79,07 correspondendo a (110), (101), (200), (211), (220), (002), (310), (112), (301), (202) e (321) planos, respectivamente (Fig. 3). Os picos de difração padrão mostram a estrutura do rutilo tetragonal de SnO 2 NPs com um tamanho médio de cristalito de 4,6 nm calculado usando a equação de Debye-Scherer [81].
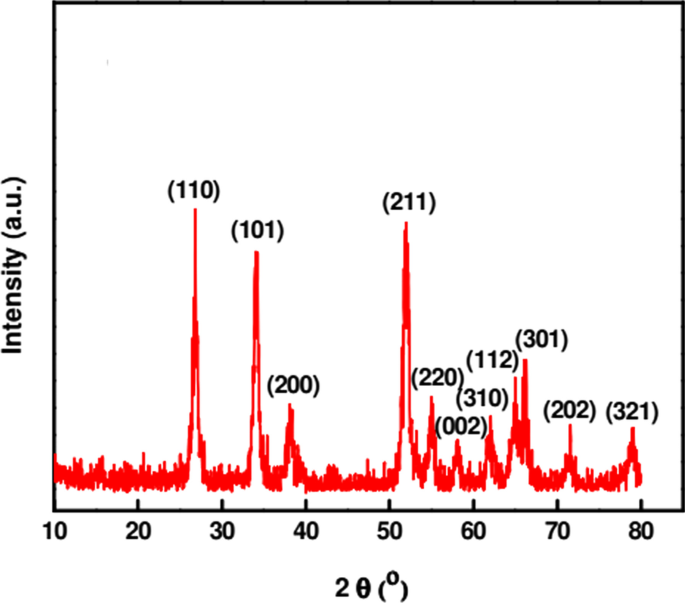
Padrões de XRD de SnO 2 NPs sintetizados usando arginina sob irradiação de microondas [81]
A espectroscopia FTIR é usada para investigar a química da superfície e identificar os grupos funcionais presentes na superfície dos NPs, que podem ser responsáveis pela redução, capeamento e estabilização dos NPs [88]. Análise FTIR de SnO 2 NPs sintetizados usando Pruni flos extrato mostrou bandas de absorção principais em 3308, 2153, 1634, 423, 403 e 383 cm −1 . As bandas fortes observadas em 3308, 2153 e 1634 cm −1 foram atribuídos ao alongamento de vibrações de grupos Sn – OH devido às moléculas de água adsorvidas no SnO 2 superfície, alongamento C – H de alcinos e vibrações C =O de flavonóides, respectivamente. As bandas entre 423 e 383 cm −1 são atribuídos ao alongamento Sn – O – Sn anti-simétrico [70]. Técnicas baseadas em microscopia, como SEM e TEM, têm sido amplamente empregadas para determinar as propriedades morfológicas das nanopartículas. No entanto, TEM fornece melhor resolução e informações sobre a estrutura interna, como estrutura cristalina e morfologia, em comparação com SEM. Os resultados mais precisos das propriedades da superfície podem ser adquiridos usando o FE-SEM. Essas técnicas também são úteis para estimar o tamanho médio das nanopartículas sintetizadas [89]. A análise de FE-SEM e TEM revelou a formação de SnO de forma esférica levemente aglomerada 2 NPs com um tamanho médio de 30–40 nm (Fig. 4) [62].

a Imagens TEM de SnO biossintetizado 2 NPs; b Imagens HR-TEM de SnO 2 NPs; c Imagens FE-SEM de SnO 2 NPs e d Padrões SAED de SnO 2 NPs
Além disso, a análise de difração de elétrons de área seletiva (SAED) mostrou que as partículas são nanocristalinas por natureza (Fig. 4) [62]. A formação da forma esférica SnO 2 NPs sintetizados usando Piper betle extrato aquoso foi determinado por FE-SEM [63]. A partir da análise de TEM e XRD, o tamanho médio dos NPs foi de 8,4 nm.
EDS é uma técnica analítica usada para analisar a composição elementar de uma amostra. Os espectros EDS de SnO 2 NPs sintetizados usando Psidium Guajava extrato de folha revelou a presença de picos Sn e O, o que confirma a formação de SnO puro 2 NPs [61].
Aplicação biológica de nanopartículas de óxido de estanho sintetizado verde
SnO sintetizado verde 2 NPs mostraram maior atividade fotocatalítica, antimicrobiana, antioxidante e anticâncer em comparação com sua forma volumosa. Nesta seção, discutimos as aplicações de SnO sintetizado em verde 2 NPs em várias áreas como orientação para novos pesquisadores para perspectivas futuras.
Atividade Antimicrobiana
Muitos pesquisadores observaram a atividade antimicrobiana SnO 2 NPs. Por exemplo, a atividade antibacteriana de SnO 2 NPs sintetizados usando aloe vera extrato de planta foi estudado usando E. coli e S. aureus . Foi sugerido que os NPs eram mais ativos contra S. aureus do que E. coli [58]. Isso pode ser porque a parede celular de E. coli é mais complexo do que S. aureus . S. aureus tem uma membrana composta de peptidoglicano espesso. No entanto, a parede celular de E. coli possui camada de peptidoglicano mais uma membrana externa composta de lipopolissacarídeo. A membrana externa de E. coli atua como uma barreira que reduz o nível de penetração de ROS na célula [90,91,92]. Another reason could be the difference in the polarity of their cell membrane. The membrane of S aureus has a more positive charge than E. coli , which result in greater penetration level of negatively charged free radicals causing more cell damage and death in S. aureus than in E. coli [93, 94]. The antibacterial activity of SnO2 NPs synthesized using Punica granatum seed extract has been tested against E. coli. The bactericidal effect increased with increasing the concentration of the nanoparticles [95]. SnO 2 NPs synthesized using Trigonella foenum-graecum seed extract also showed similar antibacterial activity against E. coli [72]. In a recent study, Clerodendrum inerme leave extract was used for the synthesis of un-doped and Co-doped SnO2 NPs [96]. The green synthesized un-doped and Co-doped SnO2 NPs were subjected toward antimicrobial activity against five disease-causing pathogens such as E. coli , B. subtillis , A. niger , A. flavus , and C. Albicans, , and their zone of inhibition diameters (ZOIs), minimum inhibitory concentration (MIC), and minimum bactericidal concentration (MBC) were calculated. The Co-doped SnO2 NPs showed substantial antibacterial activity against E. coli e B. subtillis in a concentration-dependent manner compared to the un-doped SnO2 NPs, plant extract, and standard drugs in terms of their MIC (22 ± 0.7, 18 ± 0.8 mg/mL) and MBC (31 ± 0.9, 21 ± 0.6 mg/mL) as well as ZOIs (30 ± 0.08, 26 ± 0.06 nm), respectively. The authors suggested that the broad-spectrum antibacterial activity of Co-doped SnO2 NPs is due to cobalt doping, which leads to increased grain size and surface area of the NPs as compared to un-doped SnO2 NPs. As more is the surface area with smaller particle sizes, the greater will be the antimicrobial activity. The associations of biomolecules like flavonoids and phenolic compounds with Co-doped SnO2 NPs are also responsible for the enhancement of their antimicrobial activity. Furthermore, the green synthesized Co-doped SnO2 NPs showed extraordinary antifungal activity with maximum ZOIs of 17 ± 0.04, 23 ± 0.08, and 26 ± 0.06 nm against A. niger , A. flavus, e C. Albicans, respectively, in comparison with plant extract, un-doped SnO2 NPs, and standard drugs [96].
The actual mechanism of action of SnO2 NPs against microbial strains is still unknown. However, several mechanisms of action against bacteria have been suggested for metal oxide nanoparticles, such as the decomposition of nanoparticles, electrostatic interaction of nanoparticles with the cell wall of microorganisms, and formation of reactive oxygen species (ROS) by the effect of light radiation [97,98,99]. One possible cause for the antibacterial effect of SnO2 NPs may be the accumulation of the NPs on the surface of the bacterial cell membrane. The ROS generated due to the presence of SnO2 NPs interacts with the cell membrane and disturbs the membrane permeability and respiration system of the bacteria, which leads to cell death [72, 95, 100]. For instance, Khan et al. suggested that the release of Sn 4+ e Co 2+ is responsible for the damage of bacterial DNA and mitochondria, which inactivates the bacterial enzyme and finally leads to cell death [96].
Antioxidant Activity
Many researchers examined the antioxidant activity of NPs by monitoring the ability in quenching of stable DPPH (2,2-diphenyl-1-picrylhydrazyl) radical into non-radical form (DPPH-H). Kamaraj et al. [101] reported the antioxidant activity of SnO2 NPs biosynthesized using Cleistanthus Collinus leaves extract. The antioxidant activity of SnO2 NPs increased with increasing concentration of SnO2 NPs and reaction time. In another study [95], the free radical scavenging activity of green synthesized SnO2 NPs increased in a dose-dependent manner. However, the annealed sample exhibited a lower scavenging activity as compared to the as-prepared sample. The decrease in scavenging activity with increasing annealing temperature may be due to a decrease in surface area-to-volume ratio of the NPs. Moreover, the antioxidant efficacy of SnO2 NPs against DPPH is due to the transfer of electron density between the NPs and the free radical located at nitrogen in DPPH. A similar result was found for SnO2 NPs synthesized using Trigonelle foenum-graecum aqueous extract [72]. Hong et al. [67] reported significant antioxidant properties of biosynthesized SnO2 NPs. The antioxidant activity of the biosynthesized SnO2 increased with increasing concentration of the NPs, with IC50 (half-maximal inhibitory concentration) value of 2257.4 µg/ml. Recently, Khan et al. reported significant antioxidant activity of Co-doped SnO2 NPs, as compared to un-doped SnO2 NPs and plant extract [96].
Cytotoxic Activity
SnO 2 NPs synthesized using an aqueous extract of agricultural waste of dried peel of Annona squamosa were evaluated for cytotoxicity test against the hepatocellular carcinoma cell line (HepG2) [64]. TEM results revealed the loss of cell volume, considerable swelling of the cells, and nuclear condensation. The nuclear condensation seen in SnO2 NP-treated HepG2 cells might be due to the breakdown of chromatin in the nucleus. SnO 2 NPs inhibited cell proliferation in a dose- and time-dependent manner with an IC50 value of 148 µg/mL. SnO 2 NPs synthesized using piper nigrum seed extract exhibited higher cytotoxic activity against colorectal (HCT116) and lung (A549) cancer cell lines [69]. The proliferation of both cancer cell lines increased with increasing NPs size. Besides, a gradual decline in cell viability was observed with increasing dosage of SnO2 NPs. The authors concluded that the cytotoxic effect was associated with the generation of oxidative stress from reactive oxygen species (ROS). SnO 2 NPs fabricated by using Pruni spinosae flos aqueous extract revealed an excellent cytotoxic effect against non-small cell lung cancer cell A549 and lung fibroblast CCD-39Lu cells, in concentration- and time-dependent manner [70]. Recently, Khan et al. [96] investigated the in vitro cytotoxic effect of green synthesized un-doped SnO2 NPs and Co-doped SnO2 NPs against mammary gland breast cancer (MCF-7), human amnion (WISH), and human lung fibroblast (WI38) cell lines by a colourimetric technique 3-(4,5-dimethylthiazol-2yl)-2,5-diphenyl tetrazdium bromide (MTT) assay. The green synthesized Co-doped SnO2 NPs showed significant and substantial mortality rate compared to un-doped SnO2 NPs, plant extract, and standard drug 5-FU (5-5-5-fluorouracil), while un-doped SnO2 NPs exhibited a similar mortality rate to that of the standard drug, but the lowest cytotoxicity against breast cancer cell line was observed with the plant extract. The cytotoxic effect of the plant extract, green synthesized un-doped SnO2 , and Co-doped SnO2 NPs was performed with IC50 values of 31.56 ± 1.4, 26.99 ± 1.9, and 18.15 ± 1.0 µg/mL for MCF-7, and 40.69 ± 0.9, 38.97 ± 0.8, and 36.80 ± 0.6 µg/mL for WI38, and 38.56 ± 0.8, 35.56 ± 0.9, and 31.10 ± 0.7 µg/mL, respectively, and depicted that the cytotoxicity of Co-doped SnO2 NPs was more proficient as compared to plant extract and un-doped SnO2 NPs alone. Additionally, the authors reported excellent observational results showing greater in vitro inhibition of breast cancer MCF-7 cell lines in a concentration- and dose-dependent manner. The green synthesized NPs also showed robust cytotoxicity against MCF-7 as compared to WI38 and WISH normal cell lines with Co-doped SnO2 NPs unveiling higher ROS generation than the un-doped SnO2 NPs. Figure 5 shows the probable cytotoxicity mechanism of green synthesized SnO2 NPs.
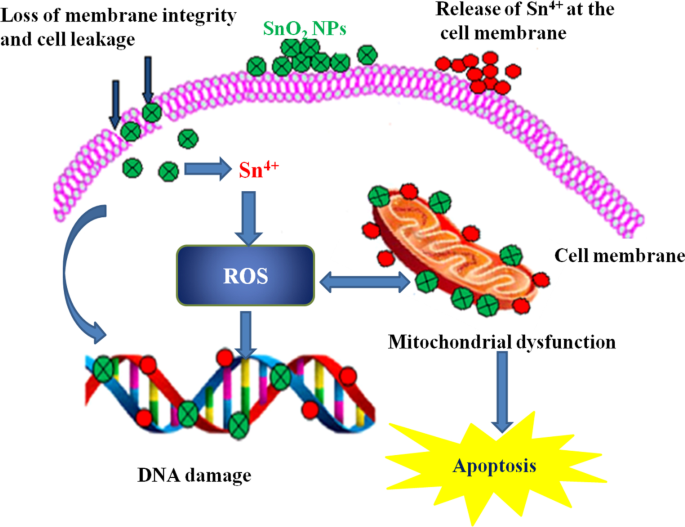
Mechanism during cytotoxicity of green synthesized SnO2 NPs
Photocatalytic Activity
The uncontrolled release of toxic chemicals, hazardous textile dyes, and pesticides from various industries into the running water has led to severe environmental problems. These superfluous water contaminants cause long-term adverse effects and pose a real threat to aquatic and human life. Besides, some organic dyes are carcinogenic and toxic. Hence, treating water that contains poisonous chemicals before disposal to the environment is very crucial to reduce environmental pollution. Recent studies have shown that nanostructured semiconductor metal oxides act as an excellent photocatalyst for the removal of various water pollutants [102,103,104,105]. Among the semiconductor metal oxides, SnO2 is extensively used in the removal of common textile dyes and organic compounds owing to its beneficial characteristics, which include physical and chemical stability, high surface reactivity, high photocatalytic efficiency, low cost, and low toxicity [68, 106]. Manjula et al. [107] synthesized SnO2 nanoparticles using glucose. The NPs were effectively used as a catalyst in degrading methyl orange (MO) dye. The effect of calcination temperature (150–500 °C) on the photocatalytic activity of the NPs was investigated, and the results revealed that the as-synthesized SnO2 NPs calcinated at 150 °C is the best photocatalyst for the reaction under study among the studied materials. Moreover, the as-prepared SnO2 nanoparticles degraded methyl orange completely in 30 min, and also, the nanomaterials may be recycled with enhanced efficiency a minimum of five times. In another study [108], the photocatalytic activity of the SnO2 QDs (quantum dots) synthesized by using serine was evaluated by monitoring the optical absorption spectra of eosin Y solution under direct sunlight. It was observed that the rate of degradation of eosin Y using SnO2 QDs (98%) is higher than that using commercial SnO2 (96%) and P25 (88%). Begum et al. [84] reported the synthesis of SnO2 NPs using an amino acid, L-lysine monohydrate. The synthesized nanoparticles were evaluated for their photocatalytic behavior toward toxic organic dyes, namely malachite green oxalate (MGO) and Victoria blue B (VBB) under direct sunlight. The absorption peak of these dyes has begun to reduce, which shows that the chromophore structure has been demolished (Fig. 6). Furthermore, the as-prepared SnO2 NPs exhibited an outstanding photocatalytic degradation of MGO (97.3%) and VBB (98%) dye within 120 min. Literature reports on the photocatalytic activity of green synthesized SnO2 NPs are summarized in Table 3.
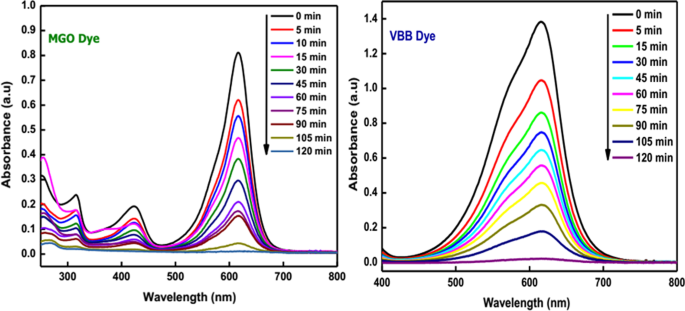
Photocatalytic degradation of malachite green oxalate dye under solar irradiation using SnO2 NPs
Gas-Sensing Property
Many metal oxide-based gas sensors are widely used for gas-sensing applications. However, SnO2 NPs has gained tremendous attention in gas sensing under atmospheric conditions because of its beneficial properties, which include high sensitivity, high selectivity, easy reversibility, and cheap manufacturing costs. Green synthesized porous SnO2 nanospheres demonstrated excellent gas sensing capabilities [107]. It was observed that the assimilation of 0.5 wt% Pd into the SnO2 matrix improved the sensitivity and made it highly selective for low-temperature hydrogen detection. Moreover, the fabric was able to respond to even 50 ppm H2 in N2 at room temperature with an interval of 10 s. These sensing properties are due to the synergetic effect of both the porous structure of SnO2 nanospheres and also the catalytic property of Pd nanoparticles. Gattu et al. [77] reported the gas-sensing behavior of biosynthesized and chemically synthesized Ni-doped SnO2 NPs thin films. The biosynthesized Ni-doped SnO2 NPs thin film showed higher NO2 gas-sensing response as compared to the chemically synthesized ones. The sensor response was found to be increased with Ni doping for both biosynthesized and chemically synthesized Ni-doped SnO2 NPs. This may be due to the reduction of particle size with Ni-doping, which results in increased surface area for adsorption of NO2 gas. Furthermore, the Ni-doped SnO2 thin film exhibited excellent selectivity toward NO2 gas when put next to other gases like NH3 , LPG and H2 S. In another study [78], the gas-sensing properties of un-doped and Fe-doped SnO2 NPs synthesized using Cicer arietnum L. extract were reported. The gas response within the presence of 100 ppm NH3 gas at 200 °C operating temperature was found to be 28% for un-doped SnO2 and 46% for Fe-doped SnO2 filmes finos. Moreover, the Fe-doped SnO2 -based sensor was found to be more selective for NH3 gas as compared to the un-doped SnO2 sensor. The biosynthesized Au-doped SnO2 NPs were found to be highly sensitive to NO2 gas at 200 °C operating temperature [79]. Gas sensor supported Au-doped SnO2 NPs showed the gas response of ~ 30% for 100 ppm of NO2 gas. Additionally, the gas sensor of Au-doped SnO2 NPs showed excellent selectivity toward NO2 gas when put next to other gases like H2 S, LPG, and NH3 . The improved gas response and selectivity toward NO2 gas are because of the lattice distortion induced by Au-doping and also the oxygen vacancies generation within the SnO2 treliça.
Conclusões
The use of green methods for the production of NPs has been the area of focused research because it is an eco-friendly, inexpensive, nontoxic, and sustainable method. Numerous studies report the possibility of producing SnO2 NPs via a green protocol using a range of plant materials, bacteria, and natural biomolecules. The literature survey shows that the green substrates act as reducing and stabilizing agents or capping agents regardless of their source. Among the various green methods of SnO2 synthesis, plant-mediated synthesis is cost-effective, easy to process, and less hazardous than microorganisms. However, the plant extracts consist of a large number of active compounds in a different composition, which makes it difficult to know the exact amount of the molecules responsible for the reduction of metal ions. Due to this complexity, it is difficult to evaluate the synthesis of nanoparticles. Therefore, further study on the mechanism of formation of SnO2 NPs is required to understand the chemical reactions that occur during the synthesis. With the knowledge of the actual reaction mechanism, it will be possible to monitor and optimize the biosynthesis process, which is essential for the large-scale production of SnO2 NPs. Hence, understanding of the rapidly growing method of synthesis discussed herein will help facilitate future research progress on SnO2 NPs and their enormous potential for industrial-scale production in the near future.
Disponibilidade de dados e materiais
Não disponível.
Abreviações
- NPs:
-
Nanopartículas
- SnO2 NPs:
-
Tin oxide nanoparticles
- UV-Vis:
-
Ultraviolet-visible spectroscopy
- SEM:
-
Microscopia eletrônica de varredura
- FE-SEM:
-
Microscopia eletrônica de varredura por emissão de campo
- TEM:
-
Microscopia eletrônica de transmissão
- HR-TEM:
-
Microscopia eletrônica de transmissão de alta resolução
- FTIR:
-
Espectroscopia de infravermelho com transformada de Fourier
- EDS:
-
Energy dispersive X-ray analysis
- PSA:
-
Particle size analyzer
- XPS:
-
X-ray photoemission spectroscopy
- SAED:
-
Selective area electron diffraction
Nanomateriais
- Refratários especiais de óxido e suas aplicações
- Nanopartículas multifuncionais de ouro para aplicações diagnósticas e terapêuticas aprimoradas:uma revisão
- Preparação de nanopartículas de mPEG-ICA carregadas com ICA e sua aplicação no tratamento de dano celular H9c2 induzido por LPS
- Síntese biogênica, caracterização e avaliação do potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
- Toxicidade potencial para fígado, cérebro e embrião de nanopartículas de dióxido de titânio em camundongos
- Propriedades de formação e luminescência de Al2O3:Nanocompósitos de SiOC na base de nanopartículas de alumina modificados por feniltrimetoxisilano
- A preparação da nanoestrutura de casca de gema de Au @ TiO2 e suas aplicações para degradação e detecção de azul de metileno
- Síntese fácil de óxido de estanho mesoporoso semelhante a buraco de minhoca via auto-montagem induzida por evaporação e propriedades aprimoradas de detecção de gás
- Adepto verde na síntese e estabilização de nanopartículas de cobre:atividades catalíticas, antibacterianas, citotoxicidade e antioxidantes
- Platycodon saponins from Platycodi Radix (Platycodon grandiflorum) para a síntese verde de nanopartículas de ouro e prata



