Nanofolhas V6O13 interconectadas 3D cultivadas em têxteis carbonizados por meio de um processo hidrotérmico assistido por sementes como cátodos flexíveis de alto desempenho para baterias de íon-lítio
Resumo
Materiais nanoestruturados autônomos tridimensionais (3D) provaram ser um dos eletrodos mais promissores para armazenamento de energia devido ao seu desempenho eletroquímico aprimorado. E também são amplamente estudados para os sistemas de armazenamento de energia vestíveis. Neste trabalho, V 6 interconectado O 13 nanofolhas foram cultivadas no têxtil carbonizado flexível (c-têxtil) por meio de um método hidrotérmico assistido por sementes para formar um eletrodo autônomo 3D para baterias de íons de lítio (LIBs). O eletrodo exibiu uma capacidade específica de 170 mA h g −1 a uma corrente específica de 300 mA g −1 . Com o revestimento de nanotubo de carbono (CNT), suas capacidades específicas aumentaram ainda mais 12–40% nas várias taxas de corrente. Ele poderia reter uma capacidade reversível de 130 mA h g −1 , 74% da capacidade inicial após 300 ciclos na corrente específica de 300 mA g −1 . Superou a maioria dos óxidos de vanádio de valência mista. O desempenho eletroquímico aprimorado foi atribuído ao efeito sinérgico da nanoestrutura 3D de V 6 O 13 para Li viável + difusão e transporte e rede condutiva hierárquica altamente condutora formada por CNT e fibra de carbono em c-têxtil.
Histórico
Óxidos de vanádio (por exemplo, V 6 O 13 , V 3 O 7 , V 2 O 5 ) são materiais catódicos aplicáveis para bateria de íon-lítio de alta energia (LIB), devido ao seu baixo custo, altas capacidades específicas e abundância de elemento vanádio [1,2,3,4,5,6]. Entre os óxidos, V 6 O 13 tem sido considerado um excelente candidato do material catódico [7,8,9,10,11,12,13,14]. Sua capacidade teórica e densidade de energia podem chegar a 417 mA h g −1 e 890 Wh kg −1 quando litiado no produto final, Li 8 V 6 O 13 [2, 8]. No entanto, V 6 O 13 eletrodos têm sofrido um ciclo de vida curto e capacidade de taxa baixa por um longo tempo porque V 6 O 13 A condutividade eletrônica diminui quando litiado enquanto Li + coeficientes de difusão (10 −8 a 10 −9 cm 2 S −1 ) são baixos [7, 9]. A construção de nanoestruturas 3D autônomas é um método eficaz para resolver os problemas acima. A nanoestrutura 3D pode melhorar o transporte / difusão de íons / elétrons enquanto evita efetivamente a auto-agregação [15,16,17,18,19,20]. Por exemplo, Yu et al. 3D V sintetizado 6 O 13 nanotêxteis montados a partir de nanogrooves interconectados por meio de uma rota de automontagem baseada em solução redox fácil com MnO 2 molde à temperatura ambiente. Em uma faixa de tensão de 1–4 V, V 6 O 13 nanotêxteis exibiram capacidades reversíveis de 326 e 134 mA h g −1 a 20 e 500 mA g −1 , respectivamente, e uma retenção de capacidade acima de 80% após 100 ciclos a 500 mA g −1 [2]. Tong et al. fabricado V 6 O 13 cátodo suportado por uma malha de aço com rugas por percurso semelhante. O eletrodo autônomo com uma quantidade de carga de V 6 O 13 até 2,0 mg cm −2 foi obtido. A uma densidade de corrente de 500 mA g −1 , o V 6 O 13 eletrodo demonstrou uma capacidade inicial de 225 mA h g −1 que se deteriorou para cerca de 150 mA h g −1 após 500 ciclos [21]. No entanto, a pesquisa acima envolveu a eletrodeposição em duas etapas e a remoção de MnO 2 . O crescimento direto da nanoestrutura de óxido de vanádio de valência mista com boas propriedades eletroquímicas permanece um grande desafio [22]. Enquanto isso, estudos anteriores não demonstraram V 6 O 13 cátodo flexível de base, que tem um uso potencial em dispositivos vestíveis.
Aqui, propomos um processo hidrotérmico simples para crescer com sucesso V 6 interconectado O 13 nanofolhas no tecido carbonizado para fabricar um eletrodo autônomo 3D. Exibiu capacidades específicas de 161 e 105 mA h g −1 nas correntes específicas de 300 e 1200 mA h g −1 , respectivamente. Com o revestimento de nanotubo de carbono (CNT) para melhorar ainda mais sua condutividade, suas capacidades específicas aumentaram para 170 e 140 mA h g −1 . Enquanto isso, seu desempenho no ciclismo também foi melhorado. Ele poderia reter 74% da capacidade inicial com revestimento de CNT, em comparação com retenção de 50% sem revestimento de CNT após 400 ciclos a 300 mA g −1 . A melhoria no desempenho eletroquímico foi principalmente atribuída ao efeito sinérgico da nanoestrutura 3D de V 6 O 13 e rede condutiva hierárquica.
Métodos
Síntese de c-têxtil
O pano de bambu disponível comercialmente foi embebido em uma solução com 2,5 g de NaF e 60 ml de H 2 O por 1 h e seco por 5 h em forno a 120 ° C. O têxtil seco foi carbonizado a 800 ° C em N 2 por 30 min para obter c-têxtil.
Crescimento de 3D V 6 O 13 Nanoestrutura em c-têxtil
3D V 6 O 13 a nanoestrutura foi cultivada em c-têxtil por um método hidrotérmico assistido por sementes. C-têxtil foi ligeiramente oxidado no ácido nítrico condensado (80% em peso) por 30 min. V 2 O 5 pó (1 mg) foi adicionado a 5 ml de água desionizada e, em seguida, ultra-sônico por 15 min para obter uma suspensão. O c-têxtil oxidado foi então imerso na suspensão por 2 h, seco e aquecido a 300 ° C por 10 min para fazer crescer a semente de óxido de vanádio em c-têxtil. V 2 O 5 pó (16 mg) foi adicionado a 224 μl de 30% em peso de H 2 O 2 e agitado durante 10 min para obter uma solução castanha. Foi então diluída com mais 40 ml de água destilada e agitada durante 30 min. Depois que a solução foi transferida para uma autoclave de aço inoxidável de 25 ml, o c-têxtil oxidado foi imerso na solução. A autoclave foi mantida a 180 ° C por 48 h, então a amostra foi lavada com água destilada e álcool e seca a 60 ° C por 8 h para finalmente obter o V 6 flexível 3D autônomo O 13 nanoestrutura suportada com c-têxtil flexível. CNT foi posteriormente revestido em V 6 O 13 nanoestrutura, mergulhando-a repetidamente na suspensão de NMP (0,5 mg / mL) de CNT de paredes múltiplas e secando para produzir um V 6 O 13 / Eletrodo composto CNT.
Caracterização de materiais
A morfologia do produto foi observada por microscopia eletrônica de varredura (SEM, Philips XL30 FEG) e microscopia eletrônica de transmissão (TEM, JEOL JEM-2010). As análises de espectroscopia de fotoelétrons de raios-X (XPS) (K-Alpha) foram realizadas usando uma fonte monocromática de Al Ka.
Fabricação de baterias e medições eletroquímicas
Células tipo moeda padrão CR2016 foram montadas em um porta-luvas cheio de argônio (Vigor Inc. Suzhou, China) com V 6 O 13 eletrodo como o eletrodo de trabalho com uma carga de massa de ~ 1 mg cm −2 . Uma folha de lítio foi usada como contra-eletrodo; 1 mol LiPF 6 em uma mistura de carbonato de etileno (EC), carbonato de dietila (DEC) e carbonato de dimetila (DMC) com uma proporção de volume de 1:1:1 foi usado como o eletrólito, e um filme de polipropileno foi usado como o separador. As células montadas foram cicladas eletroquimicamente entre 1,5 e 4,0 V vs. Li / Li + para carga / descarga galvanostática em um sistema de teste de bateria LAND (Wuhan Kingnuo Electronics Co., Ltd., China) a 25 ° C. Os estudos de espectroscopia de impedância eletroquímica (EIS) foram conduzidos com a estação de trabalho Autolab PGSTAT302N na faixa de frequência de 10 mHz a 10 kHz.
Resultados e discussão
O esquema do crescimento de 3D V 6 O 13 nanofolhas interconectadas em c-textile foi mostrado no arquivo adicional 1:Figura S1. O têxtil (Fig. 1a) foi primeiramente carbonizado a 800 ° C para se obter o c-têxtil (Fig. 1b). Imagens SEM (Fig. 2a) mostraram que c-têxtil era composto de feixes de fibras de carbono entrelaçados com um diâmetro de ~ 5 μm. O c-têxtil exibiu excelente flexibilidade e resistência mecânica. Ele foi capaz de ser enrolado e torcido conforme mostrado na Fig. 1c. A resistividade quadrada do c-têxtil foi medida em 5 Ω / sq. com o método de quatro sondas. Assim, foi utilizado como um promissor suporte / coletor flexível para os materiais do eletrodo. Foi então imerso em VO x suspensão, seca e mantida a 300 ° C durante 10 min para fazer crescer os cristais de semente. Sua mudança de peso foi indetectável (<0,1 mg). Depois de ser imerso em óxido de vanádio (VO x ) solução sol para o crescimento hidrotérmico, o c-têxtil preto foi coberto com uma camada de um filme fino verde-amarelo; entretanto, sua flexibilidade foi mantida, conforme mostrado na Fig. 1d. Sua resistividade aumentou para 50 Ω / sq. As imagens de SEM (Fig. 2b, c) mostraram ainda que ele era composto por várias nanofolhas interconectadas de comprimento mícron e várias centenas de nanômetros de largura, como blocos de construção para construir nanoestrutura 3D em c-têxtil. A imagem TEM de alta resolução (Fig. 2f) mostrou franjas de rede bem definidas das nanofolhas crescidas. O espaçamento de 3,5 Å na franja da rede era consistente com (110) distância interplanar do V ortogonal 6 O 13 fase (cartão PDF nº 71-2235) que estava de acordo com o padrão de XRD (Fig. 3c). O mecanismo de crescimento foi aquele cristal de semente primeiramente nucleado nos locais com um grupo funcional contendo oxigênio [23, 24]. Então, durante o processo hidrotérmico no VO x solução aquosa, interconectada V 6 O 13 nanofolhas foram continuamente cultivadas nos cristais de semente. Quanto à formação de microflores estruturadas em 3D, pode ser devido aos vários cristais sementes agregados no mesmo local para o crescimento das nanofolhas. Para determinar ainda mais o estado de valência do elemento vanádio em V 6 O 13 , As análises XPS foram conduzidas no V 6 interconectado sintetizado O 13 nanofolhas. A pesquisa XPS scan (Fig. 3a) revelou que a amostra era composta de elementos V, O, C e N. As energias de ligação para vanádio 2p3 / 2 e 2p1 / 2 foram identificadas na Fig. 3b em 516,0 e 523,9 eV para V 4+ e 517,3 e 525,0 eV para V 5+ , respectivamente. Foi bem consistente com o estado químico do vanádio em V 6 O 13 relatado [25,26,27]. Os resultados acima confirmaram que 3D V 6 O 13 nanoestruturas foram cultivadas com sucesso em c-têxtil por meio de um processo hidrotérmico assistido por sementes simples.

Imagens ópticas de a têxteis disponíveis comercialmente, b têxtil carbonizado, c Têxtil c enrolado e torcido e d c-têxtil com V 6 crescido O 13 no estado enrolado, inserção:no estado plano

Microestrutura de 3D autônomo interconectado V 6 O 13 nanofolhas em c-textile: a , b imagens SEM de baixa resolução de c-têxteis sem e com nanofolhas, respectivamente; c , d imagens SEM de alta resolução de nanofolhas interconectadas cultivadas em c-têxteis; e , f imagens TEM de baixa e alta resolução da nanofolha, respectivamente
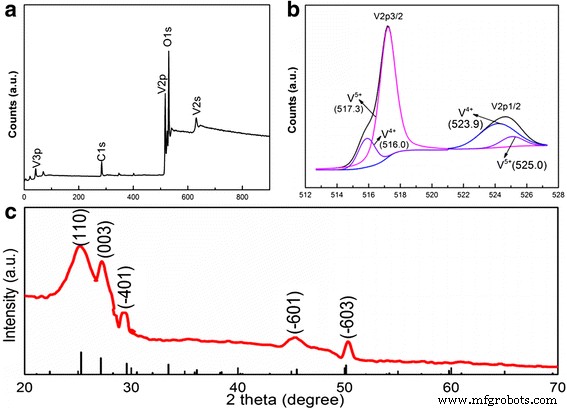
a Uma pesquisa de espectro XPS de 3D autônomo interconectado V 6 O 13 nanofolhas cultivadas em c-têxteis. b Espectro de V 2p e O 1s com uma curva ajustada. c Os padrões de XRD de V 6 O 13
Para investigar o desempenho eletroquímico de 3D V 6 O 13 nanoestruturas cultivadas em c-têxteis, baterias de moeda de meia célula foram montadas com um V 6 O 13 eletrodo como cátodo e folha de lítio como ânodo. A Figura 4a exibiu curvas típicas de voltametria cíclica (CV) de V 6 O 13 eletrodo em uma taxa de varredura de 0,2 mV s −1 entre 1,5 e 4,0 V (vs. Li / Li + ) Os principais picos redox em 2,8 / 2,5 V podem ser facilmente identificados. Pico anódico amplo em ~ 3,2 e 2,3 V e pico catódico em ~ 1,8 V também podem ser observados [11, 28]. O aparecimento dos picos acima indicou transições de fase em várias etapas, e a localização das tensões de pico foi consistente com as relatadas anteriormente [2]. A Figura 4b mostrou a curva de carga / descarga galvanostática para o primeiro ciclo na corrente específica de 30 mA g −1 . Vários platôs de tensão mal definidos podem ser identificados. Na curva de vazão, foram identificados dois platôs inclinados em 2,3 e 2,8 V, correspondentes aos picos anódicos. Quando as correntes específicas aumentaram de 30 para 150, 300, 600 e 1200 mA g −1 , as capacidades específicas foram 253, 176, 161, 133 e 105 mA h g −1 . As boas propriedades eletroquímicas foram devido à nanoestrutura 3D composta por V 6 O 13 nanofolhas. Essa estrutura aberta poderia entrar em contato com eletrólitos muito bem e encurtar o Li + caminho de transporte e difusão. A morfologia do V 6 original O 13 eletrodo e o eletrodo ciclado com SEI foi examinado em MEV (arquivo adicional 1:Figura S2). A morfologia das nanofolhas interconectadas 3D foi mantida durante o ciclo. Isso sugere ainda mais a importância da nanoestrutura 3D na integridade estrutural de V 6 O 13 eletrodo durante o ciclo eletroquímico. No entanto, a condutividade de V 6 O 13 diminuiu conforme a litiação prosseguia [7, 29]. Além disso, o comprimento da nanofolha no V 6 O 13 eletrodo atingiu várias dezenas de mícrons. Apenas uma pequena porção da nanofolha individual está diretamente conectada com as fibras de carbono condutor do c-têxtil, que servia como coletor. Isso pode dificultar a transferência de elétrons durante o processo de carga / descarga. Para aumentar ainda mais a condutividade e, portanto, as propriedades eletroquímicas do 3D autônomo V 6 O 13 eletrodo, ele foi imerso em dispersão de CNT para mergulhar o CNT em sua superfície. A Figura 5a, b mostrou imagens SEM do V 6 O 13 eletrodo com CNT. CNT foi depositado com sucesso no plano de V 6 O 13 nanofolhas e intimamente contatado com eles. Até mesmo a ponte foi construída por meio de CNTs entre nanofolhas vizinhas, como mostrado na Fig. 5c. Como esperado, a resistividade do V 6 O 13 eletrodo com CNT diminuiu de 50 para 20 Ω / sq. Após o revestimento de CNTs, o pico redox apareceu na mesma posição no perfil CV (Fig. 4a) enquanto as correntes de pico aumentaram. Indicou cinética rápida de reação eletroquímica em V 6 O 13 eletrodo com CNT. The V 6 O 13 eletrodo com CNT exibiu melhor desempenho de taxa em comparação com o eletrodo sem revestimento de CNT, como mostrado na Fig. 4c. As capacidades de descarga específicas foram 261, 185, 170, 153 e 140 mA h g −1 nas correntes específicas de 30, 150, 300, 600 e 1200 mA g −1 , respectivamente, correspondendo a um aumento de 12 ~ 40% em comparação com o cátodo composto sem CNTs. Para verificar ainda mais o papel do CNT, calculamos o coeficiente de difusão de íons de lítio com voltametria cíclica. The V 6 O 13 / Os coeficientes de difusão anódica e catódica do CNT foram 4,79 × 10 −8 e 2.01 × 10 −8 cm 2 s −1 , maior do que V 6 O 13 eletrodo 2,42 × 10 −8 e 1,7 × 10 −8 cm 2 s −1 , respectivamente (e a discussão associada está no arquivo adicional 1:Figura S3). Gráficos de Nyquist (Fig. 6a) de V 6 O 13 eletrodo e V 6 O 13 eletrodo com CNT exibiu formas semelhantes, uma forma de semicírculo no domínio de alta a média frequência e uma linha inclinada nas regiões de baixa frequência, correspondendo à impedância da reação eletroquímica (processo de transferência de carga) e processo de difusão de íons de lítio. A inserção é o circuito equivalente usado para ajustar os gráficos de Nyquist. No circuito, CPE é o elemento de ângulo de fase constante e W é a impedância de Warburg. R s e R ct representam a resistência ôhmica (resistência total do eletrólito, separador e contatos elétricos) e a resistência de transferência de carga, respectivamente [22, 30]. Arquivo adicional 1:A Tabela S1 listou os parâmetros usados para ajustar os gráficos. R ct para o V 6 O 13 / O eletrodo CNT foi calculado para ser 37,24 Ω, menor do que o de V 6 O 13 (55,58 Ω). Esta diminuição na resistência à transferência de carga foi atribuída à adição de CNT. O mecanismo foi ilustrado na Fig. 6b. CNT intimamente conectado com V 6 O 13 nanofolhas para transferência de elétrons mais rápida. Além disso, os CNTs e a fibra de carbono na rede condutiva hierárquica composta por c-têxteis para uma melhor condução de elétrons. A ciclabilidade de V 6 O 13 eletrodos foi mostrado na Fig. 4d. Na corrente específica de 300 mA g −1 , o eletrodo com revestimento de CNT poderia manter 74% da capacidade inicial de 170 mA h g −1 após 300 ciclos de carga / descarga, enquanto o V 6 O 13 eletrodo reteve apenas 42% de sua capacidade inicial. Superou a maioria dos óxidos de vanádio de valência mista de baixa dimensão ou sua nanoestrutura 3D listada no arquivo adicional 1:Tabela S2. A melhor ciclabilidade de V 6 O 13 eletrodo com CNT pode ser atribuído aos seguintes motivos:(1) Reforçado com CNT, V 6 O 13 As propriedades mecânicas de foram melhoradas. (2) Mesmo se V 6 O 13 a nanoestrutura foi quebrada durante o processo de descarga / carga, ainda estava ligada ao CNT e poderia ser ativada eletroquimicamente. (3) Auto-segregação de V 6 O 13 nanofolhas foram limitadas pelo aparecimento de CNT. (4) O revestimento de CNT pode ser uma barreira válida para aliviar a reação lateral do óxido de vanádio com o eletrólito, se houver. Assim, o revestimento de CNT pode ser uma maneira alternativa fácil de melhorar a condutividade da nanoestrutura 3D, além do revestimento de carbono e do revestimento polimérico, que geralmente requerem um tremendo trabalho de síntese química [14]. O desempenho eletroquímico geral de V 6 O 13 cátodo foi limitado pela condutividade do tecido de carbono, a difusividade de Li em V 6 O 13 materiais e transferência de elétrons entre V 6 O 13 nanoestruturas e o tecido de carbono. No trabalho futuro, melhorias adicionais podem ser feitas das seguintes maneiras:(1) reduzindo a resistência do substrato de tecido de carbono, (2) dopagem V 6 O 13 com enxofre para melhorar sua difusividade do íon de lítio e (3) revestir o V 6 O 13 com revestimento de polímero condutor.
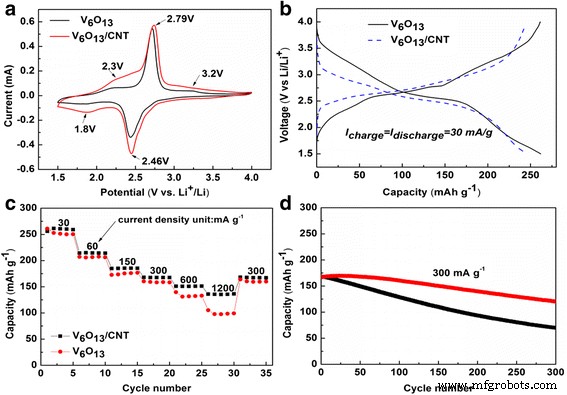
Desempenho eletroquímico do 3D autônomo V 6 O 13 eletrodos com / sem revestimento CNT. a Curvas de voltametria cíclica. b Curvas de carga / descarga galvanostática. c Avaliar. d Desempenho de ciclabilidade dos dois eletrodos

Microestrutura de V 6 revestido com CNT O 13 eletrodo. a Imagem SEM de baixa resolução do eletrodo. b , c Imagem SEM de alta resolução do eletrodo mostrando CNT cobrindo a nanofolha e fazendo a ponte entre as nanofolhas
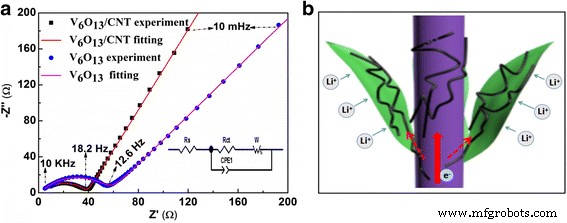
a Gráficos de Nyquist de V 6 O 13 eletrodo com / sem revestimento CNT. b Esquema do caminho de transporte de elétrons em V 6 revestido com CNT O 13 eletrodo
Conclusões
Em resumo, fabricamos com sucesso 3D autônomo V 6 O 13 nanoestrutura composta de nanofolhas interconectadas por meio de um processo hidrotérmico assistido por sementes fácil como um cátodo para LIB. O eletrodo exibiu bom desempenho eletroquímico. Ele poderia ser melhorado com o revestimento 3D V 6 O 13 nanoestrutura com CNT, superando a maioria dos óxidos de vanádio de valência mista. Seu excelente desempenho deveu-se à sua nanoestrutura 3D aberta e rede condutiva hierárquica composta por CNT em nanoescala e fibra de carbono em microescala. O projeto da nanoestrutura 3D com o bloco de construção (por exemplo, nanofio, nanofolha) combinado com a construção do caminho condutor hierárquico por revestimento de CNT pode ser estendido a outros materiais de eletrodo para melhor desempenho eletroquímico.
Abreviações
- 3D:
-
Tridimensional
- CE:
-
Eficiência Coulombic
- CNT:
-
Nanotubo de carbono
- c-textile:
-
Têxtil carbonizado
- CV:
-
Voltametria cíclica
- DEC:
-
Carbonato de dietila
- DMC:
-
Carbonato de dimetila
- EC:
-
Carbonato de etileno
- EIS:
-
Espectroscopia de impedância eletroquímica
- LIB:
-
Bateria de íon-lítio
- SEM:
-
Microscopia eletrônica de varredura
- TEM:
-
Microscopia eletrônica de transmissão
Nanomateriais
- Necessidade de desenvolver um processo de padronização de corantes
- Graus PVDF renováveis para baterias de íon-lítio
- Síntese fácil de nanopartículas de SiO2 @ C ancoradas em MWNT como materiais de ânodo de alto desempenho para baterias de íon-lítio
- Composto de MoS2 / Acetileno com poucas camadas como um ânodo eficiente para baterias de íon-lítio
- Efeito de diferentes ligantes no desempenho eletroquímico do ânodo de óxido de metal para baterias de íon-lítio
- Composto de Si / Grafeno incorporado fabricado por redução térmica de magnésio como material de ânodo para baterias de íon-lítio
- Um ânodo de filme Fe2O3 nanocristalino preparado por deposição de laser pulsado para baterias de íon-lítio
- Cátodos autônomos de folha carbonizada impregnada com selênio para baterias de sódio-selênio de alto desempenho
- Síntese de NiCo2O4 semelhante ao ouriço-do-mar por meio de estratégia de automontagem orientada por carga para baterias de íon-lítio de alto desempenho
- Perguntas e respostas:Otimizando baterias de íon de lítio para carregamento extremamente rápido



