Poli (ácido γ-glutâmico) promove maior descloração de p-clorofenol por nanopartículas de Fe-Pd
Resumo
O ferro zero valente em nanoescala (nZVI) tem se mostrado bastante promissor no tratamento de compostos orgânicos clorados, mas a rápida agregação e inativação dificultam sua aplicação. Neste estudo, nanopartículas de ferro dopadas com paládio zero-valente envolvendo poli (ácido γ-glutâmico) (Fe-Pd @ PGA NPs) foram sintetizadas. As nanopartículas eram pequenas (~ 100 nm), uniformemente distribuídas e altamente estáveis. O desempenho de decloração de Fe-Pd @ PGA NPs foi avaliado usando p -CP como modelo. Os resultados demonstraram que os NPs Fe-Pd @ PGA mostram alta atividade, mesmo em condições alcalinas fracas. A constante de taxa máxima atingiu 0,331 min - 1 em pH 9,0 com Fe para p -CP ratio de 100. Além disso, a atividade de descloração dos NPs Fe-Pd @ PGA é mais de dez vezes maior do que a dos NPs Fe-Pd nus, demonstrando o papel crucial do PGA neste sistema. Além disso, investigamos o desempenho da decloração na presença de diferentes ânions. Os resultados indicaram que Fe-Pd @ PGA NPs podem manter alta atividade na presença de Cl - , H 2 PO 4 - , e ácido húmico, enquanto HPO 4 2− e HCO 3 - os íons reduzem ligeiramente a atividade de descloração. Acreditamos que o PGA é um estabilizador e promotor promissor para Fe-Pd NPs e os Fe-Pd @ PGA NPs têm potencial para aplicações práticas.
Histórico
A poluição da água levantou preocupações globais sobre a sustentabilidade ambiental e muitos materiais de alto desempenho foram desenvolvidos para os tratamentos eficazes de poluição [1,2,3,4,5]. O ferro zero valente em nanoescala (nZVI) tem sido intensamente estudado e é considerado um dos nanomateriais mais promissores para a remediação ambiental de contaminantes diversificados, como compostos orgânicos clorados, íons de metais pesados, pesticidas e corantes orgânicos [1, 6, 7 ] Tem a capacidade extraordinária de transformar contaminantes tóxicos em formas não tóxicas por meio de processos de redução química, mas as nanopartículas de nZVI reagem facilmente com a água e perdem elétrons que contribuem para a reação de degradação [8]. Portanto, um outro metal sempre foi usado como dopante para produzir uma nanopartícula bimetálica, como Fe-Pd ou Fe-Ni, para aumentar as taxas de degradação [9, 10]. No entanto, existem van der Waals e forças magnéticas atrativas entre as partículas nZVI, que levam a agregações significativas, dificultando seu transporte em aqüíferos contaminados e prejudicando a reatividade [11, 12]. As deficiências intrínsecas de nZVI, mesmo sistemas bimetálicos, podem enfraquecer o efeito de remoção e limitar a viabilidade de utilização.
Para inibir a agregação, esforços extensivos foram feitos para aplicar estabilizadores de superfície de polímero (por exemplo, polissacarídeos, polieletrólitos e surfactantes). Esses estabilizadores podem fornecer repulsão eletrostática e estérica para evitar a agregação de partículas [13]. Por exemplo, He et al. [14] sintetizou nZVI estabilizado por carboximetilcelulose (CMC), e as nanopartículas derivadas foram usadas com sucesso para destruição in situ de etenos clorados, como tricloroetileno (TCE) e bifenilos policlorados (PCBs). Petersen et al. [15] produziram nZVI na presença de poli (ácido acrílico) (PAA), alcançando uma alta taxa de degradação para contaminantes clorados. Liu et al. [16] sintetizou nZVI estabilizado por CMC e poliacrilamida aniônica (APAM) e observou que a modificação de APAM levou à agregação de nZVI em suspensão, enquanto a modificação de CMC fez nZVI se dispersar bem. Este estudo forneceu evidências de que a estrutura molecular desempenhou um papel importante no efeito de modificação de nZVI. Muitos outros tipos diferentes de modificadores macromoleculares têm sido usados para revestir partículas nZVI. [17] Além do problema de agregação, outro problema é a passivação da superfície devido à formação de camadas de óxido, como goethita (α-FeOOH), maghemita (γ-Fe 2 O 3 ) e hematita (α-Fe 2 O 3 ) Estudos anteriores demonstraram que as condições ácidas favorecem evitar a passivação superficial do nZVI e manter sua ativação superficial [18,19,20]. Portanto, o valor do pH é um parâmetro crucial que afeta a formação da camada de óxido. Tem havido muitos relatórios estudando a reação em condições ácidas para melhorar a eficiência de descloração [21, 22]. Além disso, a rápida inativação causada por ânions comuns e ácido húmico (HA, matéria orgânica comumente encontrada na água [23]) também limitou a aplicação de campo de nZVI [24, 25]. Portanto, materiais baseados em nZVI adaptados a condições alcalinas com diferentes ânions são esperados.
O poli (ácido γ-glutâmico) (PGA), um polipeptídeo aniônico natural produzido por Bacillus subtilis, não é tóxico, é altamente solúvel em água e pode ser química, física e enzimaticamente degradado na natureza. É feito de unidades de ácidos l- e d-glutâmicos conectados com amidas entre α-amino e ácido γ-carboxílico [26]. Tem amplas aplicações nas indústrias alimentícia, química, biológica e médica [27,28,29]. Além disso, o PGA é um potencial biossorvente para a remoção e recuperação de metais pesados de águas residuais devido à sua capacidade de ligar íons metálicos. Por exemplo, Jamiu et al. [30] sintetizou uma resina à base de PGA como um sorvente para sequestrar Co 2+ íons da solução aquosa. Hu et al. [31] desenvolveram um sorvente biocompósito incorporando PGA para adsorção e recuperação de Cu 2+ íons. Bodnar et al. [32] descreveu a preparação de nanopartículas biodegradáveis com base na complexação de PGA com Pb 2+ íons, demonstrando que o PGA foi um adsorvente promissor para a remoção de metais pesados em águas poluídas. Levando em consideração que o PGA aniônico tem grupos carboxila abundantes, que podem fornecer repulsão eletrostática e estérica para evitar a agregação de partículas, bem como alta capacidade de ligação para os íons metálicos via quelação e ligação eletrostática [33, 34], tentamos usá-lo como um estabilizador e agente de coordenação para sintetizar Fe-Pd NPs e ainda quelar Fe 2+ / Fe 3+ íons gerados a partir da corrosão de NPs de Fe-Pd. Especulamos que o PGA pode melhorar o desempenho de NPs de Fe-Pd em condições alcalinas com diferentes ânions.
Aqui, sintetizamos as nanopartículas de Fe-Pd modificadas por PGA (denotadas como Fe-Pd @ PGA NPs). As nanopartículas foram caracterizadas por microscopia eletrônica de varredura (SEM), microscopia eletrônica de transmissão (TEM), difração de raios X (XRD) e espectroscopia de infravermelho com transformada de Fourier (FTIR). A estabilidade coloidal de Fe-Pd @ PGA NPs também foi avaliada. Além disso, p -Clorofenol ( p -CP) (um dos derivados fenólicos mais tóxicos [35,36,37]) foi selecionado como um poluente modelo para avaliar a atividade de descloração de Fe-Pd @ PGA NPs. A decloração de p -CP sobre os NPs com diferentes dosagens de carregamento de PGA e Pd foi investigado. Vale ressaltar que todos os experimentos foram conduzidos em condições fracamente alcalinas sem controle de pH (o valor do pH foi de aproximadamente 9). Além disso, também investigamos a descloração de p -CP na presença de diferentes ânions e HA para avaliar seu uso potencial em águas residuais reais.
Métodos
Materiais
PGA (M W 100.000–50.000 kDa) foi adquirido da Yuanye Bio-Technology (Shanghai, China). Sulfato ferroso heptahidratado (FeSO 4 · 7H 2 O,> 99,0%), boro-hidreto de potássio (KBH 4 , 97%), cloropaladita de potássio (K 2 PdCl 4 , 98%) e p -clorofenol ( p -CP, 99%) foram fornecidos pela Aladdin Reagent Company (Shanghai, China). Metanol (CH 3 OH, grau de HPLC, 99,9%) foi adquirido na Concord Technology (Tianjin, China). Cloreto de sódio (NaCl, 99%), bicarbonato de sódio (NaHCO 3 , 99,7%), hidrogenofosfato dissódico (Na 2 HPO 4 , 99%) e di-hidrogenofosfato de sódio (NaH 2 PO 4 , 99%) foram adquiridos na Chemregeant (Tianjin, China). O ácido húmico (HA, técnico) foi adquirido na Heowins (Tianjin, China). Todos os produtos químicos foram utilizados sem purificação adicional. Toda a água foi purificada por um sistema de purificação de água Sartorius arium pro VF (resistividade de 18,2 MΩ).
Preparação de Fe-Pd @ PGA NPs
Os NPs Fe-Pd @ PGA foram sintetizados usando um método de redução química no qual o boro-hidreto de potássio serviu como um reagente de redução. Em seguida, 250 mg de FeSO 4 · 7H 2 O foi adicionado em 50 mL de solução de PGA contendo diferentes massas de PGA (10, 25, 50 e 70 mg), resultando nas concentrações desejadas de Fe 2+ e PGA (% em peso). A mistura foi então purgada com argônio por aproximadamente 20 min para garantir a formação de Fe 2+ Complexo -PGA e para remover o oxigênio dissolvido (DO). Então, 3 mL de KBH 4 (50 mg mL - 1 ) foi injetado na mistura em um BH 4 -to-Fe 2+ razão molar de 3,0 para formar os NPs de Fe. Para garantir o uso eficiente do redutor, a suspensão foi purgada com Argônio por 15 min até cessar a evolução do gás (hidrogênio). Em seguida, as nanopartículas de Fe foram testadas como partículas monometálicas ou carregadas com traços (0,1, 0,2, 0,4 e 0,8% em peso de Pd / Fe) de Pd para produzir as nanopartículas bimetálicas estabilizadas por PGA adicionando quantidades conhecidas de solução aquosa de cloropaladita de potássio na suspensão de nanopartículas. Além disso, NPs de Fe-Pd nuas com diferentes graus de carregamento de Pd também foram preparadas para comparação. O sistema foi constantemente purgado com argônio durante a síntese e a reação de descloração. A temperatura da solução foi mantida a 25 ° C por um banho de água termostático.
Teste de estabilidade
Para os experimentos de sedimentação, as suspensões de NPs Fe-Pd @ PGA preparadas na última etapa foram transferidas do reator para um tubo de vidro de 50 mL. A suspensão foi agitada sem sonicação antes do experimento. Em seguida, o tubo de vidro de 50 mL foi deixado assentar e a extensão da sedimentação foi registrada tirando fotos dos tubos de vidro em intervalos periódicos.
Experimentos de descloração em lote
O 550 mg L - 1 solução estoque de p -CP foi preparado dissolvendo p -CP em água a 25 ° C. Além disso, 2 mL de p A solução estoque de -CP foi adicionada à suspensão preparada de Fe-Pd para resultar na proporção molar inicial desejada de Fe para p -CP (105:1) e inicial p -CP concentração de 20 mg L - 1 . Então, a degradação de p -CP foi iniciado e a reação foi realizada com a purga de argônio. Para a medição da concentração de p -CP, 0,8 mL de amostra líquida foi retirado da solução em tempos selecionados desejados, então um ímã foi usado para acelerar a sedimentação. O sobrenadante líquido foi então filtrado através de um filtro de membrana de seringa (0,22 μm) e posteriormente testado com cromatografia líquida de alta eficiência (HPLC). Todos os pontos experimentais foram duplicados em dois experimentos consecutivos, e os desvios padrão foram calculados.
p - Testes de remoção de CP em águas subterrâneas simuladas
Nestes testes, a concentração inicial de p -CP foi definido para 20 mg L - 1 , o mesmo que a concentração anterior de experimentos de descloração em lote, as concentrações de ânions foram definidas para 1 mM e 5 mg / L de ácido húmico foi adicionado à suspensão para simular uma situação de água subterrânea que ocorre naturalmente. A receita de água subterrânea simulada é composta por diferentes tipos de ânions após a adição de diferentes tipos de sais inorgânicos, incluindo NaCl (0,1 mM), Na 2 HPO 4 · 12H 2 O (0,1 mM), NaH 2 PO 4 (0,1 mM), e NaHCO 3 (1 mM). O pH da suspensão da reação também foi registrado durante a reação.
Caracterização
Microscopia eletrônica de varredura (SEM, Hitachi S-4800) e microscopia eletrônica de transmissão de alta resolução (HRTEM, JEM-2100F) foram usados para investigar a morfologia e o tamanho dos NPs Fe-Pd modificados por PGA e nus. As amostras HRTEM foram diluídas e ultra-sônicas em etanol, seguido de queda da suspensão resultante nas grades de cobre revestidas de carbono e secagem em temperatura ambiente. A medição da difração de raios-X (XRD) foi realizada usando um instrumento de medição Bruker D8-Focus com uma fonte de raios-X Cu Kα. As análises de espectroscopia de infravermelho com transformada de Fourier (FTIR, Nicolet Nexus 670) foram conduzidas para elucidar a interação entre os NPs Fe-Pd e PGA. As amostras mencionadas anteriormente para a seção “Caracterização” foram lavadas com água e álcool três vezes, a seguir secas em estufa a vácuo em temperatura ambiente e armazenadas. O p A concentração de -CP em solução foi medida por HPLC.
Resultados e discussão
Síntese e caracterização de Fe-Pd @ PGA NPs
Conforme mostrado no Esquema 1, Fe NPs zero-valentes (Fe @ PGA NPs) foram sintetizados reduzindo Fe 2+ com KBH 4 na presença de PGA. Depois disso, Fe-Pd @ PGA NPs foram obtidos através da reação de substituição entre Pd 2+ (K 2 PdCl 4 ) e Fe 0 . Para avaliar a atividade de descloração, p -CP foi selecionado como um poluente modelo, e o processo de descloração também é mostrado no Esquema 1.
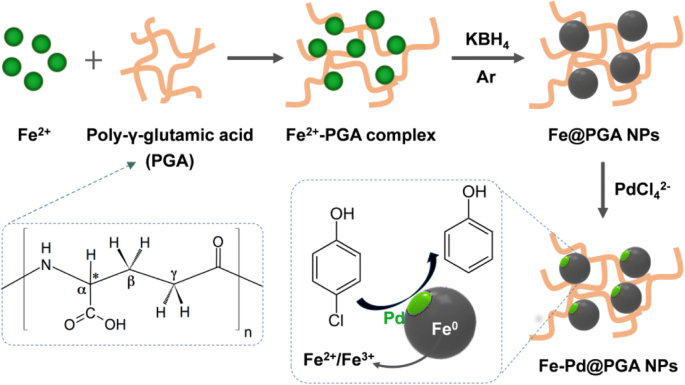
Ilustração esquemática para a síntese de Fe-Pd @ PGA NPs e a descloração de p -CP
As morfologias e o tamanho dos NPs Fe-Pd e Fe-Pd @ PGA nus foram caracterizados por SEM e TEM. Como mostrado na Fig. 1a, b, a maioria dos NPs Fe-Pd @ PGA tinha formas relativamente esféricas na faixa de tamanho de 50–200 nm e estavam conectadas a algumas estruturas semelhantes a chips, que foram atribuídas à modificação PGA. A estrutura é semelhante à relatada anteriormente usando o método de redução química [38]. A distribuição e composição elementar foram mostradas no arquivo Adicional 1:Figura S1 e Arquivo Adicional 1:Tabela S1. A imagem SEM mostra que os NPs Fe-Pd @ PGA tinham superfícies esféricas lisas, enquanto os NPs Fe-Pd nus já haviam sido oxidados, o que provou que o PGA poderia inibir a agregação e restringir a oxidação (Fig. 1c, d). Em geral, em comparação com nZVI modificado por outros estabilizadores em trabalho anterior [16]. Os NPs Fe-Pd @ PGA tinham formato e tamanho semelhantes.

a , b TEM e c Micrografias SEM dos NPs Fe-Pd @ PGA. d Micrografia SEM de NPs de Fe-Pd nuas
A Figura 2a mostra o padrão de XRD de Fe-Pd @ PGA NPs que se assentaram no ar por 1 dia. O pico em 2θ de 44,8 ° e um pico fraco em 82,5 ° indicou a presença de α-Fe 0 com uma natureza mal ordenada e amorfa nas NPs [16, 39]. Outros dois picos característicos fracos apareceram em 2θ de 35,6 ° e 65,2 ° , que combinava com os produtos de corrosão de Fe 0 , magnetita (Fe 3 O 4 ), e / ou magnetita (γ-Fe 2 O 3 ) [40, 41], sugerindo que apenas uma pequena porção de Fe 0 foi oxidado. O padrão XRD verificou que nZVI foi criado com sucesso.
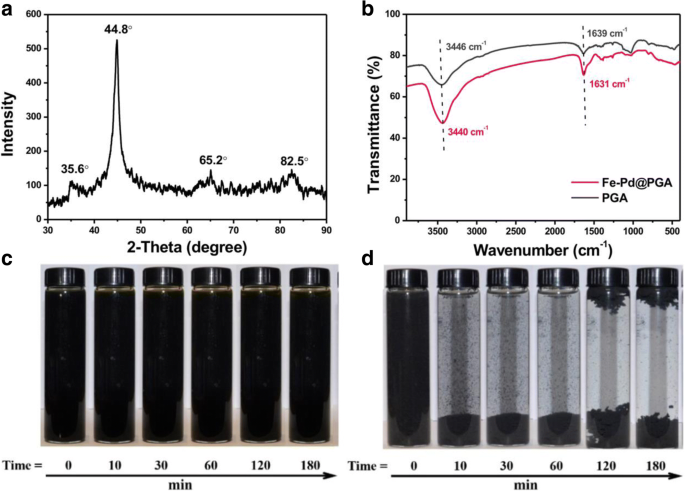
a Padrão de XRD de Fe-Pd @ PGA NPs. b Espectros FTIR de NPs PGA e Fe-Pd @ PGA. c , d Fotos de Fe-Pd @ PGA NPs ( c ) e NPs Fe-Pd simples ( d ) suspensão em momentos diferentes
A Figura 2b é o espectro de FTIR de NPs PGA e Fe-Pd @ PGA no intervalo de 4000–400 cm - 1 . O pico de absorção em 3440 cm - 1 é uma característica da vibração de alongamento O - H das hidroxilas nos grupos carboxila. O pico de absorção na vizinhança de 1631 cm - 1 é uma característica da vibração de alongamento C =O dos grupos carboxila. O pico de absorção entre 900 e 650 cm - 1 vem dos grupos amido de PGA [42, 43]. O ligeiro deslocamento do pico de absorção dos NPs Fe-Pd @ PGA indicou a interação dos NPs Fe-Pd e PGA.
A estabilidade coloidal de Fe-Pd @ PGA NPs e Fe-Pd NPs nuas foi investigada por experimentos de sedimentação. As NPs de Fe-Pd nuas agregaram-se rapidamente em 10 min, e o sedimento preto visível pode ser observado no fundo do tubo (Fig. 2d). Após 120 min, formou-se a flotagem e a floculação gerada, que pode ser atribuída à geração de hidrogênio. Como esperado, os NPs Fe-Pd @ PGA foram bem dispersos e dificilmente se acomodaram no fundo do tubo de vidro por mais de 180 min, como mostrado na Fig. 2c. Além disso, descobrimos que a agregação de NPs Fe-Pd @ PGA ocorreu após 1 dia de repouso (Arquivo adicional 1:Figura S2). A estabilidade coloidal de Fe-Pd @ PGA NPs é comparativa e ainda melhor do que os clássicos Fe-Pd NPs modificados por CMC (por exemplo, para 5 g L - 1 de CMC-nZVI, o tempo de liquidação é de 30 min [44]).
Decloração de p-CP por Fe-Pd @ PGA NPs
A atividade de decloração dos NPs Fe-Pd @ PGA foi investigada através do lote p - Testes de descloração de CP em condições fracamente alcalinas (pH =9). A Figura 3a-c mostra a remoção de p -CP usando NPs simples de Fe-Pd e Fe-Pd @ PGA com diferentes carregamentos de Pd. Os resultados indicaram que os NPs de Fe-Pd simples sem modificação de PGA poderiam remover apenas aproximadamente 50% p -CP em 4 h, enquanto os NPs Fe-Pd @ PGA têm uma eficiência de degradação amplamente aprimorada. Especificamente, os NPs de Fe-Pd @ PGA com 25 mg de PGA e 0,8% de carga de Pd podem remover mais de 90% p -CP dentro de 30 min. Um aumento adicional na carga de PGA para 50 mg poderia atingir 100% p -Remoção de CP em 30 min. Esses resultados demonstraram que o PGA promove a atividade aumentada de descloração de NPs de Fe-Pd. Do ponto de vista de uma reação mediada por superfície, a reatividade foi proporcional à área de superfície disponível [39]. A modificação do PGA poderia evitar que as nanopartículas se aglomerassem, então os NPs de Fe-Pd eram menores e, conseqüentemente, tinham uma área de superfície total maior por unidade de massa. Como esperado, os NPs Fe-Pd @ PGA foram mais eficazes do que os NPs Fe-Pd simples para remover p -CP.
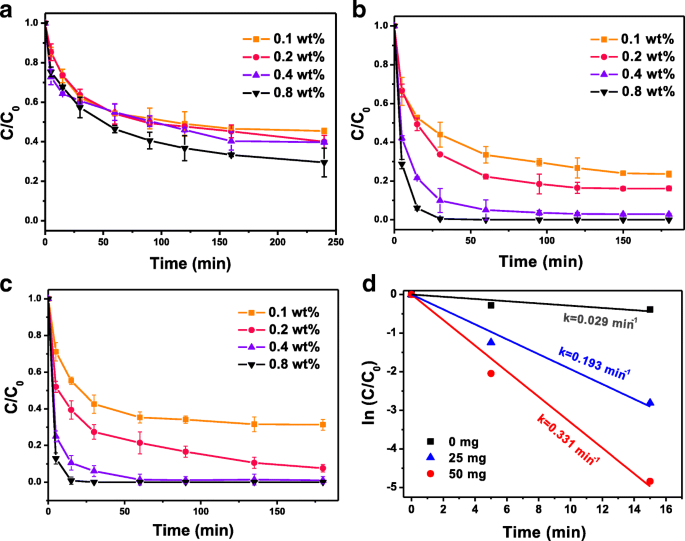
a - c Cursos de tempo de descloração usando NPs de Fe-Pd simples ( a ) e Fe-Pd @ PGA NPs ( b , c ) com diferentes carregamentos PGA ( b 25 mg de PGA; c 50 mg de PGA) e diferentes cargas de Pt variaram de 0,1 a 0,8% em peso. d A constante de taxa ( k ) para a descloração de p -CP com diferentes carregamentos de PGA em pH 9,0 (carregamento de Pd =0,8% em peso)
Durante a descloração de p -CP por Fe-Pd @ PGA NPs, o carregamento de Pd também é um fator importante para a atividade de descloração. Como mostrado na Fig. 3b, c, os NPs Fe-Pd @ PGA com maior teor de Pd exibiram maior atividade de descloração. Este fenômeno é consistente com o relatado em muitos estudos anteriores. Uma explicação é que o Fe e o Pd podem formar células galvânicas, e o Pd poderia aceitar elétrons do Fe, que desempenhava papéis catalíticos não apenas acelerando a corrosão do Fe, mas também melhorando a atividade de descloração [45]. É importante notar que, sem a modificação do PGA, é difícil alcançar alta eficiência de decloração, mesmo com alto carregamento de Pd. Portanto, a modificação do PGA é crucial para a alta atividade de descloração dos NPs Fe-Pd @ PGA.
Geralmente, descloração de p -CP por Fe-Pd NPs segue uma lei de taxa de pseudo-primeira ordem [46], que pode ser modelada usando a seguinte equação:
$$ \ mathit {\ ln} \ left (\ frac {C} {C_0} \ right) =kt $$ (1)
onde C e C 0 são concentrações químicas de p -CP às vezes t (min) e 0, respectivamente, k (min - 1 ) é a constante de taxa e t é o tempo de reação. Portanto, o k valor dos sistemas de descloração é a inclinação de ln ( C / C 0 ) versus t hora extra. Cálculos da constante de taxa para a decloração de p -CP com diferentes carregamentos de PGA são mostrados na Fig. 3d. O valor de k para os NPs Fe-Pd simples é 0,029 min - 1 , enquanto aumentou para 0,331 min - 1 para NPs Fe-Pd @ PGA a 50 mg de carregamento de PGA. A Figura 4 mostra o p - Constantes de taxa cinética de degradação do CP ( k ) das NPs de Fe-Pd com vários graus de carregamento de PGA e Pd. As constantes de taxa de pseudo-primeira ordem aumentaram com o aumento do conteúdo de Pd, semelhante à tendência de eficiência de descloração e, conforme o carregamento de PGA aumentou de 0 para 50 mg, k aumentou com o aumento do carregamento PGA. No entanto, pareceu que a reação de descloração foi restringida e, portanto, a constante de velocidade mostrou um declínio com um aumento adicional da carga de PGA de 50 para 70 mg. Conforme mostrado no arquivo adicional 1:Figura S3, as imagens SEM mostram a agregação significativa de NPs Fe-Pd @ PGA devido ao excesso de cobertura de PGA, levando à diminuição da atividade de descloração. Esta diminuição na atividade de descloração também foi observada em estudos anteriores [47, 48]. Portanto, houve um carregamento de PGA ideal (~ 50 mg) e a constante de taxa de reação de remoção máxima é de 0,331 min - 1 .
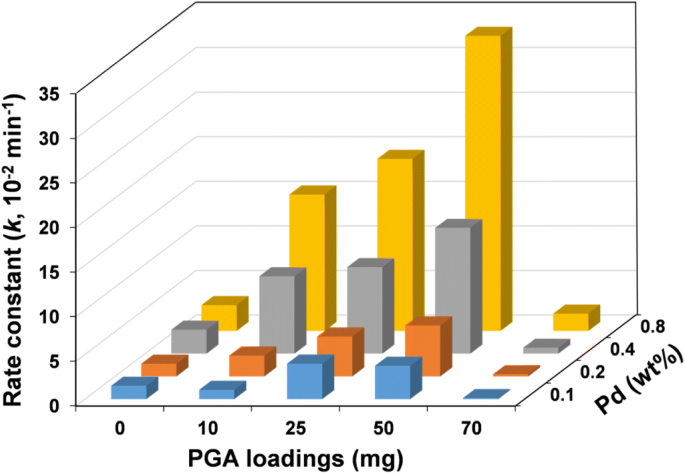
A constante de taxa de descloração de p -CP com carregamento PGA e Pd diferente
A Tabela 1 resume os diferentes estabilizadores usados para a síntese de nZVI e os parâmetros experimentais correspondentes e os resultados da reação de descloração para p -CP. Podemos descobrir que k em nosso trabalho foi mais de 1 ou 2 ordens maior do que os valores relatados em estudos anteriores, apesar da proporção menor de Fe para p -CP (n Fe / p -CP ) e maior valor de pH usado neste trabalho. Em geral, um alto n Fe / p -CP (por exemplo,> 1000) e condições neutras ou ácidas (por exemplo, pH =3) foram usadas para atingir alta atividade de descloração. Neste estudo, a n Fe / p -CP de 100 e pH 9, os NPs Fe-Pd @ PGA exibiram alta atividade de descloração, o que demonstrou que o PGA é um estabilizador promissor de nZVI para a descloração de p -CP.
Decloração de p -CP na água subterrânea estimulada
Testamos P -Remoção de CP em águas subterrâneas estimuladas para avaliar potenciais aplicações práticas. O experimento em branco foi realizado usando NPs Fe-Pd @ PGA modificados com 25 mg de PGA com carregamento de 0,8% de Pd. O impacto dos constituintes dissolvidos na água subterrânea estimulada foi avaliado na presença de quatro tipos de íons (Cl - , H 2 PO 4 - , HPO 4 2− e HCO 3 - ) e HA. Conforme mostrado na Fig. 5a-c, na presença de Cl - , H 2 PO 4 - , ou HA, o k os valores são muito próximos aos do experimento em branco, enquanto HPO 4 2− e HCO 3 - íons reduzem a atividade de descloração, o k os valores diminuíram de 0,173 para 0,06 e 0,07 min - 1 . No trabalho anterior, o aumento do pH após a adição de ânions foi considerado uma das razões importantes para a inibição da atividade [49].
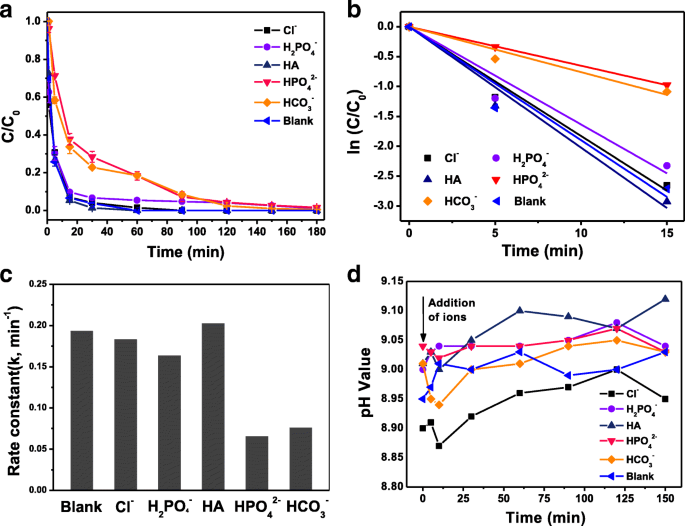
a Cursos de tempo e ( b , c ) constante de taxa de descloração de p -CP na simulação de águas subterrâneas com diferentes constituintes. d As mudanças no pH após a adição de constituintes durante a reação
O processo de reação de decloração de p -CP pode ser representado da seguinte forma [20]:
$$ {\ mathrm {Fe}} ^ 0 \ a {\ mathrm {Fe}} ^ {2 +} + 2 {\ mathrm {e}} ^ {-} $$$$ 2 {\ mathrm {H}} _2 \ mathrm {O} +2 {\ mathrm {e}} ^ {-} \ overset {\ mathrm {Pd}} {\ to} 2 {\ mathrm {H}} ^ {\ ast} +2 {\ mathrm {OH}} ^ {-} $$$$ \ mathrm {Pd} + {\ mathrm {H}} ^ {\ ast} \ to \ mathrm {Pd} - \ $$$$ \ mathrm {H} \ mathrm { Pd} - \ mathrm {H} + \ mathrm {R} - \ mathrm {Cl} \ to \ mathrm {Pd} + \ mathrm {R} - \ mathrm {H} + {\ mathrm {Cl}} ^ {- } $$
As equações acima indicam que o valor do pH é um parâmetro crucial que afeta a taxa de degradação de p -CP. Em pH mais alto, menos hidrogênio ou hidreto atômico na superfície das partículas está disponível para atacar as moléculas cloradas. Enquanto isso, os íons ferrosos e hidroxila formam hidróxido ferroso e precipitam. A camada de passivação superficial do hidróxido ferroso e precipitado pode impedir o transporte das moléculas cloradas e bloquear os locais reativos no Fe e, portanto, diminuir a taxa geral de reação. Com isso em mente, medimos os valores de pH durante a reação de descloração, conforme mostrado na Fig. 5d. O resultado mostrou que não há mudança óbvia nos valores de pH após a adição de diferentes íons, provavelmente devido à presença de PGA. Um ligeiro aumento nos valores de pH foi observado com o aumento do tempo e, finalmente, valores relativamente estáveis foram observados. Os resultados indicaram que a mudança de pH não é a razão dominante para a inibição de íons. Além disso, também investigamos a descloração de p-CP em pH 5 (Arquivo adicional 1:Figura S4). Os resultados indicaram que a condição de ácido fraco favoreceu a reação de descloração. Quanto à inibição de HPO 4 2− e HCO 3 - , é necessário um estudo mais aprofundado para compreender o mecanismo.
Mecanismo de Decloração Aprimorada de p -CP por Fe-Pd @ PGA NPs
Com base em nossos resultados experimentais, um possível mecanismo de decloração aumentada por Fe-Pd @ PGA NPs foi proposto, como mostrado na Fig. 6.
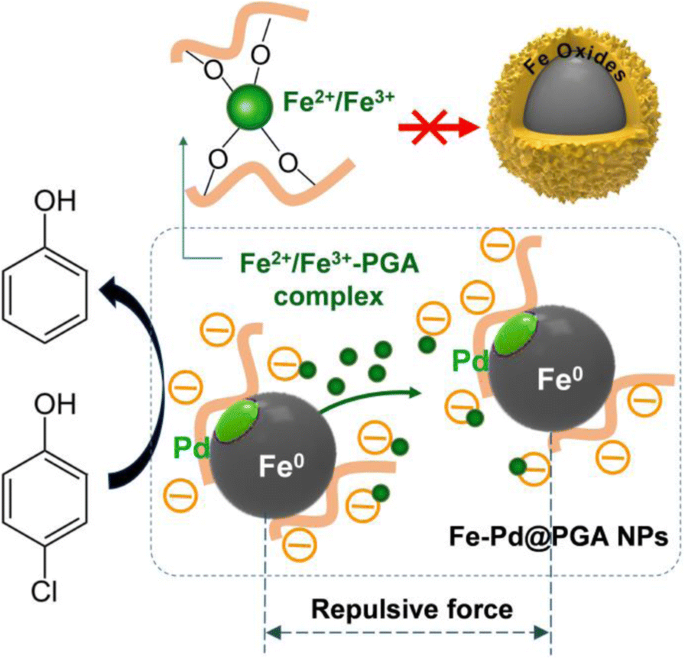
Mecanismo de descloração melhorada de p -CP por Fe-Pd @ PGA NPs
Por um lado, é geralmente assumido que nZVI tem óxido / hidróxido de ferro na casca [50], com a casca do óxido de ferro contribuindo com cargas positivas [51]. Portanto, as moléculas de PGA com grupos de ânions abundantes de carboxila (COO - ) poderia ser facilmente anexado à superfície de NPs de Fe-Pd com cargas positivas. Os grupos carboxila de PGA foram inferidos para se conectar com as superfícies de Fe-Pd NPs através de três métodos de complexação possíveis:(i) quelante monodentado, (ii) quelante bidentado e (iii) ponte bidentada [52]. Além disso, a organização de nanopartículas poliméricas fornece um arcabouço eficiente com dimensões em nanoescala, aumentando assim a área específica das nanopartículas. A modificação dos NPs de Fe-Pd com PGA não apenas estabiliza os NPs, mas também evita que os NPs se aglomerem por meio de repulsão eletrostática e estérica. Portanto, a excelente eficiência de descloração e a boa dispersidade dos NPs Fe-Pd @ PGA foram atribuídas principalmente à estrutura complexa dos NPs Fe-Pd @ PGA e à interação de repulsão estérica-eletrostática.
Por outro lado, o PGA pode ligar íons metálicos (por exemplo, Fe 2+ , Fe 3+ ) por meio de quelação e ligação eletrostática. Conforme mostrado no arquivo adicional 1:Figura S5, os espectros de UV-vis de soluções contendo íons Fe e PGA indicaram a formação de complexos de PGA-ferro [53]. Durante o processo de descloração, Fe 2+ e Fe 3+ depositam-se nas superfícies das NPs de Fe, levando à formação de hidróxidos de ferro e espessando a casca do óxido de ferro. Na presença de PGA, os íons Fe provenientes da reação de descloração formariam complexos com o PGA e restringiriam a formação de hidróxidos de ferro, evitando assim a precipitação do hidróxido de Fe na superfície, preservando os sítios ativos dos NPs Fe-Pd e proporcionando um microambiente favorável para reter a reatividade de decloração. Nesse caso, p - CP as moléculas podem acessar facilmente os sítios ativos e ser rapidamente descloradas por NPs de Fe-Pd.
Conclusões
Em resumo, sintetizamos com sucesso as nanopartículas bimetais de Fe-Pd usando PGA como estabilizador. Os NPs Fe-Pd @ PGA conforme preparados exibem boa dispersidade e estabilidade coloidal. O desempenho de decloração de Fe-Pd @ PGA NPs foi avaliado usando p -CP como o modelo. Os resultados indicaram que o PGA promove significativamente a descloração de p -CP, alcançando um alto k valor de 0,331 min - 1 . Este valor é muito maior do que os relatados anteriormente, apesar da proporção menor de Fe para p -CP e valor de pH mais alto foram usados neste trabalho. Além disso, descobrimos que os NPs Fe-Pd @ PGA mantêm alta atividade na presença de Cl - , H 2 PO 4 - e HA, que geralmente estão presentes na água. Propusemos que a alta atividade de descloração de Fe-Pd @ PGA NPs é atribuída principalmente à interação de repulsão eletrostática-estérica e à prevenção da formação de hidróxido de Fe devido à capacidade de ligação de PGA a Fe 2+ / Fe 3+ íons. Dada a boa estabilidade, alta atividade de descloração e tolerância a íons, os NPs Fe-Pd @ PGA apresentam aplicações promissoras na descloração de compostos orgânicos clorados.
Abreviações
- APAM:
-
Poliacrilamida aniônica
- CMC:
-
Carboximetilcelulose
- FAÇA:
-
Oxigênio dissolvido
- Fe-Pd @ PGA NPs:
-
Nanopartículas de ferro dopado com paládio zero-valente envolvendo poli (ácido γ-glutâmico)
- FTIR:
-
Espectroscopia de infravermelho com transformada de Fourier
- HA:
-
Ácido húmico
- HPLC:
-
Cromatografia líquida de alta performance
- nZVI:
-
Ferro zero valente em nanoescala
- PAA:
-
Poli (ácido acrílico)
- PCBs:
-
Bifenilos policlorados
- p -CP:
-
p -Clorofenol
- PGA:
-
Poli (ácido γ-glutâmico)
- SEM:
-
Microscopia eletrônica de varredura
- TCE:
-
Tricloroetileno
- TEM:
-
Microscopia eletrônica de transmissão
- XRD:
-
Difração de raios X
Nanomateriais
- Nanopartículas de FePO4 biocompatíveis:entrega de drogas, estabilização de RNA e atividade funcional
- Preparação e atividade de hidrogenação catalítica aprimorada de nanopartículas de Sb / Palygorskite (PAL)
- A detecção fotoeletroquímica aprimorada de ácido úrico em nanopartículas de Au Eletrodo de carbono vítreo modificado
- Bioflavonóide direcionado ao receptor de folato Nanopartículas de quitosana carregadas com genisteína para efeito anticâncer avançado em cânceres cervicais
- Atividades fotocatalíticas aprimoradas por nanopartículas de Au-plasmônica em fotoeletrodo nanotubo de TiO2 revestido com MoO3
- Estabilidade aprimorada de nanopartículas magnéticas de ouro com poli (ácido 4-estirenossulfônico-ácido co-maleico):propriedades ópticas sob medida para detecção de proteínas
- Poliglicerol hiper-ramificado modificado como dispersante para controle de tamanho e estabilização de nanopartículas de ouro em hidrocarbonetos
- Efeitos sinérgicos de nanopartículas de Ag / BiV1-xMoxO4 com atividade fotocatalítica aprimorada
- Desempenho de detecção de H2 altamente aprimorado de heterojunções MoS2 / SiO2 / Si de poucas camadas por decoração de superfície de nanopartículas de Pd
- Comparação entre o ácido fólico e a funcionalização baseada no peptídeo gH625 de nanopartículas magnéticas Fe3O4 para internalização celular aprimorada



