Nanopartículas de óxido de gadolínio funcionalizadas com ácido hialurônico para radioterapia de tumores guiada por ressonância magnética
Resumo
A localização imprecisa e a radiorresistência intrínseca de tumores sólidos dificultaram seriamente a implementação clínica da radioterapia. Neste estudo, nós fabricamos nanopartículas de óxido de gadolínio funcionalizadas com ácido hialurônico (HA-Gd 2 O 3 NPs) por meio de um processo hidrotérmico de um único recipiente para imagens de ressonância magnética (MR) e radiossensibilização de tumores eficazes. Em virtude da funcionalização de HA, o HA-Gd 2 como preparado O 3 NPs com um diâmetro de 105 nm mostraram dispersibilidade favorável em água, baixa citotoxicidade e excelente biocompatibilidade e prontamente entraram no citoplasma de células cancerosas por endocitose mediada por receptor de HA. É importante ressaltar que HA-Gd 2 O 3 NPs exibiram alta relaxividade longitudinal ( r 1 ) 6,0 mM −1 S −1 como agentes de contraste de ressonância magnética e aumento da radiossensibilização de uma maneira dependente da dose. Estas descobertas demonstraram que HA-Gd sintetizado 2 O 3 Os NPs como agentes teranósticos bifuncionais têm grande potencial no diagnóstico de tumores e na radioterapia.
Introdução
A radioterapia tem sido amplamente aplicada no câncer, que envolve raios-X de alta energia e deposição de doses de irradiação nos locais do tumor, causando danos por radicais livres ou danos ao DNA [1,2,3,4]. No entanto, baixa radiossensibilidade, imprecisão da localização do tumor e má discriminação entre lesões e tecidos normais que causam efeitos colaterais de irradiação limitam a implementação clínica da radioterapia [5]. Portanto, é importante desenvolver métodos para aumentar a radiossensibilidade tumoral, minimizando os efeitos colaterais sistêmicos. Uma combinação de nanotecnologia e radioterapia é uma prioridade bem estabelecida para a radiossensibilização.
Nos últimos anos, a nanotecnologia tem sido considerada uma estratégia atraente para o diagnóstico e terapia do câncer [6,7,8,9,10,11]. Uma das funções principais das nanopartículas (NPs) é um direcionamento de tumor preciso com base no acúmulo seletivo de NPs em tecidos tumorais por meio de direcionamento passivo, efeito de permeabilidade e retenção aprimorada (EPR), direcionamento ativo e tempo de circulação prolongado [12, 13,14]. Nosso trabalho anterior demonstrou que dopar NPs de carbono com heteroátomos efetivamente ajusta suas propriedades intrínsecas e introduz características benéficas [15,16,17]. Curiosamente, NPs podem ser usados como radiossensibilizadores [18]. NPs de metal pesado (com alto elemento Z) (por exemplo, Au, Bi, Gd) como radiossensibilizadores promissores podem ser usados em terapia de radiossensibilização por causa de sua alta seção transversal de captura de fótons de raios-X e efeito de espalhamento Compton [19]. Quando os raios X interagem com nanopartículas de alto Z, elétrons Auger e fotoelétrons, a liberação de elétrons secundários prejudica as células cancerosas, proporcionando aumento da dose durante a terapia de radiação [20]. Até o momento, os NPs à base de gadolínio (GdNPs) demonstraram ser agentes de contraste (CAs) de IRM eficazes [21, 22] e diferenciam o tecido normal do tecido doente e das lesões de maneira não invasiva e em tempo real. Esses agentes encurtam o tempo de relaxamento longitudinal para afetar a relaxividade longitudinal r 1 [23], e seu direcionamento impreciso freqüentemente resulta em efeitos colaterais. É bem conhecido que o ácido hialurônico (HA) é um ligante principal e um transportador de entrega de drogas para locais-alvo com receptores de HA, como o determinante de cluster 44 (CD44) [24,25,26].
Com base nos resultados de estudos anteriores, usamos HA como um ligante de direcionamento para funcionalizar Gd 2 O 3 NPs com funções duplas:MRI CAs e radiossensibilizadores eficazes de direcionamento a tumor para superar a radiorresistência inerente e a imprecisão da localização do tumor. Além disso, HA-Gd 2 O 3 NPs exibem alta relaxividade longitudinal ( r 1 ) como agentes de imagem de RM promissores com melhor qualidade de imagem de RM. Comparado com os CAs atualmente disponíveis [27, 28], o HA-Gd como resultante 2 O 3 NPs mostram três vantagens significativas:em primeiro lugar, o HA-Gd 2 O 3 NPs exibem biocompatibilidade favorável devido ao uso da matriz extracelular natural como os precursores. Em segundo lugar, a funcionalização de HA melhora significativamente o direcionamento do tumor e reduz os efeitos colaterais. Finalmente, o HA-Gd 2 O 3 NPs possuem capacidade bifuncional em diagnóstico e terapia. A fim de verificar a eficácia e explorar o mecanismo de aprimoramentos de radiossensibilização, avaliamos o efeito de radiossensibilização de HA-Gd 2 O 3 NPs sobre a viabilidade das células tumorais, o ciclo celular e a apoptose.
Resultados e discussão
Preparação e caracterização de HA-Gd 2 O 3 NPs
Neste estudo, HA-Gd 2 O 3 NPs foram preparados com sucesso usando um processo hidrotérmico simples, conforme mostrado no Esquema 1. Os tamanhos das partículas foram analisados por espalhamento de luz dinâmico, enquanto o exame morfológico foi conduzido por microscopia eletrônica de transmissão. Conforme mostrado na Fig. 1a, HA-Gd 2 O 3 NPs exibiram dispersão uniforme e formas quase esféricas discretas sem agregação aparente. Os diâmetros médios do HA-Gd 2 O 3 NPs foram de 105 nm. Em comparação com os tecidos normais, a permeabilidade endotelial capilar dos tecidos tumorais foi aumentada e o gap endotelial foi de 100–600 nm [29]. Portanto, NPs com tamanhos desejáveis foram facilmente imersos em tecidos tumorais e podem aumentar drasticamente a eficiência da entrega de drogas de direcionamento passivo.
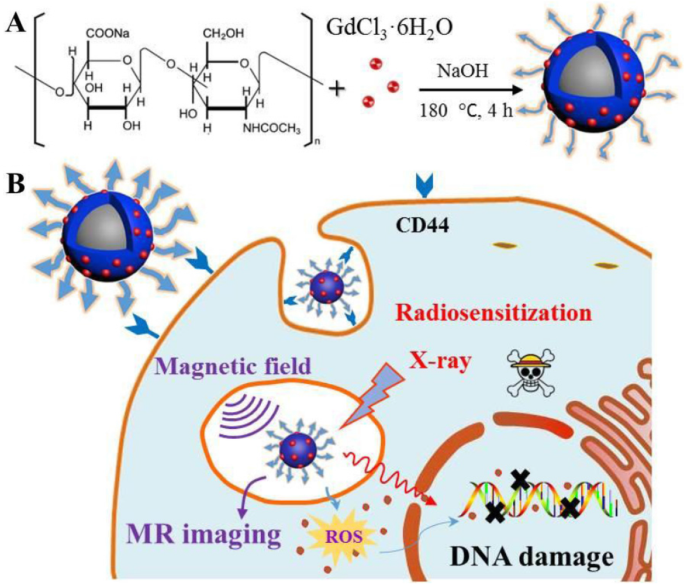
Síntese esquemática de HA-Gd 2 O 3 NPs do método hidrotérmico (A) e as seguintes aplicações biomédicas (B)
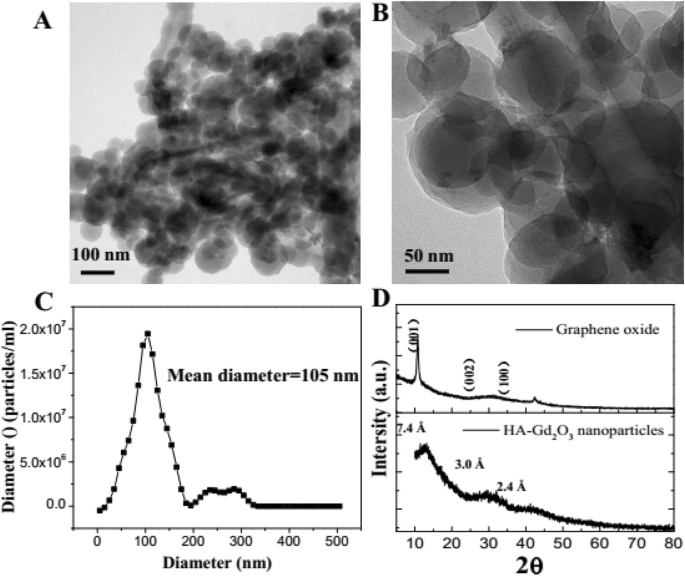
Caracterização de HA-Gd 2 O 3 NPs. Baixo ( a ) e alto ( b ) imagens TEM de ampliação. A distribuição do diâmetro ( c ) e padrões de XRD ( d ) de HA-Gd 2 O 3 NPs
A estrutura de fase de HA-Gd 2 O 3 NPs foi investigado por XRD usando óxido de grafite (GO) como um controle. Como mostrado na Fig. 1d, um pico de difração principal (2 θ =12,04 °) e dois picos menores (2 θ =29,6 °, 42,1 °) foram observados no HA-Gd 2 O 3 Padrão de difração NP, que correspondeu aos picos característicos de GO (plano 100) e grafite (plano 002), respectivamente. O espaçamento da rede principal de HA-Gd 2 O 3 NPs apresentaram espaçamento menor (0,73 nm calculado pela fórmula de Bragg) do que o espaçamento GO de d 001 =0,85 nm, onde o deslocamento para cima na posição do pico pode ser atribuído à diminuição do espaçamento entre o sp 3 camadas. Todos os picos de difração ampla demonstraram que HA-Gd 2 O 3 NPs tinham uma estrutura amorfa, que pode ser atribuída ao carbono altamente desordenado e diminuição da sp 2 (C – C) espaçamento das camadas durante o processo de carbonização. O resultado indicou ainda HA-Gd 2 O 3 NPs com uma natureza cristalina pobre possuíam uma estrutura multicamadas heterogênea, o que era consistente com nossos relatórios anteriores sobre pontos de carbono [30, 31].
Estrutura química e composição da superfície de HA-Gd 2 O 3 NPs
Grupos funcionais de superfície e composição de HA-Gd 2 O 3 NPs foram investigados usando espectro infravermelho com transformada de Fourier e espectroscopia de fotoelétrons de raios-X. Como mostrado na Fig. 2a, o espectro XPS mostrou quatro picos típicos em 284,0, 400,0, 530,6 e 1188,5 eV, indicando que HA-Gd 2 O 3 Os NPs eram compostos principalmente de elementos de gadolínio, carbono, oxigênio e hidrogênio. O espectro de alta resolução de Gd 3 d (Fig. 2b) revelou a presença de dois picos fortes em 1187,5 eV e 1221 eV, correspondendo a uma divisão spin-órbita de 32 eV, correspondendo respectivamente a 3 d 5/2 e 3 d 3/2 níveis de energia de D'us. Estas observações estavam de acordo com os relatórios anteriores do HA-Gd 2 O 3 NPs. O O (1 s ) o espectro mostrado na Fig. 2c foi dominado por um pico principal posicionado em 531,4 eV, que correspondeu à ligação entre O 2− e Gd 3+ . A espectroscopia FITR foi conduzida para HA e HA-Gd 2 O 3 Amostras NP (Fig. 2d). Para as amostras nuas, como mostrado na Fig. 2a, as bandas de absorção características de v como O – C – O em 1580 e 1380 cm −1 revelou a presença de um grupo carbonato. Os picos amplos em 3340 e 2900 cm −1 foram atribuídos às vibrações de alongamento O – H e C – H, respectivamente, que correspondiam à água adsorvida pela superfície. Para HA-Gd 2 O 3 NPs, as vibrações de alongamento do COO - em 1580 e 1380 cm −1 foram potencializados, indicando a introdução do grupo carboxílico do ácido hialurônico. Estes resultados revelaram que os grupos funcionais de HA-Gd 2 O 3 Os NPs continham principalmente certos grupos numerosos de carbonila, carboxilato e hidroxila. A presença desses grupos funcionais localizados na superfície dotada de HA-Gd 2 O 3 NPs com excelente dispersibilidade em água. É importante ressaltar que o íon Gd embutido na superfície dos NPs pode ser útil para imagens de RM e radiossensibilização, o que evitou drasticamente o vazamento do íon Gd para os ambientes circundantes.
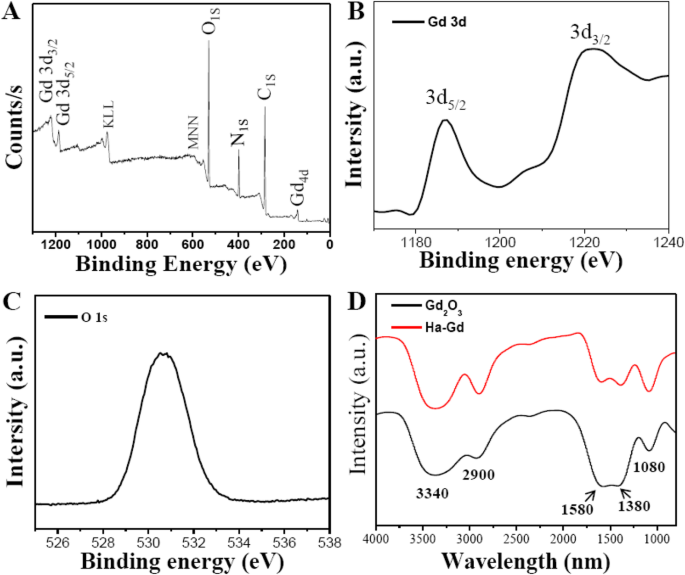
A estrutura química e composição do HA-Gd 2 O 3 NPs. a O espectro XPS de varredura completa de HA-Gd 2 O 3 NPs. b Gd 3d espectro. c O 1S espectro. d O espectro FTIR de HA-Gd 2 O 3 NPs
Biocompatibilidade de HA-Gd 2 O 3 NPs
Biocompatibilidade de HA-Gd 2 O 3 NPs, como potenciais agentes biomédicos, são essenciais para sua aplicação biomédica. Em primeiro lugar, a citotoxicidade inerente de HA-Gd 2 O 3 NPs foram avaliados em células HepG2 e VSMC usando o ensaio CCK-8. Conforme mostrado na Fig. 3a e S. Fig. 1, o HA-Gd 2 O 3 NPs não exibiram citotoxicidade óbvia até 3 dias. Mesmo a uma concentração de 200 μg / mL após um tempo de exposição de 24 horas, a viabilidade celular era de aproximadamente 90%. Em segundo lugar, a hemocompatibilidade de HA-Gd 2 O 3 NPs in vivo foram estimados usando um ensaio de hemólise. Conforme mostrado na Fig. 3b, observamos hemólise de hemácias na água (controle positivo). Em contraste, nenhuma hemólise óbvia foi observada após HA-Gd 2 O 3 Incubação de NP em diferentes concentrações de 0 a 200 μg / mL por 2 h, que foi semelhante aos resultados para solução de PBS (controle negativo). Em comparação com o controle negativo, a porcentagem de hemólise em diferentes concentrações de HA-Gd 2 O 3 Os NPs foram ligeiramente avaliados com base na absorvância do sobrenadante a 541 nm. Os resultados mostraram que as porcentagens de hemólise de HA-Gd 2 O 3 Os NPs foram todos inferiores a 3% na concentração estudada, verificando sua hemocompatibilidade favorável. A fim de examinar a toxicidade potencial, HA-Gd 2 O 3 NPs foram injetados por via intravenosa em camundongos Balb / c (como visto em S. Fig. 2). Após 1 semana, esses camundongos foram executados e a bexiga, rim e baço foram colhidos para análise de seção patológica. Como mostrado na Fig. 2 S., o resultado das secções patológicas mostrou que não houve lesão observável ou resposta inflamatória nos órgãos de HA-Gd 2 O 3 Camundongos tratados com NP. Estes resultados indicaram claramente que o HA-Gd 2 sintetizado O 3 NPs tinham citocompatibilidade favorável e boa hemocompatibilidade.
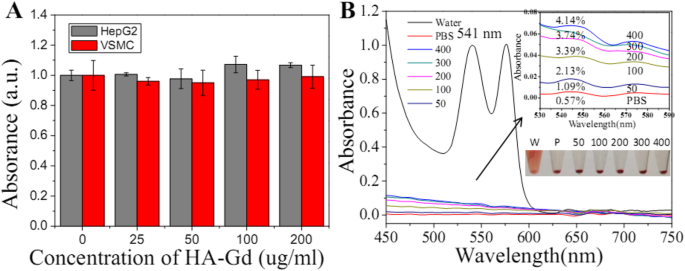
a Efeito de HA-Gd 2 O 3 NPs sobre a viabilidade de células HepG2 e VSMC usando o ensaio CCK-8. b Atividade hemolítica do HA-Gd 2 O 3 NPs em diferentes concentrações (50, 100, 200, 300 e 400 μg / mL). PBS e água foram usados como controle negativo e positivo, respectivamente
Estudo fantasma de ressonância magnética
O longitudinal ( T 1 ) tempos de relaxamento de HA-Gd 2 O 3 NPs foram investigados in vitro junto com o contraste comercial Magnevist (Gd-DTPA) como um controle usando solução salina tamponada com fosfato (pH =7,4, 0,2 M). Com o aumento das concentrações de Gd, a intensidade do sinal de T 1 imagens fantasmas de peso aumentaram claramente, indicando que todas as amostras podem gerar aumento de contraste de ressonância magnética em T 1 sequências ponderadas (Fig. 4a). Além disso, os gráficos da intensidade do sinal versus tempo de inversão deram T 1 -tempos de relaxamento de cada agente de contraste em concentrações específicas. Conforme mostrado na Fig. 4b, o r 1 valor de HA-Gd 2 O 3 NPs foram medidos em 6,0 mM −1 S −1 , que foi significativamente maior do que Magnevist (3,86 mM −1 S −1 ) nas mesmas condições. O r aprimorado 1 pode ser atribuído ao raio hidrodinâmico muito maior e área de superfície de HA-Gd 2 O 3 NPs; portanto, mais átomos de Gd dopados na rede de NPs tornaram-se acessíveis às moléculas de água, encurtando o relaxamento longitudinal e aumentando o r 1 valor.
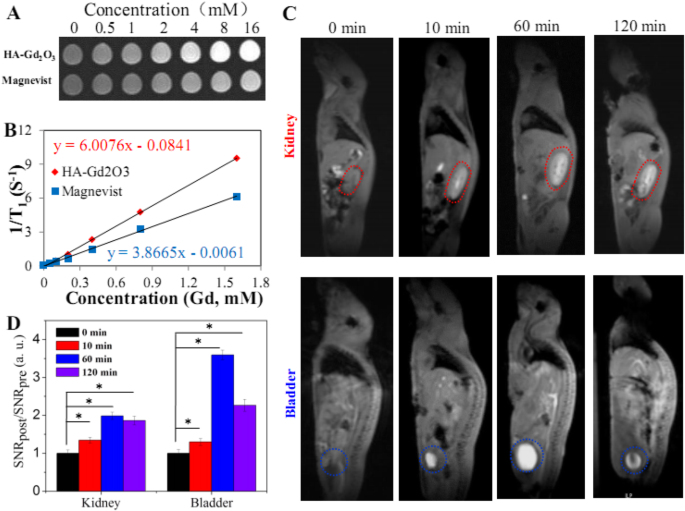
a T 1 imagens fantasmas do HA-Gd 2 O 3 NPs com diferentes concentrações de íons Gd totais. b Os gráficos correspondentes de 1 / T 1 contra as concentrações de íons Gd totais. c In vivo T 1 Imagem de RM e análise de camundongos após injeção intravenosa de HA-Gd 2 O 3 NPs como agentes de contraste. d Quantificação das mudanças de sinal (relação SNR) na bexiga e nos rins em diferentes pontos de tempo após a administração ( n =3). * p <0,05
Imagens de RM In Vivo
A fim de determinar as aplicações potenciais in vivo, o desempenho da imagem de RM e o destino de circulação de HA-Gd 2 O 3 NPs (10 mg / kg) foram investigados usando um scanner de ressonância magnética com camundongos BALB / c normais como modelo. Em comparação com as imagens pré-injeção (Fig. 4c), as regiões mais brilhantes do rim e da bexiga, conforme indicado pelos círculos tracejados, foram claramente observadas 10 min após a injeção, demonstrando que HA-Gd 2 O 3 NPs podem ser usados como CAs para melhorar T 1 relaxamento nestes órgãos principais in vivo. É importante ressaltar que o aumento de contraste de HA-Gd 2 O 3 Os NPs foram mantidos 60 min após a injeção, que foi muito mais longo do que as moléculas pequenas do complexo de Gd (meia-vida de cerca de vários minutos em pequenos animais) [27], indicando que HA-Gd 2 O 3 NPs possuíam tempos de retenção mais longos in vivo do que o contraste comercial. Para analisar o efeito de contraste de MR quantitativamente, calculamos a relação sinal-ruído (SNR) analisando com precisão as regiões de interesse das imagens de MRI e calculamos os valores de SNR pós / SNR pré para representar o aumento relativo do sinal (RSE) (Fig. 4d). Os valores RSE de HA-Gd 2 O 3 NPs no rim foram 1,35, 1,99 e 1,86. Da mesma forma, os valores RSE de HA-Gd 2 O 3 NPs na bexiga foram maiores do que nos rins (1,29, 3,59 e 2,26). HA-Gd 2 O 3 NPs com tamanho grande (mais de 100 nm) exibiram longos tempos de circulação, então podem ser eliminados com a via biliar-intestinal de acordo com resultados anteriores [32]. Além disso, o tempo de circulação prolongado in vivo pode ter aumentado o direcionamento passivo em tumores, aumentando o efeito EPR.
Imagem do tumor
HA-Gd 2 O 3 NPs com excelente desempenho de imagens de ressonância magnética e longo tempo de circulação fornecem uma grande oportunidade para imagens de tumores por meio de um efeito EPR. Assim, estabelecemos modelos de tumor hepático subcutâneo para investigar se os carcinomas hepatocelulares (HCCs) podem ser detectados por HA-Gd 2 O 3 RNM aprimorada com NP. Após a injeção intravenosa de HA-Gd 2 O 3 NPs, observamos que a região do tumor subcutâneo torna-se mais brilhante do que o tecido circundante, conforme visto por varredura coronal e transversal (Fig. 5a). O RES do tumor subcutâneo atingiu dramaticamente 1,54 e 1,83 com varredura transversal e coronal, respectivamente, indicando o acúmulo efetivo de HA-Gd 2 O 3 NPs na região do tumor por meio do efeito EPR. Estas descobertas demonstram que HA-Gd 2 O 3 NPs são altamente sensíveis para visualização de tumores por ressonância magnética. Muitos estudos mostraram que o longo tempo de circulação pode promover a eficiência do direcionamento passivo através da vasculatura com vazamento de tumores sólidos [33].
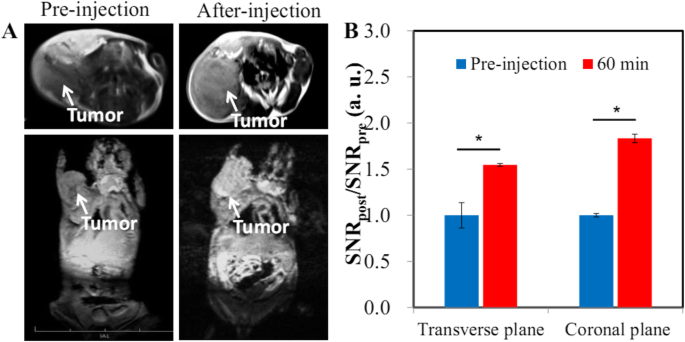
T 1 de ressonância magnética ponderada ( a ) e correspondente análise quantificacional ( b ) de tumores de xenoenxerto de câncer de fígado de camundongo Heps após injeção intravenosa de HA-Gd 2 O 3 NPs
Melhoria da radiossensibilização de HA-Gd 2 O 3 NPs
O excelente desempenho do HA-Gd 2 O 3 NPs como um T 1 O agente de contraste nos levou a determinar sua localização na radiossensibilização de tumores com precisão. Em primeiro lugar, se o aumento da dose ocorreu com este tratamento de combinação foi explorado usando um ensaio CCK-8. Conforme representado na Fig. 6a, único HA-Gd 2 O 3 NPs (concentração de 0–200 μg / mL) não influenciaram significativamente a viabilidade de HepG-2, mas a irradiação de raios-X (intervalo de 0–9 Gy) diminuiu a viabilidade das células HepG-2 para menos de 70% a 9 Gy. É importante ressaltar que uma combinação de irradiação de raios-X com HA-Gd 2 O 3 NPs diminuíram drasticamente a viabilidade das células HepG-2 para menos de 50%, particularmente a uma concentração de 200 μg / mL a 9 Gy. Em seguida, um ensaio clonogênico foi conduzido para avaliar a viabilidade celular em células HepG-2 após uma combinação de irradiação de raios-X e HA-Gd 2 O 3 NPs. Conforme mostrado na Fig. 6b, único HA-Gd 2 O 3 NPs não tiveram influência dramática na formação de colônias de células HepG-2, mas a irradiação de raios-X diminuiu a formação de colônias de células HepG-2 para 46,7%. No entanto, o tratamento com irradiação de raios-X e HA-Gd 2 O 3 NPs inibiram notavelmente a viabilidade de formação de colônias celulares em 29,8%. As imagens correspondentes verificaram ainda a radiossensibilização de HA-Gd 2 O 3 NPs contra células HepG-2.
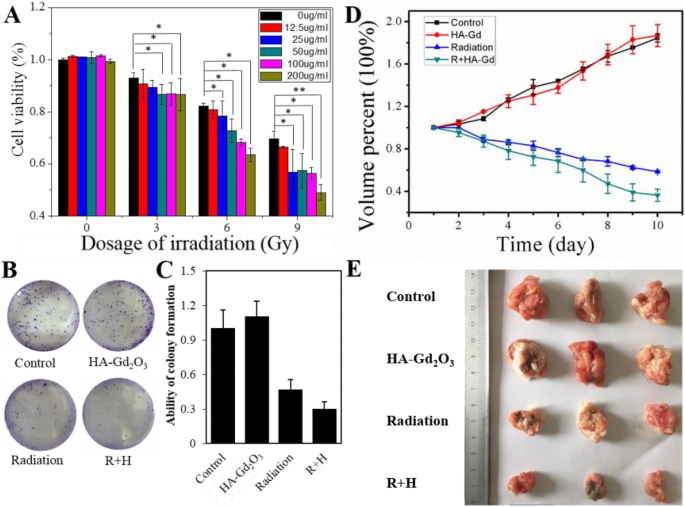
O efeito de radiossensibilização de HA-Gd 2 O 3 NPs in vitro. a O efeito sinérgico de HA-Gd 2 O 3 NPs (0 μg / mL, 12,5 μg / mL, 25 μg / mL, 50 μg / mL, 100 μg / mL e 200 μg / mL) e radiação de raios-X (0 Gy, 3 Gy, 6 Gy e 9 Gy) sobre a viabilidade de células HepG2 usando o ensaio CCK-8. * p <0,05, ** p <0,01, a diferença foi estatisticamente significativa. b Os ensaios de sobrevivência de colônias de células HepG2 tratadas com HA-Gd 2 O 3 NPs e radiação de raios-X e c a correspondente análise quantitativa das habilidades de clonegênese. d Curvas de crescimento do volume tumoral de diferentes grupos de camundongos após diferentes tratamentos. Grupos: a controle, b radiação, c HA-Gd 2 O 3 NPs e d radiação + HA-Gd 2 O 3 NPs. e Fotos de tumores coletadas de diferentes grupos de camundongos no final do tratamento
A eficácia da radioterapia in vitro nos encorajou a aplicar HA-Gd 2 O 3 NPs combinados com a irradiação para controlar o crescimento do tumor em camundongos com tumor. Os volumes de tumores no controle e único HA-Gd 2 O 3 Os tratamentos NP cresceram rapidamente e ambos aumentaram 180%. Comparado com os tratamentos de irradiação única 58%, HA-Gd 2 O 3 NPs combinados com radiação mostraram inibição tumoral eficiente em 38% após 10 dias de irradiação (Fig. 6d). O tumor foi fotografado e os volumes médios do tumor em cada grupo mostraram que o volume médio do tumor no grupo (a) foi o mais alto, enquanto que no grupo (d) foi o mais baixo entre todos os grupos (Fig. 6e). Estes resultados revelam que o HA-Gd 2 preparado O 3 NPs são promissores para a inibição do crescimento de tumores sob irradiação de raios-X.
O ensaio de citometria de fluxo e o ensaio de coloração vivo / morto foram conduzidos para compreender melhor o mecanismo de radiossensibilização no tratamento combinado de HA-Gd 2 O 3 NPs e radiação de raios-X. Como mostrado na Fig. 7a, fluorescência verde intensa sem vermelho foi observada em células HepG-2 tratadas com HA-Gd único 2 O 3 NPs, que verificaram alta viabilidade celular. Uma pequena quantidade de fluorescência vermelha foi observada após os tratamentos de radiação de raios-X, indicando um baixo nível de apoptose celular. No entanto, forte fluorescência vermelha foi observada após o tratamento de combinação de HA-Gd 2 O 3 NPs (200 μg / mL) e radiação, demonstrando que HA-Gd 2 O 3 NPs podem aumentar dramaticamente a apoptose celular induzida por irradiação de raios-X. O mecanismo de radiossensibilização de HA-Gd 2 O 3 NPs foram investigados posteriormente usando citometria de fluxo. Conforme representado na Fig. 7b, radiação única e HA-Gd 2 O 3 NPs induziram 27,55% e 19,12% da parada da fase G2 / M, respectivamente. No entanto, o tratamento de combinação de HA-Gd 2 O 3 NPs e radiação aumentaram notavelmente a parada da fase G2 / M, variando de 30,89 a 33,27% de uma maneira dependente da dose. Enquanto isso, o tratamento de combinação induziu morte celular apoptótica de 10,63 a 22,67%, conforme refletido pelas proporções sub-G1 quando o único HA-Gd 2 O 3 NPs e radiação induziram 3,02% e 13,87%. Para investigar mais a fundo o possível mecanismo de morte celular, um método de Anexina V-EGFP / PI foi conduzido por citometria de fluxo. O sinal de emissão da anexina V-EGFP foi traçado no x -eixo, enquanto o sinal de emissão de PI foi plotado no y -eixo (Fig. 8). As quantidades de células de necrose, células de apoptose precoce, células de apoptose tardia e células vivas foram determinadas pela porcentagem de anexina V - / PI + (Q3), Annexin V + / PI + (Q2), e Annexin V - / PI - (Q4), respectivamente. A porcentagem apoptótica das células no grupo de controle e único HA-Gd 2 O 3 O grupo NP (100 μg / mL) foi inferior a 5%, resultando em uma influência sutil. Em comparação com os grupos de tratamento com radiação única (8,8%), a taxa de apoptose da combinação de HA-Gd 2 O 3 NPs e radiação aumentaram com o aumento da concentração variando de 50 a 200 μg / mL. Especialmente, a taxa de apoptose precoce das células obviamente aumentou para 33,2%, e a apoptose precoce e tardia atingiu 44,3% quando a concentração é de 200 μg / mL. Geralmente, a combinação de HA-Gd 2 O 3 NPs e irradiação de raios-X tiveram um efeito sinérgico na formação de colônias celulares, na viabilidade celular de uma maneira dependente da dose e no efeito de intensificação da radiossensibilização. Com base nesses resultados, HA-Gd 2 O 3 NPs podem ser uma alternativa eficiente para aumentar a radiossensibilização para radioterapia.
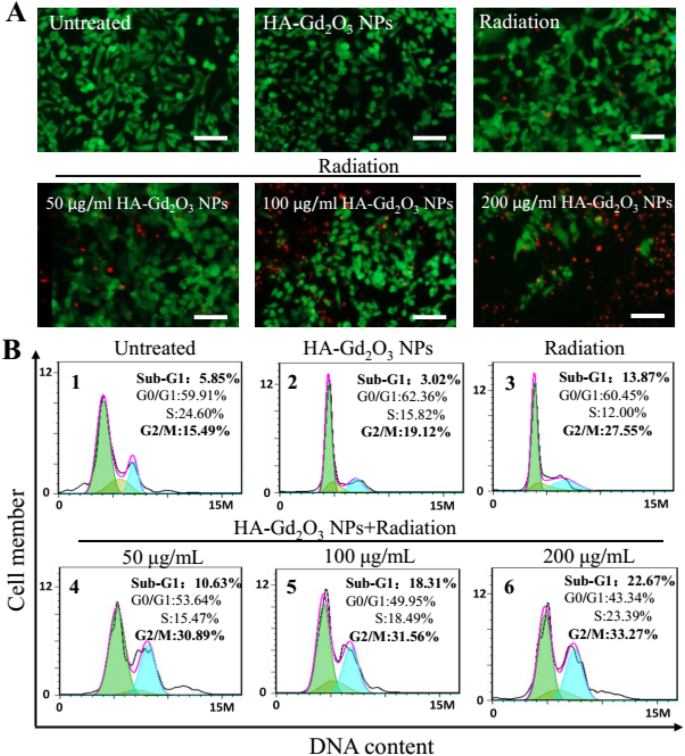
Aumento da dose de radiação de HA-Gd 2 O 3 NPs. a Coloração viva-morta de células HepG2. Verde (coloração com diacetato de fluoresceína) =células vivas, vermelho (coloração com iodeto de propídio) =células mortas. Barras de escala =200 mm. b A distribuição do ciclo celular após diferentes tratamentos foi analisada pela quantificação do conteúdo de DNA usando ensaio de citometria de fluxo
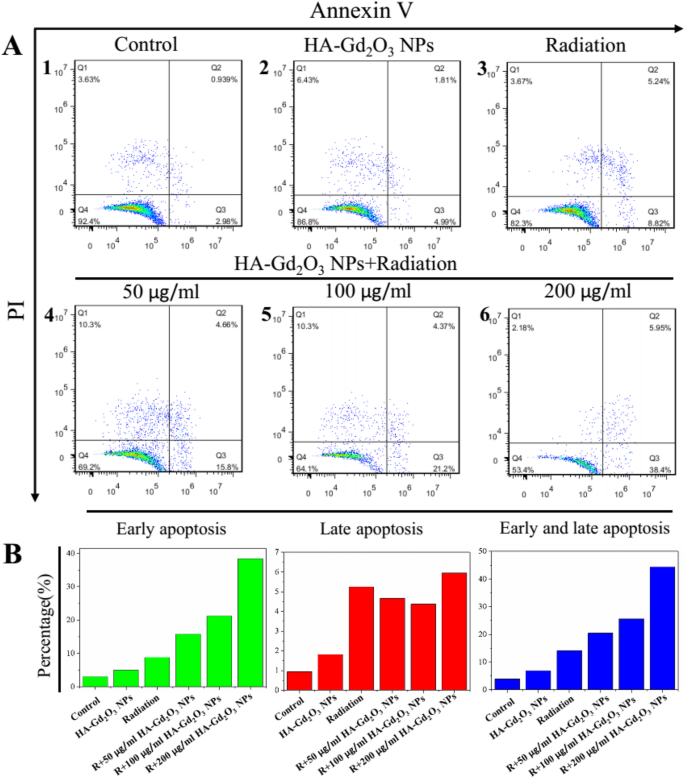
A análise de apoptose de HA-Gd 2 O 3 NPs. a Os níveis de apoptose de células HepG-2 em 24 horas após o tratamento de radiação de raios-X. b A análise quantitativa correspondente
Conclusões
Em conclusão, desenvolvemos um HA-Gd bifuncional 2 O 3 NPs para imagens de RM eficazes e radiossensibilização de tumores em um processo hidrotérmico de um único recipiente. Após o revestimento com HA, o HA-Gd como sintetizado 2 O 3 NPs exibiram dispersibilidade favorável em água, excelente biocompatibilidade. O HA-Gd 2 resultante O 3 NPs encapsulando os átomos de Gd não apenas exibiram efetivamente alta relaxividade longitudinal ( r 1 ) para ressonância magnética como um T 1 agente de contraste, mas também aumentou a radiossensibilidade de tumores induzindo a apoptose celular e bloqueando o ciclo celular como um radiossensibilizador. Assim, o romance HA-Gd 2 O 3 NPs mostram um potencial promissor para o diagnóstico de tumor e radioterapia.
Materiais e métodos
Materiais
O diacetato de fluoresceína (FDA) e o iodeto de propídio (PI) foram adquiridos da Sigma (New York, NY, EUA). GdCl 3 · 6H 2 O, etilenoglicol (99%) foram adquiridos da Hengrui Pharmaceutical Co., Ltd. (Lianyungang, Jiangsu, República Popular da China). O Cell Counting Kit-8 (CCK-8) foi comprado da Dojindo (Kumamoto, Japão). NaH 2 PO 4 , Na 2 HPO 4 , e H 2 SO 4 foram obtidos do Guangfu Fine Chemical Research Institute (Nankai, Tianjin, República Popular da China). Soro fetal bovino e meio essencial mínimo de Dulbecco (DMEM) foram adquiridos da Invitrogen China Limited (Xangai, República Popular da China). Todos os produtos químicos eram de grau analítico e foram utilizados sem purificação adicional.
Síntese de HA-Gd 2 O 3 NPs
O HA-Gd 2 O 3 NPs foram preparados usando abordagem hidrotérmica em um único recipiente como a seguir:Primeiro, 0,1 g de HA foi dissolvido em 20 mL de água sob agitação vigorosa à temperatura ambiente durante a noite. Posteriormente, 0,1 g de GdCl 3 · 6H 2 O e 0,5 mL de NaOH (1 M) foram adicionados, respectivamente. Em seguida, a mistura foi agitada por mais 5 min para formar uma solução transparente homogênea e transferida para uma autoclave de 50 mL, selada e tratada hidrotermicamente a 120 ° C por 6 h. Depois de ser resfriado à temperatura ambiente naturalmente, a suspensão transparente foi filtrada com uma membrana de 0,22 μm para remover qualquer aglomeração de grande porte. A solução preparada foi então dialisada contra água por 3 dias em uma bolsa de diálise com peso molecular de corte de 14 kDa. A solução de diálise foi recolhida e liofilizada usando um liofilizador a vácuo. O HA-Gd 2 O 3 Assim, os pós NP foram obtidos e armazenados para posterior caracterização.
Instrumentação e caracterizações
As morfologias do HA-Gd 2 O 3 NPs foram examinados por microscopia eletrônica de transmissão de alta resolução em um microscópio JEM-2100 (JEOL, Tóquio, Japão) sob uma tensão de aceleração de 200 kV. A composição elementar de HA-Gd 2 O 3 Os NPs foram determinados por medidas de XPS em um espectrômetro de fotoelétrons MK II, usando Al-Ka (1486,6 eV) como fonte de raios-X e espectrômetro de infravermelho com transformada de Fourier (FTIR) (Nicolet Nexus 470, GMI, Ramsey, MN, EUA). A estrutura cristalina do HA-Gd 2 O 3 NPs foram caracterizados por meio de padrões de difração de raios-X (XRD) em um difratômetro Rigaku-D / MAX2500 (Rigaku, Japão) equipado com Cu Kα ( λ =0,15405 nm) radiação a uma velocidade de varredura de 4 ° / min no intervalo de 5 a 80 °.
Ensaio de viabilidade celular
A influência de HA-Gd 2 O 3 Os NPs sobre a viabilidade celular foram estudados através do ensaio do kit de contagem de células CCK-8 (ensaio de CCK-8). HepG2 (hepatocarcinoma humano, número ATCC:HB-8065) e VSMCs (células de músculo liso vascular) foram semeados em uma placa de 96 poços a uma densidade de 3 × 10 3 células / poço e cultivadas a 37 ° C em 5% de CO 2 incubadora por 24 h, em seguida, usando DMEM contendo diferentes concentrações de HA-Gd 2 O 3 NPs (0 μg / mL, 25 μg / mL, 50 μg / mL, 100 μg / mL e 200 μg / mL) substituindo o meio de crescimento. Após a incubação por mais 4 h, adicionando 10 μL de solução de CCK-8 a cada poço, as células foram incubadas por 4 h em um local escuro. A absorvância foi medida a 490 nm usando o leitor de microplacas Synergy HT Multi-Mode (Bio Tek, Winooski, VT, EUA). Células não tratadas (em DMEM) foram utilizadas como controle, e a viabilidade celular relativa (SD médio, n =5) foi expresso como Abssample / Abscontrol × 100%.
Ensaio de hemólise
Resumidamente, 19-21 g, idades de camundongos BALB / c fêmeas de 6 semanas foram gentilmente preparados pelas Regras de Manejo Animal do Ministério da Saúde da República Popular da China. Três mililitros de sangue que se estabilizou com heparina sódica foram obtidos removendo os globos oculares. Em seguida, foi centrifugado para retirada do sobrenadante com 1200 rpm, 15 min conforme a literatura. Em seguida, lavar a sedimentação com PBS por cinco vezes para obter os glóbulos vermelhos de camundongo (MRBCs), em seguida, tomar cerca de 3 mL de sangue removendo o globo ocular, estabilizado com heparina sódica, centrifugado (1, 200 rpm, 15 min) para remoção do sobrenadante conforme a literatura [27], lavou-se cinco vezes com PBS para obtenção de hemácias de camundongo (MRBCs). Diluindo dez vezes com PBS, 0,1 mL de MRBCs foram transferidos para tubos de 1,5 mL pré-cheios com 0,9 mL de PBS contendo diferentes concentrações de partículas (50–200 μg / mL) de HA-Gd 2 O 3 NPs, 0,9 mL de água (como controle positivo) e 0,9 mL de PBS (como controle negativo), respectivamente. A mistura foi incubada durante 2 h à temperatura ambiente após uma agitação suave e, em seguida, centrifugada a 12.000 rpm durante 1 min. Finalmente, as fotografias de todas as amostras foram tiradas e a absorbância do sobrenadante (hemoglobina) foi medida por um espectrofotômetro UV-2450 UV-Vis. As porcentagens de hemólise de diferentes amostras foram calculadas dividindo a diferença na absorbância entre a amostra, o controle positivo e o controle negativo em 541 nm.
Estudo fantasma de MR in vitro e in vivo
Imagens de RM in vitro e in vivo foram adquiridas em scanner de RM 3 Tesla (Magnetom Trio Tim, Siemens, Alemanha). Para estudar o T 1 imagens fantasmas in vitro, a solução de HA-Gd 2 O 3 NPs with different concentrations ranging from 0 to 16 mM was added to a 96-well culture plate, using the Magnevist (commercial MR contrast agent, Gd-DTPA) as control. For MR imaging in vivo, we chose the normal BALB/c mice as the model (n =4). Animal experiments were strictly conformed to the Animal Management Rules of the Ministry of Health of the People’s Republic of China. Ten milligrams per kilogram of HA-Gd2 O 3 NPs filtering through sterilized membrane filters (pore size 0.22 μm) were intravenously injected into the animals, then immediately investigated with a MRI scanner. These samples for MR imaging in vitro and animals in vivo were imaged with the following parameters:TR/TE =300/10 ms, 256 × 256 matrices, slices =5, thickness =2 mm, averages =2, FOV =80 × 80.
Radiosensitization Effect In Vitro
CCK-8 assay was used to evaluate radiosensitizing activity of HA-Gd2 O 3 NPs in vitro. Cells were seeded in five 96-well plates at a density of 3 × 10 3 cells/well, and each plate was treated at the same condition:cultured at 37 °C in 5% CO2 incubator for 24 h, then using DMEM containing different concentrations of HA-Gd2 O 3 NPs (0 μg/mL, 12.5 μg/mL, 25 μg/mL, 50 μg/mL, 100 μg/mL, and 200 μg/mL) replacing the growth medium. After incubation for 4 h, five plates were irradiated at different X-ray doses (0 Gy, 3 Gy, 6 Gy, and 9 Gy), 300 cGy/min, respectively. After radiation, all the plates were incubated for 4 h, then measuring the absorbance under the same parameters.
Clonogenic survival assay was also conducted to study the radiosensitization effect in vitro. HepG2 cells were seeded in six-well plates at 4.0 × 10 4 cells/well and allowed to grow for 16 h. The cells were incubated with HA-Gd2 O 3 NPs diluted in cell culture medium for 6 h. The cells were then irradiated at 6 Gy using a clinical linear accelerator (Oncor, Siemens, Germany) with 6 MeV irradiation using a 10 cm × 10 cm radiation field at a source-to-skin distance (SSD) of 100 cm to cover the entire cells. Then, these irradiated cells were allowed to grow for 14 days, fixed with 4% paraformaldehyde at room temperature for 40 min, stained with a 1% crystal violet after washing the cells.
Live-Dead Staining Assay and Flow Cytometry
To study the radiosensitization effect of HA-Gd2 O 3 NPs, HepG2 cells were seeded in six-well plates at a density of 4.0 × 10 4 cells/well and allowed to grow for 12 h and set six groups (control, HA-Gd2 O 3 NPs, radiation, radiation + 50 μg/mL HA-Gd2 O 3 NPs, radiation + 100 μg/mL HA-Gd2 O 3 NPs and radiation + 200 μg/mL HA-Gd2 O 3 NPs). When cells were grown to 80% in plates, the first group had no treatment, the second group was incubated with 100 μg/mL HA-Gd2 O 3 NPs for 24 h, the third group was just irradiated, and the fourth group to the sixth group were irradiated and incubated with different concentrations of HA-Gd2 O 3 NPs (50, 100, and 200 μg/mL) for 24 h, respectively. After that, FDA and PI working buffer were added for cell staining. The fluorescence of stained cells was observed under a fluorescence microscope (×20), and live cells showed green color and dead ones exhibited red color. Furthermore, cells by different treatments were washed three times with PBS, digested, collected, and centrifuged at a speed of 2000 rpm for 5 min, then fixed with 70% ethanol at − 20 °C overnight followed by PI staining. DNA fragmentation was quantified by the fluorescence intensity of PI on a flow cytometer (BD, Accuri, C6BD, Accuri, C6), analyzed by software (FLOWJO 7. 6. 2) to make clear the cell cycle distribution.
Radiosensitization Effect In Vivo
Female BALB/c mice with body weights of 19–21 g and ages of 6 weeks were obtained from the Yangzhou University Laboratory Animal Center under the standard conditions. Animal experiments were compliant with the Animal Management Rules of the Ministry of Health of the People’s Republic of China. A subcutaneous tumor model was established as the following procedures:First, 1 × 10 6 HepS cells were inoculated into mice intraperitoneal, and the ascites were collected after 5 days. Then, these ascites were injected into subcutaneous. When the tumor sizes reached approximately 100 mm 3 , subcutaneous tumors models were established and applied to the following experiments.
Eight mice bearing subcutaneous tumors per group were treated with radiation at 3 Gy per fraction to a total dose of 9 Gy within 7 days. The radiotherapy was conducted after 3 h intravenous injection of HA-Gd2 O 3 NPs (10 mg/Kg), on a Siemens Primus clinical linear accelerator (6 MeV) using a self-made device to cover the entire tumor. These mice were anesthetized by 1% pentobarbital (50 mg/kg) to assure immobility during irradiation. The volume was measured and recorded every day, determined from caliper measurement, and calculated by the formulae:V =0.5 × a × b 2 , onde V (mm 3 ) is the volume of the tumor, and a (mm) and b (mm) are the tumor length and tumor width, respectively. Relative tumor volumes were normalized to their initial sizes. Each group was conducted on eight mice, wherein statistical analysis was performed using Student’s two-tailed t test (*p <0,05, ** p <0.001).
Disponibilidade de dados e materiais
The data sets supporting the results of this article are included within the article.
Nanomateriais
- Nanopartículas de ouro para sensores quimio
- Nanodiamonds para sensores magnéticos
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Preparação e propriedades magnéticas de nanopartículas de espinélio FeMn2O4 dopadas com cobalto
- Magnetismo de Percolação em Nanopartículas Ferroelétricas
- Efeitos de interação na montagem de nanopartículas magnéticas
- Estabilidade aprimorada de nanopartículas magnéticas de ouro com poli (ácido 4-estirenossulfônico-ácido co-maleico):propriedades ópticas sob medida para detecção de proteínas
- Poliglicerol hiper-ramificado modificado como dispersante para controle de tamanho e estabilização de nanopartículas de ouro em hidrocarbonetos
- Síntese e desempenho in vitro de nanopartículas de ferro-platina revestidas com polipirrole para terapia fototérmica e imagem fotoacústica
- Comparação entre o ácido fólico e a funcionalização baseada no peptídeo gH625 de nanopartículas magnéticas Fe3O4 para internalização celular aprimorada



