Efeito dos surfactantes nas microestruturas de nanoflores florescentes de SnO2 hierárquico e suas propriedades de detecção de gás
Resumo
SnO hierárquico 2 nanoflores florescentes foram fabricados com sucesso por meio de um método hidrotérmico simples, mas fácil, com a ajuda de diferentes surfactantes. Aqui, nos concentramos em explorar os efeitos de promoção de surfactantes na automontagem de SnO 2D 2 nanofolhas em 3D SnO 2 estruturas semelhantes a flores, bem como seus desempenhos de detecção de gás. O SnO polporoso semelhante a uma flor 2 sensor exibe excelente desempenho de detecção de gás para etanol e H 2 Gás S devido à alta porosidade quando a polivinilpirrolidona é adicionada à solução precursora como um surfactante. Os tempos de resposta / recuperação foram de cerca de 5 s / 8 s para 100 ppm de etanol e 4 s / 20 s para 100 ppm H 2 S, respectivamente. Especialmente, o valor máximo de resposta de H 2 S é estimado em 368 a 180 ° C, o que é uma ou duas ordens de magnitude maior do que o de outros gases de teste neste estudo. Isso indica que o sensor fabricado com a ajuda de polivinilpirrolidona tem boa seletividade para H 2 S.
Histórico
Os sensores de gás têm atraído muita atenção devido às suas aplicações potenciais na detecção de gases tóxicos, nocivos, inflamáveis e explosivos [1]. Atualmente, os semicondutores de óxido metálico ocupam uma posição importante em vários sensores devido ao seu processo de preparação simples, menor custo e maior sensibilidade aos gases-alvo [2,3,4]. Dióxido de estanho (SnO 2 ), um material multifuncional do tipo n com um gap direto de 3,6 eV [5], tem sido amplamente utilizado em estudos fundamentais e aplicações práticas, como sensores de gás [6], catálise [7] e dispositivos optoeletrônicos [8 ] Especialmente, SnO 2 tem sido considerado como o material de detecção de maior potencial devido à sua não estequiometria natural [9], alta sensibilidade, resposta rápida / velocidade de recuperação e alta estabilidade química [10].
É bem conhecido que o mecanismo de detecção de gás dos óxidos metálicos está relacionado aos processos de adsorção e dessorção do gás alvo na superfície do sensor, ocasionando uma mudança na condutividade elétrica [11]. Esses processos dependem fortemente do tamanho, morfologia e dimensão, bem como da estrutura cristalina das amostras [12]. Existem duas maneiras principais de melhorar efetivamente o desempenho de detecção do SnO 2 [13]. Um é sintetizar materiais compostos com base em SnO 2 , como a fabricação de junções p-n, decoração de superfície ou dopagem [14]. A outra é preparar vários SnO puros 2 materiais incluindo nanotubos [15], nanobastões [16], nanoesferas [17], estruturas ocas [14] e nanoflores [18], que têm nanoestruturas únicas, alta área de superfície específica e forte capacidade de captura de elétrons [19]. Recentemente, SnO hierárquico tridimensional (3D) 2 nanoestruturas têm chamado muita atenção por causa de seu melhor desempenho de detecção de gás causado por grande área de superfície específica e rápida difusão gasosa em comparação com nanoestruturas 1D e 2D [20]. Várias técnicas foram usadas para fabricar nanoestruturas 3D de SnO 2 [21], como deposição de vapor químico [22], método sintético solvotérmico [23], método de molde [24], método sol-gel [25] e rota hidrotérmica [26]. Dentre elas, rotas solvotérmicas e hidrotérmicas com baixo custo [27], alto rendimento e manipulação simples têm se mostrado os métodos promissores para sintetizar SnO hierárquico 3D 2 nanoestruturas. Por exemplo, Dong et al. SnO oco preparado 2 nanoesferas com diâmetro variando de 200 a 400 nm usando um método sintético solvotérmico [28]. Li et al. fabricou um novo SnO semelhante a um floco de neve 2 arquitetura hierárquica com excelentes propriedades de detecção de gás por meio de um método hidrotérmico fácil [29]. Além disso, Chen et al. sintetizado com sucesso SnO hierárquico semelhante a uma flor 2 florescendo nanoflores construídas por automontagem de muitas nanofolhas de formato regular através do método hidrotérmico convencional [30].
A aplicação prática do SnO 2 os sensores ainda são limitados até certo ponto devido à temperatura de trabalho relativamente mais alta e menor seletividade para testar os gases [31]. A fim de melhorar as propriedades de detecção de gás, os pesquisadores prestaram atenção à síntese controlável de SnO tipo flor 3D 2 nanoestruturas com efeitos surfactantes [32], mas um desafio significativo é colocado devido à variedade de surfactantes.
No presente estudo, relatamos uma otimização bem controlada do SnO hierárquico 3D 2 nanoflores baseadas na automontagem de nanofolhas finas com o auxílio de diferentes tensoativos sob condição hidrotérmica. Nosso estudo de detecção de gás sistematicamente comparativo entre sensores fabricados enfoca o efeito de promoção de surfactantes no comportamento do sensor. Os resultados mostram que os surfactantes anfifílicos não iônicos, como PVP e Triton X-100, podem ser candidatos potenciais para otimizar a morfologia de nanoflores 3D com alta porosidade e grande área superficial específica. Particularmente, o sensor baseado em PVP exibe alta resposta, tempo de resposta rápido e boa seletividade para H 2 S a uma temperatura relativamente mais baixa. Além disso, um possível mecanismo de crescimento bem controlado de SnO 2 nanoestruturas é proposto.
Métodos / Experimental
Citrato trissódico di-hidratado e cloreto de estanho di-hidratado da Sinopharm Chemical Reagent Co., Ltd. foram usados como precursores para SnO 2 síntese. Polietilenoimina, hexametileno tetramina, TritonX-100 e polivinilpirrolidona foram adquiridos de Aldrich Chemistry e usados como os agentes de direção de estrutura. Água destilada foi usada ao longo dos experimentos. Todos os produtos químicos eram de grau analítico e usados como adquiridos sem qualquer purificação adicional.
Síntese de SnO 2 Nanoflores com diferentes arquiteturas
Um procedimento de síntese típico com método hidrotérmico simples pode ser descrito como segue (Fig. 1):em primeiro lugar, 5 mmol de NaOH foram adicionados a uma mistura de 80 mL de etanol anidro e água desionizada (1:1) sob agitação magnética. Em seguida, 20 mmol de Na 3 C 6 H 5 O 7 · 2H 2 O e 10 mmol SnCl 2 · 2H 2 O foram dissolvidos na solução misturada sucessivamente sob agitação vigorosa durante 1 h à temperatura ambiente. A solução misturada foi então transferida para uma autoclave de aço inoxidável forrada com Teflon de 100 mL e mantida a 180 ° C por 12 h, e então resfriada até a temperatura ambiente naturalmente. Após a reação, o precipitado obtido foi coletado por centrifugação, lavando com água desionizada e etanol anidro várias vezes, e seco a 60 ° C por 6 h. O SnO 2 nanoflores foram finalmente obtidos após calcinação do precipitado em uma mufla sob condição de ar ambiente a 500 ° C por 2 h. Para sintetizar SnO 2 nanoflores com diferentes microestruturas, diferentes agentes tensoativos (1,0 g) foram introduzidos na solução, respectivamente, antes da dissolução do Na 3 C 6 H 5 O 7 · 2H 2 O. Neste trabalho, quatro tipos diferentes de surfactantes foram usados, incluindo PVP, PEI, HMT e TritonX-100, e os produtos finais correspondentes são nomeados como S PVP , S PEI , S HMT e S TritonX-100 , respectivamente, enquanto o produto sem surfactante é assinado como S 0 .
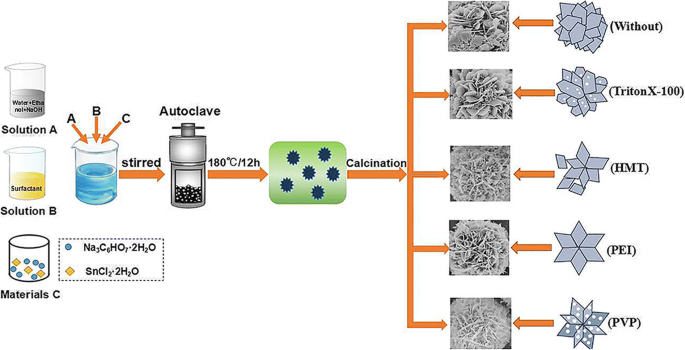
Ilustração esquemática do processo de formação do SnO hierárquico semelhante a uma flor 2 nanoestruturas usando diferentes tipos de surfactantes
Caracterizações
É bem conhecido que as propriedades de detecção de gás dos sensores de gás estão altamente relacionadas à morfologia, tamanho e dispersibilidade dos nanomateriais. Os produtos preparados foram analisados em termos de suas estruturas e morfologias por meio de difração de raios X policristalinos (XRD, Germany Bruker AXS D8 Advance), microscopia eletrônica de varredura (SEM, USA FEI Sirion 200) e microscopia eletrônica de transmissão de campo (FETEM, EUA Tecnai G2 F20 S-TWIN). A área de superfície é medida usando o Elemental Analyzer (USA ASAP 2460) com base no método Brunauer-Emmett-Teller (BET).
Fabricação de sensor e teste de detecção de gás
O sensor de gás foi fabricado usando o método de impressão de tela no topo de um tubo de alumina (visto na Fig. 2a). Normalmente, uma quantidade adequada de pó preparado foi primeiramente misturada com etanol anidro para formar uma suspensão em suspensão. Posteriormente, a suspensão da lama foi revestida no tubo de alumina por uma pequena escova, que é suportada por dois eletrodos de Au e quatro fios condutores de Pt. Em seguida, um fio de aquecimento Ni-Cr foi inserido no tubo de alumina para controlar a temperatura de trabalho ajustando a tensão de aquecimento. Finalmente, o produto foi envelhecido a 80 ° C por 72 h antes do teste.

a Diagrama esquemático da configuração do sensor de gás. b Diagrama de circuito elétrico do dispositivo sensor
As propriedades de detecção de gás foram medidas usando o sistema de análise de detecção de gás inteligente sensor de gás químico-4 temperatura baixa (CGS-4TPs) (Beijing Elliott Technology Co., Ltd., China) sob as condições de laboratório. A Figura 2b exibe o circuito elétrico esquemático típico. R s é a resistência do sensor e R l é a resistência de carga e uma tensão de aquecimento (V h ) é usado para ajustar a temperatura de trabalho. No presente trabalho, a resposta do sensor foi definida como S =(R s - R g ) / R g , onde Rs é a resistência inicial e Rg é a resistência após a injeção de gases. Os tempos de resposta e recuperação são definidos como o tempo que o sensor leva para atingir 90% da variação total da resistência no caso de adsorção e dessorção, respectivamente.
Resultados e discussão
Caracterização Estrutural e Morfológica
A fase cristalina do SnO como preparado 2 produtos foram identificados por difração de raios-X de potência, conforme mostrado na Fig. 3. A partir do padrão de XRD, todos os picos de difração observados podem ser facilmente atribuídos à estrutura de rutilo tetragonal de SnO puro 2 com o cartão de arquivo JCPDS padrão no. 41-1445, e nenhum outro pico pode ser identificado devido a impurezas. Os picos agudos indicam o alto grau de cristalinidade do nosso SnO 2 amostras, e nenhum deslocamento notável é detectado nos picos de difração, revelando que as amostras são de alta pureza.
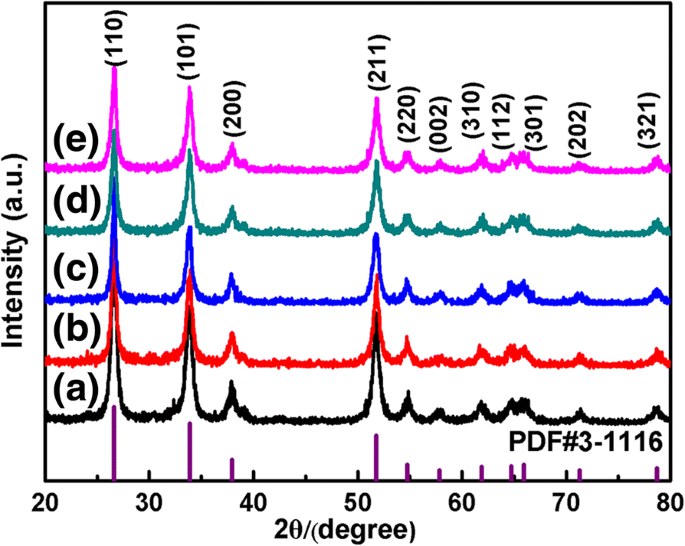
Padrões de XRD do SnO 2 amostras com morfologias diferentes. a S 0 , b S TritonX100 , c S HMT , d S PEI , e e S PVP
A Figura 4a mostra a imagem SEM do produto sem surfactante. Uma arquitetura hierárquica semelhante a uma flor pode ser observada e as nano-flores exclusivas são montadas por nanofolhas ultrafinas com uma espessura média de 20 nm ao redor. Infelizmente, essas nanofolhas são estritamente escalonadas umas em relação às outras, o que resulta em uma diminuição acentuada em seus espaços de reação. A Figura 4b-e mostra as morfologias dos produtos obtidos pela introdução de diferentes agentes tensoativos, mantendo outras condições experimentais inalteradas. Pode-se ver que após a adição do surfactante TritonX-100 (Fig. 4b), as nanofolhas são frouxamente interseccionadas entre si, e alguns mesoporos são moldados na borda das nanofolhas. Quando o HMT foi adicionado à mistura de reação como os agentes tensoativos (Fig. 4c), pode-se ver que as nanofolhas são dispostas aleatoriamente e várias nanofolhas menores são formadas entre as nanofolhas ultrafinas. A Figura 4d mostra as imagens de SEM dos produtos obtidos pela introdução do surfactante PEI na solução do precursor, o que revela que as nanofolhas com superfícies lisas estão dispostas ordenadamente e são interseccionadas verticalmente entre si, deixando um espaço de reação maior. A Figura 4e, f apresenta as imagens típicas de SEM dos produtos obtidos após a adição de surfactante PVP nas mesmas condições. Pode-se ver que as nanofolhas são distribuídas uniformemente ao longo do raio em toda a amostra para formar uma estrutura semelhante a uma flor. Além disso, em comparação com outras estruturas de S TritonX-100 , S HMT , e S PEI , as nanofolhas de S PVP são encerrados em um cone de triângulo invertido com um espaço oco relativamente maior (Fig. 4e). A imagem ampliada revela que as arquiteturas em forma de flor são montadas por nanofolhas mesoporosas para formar uma estrutura hierárquica porosa aberta, e cada nanofolha foi fabricada com vários mesoporos (Fig. 4f).

As imagens SEM do SnO 2 nanoflores com morfologias diferentes. a S 0 , b S TritonX-100 , c S HMT , d S PEI , e e , f S PVP
A fim de investigar melhor as microestruturas e propriedades cristalinas das nanoflores, TEM de baixa ampliação e HRTEM típico combinado com as técnicas de análise de difração de elétrons de área selecionada (SAED) são empregadas. A partir das imagens TEM (Fig. 5a-e), pode-se ver que as nanoflores com um diâmetro médio de 3 μm são montadas de várias nanofolhas individuais, e sua morfologia e tamanho são semelhantes às imagens SEM. Especialmente, a imagem TEM de S PVP (Fig. 5e) mostra que a estrutura mais semelhante a uma flor com a cor escura uniforme na região do meio é construída a partir da dispersão de numerosas nanofolhas uniformes ao longo da direção do raio. Combinando as medições SEM com TEM, pode-se concluir que as estruturas obtidas com a adição do surfactante PVP são as mais estáveis. As imagens TEM de alta resolução (HRTEM) mostram que para as amostras S 0 , S HMT , S PEI , e S PVP , o espaçamento de rede observado de 0,335 nm é consistente com o plano de rede (110) do rutilo tetragonal SnO 2 (Fig. 5f mostra apenas uma imagem HRTEM típica para S HMT como representante). A exposição do plano de rede (110) revela que o plano de rede (110) é o plano mais estável para SnO 2 no ar, o que é consistente com o estudo teórico. Deve-se notar que S TritonX-100 é um caso especial neste trabalho (Fig. 5b). Após a adição do surfactante TritonX-100, o crescimento e a dispersão das nanofolhas conduzem aleatoriamente a um diâmetro relativamente maior (3 ~ 4 μm) das nanoflores em comparação com outras amostras. Além disso, sua imagem HRTEM mostra que o espaçamento de rede calculado é de 0,264 nm, o que corresponde a (101) plano de rede da estrutura tetragonal do rutilo de SnO 2 . Além disso, o padrão SAED revela que S PVP tem uma estrutura cristalina única quase perfeita e os pontos de difração correspondem a (110), (\ (1 \; \ overline {1} \; 0 \)), (\ (\ overline {1} \; 1 \; 0 \)), e (200) planos de rede de SnO 2 (Fig. 5h). Ao contrário, para outras amostras, como S 0 , S HMT , S PEI e S TritonX-100 , o padrão SAED mostra uma estrutura policristalina e o anel de difração é indexado aos planos (110), (101) e (211) da estrutura rutilo tetragonal de SnO 2 (Fig. 5g).
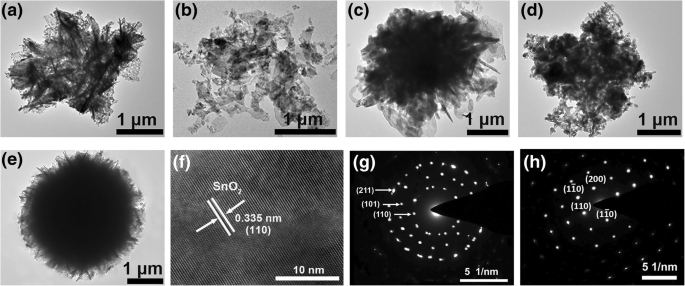
Imagens TEM de baixa ampliação de SnO 2 amostras. a S 0 , b S TritonX-100 , c S HMT , d S PEI , e e S PVP . f Micrografia HRTEM mostrando imagens ampliadas de treliça de S HMT . g Padrões SAED de S 0 . h Padrões SAED de S PVP
Mecanismo de crescimento do SnO 2 Nanoflores
Com base nas observações experimentais e análises acima, acredita-se que os surfactantes desempenham um papel significativo na formação de vários SnO 2 nanoflores [33]. O possível mecanismo de crescimento da folha-flor hierárquica SnO 2 nanoestruturas são brevemente ilustradas na Fig. 1. Neste trabalho, todos os SnO 2 nanoflores são sintetizados usando SnCl 2 como precursor [34]. Sob as condições hidrotérmicas, a reação geral para o crescimento de SnO 2 cristais com alta temperatura e pressão podem ser expressos da seguinte forma [35]:
$$ {\ mathrm {SnCl}} _ 2 + 2 {\ mathrm {OH}} ^ {-} \ to \ mathrm {Sn} {\ left (\ mathrm {OH} \ right)} _ 2 + 2 {\ mathrm { Cl}} ^ {-} $$ (1) $$ \ mathrm {Sn} {\ left (\ mathrm {OH} \ right)} _ 2 \ to \ mathrm {Sn} \ mathrm {O} + {\ mathrm { H}} _ 2 \ mathrm {O} $$ (2) $$ \ mathrm {SnO} + \ frac {1} {2} {\ mathrm {O}} _ 2 \ to {\ mathrm {SnO}} _ 2 $$ (3) $$ \ mathrm {Sn} {\ left (\ mathrm {OH} \ right)} _ 2+ \ frac {1} {2} {\ mathrm {O}} _ 2 + {\ mathrm {H}} _ 2 \ mathrm {O} \ to \ mathrm {Sn} {\ left (\ mathrm {OH} \ right)} _ 4 \ to {\ mathrm {SnO}} _ 2 + 2 {\ mathrm {H}} _ 2 \ mathrm {O} $ $ (4)
Durante todo o processo, três produtos químicos afetam muito o crescimento morfológico do SnO 2 nanoflores, incluindo NaOH, citrato de sódio e o surfactante. Em primeiro lugar, uma série de minúsculos nanocristais primários foram formados devido à hidrólise de Sn 2+ em uma solução básica de etanol-água, bem como sua rápida reação com OH - íons de NaOH. Deve-se notar que o ambiente básico de etanol-água é significativo para estimular o SnO 2 nucleação e crescimento [36]. A adição de citrato de sódio desempenha um papel crucial na distribuição espacial de precursores devido à sua forte capacidade de coordenação, que pode promover uma anisotropia no rápido crescimento e agregação de SnO 2 nanofolhas com a força motriz de diminuir a energia de superfície e acelerar a montagem de nanofolhas nas nanoflores florescentes hierárquicas estáveis [37].
Geralmente, a adição de surfactantes é favorável tanto para o aumento da área superficial quanto para o aumento da atividade superficial [38]. Dentre os surfactantes utilizados neste trabalho, o PEI é um tipo de surfactante catiônico. Quando PEI é adicionado às soluções de reação, devido ao N + existente íons com cauda hidrofílica, PEI irá adsorver preferencialmente em uma determinada faceta do cristal, o que é propício para a nucleação de SnO 2 nanocristais, bem como o crescimento ordenado de SnO 2 nanofolhas com seletividade direcional. Tanto o PVP quanto o TritonX-100 são surfactantes anfifílicos não iônicos, que podem servir como um molde macio na fabricação de materiais mesoporosos. Tomemos o PVP, por exemplo, para explicar o mecanismo de crescimento de estruturas porosas no SnO 2 nanofolhas como segue:quando o PVP é adicionado à solução, as moléculas de PVP se automontam em micelas esféricas por causa da forte atração hidrofóbica entre as caudas de alquila retas. Devido à sua anfifilicidade, o radical hidrofílico se moverá na direção da solução aquosa, e o radical hidrofóbico se moverá na direção oposta, levando à formação de domínios inorgânicos em torno de micelas de PVP organizadas periodicamente. Então, Sn 2+ e OH - íons são facilmente adsorvidos nas superfícies externas dessas micelas por meio de interações eletrostáticas até SnCl 2 é oxidado em SnO 2 nanofolhas, que são seguidas pela automontagem de nanofolhas em nanoflores florescentes com a ajuda de citrato de sódio. Finalmente, as micelas de PVP soft-template são removidas durante o processo de calcinação, produzindo SnO hierárquico 2 nanoflores com estruturas mesoporosas. Embora PVP e Triton X-100 contribuam para a formação de estruturas porosas, deve-se notar que PVP também pode desempenhar um papel de agente dispersante, o que torna o SnO 2 nanofolhas crescem mais uniformemente e separadamente devido às fortes interações e distâncias curtas de interação eletrostática entre o SnO 2 nanofolhas e PVP.
Propriedades de detecção de gás
Conforme relatado anteriormente, as nanoestruturas semelhantes a flores hierárquicas foram favoráveis para a absorção e difusão de gases de sonda em materiais sensores. Para lançar luz sobre o efeito de promoção de surfactantes e morfologia correspondente no comportamento do sensor, um estudo de detecção de gás sistematicamente comparativo entre sensores fabricados é realizado neste trabalho.
Comportamentos de detecção de gás de sensores fabricados para etanol
A temperatura operacional ideal é um fator chave para a aplicação de sensores de gás de óxido semicondutor. Em primeiro lugar, as respostas dos sensores a 100 ppm de etanol gasoso em várias temperaturas de operação de 180 a 360 ° C são testadas como mostrado na Fig. 6a. É claramente observado que todos esses sensores exibem um comportamento de detecção de gás semelhante, ou seja, os valores de resposta aumentam primeiro com um aumento da temperatura, atingem um valor máximo a 270 ° C e, em seguida, diminuem gradualmente com um aumento adicional de temperatura. Portanto, 270 ° C pode ser escolhido como a temperatura operacional otimizada para o estudo de detecção de gás de todos os SnO semelhantes a flores fabricados 2 sensores em nosso trabalho. A razão para a dependência da resposta da temperatura é a seguinte:Quando a temperatura de operação é muito baixa, um valor de resposta relativamente menor é atribuído à resposta inerte devido à ativação química, enquanto para temperatura de operação muito alta, o gás absorvido alvo as moléculas podem escapar dos sensores antes das reações, resultando também em uma resposta insatisfatória. Além disso, pode ser visto na Fig. 6a que de todos os cinco SnO 2 sensores baseados em diferentes surfactantes, S PVP mostra a maior resposta ao gás etanol e o maior valor de resposta do gás (38). Os valores máximos de resposta de outros quatro sensores são 27 para S PEI , 16 para S HMT , 11 para S TritonX-100 , e 8 para S 0 .
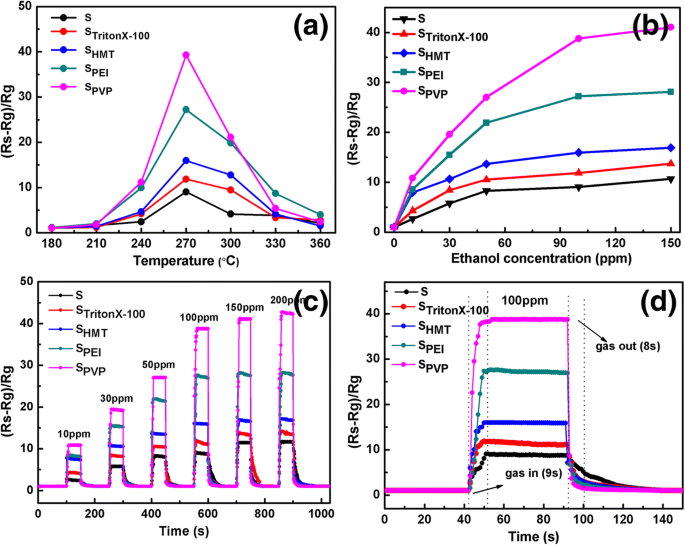
a A resposta dos sensores a 100 ppm de etanol sob diferentes temperaturas de operação (180–360 ° C). b As curvas de resposta dinâmica dos sensores ao etanol com diferentes concentrações (10-150 ppm) a 270 ° C. c Curvas de resposta versus tempo dos sensores para 10–200 ppm de etanol consecutivamente a 270 ° C. d Transiente de detecção dinâmica dos sensores para 100 ppm de etanol a 270 ° C
A Figura 6b mostra a resposta de todos os SnO 2 sensores para etanol na faixa de concentração de 10 ~ 150 ppm na temperatura ideal de trabalho 270 ° C. Pode-se observar claramente que a resposta de todos os sensores aumenta rapidamente com a concentração de gás abaixo de 50 ppm, e essa tendência torna-se suave de 50 a 150 ppm, tendendo a ficar saturada em cerca de 100 ppm. Como esperado, os surfactantes e as morfologias induzidas podem produzir uma grande influência no sensor de gás de sensores fabricados. Entre esses sensores fabricados, o S PVP sensor exibe o melhor comportamento de detecção em relação ao gás etanol e S PEI vem em segundo lugar. Para obter uma visão profunda do mecanismo de detecção de gás, BET (Brunaure-Emmett-Teller) adsorção-dessorção de nitrogênio também é realizada para determinar as áreas de superfície específicas dessas amostras, como mostrado na Tabela 1. Pode-se ver que S PEI tem a maior área de superfície específica (38,4 m 2 g −1 ) com maioria geral. É digno de nota que, apesar da área de superfície relativamente menor (15,5 m 2 g −1 ), S PVP é o melhor candidato para sensor de gás de etanol devido à sua arquitetura semelhante a uma flor perfeita, com auto-montagem de empilhamento ordenado e porosidade relativamente maior, fornecendo locais de adsorção mais ativos para moléculas de etanol. Mesmo em baixa concentração de etanol como 10 ppm, a sensibilidade de S 0 , S TritonX-100 , S HMT , S PEI , e S PVP os sensores podem atingir 2, 4, 7, 9 e 11, respectivamente, indicando sua aplicação potencial para sensores de etanol mesmo em baixas concentrações.
A Figura 6c exibe a resposta dinâmica de detecção de gás e as curvas de recuperação de sensores fabricados em relação ao etanol com uma temperatura de operação de 270 ° C, a partir da qual pode-se ver que as respostas de todos os sensores fabricados aumentam com o aumento da concentração de etanol e uma modulação notável de resistência é alcançado a cerca de 100 ppm. As respostas mostram um aumento drástico quando o sensor foi exposto aos gases-alvo e, em seguida, caiu para seu valor inicial no ar. Conforme mostrado na Fig. 6d, a resposta e o tempo de recuperação para 100 ppm de etanol são cerca de 16 se 28 s para S 0 , 14 se 18 s para S TritonX-100 , 11 se 15 s para S HMT , 9 se 11 s para S PEI , e 5 se 8 s para S PVP , respectivamente. É óbvio que o S PVP O sensor tem as melhores características de resposta / recuperação em comparação com outros sensores.
A Tabela 2 mostra uma comparação de desempenhos de detecção de etanol com base em diferentes SnO 2 abordagens fabricadas relatadas em outras literaturas e este trabalho na concentração de 100 ppm. Pode-se ver que nosso SnO polporoso 2 nanoflores apresentam comportamentos de detecção de etanol notavelmente com menor temperatura de operação ideal e maior valor de resposta, bem como tempo de resposta-recuperação mais rápido, o que pode ser atribuído à presença de numerosos mesoporos no sensor SPVP, levando a uma alta porosidade em favor da adsorção e difusão do gás etanol.
Comportamentos de detecção de gás de sensores fabricados para H 2 S
Conforme discutido na subseção anterior, S PVP O sensor exibe a melhor propriedade de detecção de gás para 100 ppm de etanol devido à sua alta porosidade. A fim de descobrir seu gás de detecção ideal, testamos a resposta de S PVP sensor para gases diferentes, incluindo acetona, metanol, formaldeído e H 2 S, com uma concentração de 100 ppm em várias temperaturas de operação (como mostrado nas Fig. 7a, b). Pode-se notar que a resposta ótima aparece a 330 ° C de metanol, a 210 ° C de formaldeído, a 360 ° C de acetona e a 180 ° C de H 2 S. Além disso, o valor máximo de resposta de S PVP para H 2 S é estimado em 368, que é uma ou duas ordens de magnitude (\ ({\ mathrm {S}} _ {{\ mathrm {H}} _ 2 \ mathrm {S}} / {\ mathrm {S}} _ {\ mathrm {etanol}} =9 \), \ ({\ mathrm {S}} _ {{\ mathrm {H}} _ 2 \ mathrm {S}} / {\ mathrm {S}} _ {\ mathrm { formaldeído}} =45 \)) mais alto do que para outros gases de teste. A temperatura de trabalho ideal mais baixa, bem como o melhor valor de resposta, indica S PVP tem excelente seletividade para H 2 S.
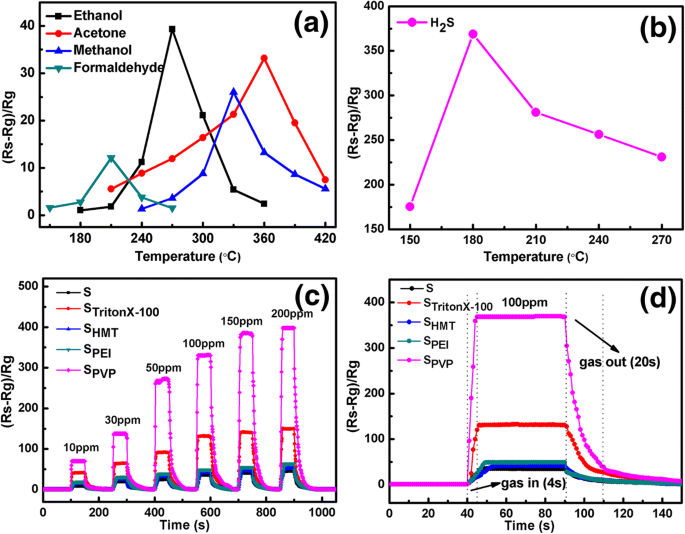
a Resposta de S PVP sensor a 100 ppm de etanol, acetona, metanol e formaldeído em diferentes temperaturas de operação. b Resposta de S PVP sensor a 100 ppm H 2 S em diferentes temperaturas de operação. c Curvas de resposta versus tempo dos sensores para 10–200 ppm H 2 S consecutivamente a 180 ° C. d Transiente de detecção dinâmica dos sensores para 100 ppm H 2 S a 180 ° C
Considerando a alta resposta de S PVP sensor para H 2 S, também realizamos uma medição sistemática de detecção de gás de todos os outros sensores. Uma resposta dinâmica de detecção de gás e curvas de recuperação de sensores fabricados em direção a H 2 S a 180 ° C são exibidos na Fig. 7c. Obviamente, os valores de resposta de todos os sensores fabricados mostram uma função crescente monotônica de H 2 Concentração S. Por 100 ppm H 2 S, o tempo de resposta e recuperação é de cerca de 9 se 43 s para S 0 , 5 se 30 s para S TritonX-100 , 14 se 40 s para S HMT , 8 se 38 s para S PEI , e 4 se 20 s para S PVP , enquanto os valores máximos de resposta são 35, 132, 41, 49 e 368 para S 0 , S TritonX-100 , S HMT , S PEI , e S PVP , respectivamente. É óbvio que o S PVP o sensor tem as melhores características de resposta / recuperação e a maior resposta a H 2 Gás S comparado com outros sensores, enquanto S TritonX-100 atinge o segundo.
A Figura 8 exibe o gráfico de barras de resposta de cinco sensores fabricados para formaldeído, metanol, etanol, acetona e H 2 S. Todos os gases foram testados com uma concentração de 100 ppm na temperatura operacional ideal. S TritonX-100 e S PVP mostram uma resposta distinta para H 2 S, enquanto S PEI mostra a maior resposta de gás ao metanol e acetona. Deve-se mencionar que a área superficial específica e a porosidade são dois fatores importantes para sensores de gás. A maior área de superfície específica fornecerá mais sítios ativos para adsorção e dessorção dos gases de teste, enquanto a maior porosidade induziria uma maior velocidade de difusão do gás devido à presença de mesoporos. Em comparação, S PEI possui uma área de superfície específica relativamente maior do que outros (visto na Tabela 1), que mostra a maior resposta do gás ao metanol e acetona (Fig. 8), enquanto S PVP e S TritonX-100 exibem a maior resposta do gás ao H 2 S devido às suas nanoestruturas tipo flor polporosas, provando boa seletividade de S TritonX-100 e S PVP em direção a H 2 S. A boa seletividade das amostras para H 2 S pode ser explicado da seguinte forma:quando o SnO 2 sensor é exposto em H 2 Gás S, ambas espécies de oxigênio adsorvido quimicamente e SnO 2 nanoestrutura reage com H 2 S durante a medição de detecção para formar SO 2 e SnS 2 , respectivamente. Comparado com SnO 2 , the body resistance of SnS2 is relatively smaller, leading to the sensitivity enhancement of the gas sensor [39]. On the contrary, the SnO2 sensor does not react with any other target gases, such as formaldehyde, methanol, ethanol, and acetone.
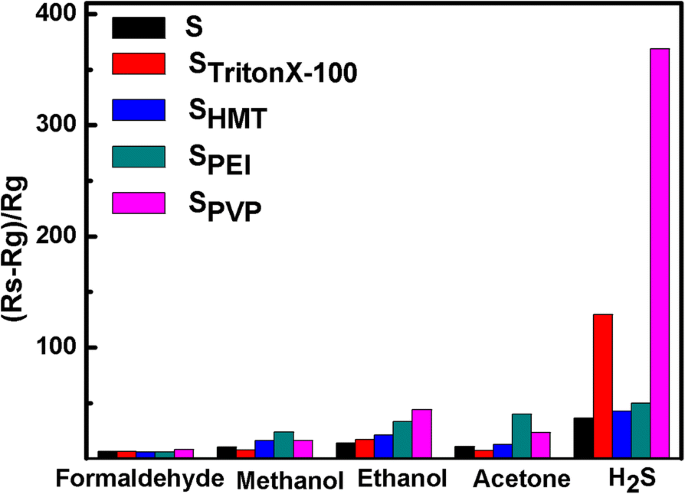
The comparison among sensor response of SnO2 nanomaterials to 100 ppm of various gases at the optimal operating temperature
Good stability and long service duration are expected from the viewpoint of practical application. To verify the stability of the sensor, the successive gas-sensing behavior of SPVP to 100 ppm ethanol was tested under the same conditions after 1 month. The samples were stored in the vacuum drying vessel during the 1-month interval. It can be seen from Fig. 9 that SPVP exhibits an excellent repeatability and stability even after 1 month. The three cyclic curves are similar to that measured 1 month ago, including the response value as well as the response-recovery time.
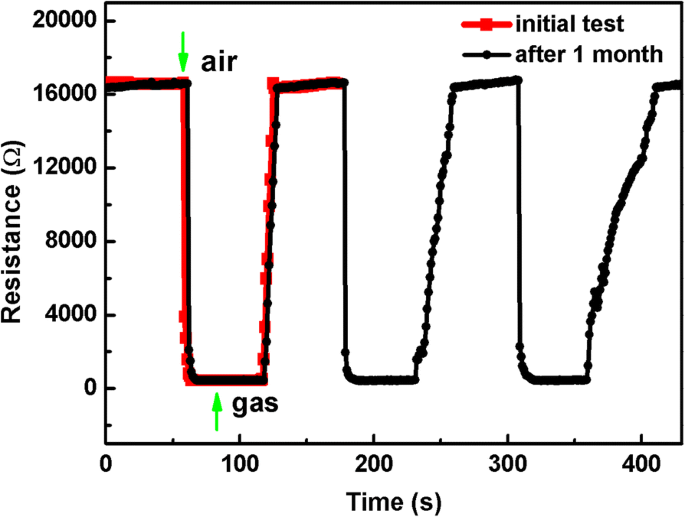
Stability of SPVP over 1 month of aging for 100 ppm ethanol at 270 °C
Gas-Sensing Mechanism
Up to now, the most widely accepted gas-sensing mechanism of semiconductor oxide is the model based on the electron transfer dynamics during an adsorption–oxidation–desorption process, which can change the resistance value of the sensors [40]. The response of typical n-type semiconductor greatly depends on the electron concentration. As shown in Fig. 10, at elevated temperature, electrons in the valence band are thermally excited to the conductive band. Once the SnO2 sensor is exposed to ambient air, oxygen molecules will be chemisorbed on the surface of SnO2 nanoflowers. Oxygen ions (O2 − , O − , and O 2− ) are then formed by capturing electrons from the conductive band of SnO2 [41], which is accompanied by an effective enlargement of electron-depleted layer. As a typical n-type semiconductor, the broadening of electron-depleted region means the decrease of carrier concentration within SnO2 nanoflowers, which will lead to the increase of resistance of the sensors. Conversely, when the SnO2 sensor is exposed in the reductive ambient, the absorbed oxygen species will quickly react with the target gas, which results in releasing the trapped electrons back to the conduction band and a reduction of the resistance of the sensors. Among the sensors fabricated in this work, SPEI and SPVP show relative better gas-sensing performances. The underlying physical mechanisms are as follows:the gas sensing properties are strongly dependent on the surface special area and the porosity. In comparison, SPEI possesses a relative larger specific surface area than others, which will provide more active sites for adsorption and desorption of test gases. SPVP exhibits a relative higher porosity due to the polyporous flower-like nanostructures, which is favorable to the rapid diffusion of gas (as shown in Fig. 10).
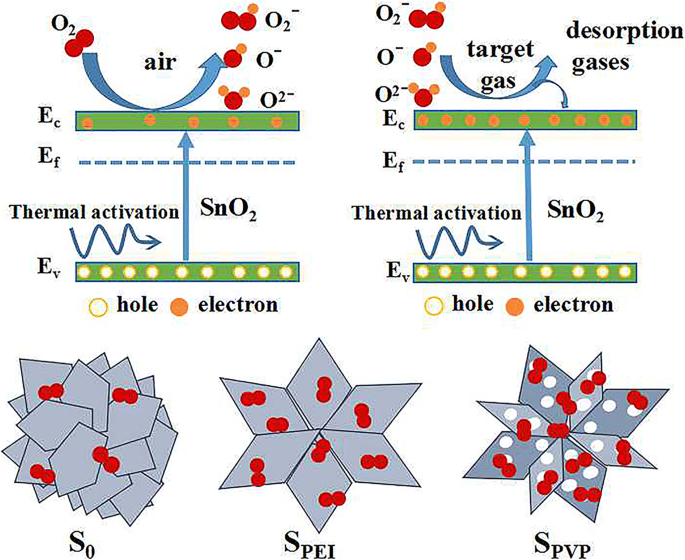
Schematic diagrams on the gas-sensing mechanism of flower-like SnO2 hierarchical nanostructures
Conclusões
We have successfully prepared the 3D hierarchical flower-like SnO2 nanostructures through a simple and low-cost facile hydrothermal route with the assistance of different surfactants. The images of SEM and TEM showed that the fabricated 3D hierarchical SnO2 nanoflowers with an average diameter of 2~4 μm were composed of many 2D nanosheets. The addition of surfactant plays an important role in the formation of nanoflowers. Based on the experimental observations, the possible growth process and gas-sensing mechanism of SnO2 nanoflowers were proposed. As a cationic surfactant, the addition of PEI is conducive to the nucleation of SnO2 nanocrystals as well as the orderly growth of SnO2 nanosheets, leading to a relative larger specific surface area. As amphiphilic non-ionic surfactants, PVP and TritonX-100 can make the nanosheets grow more uniformly and separately, which can serve as a soft template in the synthesis of advanced material, especially in the fabrication of mesoporous materials. In comparison, the sensor with the help of PVP (SPVP ) exhibits excellent gas-sensing performances to ethanol and H2 S due to its relative higher porosity. Especially, SPVP shows a high response (368), fast response/recovery time (4 s/20 s), and good selectivity toward H2 S gas. In addition, it is found that NaOH and sodium citrate are also important for the morphological formation of SnO2 nanoflowers.
Abreviações
- 1D:
-
Unidimensional
- 2D:
-
Bidimensional
- 3D:
-
Tridimensional
- BET:
-
Brunauer-Emmett-Teller
- FETEM:
-
Field emission transmission electron microscopy
- HMT:
-
Hexamethylene tetramine
- Na3 C 6 H 5 O 7 · 2H 2 O:
-
Trisodium citrate dihydrate
- PEI:
-
Polyethyleneimine
- PVP:
-
Polivinilpirrolidona
- SAED:
-
Difração de elétrons de área selecionada
- SEM:
-
Microscopia eletrônica de varredura
- XRD:
-
Difração de raios X
Nanomateriais
- O efeito do plasma sem equilíbrio de contato nas propriedades estruturais e magnéticas de Mn Х Fe3 - X О4 Spinels
- Propriedades paramagnéticas de nanomateriais derivados do fulereno e seus compostos de polímero:efeito drástico de bombeamento
- Propriedades das oscilações eletromagnéticas longitudinais em metais e sua excitação em superfícies planas e esféricas
- Influência da Água na Estrutura e Propriedades Dielétricas da Microcristalina e Nano-Celulose
- Ajustando as morfologias de superfície e propriedades dos filmes ZnO pelo projeto da camada interfacial
- Nanocompósitos de poli (N-isopropilacrilamida) magnético:efeito do método de preparação nas propriedades antibacterianas
- Síntese de pontos quânticos de sulfeto de antimônio solúvel em água e suas propriedades fotoelétricas
- Síntese fácil de óxido de estanho mesoporoso semelhante a buraco de minhoca via auto-montagem induzida por evaporação e propriedades aprimoradas de detecção de gás
- Efeito do método de síntese de La1 - xSr x MnO3 nanopartículas de manganita em suas propriedades
- Tipos de metais e suas propriedades



