Síntese passo a passo de nanoflores Au @ CdS-CdS e suas propriedades fotocatalíticas aprimoradas
Resumo
A fabricação de nanoestruturas híbridas com morfologias complexas e alta atividade fotocatalítica é um desafio difícil porque essas partículas requerem habilidades de preparação extremamente altas e nem sempre são práticas. Aqui, nanopartículas hierárquicas de Au @ CdS-CdS (nanoflores de Au @ CdS-CdS) foram sintetizadas usando um método passo a passo. As nanoflores Au @ CdS-CdS são compostas por núcleo de Au, casca de CdS e nanobastões de CdS. A faixa de absorção de UV-Vis das nanoflores Au @ CdS-CdS atinge até 850 nm, que cobre toda a faixa visível (400–760 nm). A propriedade de transferência de carga fotoinduzida de nanoflores Au @ CdS-CdS foi demonstrada usando espectroscopia de fotoluminescência (PL). Em comparação com as contrapartes CdS e as contrapartes Au @ CdS, as nanoflores Au @ CdS-CdS demonstraram a maior taxa de degradação fotocatalítica sob irradiação de λ =400-780 nm e λ =600-780 nm, respectivamente. Com base nas análises de estrutura e morfologia, propusemos um possível mecanismo de formação da nanoestrutura híbrida que pode ser usada para orientar o projeto de outras nanoestruturas semicondutoras de metal com morfologias complexas.
Introdução
A energia solar é atualmente reconhecida como a fonte de energia mais limpa e abundante. A conversão da energia solar em outras formas de energia usando fotocatalisador semicondutor tem sido considerada uma forma ideal de resolver a crise energética e a poluição do meio ambiente [1, 2]. Para fazer pleno uso da energia solar, muitos fotocatalisadores baseados em semicondutores foram projetados e desenvolvidos [3, 4]. Entre eles, o CdS, com um gap adequado de cerca de 2,4 eV para a absorção efetiva da luz visível da luz solar, é um dos poucos fotocatalisadores acionados pela luz visível [5]. No entanto, a alta taxa de recombinação do portador de carga e a fotocorrosão impedem seriamente a eficiência fotocatalítica do CdS.
Nos últimos anos, as nanoestruturas híbridas têm atraído grande atenção devido às suas propriedades físico-químicas [6,7,8,9]. Em comparação com o componente individual correspondente, as nanoestruturas híbridas baseadas em CdS mostram melhor desempenho em certas aplicações devido ao intervalo de absorção de luz aprimorado e separação de carga aprimorada. Yu et al. construíram um sulfeto ternário único - [ZnS-CdS-Cu 2-x S] -ZnS- heteronanorod que mostra uma região de absorção expandida e separação de carga eficiente, levando a um melhor desempenho na conversão de energia solar [10]. Xu et al. sintetizaram CdS em forma de bastonete e esférico @ TiO 2 nanopartículas de núcleo-casca (CSNs) que demonstram excelente desempenho fotocatalítico para reações redox seletivas sob irradiação de luz visível [11, 12]. O esquema Z em CdS-Au-TiO 2 O sistema de nanojunção de três componentes exibiu maior atividade fotocatalítica do que os sistemas de um e dois componentes, devido à transferência de elétrons ao longo da rota projetada [13]. Embora muitas nanoestruturas híbridas baseadas em CdS tenham sido sintetizadas, a síntese controlada de nanoestruturas híbridas com componentes, estruturas e fases de cristal desejados permanece um desafio notável.
Como um importante ramo das nanoestruturas híbridas, as nanoestruturas semicondutoras de metal têm sido amplamente estudadas como um novo tipo de material funcional avançado [14,15,16,17,18,19]. Entre eles, nanoestruturas híbridas de Au-CdS têm atraído cada vez mais atenção devido à interação entre plasmon e exciton. As nanoestruturas plasmônicas têm habilidades significativas para concentrar energia luminosa em nanoescala, que vem de sua natureza como uma oscilação coletiva de elétrons de superfície do metal com luz incidente em frequências combinadas [20]. Quando os metais são hibridizados com semicondutores, essa capacidade de gerenciamento de luz em nanoescala dos plasmônicos pode ser utilizada para melhorar a eficiência da fotoexcitação nos semicondutores [21]. Na pesquisa em nanociência, projetar nanoestruturas complexas controlando o tamanho e a forma dos nanocristais é fundamental para explorar suas novas propriedades [22,23,24,25]. Até agora, várias formas de nanoestruturas híbridas de Au-CdS foram preparadas e aplicadas a componentes ópticos, sensores, fotovoltaicos e dispositivos fotocatalíticos [26,27,28,29,30]. No entanto, a estrutura hierárquica 3D de nanocompósitos de Au-CdS com morfologia bem definida raramente foi relatada. A síntese de nanocompósitos complexos é um desafio muito difícil porque essas nanopartículas requerem habilidades de preparação extremamente altas e nem sempre são práticas.
Aqui, construímos nanopartículas de Au @ CdS-CdS semelhantes a flores (nanoflores de Au @ CdS-CdS) por meio de uma estratégia de síntese gradual. Que possui heteroestruturas hierárquicas construídas por crescimento epitaxial de nanobastões 1D CdS nas superfícies de Au @ CdS CSNs e estrutura heterogênea entre Au e CdS. As nanoflores de Au @ CdS-CdS sintetizadas mostram uma região de absorção expandida que atinge até 850 nm e cobre toda a faixa visível. As nanoflores de Au @ CdS-CdS demonstram atividade fotocatalítica aprimorada em comparação com CSNs de Au @ CdS e contrapartes de CdS sob a irradiação visível. Com base em seu tamanho, morfologia e estrutura, propusemos um mecanismo de crescimento viável, que provavelmente será útil para pesquisadores em áreas tão diversas como medicina, energia e eletrônica, que muitas vezes projetam nanopartículas complexas que têm funções úteis.
Métodos
Síntese de Nanoflores Au @ CdS-CdS
Todos os produtos químicos recebidos de Aladdin eram reagentes de grau analítico e usados sem purificação adicional. Au coloides com um diâmetro médio de 50 nm foram sintetizados pelo método tradicional de Frens [31] e Au @ CdS CSNs foram preparados usando um método hidrotérmico publicado [32]. Normalmente, uma solução aquosa de l-cisteína (Cys, 99%) foi misturada com nitrato de cádmio tetra-hidratado (99%) em uma proporção de 2:1 M de Cys para Cd 2+ . 2 mL de l-cisteína-Cd 2+ (Cys / Cd 2+ ) mistura foram adicionados em 10 mL de coloides Au e agitados por 15 min, em seguida, o Au- obtido (Cys / Cd 2+ ) foram diluídos para 50 mL com água e transferidos para uma autoclave de aço inoxidável forrada com Teflon (capacidade de 100 mL). Depois de selada, a autoclave foi aquecida e mantida a 130 ° C por 6 h. Para revestir a camada espessa de CdS em nanopartículas de Au, 10 mL de Cys / Cd 2+ mistura foram adicionados a coloides Au (10 mL) com as outras condições de reação inalteradas.
Nanoflores Au @ CdS-CdS foram então sintetizados da seguinte forma:os coloides Au @ CdS CSNs resultantes (10 mL), 1 mL de Cys / Cd 10 mM 2+ mistura e 20 mL de etilenodiamina (En,> 99%) foram misturados e agitados durante 15 min, e então transferidos para uma autoclave de aço inoxidável forrada com Teflon (50 mL de capacidade). A autoclave selada foi aquecida a 180 ° C e mantida a esta temperatura por 10 h, e então deixada resfriar até a temperatura ambiente. O produto foi recolhido e lavado várias vezes com água destilada e etanol para remover os iões e impurezas restantes.
As contrapartes de CdS foram sintetizadas da seguinte forma:4 mL Cys / Cd 2+ mistura e 20 mL de água foram adicionados ao reator e agitados por 15 min, então selados e aquecidos a 130 ° C por 6 h. Os produtos foram resfriados naturalmente até a temperatura ambiente e lavados várias vezes com água destilada e etanol. Por fim, as amostras foram dispersas em etanol absoluto.
Caracterizações de materiais
As medições de difração de raios X (XRD) das amostras foram realizadas em um difratômetro avançado Bruker D8 e os espectros de absorção de UV-Vis foram testados em um fotômetro PerkinElmer Lambda 35. Imagens de microscópio eletrônico de varredura por emissão de campo (FE-SEM) e espectrômetro de energia dispersiva de raios-X (EDS) foram obtidas em um dispositivo JSM-7001F. O modelo do microscópio eletrônico de transmissão (TEM) é JEM-2010 e a tensão de operação é 200 kV. Imagens de microscópio eletrônico de transmissão de alta resolução (HR-TEM) também foram testadas no JEM-2010 com uma tensão operacional de 200 kV. Os espectros de fotoluminescência (PL) foram medidos em um Perkin-Elmer LS-55 com um comprimento de onda de excitação de 400 nm. As medições de fotocorrente (curvas i – t) foram conduzidas em um sistema de célula de três eletrodos convencional usando uma estação eletroquímica CHI660C sem polarização sob uma lâmpada de arco 300 W Xe como fonte de luz. O vidro ITO limpo depositado com fotocatalisadores, floco de Pt e um eletrodo de Ag / AgCl foram, respectivamente, usados como eletrodos de trabalho, contra eletrodo e eletrodo de referência. Na 2 SO 4 (0,2 M) foi usado como o eletrólito.
Medição da atividade fotocatalítica
O sistema óptico utilizado para a reação fotocatalítica consistia em lâmpada de xenônio (300 W) e dois filtros passa-banda (com largura de banda de 400–780 nm e 600–780 nm) que garantem a irradiação na faixa visível. Quatro tipos de fotocatalisadores, incluindo nanopartículas de Au, contraparte de CdS, Au @ CdS de espessura e nanoflores de Au @ CdS-CdS foram usados para degradar a solução de rodamina 6G (R6G). Normalmente, 6 mg de fotocatalisador foram adicionados em 20 mL de solução R6G (1,0 × 10 −5 M) e agitado por 30 min no escuro para atingir o equilíbrio de adsorção antes da irradiação. Os experimentos fotocatalíticos foram conduzidos sob dois intervalos de irradiação, 400–780 nm e 600–780 nm, respectivamente. Em seguida, 2,5 mL de solução foram extraídos a cada 10 minutos e centrifugados para remover o fotocatalisador. Os espectros de absorção de UV-Vis dos filtrados foram registrados usando o fotômetro PerkinElmer Lambda 35 para monitorar a reação catalítica. Todos os experimentos de fotocatálise foram conduzidos à temperatura ambiente ao ar. A degradação de R6G foi definida como segue:
Degradação (%) =[( C 0 - C t ) / C 0 ] × 100.
onde C 0 é a concentração inicial de R6G, C t é a concentração de R6G em um determinado momento após a reação fotocatalítica.
Resultados e discussão
O mecanismo de síntese de nanoflores
O processo de síntese em etapas para as nanoflores de Au @ CdS-CdS é representado na Fig. 1. Primeiro, as nanopartículas de Au são sintetizadas com um tamanho médio de cerca de 50 nm. A camada de CdS é depositada na superfície das nanopartículas de Au por meio de uma reação hidrotérmica para produzir CSNs de Au @ CdS. Em seguida, os nanobastões de CdS são cultivados na superfície de Au @ CdS CSNs por meio de um método solvotérmico misto para produzir as nanoestruturas hierárquicas de Au @ CdS-CdS. A l-cisteína e a etilenodiamina desempenham um papel importante na síntese de nanoflores Au @ CdS-CdS. l-cisteína, possuindo três grupos funcionais (SH, COOH, NH 2 ), serve como fonte de enxofre e agente de ligação para compensar a incompatibilidade de rede entre os cristais de Au e CdS [32]. A fase de cristal pode ser controlada pela introdução de etilenodiamina como um reagente guia de estrutura no crescimento de nanobastões de CdS [33]. Além disso, é muito difícil para nós sintetizar nanoflores Au @ CdS-CdS adicionando coloides Au, Cys / Cd 2+ mistura e etilenodiamina em conjunto nas mesmas condições. Portanto, o intermediário de Au @ CdS CSNs é necessário para a síntese de nanoflores de Au @ CdS-CdS, porque a superfície da casca de CdS não é lisa e essas protuberâncias se tornam os "locais de crescimento" para o crescimento epitaxial de nanobastões de CdS.
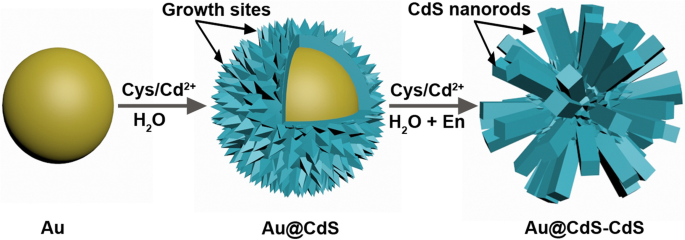
Ilustração esquemática dos processos de síntese de nanoflores Au @ CdS-CdS
Morfologia e estrutura de amostra
As imagens SEM das nanopartículas em cada procedimento foram mostradas na Fig. 2a-c. Nanopartículas de Au mostraram que eram uniformes em tamanho e bem dispersas. Os CSNs de Au @ CdS foram mostrados na Fig. 2b em que nanopartículas de Au ou CdS únicas raramente foram observadas. A superfície da casca do CdS foi serrilhada e as protuberâncias puderam ser observadas na imagem TEM da inserção. Conforme exibido na Fig. 2c, os nanocristais de Au @ CdS-CdS apresentaram-se como nanopartículas semelhantes a flores bem definidas com boa dispersão. A Figura 2d mostrou a imagem TEM de Au @ CdS CSNs com camada espessa de CdS (denotada como Au @ CdS espessa). A Figura 2e mostrou a imagem TEM de nanoflores Au @ CdS-CdS. Pode-se observar que os nanobastões 1D CdS foram cultivados epitaxialmente na superfície dos CSNs Au @ CdS. O diâmetro e o comprimento do nanobastão de CdS foi de cerca de 16 nm e 40 nm, respectivamente. A imagem HR-TEM de nanoflores Au @ CdS-CdS foram mostradas na Fig. 2f. O espaçamento da rede de 0,34 nm em nanobastões foi consistente com os (002) planos de cristal de wurtzite CdS. Os nanobastões de CdS conforme preparados eram cristais únicos com uma direção de crescimento preferencial de [001], o eixo c [34]. A análise de EDS confirmou ainda a composição elementar das nanoflores Au @ CdS-CdS, conforme mostrado na Fig. 2g, que indicou a presença dos elementos de Cd, S e Au. Nanocristais de CdS com tamanho uniforme foram mostrados na Fig. 2h. Além disso, as cores da solução de coloides Au, Au @ CdS fino, nanoflores Au @ CdS-CdS, contrapartes CdS e Au @ CdS de espessura eram vinho tinto, roxo, verde, amarelo e verde, respectivamente, mostrado na Fig . 2i.

a , b , h Imagens SEM de nanopartículas de Au, Au @ CdS com casca fina e contrapartes CdS, respectivamente. d Imagens TEM de Au @ CdS com casca espessa. c , e , f , g SEM, TEM, imagem HR-TEM e perfil EDS de nanoflores Au @ CdS-CdS. eu Fotografias de suas cores de solução
Os padrões de XRD das amostras obtidas no processo de síntese de nanaoflores Au @ CdS-CdS foram mostrados na Fig. 3. Picos de XRD de nanopartículas de Au foram observados e os picos em 2θ =38,2, 44,2 e 64,75 foram devidos ao (111 ), (200) e (220) planos, respectivamente, do cristal de Au fcc (JCPDS 04-0784). Para cristais de CdS, os picos em 2θ =25, 26,5, 28,2, 43,8, 47,8 e 51,9 foram devidos a (100), (002), (101), (110), (103) e (112) planos de o cristal Wurtzite CdS (JCPDS 41-1049). Ambos os picos de difração de cristal de fcc Au e wurtzite CdS foram observados nos padrões de XRD de Au @ CdS CSNs e Au @ CdS-CdS nanoflowers, respectivamente. Deve-se notar que a intensidade do pico de difração do plano de cristal (002) foi muito maior do que outros picos em nanocristais de Au @ CdS-CdS. Isso indicou que o pico de difração do plano de cristal (002) é proeminente e os nanobastões de CdS foram crescidos ao longo da direção [001], que estava de acordo com o resultado HR-TEM.
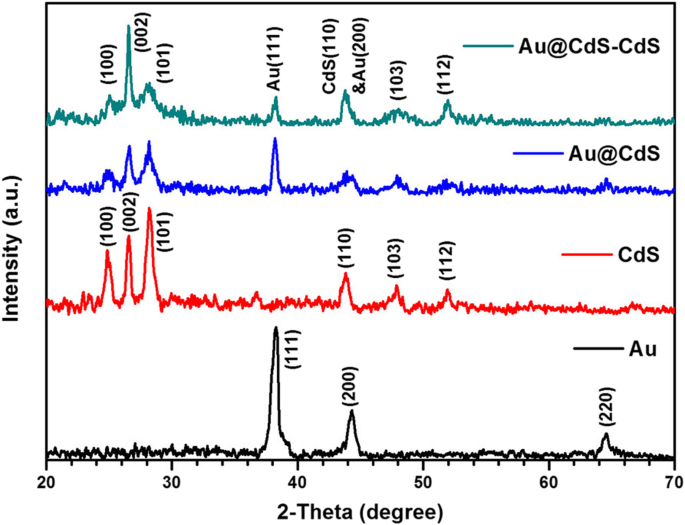
Padrões de XRD de nanoflores Au, CdS, Au @ CdS CSNs e Au @ CdS-CdS
Propriedades ópticas da amostra
As propriedades ópticas das cinco amostras foram analisadas por medidas de UV-Vis, conforme ilustrado na Fig. 4. A posição da borda da banda dos coloides CdS era inferior a 500 nm. Os coloides de Au de 50 nm exibem uma absorção de ressonância plasmônica de superfície (SPR) centrada em 530 nm. O revestimento das nanoesferas de Au com camada fina de CdS resultou em um desvio para o vermelho do pico do plasmon para 568 nm. Com o aumento da espessura da casca do CdS, a posição do SPR mudou ainda mais para o vermelho para 623 nm e 635 nm nas nanoflores de Au @ CdS de espessura e Au @ CdS-CdS, respectivamente. Os resultados experimentais mostraram que com o aumento da espessura da camada de CdS, o pico de absorção de SPR das nanopartículas de Au exibiu um desvio para o vermelho contínuo, pois a posição de SPR do metal dependia do tamanho do metal, forma e meio circundante. Fenômenos semelhantes foram observados em Au @ SiO 2 , Au @ Cu 2 O e Au-Fe 3 O 4 sistemas nanoestruturados híbridos [35,36,37]. A posição da borda da banda de nanoflores Au @ CdS-CdS alcançou até 850 nm, o que poderia colher melhor a região visível da luz solar (400-760 nm) para aumentar a atividade fotocatalítica.
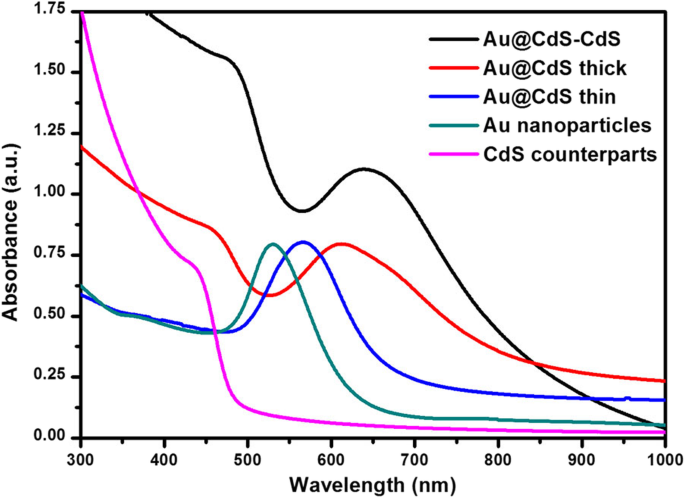
Os espectros de absorção de UV-Vis de amostras:contrapartes de CdS, nanopartículas de Au e nanoflores de Au @ CdS CSNs e Au @ CdS-CdS, respectivamente
Propriedades de transferência de carga induzida por luz
Os espectros de fotoluminescência (PL) das nanoflores de Au @ CdS-CdS sintetizados, CSNs de Au @ CdS, contrapartes de CdS e coloides de Au foram mostrados na Fig. 5a. Os colóides de ouro tiveram um pico de PL fraco em ~ 600 nm. O espectro PL das contrapartes CdS mostrou uma banda de emissão dominante em 530 nm e um pico de ombro menor em 598 nm. A banda em 530 nm pode ser atribuída à emissão de banda excitônica típica do CdS. O ombro em 598 nm pode ser devido à emissão presa que surgiu de defeitos estruturais no cristal CdS. No entanto, a intensidade espectral PL da estrutura híbrida foi significativamente reduzida, e a emissão radiativa do CdS em nanoflores Au @ CdS-CdS foi extinta mais do que em CSNs Au @ CdS. Uma vez que o nível de Fermi de Au estava localizado a + 0,5 V em relação ao eletrodo de hidrogênio normalizado (NHE), ele era inferior ao nível da banda de condução de CdS (- 1,0 V vs. NHE). Após a excitação do CdS, os elétrons livres na banda de condução seriam transferidos para o núcleo de Au devido à diferença de energia [32, 38]. O mecanismo de transferência de carga fotoinduzido levou a uma diminuição na probabilidade de recombinação elétron-buraco e supressão da emissão de exciton em CdS. A probabilidade de recombinação do elétron fotogerado e buraco foi maior nos CSNs Au @ CdS, provavelmente devido ao alto conteúdo de CdS. As nanoestruturas híbridas de Au @ CdS-CdS semelhantes a flores fornecem uma plataforma de pesquisa ideal para o estudo do mecanismo de transferência de carga fotoinduzida para heterojunção de metal-semicondutor. Os resultados da resposta de fotocorrente transitória obtida a partir de nanoflores Au @ CdS-CdS, Au @ CdS de espessura e contrapartes CdS foram mostrados na Fig. 5b. Foi fácil observar que a fotocorrente sobre Au @ CdS-CdS foi muito melhorada em comparação com a de Au @ CdS de espessura e contrapartes CdS. A fotocorrente melhorada sobre o nanocompósito Au @ CdS-CdS implicou na separação mais eficiente dos pares elétron-buraco fotoinduzidos e uma vida útil mais longa dos portadores de carga fotogerados do que o do CdS em branco, o que foi benéfico para sua atividade fotocatalítica.
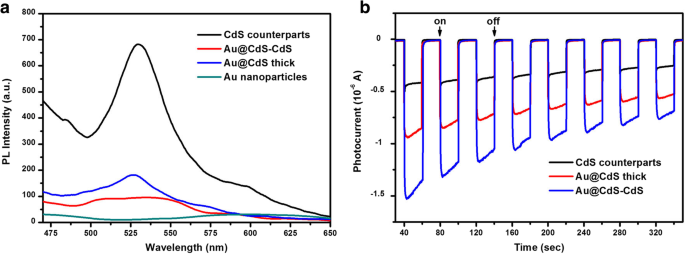
a Os espectros de PL de coloides Au, Au @ CdS de espessura, Au @ CdS-CdS e contrapartes CdS, respectivamente. b Comparação da resposta de fotocorrente transitória das nanoflores Au @ CdS-CdS, Au @ CdS de espessura e contrapartes CdS irradiadas com luz visível de λ ≥ 400 nm em 0,2 M Na 2 SO 4 solução aquosa sem polarização contra Ag / AgCl
Aplicação de materiais
As nanoflores Au @ CdS-CdS aumentaram a capacidade de captura de luz visível e as propriedades de separação de carga induzida por foto, que têm valor potencial em certas aplicações. A atividade fotocatalítica de Au @ CdS-CdS sob irradiação de 400-780 nm foi detectada usando o corante Rodamina 6G como alvo de fotodegradação. Para comparação, nanopartículas de Au, contrapartes de CdS e espessura de Au @ CdS também foram testadas nas mesmas condições. A Figura 6a foi o espectro de absorção de UV-Vis das soluções R6G sob diferentes tempos de irradiação usando nanoflores Au @ CdS-CdS. A intensidade do pico de absorção da solução R6G diminuiu rapidamente com o tempo de iluminação, e seu pico de absorção característico também mudou de 528 nm para 507 nm. Após 40 min, a concentração de R6G quase não mudou, sugerindo que a reação de degradação estava completa. A Figura 6b mostrou a mudança normalizada da concentração de soluções R6G com nanopartículas de Au, contrapartes de CdS e nanoflores de Au @ CdS de espessura e Au @ CdS-CdS. Sem catalisador, a mudança de concentração de R6G pode ser insignificante. Entre os catalisadores, a taxa de fotodegradação das nanoflores Au @ CdS-CdS foi significativamente mais rápida do que a de outros materiais. Após 40 min, 86% da solução R6G foi degradada no sistema de nanoflores Au @ CdS-CdS, enquanto apenas 71%, 46% e 12% da solução R6G foi degradada na espessura Au @ CdS, contrapartes CdS, e Sistema de nanopartículas de Au, respectivamente.
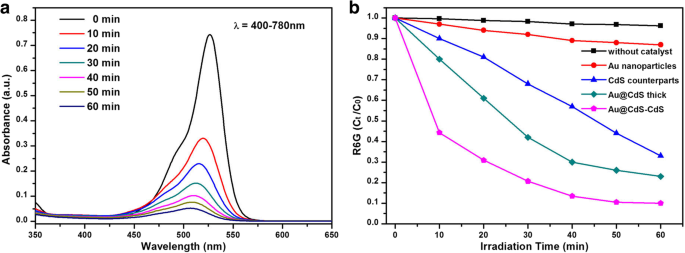
a Espectros de absorção de soluções R6G em diferentes tempos de irradiação usando nanoflores Au @ CdS-CdS como fotocatalisador sob irradiação de 400-780 nm. b C t / C 0 versus gráficos de tempo de irradiação para fotodegradação R6G na presença de diferentes fotocatalisadores
Como visto na Fig. 6b, as nanoestruturas híbridas exibiram atividade fotocatalítica superior em comparação com as correspondentes de componente único. A incorporação de nanocristais de metal plasmônico em nanoestruturas semicondutoras melhorou muito o desempenho fotocatalítico do último através do LSPR do primeiro [39, 40]. A luz concentrada e espalhada das nanopartículas de ouro contribuiu para aumentar a absorção de luz do CdS, o que levou à geração de mais excitons. A heterojunção entre Au e CdS promoveria a separação e transferência de carga. Além disso, a taxa fotocatalítica de nanoflores de Au @ CdS-CdS era obviamente maior do que a de Au @ CdS de espessura, embora tivessem o mesmo tamanho e faixa de absorção espectral semelhante. Isso pode estar relacionado à morfologia especial das nanoflores de Au @ CdS-CdS, que tinham uma área de superfície específica maior, o que significa que poderia fornecer mais locais de reação. Com a mesma massa, a área de superfície das nanoflores era mais de 4,67 vezes a das nanoesferas. Cálculos detalhados foram mostrados no arquivo adicional 1. Portanto, as nanoflores Au @ CdS-CdS têm excelente atividade fotocatalítica entre todas as amostras.
Existem vários mecanismos primários, como mecanismo de campo próximo, espalhamento de luz e injeção de elétrons quentes, que podem ser descritos para a reação fotocatalítica intensificada por plasmon. Para testar a faixa de absorção expandida de nanoflores de Au @ CdS-CdS se aumentava a atividade fotocatalítica ou não, realizamos testes fotocatalíticos sob a iluminação de λ =600-780 nm. A Figura 7a mostrou a absorção de UV-Vis de R6G degradado por nanoflores Au @ CdS-CdS sob a iluminação de λ =600-780 nm. A atividade fotocatalítica para degradar R6G por quatro fotocatalisadores foi mostrada na Fig. 7b. Após irradiação de 60 min, a degradação de nanopartículas de Au, contrapartes de CdS, Au @ CdS de espessura e nanoflores de Au @ CdS-CdS foi de 9,8%, 15%, 34% e 45%, respectivamente. A taxa de fotodegradação em sistemas de nanoestruturas híbridas foi mais rápida do que a de cristais de um único componente. A atividade fotocatalítica das nanoestruturas híbridas foi melhorada pela faixa de absorção expandida porque o CdS não foi excitado quando a luz incidente estava acima de 516 nm. Enquanto o pico de absorção de SPR de nanopartículas de Au em nanoflores de Au @ CdS-CdS foi de cerca de 650 nm. Sob a iluminação de 600-780 nm, elétrons quentes foram gerados a partir de Au e seriam transferidos para a banda de condução de CdS durante o relaxamento [41, 42]. A fim de avaliar melhor a durabilidade e reutilização desses fotocatalisadores, a mesma amostra foi centrifugada e redispersa em 20 mL H 2 O contendo 10 −5 M R6G para vários testes de ciclagem. A Figura 8a demonstrou que a eficiência de fotodegradação de R6G permanece quase inalterada durante os três ciclos de teste consecutivos, sugerindo a alta estabilidade das nanoestruturas Au @ CdS-CdS.
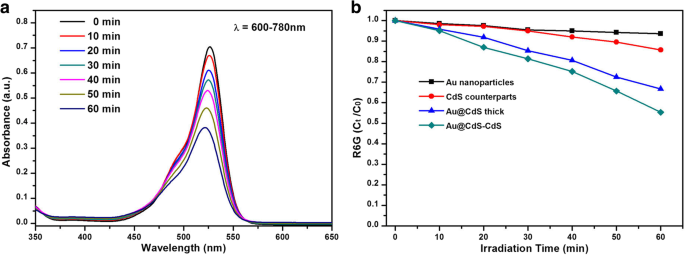
a Espectros de absorção de soluções R6G em diferentes tempos de irradiação usando nanoflores Au @ CdS-CdS como fotocatalisador sob irradiação de 600-780 nm. b C t / C 0 versus gráficos de tempo de irradiação para fotodegradação R6G na presença de diferentes fotocatalisadores
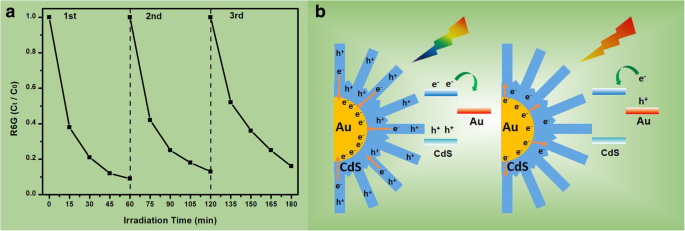
a O ciclo é executado para a degradação fotocatalítica do corante R6G sobre as nanoflores Au @ CdS-CdS sob irradiação de luz visível (400-780 nm). b Dois mecanismos de separação de carga para nanoflores de Au @ CdS-CdS sob irradiação de 400-780 nm e 600-780 nm, respectivamente
Tanto o Au plasmônico quanto o CdS semicondutor de bandgap estreito são sensíveis à luz visível na nanoestrutura de Au-CdS. Assim, espera-se que existam dois mecanismos distintos de separação e transferência de carga fotoinduzida em nanoflores de Au @ CdS-CdS, dependendo da energia de excitação incidente, conforme mostrado na Fig. 8b. Para um caso específico, se apenas o CdS estiver excitado, os elétrons serão transferidos da banda de condução do CdS para o Au. Da mesma forma, se apenas Au estiver excitado, os elétrons saltarão do estado plasmônico de superfície de Au para a banda de condução de CdS. Mas o caso se torna mais complicado quando Au e CdS são excitados juntos. A transferência de elétrons em ambos os sentidos é possível, embora mais provável seja a transferência de semicondutor para metal [43,44,45]. O aumento das probabilidades de separação de carga irá melhorar a atividade fotocatalítica de nanoestruturas híbridas de metal-semicondutor, porque elétrons separados e lacunas terão alta probabilidade de participar de reações catalíticas. Normalmente, os buracos podem oxidar os contaminantes orgânicos ou moléculas de água para formar · OH, e ao mesmo tempo, os elétrons fotogerados são facilmente capturados pelas substâncias oxidantes ou outras substâncias ativas para produzir O 2 · - . O 2 · - e · OH tem alta eficiência de oxidação e excelentes atividades químicas, que podem oxidar a grande maioria dos corantes orgânicos. A síntese hierárquica de nanoflores Au @ CdS-CdS fornecerá uma nova perspectiva para o projeto racional e síntese controlada de nanoestruturas híbridas com altas propriedades fotocatalíticas.
Conclusão
Nanoflores hierárquicas de Au @ CdS-CdS foram preparadas com sucesso pelo método passo a passo. Nos nanohíbridos obtidos, os nanobastões de CdS foram cultivados epitaxialmente na superfície dos CSNs de Au @ CdS. As nanoflores Au @ CdS-CdS exibiram excelente atividade fotocatalítica em direção à degradação de R6G sob a irradiação de λ =400-780 nm e λ =600-780 nm, respectivamente. As nanoflores de Au @ CdS-CdS hierárquicas tinham três vantagens:primeiro, a heteroestrutura melhorou a separação e a transferência de pares elétron-buraco fotogerados; segundo, a estrutura hierárquica fornece mais locais de reação; e terceiro, a faixa de absorção expandida aumentou a capacidade de capturar luz. Além disso, propusemos um possível mecanismo para a síntese gradual de nanoflores de Au @ CdS-CdS, que poderia ser usado para preparar outros nanohíbridos semicondutores de metal com morfologia complexa para futuros campos de energia limpa e restauração ambiental.
Abreviações
- CSNs:
-
Nanoprticles core-shell
- Cys:
-
l-cisteína
- Cys / Cd 2+ :
-
l-cisteína-Cd 2+
- EDS:
-
Espectrômetro dispersivo de energia
- En:
-
Etilenodiamina
- FE-SEM:
-
Microscópio eletrônico de varredura de emissão de campo
- HR-TEM:
-
Microscópio eletrônico de transmissão de alta resolução
- NPs:
-
Nanopartículas
- PL:
-
Fotoluminescência
- TEM:
-
Microscopia eletrônica de transmissão
- UV-Vis:
-
Visível por ultravioleta
- XRD:
-
Difração de raios X
Nanomateriais
- Síntese fácil e propriedades ópticas de pequenos nanocristais de selênio e nanorods
- Composto Híbrido de Sílica Nanoestruturada / Ouro-Celulose Ligado Amino-POSS via Processo Sol-Gel e Suas Propriedades
- Síntese hidrotérmica de nanopartículas de In2O3 híbridos gêmeos heteroestruturas de ZnO de disco hexagonal para atividades fotocatalíticas aprimoradas e estabilidade
- Síntese de pontos quânticos de sulfeto de antimônio solúvel em água e suas propriedades fotoelétricas
- Síntese fácil de óxido de estanho mesoporoso semelhante a buraco de minhoca via auto-montagem induzida por evaporação e propriedades aprimoradas de detecção de gás
- Efeito do método de síntese de La1 - xSr x MnO3 nanopartículas de manganita em suas propriedades
- Síntese de um vaso de nanoplacas Cu2ZnSnSe4 e sua atividade fotocatalítica orientada por luz visível
- Síntese sonoquímica fácil de uma etapa e propriedades fotocatalíticas de compostos de pontos quânticos de grafeno / Ag3PO4
- Dependência da toxicidade das nanopartículas em suas propriedades físicas e químicas
- Tipos de metais e suas propriedades



