Síntese de nanopartículas de ouro usando extrato de Mimosa tenuiflora, avaliações de citotoxicidade, absorção celular e catálise
Resumo
A síntese de nanopartículas de ouro (AuNPs) com extratos vegetais tem ganhado grande interesse no campo da biomedicina devido a sua ampla variedade de aplicações na saúde. No presente trabalho, AuNPs foram sintetizados com Mimosa tenuiflora (Mt) extrato de casca em diferentes concentrações de precursores metálicos. O extrato de Mt foi obtido pela mistura da casca da árvore em etanol-água. A capacidade antioxidante do extrato foi avaliada por meio do ensaio de 2,2-difenil-1-picrilhidrazil e polifenol total. AuNPs foram caracterizados por microscopia eletrônica de transmissão, difração de raios-X, espectroscopia de infravermelho com transformada de Fourier e UV-Vis e espectrometria de fotoelétrons de raios-X para determinação do grupo funcional em sua superfície. AuMt (coloides formados por AuNPs e moléculas de Mt) apresentam formas múltiplas com tamanhos entre 20 e 200 nm. AuMt foram testados na degradação do azul de metileno em catálise homogênea adicionando borohidreto de sódio. Os menores NPs (AuMt1) têm um coeficiente de degradação de 0,008 / se atingem 50% de degradação em 190 s . A viabilidade celular e a citotoxicidade foram avaliadas em células endoteliais da veia umbilical humana (HUVEC), e um efeito citotóxico moderado foi encontrado em 24 e 48 h. No entanto, a toxicidade não se comporta de maneira dependente da dose. A internalização celular de AuMt em células HUVEC foi analisada por microscopia confocal de varredura a laser. Para AuMt1, pode-se observar que o material está disperso no citoplasma, enquanto que no AuMt2, o material está concentrado na periferia nuclear.
Introdução
A biossíntese de nanomateriais mediada por plantas é um método ecologicamente correto que permite a síntese de NP em um único vaso. Isso porque os mesmos agentes bio-redutores dos extratos vegetais atuam como estabilizadores das partículas formadas com baixo índice de compostos tóxicos [1,2,3]. Nesse sentido, Mimosa tenuiflora A casca (Mt) possui alto teor de taninos condensados que possuem uma estrutura de quatro unidades de flavonóides [4], saponinas, glicose, alcalóides ( N , N -dimetiltriptamina) e amido [5,6,7,8]. Esses compostos (taninos condensados) podem atuar como agentes redutores de íons metálicos, mas, particularmente, o flavonóide tem sido associado à complexação de metais [4].
O extrato etanólico de Mt tem sido usado como agente antibacteriano para Gram negativos, Gram positivos e leveduras [9]. Também, como antiprotozoário (utilizando flavonóides de folhas e flores do Monte) [10] e na regeneração da pele [6]. Além disso, tem potencial para curar úlceras cutâneas graves, cujas propriedades foram atribuídas às moléculas e polifenóis da casca do Mt [11]. Extratos vegetais apresentam propriedades como antioxidantes e, particularmente, contêm polifenóis que são usados na síntese verde de NPs metálicos, como Au, Ag, Fe, Pt, Pd, Cu, suas ligas e óxidos [12, 13]. As propriedades ópticas dos sistemas NP, como a frequência de ressonância da ressonância plasmônica de superfície (SPR), são dependentes não apenas das características intrínsecas dos nanomateriais (tamanho, forma, constante dielétrica), mas também das propriedades do ambiente que circundam os NPs, como o solvente onde eles estão dispersas ou natureza das moléculas estabilizadoras, que abrangem as NPs. Esses parâmetros são decisivos para definir a posição de pico da SPR em sistemas NP [14,15,16].
Por outro lado, as propriedades catalíticas AuNPs têm sido relatadas em diversos trabalhos, relacionadas à degradação de compostos orgânicos como pesticidas, compostos fenólicos e corantes [17,18,19] e são usados em processos catalíticos relacionados à remediação ambiental, por exemplo, como limpeza de água contaminada [20]. Vários relatórios surgiram nos últimos anos sobre AuNPs sintetizados com extratos de plantas como cardamomo preto [21] e avaliações da atividade catalítica na degradação de corantes usados na indústria, como azul de metileno (MB) [22], laranja de metila [19] ou rodamina B [23]. No entanto, na direção oposta, alguns trabalhos relataram que NPs revestidos com moléculas de estabilização mostraram baixa atividade catalítica devido aos locais disponíveis para catálise na superfície de NP que foram ocupados por moléculas orgânicas [24, 25]. Além disso, AuNPs têm sido usados como sensores moleculares, como detecção colorimétrica de íons metálicos tóxicos [7] e aplicações teragnósticas (terapêuticas e diagnósticas) [26].
AuNPs funcionalizados com moléculas na superfície mostram propriedades ópticas e biológicas associadas à composição, espessura, organização e conformação que definem suas características [27]. A nanotecnologia tem vários desafios, como a agregação de AuNPs na corrente sanguínea [28]. AuNPs em concentração inferior a 20 μg / mL e com tamanho em torno de 20 nm não apresentam efeitos citotóxicos em linhagens de células saudáveis e cancerosas, e seu uso tem permitido analisar a interação entre NPs e células [13, 29, 30]. Então, a nanotecnologia oferece a possibilidade de interagir na mesma escala de receptores celulares [31] que permitem aprender sobre processos celulares [32, 33] e propriedades antimicrobianas [34], por exemplo, no estresse oxidativo que gera uma cascata de sinalização para efeitos diferentes, como citotoxicidade ou resposta de defesa antioxidante [35]. Além disso, AuNPs funcionalizados atuam como veículos transportadores de drogas, genes ou proteínas [36] e aplicações biomédicas [37, 38]. Ainda mais, ligantes AuNPs como proteínas e polímeros geram um ambiente químico que favorece a internalização de NPs para atingir o citoplasma, núcleo, ou manter fora da membrana [39].
Neste trabalho, AuNPs foram sintetizados usando um rico extrato polifenólico de casca de Mt. A citotoxicidade de AuMt foi avaliada em células HUVEC, e a internalização celular foi monitorada por microscopia confocal em 24 h. Atividade catalítica AuMt na degradação de MB, na presença de boro-hidreto de sódio (NaBH 4 ) à temperatura ambiente. Nossos resultados foram comparados com relação a trabalhos semelhantes de catálise com AuNPs sintetizados por métodos “verdes”.
Materiais e métodos
Materiais e produtos químicos
Para a síntese de AuMt, 15 g de casca de árvore Mt foram cortados em pedaços e colocados em um frasco de 100 mL. Adicionou-se 70 mililitros de etanol (Fermont, 99% puro) e 30 mL de água ultrapura (18 MΩ, Millipore), que foi coberto com alumínio e deixado em temperatura ambiente por 15 dias. A solução foi filtrada com papel filtro Whatman (8 μm) e posteriormente com um acrodisco (0,20 μm). A solução obtida foi utilizada como agente redutor (extrato de Mt) para a síntese de AuMt. Uma porção do filtrado foi rotoevaporado e então liofilizado para DPPH e ensaio de polifenol total e para construir uma curva de calibração do extrato de Mt. A concentração do extrato Mt foi de 32,5 mg / mL, determinada a partir de uma curva de calibração. Ácido tetracloroáurico (HAuCl 4 , Sigma-Aldrich 99% puro) foi usado como um precursor metálico. As concentrações de precursores usados na síntese foram de 5,3 mM para AuMt1 e 2,6 mM para AuMt2. O volume do agente redutor foi mantido constante (1,6 mL), e o volume total da amostra foi completado até 6 mL com água ultrapura. Arquivo adicional 1:A Tabela S1 mostra as formulações usadas na síntese de AuMt1 e AuMt2, bem como os valores de pH para cada reagente. A síntese foi realizada a 25 ° C sob condições de iluminação de laboratório. O protocolo utilizado foi o seguinte. Em um tubo de 50 mL, adiciona-se a solução do extrato de Mt seguida da água ultrapura e, por fim, a solução do precursor de ouro, agitando imediatamente no vórtice a 3000 rpm por 10 s. A síntese dos AuMtNPs foi confirmada visualmente em poucos minutos pela mudança na coloração da mistura. O processo de limpeza de NPs consiste na centrifugação da suspensão a 14.000 rpm por 1 h, descartando o sobrenadante, adicionando água e dispersando por sonicação, repetindo o processo duas vezes. Depois de adicionar etanol, AuMt são dispersos novamente por sonicação e centrifugados a 14.000 rpm por 1 h. O sobrenadante é descartado e precipitado e é seco em estufa à temperatura de 40 ° C. Em seguida, o nanocompósito obtido é composto por AuNPs com moléculas de extrato Mt na superfície.
Mudança de pH dependente do tempo da síntese AuMtNP
O pH da síntese de AuMtNP foi medido conforme a reação foi realizada. Para isso, foi utilizado um medidor de bancada multiparâmetro de pH / condutividade (Orion ™ VERSA STAR ™). O instrumento foi calibrado a 25 ° C usando uma solução padrão de referência tampão para calibração em pH =4,01. Um banho de recirculação foi utilizado para controlar a temperatura das amostras a 25 ° C (± 0,1 ° C) em todas as medições. O pH foi medido enquanto a reação foi realizada por 180 s imediatamente após a mistura dos reagentes. O mesmo dispositivo foi usado na medição do pH dos reagentes.
Espectro UV-Vis, 2,2-difenil-1-picrilhidrazil (DPPH) e Ensaio de polifenol total
Um espectrômetro Perkin-Elmer Lambda 40 UV / Vis de feixe duplo foi usado para obter o espectro de UV-Vis do extrato, em uma faixa de medição de 200-400 nm, com uma taxa de varredura de 240 nm / min. AuMt SPR foi monitorado entre 250 e 875 nm.
A cinética de formação de AuMt foi determinada medindo a absorbância a 550 nm a cada segundo enquanto a reação de síntese NP foi desenvolvida dentro da célula de quartzo sob agitação magnética.
Para os ensaios DPPH, todos os testes foram feitos em triplicata. Diferentes concentrações de extrato de Mt (25, 12,5, 6,25 e 3,125 μg / mL) foram testadas. Cem microlitros de etanol foram adicionados a 100 μL de cada concentração, além da solução de DPPH (300 μM). Posteriormente, as amostras foram incubadas por 2 h no escuro antes de medir a absorbância a 517 nm. Os resultados foram comparados com vitamina C e catequinas (70 μmol / L), e ambas as moléculas foram utilizadas como controle. Para a atividade de eliminação, o radical DPPH dissolvido em etanol foi usado como um branco [40, 41]. A porcentagem da atividade de eliminação foi calculada com a Eq. (1).
$$ \% \ mathrm {Eliminação} \ \ mathrm {activity} =\ left [\ left (1- \ mathrm {A} \ \ mathrm {sample} \ right) / \ mathrm {A} \ \ mathrm {control} \ right] \ times 100 $$ (1)
onde Uma amostra é a absorbância da amostra e A controle é a absorbância do branco. Os dados foram analisados por meio de análise de variância (ANOVA) com testes de comparação múltipla de Tukey.
Para o ensaio de polifenol total, as mesmas concentrações foram usadas adicionando Folin-Ciocalteu a 0,25 N e carbonato de sódio a 5% com incubação de 1 hora na ausência de luz. A absorvância foi medida a 750 nm. Os resultados são expressos como equivalentes de ácido gálico [42, 43].
Potencial Zeta e determinação do tamanho DLS
O potencial zeta (ζ) de NPs foi medido com Zetasizer NS (Malvern, PA), e os tamanhos foram medidos por espalhamento dinâmico de luz (DLS) de Zetasizer NS (resolução de 0,5 nm). O instrumento calcula o ζ determinando a mobilidade eletroforética ( μ e ) usando Henry Eq. (2) [44]:
$$ {\ mu} _e =\ frac {2 \ varepsilon \ zeta f (ka)} {3 \ eta} $$ (2)
onde ε , η , e f (ka) denotam a constante dielétrica da mídia, a viscosidade da mídia e a função de Henry, respectivamente. Dois valores são geralmente usados como aproximações para o f (ka) determinação, 1,5 ou 1,0. As determinações eletroforéticas de ζ são as mais comumente feitas em um solvente aquoso e concentração moderada de eletrólito. f (ka), neste caso, assume o valor de 1,5 e é referido como a aproximação de Smoluchowski clássica, Eq. (3) [45].
$$ {\ mu} _e =\ varepsilon \ frac {\ upzeta} {\ upeta} $$ (3)
As amostras foram colocadas em uma célula capilar dobrada em forma de U para ζ Medidas. Cada amostra foi medida à temperatura ambiente (25 ° C) em triplicado.
Avaliação da estabilidade NP em meio de cultura suplementado (s-DMEM)
A estabilidade do AuMtNP foi avaliada em s-DMEM por DLS e ζ . O diâmetro hidrodinâmico (2R H ) de AuMt1 e AuMt2 foi medido a 37 ° C em água ultrapura e s-DMEM em concentrações entre 25 e 200 μg / mL. Para AuMt1 e AuMt2 em s-DMEM, ζ foi medido a 37 ° C para estabelecer se o meio de cultura modifica a carga superficial de NP. As nanopartículas foram adicionadas a um tubo Eppendorf com s-DMEM previamente termalizado e agitadas em vórtice a 3000 rpm por 30 s. A incubação a 37 ° C é mantida por 15 min antes de fazer as medições na mesma temperatura.
Espectroscopia de infravermelho com transformada de Fourier (FTIR)
O extrato de Mt e o AuMt FTIR foram obtidos por um Perkin-Elmer Frontier FTIR usando uma amostra sólida. O espectro foi obtido no modo de transmitância a uma resolução de 2 cm - 1 , de 4500 a 500 cm −1 .
Espectroscopia de fotoelétrons de raios-X (XPS)
O experimento XPS foi realizado usando um Perkin-Elmer (Modelo PHI 5100, resolução baseada no FWHM do Ag3d5 / 2 pico 0,80 eV, ânodo padrão duplo de fonte XR (Mg / Al) e 15 kV, 300 W, 20 mA ) As análises de varredura de pesquisa foram realizadas com uma taxa de varredura de 0,5 eV / s. Para análises de alta resolução, foi utilizada uma taxa de varredura de 0,025 eV / s.
Microscopia Eletrônica de Transmissão (TEM)
Para TEM, 10 μL da amostra foram depositados em grades de cobre cobertas com um filme de carbono fomvar (Eletron Microscopy Sciences, 300 Mesh). As grades são deixadas para secar por 1 he colocadas em uma câmara de vácuo por 12 h. O equipamento de microscopia eletrônica é um Jeol 2010 F de emissão de campo operado a 200 keV. A espectroscopia de energia dispersiva de raios-X (EDS) é um detector Bruker Quantax 200, resfriado peltier e acoplado ao sistema TEM. Espaçamentos interplanares de planos de cristal revelados por TEM de alta resolução (HRTEM) foram determinados por análise digital de micrografia (versão 3.0 Gatan).
Difração de raios-X
Os dados foram coletados usando um sistema de difratômetro Bruker D8 QUEST, equipado com um monocromador de espelho de multicamadas e um tubo selado CuKα Microfocus ( λ =1,54178 Å). As molduras foram coletadas em T =300 K por meio de varreduras.
Efeito Citotóxico AuMt
O efeito citotóxico de AuMt foi avaliado em células HUVEC usando ensaio de brometo de 3- (4,5-dimetiltiazolil-2) -2,5-difeniltetrazólio (MTT). As células foram cultivadas em meio Eagle modificado por Dulbecco (DMEM, Sigma-Aldrich), suplementado com 10% de soro fetal bovino (GibcoBRL) a 37 ° C e 5% de CO 2 . As células HUVEC foram contadas em câmara de Neubauer, e a viabilidade foi determinada pelo teste de exclusão com azul de tripano (Sigma-Aldrich).
Para o ensaio de MTT, as células foram ajustadas para 100.000 células / mL e 100 μL por poço foram colocados em placas de 96 poços. AuMt1 e AuMt2 foram avaliados nas concentrações de 200, 100, 50 e 25 μg / mL. As células tratadas foram incubadas por 24 e 48 h a 37 ° C, 5% de CO 2 . Após o tempo de incubação, a placa foi lavada com solução salina tamponada com fosfato (PBS) e solução de MTT foi adicionada e incubada por 4 h. Dimetilsulfóxido (DMSO) foi adicionado para dissolver cristais de MTT. A absorvância foi medida a 570 nm em um leitor de placas multimodo (Synergy HTX, BioTek), usando o software Gen5. A viabilidade celular foi calculada usando a Eq. (4):
$$ \ mathrm {Cell} \ \ mathrm {viability} =\ left (\ mathrm {A} \ \ mathrm {sample} / \ mathrm {A} \ \ mathrm {control} \ right) \ times 100 \% $$ (4)
onde Uma amostra é a absorbância da amostra e A controle é a absorvância do branco [46, 47].
Análise estatística
Os dados são expressos como médias ± desvios padrão (DP). As diferenças significativas entre os grupos foram analisadas pelo teste de Tukey, ANOVA de um fator, conforme apropriado. P valores inferiores a 0,05 foram considerados estatisticamente significativos. O software Origin Pro 9.1 é usado para gerenciamento de dados, análise estatística e geração de gráficos. Os sinais usados são * p <0,05. O desempenho com o tratamento (AuMt1 e AuMt2) e o grupo controle por 24 e 48 h foi comparado.
Para o ensaio vivo / morto, as células HUVEC foram semeadas em lâminas de vidro e tratadas com AuMt1 e AuMt2. Após 24 horas de lâminas de incubação, estas foram coradas usando kit de viabilidade / citotoxicidade viva / morta (ThermoFisher) sob a recomendação do fabricante. As amostras foram observadas por microscopia confocal de varredura a laser (CLSM800, Carl Zeiss).
Microscopia de varredura a laser confocal:Fluorescência de AuMt
A análise de microscopia confocal foi realizada em um dispositivo LSM 800 (Carl Zeiss, Jena Germany) montado em um microscópio invertido Axio Observer.Z1 (Carl Zeiss, Jena Germany). Três lasers de 405, 488 e 640 nm, com uma respectiva potência máxima de 5, 10 e 5 mW, foram usados para o estudo. A fluorescência foi coletada usando detectores GaAsP altamente sensíveis. Imagens de campo claro foram obtidas por uma coleção de luz de laser transmitida em Photo Multiplier Tube (PMT). Para fluorescência AuMt, ensaio vivo / morto e distribuição de NP no estudo de células HUVEC, foi usada uma objetiva seca Plan-Apochromatic × 40 / 0,95. Para células de reconstrução 3D com AuMt, uma objetiva de óleo Plan-Aprochromatic × 63 / 1,40 foi usada.
Para a caracterização da fluorescência AuMt, uma gota de 20 μL de dispersão coloidal NP foi depositada em uma lamínula e seca em temperatura ambiente antes da análise por CLSM. Um laser de 640 nm foi empregado como fonte de excitação a 0,5% da potência, e a fluorescência foi coletada entre 650 e 670 nm. Imagens de AuMt de campo claro foram formadas usando um laser de 488 nm (0,2% da potência) no modo de luz transmitida. A fluorescência e o campo claro foram coletados em trilhas separadas.
Internalização celular
Para internalização de AuMt em células HUVEC, o núcleo foi corado com 4 ′, 6-diamidino-2-fenilindol (DAPI) e as fibras de actina com anticorpo anti-β actina acoplado a fluoresceína-5-isotiocinato (FITC) para delimitar a fronteira celular . DAPI estava animado com um laser de 405 nm a 1,0% da potência e FITC com um laser de 488 nm a 0,20%. As emissões de DAPI e anticorpo anti-β actina foram coletadas entre 410 e 500 nm e 500-700 nm, respectivamente. AuMt foi excitado com um laser de 640 nm (0,50% de potência), e a emissão foi coletada entre 650 e 700 nm.
Reconstruções de células 3D AuMt e projeções ortogonais foram feitas a partir de 30 imagens no modo Z-stack (total Z comprimento =8 μm), coleta de fluorescência de DAPI, FITC e AuMt conforme descrito acima. Os sinais fluorescentes foram coletados em trilhas separadas para cada Z posição. Para maior clareza, o sinal FITC foi omitido em uma reconstrução 3D.
Uma comparação relativa da absorção celular de nanopartículas foi realizada. Para isso, a intensidade média de fluorescência de AuMt1 e AuMt2 em células HUVEC foi determinada a partir da análise de imagens confocais usando o software ImageJ [48].
Catálise
Atividade catalítica em MB, a uma concentração de 3,33 × 10 −5 M, foi analisado por espectroscopia UV-Vis. Na catálise homogênea, 90 μL de NPs (2 mg / mL) foram adicionados diretamente na célula de quartzo que contém MB e 200 μL de NaBH 4 a uma concentração de 100 mM. A amostra foi homogeneizada por agitação magnética dentro da célula do espectrofotômetro. A reação foi realizada a 25 ° C.
Resultados e discussões
Síntese
Por inspeção visual, foi detectado que a síntese de NPs é muito rápida em ambos os sistemas. A cor mais intensa do sistema AuMt1 mostrado na inserção do arquivo adicional 1:A Figura S1 indica um conteúdo mais alto de NPs desta síntese. Isso ocorre porque AuMt1 tem uma concentração dupla de precursor metálico em comparação com AuMt2. No arquivo adicional 1:Tabela S1, os reagentes usados na síntese de nanopartículas têm pH ácido. Arquivo adicional 1:A Figura S1 mostra as mudanças no pH das reações conforme as sínteses de AuMtNPs são realizadas. As reações começam em um ambiente ácido (pH <2,65) e, à medida que a síntese de NPs se desenvolve, a acidez aumenta. Isso se deve à desprotonação de grupos hidroxila presentes nas moléculas polifenólicas do extrato de Mt. Na verdade, esta é a primeira etapa de um processo de redução de óxido que resulta na transferência de elétrons do grupo hidroxila desprotonado para Au 3+ íons. Como produtos da reação de redução de óxido, Au 3+ íons são reduzidos a átomos de metal Au 0 e o anel polifenólico que contribui com 2 elétrons é oxidado. O processo é descrito na inserção do arquivo Adicional 1:Figura S1.
Ensaios UV-Vis Spectra, DPPH e Polifenol Total
O espectro UV-Vis do extrato de casca de Mt é mostrado na Fig. 1a, onde o sinal consiste em uma banda bem definida com um máximo em 280 nm e largura de 50 nm. Este espectro é muito semelhante ao relatado para Rumex hymenosepalus extrato de raiz, que possui alto teor de compostos polifenólicos [49]. Determinar o conteúdo polifenólico no extrato de casca de Mt é importante porque essas moléculas podem contribuir significativamente como agentes redutores na síntese de AuNPs, fornecendo os elétrons necessários para a redução de Au 3+ íon para ouro metálico (Au 0 ) Uma vez que os NPs são formados, os compostos polifenólicos são absorvidos em sua superfície, proporcionando estabilidade aos nanomateriais.
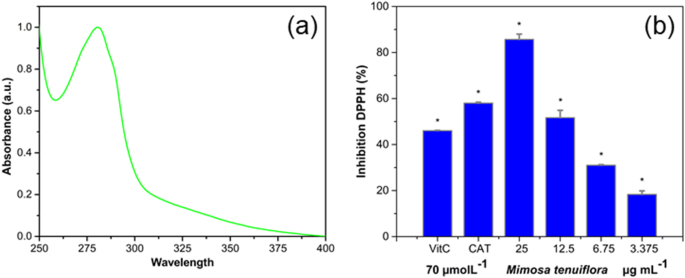
Caracterização do Extrato do Monte. a Espectro de UV-Vis de extrato Mt e b Inibição de DPPH com análise ANOVA unilateral (* p <0,05)
Para o ensaio DPPH, observou-se que para 12,5 mg / L de extrato de Mt, obtivemos 50% de inibição (L50), semelhantes aos valores relatados para Vitamina C e catequinas (46 e 58%, respectivamente). Isso indica que o extrato de Mt possui uma capacidade antioxidante muito semelhante aos compostos puros usados como controle, Fig. 1b onde diferenças significativas (* p <0,05) dos valores de controle são marcados com um asterisco. O valor de 425 mg / g obtido no ensaio de polifenóis totais indica que quase metade da massa extraída é equivalente ao ácido gálico. A alta capacidade antioxidante e o alto conteúdo polifenólico no extrato de Mt sugerem que ele pode ser usado como um bom agente redutor e estabilizador da síntese de nanomateriais no âmbito da química sustentável [50, 51].
Caracterização
Cinética de formação e UV-Vis Spectra AuMt
A Figura 2a mostra uma evolução temporal da absorbância em um pico SPR de AuNPs (550 e 560 nm para AuMt1 e AuMt2, respectivamente) conforme ocorre a reação de síntese de nanomateriais. Os dados experimentais são ajustados com a função sigmoidal de Boltzmann [52], onde pelo menos três estágios de crescimento são observados. No primeiro, a absorbância cresce lentamente no início da reação de síntese quando Au 3+ íons são reduzidos a Au 0 e formam agregados de alguns átomos que se unem para formar pequenos NPs. No segundo estágio, os pequenos NPs aumentam de tamanho por crescimento autocatalítico e a absorbância cresce de forma rápida. No último estágio, na recristalização NP, a absorbância atinge sua fase estacionária. Como pode ser visto na Fig. 2, uma absorbância máxima é atingida em 60 s para AuMt1 e 120 s para AuMt2. Curiosamente, o primeiro estágio de crescimento é de 20 s para AuMt1, enquanto é quase nulo (menos de 1 s) para AuMt2, o que é explicado pela maior proporção de moléculas redutoras (extrato de Mt) em relação ao precursor metálico. Isso favorece a formação rápida do núcleo em NPs de AuMt2 em relação a AuMt1; no entanto, o próximo estágio de crescimento dos NPs é baixo para AuMt2, e NPs com tamanho maior são obtidos. Foi relatado que a síntese de AuNPs, usando maltose e tween80 como estabilizador, mostra uma cinética de crescimento com um tempo de reação muito semelhante ao relatado neste trabalho [53]. Em outro relatório de síntese verde [54], é apontado que a menor proporção de agentes redutores / precursores gera NPs de menor tamanho.
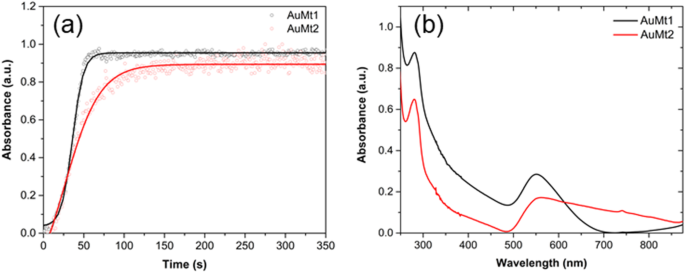
Caracterização por UV-Vis de AuMt1 e AuMt2. a Formação cinética e b Espectro UV-Vis
A Figura 2b mostra os espectros de absorção característicos de AuMt na região compreendida de 250-875 nm. SPR para AuMt1 mostra uma banda simétrica com uma absorção máxima em 550 nm e ampla de 200 nm. O pico do plasmon AuMt2 sofre um ligeiro desvio para o vermelho localizado agora em 560 nm com uma banda assimétrica e uma largura maior que 300 nm, que é devido à diferença de tamanhos entre os dois nanomateriais (d AuMt1
Tamanho, potencial Zeta e estabilidade de AuMtNPs
Os tamanhos do AuMtNP por DLS e potencial Z foram testados em diferentes condições para uma concentração (50 μg / mL), conforme mostrado na Tabela 1. AuMt1 e AuMt2 mostraram altos valores negativos (≤ 30 mV) em água, o que favorece a estabilidade eletrostática de ambas as nanopartículas sistemas. De acordo com Qu et al. [56], ζ o valor aumenta gradualmente com o tamanho do NP; em nosso caso, AuMt1 tem um tamanho menor do que AuMt2 em água, um tamanho que é controlado pela síntese NP. Esses valores de tamanho correspondem a NP ζ valores, sendo os maiores ζ corresponde ao tamanho NP maior. Potenciais Zeta ( ζ ) de AuMtNPs dispersos em s-DMEM mostram valores menos negativos em relação aos obtidos em água ultrapura (Tabela 1). Esta redução pode ser atribuída aos cátions presentes no DMEM e nas proteínas presentes no FBS que cobrem as superfícies do AuMtNP que causam uma diminuição nas interações eletrostáticas. Apesar disso ζ redução, o valor permanece próximo a - 25 mV para ambos os sistemas, o que indica que as nanopartículas preservam sua estabilidade eletrostática após a incubação de s-DMEM [57]. Além disso, a Tabela 1 mostra os resultados obtidos por DLS para diâmetros hidrodinâmicos AuMtNP (2R H ) medido a 37 ° C em água ultrapura e meio de cultura. No s-DMEM, o tamanho de ambos os sistemas aumentou devido à adsorção de proteínas na superfície das nanopartículas [58]. Para AuMt1, o crescimento de 2R H devido à proteína corona é 33,8 nm e para AuMt2 é 42,9 nm. Espera-se que quanto maior o tamanho das nanopartículas, maior do que a superfície para absorção de proteínas [59]. Isso pode explicar o valor um pouco menor em ζ para AuMt2 em comparação com AuMt1 em s-DMEM. Para AuMt1 e AuMt2, a interação com as proteínas s-DMEM se deve às moléculas do extrato que se fixam na superfície das nanopartículas. Essas moléculas diferem ligeiramente entre AuMt1 e AuMt2, conforme mostrado nos resultados de XPS. Também medimos o pH de soluções na mesma faixa de concentração. Verificou-se que não há alteração do pH e cujo valor médio ficou em torno de 7,5 para AuMt tanto na água ultrapura quanto 7,2 no s-DMEM (Tabela 1).
Arquivo adicional 1:A Figura S2 mostra os diâmetros hidrodinâmicos do AuMtNP quando disperso em água ultrapura e s-DMEM a 37 ° C, em uma faixa de concentração entre 25 e 200 μg / mL. Para cada sistema estudado, o diâmetro hidrodinâmico não muda com a concentração de nanopartículas, e apenas para AuMt2 s-DMEM a 100 μg / mL, o tamanho de partícula aumenta em relação à menor concentração avaliada, o que pode indicar processos de agregação de NP nessas concentrações [32].
Espectroscopia de infravermelho com transformada de Fourier (FTIR)
O espectro de FTIR, mostrado na Fig. 3, corresponde ao extrato de Mt, AuMt1 e AuMt2. As bandas largas características centradas em torno de 3250 cm −1 estão associados com OH fenólico principalmente de taninos e flavonóides. Picos a 1594 cm −1 correspondem à vibração de flexão N-H, em 1705 cm −1 ao trecho acíclico da cetona e região entre 1000 e 1300 cm −1 para alongamento C – O. Picos na faixa de 1600 a 500 cm −1 são identificados com polifenóis, sinais em 1235 e 1160 cm −1 estão relacionados com o alongamento da ligação C – O aromática e a 1020 cm −1 para alongamento de banda C – O alifático e em 1235 cm −1 estão especificamente relacionados com a característica da natureza cíclica do éter. Esses sinais podem ser associados aos compostos mais abundantes no extrato de Mt como tanino de Mimosa, flavona sakuranetina, saponinas triterpenóides, chalconas e N , N alcalóide -dimetiltriptamina (arquivo adicional 1:Figura S3). As amostras AuMt1 e AuMt2 apresentam os mesmos picos característicos na região dos polifenóis, confirmando que os NPs são estabilizados pelas moléculas do extrato Mt [60]. Observamos uma mudança de 1331 cm −1 na banda de largura e uma diminuição na intensidade do pico para o AuMt1 e AuMt2 corresponde à ligação entre AuNPs e grupo C-H de polifenóis; 1723 cm −1 é deslocado pela oxidação de compostos polifenólicos em compostos carboxílicos durante a redução de Au 3+ para Au 0 [51, 61, 62].
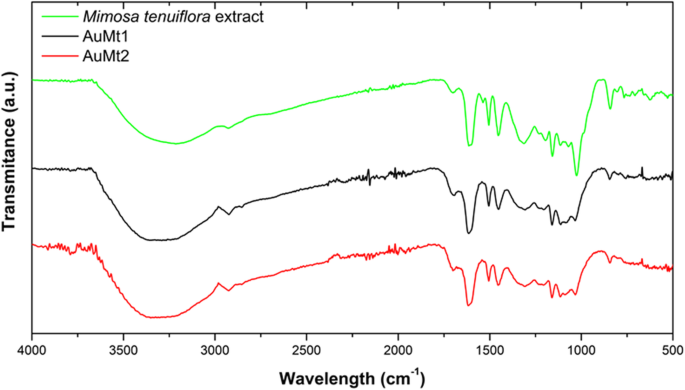
Espectros de FTIR. Extrato Mt (verde), AuMt1 (preto) e AuMt2 (vermelho)
Espectroscopia de fotoelétrons de raios-X (XPS)
Na análise de varredura de pesquisa XPS para AuMt1 e AuMt2, as amostras mostraram claramente a presença de oxigênio (O 1 s ), carbono (C 1 s ) e ouro (Au 4 f ), cujos picos estão centrados em torno de 532, 284 e 85 eV, respectivamente, como mostrado na Fig. 4a, b. Experimentos XPS de alta resolução foram feitos para estabelecer uma abundância relativa de diferentes grupos funcionais de moléculas que revestem as superfícies de AuNP. Au4 f os espectros XPS de alta resolução para AuMt1 e AuMt2 consistem em dois picos simétricos separados por 3,7 eV (Fig. 4b, e). Picos associados a 4 f 5/2 o acoplamento spin-orbital está localizado na energia de ligação (BE) de 88,6 e 87,7 eV para AuMt1 e AuMt2, respectivamente. Para 4 f 7/2, os picos de acoplamento spin-orbital estão localizados em 84,9 e 84,0 eV. The link of intensities (I4f 2/7 > I4f 5/2 ) and location and separation (ΔBE = 3.7 eV) between peaks confirm that gold ions (Au 3+ ) are reduced completely to metallic gold Au 0 [63]. Au4f signals, for AuMt1, are slightly shifted (~ 0.9 eV) at higher energies with respect to sample AuMt2. This can be explained in terms of NP size differences between samples. AuMt1 has a half population of NPs with size less to 40 nm, while AuMt2 NPs have a mean diameter of 150 nm, determined by TEM. Peak shift for Au4f signals, due to the presence of small NPs, has been reported by other authors who relate the Au4f BE increase with decreasing NP size [64, 65]. Also, the shift effect could be due to the interaction of functional groups capped on surfaces of AuNPs [66]. In Fig. 4c, f, the high-resolution XPS spectra of C1s are shown for AuMt1 and AuMt2. Spectra were deconvoluted by 3 Gaussian bands associated with C=O, C–O, and C–C or C=C. For AuMt1, peaks are centered on 286.9, 286.1, and 284.5 eV, for AuMt2 on 287.0, 286.3, and 284.7 eV, respectively. Comparing the experimental XPS curves for C 1s , we see appreciable differences between AuMt1 and AuMt2. The main difference comes from a significant decrease in AuMt1 of the signal associated with C–O group. Comparing the percentage contributions of each group, obtained from the deconvolutions (Additional file 1:Table S2), we see that in AuMt2 contribution of C–O signal is 27.8% while in AuMt1 is 16.6%. This difference can be explained in terms of the oxide-reduction reaction that gives rise to the process of AuNP formation. The synthesis of AuMt1 is added twice the metal precursor (HAuCl4 is 0.01 M) than in synthesis of AuMt2. In both cases, the same amount of extract is used as a reducing agent, so in AuMt1, more hydroxyl groups (−C–OH) are consumed to reduce a greater number of Au 3+ íons. Thus, a decrease of C–O signal in AuMt1 confirms that hydroxyl groups participate in the synthesis reaction. High-resolution XPS of O 1s revealed that carbonyl C=O is the most abundant group (Additional file 1:Figure S4 and Table S2). In addition, the content of the C=O group is higher in the AuMt1 sample, which confirms what was previously discussed.
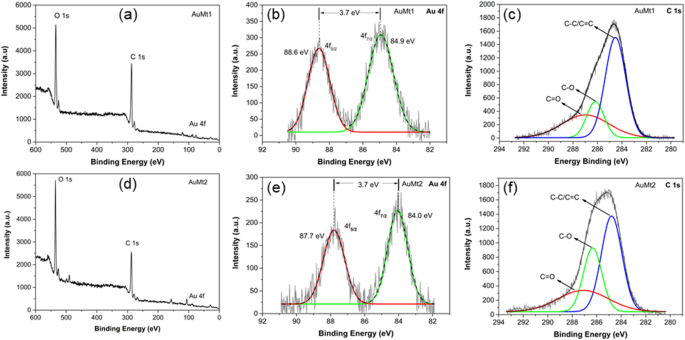
XPS spectra of AuMt1 and AuMt2. a , d Survey spectra, b , e Au4f high resolution, and c , f C1s alta resolução
XPS and FTIR indicate that AuMtNPs interact mainly with carbonyl groups (ketones) in addition to hydroxyl groups of Mimosa tannins, saponins, and other molecules that participate in the reduction of Au 3+ para Au 0 and stabilization of AuMtNPs [63, 67, 68].
Transmission Electron Microscopy
AuMt1 TEM micrographs are shown in Fig. 5a, b and AuMt2 in Fig. 5d, e showing products’ shape distribution. AuMt1 has the biggest diversity in shapes. AuMt shape is determined by the relationship between the variation of metal precursor concentration and Mt extract at a fixed concentration. In this case, NPs were observed without cleaning the extract to observe the interaction that forms around the AuMt. As observed in the micrographs, an extract is placed on the surface; however, NPs are kept dispersed and no aggregation is shown. Figure 5c, f show size distribution for each sample, and AuMt1 have an average size dispersion of 40 nm and AuMt2 of 150 nm.
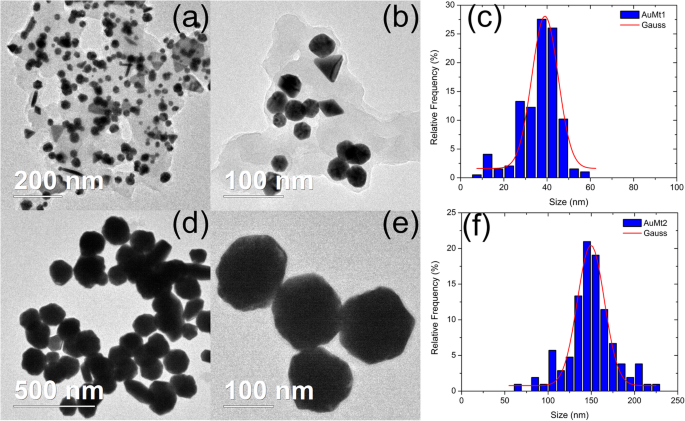
Size distributions by TEM. a , b , c AuMt1 and d , e , f AuMt2
In Fig. 6a, AuMt TEM micrographs were also analyzed by EDS (Fig. 6b), which showed Au presence. Other chemical elements such as Cl, O, and Ca, on EDS spectrum, come from the extract that surrounds NPs. According to the crystallographic tab (JCPDS file:04-0784), the obtained distances between 2.35 and 2.03 Å (Fig. 6c) correspond to Au crystalline planes (111) and (200).
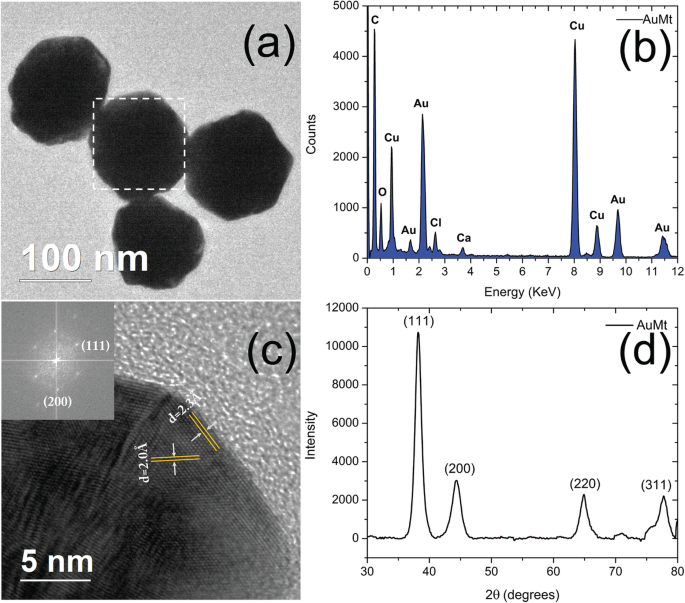
Nanostructural characterization of AuMt. a TEM, b EDS, c single HRTEM, and FFT and d XRD
X-ray Diffraction (XRD)
Figure 6d shows the characteristic AuMt XRD diffraction peak at 2Ɵ , which are in 38.17, 44.37, 64.81, and 77.66 o corresponding with the planes (111), (200), (220), and (311), respectively; these planes correspond with the face-centered cubic Au (space group Fm 3 m, JCPDS File No. 89-3722). High Score Plus and Origin software were used for the analysis [69].
Biological Tests
Cytotoxicity by MTT and Live/Dead Assay
To evaluate AuMt1 and AuMt2 toxicity, tests were performed on HUVEC cells using MTT. Four concentrations and two times for both materials were evaluated. In Fig. 7a, it is observed that at 24 h for AuMt1, cell viability decreases between 10 and 20%, only in concentrations higher than 25 μg/mL. For AuMt2, a similar effect is obtained in cell viability; however, the concentration of 100 μg/mL seems to have no effect on these tests. In Fig. 7b, MTT tests at 48 h for AuMt1 and AuMt2 are shown. For AuMt1, it is easy to notice that concentration with the greatest effect is 50 μg/mL, where the viability drops almost 30% compared to the control. The concentration of 50 μg/mL seems to be the concentration with the highest toxic effect; however, when the obtained data were analyzed, it is found that there is no significant difference between the obtained data on 24 and 48 h, a similar result obtained for 100 and 200 μg/mL, Fig. 7c. For AuMt2, a toxic effect between 20 and 30% is observed only on 100 and 200 μg/mL, while 25 and 50 μg/mL show no significant difference, compared to the observed effect at 24 h, Fig. 7d. This seems to correlate with AuMt2 size growth in s-DMEM (Additional file 1:Figure S2) where at a concentration of 100 μg/mL, they begin to aggregate. In the work published by Chandran et al. [70], they used gold nanoparticles coated with branched polyethyleneimine (BPEI), lipoic acid (LA), and polyethylene glycol (PEG), where they see an important toxicity in HUVEC cells by nanoparticles coated with BPEI, which have sizes of 40 and 80 nm, where viability is between 20 and 30%. When these particles are covered with human serum proteins, it is found that toxicity decreases; this is due to the corona effect. Recently, Zhaleh et al. [71] have reported the biogenic synthesis of 40-nm gold nanoparticles using leaf extracts from Gundelia tournefortii L. plant. Interestingly and in contrast to our results, the authors indicate that MTT cell viability tests for these particles in HUVEC, the cell viability was 95% at 1000 μg/mL; however, they do not establish if the low cytotoxicity is due to the fact that there is no material internalization or if the particles are harmless due to protein corona. In this sense, bioreductive compounds present in Gundelia tournefortii L extract are different from those reported for Mimosa tenuiflora extract (Additional file 1:Figure S3). Thus, the interactions of these two nanoparticle systems with proteins present in FBS are very different, which may explain the differences in cytotoxic responses.
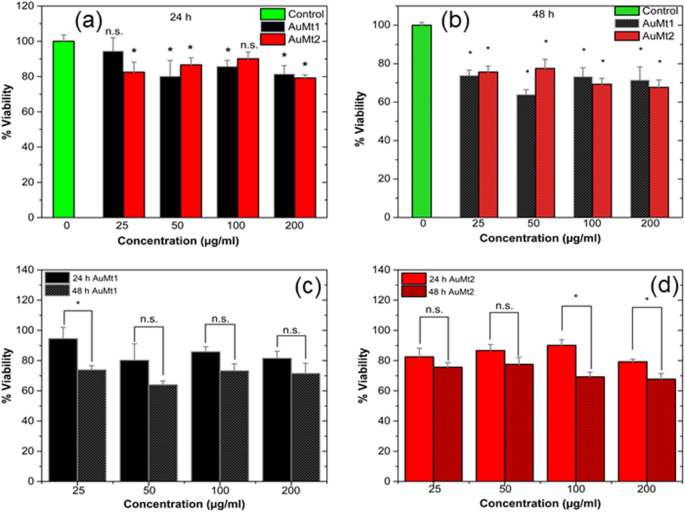
Viability assay using MTT in HUVEC cell. a For 24 h and b 48 h. 0ne-way ANOVA analysis with (*p <0,05). Comparison between 24 and 48 h for c AuMt1 and d AuMt2 with ANOVA analysis with Tukey tests (n.s. no significance and (*p < 0.05))
As mentioned above, AuMt1at a 50-μg/mL concentration shows the highest toxicity and cellular uptake. We believe that toxicity may be due to the fact that the nanomaterial has a low affinity to s-DMEM proteins, since it has only 16.6% of hydroxyl groups on the surface to promote hydrogen bonding with S-DMEM proteins. The fact that the material toxicity decreases as AuMt1 concentration increases may be due to a cellular detoxification response, like an exocytosis caused by high intracellular content of gold [70]. For AuMt2, the toxicity effect at 100 and 200 μg/mL may be due to nanomaterial agglomeration, which could be attaching to the membrane causing adverse effects for the cells; however, more experiments are required to confirm this hypothesis.
Only one concentration (50 μg/mL) was chosen to be evaluated by live/dead fluorescent dye; this is due to the purpose of confirming the MTT results and later analyzing the metallic NP internalization in HUVEC cells, avoiding a field saturation by NPs. When cells were stained with live/dead fluorescent dye kit, it was found that a large part of the cell population favorably marked for calcein and just a few for ethidium homodimer, indicating that cell culture is viable, as shown in Fig. 8.
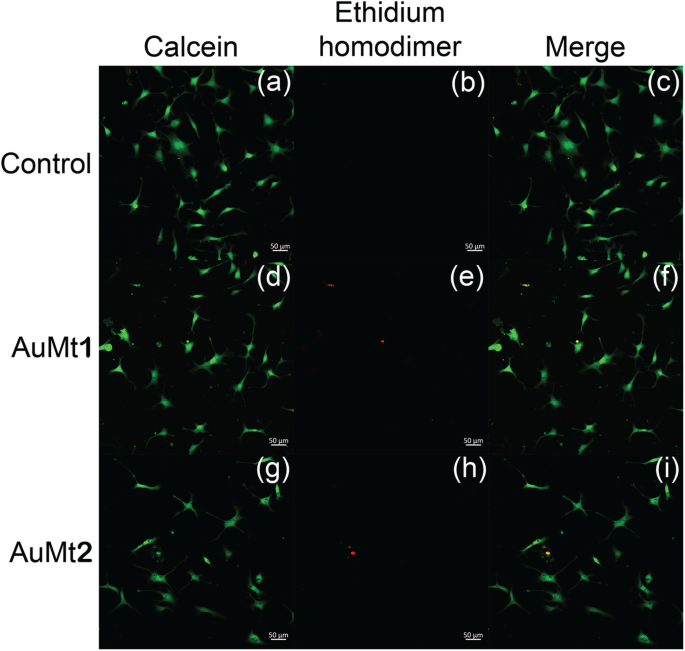
Live/dead assay in HUVEC cells. a , d , e g with calcein; b , e , e h with ethidium homodimer; e c , f , and i merge by confocal microscopy
Confocal Laser Scanning Microscopy:Fluorescence of AuMt
In Fig. 9a, d are shown micrographs of AuMt1 and AuMt2 in bright field and in Fig. 9b, e, their corresponding fluorescence, captured by confocal microscopy. Red fluorescence of AuMt (collected emission 650–700 nm) was excited employing 640 nm diode laser, and a mayor size of NPs can be appreciated in AuMt2 sample than AuMt1. In the merge images in Fig. 9c, f, it can be observed how the luminescence comes exclusively from the dark points associated with the NPs. This indicates that the cleaning process effectively removed the extract that is not complexed to the nanomaterial, so there is no background emission. It is interesting to observe that an intense fluorescence of the NPs captured by the confocal system is achieved at a very low excitation power of the laser (below 0.5 mW). So, this NPs system can be fluorescently traced efficiently in cellular systems with little risk of phototoxicity. Some authors have reported fluorescent emission about 610 nm, suggesting intrinsic Au fluorescence [72, 73]. AuNPs emission is related to the core size confinement effect that generates discreet electronic states [74]. However, in our case, the metal surface is covered with flavonoids, which show fluorescence, and when complexing with AuNPs, the fluorescence of both is enhanced. Different authors have reported that fluorescence is largely enhanced by charge transfer from the surface ligands to the metal core via S–Au bonds [75]. It has also been reported that ligands (thiol molecules, DNA oligonucleotides, dendrimers, polymers, peptides, and proteins) affect AuNPs optical and electronic properties since its fluorescent properties can be significantly affected by their surface chemistry [76].
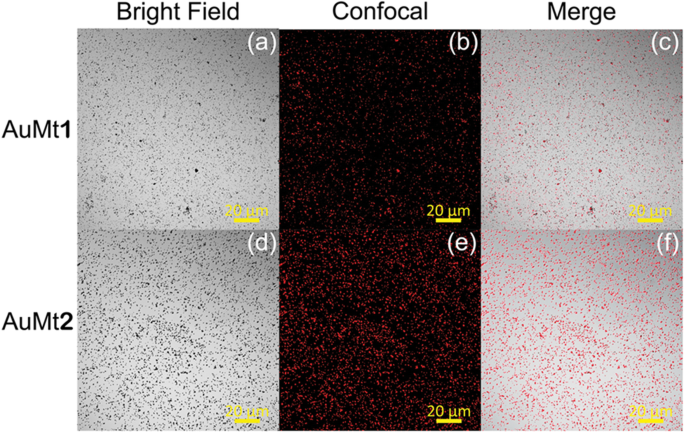
AuMt1 and AuMt2 fluorescence. a , d Bright field. b , e Confocal. c , f Merge
Cellular Internalization
Cells were also analyzed, by confocal microscopy, after 24 h incubation, with AuMt1 and AuMt2 at a concentration of 50 μg/mL. The nucleus is shown in blue color using DAPI Fig. 10a, and the cytoskeleton structure was stained with anti-beta actin in green color Fig. 10b and merge Fig. 10c. The observed micrographs were obtained through 3 different channels on separate tracks, where the excitation wavelengths were 405, 488, and 640 nm for DAPI, anti-beta actin, and AuMt, respectively.
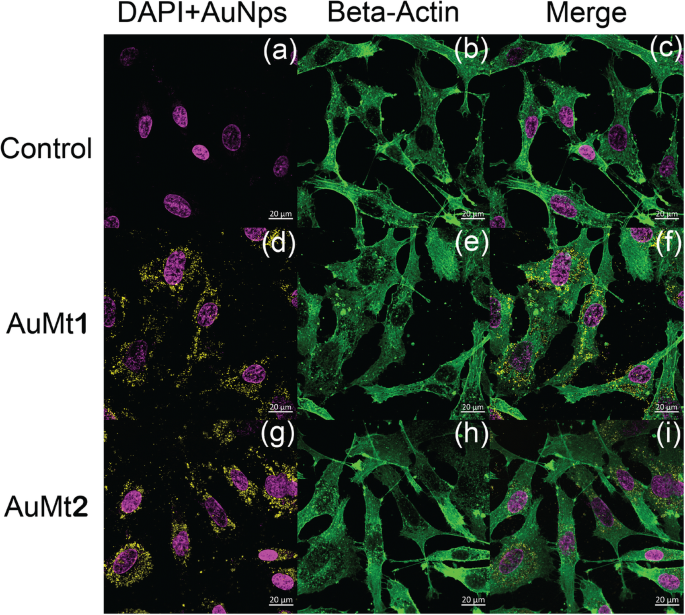
AuMt1 and AuMt2 cellular internalization. a , d , e g with DAPI; b , e , e h with beta-actin; e c , f , and i merge by confocal microscopy
As previously described, cells were also analyzed by confocal microscopy, for AuMt1 and AuMt2 internalization, at a concentration of 50 μg/mL. Confocal micrographs show that AuMt are internalized in HUVEC cells cytosolic space, and many of these particles are surrounding the nucleus, without being internalized in it. When not observing particles in the nucleus, a more meticulous analysis was carried out, by cell orthogonal projection and a 3-D reconstruction. Observing the micrographs of both reconstructions, it is possible to notice that AuMt is distributed differentially. In Fig. 11a, b for AuMt1, it can be observed that a material is dispersed in the cytoplasm, while in AuMt2, the material is concentrated in the nuclear periphery, as shown in Fig. 11c, d. We were not able to find NPs in the nucleus, and this suggests that the nanomaterial has little or no genotoxic potential, since it has no way of interacting with nuclear DNA, which is a quality for a nanocarrier. Efficient cellular uptake depends on NP size, shape, charge, and coating, the parameters that can affect their interactions with cell proteins. The fact that polyphenolic compounds are found on AuMt surface could facilitate the nanomaterial internalization, which would make it a candidate as a possible pharmacological nanocarrier [77,78,79].
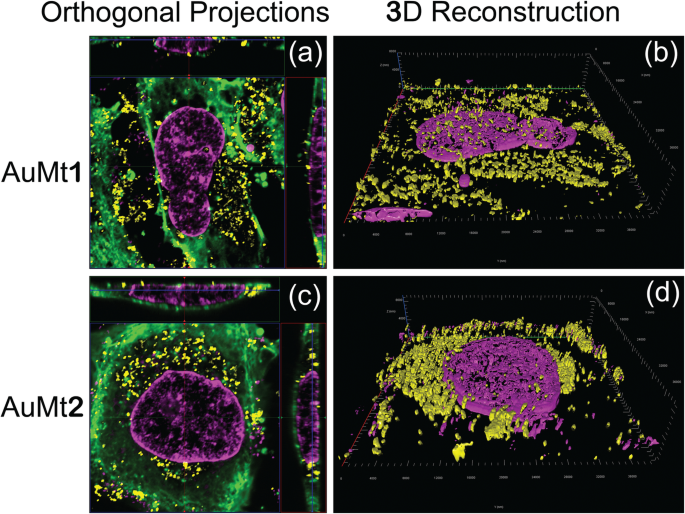
Orthogonal projections and 3-D images. a , c AuMt1 and AuMt2 cellular internalization analysis through orthogonal projection and b , d 3-D reconstruction by confocal microscopy
The obtained results for an AuMtNP cellular uptake in HUVEC by a confocal microscopy at 50 μg/mL suggests that AuMt1 interacts with the cells in a greater quantity than AuMt2 in a 3:1 ratio, as seen in Additional file 1:Figures S5–S7. If we consider that protein corona in AuMt1 is 9.1 nm smaller than in AuMt2, we can suggest that AuMt1-efficient internalization by HUVEC cells is given by a combination of factors such as AuMt1 smaller size, the highest absolute value of z potential and the lower thickness of protein corona. This indicates a poor protein coverage that allows partial exposure of the nanoparticle surface, which is rich in extract molecules. Therefore, nanoparticles can interact by means of extract molecules with surface-specific membrane receptors that facilitate the internalization of AuMt1.
Catalytic Tests
Catalysis
Analysis of catalytic reaction was realized to calculate the degradation percentage ( %D) using the Eq. (5):
$$ \%D=\frac{\left({A}_0-A\right)}{A_0}x100 $$ (5)
using the A 0 absorbance at t = 0 and A is the absorbance at time t . Langmuir-Hinshelwood equation was used to calculate the slope of the regression plot \( \ln \left(\frac{A}{A_0}\right) \) versus irradiation time [80], which is expressed in Eq. (6) and K is the first-order rate constant of the degradation ratio:
$$ \ln \left(\frac{A}{A_0}\right)=Kt $$ (6)
For the analysis of catalytic activity on MB degradation, the absorbance at 660 nm was monitored. Figure 12 shows the AuMt1 and AuMt2 catalytic activity, where a decrease on maximum absorption of MB is observed as time progresses Fig. 12a, d. MB degradation and its conversion to leucomethylene is confirmed by progressive decreases of the absorbance at 292, 614, and 660 nm correspond to MB and by the increase in time of the absorbance at 256 nm associated with leucomethylene. Homogeneous catalysis reaches a 50% MB degradation at 190 s Fig. 12b, while the degradation ratio K for the total process is 8.24 × 10 −3 s to AuMt1 Fig. 11c. AuMt2 reaches a 50% of MB degradation in 400 s, Fig. 12e, and K takes the value of 3.54 × 10 −3 /s, Fig. 12f.
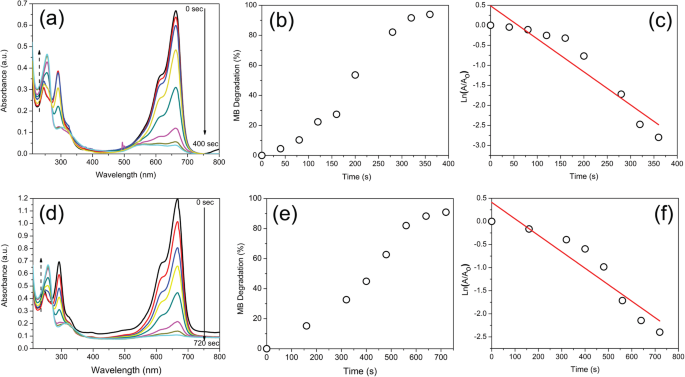
AuMt1 and AuMt2 Catalysis. a , d UV-Vis spectra. b , e Percentage. c , f Ratio of MB degradation
On this way, AuMt1 have a more efficient response than AuMt2. We observed a size-dependent effect (AuMt) in degradation ratio [81], and a total surface area of NPs is inversely proportional to the NP size [37]. Table 2 shows a comparison between different green syntheses of AuNPs and their K obtained in size function.
Conclusions
In this work, we show for the first time that the extracts of bark of Mimosa tenuiflora allow the production at room temperature of gold nanoparticles by means of one-pot synthesis. AuNP sizes are easily controlled by regulating a metal precursor/reducing an extract ratio. It was observed that AuMt1 and AuMt2 cellular uptakes generate a moderate cytotoxic effect at 24 and 48 h post exposition. However, toxicity does not behave in a dose-dependent manner, which suggests different action mechanisms for AuMt1 and AuMt2. XPS and FTIR indicate that AuMtNPs interact mainly with carbonyl groups (ketones) in addition to hydroxyl groups of Mimosa tannins, saponins, and other molecules that participate in the reduction of Au 3+ para Au 0 and stabilization of nanomaterials. Polyphenols adsorbed on AuMtNPs facilitate nanoparticle internalization. AuMt2 were located near the nuclear periphery, but for AuMt1, it was observed that nanoparticles distribute on the whole cell and present a 3 fold uptake in comparison to AuMt2. Due to the fluorescence property at low excitation power and a high cellular uptake, AuMtNPs synthesized with Mt bark extracts are candidates for its implementation as drug nanocarriers and fluorescent probes in cells. However, other strategies must be addressed, in order to reduce the nanomaterial toxicity. Finally, it was observed that AuMtNPs showed a relevant catalytic activity on MB degradation using NaBH4 as a reducing agent.
Disponibilidade de dados e materiais
All datasets are presented in the main paper.
Abreviações
- ANOVA:
-
Analysis of variance
- AuMt:
-
Colloids formed by AuNPs and molecules of Mt
- AuNPs:
-
Nanopartículas de ouro
- CLSM:
-
Confocal laser scanning microscopy
- DLS:
-
Espalhamento de luz dinâmico
- DMEM:
-
Dulbecco’s modified Eagle medium
- DMSO:
-
Dimetilsulfóxido
- DPPH:
-
2,2-Diphenyl-1-picrylhydrazyl
- EDS:
-
Energy dispersive X-rays spectroscopy
- FTIR:
-
Espectroscopia de infravermelho com transformada de Fourier
- HAuCl4 :
-
Tetracloroauric acid
- HRTEM:
-
High-resolution TEM
- HUVEC:
-
Human umbilical vein endothelial cells
- MB:
-
Azul de metileno
- Mt:
-
Mimosa tenuiflora
- MTT:
-
Brometo de 3- (4,5-dimetiltiazolil-2) -2,5-difeniltetrazólio
- NaBH4 :
-
Boro-hidreto de sódio
- PBS:
-
Phosphate-buffered saline
- PdI:
-
Índice de polidispersidade
- PMT:
-
Photomultiplier tube
- ROI:
-
Region of interest
- SD:
-
Standard deviations
- SPR:
-
Surface plasmon resonance
- TEM:
-
Microscopia eletrônica de transmissão
- UV-Vis:
-
Ultraviolet-visible
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- XRD:
-
Difração de raios X
Nanomateriais
- Nanopartículas plasmônicas
- Nanopartículas de ouro para sensores quimio
- Nanopartículas multifuncionais de ouro para aplicações diagnósticas e terapêuticas aprimoradas:uma revisão
- Síntese fácil e propriedades ópticas de pequenos nanocristais de selênio e nanorods
- Síntese fácil de compósito CuSCN colorido e condutor revestido com nanopartículas de CuS
- Estudo in vitro da influência das nanopartículas de Au nas linhas celulares HT29 e SPEV
- Propriedades de síntese e luminescência de nanopartículas α-NaGdF4 / β-NaYF4:Yb, Er Core – Shell solúveis em água
- Nanopartículas de sílica para entrega de proteína intracelular:uma nova abordagem de síntese usando proteína fluorescente verde
- Síntese e atividade de oxidação de CO de 1D óxido binário misto CeO2-LaO x catalisadores de ouro suportados
- Adepto verde na síntese e estabilização de nanopartículas de cobre:atividades catalíticas, antibacterianas, citotoxicidade e antioxidantes



