Síntese e atividade de oxidação de CO de 1D óxido binário misto CeO2-LaO x catalisadores de ouro suportados
Resumo
Nanobastões unidimensionais (1D) de Ce-La com diferentes teores de La (Ce e La na razão molar de 1:0, 3:1, 1:1, 1:3 e 0:1) foram sintetizados por processo hidrotérmico. Os catalisadores Au / Ce-La nanorod foram obtidos por um método modificado de deposição-precipitação. As amostras foram caracterizadas por N 2 adsorção-dessorção (BET), ICP, difração de raios-X (XRD), SEM, TEM, EDX, espectroscopia de fotoelétrons de raios-X (XPS), espectroscopia de refletância difusa de UV-vis (UV-vis DRS) e redução programada por temperatura (H 2 -TPR). Ele revelou que La existia como LaO x nos nanobastões 1D. Os resultados da catálise demonstraram que os óxidos de nanobastões binários Ce-La mistos podem ser um bom suporte para catalisadores de ouro. O conteúdo de La teve uma importante influência no desempenho catalítico dos catalisadores nanobastões Au / Ce-La. Entre os catalisadores, quando a razão molar Ce / La era de 3:1, o Au / Ce de 1,0% 0,75 -La 0,25 nanobastões pré-tratados a 300 ° C apresentaram a melhor atividade entre os catalisadores para a oxidação do CO, podendo converter o CO completamente a 30 ° C. Os catalisadores também apresentaram resistência a altas temperaturas e boa estabilidade para oxidação de CO nas temperaturas de reação de 40, 70 e 200 ° C.
Histórico
Como um gás muito prejudicial, o CO pode se ligar fortemente ao átomo de ferro da hemoglobina do sangue, impedindo a liberação de oxigênio. Portanto, sua presença em ambientes fechados pode até causar a morte de seres humanos e animais em um curto espaço de tempo. Tornou-se um problema cada vez mais grave de poluição do ar. A oxidação catalítica do CO tem sido uma das soluções mais eficazes para a remoção do CO para resolver esse sério problema ambiental [1,2,3,4,5,6,7,8]. Também tem recebido grande atenção recentemente pela comunidade científica nos campos dos dispositivos de controle de poluição para purificação de exaustão de veículos, limpeza do ar interno e sensores de CO de baixa temperatura [6,7,8,9,10]. Em muitos casos, o precioso Au é disperso em óxidos de metal específicos com alta capacidade de armazenamento de oxigênio, como CeO 2 , TiO 2 , e Fe 2 O 3 são candidatos altamente eficazes para a oxidação do CO [11,12,13]. Nas últimas décadas, estudos sobre catalisadores de ouro com suporte para oxidação de CO em baixas temperaturas resultaram em observações inesperadas. É geralmente aceito que as atividades catalíticas dos catalisadores de Au dependem fortemente da natureza das nanopartículas de Au e das propriedades dos suportes, como o tamanho da partícula de ouro, a interação metal-suporte de Au e a redutibilidade do suporte [14,15,16 , 17,18].
Como um dos óxidos de terras raras mais importantes, CeO 2 tem sido amplamente utilizado em catalisadores de três vias como um suporte de catalisador eficiente devido às suas propriedades físicas e químicas únicas [6, 8, 15, 17]. CeO 2 tem um excelente armazenamento de oxigênio e capacidade de liberação devido à capacidade de alternar Ce 4+ / Ce 3+ , o que torna CeO 2 tornar-se um componente óxido ativo de vários catalisadores de oxidação usados em diversas reações catalíticas redox [17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32]. Áreas de superfície, estruturas mesoporosas, defeitos de rede e efeitos sinérgicos com outros dopantes podem promover as propriedades catalíticas dos nanomateriais de céria [3, 22]. Para melhorar ainda mais o desempenho do Au-CeO 2 catalisadores para a reação de oxidação de CO, muitas estratégias têm sido tentadas, como métodos de preparação, incluindo deposição-precipitação, coprecipitação e coprecipitação de ureia-gelificação, que tem sido usada para controlar e otimizar a interação da estrutura Au-O-Ce, também como o tamanho e a forma da céria [33,34,35]. Tentativas também têm sido feitas pela modificação da superfície do suporte [4, 5, 22, 24, 26, 36,37,38]. Verificou-se que o uso de óxidos mistos binários como suporte pode fornecer uma boa solução para a estabilização de nanopartículas de ouro. Além disso, a promoção por metais nobres ou de transição aumenta a redutibilidade da céria e facilita a formação de vazios de oxigênio na superfície. Enquanto isso, a dopagem com cátions de metal de transição tem se mostrado um método eficaz para promover as propriedades físico-químicas de nanomateriais nanoestruturados unidimensionais (1D), como a atividade catalítica [38,39,40]. Wang et al. [5] modificou a superfície de Au / CeO 2 com CoO altamente disperso x e demonstrou excelente atividade catalítica na oxidação de CO em baixa temperatura. Ma et al. [37] relatou que CaO, NiO, ZnO, Ga 2 O 3 , Y 2 O 3 , ZrO 2 , e aditivos de terras raras para catalisador de ouro-titânia são benéficos para a oxidação de CO, e os catalisadores dopados podem mostrar atividade significativa à temperatura ambiente após 500 ° C de envelhecimento. Park et al. [38] relatou que CeO x TiO modificado 2 o suporte é um bom catalisador para a reação de deslocamento do gás água. Existem muitos estudos sobre óxidos metálicos mistos para a oxidação catalítica do CO. Esses íons metálicos dopados são depositados na superfície do suporte na forma de partículas de óxido ou na rede do suporte, que não poderia formar uma fase de óxido separada. O objetivo desta pesquisa é preparar nanobastões 1D binários de Ce-La, que são não perovskita ou óxido misto do tipo solução sólida. Ou seja, na estrutura de nanorod 1D, os dois óxidos de metal coexistem combinando os méritos das duas composições para maximizar o efeito sinérgico. Devido às aplicações tecnológicas potenciais, muitos nanomateriais 1D, incluindo nanobastões, nanofios e nanotubos, foram extensivamente investigados durante os últimos anos [2, 4, 41, 42]. Esses materiais nanoestruturados 1D, especialmente materiais nanobastões 1D, têm sido estudados como importantes suportes ou componentes ativos no campo da catálise, óptica e eletroquímica, como nanofios de silício bem controlados usados em células solares [42]. Verificou-se que as propriedades dos materiais de estrutura 1D, como a atividade catalítica, estão frequentemente relacionadas à sua estrutura e forma cristalina. Como consequência, o desenvolvimento de materiais nanobastões 1D para ajustar suas propriedades eletrônicas e catalíticas mostra-se intrigante e valioso.
Aqui, relatamos uma estratégia solvotérmica simples para preparar uma série de compostos nanobastões de Ce-La. No processo de síntese, o LaO x e CeO 2 poderiam crescer juntos em uma haste. A morfologia dos produtos finais não foi influenciada. Os resultados de XRD e TEM mostram que as La cações existiram na forma de LaO x . Verificou-se que o dopante de LaO x mostrou um efeito positivo sobre a atividade dos catalisadores de ouro-céria. Au / Ce 0,25 -La 0,75 nanobastões exibiram excelente atividade catalítica para a oxidação de CO.
Experimental
Todos os produtos químicos neste documento eram de grau analítico e foram usados como recebidos sem qualquer purificação.
Preparação para suporte
Os nanobastões de Ce-La foram sintetizados pelo método hidrotérmico convencional. Em uma síntese típica, soluções de NaOH (9 mol / L) e Ln (NO 3 ) 3 (Ln =Ce, La, 0,8 mol / L) foram misturados e mantidos em agitação vigorosa por 30 min à temperatura ambiente. A suspensão resultante foi vertida para uma autoclave de aço inoxidável forrada com Teflon. A autoclave foi selada e mantida a 110 ° C por 14 h e, em seguida, resfriada com ar até a temperatura ambiente. Os produtos resultantes foram filtrados, lavados com água desionizada e álcool absoluto, secos a 80 ° C por 12 h e, em seguida, calcinados a 400 ° C ao ar com uma taxa de aquecimento de 5 ° C min −1 antes de apoiar nanopartículas de ouro. Os produtos finais com diferentes teores de La (Ce e La na razão molar de 1:0, 3:1, 1:1, 1:3 e 0:1) foram denotados como nanobastões de Ce, Ce 0,75 -La 0,25 nanorods, Ce 0,50 -La 0,50 nanorods, Ce 0,25 -La 0,75 nanorods e La nanorods.
Preparação do catalisador
Um processo de deposição-precipitação foi realizado para preparar catalisadores Au / Ce-La nanorod. Resumidamente, a quantidade necessária de nanobastões de Ce-La foi dispersa em 100 mL de água desionizada e, em seguida, misturada com uma certa quantidade 0,01 mol / L de HAuCl 4 solução. Como o pH do HAuCl final 4 solução era cerca de 7, o que estava relacionado com a basicidade do suporte e acidez do HAuCl 4 , o pH da solução não seria ajustado. A suspensão foi mantida em agitação durante 12 h e refluxada a 100 ° C durante 4 h. Após o procedimento de deposição-precipitação, o precipitado foi centrifugado, lavado com água para remover Cl - iões e secos a 80 ° C sob ar durante 12 h. As concentrações de ouro foram expressas como porcentagem por conteúdo de massa.
Técnicas de caracterização
As cargas de ouro de catalisadores nanobastões Au / Ce-La foram determinadas por espectroscopia de emissão atômica com plasma indutivamente acoplado (ICP-9000, EUA Thermo Jarrell-Ash Corp). As áreas de superfície Brunauer – Emmett – Teller (BET) de amostras de nanobastões de Ce-La foram medidas por adsorção de nitrogênio a - 196 ° C usando um aparelho Micromeritics Tristar II 3020. O estudo de XRD foi realizado em um difratômetro de raios-X Rigaku D / Max-2500 ( Kα λ =0,154 nm) no 2 θ faixa de 3–80 °. DRS Uv-visível dos catalisadores foram coletados em um espectrofotômetro UV-vis NIR (JASCO Corp V-570). Observações TEM e análise de energia dispersiva de raios-X (EDX) foram obtidas com um microscópio eletrônico de transmissão JEM-2100 operando a 200 kV. Dados SEM e imagens de mapeamento de elementos foram obtidos com um microscópio eletrônico de varredura JSM-7500F operando a 15 kV. XPS foram registrados para identificar a composição química e o estado de oxidação dos catalisadores em um espectrômetro de fotoelétrons de raios-X Kratos Axis Ultra DLD usando um Al Kα monocromado fonte operada a 150 W. As energias de ligação foram calibradas usando o C 1 s pico localizado a 284,6 eV. Redução programada pela temperatura (H 2 –TPR) foi realizada em um aparelho PX200 para medir H 2 consumo. Antes de H 2 Para análise de -TPR, as amostras foram pré-tratadas em fluxo de He a 300 ° C por 1 h. Depois de resfriado a 50 ° C, o catalisador foi reduzido com 10 vol% H 2 / Ar fluxo de gás por aquecimento até 900 ° C a uma taxa de 10 ° C / min.
Teste de atividade catalítica
A avaliação da atividade catalítica foi realizada em um milirreator de fluxo de leito fixo com diâmetro interno de 8 mm. Antes da reação, 200 mg de catalisador foram diluídos com 17,6 g de areia de quartzo quimicamente inerte. Posteriormente, uma mistura de 10% de CO balanceada com ar foi introduzida no reator a uma taxa de fluxo total de 36,3 mL min −1 . Após manter a temperatura de reação por 30 min, os produtos gasosos foram analisados online por CO x analisador (cromatografia gasosa GC-508A). A conversão de CO foi calculada de acordo com a seguinte equação:
$$ \ mathrm {CO} \ kern0.5em \ mathrm {conversão} =\ frac {\ left [\ mathrm {CO} \ 2 \ right]} {\ left [\ mathrm {CO} \ right] + \ left [ \ mathrm {CO} \ 2 \ right]} \ times 100 \% $$
onde [CO] e [CO 2 ] representam a saída CO e CO 2 concentração, respectivamente. A dependência da temperatura da atividade catalítica da amostra foi registrada na faixa de 30–200 ° C com uma taxa de rampa de 10 ° C min −1 .
Resultados e discussão
Caracterização de catalisadores Au / Ce-La Nanorod
ICP
As quantidades de ouro presentes nos catalisadores nanobastões Au / Ce-La foram determinadas por ICP-AES. Os resultados apresentados na Tabela 1 revelaram que a quantidade real de ouro em todos os catalisadores era inferior à nominal. De acordo com o procedimento de preparação, o ouro deve ser perdido durante o processo de deposição-precipitação.
APOSTA
N 2 medições de absorção foram usadas para medir a área de superfície BET e o diâmetro médio em ambos CeO 2 nanobastões e nanocompósitos Ce-La. Conforme mostrado na Fig. 1, as isotermas de adsorção para os nanobastões de Ce-La eram do tipo IV e exibiam características de loops de histerese H3. Todas as amostras mostram um aumento muito forte de N 2 -volume adsorvido a uma pressão relativa maior que 0,85, que é uma característica da presença de uma quantidade apreciável de mesoporoso, [2, 22] indicando nanocompósitos de Ce-La compostos por agregados (assembléias soltas) formando poros em fenda. Com o dopante de La, os loops de histerese mudaram para uma pressão relativa de cerca de 0,95, o que significava que o tamanho dos poros se tornaria menor, correspondendo à diminuição dos compósitos Ce-La. Conforme apresentado na Tabela 2, área de superfície específica de CeO 2 nanorods tem 99,7 m 2 / g, que diminui para 74,1 m 2 / g quando La é dopado com a razão molar Ce / La de 3:1. Com o aumento do conteúdo de La, a área de superfície dos nanocompósitos de Ce-La diminuiu continuamente. Isso é principalmente resultante do conteúdo de La, que não seria incorporado na rede de CeO 2 e existem como LaO isolado x levando a pouca diferença na morfologia dos nanocompósitos de Ce-La. Pode-se observar que todos os nanobastões têm áreas de superfície semelhantes de 80-100 m 2 / g. Volume de poros de Ce 0,75 -La 0,25 os nanorods têm 0,23 cm 3 / g, que era semelhante ao dos nanobastões de Ce e maior do que os outros nanobastões de Ce-La. Os diâmetros de poros estimados a partir da análise de BJH confirmaram a natureza mesoporosa dos nanocompósitos de Ce-La. Pode ser uma vantagem para a oxidação catalítica do CO.
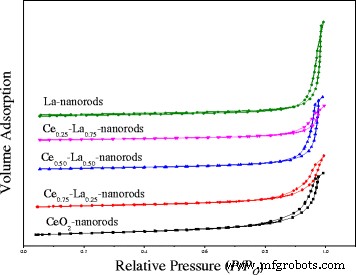
Isotermas de adsorção-dessorção de nitrogênio de nanobastões de Ce-La com diferentes conteúdos de La
XRD
As amostras sintetizadas foram submetidas à análise de difração de raios-X do pó e seus atributos estruturais foram posteriormente analisados. Os picos de cristalinidade para óxido de cério (Fig. 2a) foram observados em 2θ =28,6 °, 33,1 °, 47,6 ° e 56,3 ° correspondendo aos planos de difração (111), (200), (220) e (311) e corroborar para a estrutura de fluorita cúbica de CeO 2 cristal (JCPDS no. 34-0394). Quando o conteúdo de La era de 0,25 at.%, Os picos de difração dos compósitos La-Ce aumentam. Picos centrados em 2θ =30,0 °, 46,0 °, 52,0 ° e 53,6 ° correspondem aos planos de difração do La 2 isolado O 3 . Nenhum pico atribuído a La (OH) 3 poderia ser detectado. Mas devido ao baixo conteúdo e posição aproximada de difração, não é fácil identificar a existência de LaO x . Com o aumento do conteúdo de La, alguns picos proeminentes são observados para La 2 O 3 ou La (OH) 3 no nanocompósito. Os principais picos de difração de La 2 O 3 estão presentes em 2θ =30,0 ° (101), 39,6 ° (220), 46,2 ° (110) e 66,8 ° (112), que podem ser atribuídos à fase hexagonal (cartão JCPDS 05-0602). Os principais picos de difração de La (OH) 3 estão presentes em 2θ =15,7 ° (100), 27,3 ° (110), 27,9 ° (101) e 39,4 ° (201), que podem ser atribuídos à fase hexagonal (cartão JCPDS 36-1481). Os resultados demonstram que La pode existir como La isolada 2 O 3 ou La (OH) 3 no composto. Após a deposição do ouro, não houve pico de difração que pudesse ser indexado à estrutura cristalina pura de ouro centrada na face (Fig. 2b). Isso pode ser devido ao baixo conteúdo e / ou pequeno tamanho de partícula de nanopartículas de ouro.
Padrões de XRD de nanobastões de Au / Ce-La a 1% com diferentes conteúdos de La (0-100 at.%) ( a ) e Au / Ce 0,75 -La 0,25 nanobastões com diferentes carregamentos de Au calcinados a 300 ° C por 2 h ( b )
SEM e TEM
A Figura 3a-e mostra as fotografias SEM do CeO 2 e nanocompósitos Ce-La obtidos em diferentes concentrações de La 3+ íons. É visto que todos os nanocompósitos de Ce-La exibiram estrutura em forma de bastonete. Obviamente, muitas hastes se amontoaram em feixes de Ce-La, levando à formação de poros em forma de fenda com tamanhos diferentes. Os resultados estão de acordo com o N 2 isotermas de adsorção-dessorção. Conforme mostrado na Fig. 2a, o produto consiste principalmente em nanobastões com diâmetro de 5–10 nm e comprimento de 100–300 nm. Na Fig. 3e, uma grande quantidade de nanobastões com diâmetro de cerca de 12,5 nm foi vista claramente, e também havia uma pequena quantidade de nanobastões curtos com um diâmetro médio de cerca de 8,0 nm. Na Fig. 3b-d, com o aumento da concentração de dopagem de La 3+ , as amostras sempre apresentam morfologia de nanobastões. No entanto, enquanto a concentração de dopagem foi de 25 mol%, as amostras conforme obtidas exibiram os nanobastões mais uniformes com diâmetro de 5–20 nm e comprimento de 100–300 nm entre todas as amostras. A Figura 3f exibe imagens TEM dos nanobastões de Ce-La individuais obtidos. Pode-se ver que há muitos poros no suporte, conforme revelado pelas isotermas de adsorção-dessorção de nitrogênio. A imagem HRTEM dos nanobastões Ce-La revelou que eles são estruturalmente uniformes e monocristalinos na natureza. As franjas de rede inseridas na Fig. 3f ilustram dois valores de espaçamento interplanar, ou seja, 0,31 e 0,34 nm, que são consistentes com os planos (111), (110) do CeO 2 e La 2 O 3 , respectivamente [3, 15, 43]. Ele revelou que o La 3+ íons foram efetivamente gerados em La 2 O 3 , que é consistente com o espectro de XRD.

Imagens SEM de nanobastões Ce-La com diferentes conteúdos de La:0 ( a ), 25 at.% ( b ), 50 at.% ( c ), 75 at.% ( d ), 100 at.% ( e ); Imagem TEM de Ce 0,50 -La 0,50 nanorods ( f ); e a inserção mostra a imagem HRTEM correspondente
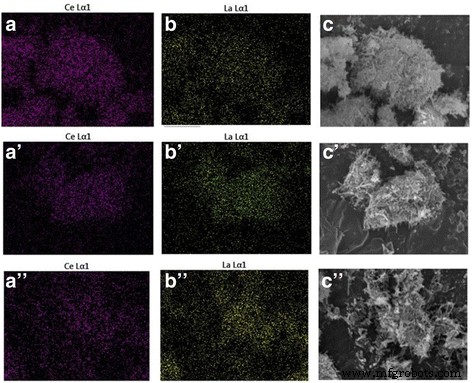
O mapeamento de elementos e a análise de EDS foram empregados para determinar a composição química das amostras de Ce-La (Fig. 4 e Tabela 3). Os resultados mostraram relações molares La / Ce uniformes em boa concordância com os valores esperados da síntese. As imagens TEM de Au / Ce 0,75 -La 0,25 as amostras calcinadas a 300 ° C (Fig. 5a) e 400 ° C (Fig. 5c) mostraram claramente que as formas dos nanocristais de Ce-La permaneceram essencialmente inalteradas após a adição de ouro. Nenhuma partícula de ouro foi observada por TEM nos nanobastões Ce-La. A presença de aglomerados de ouro muito dispersos ( d <1 nm) foi evidenciado por mapeamento de elemento e análise EDX (inserção na Fig. 5b, e e f). Em concordância, a análise de XRD realizada nesta amostra (Fig. 2) não revelou nenhum pico relacionado ao ouro devido ao fato de as partículas de ouro serem muito pequenas para serem detectadas. Isso indica que as superfícies do nanobastão Ce-La podem dispersar e estabilizar átomos de ouro como aglomerados sub-nanométricos (TEM invisível). Isso está de acordo com a literatura [2, 44,45,46]. No entanto, alguns grandes aglomerados de partículas de ouro (média d ~ 7 nm) foram observados em Au / Ce 0,75 -La 0,25 nanobastões calcinados a 400 ° C devido às franjas com espaçamento de 0,236 nm sendo atribuídas ao plano (1 1 1) do Au metálico (Fig. 5c na qual um aglomerado de partículas de ouro é mostrado). Pôde-se observar que acompanhando a alta temperatura de calcinação, as partículas de ouro obviamente cresceram, levando à perda de atividade catalítica.

As imagens de mapeamento de elemento de Ce e La, imagens de SEM das amostras mistas para nanobastões de Ce-La com conteúdo de La de 25 at.% ( a - c ), 50 at.% ( a ′ - c ′), 75 at.% ( a ′ ′ - c ″)
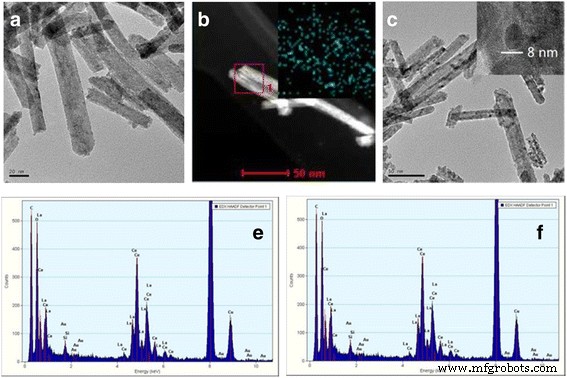
Imagens TEM e STEM de 0,5% Au / Ce 0,75 -La 0,25 nanobastões calcinados a 300 ° C ( a - b ) e 400 ° C ( c ), Análise EDX ( e - f ) das imagens de ( a - b ) indicando a presença de sinal Au
XPS
Os espectros de XPS na Fig. 6 são realizados para investigar o composto químico e os estados em 1% Au / Ce 0,75 -La 0,25 amostras de nanorod calcinadas a 300 ° C por 2 h. O espectro XPS de Ce 3 d mostra os picos distintos de 3 d 3/2 estados de rotação-órbita e 3 d 5/2 estados spin-órbita na Fig. 6a. Como é conhecido, os picos estão localizados na energia de ligação de cerca de 899, 903 e 916 eV normalmente usados como o marcador espectroscópico para detectar a presença de Ce 4+ Estado. Em nosso caso, Ce 3 d os níveis do núcleo mostram três dupletos orbitais de spin, que são os picos característicos dos estados tetravalentes de Ce 4+ . Os picos localizados em torno de 882,8, 888,1 e 898,4 eV são atribuídos ao Ce 3 d 5/2 , e aqueles em torno de 901,3, 907,0 e 916,7 eV são atribuídos ao Ce 3 d 3/2 , correspondendo a dupletos de divisão spin-órbita de compostos Ce (IV). Os resultados observados são comparados com literaturas relatadas geralmente [19, 28, 29, 32]. É óbvio que as amostras estão no estado Ce 4+ sem qualquer impureza do Ce 3+ Estado. A Figura 6b mostra os espectros de XPS do La 3 d região de 1% Au / Ce 0,75 -La 0,25 amostras de nanorod. Tanto a divisão spin-órbita 3 d 5/2 e 3 d 3/2 os níveis mostraram estruturas de pico duplo. A divisão de rotação-órbita entre os 3 d 3/2 e 3 d 5/2 os níveis eram cerca de 17,0 eV, e a separação entre o satélite e o pico principal era de 4,1 eV, o que estava de acordo com os valores relatados para La 3+ compostos [11, 47]. Como seria de se esperar, o La sai no estado de oxidação + 3 e pode ter uma influência importante na atividade catalítica. O 1 s O espectro de XPS (Fig. 6c) é assimétrico e deconvoluído em 529,3, 531,6 e 527,6 eV, respectivamente. O pico em 529,3 eV é atribuído ao oxigênio da rede e aquele em torno de 531,9 eV é atribuído a grupos hidroxila na superfície do suporte [27, 28, 32]. O pequeno pico do ombro em 527,6 eV é atribuído a La-O, que também pode revelar a presença de LaO x nos catalisadores [11, 48]. Claramente, há um grande número de grupos hidroxila na superfície do suporte de acordo com a alta intensidade de pico. Os espectros de XPS no Au 4 f região dos catalisadores calcinados a 300 e 400 ° C são mostrados na Fig. 6d. Na Fig. 6d, os catalisadores calcinados a 300 ° C mostraram o Au 4 f 2/7 sinais de energia de ligação em 84,6 eV. Os sinais eram característicos para Au + catiônico espécies [14, 15, 31]. Em comparação, após os catalisadores calcinados a 400 ° C, o Au 4 f 2/7 pico foi localizado na energia de ligação de 83,6 eV, e Au 4 f 5/2 foi localizado a uma energia de ligação de 87,7 eV. A presença de Au 0 metálico é claramente observado. Os pequenos picos localizados em torno de 85,0 e 88,2 eV, correspondentes a espécies de ouro oxidadas, também foram detectados. É claro que os catalisadores calcinados a 300 ° C mostraram Au praticamente principalmente catiônico + espécies (> 90% de Au + espécies). Em contraste, as amostras calcinadas a 400 ° C têm 90% de Au 0 e 10% de Au δ + . A transferência da densidade eletrônica do Au metálico para o suporte resultou na oxidação parcial do Au e forte interação entre o ouro e o suporte. A presença de Au δ + é responsável pela redução parcial da superfície de apoio. Assim, Au δ + é considerado mais ativo do que Au 0 para oxidação de CO [11, 21]. Em nosso caso, os catalisadores calcinados a 300 ° C tiveram mais Au δ + do que aquele calcinado a 400 ° C, então não é difícil deduzir que os catalisadores calcinados a 300 ° C foram mais ativos do que os catalisadores calcinados a 400 ° C, o que foi consistente com os resultados da atividade.
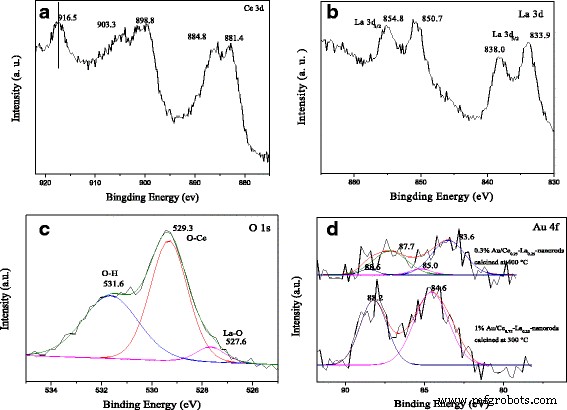
Espectro XPS de 1% Au / Ce 0,75 -La 0,25 nanobastões calcinados a 300 ° C por 2 h:Ce 3 d picos ( a ), La 3 d picos ( b ), e O 1 s picos ( c ) Au 4 f picos ( d ) de Au / Ce 0,75 -La 0,25 nanobastões calcinados a 300 e 400 ° C por 2 h
UV-visível
O espectro de refletância difusa de UV-vis do Ce 0,75 -La 0,25 nanobastões e 0,5% Au / Ce 0,75 -La 0,25 nanobastões calcinados em diferentes temperaturas são apresentados na Fig. 7. Como visto nesta figura, em comparação com os espectros do suporte, os espectros dos catalisadores calcinados em diferentes temperaturas exibiram banda de absorção fraca e ampla entre 500 e 600 nm, que foi caracterizada por a ressonância plasmônica de superfície (SPR) de nanopartículas de ouro metálico [21, 24, 49]. O SPR poderia ser atribuído às oscilações coletivas de elétrons em resposta à excitação óptica, o que resultaria na absorção de luz na região de Uv-vis. A localização da ressonância do plasmão de superfície foi afetada pelo tamanho da partícula de ouro disperso, a forma da partícula e as propriedades dielétricas do material circundante. No presente estudo, o pré-tratamento de calcinação causou um grande desvio para o vermelho das bandas de absorção e as posições das bandas de absorção (500–600 nm) foram deslocadas para o vermelho com o aumento da temperatura de calcinação. As classificações de deslocamento são as seguintes:80 ° C → 200 ° C → 300 ° C. Com um novo aumento da temperatura de calcinação para 400 ° C, as bandas de absorção mudaram para o comprimento de onda curto. Houve vários relatórios sobre a explicação da mudança da posição do pico [24, 50,51,52,53]. Embora o diâmetro da partícula de ouro seja <2 nm, a posição de pico de deslocamento ampliada foi causada principalmente pelo amortecimento dependente do tamanho da função dielétrica do metal. Também ocorreu uma redução da densidade do elétron nas partículas de ouro devido às interações químicas com os óxidos de metal circundantes, o que poderia explicar o mecanismo que leva a um desvio para o vermelho ainda mais [52]. Um aumento no tamanho das partículas de ouro causaria um deslocamento para o azul no pico de absorção (diâmetro médio menor que 25 nm), e para partículas grandes (diâmetro médio maior que 25 nm), o efeito oposto foi observado [53]. De acordo com os dados do TEM, o tamanho das partículas de ouro no catalisador era <1 nm para o catalisador calcinado a 300 ° C. No entanto, com um aumento adicional da temperatura de calcinação para 400 ° C, as partículas de ouro cresceram e o tamanho médio foi de cerca de 7 nm. Como mencionado antes, a posição da banda de plasmon depende fortemente da forma e do tamanho das partículas de ouro. No caso presente, essa grande mudança pode ser explicada em termos da diferença no tamanho das partículas de ouro. Os dados foram consistentes com os resultados do teste de atividade catalítica. Também indicou que as nanopartículas de ouro se dispersaram bem na superfície dos suportes.
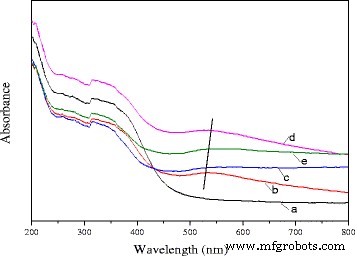
UV-vis DRS de Ce puro 0,75 -La 0,25 suporte de nanorod (a) e 0,3% Au / Ce 0,75 -La 0,25 nanobastões calcinados a 80 ° C (b), 200 ° C (c), 300 ° C (d) e 400 ° C (e)
H 2 -TPR
A Figura 8a mostra o perfil de TPR para amostras de óxidos puros e mistos. Para CeO puro 2 nanobastões, o pico de redução centrado em cerca de baixa temperatura (410 ° C) e alta temperatura (620 ° C) pode ser atribuído à redução das espécies de oxigênio da superfície e a granel de CeO 2 , respectivamente [1, 32]. Para nanobastões de La puros, picos de redução óbvios podem ser detectados a ~ 700 ° C atribuídos à redução de La em massa 2 O 3 . Foi interessante descobrir que os picos de redução em ~ 500 ° C dos nanobastões de Ce-La apareceram. O pico de redução das três amostras com 25, 50 e 75% at.% La de dopagem mostra uma mudança para temperaturas mais altas em cerca de 20 ° C após a dopagem de La. Quando o conteúdo de La é de 25 at.%, Uma temperatura de pico de forte redução de 520 ° C foi observada. É uma nova temperatura de redução e notavelmente em relação ao CeO puro 2 nanorods. Em comparação com a referência, devido à interação sinérgica entre La – O e Ce – O, a temperatura de redução dos nanobastões Ce-La foi maior do que CeO puro 2 [31, 54]. Pode-se descobrir que os óxidos binários devem ter CeO 2 independente e LaO x . Conforme mostrado na Fig. 8b, após a deposição de ouro, um novo pico de redução em temperatura muito baixa (100–200 ° C) aparece para Au / CeO 2 e nanobastões Au / La-Ce. Aqui, devido aos resultados de XPS, depois que os catalisadores foram calcinados a 300 ° C, Au era principalmente Au δ + , então os picos de redução em ~ 200 ° C são atribuídos à redução de espécies de Au em alta valência [21]. O pequeno pico centrado em ~ 350 ° C pode ser associado à redução de nanobastões de Ce-La. Além disso, para 1% Au / Ce 0,75 -La 0,25 nanobastões, outro pico de redução em cerca de 230 ° C pode ser atribuído à redução promovida pelo ouro de CeO 2 . Um por cento Au / Ce 0,75 -La 0,25 nanorods tem a menor temperatura de redução entre os catalisadores, o que poderia ajudá-lo a ser o catalisador mais ativo para a oxidação do CO. This was in agreement with the activity results. Since the surface reduction peaks for all oxide supports are significantly decreased after gold deposition, it indicates that most available oxygen is reduced at this lower temperature and suggests that H2 dissociation on gold and spill-over onto the adjacent oxide surface are more likely to be responsible for the strong low-temperature reduction peak [31]. TEM and XPS data indicated that the cationic gold particles with small size highly dispersed on the surface of the supports. The presence of LaO x could also help stabilize cationic Au. This is beneficial for the strength of gold-support interaction [11]. The strong interaction between gold and support promoted the reduction of Au/Ce-La nanorods shifted to low temperature. The results indicated that the reducibility of Ce-La nanorods is strongly affected by the gold deposition.
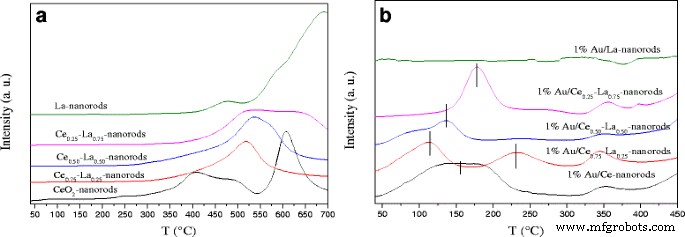
H 2 -TPR profiles of a La-Ce nanorods with different La content (0–100 at.%) and b 1% Au/La-Ce nanorods with different La content calcined at 300 °C
Catalytic Activity
Effect of La Content
As shown in Fig. 9, catalytic activity results for Au/Ce-La nanorod samples ranging from pure CeO2 to 100 at.% La-content nanorod supports. The most striking feature in the figure is the high activity of the Au/Ce0.75 -La0.25 nanorod catalyst with the 100% conversion at temperature as low as 30 °C. In contrast, the other Au/La-Ce catalysts showed lower activity compared to Au/Ce0.75 -La0.25 nanorods catalysts under the same reaction conditions. The results indicated that La doping has very much impact on this high CO conversion activity with a La content of 25 at.%, while a further increase results in a significant drop in activity. This again closely mirrors the trends seen in the reducibility of the samples, where an increase of La content from 25 at.% results in a strong loss of reducibility.
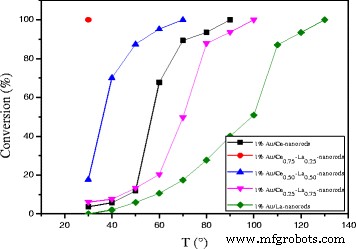
Catalytic activities of 1% Au/ La-Ce nanorods with different La content calcined at 300 °C for 2 h
In consideration of the preparation methods, gold loadings, gold particle size and distribution on different Ce-La nanorods supports, XRD, TEM and XPS data showed that all the catalysts should have the same number and type of active Au sites. So this high activity of the Au/Ce0.75 -La0.25 nanorods catalysts correlates well with the reducibility data discussed above. H 2 -TPR results indicated that Au/Ce0.75 -La0.25 nanorods has the lowest reducibility temperature and highest reducibility in the region of 50–400 °C, especially in the region of 50–150 °C, which could exactly approach the region of reaction temperature. In the process of reaction, the Ce0.75 -La0.25 nanorod support served as oxygen carrier. The reducibility of Ce0.75 -La0.25 nanorods could promote the formation of active oxygen. That is to say high reducibility of the catalyst, good activity the catalyst has. Au/Ce0.75 -La0.25 nanorod catalyst subsequently has the best activity.
Effect of Gold Content
The catalytic activities for CO oxidation were measured from low conversion to 100% conversion for the Au/Ce0.75 -La0.25 nanorod catalysts calcined at 300 °C for 2 h with a series of low gold contents. As shown in Fig. 10, all of the catalysts showed high catalytic activities. The CO conversion increased greatly with increasing gold content. The complete CO conversion could be attained at 50 °C over 0.5% Au/Ce0.75 -La0.25 nanorod catalyst. The size and chemical states of gold nanoparticles are generally thought to be vital for the performance of supported gold catalysts. It has been reported that its gold nanoparticles with the diameter of < 5 nm would be suitable for the supported gold catalysts in the catalytic CO oxidation [27, 28]. The XPS data proved that gold in Au/Ce0.75 -La0.25 nanorod catalyst exists in the form of cationic Au + . TEM images of the samples were also shown to investigate the diameter of gold nanoparticles in the catalysts. Consequently, the gold particles of Au/Ce0.75 -La0.25 nanorods were detected as sub-nanometer. Taking into account the particle size, mass content, and chemical states of the gold nanoparticles, gold particles with small diameter highly dispersed on the surface of Ce0.75 -La0.25 nanorods and interacted strongly with the support [17, 21, 23]. The strong interaction between gold particles and the support would help improve CO adsorption and accelerate active oxygen spillover to gold particles from the support, so 0.5% Au/Ce0.75 -La0.25 nanorods which had relatively high content of gold should exhibit the best CO oxidation activity. In fact, 0.5% Au/Ce0.75 -La0.25 nanorods indeed present high performance. The results demonstrated the activity of supported gold catalysts is strongly dependent on the gold nanoparticle size, chemical states, and the quantity of the active species, an increase of which implied an increase of the catalytic activity. In the case of Au/Ce0.75 -La0.25 nanorod catalyst, catalysts with low gold content could also exhibits high activity at low temperature, which would promote the progress of supported gold catalyst. The results indicated that supported gold catalysts prepared by deposition-precipitation with pH value of 6–10 for HAuCl4 solution could have high catalytic activity due to small diameter of gold nanoparticles, corresponding with the references [8,9,10].
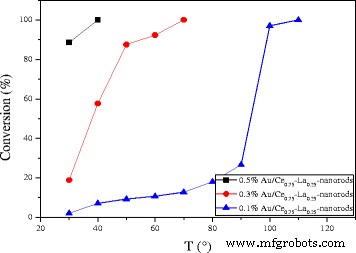
Catalytic activities of Au/Ce0.75 -La0.25 nanorods with different gold goadings calcined at 300 °C for 2 h
Effect of Calcination Temperature
The effect of calcination temperature on the catalytic activity of 0.5%Au/Ce0.75 -La0.25 nanorods is also shown in Fig. 11. The results indicated an increase in the activity of catalyst with the calcination temperature from 80 to 300 °C. The 0.5% Au/Ce0.75 -La0.25 nanorod catalyst calcined at 200 °C could convert CO to CO2 completely at 80 °C. While for 0.5% Au/Ce0.75 -La0.25 nanorod catalyst calcined at 80 °C, the temperature increased to 100 °C. The results showed that CO conversion increased with increasing calcinations temperature. Then, for the sample calcined at 400 °C, about 90% CO can be converted to CO2 at 100 °C and CO could be converted to CO2 completely at 120 °C. The sample calcined at 300 °C possessed the best catalytic activity. The catalytic performance of supported gold catalysts strongly depends on gold nanoparticle size and metal-support interaction due to “synergic effect” at the gold-support interface [10, 13, 15, 18]. The gold-support interaction largely depended on calcination temperature of catalysts. The electron could transfer from gold to the support [10]. Thus, with increasing calcination temperature, the charges on gold particles became increasingly positive, which is good for the enhancement of catalytic activity for CO oxidation. Here, as shown in the Fig. 5, size of gold particles in the catalysts calcined at 300 °C was small. The XPS data also indicated that gold was main Au δ+ after calcination at 300 °C. Thus, the stronger metal-support interaction could account for the relative good catalytic performance for catalysts calcined at 300 °C. From 80 to 300 °C, the higher the calcination temperature is, the stronger interaction exists between gold particles and support. As a consequence, from 80 to 300 °C, the activity of catalysts increased. However, after the 0.5% Au/Ce0.75 -La0.25 nanorod catalyst calcined at 400 °C, complete conversion temperature increased. The main reason might be that the high-temperature treatment led to increased mobility and growth of gold nanoparticles, which correspondingly led to the loss of catalytic activity. The XPS also suggested that the catalysts calcined at 400 °C, Au was mainly Au 0 . It could be concluded that the activities of supported gold nanoparticles were influenced by both the oxidation state and the size of gold nanoparticles, and the appropriate calcination temperature was 300 °C.
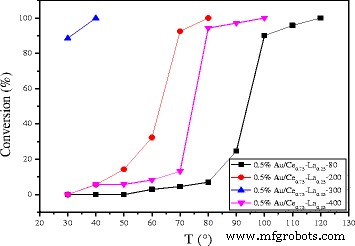
Catalytic activities of 0.5% Au/Ce0.75 -La0.25 nanorods calcined at different temperatures
Stability Observations
The stability of the 0.3% Au/Ce0.75 -La0.25 nanorod catalyst during CO oxidation at different reaction temperatures was measured, as shown in Fig. 12a. When the reaction was carried out at 70 °C, the initial CO conversion over 0.3% Au/Ce-La catalyst can reach 100% and has almost no change with continuously increasing reaction time. 0.3% Au/Ce-La catalyst with 60% CO conversion rate at 40 °C is also attained even after 10-h running period, and no obvious decline in CO conversion is observed. Although the catalytic activity of 0.3% Au/Ce0.75 -La0.25 nanorod catalyst at 40 °C was lower than that of 0.3% Au/Ce0.75 -La0.25 nanorod catalyst at 70 °C, the conversion of CO over the catalysts at both temperatures still seemed to be stable over 10 h on stream. It is thought that the catalyst was of good durability. It was clear that the activity over 0.3% Au/Ce0.75 -La0.25 nanorod catalyst did not strongly depend on the reaction temperature. As the reaction temperature decrease the activation rate barely becomes little slower and then finally reaching a steady state in which the CO conversion was still around 90%. For comparison, the stability of 0.5% Au/Ce0.75 -La0.25 nanorod catalyst at the reaction temperature of 40 °C with initial conversion of 100% was also provided in Fig. 12b. It was obvious that in 10 h, no decrease of CO conversion for 0.5% Au/Ce0.75 -La0.25 nanorods was detected. The results depicted that with the change of gold content, Au/Ce0.75 -La0.25 nanorods could still perform good stability.
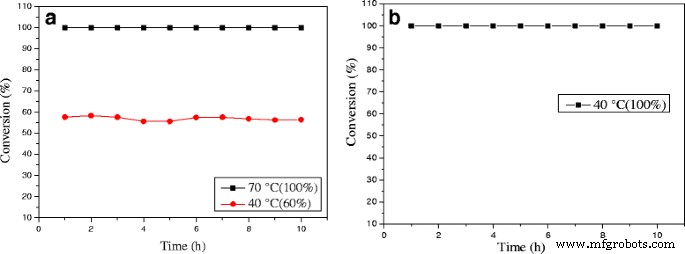
The stability of 0.3% Au/Ce0.75 -La0.25 nanorods, reaction temperature:40 and 70 °C (a ) and 0.5% Au/Ce0.75 -La0.25 nanorods, reaction temperature:40 °C (b ) for the CO oxidation
As engine efficiency increases and automotive exhaust temperatures decrease, traditional supported gold catalysts would be insufficient to meet emission regulations. And there are also a number of industrial catalytic processes which (e. g., the catalytic oxidation of CO in automotive exhaust gas) are sometimes carried out at high temperatures. Thus, the development of new catalysts that are active at lower temperature, yet still stable at periodic high temperatures, will be vital. In the two regards, catalysts with good activity at low temperature that are stable at high reaction temperatures are desirable. It is necessary to investigate their catalytic performance for CO oxidation at a certain high temperature which is a very stringent test for the stability of gold nanocatalysts against sintering. In the present work, the stability of 0.3% Au/Ce0.75 -La0.25 nanorod catalyst was also measured at 200 °C (100%) for high-temperature treatment. As shown in Fig. 13, no decline of catalytic activity was observed within 50 h indicates that the catalyst keeps good stability within 50 h. Remarkably, very few serious gold sintering occurred during the reaction. It indicated that 0.3% Au/Ce-La catalyst can exhibit good catalytic stability at both low and high reaction temperatures.
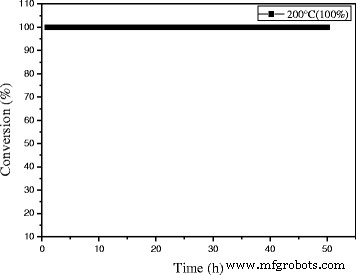
The stability of 0.3% Au/Ce0.75 -La0.25 nanorods at the reaction temperature of 200 °C for CO oxidation
Reaction Mechanism Speculate
Combined with H2 -TPR and XPS experiments, it suggested that CO oxidation over LaO x -doped CeO2 -supported Au catalysts might follow the Langmuir–Hinshelwood + Redox mechanism [1, 20, 26, 30, 32]. The XPS results suggest that there are Ce 3+ and Ce 4+ on the surface of the catalyst. H 2 -TPR data also proved that reducibility of this binary Ce-La nanorod oxides could be promoted by Au deposition. The reducibility of Au/Ce-La nanorods was much higher than pure Au/CeO2 or Au/LaO x catalysts. This would help the produce of oxygen vacancies. The oxygen vacancy is a very lively activity center. The active center can promote the activation of O2 . Thus, the CO oxidation reaction could become more easily. There are also amount of adsorbed oxygen species on the surface of catalyst. Usually adsorbed oxygen species play an important role in the oxidation of CO. The O2 of the reaction will form the chemisorbed oxygen, and the oxygen vacancy would be replenished by O2 of reaction gas to form new active lattice oxygen. XPS data also proved that gold in the catalysts was mainly Au δ+ species, which would accelerate the adsorption of CO. The possible reaction mechanisms of Au/Ce-La nanorod catalyst could be described as follows. Firstly, CO and O2 were chemisorbed on the surface of the catalysts. Then, the chemisorbed oxygen directly reacts with CO, or the active lattice oxygen of the catalyst reacts with CO, and the catalyst produced the oxygen vacancy with oxygen from gas-phase O2 . At last, CO was oxidized into CO2 (shown in Fig. 14).
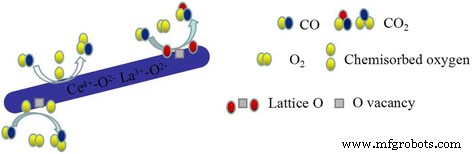
Proposed CO reaction pathways over the catalysts, Au/Ce-La nanorods
Conclusions
In summary, a series of mixed Ce-La nanorods with various amounts of La was prepared via a simple hydrothermal reaction at high concentration of NaOH and without surfactant. Gold was loaded by deposition-precipitation. After La doping, the composite could retain the initial rod morphology. As a result, Ce-La nanorods with 25 at.% La maintained the optimal nanorods with the length of 0.6 um and the diameter of 3–5 nm. Gold particles were dispersed well on the support. The reducibility of Ce-La nanorods could be affected significantly by LaO x doping. The deposition of gold had important influence on the reducibility of catalyst. Thus, the CO oxidation activity of Au/Ce-La nanorods was essentially changed in comparison with pure Au/CeO2 and Au/La nanorods. One percent Au/Ce0.75 -La0.25 nanorods could convert CO to CO2 completely at 30 °C. Further increase in La content results in decreased activity due to the decrease in reducible oxygen sites. The Au/Ce0.75 -La0.25 nanorod catalyst with low gold concentration also showed high activity. With the increase of gold content, there is an increase in the activity. The stability test of 0.3% Au/Ce0.75 -La0.25 nanorods indicated that the catalyst not only kept 100% conversion after continuous operation for 10 h under 70 °C but also showed no deactivation after 10 h on stream at 40 °C. As expected, the activity of 0.3% Au/Ce0.75 -La0.25 nanorods also retained a 100% CO conversion during 50 h at 200 °C. The results revealed that LaO x as the dopant could grow together with CeO2 in one rod. The 1D binary mixed Ce-La nanorods could be a good support for precious metal group catalysts with low content of gold.
Nanomateriais
- Avanços e desafios dos nanomateriais fluorescentes para aplicações biomédicas e de síntese
- Síntese biogênica, caracterização e avaliação do potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
- Síntese de nanofibra de sílica condutora elétrica / nanopartícula composta de ouro por pulsos de laser e técnica de pulverização catódica
- Biossegurança e capacidade antibacteriana do grafeno e do óxido de grafeno in vitro e in vivo
- Síntese de nanocristais de ZnO e aplicação em células solares de polímero invertido
- Síntese de aquecimento de estado sólido de composto de poli (3,4-etilenodioxitiofeno) / ouro / grafeno e sua aplicação para determinação amperométrica de nitrito e iodato
- Síntese fácil de óxido de estanho mesoporoso semelhante a buraco de minhoca via auto-montagem induzida por evaporação e propriedades aprimoradas de detecção de gás
- Síntese de um vaso de nanoplacas Cu2ZnSnSe4 e sua atividade fotocatalítica orientada por luz visível
- Platycodon saponins from Platycodi Radix (Platycodon grandiflorum) para a síntese verde de nanopartículas de ouro e prata
- Síntese Verde de Nanopartículas de Metal e Óxido de Metal e Seu Efeito na Alga Unicelular Chlamydomonas reinhardtii



