Adepto verde na síntese e estabilização de nanopartículas de cobre:atividades catalíticas, antibacterianas, citotoxicidade e antioxidantes
Resumo
Nanopartículas de cobre (CuNPs) são de grande interesse devido às suas propriedades extraordinárias, como alta relação superfície-volume, alta resistência ao escoamento, ductilidade, dureza, flexibilidade e rigidez. CuNPs mostram atividades catalíticas, antibacterianas, antioxidantes e antifúngicas, juntamente com citotoxicidade e propriedades anticâncer em muitas aplicações diferentes. Muitos métodos físicos e químicos foram usados para sintetizar nanopartículas, incluindo ablação a laser, processo assistido por micro-ondas, sol-gel, co-precipitação, descarga de fio pulsado, deposição de vapor a vácuo, irradiação de alta energia, litografia, moagem mecânica, redução fotoquímica, eletroquímica , síntese por electrospray, reação hidrotérmica, microemulsão e redução química. A fitossíntese de nanopartículas tem sido sugerida como uma alternativa valiosa aos métodos físicos e químicos devido à baixa citotoxicidade, perspectivas econômicas, favorável ao meio ambiente, biocompatibilidade aprimorada e alta atividade antioxidante e antimicrobiana. A revisão explica as técnicas de caracterização, seu principal papel, limitações e sensibilidade usadas na preparação de CuNPs. Uma visão geral das técnicas usadas na síntese de CuNPs, procedimento de síntese, parâmetros de reação que afetam as propriedades dos CuNPs sintetizados e uma análise de triagem que é usada para identificar fitoquímicos em diferentes plantas é apresentada a partir da literatura publicada recente que foi revisada e resumida . São apresentados mecanismos hipotéticos de redução do íon cobre pela quercetina, estabilização das nanopartículas de cobre pela santina, atividade antimicrobiana e redução do 4-nitrofenol com ilustrações diagramáticas. O objetivo principal desta revisão foi resumir os dados de plantas utilizadas para a síntese de CuNPs e abrir um novo caminho para os pesquisadores investigarem aquelas plantas que não foram utilizadas no passado.
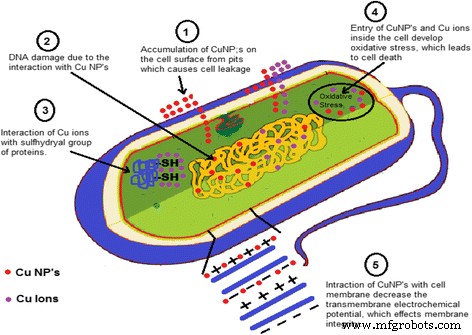
Mecanismo proposto para atividade antibacteriana de nanopartículas de cobre.
Histórico
Nanopartículas (NPs) têm uma série de aplicações interessantes no campo industrial, como tecnologia espacial, magnetismo, optoeletrônica e eletrônica, cosméticos e aplicações catalíticas, farmacêuticas, biomédicas, ambientais e de energia [1, 2]. As propriedades extraordinárias de NPs, como ductilidade, alta resistência ao escoamento, dureza, flexibilidade, rigidez, alta relação superfície-volume, efeito de tunelamento macroquântico e tamanho quântico são atribuíveis em comparação às propriedades de materiais a granel com a mesma composição química [3 ] Na verdade, as propriedades das NPs, que podem diferir consideravelmente daquelas observadas para partículas finas, são área de superfície específica maior, propriedades ópticas específicas, pontos de fusão mais baixos, magnetizações específicas, resistência mecânica e inúmeras aplicações industriais [4]. Nanopartículas de cobre (CuNPs) são de grande interesse devido à fácil disponibilidade, baixo custo e suas propriedades semelhantes às dos metais nobres [5,6,7,8,9]. CuNPs também podem ser usados em sensores, sistemas de transferência de calor [10,11,12] e eletrônicos (célula de combustível e célula solar), como catalisadores em muitas reações e como agentes bactericidas e antimicrobianos usados para revestir equipamentos hospitalares [13,14, 15,16,17,18,19].
Muitos métodos físicos e químicos, incluindo ablação a laser [20], processo assistido por micro-ondas, sol-gel [21], co-precipitação [22], descarga de fio pulsado [23], deposição de vapor a vácuo [24], irradiação de alta energia [ 25], litografia [26], moagem mecânica [27], redução fotoquímica, eletroquímica [28,29,30,31,32], síntese por eletrospray [33], reação hidrotérmica [34], microemulsão [35] e redução química são usados para sintetizar nanopartículas. Embora os métodos físicos e químicos produzam nanopartículas puras e bem definidas, esses métodos não são econômicos nem ecológicos devido ao uso de produtos químicos tóxicos. Um dos critérios mais importantes da nanotecnologia é o desenvolvimento de procedimentos ecológicos, não tóxicos e de química verde limpa [36]. Portanto, a biossíntese de nanopartículas contém um método baseado na química verde que emprega diferentes corpos biológicos, como plantas [37, 38], actinomicetos [39, 40], fungos [41,42,43,44], bactérias [45,46, 47,48,49], levedura [50,51,52] e vírus [53, 54]. As entidades biológicas oferecem uma abordagem não tóxica, limpa e favorável ao meio ambiente para sintetizar os NPs com uma ampla gama de tamanho, propriedades físico-químicas, formas e composições [55].
Nanopartículas de cobre foram sintetizadas e estabilizadas na literatura usando diferentes plantas, como Euphorbia esula [56], Punica granatum [57], Ocimum sanctum [58], Ginkgo biloba [59], Calotropis procera [60], Lawsonia inermis [61], Citrus medicalinn [62], Camellia sinensis [63], Datura innoxia [64], Syzygium aromaticum [65], Sesamum indicum [66], Citrus limon , Curcumina açafrão [67], Gloriosa superba L. [68], Ficus carica [69], Aegle marmelos [70], Caesalpinia pulcherrima [71], fístula de cássia [72], Leucas aspera , Leucas chinensis [73], Delonix elata [74], Aloe barbadensis Miller [75], Thymus vulgaris [76], Phyllanthus emblica [77], Magnolia kobus [78], Eucalipto [79], Artabotrys odoratissimus [80], Capparis zeylanica [81], Vitis vinifera [82], Hibiscus rosa-sinensis [83], Zingiber officinale [84], Datura metel [85], Zea mays [86], Urtica , Matricaria chamomilla , Glycyrrhiza glabra , Schisandra chinensis , Inula helenium , Cinnamomum [87], Dodonaea viscosa [88], Cassia auriculata [89], Azadirachta indica , câmera Lantana , Tridax procumbens [90], Allium sativum [91], Asparagus adscendens , Bacopa monnieri , Ocimum bacilicum , Withania somnifera [92], Smithia sensitiva , Colocasia esculenta [93], Nerium oleander [94] e Psidium guajava [95]; usando diferentes algas / fungos, como Phaeophyceae [96], Stereum hirsutum [97] e Hypocrea lixii [98]; e usando alguns microrganismos como Pseudomonas fluorescens [99] e Enterococcus faecalis [100] culturas.
Biossíntese de Nanopartículas de Cobre
Partes da planta usadas para extração
Diferentes partes das plantas são usadas para a preparação de extratos vegetais, como folhas, sementes, cascas, frutas, cascas, fibras de coco, raízes e goma. Folhas e raízes são usadas de duas maneiras. Em primeiro lugar, as folhas e raízes frescas são usadas para a preparação de extratos de plantas e, em segundo lugar, as folhas e raízes secas em forma de pó são usadas.
Procedimento para a síntese de CuNPs
Para a síntese de CuNPs, o extrato vegetal foi preparado usando diferentes partes de diferentes plantas. Para síntese do extrato parcial da planta de interesse, as folhas são coletadas e lavadas com água corrente e posteriormente com água destilada para remoção de partículas de poeira. As folhas lavadas são utilizadas de duas maneiras. Primeiro, essas folhas são secas ao sol por 1–2 h para remover a umidade residual. Os pesos conhecidos dessas folhas secas ao sol são divididos em pequenas partes e embebidos em água desionizada ou solução de etanol. Esta mistura é agitada durante 24 h à temperatura ambiente usando um agitador magnético e depois filtrada para uso posterior. Em segundo lugar, essas folhas são secas ao sol por 4–7 dias ou secas em um forno a 50 ° C por 1 dia e pulverizadas em um liquidificador doméstico. Peso conhecido de pó vegetal é misturado em água ou solução de etanol e, em seguida, agitado e filtrado.
Para a síntese de CuNPs, uma solução aquosa de sais precursores como sulfato de cobre, cloreto de cobre, acetato de cobre e nitrato de cobre com diferentes concentrações é misturada com extrato vegetal. A solução aquosa de hidróxido de sódio também é preparada e adicionada à mistura de reação para controlar o pH do meio. A mistura de reação é fortemente agitada por diferentes intervalos de tempo em um agitador elétrico e aquecida em um forno em diferentes intervalos de tempo e em diferentes temperaturas. A formação de CuNPs também pode ocorrer à temperatura ambiente e é confirmada pela alteração da cor da mistura de reação. Ao final, as nanopartículas foram centrifugadas e secas em diferentes temperaturas. As otimizações de reação ocorrem alterando o pH da mistura, a concentração do sal precursor, o tempo de aquecimento e a temperatura da mistura de reação. Na literatura, diferentes plantas têm sido usadas para a formação de nanopartículas de cobre usando diferentes sais precursores com diferentes condições de reação, conforme mostrado na Tabela 1. A partir da tabela, pode-se ver que as diferentes condições de reação afetam a forma e o tamanho do cobre. nanopartículas.
Efeito dos parâmetros de reação nas propriedades de NPs
A concentração de extrato vegetal desempenha um papel principal na redução e estabilização dos CuNPs. Foi relatado que ao aumentar a concentração do extrato da planta, o número de partículas aumentou [88]. Ao aumentar a concentração do extrato vegetal, a concentração de fitoquímicos aumentou e a redução do sal de cobre também aumentou. Devido à rápida redução do sal metálico, o tamanho das nanopartículas também diminuiu [101].
O tamanho e a estrutura dos CuNPs são altamente afetados pelo sal de cobre. A morfologia das nanopartículas muda quando o sal (por exemplo, cloreto de cobre, acetato de cobre, nitrato de cobre ou sulfato de cobre) é usado na presença de hidróxido de sódio. Foi relatado que a forma era triangular e tetraedro no caso do cloreto de cobre, em forma de bastonete no caso do acetato de cobre e esférica no caso do sulfato de cobre [102]. Ao aumentar a concentração do sal precursor, o tamanho dos CuNPs também aumentou.
A síntese de CuNPs dá melhores resultados, variando o pH do meio de reação dentro da faixa preferida. O tamanho das nanopartículas foi controlado alterando o valor de pH da mistura de reação. Em pH mais alto, nanopartículas de menor tamanho foram obtidas em comparação com aquelas obtidas em valor de pH baixo. Essa diferença pode ser atribuída à diferença na taxa de redução dos sais metálicos pelo extrato vegetal. A relação inversa entre o valor do pH e o tamanho da nanopartícula mostrou que um aumento no valor do pH nos permite obter nanopartículas esféricas de pequeno tamanho, enquanto uma diminuição no valor do pH resulta em nanopartículas de grande tamanho (em forma de bastonete e triangular). O efeito no espectro de absorção de diferentes valores de pH (4, 6, 8, 10 e 12) é representado na Fig. 1 [36]. Foi relatado que a adição de extrato vegetal ao CuCl 2 não levou à formação de CuNPs, mas, em vez disso, os CuNPs foram obtidos alterando o pH da mistura de reação para meio básico. O mesmo comportamento foi observado por Wu e Chen, e concluiu-se que o pH desempenha um papel importante na síntese de CuNPs [103].
Partes da planta utilizadas para a preparação do extrato vegetal
Mecanismo para Fitosíntese de Nanopartículas de Cobre
Triagem fitoquímica:uma análise qualitativa
A análise fitoquímica é uma análise química realizada para a detecção de fitoquímicos em diferentes plantas. Extrato vegetal fresco com produtos químicos ou reagentes químicos é usado para esta análise [77], conforme mostrado na Tabela 2.
Fitoquímicos para redução de metal e estabilização de NPs
A síntese verde de CuNPs pelo uso de fitoquímicos oferece um controle mais flexível sobre a forma e o tamanho dos NPs (ou seja, alterando a temperatura de reação, concentração de extrato vegetal, concentração de sal de metal, tempo de reação e pH da mistura de reação). A mudança de cor do meio de reação indica redução do íon metálico e formação de NPs. A redução verde dos sais de cobre começa instantaneamente, e a formação de nanopartículas de cobre é indicada pela mudança de cor da mistura de reação. Os fitoquímicos têm um papel principal em primeiro reduzir os íons metálicos e, em seguida, estabilizar os núcleos do metal na forma de nanopartículas, conforme mostrado na Fig. 2. A interação dos fitoquímicos com os íons metálicos e a concentração desses fitoquímicos controlam a forma e o tamanho dos CuNPs.
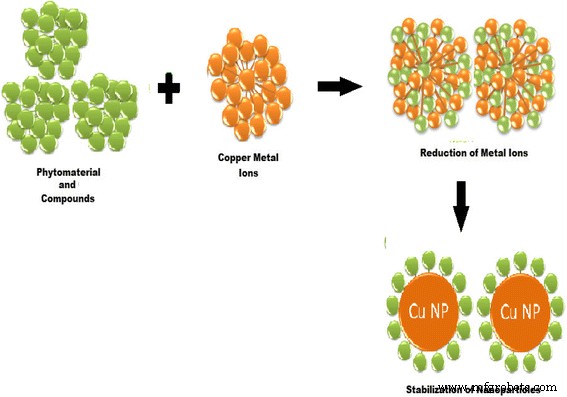
Um protocolo para reduzir os íons metálicos e, em seguida, estabilizar os núcleos do metal
Os flavonóides contêm compostos polifenólicos, por exemplo, quercetina, catequinas, flavanonas, isoflavonas, santina, penduletina, alizarina, pinocembrina, antocianinas, flavonas, taninos e saponinas, que estão presentes em diferentes plantas, como Ginkgo biloba [59], Citrus medicalinn [62], Phyllanthus emblica [77], Hibiscus rosa-sinensis [83], e Dodonaea viscosa [93]. Esses compostos desempenham um papel principal na redução e quelação do metal. Vários grupos funcionais presentes nos flavonóides são responsáveis pela redução do íon cobre. Foi assumido que um átomo de hidrogênio reativo nos flavonóides pode ser liberado durante as alterações tautoméricas da forma enol para a forma ceto, o que pode reduzir os íons de cobre para formar núcleos de cobre ou CuNPs. Por exemplo, presume-se que no caso de Ginkgo biloba extratos de plantas, é a transformação da quercetina (flavonóide) que desempenha um papel principal na redução de íons de cobre em núcleos de cobre ou CuNPs devido à mudança da forma enol para a forma ceto, como mostrado na Fig. 3.
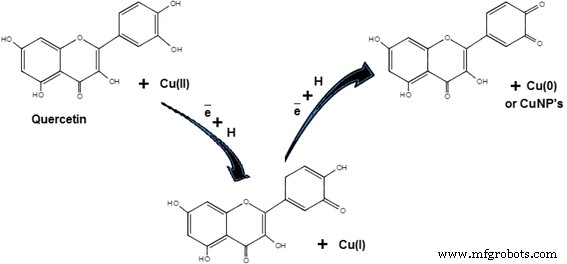
Redução de íons de cobre pela quercetina
Durante o processo de síntese de CuNPs, íons metálicos com estados de oxidação monovalente ou divalente são convertidos em núcleos de cobre de oxidação zero e esses núcleos são fundidos para obter formas diferentes. Durante a nucleação, os núcleos se agregam para formar diferentes formas, como fios, esferas, cubos, hastes, triângulos, pentágonos e hexágonos. Alguns flavonóides têm a capacidade de quelar os CuNPs com seus π elétrons e grupos carbonil. A quercetina e a santina são flavonóides com forte atividade quelante devido à presença de dois grupos funcionais envolvendo as hidroxilas e as carbonilas. Esses grupos quelam com nanopartículas de cobre seguindo o mecanismo anterior e também explicam a capacidade de adsorção de santina (flavonóide) na superfície de CuNPs, conforme mostrado na Fig. 4.
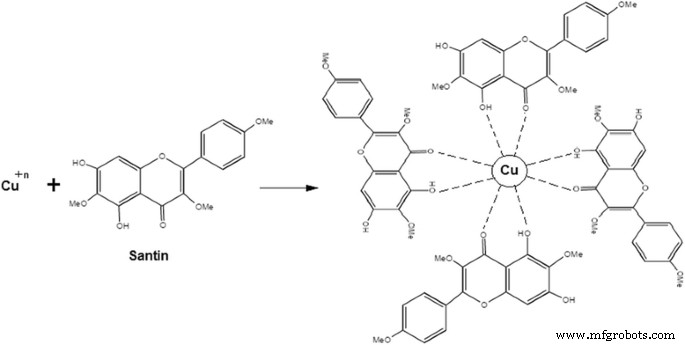
Estabilização de nanopartículas de cobre por santina
Foi assumido que as moléculas de proteína (superóxido dismutase, catalase, glutationa) em diferentes plantas, como Hibiscus rosa-sinensis [83] e Camellia sinensis [104] exibem uma alta atividade redutora para a formação de nanopartículas a partir de íons metálicos, mas sua atividade quelante não é excessiva. Açúcares como monossacarídeos (glicose), dissacarídeos (maltose e lactose) e polissacarídeos em Camellia sinensis planta [63] pode atuar como agentes redutores ou antioxidantes e ter uma série de transformações tautoméricas de cetona em aldeído.
Outros fitoquímicos, como polifenóis (por exemplo, ácido elágico e ácido gálico) que estão presentes em Hibiscus rosa-sinensis [40], fenilpropanóides (fenilalanina, tirosina) em Aegle marmelos [70], terpenóides em Ocimum sanctum e Asparagus adscendens [58, 92], proteases de cisteína em Calotropis procera [60], curcuminanilineazometina em curcumina de cúrcuma [67], ácido ascórbico em Citrus medicalinn [62], eugenol em Syzygium aromaticum [65] e alcalóides em Aegle marmelos [70] desempenham o mesmo papel de reduzir os íons de cobre e estabilizar as nanopartículas de cobre. Carboidratos, antraquinona, quinona e antocianósido em Phyllanthus emblica [77]; ligninas e xantonas em Hibiscus rosa-sinensis [83]; e glicosídeo cardíaco, triterponóide, glicosídeo carotenóide e glicosídeo antraquinona em Colocasia esculenta plant [93] também são fitoquímicos que estão presentes em extratos de diferentes plantas e atuam como agentes redutores e estabilizadores. Exemplos de certos fitoquímicos com estruturas são mostrados na Fig. 5.
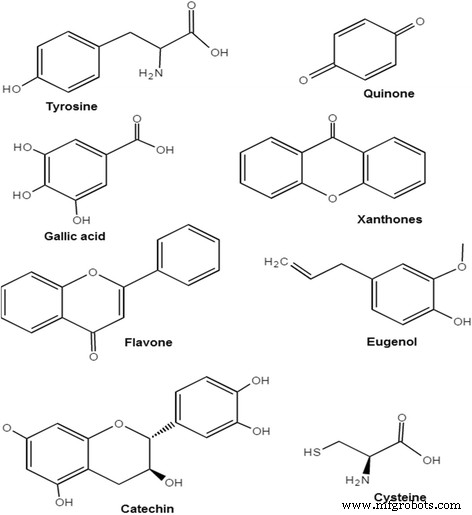
Fitoquímicos com suas estruturas
Técnicas de caracterização
Para a caracterização das nanopartículas sintetizadas, diferentes técnicas foram utilizadas, tais como espectroscopia ultravioleta-visível (UV-vis), microscopia eletrônica de transmissão (TEM), espalhamento de raios-X de baixo ângulo (SAXS), espectroscopia infravermelha por transformada de Fourier (FTIR), X- espectroscopia de fluorescência de raios (XRF), difração de raios X (XRD), espectroscopia de fotoelétrons de raios X (XPS), microscopia eletrônica de varredura (SEM), microscopia eletrônica de varredura de emissão de campo (FESEM), análise de tamanho de partícula (PSA), Malvern Zetasizer ( MZS), espectroscopia de energia dispersiva de raios-X (EDX / EDS), análise de rastreamento de nanopartículas (NTA), refletometria de raios-X (XRR), análise Brunauer-Emmett-Teller (BET), difração de elétrons de área selecionada (SAED) e microscopia de força atômica (AFM) (Tabela 3).
Aplicações de nanopartículas de cobre
Devido às suas excelentes propriedades químicas e físicas, grande relação superfície-volume, superfície constantemente renovável, baixo custo e preparação não tóxica, os CuNPs têm sido de grande interesse para aplicações em diferentes campos. Nanopartículas de cobre apresentam atividade catalítica, atividade antibacteriana, citotoxicidade ou atividade anticâncer, atividade antioxidante e atividade antifúngica em diferentes aplicações. Na atividade catalítica, nanopartículas de cobre são usadas para a cicloadição Huisgen [3 + 2] de alcinos e azidas em muitos solventes sob condições livres de ligante [59], 1-metil-3-fenoxibenzeno, 3,3-oxibis (metilbenzeno) [94], síntese de 1-substituído 1 H -1,2,3,4-tetrazol [76], adsorção de dióxido de nitrogênio e adsorção de dióxido de enxofre [66]. Na maioria dos metais de transição catalisados, ligantes de reação de acoplamento de Ullmann, como fosfinas, são relatados na literatura e a maioria dos ligantes são caros, difíceis de preparar e sensíveis à umidade. Para este trabalho, nanopartículas de cobre sintetizadas são utilizadas para o acoplamento de Ullmann livre de ligante de éter difenílico. Diferentes corantes e compostos orgânicos tóxicos e pesticidas presentes nos resíduos industriais são muito prejudiciais ao meio ambiente e aos organismos vivos. Nanopartículas de cobre são usadas para degradação de diferentes corantes, como azul de metileno [73], degradação da atrazina [86] e redução do 4-nitrofenol [76].
Entre os agentes antimicrobianos, os compostos de cobre têm sido comumente usados na agricultura como herbicidas [105], algicidas [106], fungicidas [107] e pesticidas, bem como na pecuária como desinfetante [108] (mostrado na Tabela 4). As nanopartículas biogênicas de cobre mostraram uma poderosa atividade antibacteriana contra patógenos gram-positivos e gram-negativos, como Pseudomonas aeruginosa (MTCC 424), Micrococcus luteus (MTCC 1809), Enterobacter aerogenes (MTCC 2832) [57], Salmonella enterica (MTCC 1253), Rhizoctonia solani , Xanthomonas axonopodis pv. citri , Xanthomonas axonopodis pv. punicea [58], Escherichia coli (ATCC 14948) [62], Staphylococcus aureus (ATCC 25923), Bacillus subtilis (ATCC 6633), Pediococcus acidilactici [69] e Klebsiella pneumoniae (MTCC 4030). Na atividade antifúngica, nanopartículas de cobre são usadas contra Alterneria carthami , Colletotrichum gloeosporioides , Colletotrichum lindemuthianum , Drechslera sorghicola , Fusarium oxysporum f.sp. carthami , Rhizopus stolonifer , Fusarium oxysporum f.sp. ciceris , Macrophomina phaseolina , Fusarium oxysporum f.sp. udum , Rhizoctonia bataticola [58], Candida albicans , Curvularia , Aspergillus niger e Trichophyton simii [67]. Na citotoxicidade, as nanopartículas de cobre são usadas para um estudo nas linhas celulares HeLa, A549, MCF7, MOLT4 e BHK21 (tumores cancerígenos) [60, 104].
Mecanismo hipotético de atividade antimicrobiana
Observou-se que os CuNPs apresentam excelente atividade antimicrobiana e apenas relatos limitados apresentam na literatura o mecanismo da atividade antibacteriana das nanopartículas de cobre, mas esses mecanismos são hipotéticos. Foi observado que bactérias e enzimas / proteínas foram destruídas devido à interação de CuNPs com o grupo –SH (sulfidrila) [109, 110]. Também foi relatado que a estrutura helicoidal das moléculas de DNA é perturbada pela interação de CuNPs [111]. A interação dos CuNPs com a membrana celular da bactéria diminuiu o potencial eletroquímico transmembrana e, devido à diminuição do potencial eletroquímico transmembrana, afetou a integridade da membrana [112]. Foi assumido que os NPs de metal liberam seus respectivos íons de metal. Nanopartículas de cobre e íons de cobre se acumulam na superfície celular da bactéria e formam caroços na membrana, causando vazamento do componente celular da célula e no interior da célula, causando estresse oxidativo que leva à morte celular [112,113,114]. Um mecanismo hipotético de atividade antibacteriana que representa as possibilidades acima é mostrado na Fig. 6.
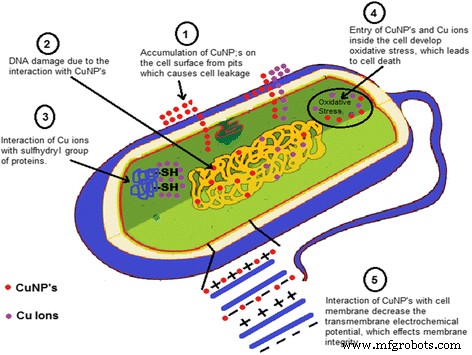
Mecanismo para atividade antibacteriana de nanopartículas de cobre
Atividade catalítica para redução de 4-nitrofenol
O 4-nitrofenol (4-NP), normalmente encontrado em águas residuais agrícolas e produtos industriais, é perigoso e não é amigo do ambiente. A hidrogenação ou redução do 4-NP, que é convertido em 4-aminofenol (4-AP), ocorre na presença de CuNPs. Os CuNPs podem catalisar a reação para superar a barreira cinética, auxiliando na transferência de elétrons dos íons borohidrato doadores para o receptor 4-NP.
A atividade catalítica dos CuNPs sintetizados tem sido estudada na redução de 4-nitrofenol em meio aquoso à temperatura ambiente na presença de solução aquosa de borohidreto de sódio [56]. A redução de 4-NP usando CuNPs é um processo simples e ecológico. A eficiência catalítica de CuNPs para a redução de 4-NP foi examinada usando um espectrômetro UV-vis. Observou-se que o pico máximo de absorção para 4-NP em meio aquoso estava em 317 nm e o pico de adsorção mudou para 403 nm pela adição de borohidreto de sódio devido à formação de íons 4-nitrofenolato. Um pico a 403 nm permaneceu inalterado mesmo após 2 dias, o que indicou que a redução de 4-NP não pode ocorrer na ausência de um catalisador. Depois de adicionar os CuNPs, o pico de absorção da solução mudou para 300 nm e o pico a 403 nm desapareceu completamente, o que indicou a redução de 4-NP para 4-AP sem qualquer produto secundário. Um mecanismo hipotético para a redução de 4-NP é mostrado na Fig. 7. No mecanismo, 4-NP e borohidreto de sódio estão presentes na solução na forma de íons. Os prótons do íon borohidreto são adsorvidos na superfície das nanopartículas de cobre e BO 2 produzido. Os íons 4-nitrofenolato também são adsorvidos na superfície dos CuNPs. Devido à adsorção de prótons e do íon 4-nitrofenolato, os CuNPs superam a barreira cinética dos reagentes e o íon 4-nitrofenolato é convertido no íon 4-aminofenolato. Após a conversão, ocorre a dessorção do íon 4-aminofenolato e este é convertido em 4-aminofenol.
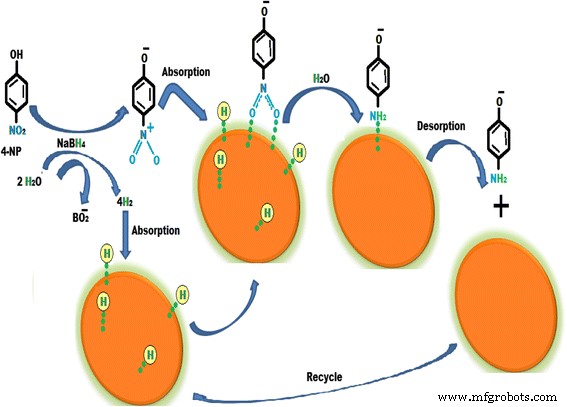
Mecanismo para a redução de 4-nitrofenol
Conclusões
Este artigo revisou e resumiu informações recentes de métodos biológicos usados para a síntese de nanopartículas de cobre (CuNPs) usando diferentes plantas. A síntese verde de CuNPs tem sido proposta como uma alternativa valiosa aos métodos físicos e químicos com baixa citotoxicidade, perspectivas econômicas, ambientalmente amigável, biocompatibilidade aprimorada, viabilidade e alta atividade antioxidante e alta atividade antimicrobiana dos CuNPs. O mecanismo de biossíntese dos NPs ainda é desconhecido, e mais pesquisas precisam ser focadas no mecanismo de formação das nanopartículas e no entendimento do papel dos fitoquímicos na formação dos NPs. Esta revisão fornece dados de plantas usadas na síntese de nanopartículas de cobre, procedimento de síntese e os parâmetros de reação que afetam as propriedades de CuNPs sintetizados. Uma análise de triagem fitoquímica é uma análise química usada para identificar os fitoquímicos, como detecção de carboidratos, taninos, saponinas, flavonóides, alcalóides, antraquinonas e antocianósidos em diferentes plantas. O mecanismo de redução do íon cobre pela quercetina e estabilização das nanopartículas de cobre pela santina é descrito neste artigo. As técnicas de caracterização utilizadas na literatura para nanopartículas de cobre são UV-vis, FTIR, XRD, SEM, FESEM, TEM, PSA, MZS, EDX, NTA, SAXS, XRR, XRF, XPS, BET, SAED e AFM. Nanopartículas de cobre apresentam atividade catalítica, atividade antibacteriana, citotoxicidade ou atividade anticâncer, atividade antioxidante e atividade antifúngica em diferentes aplicações. Mecanismos hipotéticos de atividade antimicrobiana e redução de 4-nitrofenol com diagramas são mostrados neste artigo.
CuNPs com diferentes propriedades estruturais e efeitos biológicos eficazes podem ser fabricados usando novos protocolos verdes nos próximos dias. O controle sobre o tamanho das partículas e, por sua vez, as propriedades dependentes do tamanho dos CuNPs abrirão novas portas para suas aplicações. Este estudo fornece uma visão geral da síntese de CuNP usando extrato de planta, extrato microbiano e biomoléculas de ocorrência natural. Embora todos esses protocolos verdes para a síntese de CuNP tenham suas próprias vantagens e limitações, o uso de extrato vegetal como redutor é mais benéfico em comparação ao uso de extrato microbiano por causa da rápida taxa de produção de nanopartículas com o antigo redutor verde.
Nanomateriais
- Síntese biogênica, caracterização e avaliação do potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
- Síntese fácil e propriedades ópticas de pequenos nanocristais de selênio e nanorods
- Preparação e atividade de hidrogenação catalítica aprimorada de nanopartículas de Sb / Palygorskite (PAL)
- Síntese One-Pot Green da Microsfera SnO2 Decorada com Ag:um Catalisador Eficiente e Reutilizável para Redução de 4-Nitrofenol
- Síntese fácil de compósito CuSCN colorido e condutor revestido com nanopartículas de CuS
- Síntese hidrotérmica de nanopartículas de In2O3 híbridos gêmeos heteroestruturas de ZnO de disco hexagonal para atividades fotocatalíticas aprimoradas e estabilidade
- Método de pós-tratamento para a síntese de nanopartículas FePt-Fe3O4 binárias monodispersas
- Platycodon saponins from Platycodi Radix (Platycodon grandiflorum) para a síntese verde de nanopartículas de ouro e prata
- Síntese Verde de Nanopartículas de Metal e Óxido de Metal e Seu Efeito na Alga Unicelular Chlamydomonas reinhardtii
- Síntese fácil de nanopartículas de irídio livres de ligante e sua biocompatibilidade in vitro



