Fabricação fácil de nanocompósitos mesoestruturados de borracha natural / sílica com estabilidade térmica e hidrofobicidade aprimoradas
Resumo
Nanocompósitos de borracha natural (NR) / sílica mesoporosa hexagonal (HMS) (NRHMS) com propriedades térmicas e hidrofóbicas aprimoradas foram facilmente preparados via in situ formação de sol-gel com ajuste de pH usando ácido sulfúrico baixo (H 2 SO 4 ) concentração de ácido. O efeito da quantidade de 0,5 M H 2 SO 4 (2,5–10 g) adicionado à mistura de pré-síntese nas propriedades físico-químicas dos nanocompósitos NRHMS obtidos foi investigado. Com uma pequena adição de H 2 SO 4 solução, o nanocompósito NRHMS fabricado possuía um arranjo de mesoestrutura tipo buraco de minhoca melhorado com uma parede de sílica mais espessa, que retardou a decomposição térmica da fase NR, conforme deduzido da auto-oxidação de NR por análise termogravimétrica. O H 2 A medição de adsorção-dessorção revelou um aumento da hidrofobicidade dos compósitos NRHMS, explicada pela ponte catalisada por ácido de grupos silanol livres para ligações de siloxano, que foi apoiada pela análise de espectroscopia de fotoelétrons de raios-X. A microscopia eletrônica de transmissão de varredura com mapeamento elementar de espectroscopia de raios-X dispersiva de energia revelou uma boa dispersão da fase NR dentro da sílica mesoestruturada. No entanto, uma grande quantidade de H 2 adicionado SO 4 solução levou à separação de fases sílica-NR devido à diminuição da interação hidrofóbica entre o precursor de sílica e a cadeia de borracha, bem como uma aglomeração da própria fase NR. O mecanismo de formação de nanocompósitos de NRHMS em condições de pH controlado foi proposto para proceder por meio de uma rota de automontagem cooperativa.
Introdução
Nas últimas décadas, o método de síntese baseado em molde soft tem sido utilizado para preparar uma variedade de materiais estruturados mesoporosos [1]. A sílica mesoporosa hexagonal (HMS) semelhante a um buraco de minhoca foi preparada com sucesso por meio de um modelo neutro com base na ligação de hidrogênio de aminas primárias de cadeia longa auto-montadas e precursores de sílica hidrolisada [2]. A escolha de HMS reflete suas propriedades físico-químicas excepcionais em comparação com a sílica mesoporosa periódica convencional, incluindo uma estabilidade térmica e hidrotérmica melhorada devido à parede de silicato mais espessa [3], tamanho de domínio pequeno com canais curtos [4, 5] e recuperação de modelo simplista com extração por solvente [6]. Além disso, a distinta estrutura em forma de esponja, que exibe uma estrutura mesoporosa complementar, melhora a acessibilidade da estrutura e facilita a difusão em massa [7,8,9]. Essas vantagens têm atraído interesse em HMS em muitos campos promissores, como catálise, entrega de drogas e adsorção [10,11,12,13,14,15].
A modificação das propriedades da superfície do HMS, tanto química quanto fisicamente, tem sido amplamente investigada para a preparação de materiais exclusivos que são adequados para vários fins específicos. Os materiais HMS modificados hidrofobicamente fornecem uma baixa afinidade com a água na superfície, embora ainda possuam suas propriedades distintas e, portanto, exibem um bom desempenho na adsorção de N -nitrosaminas da solução de extrato de tabaco [16] e liberação controlada de drogas pouco solúveis em água [17]. Além disso, uma hidrofobicidade aprimorada melhorou a estabilidade hidrotérmica dos materiais resultantes [18], tornando-os adequados para aplicações em soluções de fase aquosa. A modificação física de HMS com polímeros orgânicos é um método interessante para aumentar sua hidrofobicidade devido à sua abordagem relativamente fácil e baixo custo, e que fornece uma possível funcionalização posterior tanto da sílica quanto das fases orgânicas. A preparação de nanocompósitos de polímero à base de sílica mesoporosa foi amplamente resumida nos quatro métodos de (i) mistura, uma mistura direta de polímero e sílica mesoporosa por fusão ou mistura de solução [19, 20], (ii) in situ polimerização, uma dispersão da fase de sílica modificada por superfície em monômeros seguida por polimerização [21, 22], (iii) polimerização iniciada por superfície, um enxerto de frações poliméricas em sílica mesoporosa via interação covalente [23, 24], e (iv ) in situ formação de sol-gel, uma preparação direta por impregnação de moléculas poliméricas na estrutura de sílica [25] ou fabricação de um nanocompósito de sílica / polímero mesoporoso via automontagem de modelo suave [26].
Os nanocompósitos de borracha natural / sílica mesoporosa hexagonal (NRHMS) sinergizam as vantagens de uma matriz de sílica mesoporosa (estrutura ordenada, estabilidade térmica, alta área de superfície e simplicidade de funcionalização) com a fase de poliisopreno dispersa que oferece hidrofobicidade [27]. Além disso, a presença de ligações duplas carbono-carbono (C =C) na estrutura de isopreno pode ser potencialmente modificada quimicamente por meio de reações relacionadas ao alceno, como adição eletrofílica no C =C [28]. O in situ a síntese sol-gel de NRHMS, uma síntese de automontagem em um único recipiente, é uma estratégia simples sob uma condição moderada e produz um material com propriedades desejáveis [27]. A síntese foi realizada na presença de tetrahidrofurano (THF) como co-solvente, utilizando-se dodecilamina (DDA) como agente direcionador de estrutura e tetraetilortossilicato (TEOS) como precursor da sílica. Apesar de sua alta mesoporosidade e hidrofobicidade, a baixa estabilidade térmica da borracha natural (NR) incorporada foi uma grande desvantagem.
A presença de NR durante a formação da mesofase dificultou a hidrólise e condensação do precursor de sílica, deixando uma quantidade considerável de grupos etoxi e hidroxila remanescentes nos nanocompósitos resultantes, o que é prejudicial às suas propriedades físico-químicas [29, 30]. A taxa de hidrólise e condensação na formação da rede de sílica depende fortemente do pH [31, 32]. Lin et al. empregou um método de mudança de pH para a síntese de nanopartículas de sílica mesoporosa [33]. Solução de sulfato ácido e acetato de água foi usada para ajuste de pH, o que resultou em uma sílica mesoestruturada com uma parede de canal mais espessa e uma estabilidade térmica e hidrotérmica melhorada. No entanto, a melhoria na estabilidade térmica do NRHMS via ajuste de pH não foi estudada, mas sabe-se que a adição de uma solução de ácido suave na reação sol-gel afeta não apenas a rede de sílica, mas também as propriedades do NR [34 ]
Nesta pesquisa, exploramos uma abordagem simples para a fabricação de nanocompósitos NRHMS com estabilidade térmica aprimorada e hidrofobicidade com base no ajuste de pH usando uma solução de ácido sulfúrico suave (0,5 M H 2 SO 4 ) O efeito da quantidade de H adicionado 2 SO 4 sobre as propriedades físico-químicas e térmicas dos nanocompósitos NRHMS resultantes, bem como a dispersão da fase NR, foi investigado usando várias técnicas de caracterização. O ambiente químico, em termos de teor de carbono, oxigênio e sílica, forneceu informações úteis sobre a quantidade dependente do pH de grupos etoxi e hidroxila remanescentes. A fabricação fácil de nanocompósitos NRHMS por meio desta abordagem deu nanopartículas (NPs) de tamanho homogêneo, um arranjo de mesoestrutura hexagonal compacto e melhorado, área de superfície elevada e uma hidrofobicidade e estabilidade térmica aprimoradas, que são caracteres promissores para materiais catalíticos e adsorventes.
Métodos
Materiais e reagentes químicos
O TEOS e o DDA (ambos de grau AR, 98%) foram adquiridos da Sigma Aldrich, enquanto o H 2 SO 4 (98%), THF (99,5%) e etanol absoluto (99,9%) foram obtidos comercialmente (grau AR) do QRëC. O etanol (grau comercial, 95%) foi adquirido da Alcoh. O NR foi fornecido pela Thai Hua Chumporn Natural Rubber Co. Ltd (Tailândia). Todos os reagentes químicos e materiais foram usados sem purificação adicional.
Síntese de HMS puro
O HMS original foi sintetizado pela formação de sol-gel, conforme descrito em outro lugar [27]. Em um lote típico, 3,75 g de DDA foram dissolvidos em uma solução de THF (26,67 g) e água desionizada (53,05 g) com agitação e em seguida 10,5 g de TEOS foram adicionados gota a gota. A mistura foi envelhecida com agitação durante 1 dia a 40 ° C. Subsequentemente, o produto sólido branco foi recuperado por filtração e seco a 60 ° C durante 18 h. A remoção do modelo foi obtida por extração com 0,05 M H 2 SO 4 / etanol a 80 ° C durante 4 h, e o sólido resultante foi completamente lavado com etanol e seco a 60 ° C durante 12 h.
Síntese de nanocompósitos NRHMS
Uma folha de 0,5 g de NR foi diretamente inchada em 10,5 g de TEOS durante a noite. A folha de NR inchada, que absorveu 2 g de TEOS, foi então agitada durante a noite em 26,67 g de THF para obter uma mistura coloidal, à qual 3,75 g de DDA e 8,5 g de TEOS foram adicionados sequencialmente gota a gota com agitação. A seguir, 53,05 g de água desionizada foram adicionados gota a gota e a mistura resultante foi agitada e envelhecida a 40 ° C durante 2 dias. O produto sólido foi recuperado por precipitação em etanol, filtração e secagem a 60 ° C durante 18 h. A extração e acabamento do produto foram realizados no mesmo procedimento da síntese de HMS acima.
Síntese de nanocompósitos NRHMS usando um H baixo 2 SO 4 concentração para ajuste de pH
A mistura coloidal de NR preparada da mesma maneira conforme detalhado acima para a síntese de NRHMS foi envelhecida a 40 ° C por 1 dia e, em seguida, a quantidade necessária de 0,5 M H 2 SO 4 (0, 2,55, 5,10 ou 10,2 g) foi gotejado lentamente na mistura sob agitação para ajustar o pH, e a mistura foi posteriormente envelhecida por 1 dia. O produto sólido foi recuperado, extraído e completado pelo mesmo procedimento que para a síntese de NRHMS. Os nanocompósitos obtidos foram designados como NRHMS ( X ), onde X representa o peso (g) de 0,5 M H 2 SO 4 adicionado durante a síntese. A composição de peso dos materiais sintetizados é resumida no arquivo adicional 1:Tabela S1.
Caracterização de materiais sintetizados
A análise de difração de raios-X de pó (XRD) foi realizada em um difratômetro de raios-X Bruker D8 Advanced equipado com radiação Cu Kα operado a uma potência de raios-X de 40 kV e 40 mA. Os padrões de XRD foram registrados em temperatura ambiente, digitalizando a partir de 2 θ de 1 ° –10 ° a um tamanho de etapa de 0,02 ° e tempo de contagem de 1 s. O parâmetro de rede característico ( a 0 ) foi calculado a partir do espaçamento interplanar ( d -spacing) do pico de reflexão (100) usando a equação:\ ({a} _0 =2 {d} _ {100} / \ sqrt {3} \).
Nitrogênio (N 2 ) A medição de adsorção-dessorção a −196 ° C foi realizada em um analisador de área de superfície e porosidade Mircrometrics ASAP2020 para determinar as propriedades texturais dos materiais sintetizados. Todas as amostras foram desgaseificadas a 150 ° C por 2 h no aparelho de adsorção antes da análise. A área de superfície específica ( S APOSTA ) foi calculado usando a equação de Brunauer-Emmett-Teller (BET) a partir dos dados de adsorção dentro da pressão relativa ( P / P 0 ) intervalo de 0,02–0,2. Área de superfície externa ( S ext ) foi estimado a partir da inclinação do t -enredo. O volume do mesóporo ( V m ) foi calculado a partir da interceptação da porção linear do t -plotar na faixa de pressão relativa acima da qual N 2 foi condensado dentro dos mesoporos primários. A distribuição do tamanho dos poros foi determinada pelo cálculo de Barrett-Joyner-Halenda (BJH) usando os dados de dessorção. O volume total do poro ( V T ) foi obtido a partir do N 2 acumulativo volume adsorvido em P / P 0 de 0,990.
A análise termogravimétrica (TGA) foi usada para determinar o conteúdo de sílica e NR e a estabilidade térmica dos nanocompósitos. Cada amostra (cerca de 10 mg) foi aquecida de 40–850 ° C a uma taxa de rampa de 10 ° C / min sob um fluxo de ar (50 mL / min) usando um analisador termogravimétrico PerkinElmer Pyris Diamond.
A espectroscopia de infravermelho com transformada de Fourier (FTIR) foi aplicada para identificar os grupos funcionais e a fase NR nos materiais sintetizados. Os espectros de FTIR de transmitância foram registrados em um espectrômetro Nicolet iS10 FT-IR no intervalo de 500–4000 cm -1 com 64 digitalizações com resolução de 4 cm -1 .
A morfologia das amostras foi examinada por microscopia eletrônica de varredura por emissão de campo (FESEM) usando um instrumento HITACHI SU-8030 operado a 10 kV em uma grade de amostra pulverizada com ouro. A distribuição do tamanho de partícula foi medida pelo software ImageJ. O arranjo mesoestruturado dos materiais foi observado por microscopia eletrônica de transmissão (TEM) usando um microscópio eletrônico de transmissão JEOL JEM-2010 a uma tensão de aceleração de 200 kV. A distribuição dos elementos principais no material mesoporoso foi examinada por microscopia eletrônica de transmissão de varredura com mapeamento de espectroscopia de raios-X dispersiva de energia (STEM-EDS) usando um microscópio eletrônico de transmissão JEOL JEM-2010 na tensão de aceleração de 200 kV no modo de campo escuro.
O estado químico do carbono, silício e oxigênio na superfície dos materiais sintetizados foi analisado por espectroscopia de fotoelétrons de raios-X (XPS) usando um espectrômetro de fotoelétrons de raios-X Kratos Axis Ultra DLD equipado com uma fonte de raios-X monocromática Al Kα (1486,7 eV) operado a 15 kV e 5 mA. Varreduras de pesquisa foram medidas em um tamanho de ponto de 400 μm e uma energia de passagem constante de 200 eV. A calibração foi realizada definindo a banda C1s em 284,5 eV. A deconvolução de espectros de elemento XPS de alta resolução foi realizada usando o software XPSPEAK41.
Resultados e discussão
Conteúdo de NR e estabilidade térmica
As curvas termogravimétricas (TG) e termogravimétricas diferenciais (DTG) dos materiais sintetizados são mostradas na Fig. 1. Três etapas principais de perda de peso foram observadas para todas as amostras. A primeira etapa ocorreu entre 40-150 ° C, atribuída à perda de etanol, um subproduto da hidrólise e condensação de TEOS, e água fisissorvida na superfície do material. A segunda perda de peso foi detectada em diferentes faixas de temperatura para as séries HMS e NRHMS originais. Para o HMS puro (Fig. 1a), a perda de peso variou de 270-450 ° C e correspondeu à decomposição térmica de grupos etoxi remanescentes [35], uma característica típica das partículas de sílica preparadas pelo método de Stöber [30]. No caso dos nanocompósitos NRHMS (Fig. 1), a faixa de decomposição relativamente ampla se estendeu de 200-450 ° C, indicando a decomposição da fase NR e grupos etoxi. A perda de peso final foi encontrada na faixa de 450-700 ° C e correspondeu à desidroxilação dos grupos silanol [36] e decomposição do resíduo de carbono [37]. A quantidade de NR foi determinada a partir da diferença no peso do resíduo entre as séries de HMS e NRHMS originais. Todos os nanocompósitos de NRHMS possuíam um teor de NR de 12% em peso (% em peso, Tabela 1).
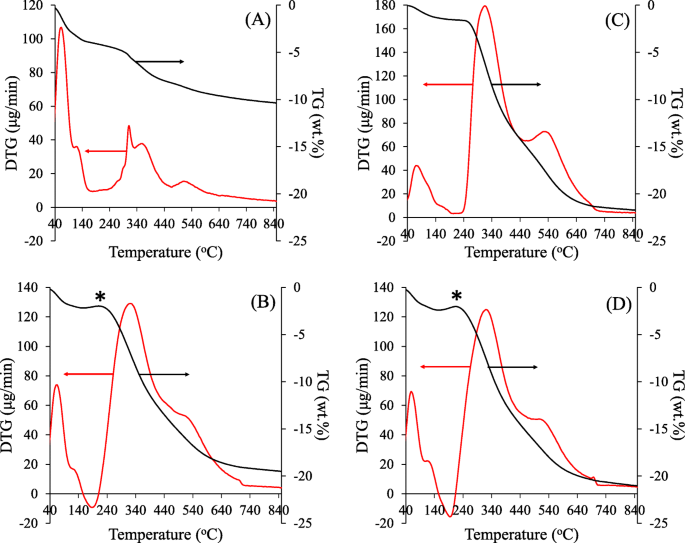
Curvas TG e DTG representativas de ( a ) HMS, ( b ) NRHMS, ( c ) NRHMS (2,5) e ( d ) NRHMS (10). O asterisco representa a etapa na qual o NR foi auto-oxidado
É importante notar que ocorreu um ligeiro ganho de peso na faixa de 180–200 ° C, atribuído à auto-oxidação do polímero [38], que ocorreu no NRHMS puro. Para NRHMS (2,5) e NRHMS (5), esta etapa de degradação não foi encontrada, e a temperatura de decomposição inicial de NR foi deslocada para 240 ° C (Fig. 1c e Arquivo adicional 1:Figura S1, respectivamente). Foi sugerido que a condensação aumentada sob a condição de ácido moderado aumentava a cobertura da estrutura de sílica sobre o NR, o que então limitava a acessibilidade do oxigênio à fase NR e, assim, retardava a decomposição das cadeias NR aprisionadas [39]. No entanto, a etapa de auto-oxidação foi observada em NRHMS (10), o que possivelmente implicou na incorporação limitada de NR na estrutura de silicato. As amostras de NRHMS (10) exibiram aglomerados de NR separados, conforme mostrado no Arquivo Adicional 1:Figura S2.
Análise de propriedades estruturais
A análise de XRD de baixo ângulo das séries HMS e NRHMS foi usada para identificar o arranjo ordenado da estrutura de sílica mesoestruturada. Todas as amostras possuíam a reflexão característica em 2 θ de cerca de 2 ° (Fig. 2), que estava relacionado a d 100 espaçamento interplanar. Em comparação com a sílica HMS pura, a série NRHMS exibiu um arranjo de mesoestrutura menos ordenado, o que indicou que a presença da fase NR nos nanocompósitos de NRHMS possivelmente induziu os canais mesoporosos tortuosos. Além disso, a reflexão característica foi deslocada para ângulos menores, representando uma expansão da célula unitária hexagonal, o que indicava a incorporação de NR na estrutura de silicato da mesoestrutura [27].
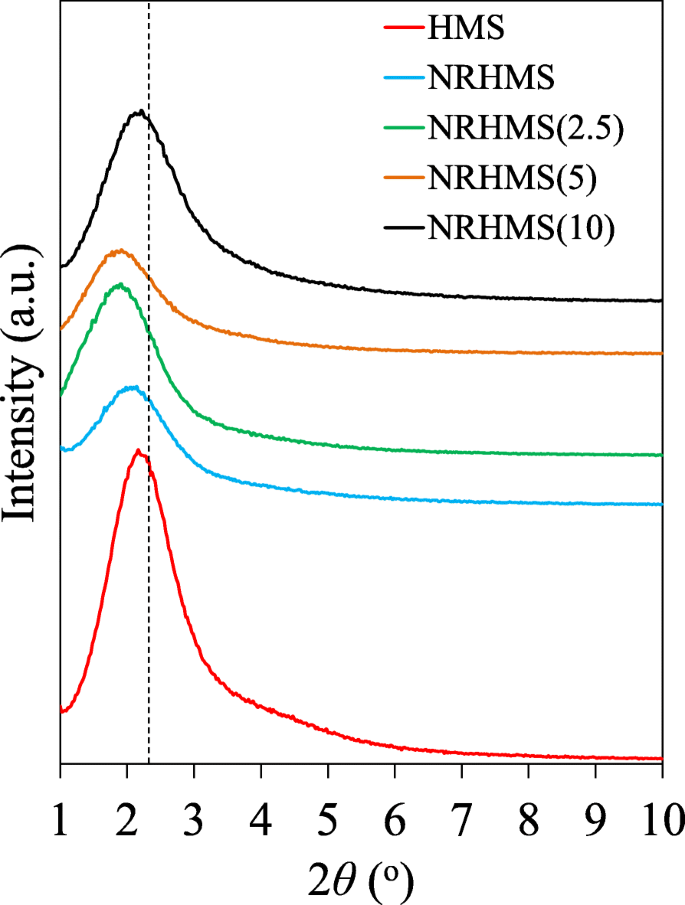
Padrões de XRD de baixo ângulo representativos de nanocompósitos de HMS e NRHMS
A fabricação de NRHMS adicionando um baixo H 2 SO 4 concentração resultou em um incremento no d -spaceamento e parâmetro de célula unitária ( a 0 ) (Tabela 1). A maior intensidade de reflexão de NRHMS (2,5), em comparação com o NRHMS original, foi atribuída a maior ordenação de estrutura devido à taxa de hidrólise-condensação catalisada por ácido de espécies de silicato [40]. NRHMS (5) possuía quase o mesmo parâmetro de célula unitária que NRHMS (2,5), mas forneceu uma mesoestrutura ordenada relativamente inferior, sugerindo que a dispersão de NR foi reduzida conforme o pH da mistura de síntese diminuiu [41], possivelmente causando a não incorporação uniforme de NR na estrutura de silicato de matriz hexagonal. Para NRHMS (10), o pico de reflexão foi deslocado de volta para uma posição superior concomitantemente com um aumento de intensidade, refletindo que quanto maior H 2 SO 4 a concentração induziu a separação das espécies de silicato e da fase NR devido à aglomeração de NR, conforme mencionado anteriormente.
Análise de propriedades texturais
O N 2 fisissorção dos nanocompósitos HMS e NRHMS prístinos exibiram isotermas do tipo IV (Fig. 3a), indicando a mesoporosidade desses materiais [42]. Havia duas etapas principais de condensação capilar em P / P 0 varia de 0,2-0,4 e 0,8-1,0, significando a presença de uma distribuição bimodal do mesóporo, conforme suportado pelo gráfico BJH (Fig. 3b). Os poros menores com uma distribuição de tamanho de poro relativamente estreita foram atribuídos à rede mesoporosa modelada por surfactante, enquanto os vazios interpartículas derivados dos aglomerados NP contribuíram para os poros maiores com uma ampla distribuição [43]. Em comparação com o HMS original, a série NRHMS teve uma área de superfície inferior e volume do mesóporo primário (Tabela 1) devido ao seu bloqueio por NR. A parede de poro mais espessa também causou uma diminuição da área superficial e da porosidade, conforme descrito anteriormente [33]. A maior espessura da parede do NRHMS afirmou que as cadeias de borracha foram aprisionadas na estrutura de silicato, enquanto o tamanho reduzido dos poros sugeriu que algumas moléculas poliméricas foram posicionadas dentro dos mesoporos.
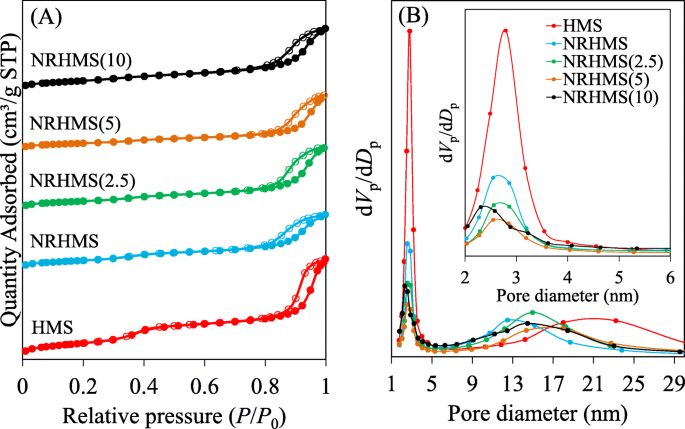
Representante ( a ) N 2 isotermas de fisissorção e ( b ) Distribuição de tamanho de poro BJH de nanocompósitos de HMS e NRHMS
Quando comparado com o NRHMS puro, o NRHMS (2.5) exibiu uma espessura de parede relativamente maior com uma área de superfície e volume de poro diminuídos, significando que a adição de um baixo H 2 SO 4 a concentração promoveu a condensação de espécies de silicato, espessando a parede de sílica. NRHMS (5) tinha uma parede de poro levemente espessada, mas ainda uma área de superfície e volume de poro visivelmente diminuídos, o que estava relacionado à aglomeração parcial de NR, conforme descrito nos resultados de XRD. Para NRHMS (10), a separação de fases causou mudanças significativas nas propriedades texturais, proporcionando uma alta área de superfície, mas menor célula unitária e espessura de parede de poro, pois menos fase NR foi incorporada na estrutura de silicato. Além disso, seu tamanho de poro era menor do que nas outras amostras de NRHMS devido à adição do baixo H 2 SO 4 a concentração levou a um aumento da polaridade da mistura de síntese, o que diminuiu o tamanho das micelas devido a uma interação enfraquecida entre as próprias micelas [44].
Morfologia e análise de estrutura porosa
A análise FESEM revelou que o HMS silicioso formou agregados esféricos de sílica NP, proporcionando espaços vazios visivelmente interpartículas (Fig. 4). Para a série NRHMS, a presença de NR possivelmente agiu como módulos de ligação, anexando partículas em um arranjo mais compacto. Como resultado, as amostras de NRHMS tinham vazios interpartículas menores do que o HMS, o que suportava a distribuição de tamanho de poro BJH (Fig. 3b). O NRHMS (2.5) possuía uma morfologia semelhante ao NRHMS original, enquanto a morfologia do NRHMS (10) parecia semelhante à do HMS, suportando o baixo nível de incorporação de NR na estrutura de silicato devido à agregação de NR. A partir da medição da distribuição do tamanho de partícula (arquivo adicional 1:Figura S3), NRHMS e NRHMS (2,5) exibiram tamanho maior do que HMS. A adição de solução ácida levou a tamanhos de partícula um tanto aumentados por uma taxa aumentada na formação da estrutura de silicato, exceto para NRHMS (10) que forneceu tamanho de partícula menor do que o NRHMS puro devido à menor quantidade de NR incorporado e ligado.

Imagens representativas da FESEM de ( a ) HMS, ( b ) NRHMS, ( c ) NRHMS (2,5) e ( d ) NRHMS (10) com uma ampliação de × 100.000
A análise TEM de HMS e amostras representativas de NRHMS (Fig. 5) revelou a sílica pura HMS e a série NRHMS possuía uma estrutura de motivo semelhante a um buraco de minhoca, uma característica proeminente do HMS [5]. Isso indicou a retenção da estrutura de silicato mesoestruturada na matriz de HMS com moléculas de NR aprisionadas. Infelizmente, o modo TEM convencional não conseguiu detectar a fase NR dispersa devido ao baixo peso atômico dos elementos constituídos. Além disso, os mesoporos de materiais HMS e NRHMS sintetizados eram difíceis de serem medidos devido à sua estrutura mesoestruturada tortuosa e à ausência de ordenação de mesoporos de longo alcance. Foi sugerido que o HMS exibia uma estrutura semelhante a um buraco de minhoca com simetria hexagonal local [45].

Imagens representativas de TEM de HMS ( a ) e NRHMS ( b ) com uma ampliação de × 300.000
Os nanocompósitos fabricados foram, portanto, ainda caracterizados por STEM-EDS para localizar o paradeiro da fase NR (Fig. 6). O HMS puro tinha uma distribuição uniforme de silício (Si) e oxigênio (O), correspondendo à estrutura de silicato [23], enquanto uma pequena quantidade de carbono (C) foi detectada, o que foi explicado pela presença de grupos etoxi remanescentes. O NRHMS puro forneceu uma quantidade maior de C, o que foi detectado de forma consistente nos nanocompósitos de NRHMS, indicando que a fase NR estava uniformemente dispersa em sua mesoestrutura. Em contraste, um grande agrupamento de C foi detectado para o NRHMS (10) com aglomerados de NR separados.

STEM representativo com imagens de mapeamento EDS de ( a ) HMS, ( b ) NRHMS e ( c ) NRHMS (10) com uma ampliação de × 200.000
O ambiente químico na superfície dos materiais foi avaliado por análise XPS. O amplo espectro de varredura XPS do HMS silicioso (Fig. 7a) revelou quatro bandas distintas a uma energia de ligação (BE) de 284,5, 533,0, 151,0 e 100,0 eV, que foram atribuídas a C1s, O1s, Si2s e Si2p, respectivamente . Na Fig. 7b, a composição elementar de NRHMS forneceu um padrão característico semelhante ao HMS, sustentando que não havia nenhuma outra contaminação elementar na presença de NR.
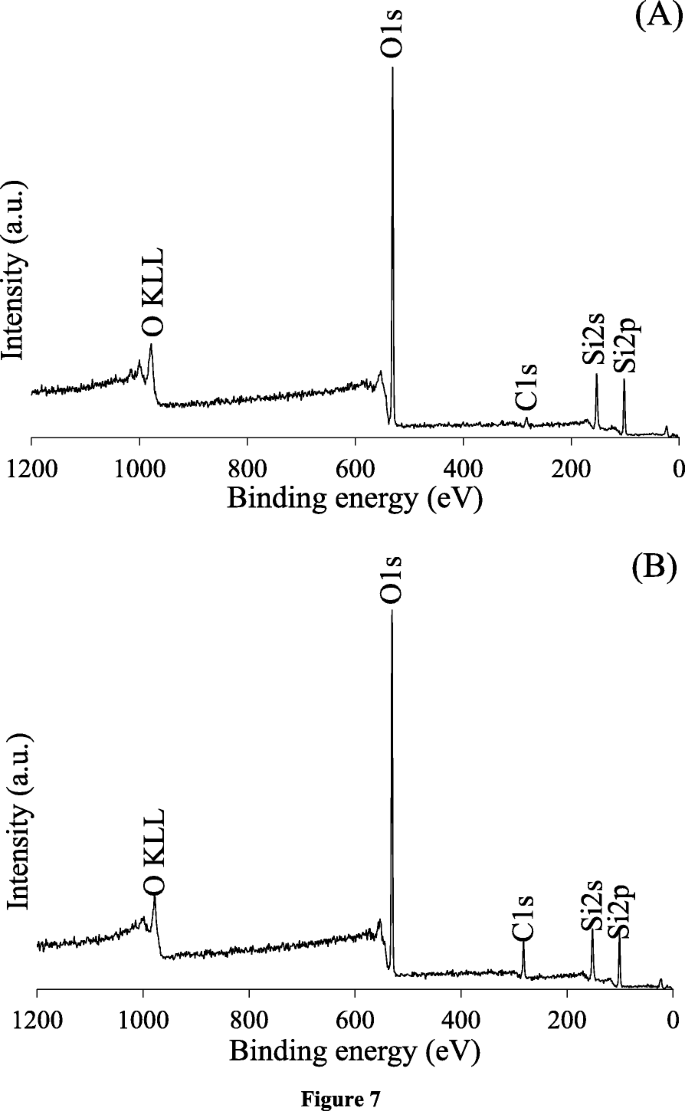
Espectro XPS de varredura ampla representativo de ( a ) HMS e ( b ) NRHMS
Os espectros de C1s e O1s de alta resolução de HMS são mostrados na Fig. 8a. O primeiro estado químico em um BE de 284,5 eV correspondeu às ligações C – C / C – H dos hidrocarbonetos alifáticos na amostra e no carbono superficial adventício. A banda em um BE de 285,9 eV foi atribuída às espécies C – O de grupos etoxi remanescentes, enquanto uma pequena banda deconvoluída em um BE de 287,2 eV foi relacionada à contaminação residual durante a síntese [46]. Para o espectro de O1s de alta resolução, as ligações Si – O – Si da rede de silicatos contribuíram com BE de 533,0 eV. Dois componentes adicionais foram detectados em um BE de 532,2 e 534,3 eV, correspondendo às ligações Si – O – C dos grupos etoxi remanescentes e o Si – O – H dos grupos silanol, respectivamente.
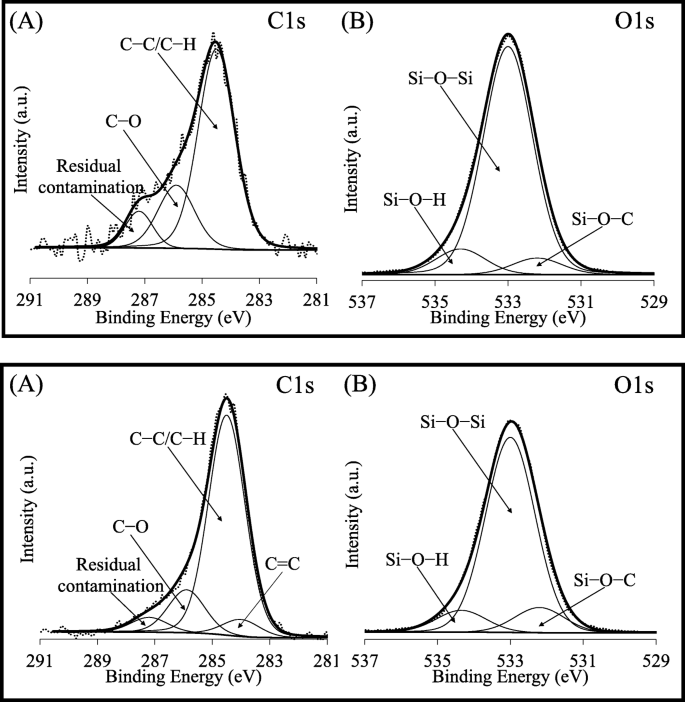
Espectros de C1s e O1s de alta resolução de nível central representativos de ( a ) HMS e ( b ) NRHMS
O NRHMS puro exibiu um espectro C1s de alta resolução semelhante ao HMS, mas com a espécie C =C de estrutura de borracha polimérica em um BE de 284,0 eV (Fig. 8b). De acordo com os espectros de O1s obtidos, NRHMS possuía a maior concentração relativa de Si – O – C, quando comparado ao HMS, o que implica que a presença de NR de fato dificultou a hidrólise do precursor de sílica em razão da interação entre grupos etoxi e moléculas de borracha [47]. Do arquivo adicional 1:Figura S5, os estados C1s e O1s de NRHMS (2,5) e NRHMS (5) eram semelhantes aos do NRHMS original. Este resultado suportou que a adição de um H 2 baixo SO 4 a concentração aumentou a estabilidade térmica do nanocompósito NRHMS fabricado ao aprisionar o NR entre a parede de sílica espessada, não por ligação química entre as moléculas de NR e a estrutura de silicato.
A Tabela 2 resume a porcentagem atômica (em%) para os picos do núcleo C1s, O1s e Si2p observados nos nanocompósitos HMS e NRHMS. Quando o H 2 SO 4 foi adicionado à mistura NR / HMS durante a síntese, a quantidade de grupos etoxi remanescentes e grupos silanol diminuiu enquanto as espécies de siloxano aumentaram. O resultado suportou a adição de um H 2 baixo SO 4 a concentração aumentou a taxa de hidrólise e condensação das espécies de silicato. Além disso, a quantidade diminuída de grupos silanol resultou possivelmente de íons de sulfato (SO 4 2- ) efetivamente ligando-se aos grupos hidroxila na superfície para formar ligações de siloxano [48].
Medição de hidrofobicidade
Dado que o NR é um polímero hidrofóbico, sua incorporação na estrutura de silicato da mesoestrutura proporcionou ao nanocompósito NRHMS resultante propriedades hidrofóbicas. A Tabela 1 mostra o volume de água adsorvido em monocamada ( V m, H2O ), conforme obtido do H 2 O medição de adsorção – dessorção. O HMS puro possuía a maior afinidade por água devido à presença de grupos silanol como os principais grupos funcionais em sua superfície. A hidrofobicidade da fase NR incorporada reduziu a afinidade com água dos nanocompósitos de NRHMS. Para NRHMS (2,5) e NRHMS (5), uma hidrofobicidade aumentada foi observada desde a adição do baixo H 2 SO 4 a concentração reduziu a quantidade de grupos silanol via condensação catalisada por ácido para ligações de siloxano, o que diminuiu consideravelmente a afinidade com a água (Tabela 2) [49]. No entanto, a incorporação malsucedida de NR, que ocorreu no NRHMS (10), resultou em uma diminuição da hidrofobicidade, uma vez que a hidrofilia da estrutura de silicato foi mais dominante do que os aglomerados de NR.
Mecanismo de formação de nanocompósitos NRHMS
A formação mecanística dos nanocompósitos NRHMS foi relatada anteriormente [47], onde NR foi incorporado na estrutura de sílica devido a interações hidrofóbicas entre as moléculas de poli (cis 1,4-isopreno) e os grupos etoxi do precursor de sílica parcialmente hidrolisado, formar uma mesofase híbrida por meio de uma rota de automontagem cooperativa. O nanocompósito NRHMS exibiu propriedades físicas inferiores em comparação ao HMS silicioso, mas uma hidrofobicidade superior devido ao NR estar uniformemente disperso dentro da estrutura de silicato. No entanto, a presença de grupos etoxi remanescentes sugeriu que a fase borracha dificultou a hidrólise e condensação do precursor de sílica (TEOS), resultando em uma rede de silicato mesoestruturada menos condensada e ordenada (Esquema 1A). Após a fabricação na presença de baixo H 2 SO 4 concentração (Esquema 1B), a quantidade de grupos etoxi e grupos silanol foi diminuída por meio do processo sol-gel catalisado por ácido, resultando em uma mesoestrutura ordenada melhorada com paredes de poros mais espessas aprisionando a cadeia de borracha. A cobertura de NR na parede de sílica evitou a decomposição de moléculas poliméricas via auto-oxidação, conforme observado no resultado de TGA (Fig. 1). Além disso, a quantidade diminuída de grupos silanol na superfície melhorou a hidrofobicidade do NRHMS fabricado resultante. Esquema 1C ilustra que o H 2 superior SO 4 a concentração na mistura de síntese diminuiu a estabilidade da dispersão do NR, uma vez que a redução do pH desestabilizou as cargas negativas em torno das pequenas partículas de NR, permitindo sua aglomeração [50]. Simultaneously, the decreased pH (increased the amount of acid solution added) rapidly promoted the condensation of the silica precursor, potentially causing silicate species to form a mesostructure with less incorporated NR. This catalytic effect also diminished the level of ethoxy groups, which acted as anchoring points between the silicate species and NR molecules. As a result, the previous entrapped NR molecules, which were directly exposed to the mixture environment, partially coiled within the mesostructured silica framework, and hampered the formation of an ordered hexagonal mesophase. At higher amount of acid solution added, separation of the NR phase and silicate framework became more obvious (Scheme 1D).
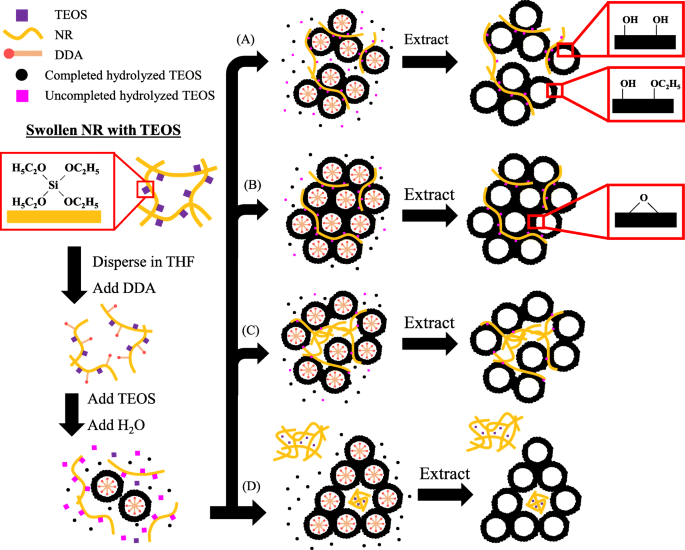
Mechanistic aspect for the formation of (a ) pristine NRHMS, (b ) NRHMS(2.5), (c ) NRHMS(5) and (d ) NRHMS(10)
Conclusão
We successfully demonstrated a facile fabrication of NRHMS nanocomposites via the in situ sol–gel method with pH adjustment to different acid levels using 0.5 M H2 SO 4 solução. Compared to the pristine NRHMS, NRHMS(2.5) exhibited an increased pore wall thickness and hexagonal mesostructure ordering, since the addition of H2 SO 4 at a low concentration, enhanced the acid-catalyzed sol–gel reaction of silicate species, while retaining the remnant ethoxy groups derived from TEOS as anchoring points between the silicate and NR phase. The strengthened silica wall also entrapped the NR chains within its framework, which retarded the thermal decomposition of NR. The improved hydrophobicity of the fabricated nanocomposite was explained by the acid-induced condensation of surface silanol groups to siloxane bonds. However, the advantages of adding H2 SO 4 at a low concentration were reduced with increasing the amount of acid solution added by the agglomeration of the NR phase and depletion of remnant ethoxy groups, leading to less entrapped NR chains within the mesostructured silicate framework and eventually to phase separation between the NR and silica phases, as observed for the NRHMS(5) and NRHMS(10) nanocomposites, respectively. The fabricated NRHMS nanocomposites with enhanced thermal and hydrophobic properties would be a potential porous carrier in the field of catalysis, adsorption, and drug delivery.
Disponibilidade de dados e materiais
The datasets analysed during the current study are available from the corresponding author on reasonable request.
Abreviações
- DDA:
-
Dodecylamine
- DTG:
-
Differential thermogravimetric
- FESEM:
-
Microscopia eletrônica de varredura por emissão de campo
- FTIR:
-
Fourier-transform infrared spectroscopy
- HMS:
-
Hexagonal mesoporous silica
- NP:
-
Nano-partícula
- NR:
-
Natural rubber
- NRHMS:
-
Natural rubber/hexagonal mesoporous silica nanocomposites
- STEM-EDS:
-
Scanning transmission electron microscopy with energy dispersive X-ray spectroscopy
- TEM:
-
Microscopia eletrônica de transmissão
- TEOS:
-
Tetraethyl orthosilicate
- TG:
-
Thermogravimetric
- TGA:
-
Análise termogravimétrica
- THF:
-
Tetrahidrofurano
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- XRD:
-
Difração de raios X
Nanomateriais
- Pesquisa Experimental sobre Estabilidade e Convecção Natural de Nanofluido de TiO2-Água em Compartimentos com Diferentes Ângulos de Rotação
- Síntese fácil de compósito CuSCN colorido e condutor revestido com nanopartículas de CuS
- Síntese fácil de nanofios de prata com diferentes proporções de aspecto e usados como eletrodos transparentes flexíveis de alto desempenho
- Fabricação fácil de composto de polianilina porosa multi-hierárquica como sensor de pressão e sensor de gás com sensibilidade ajustável
- RGO e redes de grafeno tridimensionais TIMs co-modificados com alto desempenho
- Síntese fácil de óxido de estanho mesoporoso semelhante a buraco de minhoca via auto-montagem induzida por evaporação e propriedades aprimoradas de detecção de gás
- Fabricação, Caracterização e Atividade Biológica de Sistemas de Nanotransmissão de Avermectina com Diferentes Tamanhos de Partículas
- Síntese fácil e ecológica de nanofios de Co3O4 e sua aplicação promissora com grafeno em baterias de íon-lítio
- A Fabricação e Desempenho de Absorção de Ondas Eletromagnéticas de Alta Eficiência de Nanocompósitos Estruturados com CoFe / C Core – Shell
- Simplificando a fabricação de sensores com compostos adesivos



