Hidrotérmico Sintetizado de Microesferas CoMoO4 como Excelente Material de Eletrodo para Supercapacitor
Resumo
O CoMoO monofásico 4 foi preparado através de um método hidrotérmico fácil juntamente com tratamento de calcinação a 400 ° C. As estruturas, morfologias e propriedades eletroquímicas de amostras com diferentes tempos de reação hidrotérmica foram investigadas. A estrutura da microesfera, que consistia em nanoflocos, foi observada nas amostras. As capacitâncias específicas em 1 A g −1 são 151, 182, 243, 384 e 186 F g −1 para amostras com tempos hidrotérmicos de 1, 4, 8, 12 e 24 h, respectivamente. Além disso, a amostra com o tempo hidrotérmico de 12 h mostra uma boa capacidade de taxa e há retenção de 45% da capacitância inicial quando a densidade de corrente aumenta de 1 para 8 A g −1 . As capacitâncias de alta retenção das amostras mostram a estabilidade de ciclo longo fino após 1000 ciclos de carga-descarga na densidade de corrente de 8 A g −1 . Os resultados indicam que CoMoO 4 as amostras podem ser uma escolha de materiais de eletrodo excelentes para o supercapacitor.
Histórico
É importante desenvolver a conversão e o armazenamento de energia alternativa renovável devido à rápida deterioração dos combustíveis fósseis. O supercapacitor, como um tipo de dispositivo de armazenamento de energia, tem atraído muita atenção nos últimos anos [1,2,3,4,5]. Os supercapacitores apresentam desempenho desejável, como alta densidade de potência, curto tempo de carregamento e longo ciclo de vida [6,7,8]. De acordo com o mecanismo de armazenamento de carga, os supercapacitores podem ser classificados em capacitores eletroquímicos de camada dupla (EDLCs) e capacitores eletroquímicos redox (isto é, pseudocapacitância (PCs)). O mecanismo de armazenamento de carga dos EDLCs está relacionado à adsorção e dessorção reversível de íons eletrolíticos na superfície do eletrodo / eletrólito, enquanto que o dos PCs está relacionado às reações redox na superfície do eletrodo [4, 6, 8, 9]. Portanto, seja para EDLCs ou PCs, os eletrodos são muito importantes, sendo necessário encontrar um material de eletrodo interessante para aplicação de supercapacitor. Geralmente, a densidade de energia dos PCs é maior do que a dos EDLCs [10, 11]. Muitos materiais de óxido de metal, como NiO [12, 13], Co 3 O 4 [3], CuO [14], MnO 2 [15], e SnO 2 [16], têm atraído muita atenção para o uso como eletrodos supercapacitores. Dentre esses óxidos metálicos, óxidos de molibdênio e óxidos de cobalto são os candidatos promissores para aplicações devido a sua alta atividade redox, múltiplos estados de oxidação, alta capacitância específica teórica, armazenamento reversível de pequenos íons e baixo custo [11]. Zhou et al. MoO preparado 2 nanopartículas, e a amostra mostra uma alta capacitância específica de 621 F g −1 [17] e Wu et al. investigou as propriedades de MoO 2 / CNTs com a capacitância de 467,4 F g −1 [18].
Óxidos de metais mistos têm atraído muita atenção por causa de sua alta atividade redox, boa condutividade elétrica, armazenamento reversível de pequenos íons e baixo custo [11]. Entre eles, os molibdatos metálicos têm atraído muita atenção para aplicações de armazenamento de energia. Como NiMoO 4 [19,20,21], MnMoO 4 [22, 23], CoMoO 4 [6, 8, 11, 24, 25] e outros molibdatos de metal foram extensivamente investigados como excelentes materiais de eletrodo para supercapacitor. Conforme relatado nas Refs. [26,27,28], CoMoO 4 é vantajoso devido ao seu baixo custo e não toxicidade e exibe propriedades eletroquímicas aprimoradas. Veerasubramani et al. preparou o CoMoO em forma de placa 4 com uma capacitância específica de cerca de 133 F g −1 a 1 mA cm −2 [26]. Padmanathan et al. sintetizou o α-CoMoO 4 nanoflakes / CFC usados como supercapacitor simétrico com uma capacitância específica de 8,3 F g −1 a uma densidade de corrente de 1 A g −1 em eletrólito orgânico [29]. Além disso, Kazemi et al. obteve o CoMoO em forma de dente-de-leão 4 com uma excelente capacitância específica de 2100 F g −1 a uma densidade de corrente de 1 A g −1 [8]. Xia et al. relatou que o CoMoO 4 / compostos de grafeno mostram uma capacitância específica de 394,5 F g −1 (na taxa de varredura de 1 mV s −1 ), que é cerca de 5,4 vezes o valor do CoMoO 4 puro [30].
Neste artigo, o CoMoO 4 nanoflocos foram sintetizados por um método hidrotérmico simples em diferentes tempos de reação hidrotérmica, seguido de calcinação a 400 ° C em mufla. As propriedades eletroquímicas das amostras foram investigadas usando os métodos de voltametria cíclica (CV), carga-descarga galvanostática (GCD) e espectroscopia de impedância eletroquímica (EIS). De acordo com os resultados do teste GCD, as amostras mostram capacitâncias específicas de 151, 182, 243, 384 e 186 F g −1 na densidade de corrente de 1 A g −1 em eletrólito 2 M KOH. A amostra CMO-12 mostra uma propriedade eletroquímica interessante.
Experimental
Síntese de CoMoO 4
O CoMoO 4 as amostras foram sintetizadas por um método hidrotérmico simples. Em primeiro lugar, 0,4410 g Co (NÃO 3 ) 2 · 6H 2 O e 0,2675 g (NH 4 ) 6 Mo 7 O 24 · 4H 2 O (AHM) foram dissolvidos em 30 mL de água destilada com agitação magnética por 10 min em temperatura ambiente para obter uma solução mista límpida. Em segundo lugar, 0,3621 g de ureia foi adicionado lentamente à solução mista de Co (NO 3 ) 2 · 6H 2 O e AHM sob agitação magnética. A mistura foi agitada durante 1 h para formar uma solução homogênea. Em seguida, a solução homogênea foi transferida para uma autoclave de aço inoxidável forrada com Teflon de 50 mL e mantida a 180 ° C em um forno elétrico por 1 h. Outras amostras foram preparadas com os tempos hidrotérmicos de 4, 8, 12 e 24 h, respectivamente. Os produtos sintetizados foram resfriados à temperatura ambiente com o forno. Em seguida, a solução resultante foi centrifugada com água destilada e etanol. O precipitado obtido foi seco a 60 ° C em estufa a vácuo durante 10 h. Finalmente, o precipitado seco foi calcinado a 400 ° C em mufla por 2 h para obtenção dos produtos finais. Os produtos finais foram marcados como CMO-1, CMO-4, CMO-8, CMO-12 e CMO-24, respectivamente.
Caracterização do material
As estruturas cristalinas das amostras foram determinadas por difração de raios-X (XRD; Bruker, D8 Discover) a 40 kV e 40 mA. As morfologias das amostras foram examinadas por microscopia eletrônica de varredura por emissão de campo (FE-SEM; Zeiss, SUPRA 40) e microscopia eletrônica de transmissão (TEM; JEM-2100). As isotermas de adsorção-dessorção de nitrogênio das amostras foram obtidas usando o aparelho de fisico-adsorção Autosorb-iQ. Em seguida, as áreas de superfície específicas e as distribuições de tamanho de poro das amostras foram obtidas pelos métodos Brunauer-Emmett-Teller (BET) e Barrett-Joyner-Halenda (BJH).
Preparação do eletrodo de trabalho e medições eletroquímicas
Os eletrodos de trabalho foram preparados de acordo com o método relatado na literatura [31]. Os produtos sintetizados, negros de acetileno e politetrafluoroetileno (PTFE) foram misturados com uma proporção em peso de 70:20:10 para formar uma pasta homogênea. Em seguida, ele foi revestido sobre a espuma de níquel limpa com a área de 1 cm x 1 cm. Depois de secar em um forno a vácuo a 50 ° C por 6 h para remover o solvente, a espuma de níquel foi então prensada a 10 MPa por 2 min por uma máquina de grânulos. A massa do material ativo no eletrodo era de cerca de 3 ~ 5 mg.
As propriedades eletroquímicas das amostras foram caracterizadas usando uma estação de trabalho eletroquímica CS 350 (CorrTest, Wuhan) em temperatura ambiente. Dois moles por litro de soluções de KOH foram usados como solução eletrolítica, e um sistema de três eletrodos foi usado na medição. CoMoO 4 , platina e um eletrodo de calomelano saturado (SCE) foram servidos como o eletrodo de trabalho, o contra-eletrodo e o eletrodo de referência, respectivamente. As curvas CV foram realizadas na faixa de potencial de - 0,2 a + 0,6 V em diferentes taxas de varredura de 5, 10, 20, 40, 50 e 100 mV s −1 . As curvas GCD foram testadas em diferentes densidades de corrente de 1, 1,5, 2, 3, 5 e 8 A g −1 . O EIS das amostras foi investigado de 0,01 Hz a 100 kHz.
Resultados e discussão
Caracterização estrutural e morfológica
Conforme mostrado na Fig. 1, os padrões de XRD das amostras são consistentes com o padrão padrão do CoMoO 4 (JCPDS No. 21-0868), e são semelhantes aos relatados em [6, 8, 32, 33] anterior. Os picos de difração a 13,1 °, 19,1 °, 23,3 °, 26,5 °, 27,2 °, 28,3 °, 32,0 °, 33,6 °, 36,7 °, 40,2 °, 43,6 °, 47,0 °, 52,1 °, 53,7 °, 58,4 °, e 64,5 ° correspondem às reflexões de (001), (\ (\ overline {2} \) 01), (021), (002), (\ (\ overline {1} \) 12), (\ (\ overline {3} \) 11), (\ (\ overline {1} \) 31), (\ (\ overline {2} \) 22), (400), (003), (\ (\ overline {2 } \) 41), (241), (\ (\ overline {2} \) 04), (\ (\ overline {4} \) 41), (024) e (243) planos, respectivamente. Como mostrado na Fig. 1, os picos de difração mais amplos e mais fracos dos padrões de XRD para CoMoO 4 amostras foram observadas, indicando a cristalização mais fraca nas amostras. Conforme relatado nas Refs. [8, 34], a cristalinidade mais fraca desempenha um papel crítico para aumentar o comportamento eletroquímico em aplicações de supercapacitores.
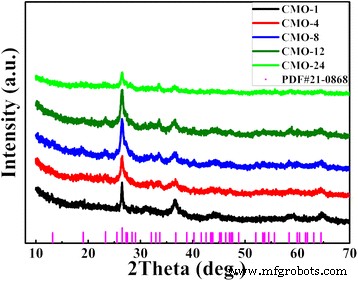
Padrões de XRD de cinco amostras
As morfologias da superfície do CoMoO 4 as amostras foram caracterizadas por SEM e TEM. Conforme mostrado na Fig. 2, as estruturas da microesfera foram observadas para todas as amostras, e a microesfera consistia em nanoflocos. Com o aumento do tempo hidrotérmico, a espessura das nanofolhas primeiro aumenta e depois diminui, sendo que as nanoflocos mais espessas foram obtidas na amostra com o tempo hidrotérmico de 12 h. A Figura 3a, b mostra as imagens de mapeamento de elemento de espectroscopia de energia dispersiva (EDS) e o espectro de EDS de CMO-12. De acordo com as imagens de mapeamento dos elementos, os elementos Co, Mo e O estão uniformemente distribuídos na microesfera. A razão molar do elemento de Co, Mo e O é de cerca de 1:1:4, que corresponde à composição de CoMoO 4 . A Figura 3c, d mostra as imagens TEM do CMO-12. Como mostrado na inserção da Fig. 3c, os padrões de difração de elétrons de área selecionada (SAED) revelam a natureza monocristalina do CoMoO 4 . Os pontos de difração claros podem ser atribuídos aos planos cristalinos (\ (\ overline {2} \) 22), (024), (\ (\ overline {1} \) 31) e (002) do CoMoO 4 . A Figura 3d é a imagem HRTEM; mostra o espaçamento da rede de 0,34 e 0,27 nm, que pode estar relacionado aos planos (002) e (\ (\ overline {1} \) 31) de CoMoO 4 , respectivamente.
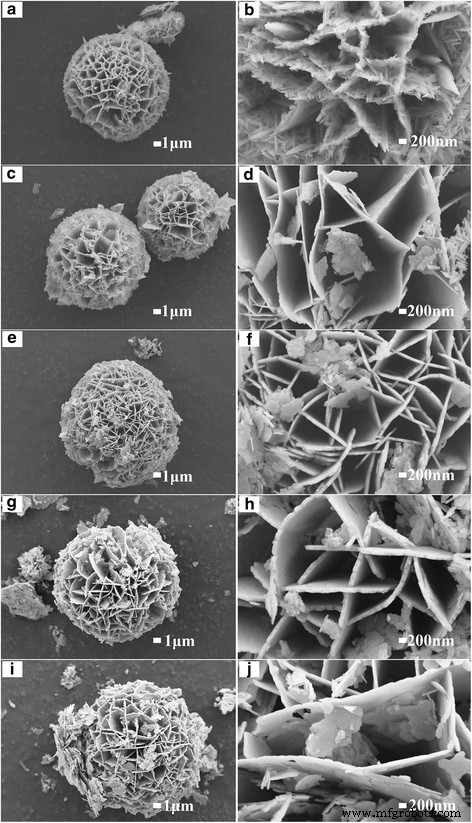
As imagens SEM de baixa e alta ampliação das amostras. a , b CMO-1. c , d CMO-4. e , f CMO-8. g , h CMO-12. eu , j CMO-24
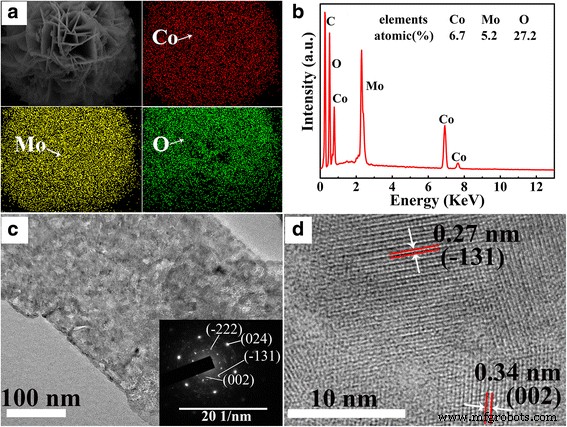
a Imagem de mapeamento de elemento de espectroscopia dispersiva de energia (EDS) e distribuição de Co, Mo e O. b O espectro EDS e a inserção são a porcentagem da razão molar dos elementos Co, Mo e O. c TEM de alta ampliação e inserção são o padrão de difração de elétrons da área selecionada. d A imagem HRTEM da amostra CMO-12
A Figura 4 mostra as distribuições de tamanho de poro e N 2 isotermas de adsorção-dessorção de CoMoO 4 amostras. De acordo com o N 2 isotermas de adsorção-dessorção de amostras, todas as isotermas mostram a característica do tipo IV com H 3 -tipo loops de histerese. As áreas de superfície específicas de BET de CMO-1, CMO-4, CMO-8, CMO-12 e CMO-24 foram calculadas em 18,4, 29,2, 42,8, 74,1 e 26,2 m 2 g −1 , respectivamente. A amostra CMO-12 mostra a maior área de superfície BET, e a alta área de superfície BET poderia aumentar a área de contato do eletrodo / eletrólito e fornecer locais mais ativos para o transporte eficiente de elétrons e íons no sistema de eletrodo [35]. Como mostrado na Fig. 4, os picos agudos nas distribuições de tamanho de poro das amostras estão localizados a 145,9, 74,1, 22,6, 27,9 e 75,3 nm, respectivamente. Isso indica que existem mesoporos em CMO-8 e CMO-24. No entanto, alguns macroporos são detectados nas amostras CMO-1, CMO-4 e CMO-24. Quando os materiais são usados em supercapacitores, as estruturas mesoporosas dos materiais também podem aumentar a área de contato entre o eletrodo e o eletrólito; existem locais ativos mais suficientes para o transporte eficiente de elétrons e íons no sistema de eletrodos [36,37,38]. Portanto, CMO-12 com maior área de superfície BET e estrutura mesoporosa pode apresentar melhores propriedades eletroquímicas do que outras amostras.
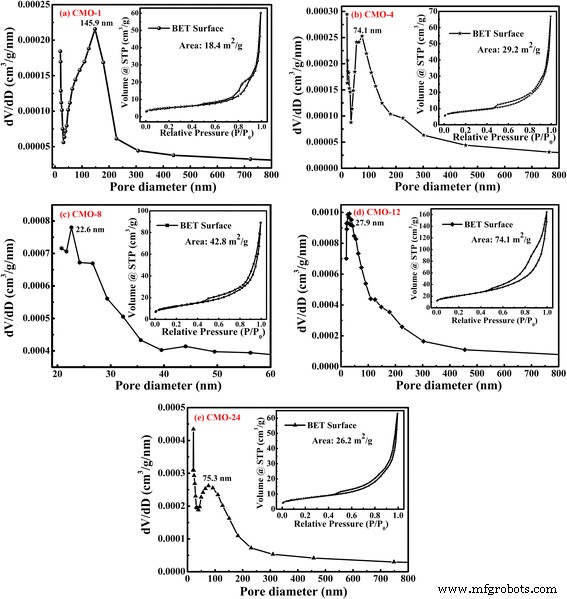
Distribuições de tamanho de poro e N 2 isotermas de adsorção-dessorção de amostras
Caracterização eletroquímica
Curvas CV de CoMoO 4 amostras em diferentes taxas de varredura de 5–100 mV s −1 em eletrólito 2 M KOH com faixa de potencial de - 0,2 V a + 0,6 V (vs. Hg / HgO) são mostrados na Fig. 5a –e. Os picos de reação Faradic típicos podem ser vistos claramente em todas as curvas, o que indica que o CoMoO 4 eletrodos são eletrodos pseudocapacitores. O pico redox observado é devido à cinética de transferência de carga de Co 2+ e Co 3+ associado ao OH - em eletrólito [8, 26]. A reação redox de Co 2+ / Co 3+ está listado da seguinte forma [39, 40]:
$$ {\ mathrm {CoMoO}} _ 4 + {\ mathrm {OH}} ^ {-} \ to \ mathrm {CoOOH} + {\ mathrm {MoO}} _ 3 + {\ mathrm {e}} ^ {-} $$ (1) $$ \ mathrm {CoOOH} + {\ mathrm {OH}} ^ {-} \ kern0.28em \ iff \ kern0.28em {\ mathrm {CoO}} _ 2 + {\ mathrm {H}} _ 2 \ mathrm {O} + {\ mathrm {e}} ^ {-} $$ (2) $$ \ mathrm {CoOOH} + {\ mathrm {H}} _ 2 \ mathrm {O} + {\ mathrm {e}} ^ {-} \ kern0.28em \ iff \ kern0.28em \ mathrm {Co} {\ left (\ mathrm {OH} \ right)} _ 2 + {\ mathrm {OH}} ^ {-} $$ (3)
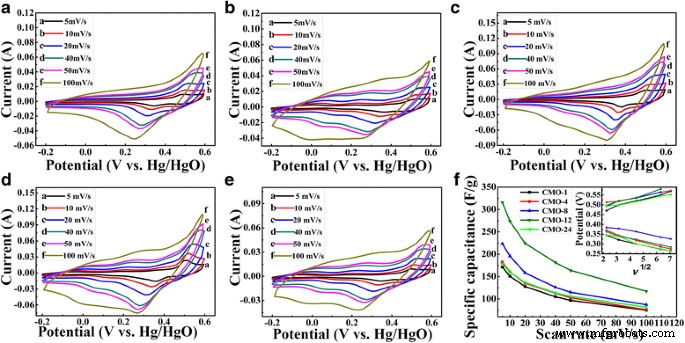
As curvas CV sob diferentes taxas de varredura de 5, 10, 20, 40, 50 e 100 mV s −1 de amostras a CMO-1, b CMO-4, c CMO-8, d CMO-12 e e CMO-24 na janela potencial variou de - 0,2 a + 0,6 V. f A capacitância específica das amostras sob diferentes taxas de varredura de 5–100 mV s −1 . A inserção em f são os gráficos da corrente de pico anódica e catódica em relação à raiz quadrada da taxa de varredura
Conforme mostrado na Fig. 5a-e, com o aumento das taxas de varredura, os picos redox mudam para potenciais mais altos e mais baixos, respectivamente. A diferença potencial entre os picos de oxidação e os picos de redução também aumentou com o aumento da taxa de varredura. Isso indica que o grau irreversível e a reação quase reversível são aumentados com o aumento da taxa de varredura [36, 41]. O deslocamento está principalmente relacionado à resistência interna do eletrodo e à polarização causada pela alta taxa de varredura [36, 42]. Uma relação quase linear entre os potenciais de picos redox e a raiz quadrada da taxa de varredura foi observada, o que pode ser visto no detalhe da Fig. 5f. A relação aproximadamente linear também indica que a cinética da reação durante o processo redox é provavelmente controlada pelo processo de difusão de íons [6].
De acordo com as curvas CV, a capacitância específica das amostras pode ser calculada pela seguinte equação:
$$ {C} _ {\ mathrm {sp}} =\ frac {\ int_ {V_1} ^ {V_2} IdV} {m \ vezes v \ vezes \ Delta V}, $$ (4)
onde C sp (F g −1 ) é a capacitância específica, V 1 e V 2 são a tensão inicial e final, ∫ IdV é a área integral das curvas CV, m (g) é a massa de materiais ativos carregando no eletrodo, v (mV s −1 ) são as taxas de varredura potenciais e ∆ V (V) é a janela do potencial de varredura. As capacitâncias específicas das amostras foram calculadas com base nas curvas CV usando a Eq. (4), que são mostrados na Fig. 5f. As capacitâncias específicas de todas as amostras diminuem com o aumento das taxas de varredura. Mais OH - pode atingir o sítio ativo com condições mais favoráveis em baixa taxa de varredura potencial [31, 43]. Além disso, uma taxa de varredura mais alta leva ao esgotamento ou à saturação dos prótons no eletrólito dentro do eletrodo durante o processo redox, e apenas a superfície externa pode ser utilizada para o armazenamento de carga [41, 43, 44]. Quando o tempo de síntese hidrotérmica aumenta de 1 para 12 h, as capacitâncias específicas das amostras mostram um aumento óbvio de 171,3 para 315,7 F g −1 a uma taxa de varredura de 5 mV s −1 . No entanto, a capacitância específica diminui de 315,7 para 178,7 F g −1 quando o tempo hidrotérmico aumenta de 12 para 24 h. Portanto, a amostra CMO-12 (isto é, o tempo hidrotérmico é de 12 h) mostra uma excelente capacitância específica. A capacitância específica de 315,7 F g −1 a 5 mV s −1 é melhor do que 286 F g −1 para CoMoO 4 nanorods [11] e 95,0 F g −1 para CoMoO puro 4 [45] e comparável com 322,5 F g - 1 para RGO / CoMoO 4 [45].
Essa propriedade eletroquímica aprimorada pode ser confirmada pelos seguintes testes de descarga de carga galvanostática. Os testes de GCD das amostras foram realizados em diferentes densidades de corrente de 1, 1,5, 2, 3, 5 e 8 A g −1 em eletrólito KOH 2 M, e os resultados são mostrados na Fig. 6a-e. As curvas GCD não lineares podem ser atribuídas pela reação redox [46], e isso é consistente com as curvas CV. Conforme mostrado nessas curvas, o tempo de descarga de CMO-12 é significativamente maior do que outras amostras, indicando uma capacitância específica muito maior em CMO-12. Isso pode ser confirmado adicionalmente pelos seguintes resultados calculados. As capacitâncias específicas do CoMoO 4 eletrodo pode ser calculado usando a equação a seguir:
$$ C =\ frac {I \ times \ Delta t} {m \ times \ Delta V}, $$ (5)
onde C (F g −1 ) é a capacitância específica, I (A) é a corrente de descarga, ∆ t (s) refere-se aos tempos de alta, m (g) é a massa de carga de material ativo na superfície do eletrodo, e ∆ V (V) é a janela de potencial aplicada [6, 8, 26]. A Figura 6f mostra a capacitância específica calculada de amostras em diferentes densidades de corrente. Com o aumento da densidade de corrente, as capacitâncias específicas das amostras são diminuídas. Isso pode ser atribuído ao contato efetivo entre os íons e os locais eletroativos do eletrodo. Em alta densidade de corrente, há apenas parte do total de locais de reação disponíveis porque os íons de eletrólito sofrem de baixa difusão, o que leva a uma reação de inserção incompleta e uma baixa capacitância específica [19, 45]. Na Fig. 6f, podemos ver que o CMO-12 tem a maior capacitância específica, que são 384, 337, 307, 269, 229 e 172 F g −1 na densidade de corrente de 1, 1,5, 2, 3, 5 e 8 A g −1 , respectivamente. A capacitância específica do CMO-12 mostra uma boa capacidade de taxa. Além disso, a capacitância específica do CMO-12 também é maior do que a relatada em algumas literaturas anteriores. Conforme relatado por Tian et al. [39], a capacitância específica de Co-Mo-O semelhante a agulha é 302 F g −1 a uma densidade de corrente de 1 A g −1 . A capacitância específica máxima de CoMoO 4 era cerca de 133 F g −1 a 1 mA cm −2 no artigo de Veerasubramani [26]. Na Ref. [29], a capacitância específica de α-CoMoO 4 nanoflakes / CFC usado como supercapacitor simétrico é apenas 8,3 F g −1 na densidade de corrente de 1 A g −1 . Além disso, uma alta taxa de descarga ou uma alta densidade de corrente é muito importante para um dispositivo supercapacitor real, que envolve um rápido processo de carga-descarga [43]. Em uma alta densidade de corrente de 8 A g −1 , as capacitâncias específicas para as cinco amostras são 97, 109, 148, 172 e 98 F g −1 , respectivamente.
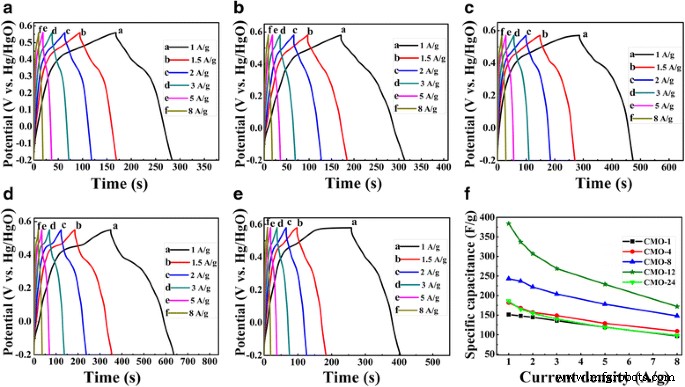
As curvas GCD sob diferentes densidades de corrente de 1, 1,5, 2, 3, 5 e 8 A g −1 de amostras a CMO-1, b CMO-4, c CMO-8, d CMO-12 e e CMO-24 na janela potencial variou de - 0,2 a + 0,58 V. f A capacitância específica das amostras calculadas pelos resultados do GCD
As estabilidades do CoMoO 4 eletrodos foram detectados em eletrólito 2 M KOH a uma densidade de corrente de 8 A g −1 para 1000 ciclos, que são mostrados na Fig. 7. Após 1000 ciclos, as cinco amostras mostram a retenção de 102,9, 87,8, 101,5, 94,2 e 100,5%, respectivamente. Para o aumento da capacitância específica durante o processo cíclico de carga-descarga, isso poderia ser atribuído à ativação do CoMoO 4 superfície com o tempo [6]. Faz a superfície do CoMoO 4 contato totalmente com o eletrólito, o que leva à melhoria da propriedade eletroquímica [6, 47, 48]. A Figura 7b mostra a eficiência coulômbica de CoMoO 4 amostras durante os 1000 ciclos de carga-descarga, que também mostram alta capacitância específica. Os resultados indicam que todas essas amostras têm estabilidade de ciclo longo fina. A capacitância altamente específica, grande capacidade de taxa e estabilidade de ciclo longo fino indicam que a amostra CMO-12 tem uma excelente propriedade eletroquímica.
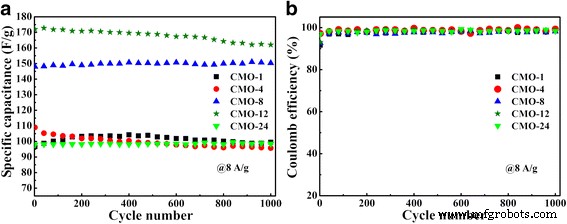
a Desempenho de ciclagem dos eletrodos em 8 A g −1 . b A eficiência coulômbica correspondente de amostras durante o teste de ciclagem
Para avaliar melhor a propriedade eletroquímica do CoMoO 4 eletrodo, o EIS de cinco amostras são registrados em eletrólito 2 M KOH. A Figura 8 são os gráficos de Nyquist de cinco amostras. Os gráficos de Nyquist representam a resposta em frequência do sistema eletrodo / eletrólito [26, 49]. Os espectros EIS podem ser ajustados pelo diagrama de circuito equivalente, que foi inserido na Fig. 8. O gráfico de Nyquist é composto por um semicírculo em alta frequência e uma linha reta em baixa frequência. O diâmetro do semicírculo em alta frequência representa a resistência de transferência de carga da interface Faraday ( R ct ), e a inclinação da linha reta em baixa frequência é o representante da resistência típica de Warburg (W 0 ) [41], respectivamente. CPE1 é um elemento de fase constante, responsável pela capacitância de camada dupla [43]. Além disso, a resistência em série R s é a resistência interna, que poderia ser obtida a partir da interceptação das plotagens no eixo real [11]. O R medido s os valores são 2,83, 2,41, 1,51, 1,22 e 2,26 Ω para as cinco amostras, respectivamente. E o equipado R ct os valores das cinco amostras são 1,69, 1,48, 0,72, 0,23 e 1,28 Ω. Os resultados do EIS mostram que a amostra CMO-12 possui valores mais baixos de R s e R ct do que as outras quatro amostras. Isso indica que a amostra CMO-12 tem condutividades eletrônicas e iônicas mais altas do que as outras amostras [35, 50, 51]. Além disso, CMO-12 com estrutura de mesoporos possui área de superfície BET maior do que as outras amostras. A alta área de superfície BET e boa condutividade são benéficas para a reação redox no sistema eletrodo / eletrólito.
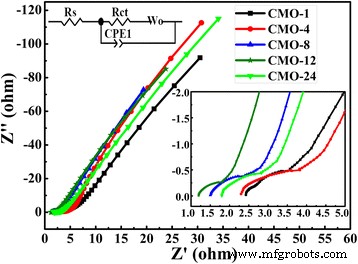
Espectros EIS de amostras obtidas na frequência que varia de 0,01 Hz a 100 KHz. A inserção é a amplificação local dos espectros EIS e o diagrama de circuito equivalente
Conclusões
Em resumo, o CoMoO 4 microesferas foram sintetizadas com sucesso pelo processo de crescimento hidrotérmico acoplado ao tratamento de calcinação. Os tempos de síntese hidrotérmica são 1, 4, 8, 12 e 24 h, respectivamente. Os padrões de XRD indicam que CoMoO de fase única 4 estrutura foi obtida. Imagens SEM mostram que as microesferas eram compostas por nanoflocos. O CMO-12, que foi preparado com o tempo hidrotérmico de 12 h, demonstrou excelente desempenho do supercapacitor. De acordo com os testes de GCD, as capacitâncias específicas do CMO-12 são 384, 337, 307, 269, 229 e 172 F g −1 em densidades de corrente de 1, 1,5, 2, 3, 5 e 8 A g −1 , respectivamente, enquanto atingiu apenas 151, 182, 243 ou 186 F g −1 na densidade atual 1 A g −1 para outras amostras com tempos hidrotérmicos diferentes. As capacitâncias retidas da amostra CMO-12 após 1000 ciclos de carga e descarga na densidade de corrente de 8 A g −1 mostram a estabilidade de ciclo longo fino. Esse excelente comportamento capacitivo pode ser atribuído à estrutura da microesfera e à alta área de superfície BET, e a boa condutividade no eletrodo CMO-12 também é útil para a melhoria do comportamento capacitivo. A alta capacitância específica, boa capacidade de taxa e excelente estabilidade de ciclo promovem a aplicação prática do CoMoO 4 materiais em supercapacitores.
Abreviações
- BET:
-
Brunauer-Emmett-Teller
- CV:
-
Voltametria cíclica
- EDS:
-
Espectroscopia de energia dispersiva
- EIS:
-
Espectroscopia de impedância eletroquímica
- FE-SEM:
-
Microscopia eletrônica de varredura por emissão de campo
- GCD:
-
Descarga de carga galvanostática
- PTFE:
-
Politetrafluoroetileno
- SAED:
-
Difração de elétrons de área selecionada
- SCE:
-
Eletrodo de calomelano saturado
- TEM:
-
Microscopia eletrônica de transmissão
- XRD:
-
Difração de raios X
Nanomateriais
- Compostos de grafeno e polímero para aplicações de supercapacitor:uma revisão
- Nanoesferas de carbono monodispersas com estrutura porosa hierárquica como material de eletrodo para supercapacitor
- Síntese de material anódico esférico Li4Ti5O12 revestido de prata por um método hidrotérmico assistido por Sol-Gel
- Microarranjos mesoporosos de VO2 bidimensional para supercapacitor de alto desempenho
- Silício poroso passivado de folha de grafeno de poucas camadas para um excelente eletrodo eletroquímico de supercapacitor de camada dupla
- Microesferas de silício mesoporosas produzidas a partir de redução magnesiotérmica in situ de óxido de silício para material de ânodo de alto desempenho em baterias de íon de sódio
- Guia de seleção de materiais para usinagem CNC
- Eletrodo de estanho amplifica supercapacitores
- O material de eletrodo certo para sua aplicação de soldagem por resistência
- As propriedades de cobre e tungstênio fazem um material de eletrodo EDM ideal



