Preparação assistida por ácido sulfúrico de pontos poliméricos carbonizados emissores de vermelho e a aplicação de bioimagem
Resumo
Os pontos de polímero carbonizado de emissão vermelha (CPDs) foram preparados a partir de p -fenilenodiamina ( p -PD) solução aquosa com auxílio de ácido sulfúrico (H 2 SO 4 ), e as propriedades ópticas e a aplicação de bioimagem foram estudadas neste artigo. Comparado com outros sistemas assistidos por ácidos fortes, SA-CPDs (preparado a partir de H 2 SO 4 sistema assistido, o diâmetro médio é ~ 5 nm) é o mais brilhante. O rendimento quântico de fotoluminescência (QYs) é de 21,4% (em água) e o rendimento do produto é de 16,5%. A solução aquosa de SA-CPDs emite a 600 nm quando excitada pela luz de 300 a 580 nm. O comprimento de onda de emissão é independente do comprimento de onda de excitação. As energias de formação de CPDs de duas maneiras foram calculadas para mostrar que o crescimento longitudinal (formando polímeros) é difícil, e o crescimento transversal (formando CPDs) é fácil. Além disso, as propriedades de fotoluminescência de dois fótons (emitindo a 602 nm quando excitado por laser de pulso de femtossegundo de 850 nm) de SA-CPDs também foram utilizadas nos experimentos para coloração de células HeLa e mostraram ter aplicações potenciais em bioimagem.
Histórico
Os pontos de carbono (CDs) têm atraído muita atenção devido às suas vantagens, incluindo excelente solubilidade em água, estabilidade óptica, propriedades únicas de fluorescência, baixa toxicidade, baixo custo, etc [1]. A maioria dos CDs foram estudados como candidatos potenciais para várias aplicações, como imuno-sensores eletroquímicos [2], bio-imagem [3,4,5,6] sensores [7,8,9,10,11,12], foto- catálise [13,14,15], dispositivos emissores de luz [16] e optoeletrônica [17,18,19]. A síntese de CDs desempenha um papel importante nos estudos sobre as propriedades ópticas e aplicações. As abordagens relatadas para preparar CDs podem ser resumidas principalmente como "de cima para baixo" de vários materiais de carbono e "de baixo para cima" de moléculas orgânicas, polímeros ou produtos naturais [20]. Os métodos “bottom-up” são rotas eficientes para a síntese de CDs fluorescentes em larga escala [21]. Grupos nas moléculas aplicadas, incluindo –OH, –COOH, –C =O e –NH 2 pode ser desidratado e carbonizado em temperatura elevada por hidrotermal, microondas, combustão, pirólise e assim por diante.
Os pontos emissores de vermelho têm despertado interesses consideráveis devido, ou seja, à maior profundidade de penetração no campo de bioimagem. Especialmente, os pontos de cores puras são essenciais para uma determinada ocasião porque os materiais de luminescência independente do comprimento de onda da excitação podem fornecer uma luz de fotoluminescência (PL) única e estável. A maioria das emissões de CDs é dependente do comprimento de onda da excitação, e os CDs geralmente emitem luz azul, verde ou amarela, poucos CDs emitem luz vermelha brilhante [22].
Recentemente, isômeros de fenilenodiamina (PD), como o -, m -, e p -PD, foram estudados como fontes de carbono para preparar CDs [8, 9, 23, 24]. CDs com emissão de azul, verde e vermelho podem ser preparados a partir de m -, o -, e p Solução de etanol -PD, respectivamente [23]. CDs emissores de luz em cores podem ser preparados a partir de p -PD e solução aquosa de ureia [24]. Em nosso trabalho anterior [25], propusemos que novos pontos de carbono vermelho (rendimentos quânticos =15,8%, em água) podem ser sintetizados facilmente a partir de “ p -PD + HNO 3 ”Sistema aquoso e aplicado na detecção de íons metálicos em água. Recentemente, o semelhante “ o -PD + H 3 PO 4 ”[26] e“ o -PD + HNO 3 ”[27] sistemas foram relatados, e Liu et al. [27] renomearam seus CDs (QYs =10,8%, em água) como "pontos de polímero carbonizado (CPDs)". Ao contrário dos pontos de carbono tradicionais, os comprimentos de onda de emissão dos CPDs não dependem do comprimento de onda de excitação e, portanto, os "CDs" baseados em PD devem ser nomeados com mais precisão como CPDs.
Aqui, relatamos um método fácil e de alta eficiência de rota hidrotérmica assistida por ácido forte para preparar CPDs emissores de vermelho e a aplicação de bioimagem com propriedades de fotoluminescência de dois fótons. O mecanismo para a formação de CPDs é proposto usando o pacote de programa Gaussian 09.
Métodos
Síntese de CPDs vermelhos com auxílio de ácido p -PD Systems
Com base em nosso trabalho anterior [25], selecionamos ácido sulfúrico (H 2 SO 4 ), ácido clorídrico (HCl) e ácido perclórico (HClO 4 ) como assistentes para a preparação de CPDs vermelhos, os CPDs correspondentes foram rotulados como SA-CPDs, HC-CPDs e PA-CPDs, respectivamente. A fim de otimizar as condições experimentais de H 2 SO 4 sistema assistido, selecionamos vários parâmetros, como c (ácido) para c ( p -PD) proporção, c ( p -PD), temperatura ( T ) e tempo de reação ( t ) Os produtos de CPDs foram lavados com hexano para remover o p que não reagiu -PD e por álcool etílico para remover ácidos, centrifugado a 14000 rpm por 30 min para remover a precipitação do polímero e filtrado através de uma membrana de filtro de 0,22 μm. Se o pó for desejável, a solução de CPDs purificada pode ser posteriormente evaporada por evaporador rotativo até o estado quase seco a 80 ° C e uma condição de baixo vácuo (o restante será na forma de pó).
Caracterização e medição
Imagens TEM de alta resolução (HR-TEM) foram registradas no microscópio de transmissão JEM-2100 operando a 200 kV. Os espectros de infravermelho das soluções de CPDs foram coletados usando o espectrômetro Prestige-21 FT-IR por meio de fatias de janela KRS-5 (mistura de TlBr e TlI), normalmente, as fases líquidas foram derramadas em uma fatia e secas. A fatia foi coberta pela outra fatia e fixada na bancada de teste. Em seguida, os espectros infravermelhos foram registrados.
Os espectros de fluorescência dos CPDs foram medidos no espectrofotômetro de fluorescência F-2500. Os espectros de absorção de UV-Vis foram registrados no Espectrômetro Lambda 950 UV / VIS / NIR. Os espectros de emissão de dois fótons de CPDs foram registrados por um espectrógrafo de fibra (QE65000, Ocean Optics) no sistema de microscópio. A solução aquosa de SA-CPDs e a solução de pós redissolvida foram centrifugadas em lâminas e as propriedades de fotoluminescência de dois fótons foram então medidas.
Rendimentos quânticos de fotoluminescência (QYs) dos CPDs foram medidos com Rodamina B (QYs =56% em etanol) como corante de referência na faixa de emissão de 580-610 nm excitada por luz UV 365 nm [25, 28], o procedimento de As medições de QYs foram mostradas no arquivo adicional 1.
Métodos de cálculo
O pacote Gaussian 09 foi usado para os cálculos da teoria da função de densidade (DFT) [29]. As estruturas de equilíbrio foram otimizadas pelo método B3LYP em conjunto com o nível de conjunto de base 6–311 ++ G (d) [30]. Para investigar o papel dos efeitos do solvente, a água foi utilizada no modelo contínuo polarizado (PCM). As análises de frequência foram feitas com o mesmo nível para confirmar que cada estrutura otimizada correspondia a um ponto estacionário.
Cultura de células e tratamento
1,35 mL de células HeLa em meio Eagle modificado por Dulbecco (DMEM; Gibco) a uma densidade inicial de 4 × 10 4 células por mililitros foram semeadas em cada placa e cultivadas a 37 ° C por 24 h sob uma atmosfera umidificada contendo 5% de CO 2 . Os pós de SA-CPDs foram redissolvidos em água para preparar a solução de reserva (400 μg mL - 1 ) 1350 μL de células foram cultivadas com 150 μL de solução de reserva SA-CPDs (a concentração final é de 40 μg mL - 1 ) por 12 h e, em seguida, lavado três vezes com PBS para remover os SA-CPDs livres. Finalmente, os resultados da imagem celular foram coletados com um microscópio confocal sob excitação a laser de femtossegundo de 850 nm (30 mW).
Resultados e discussão
Otimizando a preparação para CPDs vermelhos
Em experimentos básicos, diferentes sistemas assistidos por ácido com várias taxas de concentração, temperaturas de reação e tempos foram investigados (consulte o arquivo adicional 1:Figura S1). Descobrimos que os CPDs vermelhos podem ser formados acima de 180 ° C (reagindo por 2 h) para diferentes sistemas de ácidos, e as reações não são afetadas pelos ânions nas soluções. Longo tempo (4–12 h, 240 ° C para H 3 PO 4 e sistemas HF, consulte o arquivo adicional 1:Figura S1f), a reação aumentará o tamanho da partícula e a fluorescência vermelha será eventualmente desbotada, enquanto a mudança de fluorescência não é óbvia para o sistema HCl (2-6 h, 200 ° C, consulte Adicional arquivo 1:Figura S2). Considerando a economia de energia e o limite superior de temperatura do revestimento de Teflon, a temperatura e o tempo de reação ideais são selecionados como 200 ° C e 2 h, respectivamente. Com base na estratégia de otimização de p Sistema -PD + HCl (ver arquivo adicional 1:Figura S2), otimizamos o p -PD + H 2 SO 4 e p -PD + HClO 4 sistemas e obteve os resultados de otimização mostrados na Tabela 1.
SA-CPDs, HC-CPDs e PA-CPDs foram preparados a partir de p Solução -PD com a ajuda de H 2 SO 4 , HCl e HClO 4 , respectivamente. O c otimizado (ácido) para c ( p -PD) relações de H 2 SO 4 -, HCl-, e HClO 4 os sistemas assistidos são 1, 3 e 3, respectivamente (consulte o arquivo adicional 1:Figura S3a). O c adequado ( p -PD) a faixa para a preparação de CPDs vermelhos é ampla (de 0,02 a 0,20 mol L - 1 ) A temperatura otimizada ( T ) e o tempo de reação ( t ) são 200 ° C e 2 h. SA-CPDs é o mais brilhante CPDs vermelho com um alto QYs de 21,4% (arquivo adicional 1:Figura S3b). Existem duas razões pelas quais H 2 SO 4 pontos de carbono com assistência têm uma qualidade melhor em comparação com HCl-, HClO 4 -, e HNO 3 assistidos (publicado em nosso trabalho anterior [25]). Primeiro, H 2 SO 4 é um ácido forte não volátil que mantém sua acidez em uma solução de reação de alta temperatura e alta pressão. Em segundo lugar, H 2 SO 4 O sistema assistido é o único que pode formar precipitação de sal de amônio no precursor, e os precipitados liberam os reagentes livres lentamente, evitando a formação de precipitação de polímero de partículas grandes e promovendo ainda mais a formação de pontos de carbono de alta qualidade. HA-CPDs e PA-CPDs são soluções espessas vermelho-escuro-marrom e emitem PL vermelho-escuro sob irradiação de luz UV de 365 nm, enquanto os SA-CPDs preparados são uma solução fina transparente vermelha brilhante e emite luz vermelha brilhante (arquivo adicional 1:Figura S3c). Após serem purificados por lavagem, concentração, filtração e evaporação, foram obtidos pós vermelho-escuro-marrom-escuros de SA-CPDs (Arquivo adicional 1:Figura S3d) com o rendimento do produto de 16,5%. Os pós podem ser redissolvidos em água e a solução emite fluorescência brilhante e vermelha (Arquivo adicional 1:Figura S3e).
Caracterização TEM e análise FT-IR
Imagens TEM do OpPD de amostra (sem H 2 SO 4 ) e SA-CPDs (com H 2 SO 4 ) foram mostrados na Fig. 1. A amostra OpPD é composta por fragmentos (oligômeros, Fig. 1a) e polímeros (inserção da Fig. 1a). SA-CPDs são CPDs monodispersos com o tamanho médio de ~ 5 nm (Fig. 1c). Ele exibe dedos de rede bem resolvidos com um espaço de ~ 0,21 nm (inserção da Fig. 1b), correspondendo ao (100) espaçamento de rede no plano do grafeno [31, 32].
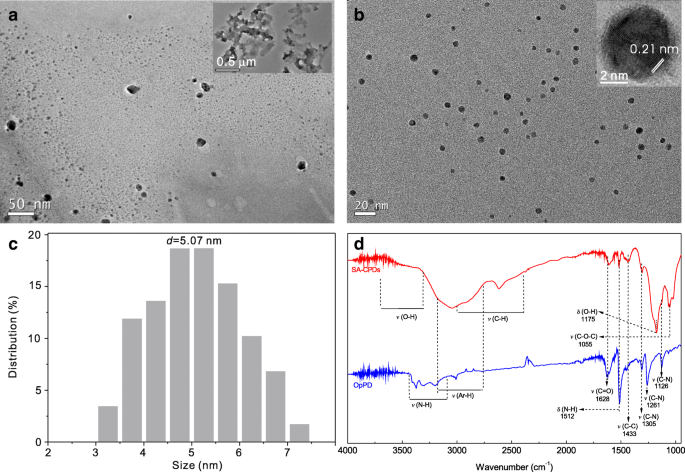
Imagens TEM do OpPD de amostra (sem H 2 SO 4 ) ( a ) e SA-CPDs ( b ) c A distribuição de tamanho de SA-CPDs. d Os espectros FT-IR do OpPD de amostra e CPDs vermelhos. Amostras de OpPD e SA-CPDs foram preparadas a partir de p -PD solução aquosa sem e com H 2 SO 4 -assistido
Os estados de superfície dos CPDs podem afetar as propriedades ópticas. Os grupos químicos de superfície da amostra de OpPD e SA-CPDs foram caracterizados por espectros de FT-IR (Fig. 1d). Duas amostras têm vários grupos semelhantes, como Ar-H (2700–3200 cm - 1 [33], pertence à vibração de alongamento aromático C-H), C-C (~ 1433 cm - 1 , pertence à vibração de alongamento do osso C aromático, revela a presença de vibrações de alongamento aromáticas características de unidades benzenoides) [34], e C =O (1628 cm - 1 , pertence aos grupos –COOH). Comparado com a amostra OpPD, os novos grupos, como O-H (3300–3700 cm - 1 e 1175 cm - 1 pertencem aos grupos –COOH), C-O-C (1055 cm - 1 , existem em ésteres) e C-H (2400–3000 cm - 1 pertence a radicais alquil formados na reação de abertura do anel), são encontrados nos CPDs, enquanto o –NH 2 ou –NH– grupos relacionados, como N-H (3100–3300 cm - 1 e 1512 cm - 1 e C-N (1126, 1261 e 1305 cm - 1 pertencem ao livre –NH 2 ou grupos –NH– de p -PD precursores, enfraquecem ou desapareceram. A existência de grupos –OH ou –COOH indica que o grau de oxidação da superfície de SA-CPDs (com H 2 SO 4 adição) é maior do que o OpPD da amostra (sem adição de ácido).
Mecanismo proposto para a formação de CDs
As energias de formação foram calculadas usando o pacote de programa Gaussian 09. Depois de serem protonados por auxílio de ácido, os bi-polímeros podem ser polimerizados de duas maneiras chamadas de crescimento longitudinal e transversal. A energia de formação calculada de crescimento transversal (- 1406,07 kJ mol - 1 ) é significativamente maior do que o crescimento longitudinal (- 616,25 kJ mol - 1 ) Mostra que os bi-polímeros totalmente protonados (pH 3, após excesso de H + foi adicionado) tendem a ser polimerizados de forma transversal para formar uma estrutura plana (Fig. 2). Essas estruturas planas foram então automontadas para formar CPDs esféricos.
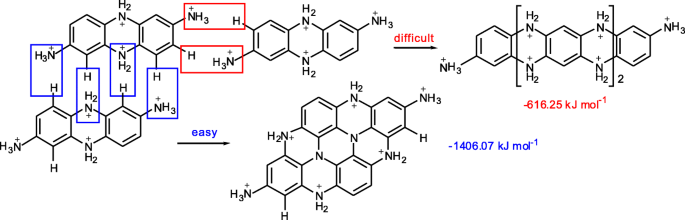
Energias de formação de crescimentos longitudinais e transversais
Propriedades ópticas
Apesar de serem preparados com o auxílio de diferentes ácidos, todos os CPDs possuem propriedades ópticas semelhantes [25]. Para os espectros de UV-Vis da solução aquosa de SA-CPDs (Fig. 3a), o pico de absorbância localizado em ~ 290 nm está associado às transições no anel de benzeno, e os picos localizados em 430 nm e 510 nm podem ser atribuídos a π -π * transição de fenazina substituída conjugada aos pares de elétrons solitários no grupo amina adjacente e a transição de elétrons do anel benzenoide para os anéis quinóide, respectivamente [32]. A curva de excitação descreve uma ampla e gradual tendência ascendente na região visível, e o pico máximo de excitação (~ 580 nm) está próximo ao pico de emissão (~ 600 nm). Os CPDs emitem na zona de luz vermelha (600-700 nm) quando são excitados de 220 nm a 310 nm, enquanto emitem em luz laranja (~ 600 nm) quando excitados de 310 nm a 580 nm (Fig. 3b). É importante notar que a fluorescência deste tipo de CPDs emissores de vermelho é independente do comprimento de onda da excitação [22, 35].
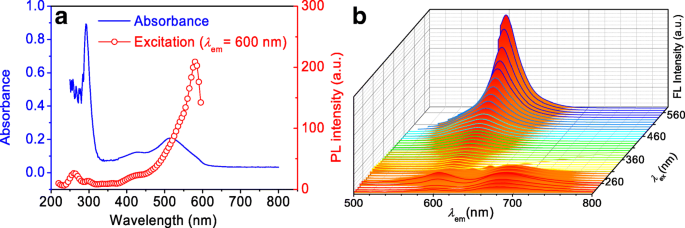
a Absorção UV-Vis, excitação (pico a 600 nm) e b espectros de emissão (excitados 220-580 nm) de SA-CPDs
Imagens celulares
As propriedades de fotoluminescência de dois fótons de SA-CPDs antes e depois do processo de pulverização são mostradas na Fig. 4a. Há um desvio para o azul de 602 nm (antes do processo de pulverização) para 529 nm (após o processo de pulverização) no mesmo comprimento de onda de excitação de 850 nm por pulso de laser de femtossegundo (30 mW). A intensidade do PL foi aumentada após o processo de pulverização.
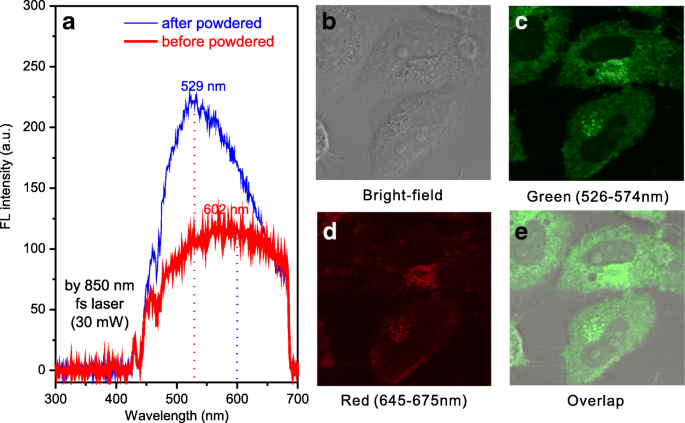
Espectro de fotoluminescência de dois fótons de SA-CPDs ( a ) e imagens de microscopia de fluorescência confocal de células HeLa tratadas com SA-CPDs excitadas por laser de pulso de femtossegundo de 850 nm, 30 mW ( b - e )
Os pós de SA-CPDs foram redissolvidos em PBS (1X) e foram aplicados em imagens de células HeLa usando microscopia de fluorescência confocal e laser de pulso de femtossegundo de 850 nm (30 mW) (ver Fig. 4b-e). Depois de cultivados com células HeLa por 12 h, os SA-CPDs foram engolidos por células HeLa e os CPDs entraram no citoplasma. A intensidade FL do canal vermelho (645-675 nm) é fraca, enquanto o canal verde (526-574 nm) é brilhante, é consistente com o deslocamento para o azul no processo de pulverização.
Conclusões
Um método fácil de rota hidrotérmica assistida por ácido para preparar pontos de carbono e a aplicação de bioimagem foram relatados. Dentro de H 2 SO 4 -, HCl- e HClO 4 sistemas assistidos, SA-CPDs preparados a partir de H 2 SO 4 sistema assistido é o mais brilhante CPDs com o tamanho médio de ~ 5 nm, o QYs de 21,4% e o rendimento do produto de 16,5%. A solução aquosa de SA-CPDs emite a 600 nm quando excitada pela luz de 300 a 580 nm. O comprimento de onda de emissão é independente do comprimento de onda da excitação. Além disso, os SA-CPDs têm propriedades de fotoluminescência de dois fótons emitindo a 602 nm quando excitados por laser de pulso de femtossegundo de 850 nm (30 mW). O método também tem sido utilizado na geração de imagens para células HeLa e tem potencial em, por exemplo, aplicações de bioimagem.
Abreviações
- CDs:
-
Pontos de carbono
- CPDs:
-
Pontos de polímero carbonizados
- HC-CPDs:
-
Os pontos de carbono foram preparados a partir de p -PD com sistema assistido por HCl
- PA-CPDs:
-
Os pontos de carbono foram preparados a partir de p -PD com HClO 4 sistema assistido
- p -PD:
-
P -fenilenodiamina
- QYs:
-
Rendimentos quânticos
- SA-CPDs:
-
Os pontos de carbono foram preparados a partir de p -PD com H 2 SO 4 sistema assistido
Nanomateriais
- Aplicação de corantes ácidos no mundo dos tecidos
- O desenvolvimento e aplicação de tecido de fibra de vidro
- Preparação de nanopartículas de mPEG-ICA carregadas com ICA e sua aplicação no tratamento de dano celular H9c2 induzido por LPS
- Síntese de pontos quânticos do tipo II / tipo I suprimida por reabsorção / CdS / ZnS Core / Shell Quantum Dots e sua aplicação para ensaio de imunossorvente
- Absorvedor perfeito de banda ultra-estreita e sua aplicação como sensor plasmônico na região visível
- Os efeitos da relação Li / Nb na preparação e desempenho fotocatalítico de compostos Li-Nb-O
- A preparação da nanoestrutura de casca de gema de Au @ TiO2 e suas aplicações para degradação e detecção de azul de metileno
- Síntese de nanocristais de ZnO e aplicação em células solares de polímero invertido
- Estudo da Força de Adesão e Transição de Vidro de Filmes de Poliestireno Fino por Microscopia de Força Atômica
- Película de capacitor:as propriedades, construção e aplicação



