Projeto Racional de Compostos SnS2 Quantum Dots / rGO semelhantes a Honeycomb 3D como Materiais de Ânodo de Alto Desempenho para Baterias de Lítio / Íon de Sódio
Resumo
A pulverização da estrutura e a baixa condutividade elétrica dos dichalcogenetos metálicos resultam em um sério declínio da capacidade tanto nas baterias de íons de lítio (LIBs) quanto nas baterias de íons de sódio (SIBs). Para resolver os problemas acima, uma combinação de dichalcogenetos metálicos com andaimes condutores como materiais de eletrodo de alto desempenho tem despertado um enorme interesse recentemente. Aqui, sintetizamos um rGO 3D semelhante a um favo de mel ancorado com SnS 2 pontos quânticos (3D SnS 2 QDs / rGO) composto por secagem por pulverização e sulfetação. A estrutura única em forma de favo de mel ordenada em 3D pode limitar a mudança de volume de SnS 2 QDs nos processos de litiação / delitiação e sodiação / desodiação, fornecem espaço suficiente para reservatórios de eletrólitos, promovem a condutividade do SnS 2 QDs, e melhorar a transferência de elétrons. Como resultado, o 3D SnS 2 O eletrodo composto QDs / rGO oferece alta capacidade e estabilidade de ciclo longo (862 mAh / g para LIB a 0,1 A / g após 200 ciclos, 233 mAh / g para SIB a 0,5 A / g após 200 ciclos). Este estudo fornece uma rota de síntese viável para a preparação de redes porosas ordenadas em 3D em materiais variados para o desenvolvimento de LIBs e SIBs de alto desempenho no futuro.
Histórico
O armazenamento de energia desempenha um papel notável na vida moderna. As baterias de íon-lítio (LIBs) têm sido amplamente aplicadas como fonte de energia para dispositivos eletrônicos portáteis e veículos elétricos devido à sua longa estabilidade de ciclo de vida e alta densidade de energia. Enquanto isso, as baterias de íons de Na (SIBs) têm atraído muita atenção no armazenamento de energia renovável por causa de seu baixo custo e benignidade ambiental. Embora os ânodos de grafite comerciais de LIBs mostrem baixa capacidade teórica (372 mAh / g) e sofram de instabilidade estrutural e problemas de segurança durante um processo de descarga de carga de alta taxa, também não podem ser usados em SIBs devido ao seu pequeno espaço entre camadas [ 1,2,3,4]. Portanto, novos materiais de ânodo com alta capacidade precisam ser desenvolvidos para os LIBs e SIBs de próxima geração.
Os dichalcogenetos metálicos, possuindo altas capacidades teóricas, são candidatos promissores para substituir o grafite comercial em aplicações LIB e SIB. Entre os dichalcogenetos metálicos, SnS em camadas 2 exibe uma capacidade teórica superior à do grafite e é considerado um material de ânodo atraente. SnS 2 é um típico CdI 2 -tipo, onde cada camada se conecta entre si principalmente por uma força fraca de Van der Waals. Tal recurso o torna um candidato de intercalação / desintercalação desejado para Li + e Na + na primeira etapa da reação de conversão. No entanto, SnS 2 sofre de grande mudança de volume e baixa condutividade elétrica no processo de carga-descarga, resultando assim em severa queda de capacidade.
Integrando SnS 2 com outros scaffolds condutores para projetar uma estrutura racional, especialmente uma rede porosa ordenada tridimensional (3D) tem sido considerada como estratégias viáveis para melhorar a condutividade elétrica e estabilidade de ciclo de LIBs e SIBs [5, 6]. O grafeno é considerado um candidato promissor para andaimes devido às suas excelentes características mecânicas e condutividade eletrônica. Em primeiro lugar, em comparação com as estruturas 1D e 2D, uma rede porosa ordenada em 3D é mais propícia ao contato completo entre o eletrodo e o eletrólito. Assim, ele pode atuar como um canal para o transporte rápido de elétrons ao longo da direção 3D e restringir a agregação de forma eficaz [7]. Em segundo lugar, os poros ricos na rede porosa ordenada em 3D podem aliviar a expansão do volume no espaço tridimensional e, portanto, faz com que exiba estabilidade de ciclo de vida longo [8,9,10,11,12,13,14]. Zhu et al. projetado Co 3 O 4 com uma rede mesoporosa 3D e apresentou excelente desempenho em LIBs [15]. Deng et al. demonstrou um novo MoS macroporoso ordenado em 3D 2 / a nanoestrutura de carbono é benéfica para a obtenção de alto desempenho de LIBs [16]. Choi et al. WS em camadas sintetizado 2 microesferas 3D-RGO decoradas com nanosheet como um material de ânodo para SIBs [17]. Com base na discussão acima, projetamos uma estrutura única em forma de favo de mel 3D para amortecer a grande mudança de volume e melhorar a condutividade elétrica de SnS 2 por secagem por pulverização e sulfetação. O composto atinge excelente desempenho eletroquímico em ambos os LIBs e SIBs (862 mAh / g para LIB a 0,1 A / g após 200 ciclos, 233 mAh / g para SIB a 0,5 A / g após 200 ciclos).
O rGO estruturado em 3D semelhante a um favo de mel ancorado com SnS 2 composto de pontos quânticos (3D SnS 2 QDs / rGO) por meio de um método de duas etapas. Em primeiro lugar, o rGO 3D semelhante a um favo de mel ancorado com SnO 2 composto (3D SnO 2 / rGO) é sintetizado através de secagem por pulverização e pós-calcinação. Em seguida, é recozido com tiouréia para obter o 3D SnS 2 Composto QDs / rGO sob a atmosfera de argônio. A estrutura em forma de favo de mel 3D pode reduzir a resistência de contato da junção entre as folhas de forma eficaz, fornecer uma grande área de superfície ativa acessível para a adsorção / dessorção de íons, restringir a agregação de SnS 2 QDs e buffer da expansão de volume de SnS 2 QDs [18,19,20]. Como resultado, o SnS 2 QDs com um diâmetro de ~ 6 nm são uniformemente distribuídos dentro da camada rGO após 200 ciclos de carga / descarga no teste LIB. Além disso, o 3D SnS 2 O eletrodo composto QDs / rGO possui alta capacidade e estabilidade de longo ciclo (862 mAh / g para LIB a 0,1 A / g após 200 ciclos, 233 mAh / g para SIB a 0,5 A / g após 200 ciclos). Os materiais de grafeno poroso 3D à base de sulfeto de metal exclusivos apresentados neste estudo fornecem uma maneira para o desenvolvimento de LIBs e SIBs de alto desempenho.
Métodos
Síntese de nanoesferas de poliestireno
Todos os reagentes usados eram de grau analítico e foram usados diretamente sem qualquer purificação. O estireno foi lavado alternativamente com água DI e NaOH 1 M para remover os inibidores de polímero. Em seguida, 8 ml de estireno, 92 ml de água DI e 0,2 g de K 2 S 2 O 8 foram misturados e depois agitados a 80 ° C durante 10 h em atmosfera de árgon. Finalmente, um produto branco foi obtido por centrifugação. Depois de lavado com água DI e etanol por pelo menos cinco vezes, o produto foi liofilizado a -50 ° C por 24 h [16].
Fabricação de 3D SnS 2 QDs / rGO Composite
Em uma síntese típica, 24 g de óxido de grafeno (GO) coloidal (2,5% em peso) que foi obtido pela abordagem Hummer modificada foram adicionados a 500 ml de água DI. Em seguida, nanoesferas de 3 g de poliestireno (PS) foram dispersas na solução anterior [21, 22]. Além disso, 1,5 g de cloreto de estanho (IV) penta-hidratado (SnCl 4 . 5H 2 O) foi colocado na mistura e ultra-sonicação por 1 h. A solução da mistura foi seca por pulverização com temperatura de saída de 140 ° C e uma taxa de fluxo de 800 ml / h. Posteriormente, o produto coletado foi recozido a 450 ° C por 2 h a uma taxa de rampa de 3 ° C min −1 na atmosfera de Ar para remover nanoesferas PS e, em seguida, o 3D SnO 2 / rGO foi obtido. Finalmente, a tiouréia, agindo como fonte de enxofre, foi misturada com o SnO 2 / rGO. E então foi recozido a 350 ° C por 12 h a uma taxa de aquecimento de 2 ° C min −1 na atmosfera de Ar para garantir o 3D SnO 2 / rGO composto completamente transformado em 3D SnS 2 Composto QDs / rGO [23]. O SnS puro 2 O composto foi sintetizado na ausência de nanoesferas GO e PS.
Caracterização
A estrutura cristalina e a fase dos compósitos foram testadas por difração de raios X (XRD, D8-Advance Bruker) com radiação Cu-Kα (λ =1,5418 Å) a 40 kV e 40 mA, variando de 10 a 80 ° C em ambiente temperatura. A composição química da superfície dos compósitos foi analisada por espectroscopia de fotoelétrons de raios-X modificada (XPS, PHI 5600). As morfologias e estruturas foram examinadas por microscópio eletrônico de varredura por emissão de campo (FESEM, JEOL S-4800) e microscópio eletrônico de transmissão (TEM, JEOL JEM-2010). A área de superfície de Brunauer – Emmett – Teller (BET) e o tamanho dos poros foram identificados usando as isotermas de adsorção / dessorção de nitrogênio obtidas a 77 K em um analisador de área de superfície e porosidade (Quadrasorb SI-MP, Quantachrome). O espectro Raman foi obtido por uma microssonda INVIA Raman (Renishaw Instruments) com fonte de laser 532 nm e lente objetiva × 50. A curva do analisador termogravimétrico (TGA) foi realizada usando um STD Q600 TA com 100 ml min −1 de fluxo de ar de 30 a 800 ° C a uma taxa de aquecimento de 10 ° C min −1 .
Teste eletroquímico
Para preparar eletrodos de trabalho, 70% em peso 3D SnS 2 Composto QDs / rGO, 20% em peso de preto de acetileno e 10% em peso de fluoreto de polivinilideno foram misturados e dissolvidos em N -metil-2-pirrolidinona. Após agitação durante 5 h, a pasta obtida foi revestida sobre a folha de cobre (atuou como um coletor de corrente) e seca a 80 ° C em vácuo durante a noite. Os testes eletroquímicos foram realizados em células de dois eletrodos montadas em um porta-luvas preenchido com argônio. Os metais Li e Na atuaram como contra-eletrodo. O eletrólito orgânico em LIBs era constituído de 1,0 M LiPF 6 em carbonato de etileno (EC) e carbonato de dietil (DEC) (1:1, v / v ) Para SIBs, o eletrólito era NaClO 1 M 4 em uma mistura de EC / DEC (1:1, v / v ) As medições de carga / descarga galvanostática foram realizadas por um sistema de teste de bateria (NEWARE, Shenzhen Xinwei Electronics, Ltd) em diferentes densidades de corrente com uma faixa de tensão de 0,01–3,00 V. Voltametria cíclica (CV) e os voltamogramas cíclicos foram registrados na faixa de potencial de 0,01–3,00 V com uma taxa de varredura de 0,1 mV / s.
Resultados e discussão
Esquema 1 ilustra o processo de síntese do 3D SnS 2 Composto QDs / rGO. Uma solução coloidal, consistindo em nanofolhas de GO uniformemente dispersas, nanoesferas de PS e cloreto de estanho (IV) penta-hidratado, é agitada por 6 h em temperatura ambiente. Para garantir que nenhum precipitado seja formado, a solução coloidal é colocada em repouso por várias horas antes de ser nebulizada. Posteriormente, o composto sal Sn-GO-PS é formado dentro do reator em 10 s (Fig. 1a). Em segundo lugar, o 3D SnO 2 O composto / rGO é sintetizado por calcinação em atmosfera de Ar, conforme mostrado no arquivo adicional 1:Figuras S1a e S1b. Durante a formação do 3D SnO 2 / rGO composto, as nanoesferas PS com um tamanho médio de 200-300 nm agem como um modelo sacrificado é uniformemente ancorado nas camadas rGO. Após a calcinação, a decomposição das nanoesferas PS resulta em vazios de 200-300 nm, levando à formação de uma estrutura semelhante a um favo de mel 3D, conforme mostrado no arquivo adicional 1:Figura S1c. Finalmente, a tioureia é usada como fonte de enxofre e redutor para reagir com o precursor 3D SnO 2 / rGO para obter SnS 3D tipo favo de mel 2 Composto QDs / rGO (Fig. 1b, c). A imagem TEM na Fig. 1d demonstra ainda a estrutura em forma de favo de mel 3D, que é consistente com a morfologia apresentada nas imagens SEM. Além disso, as camadas finas de nanofolhas rGO do 3D SnS 2 O composto QDs / rGO pode ser claramente observado na imagem TEM mostrada no arquivo adicional 1:Figura S1d. O SnS ultrafino 2 QDs com vários nanômetros de tamanho são distribuídos dentro das camadas 3D rGO enquanto as Figs comparadas. 1e, f com arquivo adicional 1:Figura S1d. A imagem TEM ampliada do SnS 2 Os QDs mostrados na Fig. 1f indicam franjas de rede claras separadas por 0,32 nm, que correspondem ao plano (100) de SnS 2 . A distribuição de Sn, S e C no composto era uniforme, conforme mostrado na Fig. 1g – j.
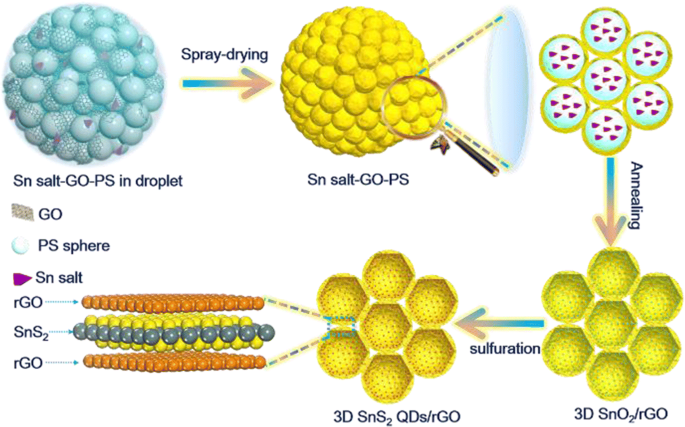
Esquema da fabricação do 3D SnS 2 Composto QDs / rGO por secagem por pulverização e sulfuração e o modelo de microestrutura de interface do SnS 2 / rGO composto

a Imagem SEM do composto Sn salt-GO-PS. b Imagem SEM do 3D SnS 2 Composto QDs / rGO. c Fotografia de uma estrutura semelhante a um favo de mel. d , e Imagens TEM do 3D SnS 2 Composto QDs / rGO. f Imagem HRTEM do 3D SnS 2 Composto QDs / rGO. g – j Imagens de mapeamento elementar de elementos Sn, S e C
Os padrões de XRD de rGO e 3D SnS 2 Compostos QDs / rGO são mostrados na Fig. 2a. O rGO apresenta três picos de difração em 2θ =15,04 °, 26,14 ° e 44,52 °. O primeiro pico pertence ao pico característico de GO, que é verificado posteriormente pelo seguinte espectro Raman. Os próximos dois picos são atribuídos aos planos de rede (002) e (100) do grafeno hexagonal (JCPDS No. 03-065-2023). Os picos de difração de 3D SnS 2 QDs / rGO podem ser observados em 15,0 °, 28,2 °, 30,26 °, 41,9 °, 49,96 °, 58,35 ° e 70,33 °, que correspondem aos planos de cristal (001), (100), (002), (102) , (110), (200), e (113) (JCPDS No. 23-0677) de SnS 2 , respectivamente [24]. Comparado com o SnS puro 2 mostrado no arquivo adicional 1:Figura S2a, os picos de difração relativamente amplos do 3D SnS 2 O composto QDs / rGO indica tamanhos de partícula menores, que estão de acordo com os resultados de TEM. Para investigar mais a estrutura do 3D SnS 2 Composto QDs / rGO, os espectros Raman do composto e rGO são obtidos na Fig. 2b. Os picos Raman de rGO que apareceram em 1596 e 1348 cm −1 são atribuídos às bandas G e D da estrutura do carbono, respectivamente. Geralmente, a banda D é relevante para os defeitos dos átomos de carbono em camadas grafíticas, enquanto a banda G pertence à vibração de alongamento de -C =C- em uma rede hexagonal 2D. Um pico muito mais fraco apareceu em cerca de 309 cm −1 no 3D SnS 2 Composto QDs / rGO, que corresponde ao pico característico do A 1g modo do SnS 2 fase [25]. Além disso, a banda D observada em 1349 cm −1 e a banda G observada em 1587 cm −1 pertencia a 3D SnS 2 QDs / rGO [26]. Enquanto o SnS 2 pode influenciar a redução do GO e dificultar a sua redução, o compósito exibe uma intensidade ligeiramente maior no D pico do que o rGO [27]. Tal resultado também pode explicar o pico que aparece em 2θ =15,04 ° nos padrões de XRD. Para investigar a área de superfície BET e o tamanho dos poros, a porosidade interna e a microestrutura do SnS 3D como preparado 2 Os compostos QDs / rGO são medidos por medições de adsorção-dessorção de nitrogênio. Os notáveis loops de histerese de N 2 As isotermas de adsorção-dessorção mostradas na Fig. 2c podem ser atribuídas ao loop do tipo IV, que demonstra a estrutura nanoporosa padrão do compósito. A área de superfície específica do composto é calculada em 21,99 m 2 g −1 usando um método BET multiponto de acordo com o ramo de adsorção da isotérmica. Como consequência, o 3D SnS 2 O composto QDs / rGO com tal estrutura de poro pode fornecer locais mais ativos e é propício para a difusão de íons no processo de carga / descarga [28, 29].
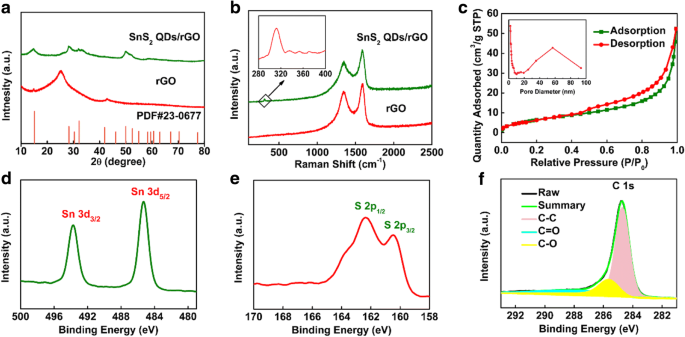
a Padrão XRD e b Espectros Raman do rGO e 3D SnS 2 Composto QDs / rGO. c N 2 isotermas de adsorção-dessorção e as distribuições de tamanho de poro correspondentes do 3D SnS 2 Composto QDs / rGO. Espectros XPS de alta resolução de d Sn 3d, e S 2p e f C 1 s do 3D SnS 2 Composto QDs / rGO
A composição química da superfície e o estado de oxidação do compósito são analisados pelo sistema XPS. Na Fig. 2d, os dois picos proeminentes em 487,3 e 495,7 eV são atribuídos a Sn 3d 3/2 e Sn 3d 5/2 , respectivamente. A diferença de energia entre Sn 3d 5/2 e Sn 3d 3/2 é 8,4 eV, o que indica o Sn 4+ estado de oxidação [30]. O espectro de pesquisa XPS S 2p é apresentado na Fig. 2e. Os picos característicos que aparecem em 161,3 e 163,4 eV são atribuídos a S 2p 3/2 e S 2p 1/2 para S 2− em SnS 2 [27, 31]. O espectro XPS de C 1s mostrado na Fig. 2f pode ser ajustado e dividido em três picos diferentes de 284,7, 285,7 e 288,1 eV, respectivamente. Os três picos pertenciam às ligações C-C, C-O e C =O, respectivamente [25, 32].
A porcentagem de massa de SnS 2 em 3D SnS 2 O composto QDs / rGO foi conduzido por TGA de 30 a 800 ° C a uma taxa de aquecimento de 10 ° C / min no ar. No arquivo adicional 1:Figura S4a, o 3D SnS 2 O composto QDs / rGO foi completamente oxidado a SnO 2 acima de 800 ° C, produzindo uma perda de peso total de cerca de 29,5%. O processo de perda de peso continha três processos, a saber, a dessorção de moléculas de água (1,4%) adsorvidas no 3D SnS 2 Composto QDs / rGO, oxidação de SnS 2 , e a queima sucessiva de rGO. As porcentagens em peso de SnS 2 no 3D SnS 2 O composto QDs / rGO pode ser calculado em 83,7%, com base na perda de peso completa da combustão rGO e na perda de peso parcial da transformação de SnS 2 em SnO 2 [28].
Para investigar os processos de armazenamento de lítio do 3D SnS 2 QDs / rGO e o SnS puro 2 como materiais de ânodo para LIBs, suas curvas CV são testadas a uma taxa de varredura de 0,1 mV / s, conforme mostrado na Fig. 3a, b. Na Fig. 3a, os picos de redução em 1,0-1,5 V são atribuídos à decomposição de fase, colapso da estrutura e formação de uma camada de interface de eletrólito sólido (SEI). Na Fig. 3b, o primeiro pico de redução em 1,7 V é atribuído à intercalação de Li + no SnS 2 nanoestrutura durante o primeiro ciclo [33]. O segundo pico de redução em 1,1 V é atribuído à decomposição de SnS 2 QD para Sn metálico e Li 2 S (como mostrado na reação (1)) [34]. O terceiro pico de redução abaixo de 0,5 V indica o aparecimento de Li x Ligas Sn de acordo com a reação (2) e Li + inserido na nanoestrutura em camadas rGO [35, 36]. Durante a varredura reversa, o primeiro pico de oxidação em 0,52 V indica a desligação de Li x Sn de acordo com a reação (2). O segundo pico de oxidação em 1,8 V pode ser atribuído ao fato de que Li 2 S pode se decompor parcialmente e o Sn pode ser oxidado a Sn 4+ (veja a reação reversa (1)) [34, 37, 38]. As reações do acima mencionado são as seguintes:
$$ \ mathrm {Sn} {\ mathrm {S}} _ 2 + 4 {\ mathrm {Li}} ^ {+} + 4 \ {\ mathrm {e}} ^ {-} \ a 2 {\ mathrm {Li }} _ 2 \ mathrm {S} + \ mathrm {Sn} $$ (1) $$ \ mathrm {Sn} + \ mathrm {x} \ {\ mathrm {Li}} ^ {+} + \ mathrm {x} {\ mathrm {e}} ^ {-} \ leftrightharpoons {\ mathrm {Li}} _ x \ mathrm {Sn} \ \ left (0 \ le \ mathrm {x} <4,4 \ right) $$ (2)
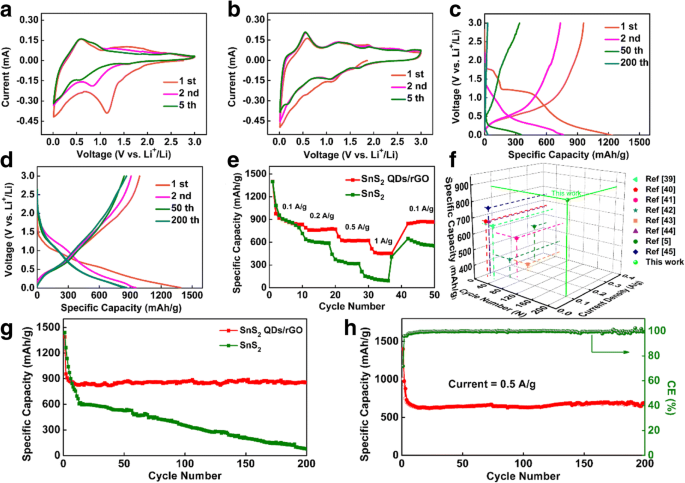
Desempenho eletroquímico do SnS puro 2 e 3D SnS 2 Eletrodos compostos QDs / rGO para LIBs: a , b Curvas de CV do SnS puro 2 e 3D SnS 2 Eletrodos compostos QDs / rGO a uma taxa de varredura de 0,1 mV / s para os primeiros cinco ciclos. c Curvas de carga / descarga do SnS puro 2 eletrodo composto e d o 3D SnS 2 Eletrodo composto QDs / rGO a uma densidade de corrente de 0,1 A / g na faixa de tensão de 0,01–3,0 V vs. Li + / Li. e Avalie o desempenho do 3D SnS 2 QDs / rGO e SnS puro 2 eletrodos compostos em taxas que variam de 0,1 a 1 A / g. f Comparação do desempenho eletroquímico entre o 3D SnS 2 Composto QDs / rGO (o estudo atual) e SnS 2 relatado anteriormente à base de material composto. g Desempenhos de ciclismo de 3D SnS 2 QDs / rGO e SnS puro 2 eletrodos compostos a uma densidade de corrente de 0,1 A / g. h Desempenho de ciclismo e eficiência Coulombic de 3D SnS 2 Eletrodo composto QDs / rGO a uma densidade de corrente de 0,5 A / g
Observe que as intensidades dos picos de redução de SnS 2 diminuir drasticamente na segunda e na quinta varredura. Em contraste, os picos de redução do 3D SnS 2 O eletrodo QDs / rGO se sobrepõe perfeitamente na segunda e quinta varreduras, sugerindo sua excelente reversibilidade e estabilidade eletroquímica.
Medições de carga / descarga galvanostática do SnS puro 2 e 3D SnS 2 Eletrodos QDs / rGO também são realizados em uma densidade de corrente de 0,1 A / g entre 0,01 e 3,00 V vs Li + / Li. As curvas de carga / descarga (1º, 2º, 50º e 200º ciclos) são mostradas na Fig. 3c, d, respectivamente. Na Fig. 3c, a curva de carga / descarga do SnS puro 2 eletrodo mostra uma diminuição drástica para 16 mAh / g após o 200º ciclo. Na Fig. 3d, a capacidade de descarga inicial para o 3D SnS 2 O eletrodo QDs / rGO é 1400 mAh / g. É maior do que a capacidade de armazenamento teórica de Li + (1231 mAh / g) de SnS 2 calculado a partir de ambas as reações (1) e (2) de acordo com a equação de Faraday. Isso é atribuído à formação de uma camada SEI na superfície do 3D SnS 2 Eletrodo QDs / rGO causado pela inserção irreversível de Li + e a decomposição do eletrólito [3]. Ao aumentar os ciclos para 2, 50 e 200, as capacidades do 3D SnS 2 Os eletrodos QDs / rGO são mantidos em 975, 867 e 870 mAh / g, respectivamente. Obviamente, o 3D SnS 2 O eletrodo QDs / rGO possui uma excelente estabilidade de carga / descarga e ciclo de vida longo do que o SnS puro 2 eletrodo.
As taxas de desempenho dos eletrodos são apresentadas na Fig. 3e. Pode ser visto que a capacidade de descarga a uma taxa de 0,1, 0,2, 0,5 e 1 A / g é 870, 770, 622 e 452 mAh / g, respectivamente. Em seguida, ele retorna facilmente a 867 mAh / g a 0,1 A / g, indicando que o 3D SnS 2 O composto QDs / rGO pode suportar variações graduais de taxa e possui notável estabilidade e reversibilidade eletroquímica. Enquanto o SnS puro 2 a capacidade do eletrodo decai para 792, 587, 319 e 106 mAh / g com as taxas de descarga / carga aumentadas para 0,1, 0,2, 0,5 e 1 A / g, respectivamente. E ele só restaura para 662 mAh / g quando a taxa de descarga / carga é recuperada para 0,1 A / g. O excelente desempenho eletroquímico de 3D SnS 2 Eletrodos compostos QDs / rGO são apresentados posteriormente na Fig. 3g. A capacidade do SnS puro 2 eletrodo diminui drasticamente para quase 16 mA / g após 200 ciclos, enquanto o 3D SnS 2 O eletrodo QDs / rGO ainda pode manter um valor de 870 mAh / g após 200 ciclos a uma densidade de corrente de 0,1 A / g. Além disso, na Fig. 3h, o teste é realizado para comprovar o melhor desempenho de ciclagem do compósito a uma taxa de varredura de 0,5 A / g. Após 200 ciclos de carga / descarga, uma alta capacidade reversível de 622 mAh / g permaneceu e a eficiência colombiana média chega a 99,44%.
Para entender melhor o ciclo de vida do 3D SnS 2 Eletrodo QDs / rGO, uma imagem TEM é adquirida para provar a distribuição do SnS 2 QDs (no arquivo adicional 1:Figura S3, medindo 100 partículas representativas usando o software Nano-Measure). O SnS 2 QDs com ~ 6 nm são quase uniformemente ancorados e limitados dentro das camadas rGO, indicando uma forte adsorção entre SnS 2 QDs e as camadas rGO. No geral, os resultados do teste eletroquímico e da distribuição de partículas demonstram que a introdução de rGO e a rede 3D tipo favo de mel oferece abundantes espaços vazios para expansão de volume de SnS 2 QDs. Essas estruturas atuam como canais para o transporte rápido de elétrons ao longo das três direções e efetivamente restringem a agregação. Assim, o desempenho da taxa e a estabilidade do ciclo do composto são aprimorados. A Figura 3f mostra uma comparação do desempenho eletroquímico entre o 3D SnS 2 Composto QDs / rGO (o estudo atual) e o SnS 2 relatado anteriormente à base de materiais compostos. Pode-se observar que a capacidade do 3D SnS 2 QDs / rGO em nosso estudo permanece 862 mAh / g LIB em 0,1 A / g após 200 ciclos, que é maior do que o outro rGO e SnS 2 material baseado em grafeno, como o grafeno-SnS 2 híbridos [39], acetileno preto-SnS 2 [40], SnS 2 @ óxido de grafeno reduzido [41], carbono mesoporoso ancorado com SnS 2 nanofolhas [42], grafeno-SnS 2 [43], SnS 2 grafema carregado com nanopartículas [44], SnS 2 @graphene [5] e Ultrathin SnS 2 nanopartículas em nanofolhas de grafeno [45].
Para investigar os processos de armazenamento de sódio de 3D SnS 2 QDs / rGO e SnS puro 2 como materiais anódicos para SIBs, a voltametria cíclica é realizada a uma taxa de varredura de 0,1 mV / s entre 0,01 e 3,00 V vs Na + / Na, como mostrado na Fig. 4a, b. Na Fig. 4a, o pico de redução em 0,3-1,0 V é correspondente à conversão, reações de liga (Eqs. (4) e (5)) e a formação da camada SEI no ciclo inicial. Na Fig. 4b, o pico bastante amplo em ~ 1,0 V no primeiro processo de redução corresponde à inserção de Na + no SnS 2 camadas (análogas à da intercalação de Li) de acordo com as Eqs. (3) [46, 47]:
$$ \ mathrm {Sn} {\ mathrm {S}} _ 2+ \ mathrm {x} \ {\ mathrm {Na}} ^ {+} + {\ mathrm {x} \ mathrm {e}} ^ {-} \ para {\ mathrm {Na}} _ {\ mathrm {x}} \ mathrm {Sn} {\ mathrm {S}} _ 2 $$ (3) $$ {\ mathrm {Na}} _ {\ mathrm {x} } \ mathrm {Sn} {\ mathrm {S}} _ 2+ \ left (4- \ mathrm {x} \ right) {\ mathrm {Na}} ^ {+} + \ left (4- \ mathrm {x} \ direita) {\ mathrm {e}} ^ {-} \ to \ mathrm {Sn} +2 {\ mathrm {Na}} _ 2 \ mathrm {S} $$ (4) $$ \ mathrm {Sn} + \ mathrm {x} {\ mathrm {Na}} ^ {+} + \ mathrm {x} {\ mathrm {e}} ^ {-} \ to {\ mathrm {Na}} _ {\ mathrm {x}} \ mathrm {Sn} $$ (5)
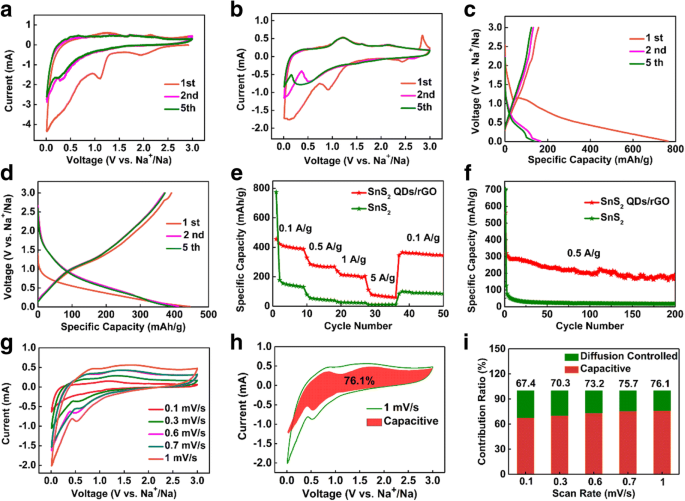
Desempenho eletroquímico do SnS puro 2 e 3D SnS 2 Eletrodos compostos QDs / rGO para SIBs. a , b Curvas de CV do SnS puro 2 eletrodo e 3D SnS 2 Eletrodo composto QDs / rGO a uma taxa de varredura de 0,1 mV / s para os primeiros cinco ciclos. c Curvas de carga / descarga do SnS puro 2 eletrodo composto e d o 3D SnS 2 Eletrodo composto QDs / rGO a uma densidade de corrente de 0,1 A / g na faixa de tensão de 0,01–3,0 V vs. Na + /N / D. e Avalie o desempenho de 3D SnS 2 QDs / rGO e o SnS puro 2 eletrodo composto em taxas que variam de 0,1 a 5 A / g. f Desempenho de ciclismo de 3D SnS 2 Eletrodo composto QDs / rGO e o SnS puro 2 eletrodo a uma densidade de corrente de 0,5 A / g. g Curvas CV de 3D SnS 2 Eletrodo composto QDs / rGO em diferentes taxas de varredura. h Contribuição capacitiva na taxa de varredura de 1 mV / s. eu Razão de contribuição da carga capacitiva e controlada por difusão vs. diferentes taxas de varredura
Na varredura reversa, os picos de oxidação discretos em 0,35, 1,2 e 2,25 V são atribuídos à desodiação de Na x Sn. O pico de oxidação óbvio em 1,2 V pertence à resiliência do SnS 3D inicial 2 Eletrodo QDs / rGO [25]. Observe que as varreduras de CV subsequentes de 3D SnS 2 Os QDs / rGO se sobrepõem bem após o primeiro ciclo, indicando boa reversibilidade do mesmo para as reações de sodiação e desodiação.
Os perfis de tensão de descarga-carga do SnS puro 2 e 3D SnS 2 Eletrodos QDs / rGO são realizados entre 0,01 e 3 V a uma densidade de corrente de 0,1 A / g. Os perfis de carga / descarga correspondentes (1º, 2º e 5º ciclos) são mostrados na Fig. 4c, d, respectivamente, que estão de acordo com os resultados de CV. Na Fig. 4c, um platô notável aparece em ~ 1,0 V no processo de descarga, pertencente à formação de Na x SnS 2 . O platô em 0,5-1,0 V é atribuído à conversão, enquanto que abaixo de 0,5 V é atribuído às reações de liga entre Na + e Sn. Então, a curva CV do 3D SnS 2 Eletrodo QDs / rGO (Fig. 4d) indica que a voltagem de platô imperceptível em ~ 1,0 V é atribuída à intercalação de Na + em SnS 2 camadas durante o primeiro processo de descarga e esta reação é expressa como Eq. (3). O platô da inclinação em 0,3-1,0 V corresponde à reação de conversão (Eq. (4)), a formação da camada SEI pela inserção irreversível de Na + , e a decomposição do eletrólito. O platô abaixo de 0,3 V corresponde à reação de liga (Eq. (5)) [48,49,50]. O eletrodo mostra um platô em ~ 1,0 V e um platô de inclinação em ~ 1,6 V no processo de carga, que também estão de acordo com os resultados de CV.
A capacidade de taxa do SnS puro 2 e 3D SnS 2 Eletrodos QDs / rGO de 0,1 a 5 A / g no teste SIB são dados na Fig. 4e. O 3D SnS 2 O eletrodo QDs / rGO é notavelmente superior em comparação. Pode ser visto que as capacidades de descarga na taxa de 0,1, 0,5, 1 e 5 A / g são 397, 286, 213 e 95 mAh / g, respectivamente, e então retornam facilmente a 393 mAh / g a 0,1 A / g. Mas para o SnS puro 2 eletrodo, a capacidade de descarga decai para 180, 59, 25 e 11 mAh / g com a taxa de descarga aumentada para 0,1, 0,5, 1 e 5 A / g, respectivamente. Então, a capacidade de descarga só é restaurada para 102 mAh / g quando a taxa de descarga volta para 0,1 A / g. O 3D SnS 2 O eletrodo QDs / rGO mostra pequenas mudanças na capacidade de descarga após a descarga em diferentes densidades de corrente, o que indica melhor resiliência da nanoestrutura. Obviamente, a estrutura única em forma de favo de mel 3D permite Na + transporte em alta densidade de corrente sem criar muitas mudanças irreversíveis da nanoestrutura do eletrodo, resultando em um excelente desempenho em SIBs. A capacidade de descarga do SnS puro 2 eletrodo retém apenas 6 mAh / g após 200 ciclos a uma taxa de varredura de 0,5 A / g, que é significativamente menor do que 233 mAh / g no 3D SnS 2 Eletrodo QDs / rGO, conforme apresentado na Fig. 4f. Uma grave deterioração da capacidade do SnS puro 2 eletrodo pode resultar da baixa condutividade eletrônica do SnS 2 sem suporte e as agregações incontroláveis de Sn (ou seus produtos de descarga) durante o ciclismo. Assim, o excelente desempenho eletroquímico do eletrodo corresponde à estrutura semelhante a um favo de mel 3D. Os poros existentes na estrutura podem ajustar de forma eficiente a mudança de volume no processo de liga e de-liga.
Para entender melhor o processo de armazenamento de carga, as curvas CV em várias taxas de varredura (0,1–1 mV / s) são realizadas para entender o processo eletroquímico (Fig. 4g). Um deslocamento de pico aparece com a taxa de varredura aumentando de 0,1 a 1 mV / s, indicando a polarização do eletrodo. A contribuição de capacidade da carga capacitiva e controlada por difusão pode ser quantificada de acordo com a relação [51] i (V) =k 1 v + k 2 v 1/2 , onde k 1 v e k 2 v 1/2 são as contribuições dos processos capacitivos e controlados por difusão, respectivamente. Da Fig. 4h, pode-se observar que a capacidade controlada por capacitância é responsável por 76,1% do armazenamento de carga total a uma taxa de varredura de 1 mV / s. Com a taxa de varredura aumenta na ordem de 0,1, 0,3, 0,6, 0,7 e 1 mV / s, a proporção do processo controlado por capacitância aumenta de 67,4, 70,3, 73,2, 75,7, para 76,1%, respectivamente (Fig. 4i ) O resultado indica que o armazenamento capacitivo de carga desempenha um papel importante na capacidade total do eletrodo [52]. No entanto, a capacidade relativa rápida diminui na taxa de varredura mais alta é atribuída ao processo de conversão de energia eletroquímica de difusão limitada [53].
As vantagens estruturais do 3D SnS 2 O composto QDs / rGO em LIBs e SIBs pode ser resumido da seguinte forma (Fig. 5):(i) a estrutura 3D pode tamponar a expansão do volume e inibir a aglomeração de SnS 2 QDs durante o processo de carga / descarga. (ii) A estrutura porosa em forma de favo de mel 3D pode fornecer espaço suficiente para o armazenamento de eletrólitos. (iii) A rede interconectada 3D é benéfica para aumentar a condutividade do elétron e permitir que o elétron se transfira rapidamente nos caminhos contínuos. (iv) O SnS 2 QDs com um tamanho de partícula de cerca de ~ 6 nm podem encurtar a distância de difusão de Li + / Na + , resultando em um bom desempenho eletroquímico.
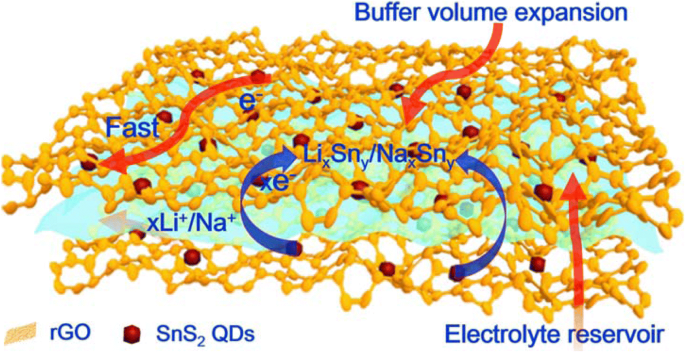
A ilustração esquemática destaca os benefícios estruturais do 3D SnS 2 Composto QDs / rGO durante o processo de carga / descarga
Conclusões
Um romance 3D em forma de favo de mel SnS 2 O compósito QDs / rGO foi sintetizado por atomização e sulfetação em um recipiente. O SnS 2 QDs (~ 6 nm) foi uniformemente distribuído nas camadas rGO. As espessuras das folhas rGO podem ser reguladas alterando a concentração de GO na solução de pulverização. Além disso, o tamanho dos nanovoides rGO pode ser facilmente ajustado usando diferentes tamanhos de nanoesferas PS. O rGO 3D semelhante a um favo de mel não só conseguia armazenar em buffer a expansão de volume do SnS 2 QDs, mas também aumentam sua baixa condutividade elétrica. Além disso, pode fornecer espaço suficiente para reservatórios de eletrólitos. Como resultado, a retenção da capacidade reversível do 3D SnS 2 O eletrodo QDs / rGO para LIB a 0,1 A / g era quase 862 mAh / ge a capacidade era tão alta quanto 622 mAh / g após 200 ciclos a 0,5 A / g. Além disso, uma capacidade de 233 mAh / g pode ser fornecida após 200 ciclos a 0,5 A / g no teste SIB. O romance 3D em forma de favo de mel SnS 2 O composto QDs / rGO sugeriu uma nova estratégia para preparar material anódico em LIBs e SIBs. É previsível que esses materiais anódicos avançados tenham uma influência significativa no campo de armazenamento de energia e, portanto, fornecem novas oportunidades para aprimorar o desempenho eletroquímico de Li + e Na + dispositivos de armazenamento.
Abreviações
- 3D SnS 2 QDs / rGO:
-
SnS 3D semelhante a Honeycomb 2 Quantum Dots / rGO
- 3D:
-
Tridimensional
- BET:
-
The Brunauer – Emmett – Teller
- CV:
-
Voltametria cíclica
- DEC:
-
Carbonato de dietila
- EC:
-
Carbonato de etileno
- GO:
-
Óxido de grafeno
- LIBs:
-
Baterias de íon-lítio
- PS:
-
Poliestireno
- SEI:
-
Interface de eletrólito sólido
- SEM:
-
Microscópio eletrônico de varredura de emissão de campo
- SIBs:
-
Baterias de íon sódio
- TEM:
-
Microscopia eletrônica de transmissão
- TGA:
-
Analisador termogravimétrico
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- XRD:
-
Difração de raios X
Nanomateriais
- Nanocristais de estanho para bateria futura
- S, N Co-dopado de grafeno Quantum Dot / TiO2 Compósitos para geração eficiente de hidrogênio fotocatalítico
- Síntese fácil de nanopartículas de SiO2 @ C ancoradas em MWNT como materiais de ânodo de alto desempenho para baterias de íon-lítio
- Uma abordagem simples para sintetizar pontos quânticos de carbono fluorescentes de águas residuais de Tofu
- Um ânodo de filme Fe2O3 nanocristalino preparado por deposição de laser pulsado para baterias de íon-lítio
- Transformação da lama de Si em estrutura de nano-Si / SiOx por difusão interna de oxigênio como precursor para ânodos de alto desempenho em baterias de íon de lítio
- Síntese assistida por humate de nanocompósitos MoS2 / C via co-precipitação / rota de calcinação para baterias de íon de lítio de alto desempenho
- Síntese e investigação de nanofios de CuGeO3 como materiais de ânodo para baterias de íon de sódio avançadas
- Projeto de pontos quânticos GeSn / GeSiSn com engenharia de tensão para emissão de bandgap direta de infravermelho médio no substrato de Si
- Microesferas de silício mesoporosas produzidas a partir de redução magnesiotérmica in situ de óxido de silício para material de ânodo de alto desempenho em baterias de íon de sódio



