Integrina dupla αvβ 3 e lipossoma paramagnético de direcionamento NRP-1 para detecção precoce de tumor em imagens de ressonância magnética
Resumo
A ressonância magnética aprimorada (ressonância magnética) desempenha um papel vital na detecção precoce do tumor, mas com baixa especificidade. A imagem molecular da angiogênese pode entregar eficientemente agentes de contraste ao local do tumor por meio de transportadores direcionados específicos. Nós projetamos e sintetizamos lipossomas paramagnéticos de alvo duplo funcionalizados com dois ligantes de direcionamento de angiogênese, o RGD específico da integrina αVβ3 (Arg-Gly-Asp) e o ATWLPPR específico do receptor da neuropilina-1 (NRP-1) (Ala-Thr-Trp) -Leu-Pro-Pro-Arg) (A7R). Estes lipossomas provaram estar na gama das nanopartículas e demonstraram encapsular eficazmente os agentes de contraste paramagnéticos de MRI Gd-DTPA (ácido gadolínio-dietilenotriamina pentacético). A relaxividade T1 de várias formulações de lipossomas foi inferior à de Gd-DTPA puro, mas sem diferença estatisticamente significativa. A absorção celular in vitro e o ensaio de inibição competitiva mostraram a maior afinidade de ligação de lipossomas de duplo direcionamento a HUVECs (células endoteliais da veia umbilical humana) e células A549 em comparação com Gd-DTPA puro, não direcionado e lipossomas de direcionamento único, o que foi comprovado para ser mediado pela ligação de RGD / ανβ3-integrina e A7R / NRP1. Para imagens de RM de camundongos com células A549 in vivo, os lipossomas de alvo duplo atingiram o valor de SER (taxa de aumento de sinal) mais alto com uma diferença significativa em todos os pontos de tempo experimentais. Foi um aumento de cerca de três vezes em comparação com Gd-DTPA puro e lipossomas não direcionados e foi 1,5 vezes maior que os lipossomas de direcionamento único 2 h após a injeção. O SER foi reduzido gradualmente e diminuído apenas em 40% do valor de pico em 6 h. Os lipossomas de duplo direcionamento provavelmente exerceram um efeito sinérgico e a especificidade de entrega de Gd-DTPA ao local do tumor. Portanto, lipossoma paramagnético de alvejamento de integrina NRP1 dual-ανβ3 com um peptídeo heterodimérico RGD-ATWLPPR pode ser um sistema potente para imagiologia molecular de tumor.
Introdução
A ressonância magnética (MRI) desempenha um papel vital na detecção de tumores sólidos em um estágio inicial, pois fornece uma melhor resolução espacial do que a tomografia computadorizada (TC) e a tomografia por emissão de pósitrons (PET) [1]. Além disso, a aplicação de agentes de contraste paramagnético, como o ácido gadolínio-dietilenotriamina pentacético (Gd-DTPA), melhora ainda mais a relação sinal-ruído (S / N) [2, 3]. No entanto, a baixa especificidade da ressonância magnética no diagnóstico precoce de tumores ainda é um problema.
O lipossoma pode transportar “carga” hidrofílica no ambiente aquoso com agentes anfifílicos ou hidrofílicos integrados em sua bicamada lipídica. O lipossoma protege seu conteúdo da interação com componentes do plasma, alcançando uma meia-vida biológica prolongada de “carga” hidrofílica; portanto, o lipossoma é usado com mais frequência como um transportador de agentes de contraste em ressonância magnética [4,5,6]. Além disso, ao conjugar peptídeos, anticorpos, aptâmeros ou pequenas moléculas à bicamada lipídica [7,8,9], as propriedades da superfície do lipossoma podem ser modificadas para aumentar sua atividade na entrega de "carga" ou direcionamento para células e tecidos específicos [10 , 11]. Para direcionar o tumor, os peptídeos são comumente usados para se ligar a proteínas como ανβ3-integrina, receptor do fator de crescimento endotelial vascular (VEGF-R) e galectina-1 que são superexpressas em ambas as células endoteliais e uma miríade de células tumorais [12,13 , 14]. Ao direcionar e interferir nessas proteínas, esperava-se que o processo de angiogênese em tumores sólidos fosse bloqueado, para posteriormente inibir o crescimento e a metástase das células tumorais [15,16,17,18]. Essas proteínas superexpressas também são candidatos atraentes para imagens moleculares para identificar a localização do tumor em seu estágio inicial [19,20,21].
No entanto, a expressão heterogênea de vários receptores para a angiogênese tumoral pode interferir na capacidade de direcionamento de sondas de direcionamento único [22]. Para resolver o problema, o direcionamento simultâneo de receptores duplos pode expandir a população de células reconhecidas e fornecer afinidade de ligação fortalecida por meio de conjugações de dois ligantes diferentes aos receptores na mesma superfície celular. Teoricamente, os transportadores de alvo duplo poderiam entregar com eficiência mais agentes de contraste ao local do tumor para imagens moleculares [23,24,25,26].
Em nosso estudo anterior, os lipossomas paramagnéticos com o conjugado Arg-Gly-Asp (RGD) -lipopeptídeo poderiam efetivamente entregar uma quantidade suficiente de agentes de contraste no tumor [27]. Assim, formulamos a hipótese de que o direcionamento de duas moléculas simultaneamente na angiogênese tumoral, por exemplo, ανβ3-integrina e neuropilina-1, poderia aumentar o sinal de imagem de RM baseada em lipossomas paramagnéticos do tumor. Dois ligantes de alta afinidade de RGD para ανβ3-integrina e Ala-Thr-Trp-Leu-Pro-Pro-Arg (ATWLPPR, A7R) para neuropilina-1 (NRP1, um co-receptor VEGF-R) foram funcionalizados para o lipossoma por conjugação com ácido 6-aminohexanóico (C6) -ácido palmítico (Pal). Estes lipossomas encapsulados com Gd-DTPA de alvo duplo foram avaliados por comparação com Gd-DTPA puro, não direccionado e lipossomas de alvo único usando ensaios in vitro e in vivo.
Materiais e métodos
Químicos
Fosfatidilcolina de ovo (C40H82NO9P, ovo PC, MW 775 Da) e N- (carbonil-metoxipolietilenoglicol-2000) -1,2-distearoil-sn-glicero-3-fosfoetanolamina (mPEG2000-DSPE, MW 2788 Da) foram obtidos da Avanti Polar Lipids (Alabaster, AL, USA) e colesterol (C27H46O, MW 386 Da) foram obtidos de Bio Basic (Ontario, Canada). A injeção de sal dimeglumina de ácido gadopentético (Gd-DPTA, Magnevist) foi adquirida na Bayer Schering Pharma (Berlin, German). Os peptídeos e conjugados foram sintetizados por Yishengyuan (Shanghai, China).
Peptídeos e Conjugados
Três peptídeos incluem o peptídeo de alvo duplo P1 (GARYC RGD CFD ATWLPPR , MW 2435 Da), peptídeo de alvo único P2 (GARYC RGD CFDG, MW 1670 Da), e peptídeo de alvo único P3 (ATWLPPR, MW 1191 Da). Os peptídeos foram conjugados com ácido 6-aminohexanóico (C6) -ácido palmítico (Pal), e os peptídeos-alvo de Pal-C6-P1, Pal-C6-P2 e Pal-C6-P3 foram todos sintetizados usando fluorenilmetoxicarbonil (FMOC) química de síntese em fase sólida. A pureza do peptídeo foi confirmada como> 90% por HPLC.
Preparação de lipossomas
Os lipossomas foram preparados usando o método de hidratação de película fina. A composição dos lipossomas era PC de ovo / colesterol / mPEG2000-DSPE a uma razão molar de 1,85 / 1 / 0,15. Três componentes foram misturados e dissolvidos em clorofórmio, o solvente foi evaporado a 37 ° C e um filme fino formado no fundo do frasco redondo. A película fina foi seca durante a noite à temperatura ambiente. Para a preparação de lipossomas direcionados, os peptídeos foram dissolvidos em dimetilsulfóxido (DMSO) e depois diluídos em clorofórmio (concentração final de DMSO de 1%). O lipossoma de P1-Gd-LP, P2-Gd-LP, P3-Gd-LP e P2 / P3-Gd-LP adicionou Pal-C6-P1 a uma proporção de 4,5 μg / μmol de peptídeo / lipídio total, Pal-C6 -P2 para uma proporção de peptídeo / lipídio total de 3 μg / μmol, Pal-C6-P3 para uma proporção de peptídeo / lipídio total de 2,5 μg / μmol, Pal-C6-P2 e Pal-C6-P3 para 3 e 2,5 μg / μmol proporções de peptídeo / lipídeo total, respectivamente. Na preparação do lipossoma paramagnético, o filme fino foi hidratado com solução aquosa de Gd-DTPA, em seguida a suspensão foi extrudada dez vezes sequencialmente através de membranas de policarbonato de 0,4 μm, 0,2 μm, 0,1 μm por mini extrusora (Avanti Polar Lipids, EUA). Gd-DTPA não encapsulado foram removidos por centrifugação a 10.000 × g a - 4 ° C (Avanti J-E, Beckman Coulter, CA, EUA) através de tubos de centrifugação de ultrafiltração de 100.000 MWCO, Amicon Ultra-15 (Millipore, MA, EUA). A suspensão final incluindo lipossomas não direcionados (Gd-LP), lipossomas de direcionamento duplo (P1-Gd-LP), lipossomas de direcionamento único (P2-Gd-LP ou P3-Gd-LP) e misto de direcionamento único lipossomas (P2 / P3-Gd-LP) foram armazenados a 4 ° C sob nitrogênio.
Caracterização de lipossomas
A distribuição de tamanho dos lipossomas preparados foi determinada usando um analisador de tamanho de partícula submicrônico (Zetaplus, Brookhaven Instruments, EUA). A morfologia dos lipossomas foi observada por microscópio eletrônico de transmissão (TEM, JEM-1230, JEOL, Tóquio, Japão) na coloração do acetato de uranila. A concentração de gadolínio foi determinada por espectrômetro de emissão óptica com plasma indutivamente acoplado (ICP-OES, Optima 7000DV, PerkinElmer, EUA).
Medição da relaxividade T1
As imagens ponderadas em T1 da suspensão lipossomal foram obtidas usando um analisador de ressonância magnética nuclear 3.0 Tesla (Philips, GE, EUA). Solução pura de Gd-DTPA, Gd-LP, P1-Gd-LP, P2-Gd-LP e P3-Gd-LP foram diluídos respectivamente com solução salina tamponada com fosfato (PBS) para uma concentração de gadolínio de 1 × 10 - 3 mM a 1 × 10 mM Gd / L. Para medir o relaxamento longitudinal T1 (s), uma sequência spin-eco de recuperação de inversão (STIR) foi usada com dez diferentes tempos de inversão (TI) variando de 200 ~ 9000 ms, e outros parâmetros de varredura foram os seguintes:tempo de repetição (TR) 10.000 ms, tempo de eco (TE) 7,6 ms, o campo de visão (FOV) 2 × 2 cm 2 , tamanho de matriz 320 × 320 e uma espessura de fatia de 5,0 mm. A relaxação T1 (s −1 mM −1 ) poderia ser obtido por meio da seguinte fórmula:r1 =(R1obs-R1m) / C. R1obs e R1m foram as taxas de relaxamento R1 (s −1 ) das preparações e da matriz correspondente, e C era a concentração de gadolínio (mM).
Linhas celulares e cultura
As células A549 (célula de adenocarcinoma humano) e HUVECs (células endoteliais da veia umbilical humana), ambas expressando família de receptores ανβ3-integrina e receptores de neuropilina-1, foram fornecidas pelo Instituto do Câncer da Escola de Medicina da Universidade de Tongji (Xangai, China). As células foram cultivadas em Dulbecco’s Modified Eagle Media (DMEM, Invitrogen, EUA) suplementado com 10% de soro bovino neonatal e 100 U mL −1 penicilina e 100 μg mL −1 estreptomicina a 37 ° C, CO2 a 5%. As células foram cultivadas em placas de 6 poços até confluência de 80-90% nos ensaios.
Captação celular e vinculação competitiva
Cinco lipossomas paramagnéticos incluindo Gd-LP, P1-Gd-LP, P2-Gd-LP, P3-Gd-LP e P2 / P3-Gd-LP com concentração de gadolínio de 10 mM foram administrados a HUVECs e células A549 a 37 ° C por 4 h. Seguindo duas vezes de enxágue com PBS, o ácido nítrico foi adicionado e, em seguida, as células no meio foram nitradas a 65 ° C durante a noite. No ensaio de ligação competitiva, os peptídeos livres correspondentes foram incubados simultaneamente com lipossomas e células conjugadas. As concentrações finais de gadolínio foram determinadas por ICP-OES.
Capacidade de detecção de ressonância magnética in vivo
Todos os procedimentos com animais estão em conformidade com o Guia para o cuidado e uso de animais de laboratório. Os camundongos nus BalB / C fêmeas de 4 semanas de idade (SLAC, Shanghai, China) foram injetados por via subcutânea com células A549 (1 × 10 −4 células por rato) no flanco direito. Quando o tamanho do tumor atingiu 50-100 mm 3 , os camundongos com tumor foram distribuídos aleatoriamente em cinco grupos (cada n =5). Para imagens de RM, os camundongos foram anestesiados com uma injeção peritoneal de uretano a 10% (m / v) e examinados em um analisador de ressonância magnética nuclear 1,5 Tesla (Philips, GE, EUA). Primeiro, imagens ponderadas em T2 foram adquiridas para localizar o tumor usando o procedimento a seguir:TR =7,3 ms, TE =2,7 ms, FOV =12,0 × 12,0 cm 2 , espessura do corte =2 mm, tamanho da matriz =256 × 128. Antes da injeção intravenosa de agentes de contraste, imagens ponderadas em T1 foram adquiridas para varredura simples pela sequência spin-eco:TR =420 ms, TE =14,8 ms, FOV =12,0 × 12,0 cm 2 , espessura de corte =2,0 mm, matriz =256 × 128, então seis cortes consecutivos foram observados. Após a injeção de agentes de contraste paramagnético, imagens pesadas em T1 foram adquiridas em pontos de tempo de 0,5, 1, 2, 4 e 6 h. As regiões de interesse (ROIs) do tumor e as áreas dos músculos dos membros posteriores em imagens de RM foram delimitadas, e a intensidade média do sinal (SI) nas ROIs antes e depois da injeção de contraste foi usada para estimar o SER conforme descrito em nosso estudo anterior [27 ]
Análise estatística
Os dados foram expressos como média ± DP, e as comparações múltiplas entre as médias foram analisadas com ANOVA de uma via pelo software SPSS 22.0. Bicaudal P valor inferior a 0,05 foi considerado significativo.
Resultados
Caracterização de lipossomas
Todos os lipossomas carregados com agentes com peptídeos de alvo não, único e duplo foram mostrados em forma redonda ou oval de tamanho semelhante circundando a estrutura lipoide clara sob TEM. Essas nanopartículas tinham menos de 100 nm de diâmetro, e o potencial zeta variou de -15 mv a -60 mv medido por potenciômetro zeta. Os tamanhos médios de Gd-LP, P1-Gd-LP, P2-Gd-LP e P3-Gd-LP foram 87,75 ± 0,87 nm, 103,50 ± 1,21 nm, 89,91 ± 1,46 nm e 89,90 ± 1,18 nm, respectivamente.
Relaxividade T1 do lipossoma de alvo duplo
O Gd-DTPA puro possuía o maior valor de relaxividade em cinco grupos, mas não era diferente dos outros quatro tipos de lipossomas ( P > 0,05) (Fig. 1), indicando que a adição de composições de lipídeos e peptídeos causou poucos efeitos na relaxividade de Gd-DTPA encapsulado. Assim, sugeriu que se poderia esperar que lipossomas de alvo único, não, único e duplo encapsulados com Gd-DTPA tivessem capacidade suficiente para imagiologia molecular.
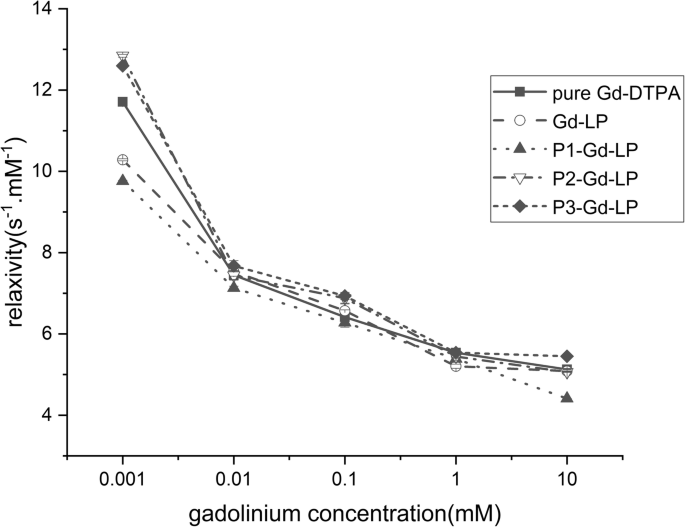
Relaxividade T1 (s −1 mM −1 ) de solução pura de Gd-DTPA, Gd-LP, P1-Gd-LP, P2-Gd-LP e P3-Gd-LP medida em diferentes concentrações de gadolínio (mM). Os dados representam a média ± desvio padrão ( n =3), ( P > 0,05)
Captação celular e vinculação competitiva
A concentração de gadolínio no grupo de lipossomas de alvo duplo foi maior do que outras fórmulas no estudo de captação celular. Em comparação com os lipossomas não direcionados, a concentração de gadolínio do grupo duplo direcionado aumentou em 50% (Fig. 2a). Foi um aumento de até 20% na concentração de gadolínio de grupos de lipossomas de alvo único. Além disso, a concentração de gadolínio de lipossomas de alvo único mistos (P2 / P3-Gd-LP) foi significativamente mais baixa do que o lipossoma de alvo duplo.
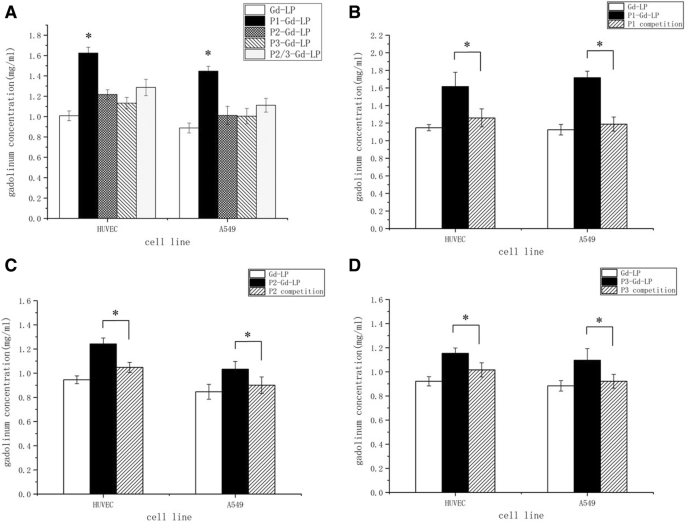
a Experimentos de captação celular de Gd-LP, P1-Gd-LP, P2-Gd-LP, P3-Gd-LP e P2 / P3-Gd-LP em células A549 e HUVECs. b - d Estudo de competição celular de P1-Gd-LP, P2-Gd-LP e P3-Gd-LP, com P1, P2 e P3 respectivamente adicionados para inibir receptores nos grupos de competição. * P <0,05, vs os outros grupos
As concentrações de gadolínio em grupos de lipossomas direcionados diminuíram significativamente na ligação competitiva com os ligantes P1, P2 ou P3 para integrina ανβ3 e / ou receptores de neuropilina-1. A captação celular em grupos competitivos foi próxima à do lipossoma não direcionado (Fig. 2b-d e Tabela 1). Estes dados indicaram que o lipossoma de duplo direcionamento tinha a melhor capacidade de direcionamento de tumor entre esses grupos, que foi mediado pela ligação de RGD / ανβ3-integrina e A7R / NRP1.
Análise de imagem MR
Lipossomas convencionais e lipossomas com agentes de contraste gadolínio encapsulados foram injetados em camundongos com tumor para avaliar o efeito no aumento do sinal do tumor em MRI (Fig. 3). Em termos de SER, os efeitos de imagem de Gd-DTPA puro e grupos de lipossomas não direcionados foram semelhantes (Fig. 4). O SER atingiu o pico em 1 hora após a injeção e caiu drasticamente nas 6 horas seguintes, enquanto o lipossoma de alvo único e duplo indicou padrões de realce diferentes com os dois grupos acima. O SER atingiu o pico em 1 h, mas desceu lentamente de 2 a 6 horas. Entre eles, os lipossomas de alvo duplo atingiram o valor de SER mais alto com estatisticamente significativo em todos os pontos de tempo. Foi um aumento de cerca de três vezes em comparação com Gd-DTPA puro e lipossomas não direcionados e foi 1,5 vezes maior que os lipossomas de direcionamento único 2 h após a injeção. O SER foi reduzido gradualmente e diminuído apenas em 40% do valor de pico em 6 h.

Imagens de RM de camundongos com tumor antes e após a injeção com diferentes agentes de contraste em diferentes momentos. a Gd-DTPA puro. b Gd-LP. c P1-Gd-LP. d P2-Gd-LP. e P3-Gd-LP
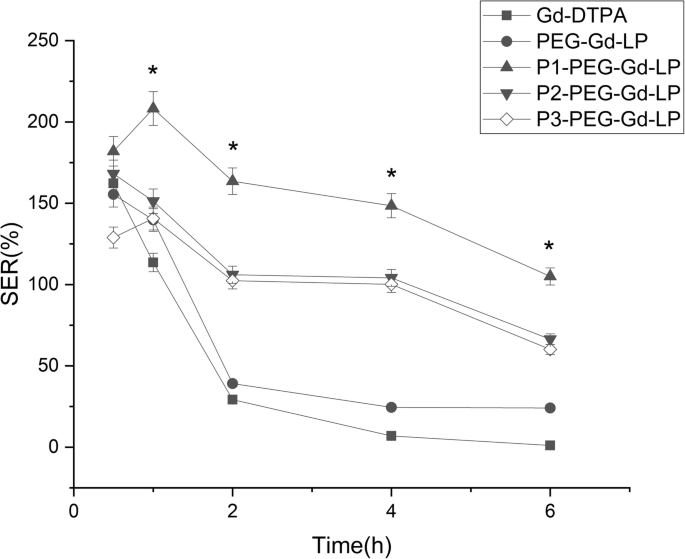
Determinação de SER em diferentes momentos com injeção de Gd-DTPA, Gd-LP, P1-Gd-LP, P2-Gd-LP e P3-Gd-LP puro. N =3 e * P <0,05 P1-Gd-LP vs os outros quatro grupos
Discussão
Partículas pequenas de lipossomas, especialmente aquelas com diâmetro menor que 100 nm, tendem a estender a meia-vida biológica com o aumento da permeabilidade no tumor sólido e, conseqüentemente, acumuladas no tecido tumoral local [4]. Nós construímos com sucesso lipossomas modificados com peptídeos não, únicos e duplos com diâmetros na faixa de nanopartículas e demonstramos que esses lipossomas poderiam encapsular efetivamente o agente de contraste paramagnético de MRI Gd-DTPA. A relaxividade T1 de várias formulações de lipossomas foi inferior à de Gd-DTPA puro, mas sem diferença estatisticamente significativa ( P > 0,05). Uma possível razão poderia ser que a bicamada lipídica efetivamente encapsulou os íons gadolínio e impediu sua troca com água [28]. Além disso, a modificação do peptídeo na superfície do lipossoma não alterou a integridade do lipossoma [29]. Outra razão pode ser a dureza do lipossoma atribuível aos seus componentes de colesterol e fosfolipídios saturados, que possuem baixos coeficientes de permeabilidade à água [30]. Nesse sentido, os componentes do lipossoma tiveram apenas uma leve influência na capacidade de imagem dos agentes de contraste Gd-DTPA.
A angiogênese, a formação de neovasos a partir de um vaso sanguíneo existente, é um evento chave em muitos progressos patológicos, especialmente na invasão do crescimento e metástase do tumor [15, 16]. Um grande número de moléculas está envolvido no progresso da angiogênese tumoral, por exemplo, VEGF e outros fatores para vascularização de tumores sólidos, que envolvem interação com receptores de membrana [17, 31]. Um desses receptores é a neuropilina-1 (NRP1), um co-receptor para VEGFR-2, que aumenta a ligação e a atividade biológica do VEGF165, que tem uma ampla distribuição no tecido que inclui algumas células derivadas de tumor e células endoteliais [32]. Foi demonstrado que Ala-Thr-Trp-Leu-Pro-Pro-Arg (ATWLPPR), um heptapeptídeo, se liga especificamente a NRP1 e é usado com sucesso para detectar tumores NRP-1positivos [12, 17]. No entanto, a afinidade relativamente baixa do A7R monomérico indica uma melhoria adicional para fornecer uma imagem bem-sucedida [33]. As integrinas, um dos receptores de adesão celular, também desempenham um papel crítico na angiogênese e metástase tumoral, especialmente a integrina αvβ3, que é altamente expressa em células tumorais e células endoteliais vasculares ativadas [34]. A sequência de aminoácidos Arg-Gly-Asp (RGD), que se liga especificamente à integrinaαvβ3, tem sido amplamente utilizada para imagiologia não invasiva de tumores [7, 21, 27, 35].
Durante a última década, o direcionamento simultâneo de múltiplos receptores é cada vez mais estudado no campo da imagem [23, 25, 26, 36]. Os sistemas de entrega TF LP ou RGD LP, αvβ3 e galectina-1 com lipossomas paramagnéticos Anx / RGD foram usados para imagiologia de tumor [37, 38]. O efeito sinérgico de motivos de alvo duplo pode agir de várias maneiras. Em primeiro lugar, a disponibilidade de locais de ligação foi um elemento chave da conjugação com ligantes peptídicos. Direcionar dois receptores simultaneamente pode aumentar os locais de ligação nas mesmas células. Em segundo lugar, os peptídeos de duplo direcionamento poderiam ligar dois receptores diferentes para aumentar a probabilidade de agentes de entrega para a região interessada. Além disso, a ligação a duas famílias de receptores diferentes, aumentando a possibilidade de ligação a células tumorais heterogêneas.
Em nosso estudo anterior, novos lipossomas aprisionados com paclitaxel de alvo duplo foram construídos com sucesso ligando uma sequência contendo RGD e um motivo ATWLPPR com um conjugado com um espaçador lys-gly-gly (KGG) e ácido palmítico (Pal) âncora e, em seguida, conjugado à superfície dos lipossomas [39]. Ele revelou que, em comparação com dois peptídeos de alvo único, o peptídeo de alvo duplo tinha a maior atividade de ligação. Estes lipossomas de alvo duplo também mantiveram uma melhor propriedade de ligação do que as formulações de alvo único.
No presente estudo, em vez de drogas terapêuticas, encapsulamos o agente de contraste de MRI Gd-DTPA em lipossomas para imagens moleculares. A absorção celular de lipossomas paramagnéticos de direcionamento foi elevada e os lipossomas de direcionamento duplo indicaram maior afinidade de ligação do que de direcionamento único e, além disso, os lipossomas de direcionamento único mistos. Atualmente, existem duas estratégias comumente usadas para duplo direcionamento, uma é uma mistura de dois ligantes únicos [25, 38] e a outra é a combinação de dois ligantes em uma molécula [39, 40]. Em comparação com a utilização de uma mistura de peptídeos individuais, formulamos a hipótese de que a aplicação de uma conjugação acoplada a dois alvos poderia enxertar um número maior de peptídeos por superfície de lipossoma. No teste de ligação competitiva, forneceu uma evidência crítica de que o direcionamento eficaz do lipossoma às células tumorais foi mediado pela ligação específica de ligantes e receptores de ανβ3-integrina e neuropilina-1. Estes dados confirmaram mais uma vez que os lipossomas de alvo duplo combinados com RGD-ATWLPPR facilitaram a distribuição e acumulação da droga no tumor.
No experimento de imagem MR, Gd-DTPA puro e lipossomas não direcionados foram metabolizados rapidamente por causa de sua molécula pequena, solubilidade em água e efeitos de permeabilidade e retenção aprimorados (efeitos EPR) [41, 42]. Em contraste, um período de circulação prolongado e o acúmulo gradual de lipossomas de alvo duplo no tecido tumoral demonstraram a capacidade de se ligar especificamente a receptores em células tumorais. P articularmente , os lipossomas de alvo duplo foram mais eficazes do que os lipossomas de alvo único. Os lipossomas de duplo direcionamento provavelmente exerceram um efeito sinérgico e a especificidade de entrega de Gd-DTPA ao local do tumor.
Nos últimos anos, um grande número de nanopartículas de alvo duplo foi projetado e sintetizado com sucesso para imagens de tumor devido à sua afinidade de ligação e especificidade melhoradas. Por exemplo, Wu et al. também usou motivos RGD e ATWLPPR para projetar um αvβ3 duplo e um peptídeo heterodimérico direcionado a NRP-1 para a detecção de glioma maligno por imagem de tomografia por emissão de pósitrons (PET) [43]. Em seu estudo, o peptídeo c (RGDyK) foi conectado com ATWLPPR através de um ligante de glutamato e então marcado com flúor-18 (F-18) para imagens de radionuclídeos. O ensaio de ligação ao receptor in vitro demonstrou absorção celular melhorada e afinidade de ligação da sonda de alvo duplo. Além disso, a absorção tumoral in vivo de RGD-ATWLPPR duplo marcado com F-18 foi significativamente maior do que a da molécula de alvo único, e este peptídeo heterodimérico também teve as razões tumor-para-órgão mais altas. Em comparação com sua sonda de peptídeo radiomarcada, nossos lipossomas paramagnéticos de alvo duplo não radioativos poderiam entregar agentes de contraste de forma mais eficaz ao local do tumor devido a uma maior capacidade de carga. Em outro estudo, Zhang et al. construiu com sucesso 68Ga-BBN (Bombesin) -RGD, um rastreador PET heterodimérico direcionado a GRPR (receptor de peptídeo liberador de gastrina) e integrina αvβ3, e os dados clínicos indicaram a segurança e eficiência do radiotraçador PET de duplo direcionamento no diagnóstico e estadiamento do câncer de próstata [44]. No entanto, este radiotraçador PET de alvo duplo só pode ser usado para imagens não invasivas do câncer de próstata porque GRPR foi um biomarcador importante para o câncer de próstata. Ao contrário da sonda de peptídeo BBN-RGD, o peptídeo RGD-ATWLPPR pode se ligar à maioria dos tumores com a superexpressão de VEGFR e / ou integrina na neovasculatura de tumores sólidos. Portanto, espera-se que este lipossoma paramagnético de alvejamento de integrina-NRP1 duplo ανβ3 seja usado para a detecção precoce de vários tumores.
Conclusões
Em nosso estudo, lipossomas paramagnéticos de alvo duplo foram preparados pela conjugação de dois ligantes para ανβ3-integrina e receptores de neuropilina-1 na superfície e carregando o agente de contraste de MRI Gd-DTPA no núcleo dos lipossomas. Esta modificação não interferiu significativamente com a propriedade de Gd-DTPA. O lipossoma de duplo direcionamento facilitou a captação celular específica in vitro, indicando que a afinidade e a ligação do ligante de duplo direcionamento pareciam ser aumentadas sinergicamente. Além disso, a imagem in vivo mostrou que os lipossomas modificados com peptídeos duplos poderiam permanecer em circulação por uma porção maior e por um período mais longo do que a contraparte não direcionada ou de direcionamento único e, então, exibir seletividade e especificidade superiores. Resumindo, nós construímos com sucesso um novo lipossoma paramagnético direcionado à angiogênese com um peptídeo heterodimérico de alvo duplo que poderia se ligar de forma eficiente ao tecido tumoral, e esperamos que esses lipossomas paramagnéticos de alvo duplo tenham o potencial de melhorar o efeito do agente de contraste de MRI para imagens específicas do tumor em um estágio inicial.
Abreviações
- ATWLPPR:
-
Ala-Thr-Trp-Leu-Pro-Pro-Arg
- BBN:
-
Bombesin
- C6:
-
Ácido 6-aminohexanoico
- CT:
-
Tomografia computadorizada
- DMEM:
-
Mídia Eagle Modificada por Dulbecco
- DMSO:
-
Dimetilsulfóxido
- FMOC:
-
Fluorenilmetoxicarbonil
- FOV:
-
Campo de visão
- Gd-DTPA:
-
Ácido gadolínio-dietilenotriamina pentacético
- HPLC:
-
Cromatografia líquida de alta performance
- HUVEC:
-
Célula endotelial da veia umbilical humana
- ICP-OES:
-
Espectrômetro de emissão óptica de plasma indutivamente acoplado
- mPEG2000-DSPE:
-
N- (carbonil-metoxipolietilenoglicol-2000) -1,2-distearoil-sn-glicero-3-fosfoetanolamina
- MRI:
-
Imagem de ressonância magnética
- NRP1:
-
Neuropilina-1
- Pal:
-
Ácido palmítico
- PBS:
-
Salina tamponada com fosfato
- PC:
-
Fosfatidilcolina
- PET:
-
Tomografia por emissão de pósitrons
- RGD:
-
Arg-Gly-Asp
- ROIs:
-
Regiões de interesse
- S / N:
-
Sinal para ruído
- SER:
-
Relação de intensificação do sinal
- SI:
-
Intensidade do sinal
- STIR:
-
Spin-echo de recuperação de inversão
- TE:
-
Hora do eco
- TEM:
-
Microscopia eletrônica de transmissão
- TR:
-
Tempo de repetição
- VEGF-R:
-
Receptor do fator de crescimento endotelial vascular
Nanomateriais
- Imagem de Ressonância Magnética (MRI)
- Demonstração de um biossensor flexível à base de grafeno para detecção sensível e rápida de células cancerosas do ovário
- Novel Biocompatible Au Nanostars @ PEG Nanopartículas para imagens In Vivo CT e propriedades de depuração renal
- Síntese e desempenho in vitro de nanopartículas de ferro-platina revestidas com polipirrole para terapia fototérmica e imagem fotoacústica
- Nanomontagens de ácido 5-aminolevulínico-esqualeno para fotodetecção e terapia de tumor:estudos in vitro
- Novela dupla mitocondrial e nanopartículas de direcionamento do receptor CD44 para liberação desencadeada por estímulos redox
- Anticorpo monoclonal de heparanase marcado com nanopartículas de ouro magnético e sua aplicação subsequente para imagens de ressonância magnética de tumor
- Caracterização de ressonância magnética e de micro-ondas dependente da espessura de filmes FeCoBSi padronizados de listras combinadas
- Nanopartículas de albumina conjugada com corante próximo ao infravermelho e carregadas com artesunato como agente fotoquimo teranóstico direcionado a tumor de alta eficiência
- Nanosensibilizador magnético modificado por aptâmero para imagens de ressonância magnética in vivo de câncer que expressa HER2



