Preparação e caracterização de nanopartículas de heme em forma de girino e esfera para maior solubilidade
Resumo
Hemin é um suplemento de ferro potente. Uma limitação importante da aplicabilidade da hemina é a sua solubilidade e biodisponibilidade aquosa extremamente baixas. O objetivo deste trabalho é preparar nanopartículas de hemina com melhor solubilidade. Imagens de microscopia eletrônica de transmissão mostraram que nanopartículas de hemina com diferentes concentrações iniciais de hemina (0,1 e 0,5 mg / mL) eram em forma de girino (cabeça de aproximadamente 200 nm e cauda de 100 nm) e em forma de esfera (50–100 nm), respectivamente. Além disso, as nanopartículas de hemina exibiram maior solubilidade do que a hemina livre. A solubilidade das nanopartículas em forma de esfera foi 308,2 vezes maior do que a da hemina pura a 25 ° C. As nanopartículas de hemina foram estáveis em condições ácidas e exibiram excelente estabilidade térmica. Esses resultados sugerem que as nanopartículas de hemina podem servir como um suplemento potencial de ferro com aplicações potenciais nos campos da terapia alimentar, biomédica e fotodinâmica-fototérmica.
Introdução
O ferro é um elemento essencial nos processos metabólicos do corpo, como transferência de elétrons, armazenamento e transporte de oxigênio [1]. A deficiência de ferro é uma das deficiências nutricionais mais comuns, influenciando cerca de 20% da população mundial [2]. A consequência mais negativa da deficiência de ferro é a anemia sideropênica. É causada principalmente por ingestão insuficiente de ferro na dieta, geralmente quando a demanda é alta. Em humanos, o ferro dietético pode entrar no corpo em duas formas principais:uma é o ferro inorgânico (ferro não heme), liberado principalmente de vegetais e alimentos à base de plantas, e a outra é o ferro heme, adquirido da degradação da hemoglobina ou mioglobina presente em animais. O hemina foi encontrado no sangue e em produtos cárneos, é um componente de muitas hemoproteínas (incluindo mioglobina, hemoglobina e citocromos bec) e é duas ou três vezes mais facilmente absorvido (50-87%) do que o ferro não heme [3] . Recentemente, pesquisadores testemunharam grandes avanços em nossa compreensão do papel fisiológico da hemina. Infelizmente, a hemina é hidrofóbica devido à presença de um grande macrociclo tetrapirrólico [4]. Devido à alta hidrofobicidade e baixa solubilidade da hemina em solução aquosa neutra, sua aplicação em vários campos tem sido limitada. Assim, há uma necessidade urgente de aumentar a solubilidade da hemina.
Para enfrentar este desafio, muitos esforços foram dedicados a melhorar a solubilidade da hemina. Berner [5] descobriu que a proteína da solução enzimática parcial (isolado de soja, farinha de soja ou concentrado de soja) pode se unir ao ferro heme para aumentar a absorção de ferro, o que melhora a biodisponibilidade do ferro. Wang et al. [6] indicaram que hemina e L-arginato cristalinos podem preparar a coacervação de hemina-arginato solúvel em água, que pode ser usada como um novo suplemento de ferro heme em aditivos alimentares, alimentos funcionais e produtos farmacêuticos. Zhang et al. [7] relataram que a hemina poderia se combinar com a β-ciclodextrina por um oligossacarídeo cíclico de sete unidades de glicose ligadas a α [1, 4], levando a uma melhora significativa na solubilidade da hemina. Embora tenha havido algum progresso na melhoria da solubilidade do ferro heme, a industrialização não foi fácil devido ao complicado processo de preparação. Portanto, desenvolver um método simples para melhorar a solubilidade da hemina ainda é um grande desafio.
A nanociência e a nanotecnologia têm o potencial de fornecer novas soluções no desenvolvimento de substâncias funcionais, principalmente a inclusão de compostos bioativos sem afetar a percepção sensorial dos consumidores e melhorando a absorção de determinados componentes [8]. As nanopartículas têm várias vantagens [9], incluindo a promoção da solubilidade de substâncias hidrofóbicas [10]. Duhem et al. [11] desenvolveram novos nanomedicamentos baseados em vitamina E por meio de nanotecnologias, que ofereciam múltiplas vantagens na entrega de medicamentos, como biocompatibilidade, melhor solubilidade do medicamento e atividade anticâncer. Chang et al. [12] relataram que as nanopartículas preparadas por cadeias curtas de glucana modificadas com anidrido succínico poderiam carregar luteína hidrofóbica, o que poderia aumentar a solubilidade da luteína em água. Apesar do enorme potencial das nanopartículas, a hemin em nanoescala ainda não foi relatada. Postulamos que a solubilidade das nanopartículas de hemina poderia ser aumentada em comparação com a hemina livre, que poderia ter aplicações valiosas.
O objetivo principal do presente trabalho é desenvolver nanopartículas de hemin com diferentes formatos usando uma técnica de diálise fácil e aumentar sua solubilidade. Foram avaliados os parâmetros de preparação da concentração inicial de hemin e as condições de diálise. Além disso, foram avaliadas a solubilidade e estabilidade contra o pH, tratamento térmico e sal das nanopartículas de hemina formadas. No geral, as melhorias na solubilidade da hemina têm uma variedade de campos de aplicação potenciais.
Materiais e métodos
Materiais
Membranas de heme e diálise com peso molecular de corte de 8–12 kDa foram adquiridas de Beijing Solarbio Science &Technology Co., Ltd. (Pequim, China). Acetona (CH 3 COCH 3 , ≥ 99,5%) foi adquirido da Kant Chemical Co., Ltd. (Laiyang, China). Todos os outros reagentes usados eram de grau analítico.
Preparação de Nanopartículas de Hemin
Nanopartículas de hemina foram preparadas usando um método de diálise:0,1 mg / mL (ou 0,5 mg / mL) de hemina dissolvida em acetona acidificada com 0,1 mL de ácido clorídrico concentrado. A solução de hemina foi dialisada por diferentes dias, a água foi trocada a cada dia e foi liofilizada para obtenção de nanopartículas de hemina. Para verificar o efeito de parâmetros variáveis na preparação de nanopartículas de hemina, as relações de volume de hemina / água foram estabelecidas em 1:3, 1:5, 1:10 e 1:50; as temperaturas de cultivo foram fixadas em 4 e 25 ° C; e os tempos de incubação foram fixados em 1, 3 e 5 dias.
Microscopia Eletrônica de Transmissão (TEM)
Imagens TEM de nanopartículas foram tiradas com um microscópio eletrônico de transmissão 7700 (Hitachi, Tóquio, Japão) com uma tensão de aceleração de 80 kV. Uma pequena gota de amostra foi depositada em uma grade de cobre revestida de carbono e, em seguida, liofilizada para observação.
Tamanho médio e medições de potencial Zeta
O tamanho médio, o potencial zeta (potencial ζ) e o índice de polidispersidade (PDI) das partículas foram medidos por meio de dispersão de luz dinâmica (DLS), usando um Malvern Zetasizer Nano (Malvern Instruments Ltd., Reino Unido). As amostras foram diluídas em água MilliQ e analisadas a 25 ° C. A concentração das amostras diluídas foi de 0,05%.
Espectro de absorção de UV-Vis
As medições de espectroscopia de UV-Vis das nanopartículas de hemina e hemina livres dissolvidas em acetona aquosa acidificada foram realizadas em um espectrofotômetro de UV-Vis (TU-1810, Pequim, China). A absorção molecular foi digitalizada em um comprimento de onda de 200-800 nm em intervalos de 1 nm para obter um espectro.
Ensaio de solubilidade
A solubilidade aquosa quantitativa de hemina e nanopartículas puras foi investigada de acordo com o método relatado por Gidwani et al. [13]. Resumidamente, soluções supersaturadas de hemina pura e nanopartículas foram adicionadas separadamente a 5 ml de água desionizada em tubos de ensaio, respectivamente. Os tubos de ensaio foram agitados constantemente (500 rpm) a diferentes temperaturas (25, 37, 60 e 80 ° C) durante 30 min. Em seguida, a solução foi centrifugada a 3500 g e o sobrenadante foi diluído adequadamente com acetona aquosa acidificada. A concentração das amostras foi determinada em 640 nm por um espectrofotômetro UV-Vis. Para cada medição, a linha de base foi estabelecida usando acetona aquosa acidificada em branco como referência.
pH, temperatura e estabilidade do sal
O tamanho, potencial ζ, PDI e turbidez das nanopartículas (0,5 mg / mL) foram medidos e comparados com os valores iniciais para avaliar a estabilidade das nanopartículas. As suspensões de partículas foram divididas em dez grupos:seis grupos foram ajustados aos valores de pH desejados [2, 3, 5, 7, 9, 11], e utilizando ácido clorídrico (0,1 M) ou solução de hidróxido de sódio (0,1 M); três grupos foram aquecidos a 25, 60 e 80 ° C e, em seguida, resfriados à temperatura ambiente; outro foi conduzido com diferentes concentrações de cloreto de sódio (NaCl, 0, 10, 50, 100, 250 e 500 mM), respectivamente. As soluções misturadas permaneceram durante a noite a 25 ° C.
Espectroscopia de infravermelho com transformada de Fourier (FTIR)
As estruturas químicas das nanopartículas de hemina foram confirmadas usando espectros FTIR (Tensor 27, Jasco Inc., Easton, MD, EUA). Um total de 32 digitalizações com resolução de 4 cm - 1 foram acumulados usando o software de varredura rápida em OMNIC 8.0 para obter um único espectro. A faixa espectral foi de 400–4000 cm - 1 .
Espectroscopia de fluorescência
As medições de fluorescência de hemina livre e nanopartículas foram realizadas usando um espectrofotômetro de fluorescência (F-7000, Hitachi, Japão). Os espectros de fluorescência das amostras foram obtidos em comprimentos de onda entre 300 e 600 nm com excitação em 402 nm.
Difractograma de Raios-X (XRD)
O XRD de hemina livre e nanopartículas foi obtido usando um difratômetro de raios-X (AXS D8 ADVANCE; Bruker, Karlsruhe, Alemanha), e as amostras foram investigadas no 2 θ faixa de 4–40 °. A cristalinidade relativa de hemina livre e nanopartículas foi determinada traçando a linha de base dos picos no difractograma e calculando a área usando o visualizador de espectro de software com base no método relatado por Jivan et al. [14]. A área acima e abaixo da curva correspondia a domínios cristalinos e regiões amorfas, respectivamente. A proporção da área superior para a área total foi tomada como a cristalinidade relativa:
Cristalinidade relativa (%) =Área sob os picos / Área total da curva × 100.
Análise estatística
Amostras em triplicado de todos os resultados quantitativos foram obtidas. Os resultados foram relatados como valores médios e desvios padrão. A análise estatística foi realizada pelos testes de intervalo múltiplo de Duncan usando o pacote de software estatístico SPSS V.17 (SPSS Inc., Chicago, IL, EUA).
Resultados e discussão
Formação e caracterização de nanopartículas de Hemin
A morfologia e o tamanho das nanopartículas de hemin fabricadas usando o método de diálise foram examinados por TEM. Quando a concentração de hemina era de 0,5 mg / mL, nanoestruturas de hemina com diferentes tamanhos foram formadas em várias relações de volume de hemina / água e para diferentes dias de diálise (Fig. 1, Arquivo adicional 1:Figura S1-S3). As nanopartículas tinham formas esféricas bem definidas e diâmetros de 50–100 nm quando a relação volume de hemina / água era de 1:10 após 3 dias de diálise. Com um aumento na relação volume de hemina / água (1:50), as nanopartículas foram reunidas em partículas em forma de bastonete (Fig. 1). Particularmente, descobrimos que à medida que o tempo de diálise aumentou de 1 para 3 dias, as nanopartículas de hemina se tornaram uniformemente dispersas (Arquivo adicional 1:Figura S1-S3). A temperatura (4 e 25 ° C) da diálise teve pouca influência no tamanho das partículas e na dispersão das nanopartículas de hemin (Arquivo adicional 1:Figura S4).

Imagens TEM de nanopartículas de hemina preparadas por diálise por 3 dias com várias relações de volume de hemina / água, incluindo 1:3 ( a ), 1:5 ( b ), 1:10 ( c ) e 1:50 ( d ) a 25 ° C. A concentração de hemina foi de 0,5 mg / mL
A Figura 2 mostra as imagens típicas de TEM de nanopartículas de hemina preparadas para diferentes dias de diálise com a concentração de hemina de 0,1 mg / mL. Os produtos eram principalmente nanopartículas bem definidas, dispersas individualmente, estruturalmente incomuns e em forma de girino. As nanopartículas semelhantes a girinos foram distribuídas preferencialmente com 3 dias de diálise. O girino exibiu uma disparidade significativa de tamanho desde a largura máxima da cabeça (200 nm) até a cauda (100 nm). Nossos resultados mostraram que nanopartículas uniformemente dispersas podem ser formadas na proporção hemina / volume de água de 1:10 e após diálise por 3 dias a 25 ° C para as nanopartículas em forma de esfera e girino. Assim, escolhemos esses dois tipos de nanopartículas de hemina para as pesquisas seguintes.

Imagens TEM de nanopartículas de hemina preparadas com a razão de volume de hemina / água de 1:10 em vários dias de diálise, incluindo 1 dia ( a ), 3 dias ( b ) e 5 dias ( c ) a 25 ° C. A concentração de hemina foi de 0,1 mg / mL
Para examinar melhor o tamanho das nanopartículas de hemina, a determinação de DLS foi usada para confirmar a formação de nanoestruturas. Os diâmetros das nanopartículas em forma de esfera e girino foram de aproximadamente 218,2 ± 6,2 e 299,8 ± 7,6 nm, respectivamente (Fig. 3a). O tamanho das nanopartículas medido por DLS foi um pouco maior do que os resultados medidos por TEM; esta diferença foi atribuída ao inchaço das nanopartículas em solução aquosa. A medição DLS era conhecida por indicar os diâmetros hidrodinâmicos das nanopartículas em uma solução [15]. O potencial ζ das nanopartículas em forma de esfera (- 21,4 mV) foi aproximadamente duas vezes maior do que as nanopartículas em forma de girino (- 10,8 mV) (Fig. 3b). O PDI das nanopartículas de hemina também foi determinado para analisar a distribuição do tamanho de partícula. Os resultados mostraram que o PDI das nanopartículas em forma de esfera e em forma de girino foi de 0,348 e 0,402, respectivamente (Fig. 3c). Esta descoberta indicou que as nanopartículas de hemina obtidas tinham boa polidispersidade.
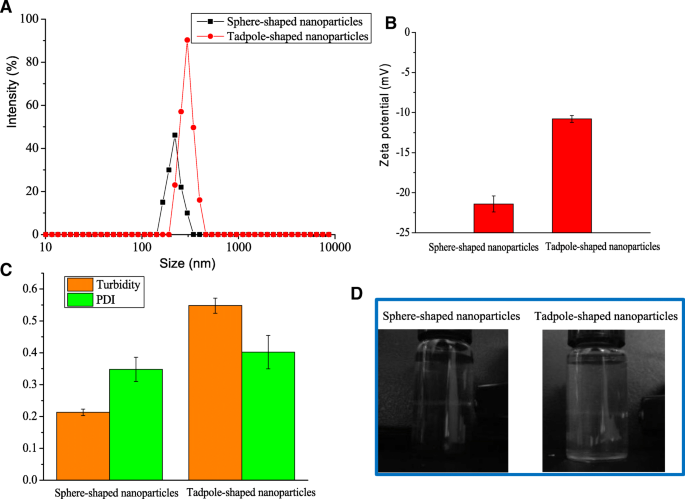
O tamanho médio ( a ), potencial ζ ( b ), PDI e turbidez ( c ), e efeito Tyndall ( d ) de nanopartículas de hemina de formas diferentes
Conforme um feixe de luz passa por uma dispersão coloidal, uma porção da luz é espalhada pelas partículas coloidais presentes na solução, levando a uma divergência do feixe de luz. Este comportamento é denominado efeito Faraday-Tyndall [16]. Neste caso, a solução de hemina livre não apresentou efeito Tyndall (Arquivo Adicional 1:Figura S5). No entanto, o efeito Tyndall foi observado na suspensão de nanopartículas em forma de esfera e girino (Fig. 3d), verificando a formação de coloides ou nanopartículas na suspensão fina. O mecanismo de formação das nanopartículas de hemina pelo método de diálise pode ser devido à difusão do solvente pela interface entre a fase aquosa externa e a fase orgânica solvente interna, o que resultou na diminuição da solubilidade da hemina e na formação do núcleo cristalino. Posteriormente, nanopartículas de hemina de diferentes formas foram formadas devido ao crescimento e automontagem do núcleo de um único cristal de maneiras diferentes.
Análise de absorção de UV-Vis
De acordo com os resultados acima, investigamos se havia alguma diferença entre as duas formas de nanopartículas de hemina em sua geração de cromóforo. O espectro UV-Vis de nanopartículas em forma de esfera e girino mostrou as mesmas bandas de absorção em 265 nm (Fig. 4a). As nanopartículas em forma de esfera apresentaram uma banda de absorção estreita em 667 nm e 775 nm. Em comparação, a solução de nanopartículas em forma de girino apresentou um pico largo a 658 nm sem um pico de 775 nm. Além disso, a intensidade de absorção de nanopartículas em forma de esfera foi maior do que a de nanopartículas em forma de girino. Uma diferença tão grande não poderia ser explicada considerando o girino como a soma de uma esfera e uma haste cônica, nem por uma configuração de esfera um tanto imperfeita. A oscilação de elétrons correspondente a uma absorção de plasmon ao longo do eixo longo é retardada e / ou em um caminho reflexivo. Assim, as propriedades ópticas das nanopartículas de hemina eram dependentes da forma, semelhante ao relatório de Hu et al. [17], que descobriu que nanopartículas de ouro em forma de girino e esfera tinham propriedades ópticas diferentes.
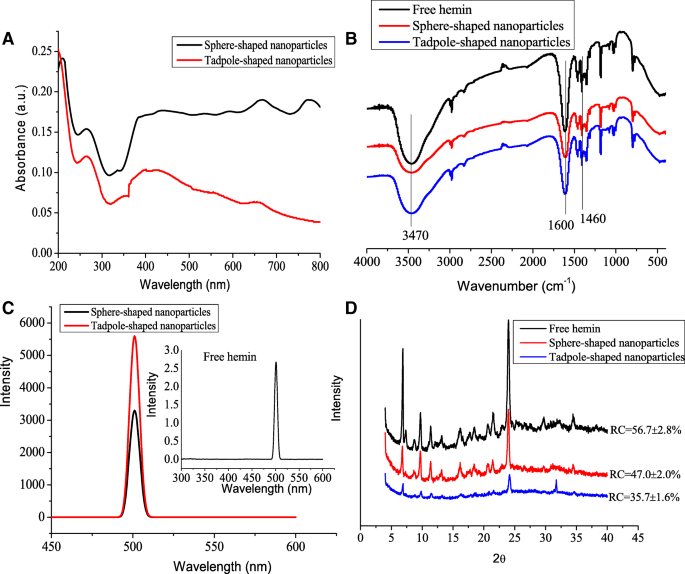
a Espectro UV-Vis, b Espectro FTIR, c espectro de emissão de fluorescência e d Padrões de XRD de hemina livre, nanopartículas em forma de esfera e nanopartículas em forma de girino. As nanopartículas foram dispersas em água desionizada. RC, cristalinidade relativa
A solução de hemina livre exibiu uma absorção máxima a 344 nm, e isso foi atribuído à banda de Soret comumente associada às porfirinas (Arquivo adicional 1:Figura S5). A banda de absorção das nanopartículas de hemina mudou de 344 para 265 nm, o que sugeriu que o efeito conjugativo π-π das nanopartículas de hemina foi aumentado. Surpreendentemente, em comparação com a hemina livre, ambos os tipos de nanopartículas exibiram uma absorção alta e forte no infravermelho próximo, que é altamente apropriada para aplicações baseadas em absorção, como terapia fototérmica e imagem fotoacústica [18]. Magno et al. [19] também relataram que nanopartículas de porfirina com absorção no infravermelho próximo receberam considerável interesse para aplicações em fototerapias e fotodiagnósticos, mesmo como nanopartículas magnéticas para terapia de hipertermia magnética e sistemas de entrega de drogas.
Solubilidade
A solubilidade da hemina é um fator importante, que pode afetar diretamente a eficácia de absorção no corpo. A solubilidade aquosa quantitativa de hemin e nanopartículas de hemin pura em diferentes temperaturas foi testada (Tabela 1). Conforme a temperatura aumentou, a solubilidade aquosa de todas as amostras aumentou. Por exemplo, a solubilidade da hemina livre a 25, 37, 60 e 80 ° C foi 0,009 ± 0,000, 0,060 ± 0,002, 0,144 ± 0,004 e 0,245 ± 0,008 mg / mL, respectivamente (Tabela 1).
A quantidade de nanopartículas em forma de esfera dissolvidas a 25, 37, 60 e 80 ° C foi de 1,333 ± 0,023, 1,499 ± 0,072, 1,889 ± 0,081 e 3,853 ± 0,124 mg / mL, respectivamente, e as nanopartículas em forma de girino foram 0,997 ± 0,045, 1,231 ± 0,035, 1,521 ± 0,058 e 1,795 ± 0,050 mg / mL, respectivamente. Os resultados do estudo da solubilidade aquosa das nanopartículas mostraram um aumento significativo em comparação com a hemina pura. As nanopartículas em forma de esfera exibiram maior solubilidade em temperaturas de 25, 37, 60 e 80 ° C do que as nanopartículas em forma de girino. Esta descoberta sugere que a solubilidade das nanopartículas em forma de esfera pode ser 308,2 vezes maior em comparação com a hemina livre a 25 ° C. Este aumento na solubilidade foi principalmente devido ao tamanho de partícula em nanoescala único. Este resultado foi consistente com outros estudos relatados por Gidwani e Vyas [13].
Análises de espectros de FTIR
Os espectros de FTIR podem ser usados para identificar tipos de grupos funcionais. A banda em 3470 cm - 1 é atribuída principalmente ao alongamento da vibração dos grupos N – H e hidroxila da hemina (Fig. 4b). Uma banda em 1460 cm - 1 é atribuída à vibração no plano N – H devido à vibração de flexão fora do plano de –CH 3 do anel pirrole aromático de hemina. O pico em 1600 cm - 1 é o pico característico da ligação amida devido à vibração de alongamento de C =O do grupo carboxila ligado à superfície da hemina, que revela que a ligação amida secundária existe na hemina. Esses resultados são consistentes com os de Xi et al. [20]. No entanto, o pico em 3470 cm - 1 de nanopartículas de hemina foi mais amplo do que a de hemina livre, indicando claramente a interação de ligação de hidrogênio aprimorada entre nanopartículas.
Espectros de fluorescência
As propriedades de fluorescência de hemina livre e nanopartículas de hemina também foram monitoradas por espectroscopia de fluorescência. Os sinais de fluorescência de nanopartículas em forma de esfera e girino foram aumentados no máximo de emissão aparente a 500 nm em comparação com a hemina livre (Fig. 4c). Isso pode ser devido ao aumento da solubilidade da hemina após a formação das nanopartículas [21].
Análise de XRD
A natureza cristalina das nanopartículas de hemina e hemina livres foi confirmada por XRD. Conforme ilustrado na Fig. 4d, os padrões de XRD de hemina livre exibiram vários picos de reflexão relativamente fortes em 2 θ =6,8, 9,6, 11,5, 16,2, 21,5 e 23,9 °. Os picos característicos das nanopartículas esféricas foram iguais aos da hemina livre, indicando que a estrutura cristalina das nanopartículas esféricas não se alterou nas formulações das nanopartículas. No entanto, para as nanopartículas em forma de girino, a maioria dos picos característicos desapareceram. Além disso, a cristalinidade relativa das nanopartículas em forma de esfera e girino diminuiu significativamente para 47,0% e 35,7%, respectivamente, em comparação com 56,7% para a hemina livre. Esses resultados indicaram que as formulações de nanopartículas podem destruir as regiões cristalinas parciais da hemina.
Efeitos do pH, temperatura e concentração de sal na estabilidade
As variações no tamanho, PDI, potencial ζ e turbidez das nanopartículas de hemina após a incubação em diferentes níveis de pH [2,3,4,5,6,7,8,9,10,11] foram medidas (Fig. 5a , b). O tamanho das nanopartículas de hemina permaneceu quase inalterado com diâmetros médios de aproximadamente 200 nm em condições ácidas (Fig. 5a). Em baixos valores de pH de 2, o tamanho das nanopartículas de hemina foi diminuído para aproximadamente 122,4 nm. A um pH de 7, o tamanho das nanopartículas aumentou para 293,6 nm e aumentou significativamente ( P <0,05) em condições alcalinas (um pH de 9 e 11,0) com diâmetros médios acima de 400 nm. O PDI das nanopartículas foi inferior a 0,5 em condições ácidas, demonstrando nenhuma agregação aparente das nanopartículas [22]. O potencial ζ das nanopartículas diminuiu com o aumento dos valores de pH (Fig. 5b). A turbidez das nanopartículas apresentou a mesma tendência em tamanho. Esses resultados indicaram que as nanopartículas eram estáveis em condições ácidas e instáveis em condições alcalinas.
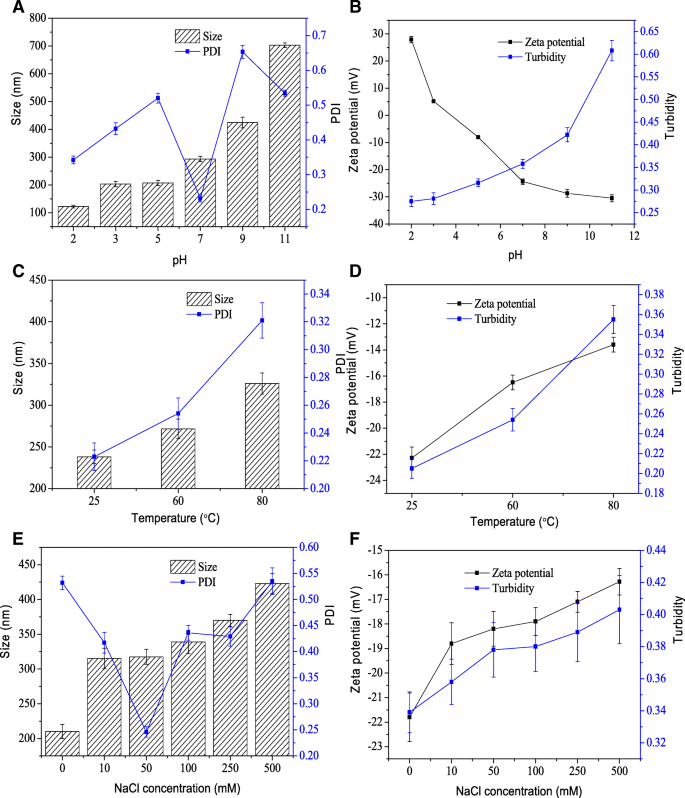
Estabilidade das nanopartículas de hemina. O efeito de vários níveis de pH ( a ), temperaturas ( c ), e concentrações de sal ( e ) no tamanho de partícula e PDI de nanopartículas. O efeito de vários níveis de pH ( b ), temperaturas ( d ) e concentrações de sal ( f ) no potencial ζ e turbidez
Os efeitos do tratamento térmico (25, 60 e 80 ° C) por 30 min no tamanho, PDI, potencial ζ e turbidez das nanopartículas de hemina foram determinados (Fig. 5c, d). Quando a temperatura foi aumentada, o tamanho da partícula, PDI, potencial ζ e turbidez das nanopartículas aumentaram ligeiramente. Os resultados sugerem que as nanopartículas de hemina apresentam excelente estabilidade térmica. Da mesma forma, conforme a força iônica foi aumentada, o tamanho, o potencial ζ e a turbidez das nanopartículas também aumentaram, o que causou a dissociação das nanopartículas (Fig. 5e, f).
Conclusões
Neste trabalho, primeiro desenvolvemos nanopartículas de hemina em forma de girino e esfera usando uma técnica de diálise fácil, que poderia aumentar significativamente a solubilidade em 308,2 vezes a 25 ° C. Além disso, as nanopartículas de hemina foram estáveis em condições ácidas e exibiram excelente estabilidade térmica. Além disso, ambas as nanopartículas exibiram forte absorção no infravermelho próximo. O trabalho futuro se concentrará no estudo aprofundado do projeto de um sistema nanocarreador de hemin de resposta optotérmica para carregamento de ingrediente ativo. Nanopartículas de hemina com solubilidade aprimorada podem ter aplicações potenciais nos campos biomédico, alimentar, terapia fotodinâmica e terapia fotodinâmica-fototérmica.
Abreviações
- DLS:
-
Espalhamento de luz dinâmico
- FTIR:
-
Transformada de Fourier Infra-vermelho
- TEM:
-
Microscopia eletrônica de transmissão
- XRD:
-
Difractograma de raios-x
Nanomateriais
- Nanofibras e filamentos para entrega aprimorada de drogas
- Nanopartículas multifuncionais de ouro para aplicações diagnósticas e terapêuticas aprimoradas:uma revisão
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Preparação e propriedades magnéticas de nanopartículas de espinélio FeMn2O4 dopadas com cobalto
- Preparação e atividade de hidrogenação catalítica aprimorada de nanopartículas de Sb / Palygorskite (PAL)
- Bioflavonóide direcionado ao receptor de folato Nanopartículas de quitosana carregadas com genisteína para efeito anticâncer avançado em cânceres cervicais
- Síntese hidrotérmica de nanopartículas de In2O3 híbridos gêmeos heteroestruturas de ZnO de disco hexagonal para atividades fotocatalíticas aprimoradas e estabilidade
- Novel Biocompatible Au Nanostars @ PEG Nanopartículas para imagens In Vivo CT e propriedades de depuração renal
- Método de pós-tratamento para a síntese de nanopartículas FePt-Fe3O4 binárias monodispersas
- Tornos aprimorados para polimento e rebarbação



