Síntese, caracterização e avaliação de nanopartículas de oligossacarídeo de quitosana sensível a redox revestidas com ficocianina para administração de medicamentos
Resumo
Neste artigo, um tipo de nanopartículas de curcumina com ácido ditiodipropiônico-ácido ditiodipropiônico (BCSC) com ficocianina (PC) e curcumina carregada com curcumina (CUR), foram projetadas para aumentar a biocompatibilidade de CUR. A estrutura do BCSC foi confirmada usando 1 H-NMR. Em CUR-BCSC @ PCs com um diâmetro hidrodinâmico médio de 160,3 ± 9,0 nm, a proteína biomimética corona deu às nanopartículas uma excelente estabilidade e potencial para evitar a adsorção de proteínas na circulação sanguínea. O experimento de liberação in vitro verificou que CUR-BCSC @ PCs com conchas responsivas a redox eram sensíveis a altas concentrações de glutationa. Além disso, os CUR-BCSC @ PCs foram eficazes no aumento da atividade inibitória na proliferação de células A549 ao aumentar a absorção intracelular de CUR. Estes resultados indicaram que os CUR-BCSC @ PCs têm grandes perspectivas de aplicação na terapia do câncer como transportadores eficazes de distribuição de drogas.
Histórico
Oligossacarídeo de quitosana (COS) com a estrutura de D- β- (1-4) -ligado glucosaminas é um produto de despolimerização preparado principalmente por desacetilação e hidrólise enzimática de quitosana ou quitina, que é derivada de exoesqueletos de artrópodes ou das paredes celulares de fungos [1, 2]. Vale ressaltar que metais pesados e corantes podem ser removidos pela quitosana e sua forma modificada de materiais, nos quais a quitosana atua como adsorvente [3]. Vários estudos têm demonstrado que o COS possui várias propriedades biológicas, como ser anticâncer, antiinflamatório, antioxidante e imunoestimulante [4]. O COS é considerado um material carreador de drogas não tóxico, devido à sua biocompatibilidade, alta solubilidade em água e modificabilidade química [5, 6].
A fim de melhorar a solubilidade de drogas anticâncer hidrofóbicas e reduzir a toxicidade aos tecidos normais, pesquisadores médicos têm estudado copolímeros, que podem se automontar em micelas de uma certa faixa de tamanho de partícula [7, 8]. Esses conjuntos copoliméricos podem atingir e penetrar no local do tumor passiva ou ativamente. As micelas são compostas por duas seções funcionais individuais:o núcleo, no qual as drogas hidrofóbicas são encapsuladas, e a camada externa ou coroa, que controla as propriedades farmacocinéticas in vivo [8]. Wang et al. [9] enxertou ácido desoxicólico nas cadeias COS por meio de uma modificação química para formar copolímeros em bloco anfifílicos, que poderiam se automontar em micelas em solventes inorgânicos de baixo custo. O núcleo hidrofóbico das micelas continha quercetina, o que melhorou muito a solubilidade em água de drogas anticâncer e, por sua vez, aumentou a biodisponibilidade da quercetina.
A curcumina (CUR) é um dos principais constituintes químicos da cúrcuma [10]. Nos últimos anos, muitos pesquisadores estudaram as propriedades anticâncer do CUR, e muitos estudos confirmaram que este produto químico pode influenciar o crescimento das células tumorais por meio de várias vias de sinalização e melhorar o sistema imunológico [11]. Além disso, o CUR é um fotossensibilizador com boas propriedades fotodinâmicas [12]. Assim, o CUR é um medicamento promissor para a terapia do câncer. No entanto, sua baixa solubilidade, estabilidade e biodisponibilidade limitam sua aplicação clínica [13]. Para mitigar essas desvantagens, muitos pesquisadores melhoraram a biodisponibilidade de CUR por meio de sistemas de entrega de drogas. Por exemplo, Chen et al. [14] desenvolveram um novo tipo de transportador de droga sensível ao pH duplo, que aumentou a solubilidade da CUR em água e melhorou seu efeito no tratamento do tumor.
A ficocianina (PC), obtida principalmente de cianobactérias, é conhecida como uma proteína pigmentar solúvel em água e captadora de luz, que desempenha um papel na captura e transferência de luz em energia química durante a fotossíntese [15]. O PC exerce múltiplas propriedades biológicas, como ser anticancerígeno [16], antiinflamatório e antioxidante que tem atraído muita atenção nas áreas de alimentos e medicamentos [15, 17]. Hao et al. [16] descobriram que o PC inibiu o crescimento de células de câncer de pulmão de células não pequenas ao regular negativamente a proteína adaptadora contendo o domínio do receptor de toll / interleucina-1 (TIRAP). Além disso, o PC também é utilizado na terapia fotodinâmica (TFD) de tumores, pois é um excelente agente sem efeitos colaterais [18,19,20]. A utilização de PC como sondas fluorescentes precisa ser conjugada com elementos de identificação específicos, como biotina, anticorpos e estreptavidina [21, 22]. A biotina, uma vitamina solúvel em água, é um micronutriente essencial no corpo humano, que possui propriedades de direcionamento a tumores [23]. As proteínas receptoras específicas da biotina, como avidina, neutravidina e estreptavidina, são altamente superexpressas na superfície de várias células cancerosas em comparação com as células normais [24, 25]. Assim, nanopartículas biotiniladas têm sido extensivamente estudadas para serem uma entrega de drogas via endocitose mediada por receptor [24].
No presente estudo, um novo tipo de nanocarreador PC funcionalizado foi construído, e a preparação de CUR-BCSC @ PCs é apresentada na Fig. 1. A ligação dissulfeto entre COS e CUR contribuiu para a sensibilidade redutiva do material carreador anfifílico [26 ] CUR estava localizado no núcleo interno hidrofóbico protegido pelo escudo COS / PC. A interação entre a biotina e o PC e a interação eletrostática, que foi entre o COS carregado positivamente e o PC carregado negativamente, foram usados para modificar o PC na superfície dos CUR-BCSCs. Esperava-se que os CUR-BCSC @ PCs atingissem os tecidos tumorais devido à permeabilidade aprimorada, o efeito de permeabilidade e retenção aprimoradas (EPR) e o efeito de direcionamento do receptor de biotina [27]. No microambiente tumoral, que tem uma concentração de glutationa mais alta do que as células normais, o CUR-BCSC @ PCs se desintegrou por meio de reações de troca de dissulfeto de tiol, atingindo uma alta concentração de droga nas células tumorais [23, 28, 29]. O sistema de nanotransmissão CUR-BCSC @ PC descrito neste artigo não apenas melhorou a biodisponibilidade de CUR, mas também tem o potencial de ser eficaz no tratamento clínico de tumores.
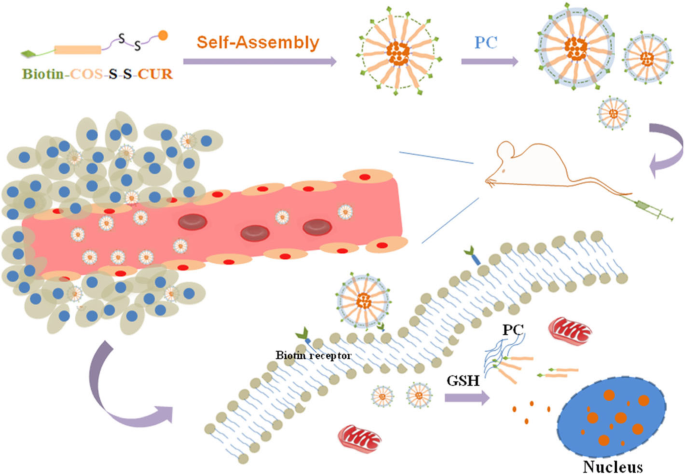
Projeto e ilustração esquemática de CUR-BCSC @ PCs
Materiais e métodos
Materiais
O CUR foi adquirido a Zhanyun Chemical Co., Ltd. (Xangai, China). COS foi adquirido de Shandong Weikang Biomedical Science and Technology Co., Ltd. PC foi obtido de Zhejiang Binmei Biotechnology Co., Ltd. O ácido 3,3-ditiodipropiônico foi obtido de Adamas Reagent Co., Ltd. (Shanghai, China). Cloridrato de carbodiimida carbonizada (EDCI), dimetilamino piridina (DMAP), tetrahidrofurano (THF), cloreto de oxalil e biotina foram adquiridos da Aladdin Chemistry Co., Ltd. L-Glutationa (GSH) e Hoechst 33342 foram adquiridos da Sigma-Aldrich (Shanghai , China). Os sacos de diálise (MWCO 300 Da) foram obtidos de Beijing Biotopped Technology Co., Ltd. A formamida foi preparada por Tianjin Fuyu Fine Chemical Co., Ltd. A água desionizada foi produzida pelo próprio no laboratório.
Uma linha de células A549 (células de carcinoma de pulmão humano) (Bena Culture Collection (Beijing, China)) foi escolhida para avaliar a citotoxicidade do novo nanocarreador. As células A549 foram cultivadas em DMEM (Saiersi Biotechnology Co., Ltd. (Shangdong, Yantai, China)). O soro fetal bovino (FBS) foi obtido na Hyclone (Logan, UT, EUA). A penicilina e a estreptomicina foram adquiridas na Sigma-Aldrich (Shanghai, China). O brometo de 3- (4,5-dimetil-2-tiazolil) -2,5-difenil-2-H-tetrazólio (MTT) também foi adquirido da Sigma-Aldrich (Shanghai, China).
Síntese de CUR-BCSC @ PCs
As rotas sintéticas usadas para preparar CUR-BCSC @ PCs são mostradas na Fig. 2. Os procedimentos experimentais detalhados são descritos abaixo.
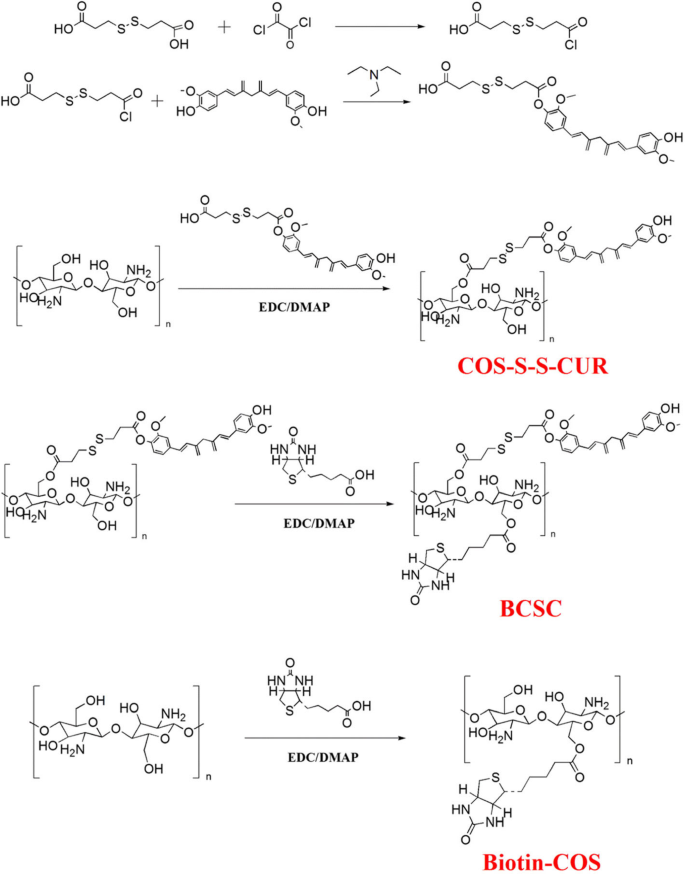
Via sintética de COS-S-S-CUR, BCSC e Biotina-COS
Síntese de COS-S-S-CUR
COS funcionalizado com ácido 3,3-ditiodipropiônico foi sintetizado por esterificação catalisada por cloreto de ácido por meio de uma reação em duas etapas.
Etapa 1:Ácido 3,3-ditiodipropiônico (42,05 mg, 0,25 mmol) e THF seco (4 mL) foram carregados em um frasco de fundo redondo marrom, com um agitador para dissolver o ácido. Em seguida, cloreto de oxalila (0,3 mmol) diluído com THF foi adicionado a um frasco, colocado em um banho de gelo. A reação foi mantida a 35 ° C. Após agitação durante 3 h, o cloreto de oxalilo que não reagiu foi removido por evaporação rotativa. O produto 1 foi preparado pelas etapas acima. O CUR foi dissolvido em 3 mL de THF, contendo 34 μL de trietilamina, que foi adicionado gota a gota ao frasco contendo o produto 1 em condições de banho de gelo e, em seguida, agitado por 15 min. Subsequentemente, a mistura foi agitada a 50 ° C sob uma atmosfera de azoto durante 6 h. O produto obtido foi submetido a destilação rotativa para remover a trietilamina e o THF e foi então purificado por cromatografia em coluna para adquirir o produto HOOC-S-S-CUR puro.
Etapa 2:O produto puro HOOC-S-S-CUR foi ativado com EDCI (1,2 eq) e DMAP (1,2 eq) em formamida por 2 h. Subsequentemente, COS dissolvido em 4 mL de formamida foi adicionado e agitado a 55 ° C durante 12 h. Após a reação estar completa, a solução foi dialisada com um saco de diálise (MWCO 300 Da) e liofilizada por 12 h.
Síntese de BCSC e Biotina-COS
Resumidamente, biotina, EDCI e DMAP foram dissolvidos em 3 mL de formamida e transferidos para um frasco de fundo redondo marrom. Após agitação durante 2 h a 30 ° C, COS-S-S-CUR foi dissolvido em 3 mL de formamida e adicionado gota a gota ao frasco. A reacção foi mantida a 45 ° C durante 2 dias. Os produtos finais foram dialisados (MWCO 300 Da) em água deionizada e submetidos à centrifugação e liofilização para obtenção de BCSC redox-sensível. Além disso, a síntese de biotina-COS foi conduzida pelo mesmo método para ligar a biotina às cadeias COS.
1 H-NMR de COS-S-S-CUR, BCSC e biotina-COS foram medidos usando uma mistura de DMSO-D 6 e D 2 O como solvente.
Preparação de Micelas de BCSC carregadas com CUR (CUR-BCSCs)
Os CUR-BCSCs foram preparados pelo método de automontagem. Dez miligramas de BCSC foram dissolvidos em 4 mL de formamida e depois misturados com 1 mL de solução CUR (1 mg / mL) que foi dissolvida em formamida. A solução mista foi dialisada em bolsa de diálise (MWCO 300 Da) em água desionizada por 24 he troca da água desionizada a cada 2 h. CUR-BCSCs foram filtrados usando membranas millipore de 800 nm, 450 nm e 220 nm.
Preparação de CUR-BCSC @ PCs
Os CUR-BCSCs preparados foram misturados com uma solução aquosa de PC (1,0 mg / mL) e incubados por 30 min a 4 ° C. Posteriormente, o PC foi removido usando um filtro centrífugo de 100 kDa e lavado com água três vezes. O produto final (CUR-BCSC @ PC) foi armazenado a 4 ° C no escuro para estudo posterior.
Caracterizações
As medições de espalhamento de laser dinâmico (DLS) foram realizadas em um analisador de partículas Delsa Nano C (Beckman Coulter Inc.) para observar o tamanho de partícula, potencial zeta e índice de polidispersidade (PI). A morfologia de CUR-BCSCs e CUR-BCSC @ PCs foi confirmada por medições de microscopia eletrônica de transmissão (TEM, H-600; Hitachi, Tóquio, Japão).
Eficiência de encapsulamento (EE) e capacidade de carga de drogas (DL)
HPLC (Agilent 1260GB12C) foi usado para determinar o EE e DL de nanopartículas. Primeiro, 2 mL de CUR-BCSCs ou CUR-BCSC @ PCs foram misturados com 3 mL de acetonitrila e desmulsificados por ultrassom, em que acetonitrila foi então adicionada a 10 mL. Antes da medição, a temperatura da coluna Phenomenex C18 (250 mm × 4 . 6 mm, 5 um) foi ajustado para 25 ° C, enquanto a taxa de fluxo da fase móvel foi ajustada para 1,0 mL · min - 1 . A proporção de 0,5% de ácido acético glacial para acetonitrila foi de 40:60 (v / v). No processo de detecção, com comprimento de onda de detecção de 425 nm, foram injetados 20 μL de amostras [30]. A seguinte fórmula foi usada para calcular o EE e DL:
$$ \ mathrm {EE} \% =\ left (\ mathrm {Peso} \ \ mathrm {of} \ \ mathrm {Cur} \ \ mathrm {in} \ \ mathrm {the} \ \ mathrm {nanopartículas} / \ mathrm {Peso} \ \ mathrm {of} \ \ mathrm {the} \ \ mathrm {alimentação} \ \ mathrm {Cur} \ right) \ times 100 \% $$$$ \ mathrm {DL} \% =\ left (\ mathrm {Massa} \ \ mathrm {de} \ \ mathrm {Cur} \ \ mathrm {in} \ \ mathrm {o} \ \ mathrm {nanopartículas} / \ mathrm {Massa} \ \ mathrm {de} \ \ mathrm {the} \ \ mathrm {nanopartículas} \ right) \ times 100 \% $$
Teste de estabilidade in vitro
A solução salina tamponada com fosfato (PBS) contendo GSH (0, 20 μM, 10 mM) foi preparada e tratada com CUR-BCSC @ PCs por 4 h para observar as mudanças no tamanho de partícula sob diferentes concentrações de glutationa a 37 ° C. Além disso, o diâmetro hidrodinâmico de CUR-BCSC @ PCs foi investigado em solução de PBS usando um Analisador de Partículas Delsa Nano C (Beckman Coulter Inc.) a 37 ° C em diferentes pontos de tempo (4, 8, 12 e 24 h).
Liberação de CUR in vitro de CUR-BCSC @ PCs
Os comportamentos de liberação de CUR in vitro de CUR-BCSC @ PCs foram investigados usando o método de diálise. Soluções de PBS contendo glutationa (GSH:20 μmol / L, 1 mmol / L, 5 mmol / L, 10 mmol / L) foram preparadas e Tween 80 a 0,5% foi adicionado. Tampão PBS (45 mL), contendo diferentes concentrações de GSH, foi adicionado a tubos de centrífuga de 50 mL; em seguida, um saco de diálise contendo 1 mL de CUR-BCSC @ PCs foi colocado em cada tubo de centrífuga, o qual foi agitado a 37 ° C. Em diferentes pontos de tempo (0,2, 1, 4, 8, 12, 24, 48, 72 h), 2 mL de meio de liberação foram coletados e meio de liberação fresco do mesmo tipo foi adicionado para manter seu volume inalterado. HPLC foi usado para determinar a concentração de CUR no meio de liberação coletado.
Cultura de células
As células A549 de carcinoma de pulmão humano foram cultivadas em DMEM, que incluiu 10% de FBS e 1% de penicilina-estreptomicina, e foram incubadas a 37 ° C em 5% de CO 2 atmosfera [31, 32].
Inibição da proliferação celular in vitro
A citotoxicidade in vitro de CUR, micelas BCSC (BCSCs), CUR-BCSCs e CUR-BCSC @ PCs contra a linha celular A549 foi avaliada usando um ensaio MTT padrão [33]. As células A549 foram semeadas em placas de 96 poços (5000 células por poço) durante 24 horas para aderir à parede. O meio original foi descartado e, em seguida, 100 μL de meio fresco contendo CUR livre, BCSCs, CUR-BCSCs e CUR-BCSC @ PCs (0,1, 1, 5, 10, 15 e 20 μg / mL com base no CUR) foi adicionado e cultivado por 24 h. Poços sem administração foram usados como controles em branco. As células foram submetidas ao ensaio de MTT removendo o meio e adicionando 20 μL de solução de MTT (5 mg / mL). Após incubação por mais 4 h a 37 ° C em 5% de CO 2 atmosfera, a solução de MTT foi substituída por 150 μL de DMSO para dissolver o MTT-formazan roxo. Posteriormente, um leitor de microplaca (Thermo Fisher Scientific Co., Waltham, MA) foi usado para medir a absorbância de cada poço a 570 nm.
Captação e localização de células in vitro
A capacidade de absorção celular de CUR-BCSCs e CUR-BCSC @ PCs foi investigada sob um microscópio de fluorescência (FM, Eclipse E400; Nikon Corporation, Tóquio, Japão). As células A549 foram semeadas em placas de 24 poços em 4 × 10 4 células por poço e foram co-incubadas com CUR-BCSCs e CUR-BCSC @ PCs (concentração de CUR:20 μg / mL) a 37 ° C em uma atmosfera umidificada contendo 5% de CO 2 por 1, 2 e 4 h. As células A549 foram lavadas com PBS três vezes após a remoção do meio de cultura contendo as drogas. Em seguida, PBS contendo 4% de paraformaldeído foi adicionado por 20 min e lavado com PBS por mais três vezes. Os núcleos das células foram corados por Hoechst 33342 por 15 min e observados usando um microscópio de fluorescência invertido.
Análise estatística
Todos os experimentos foram realizados pelo menos três vezes e expressos como média ± DP. Os testes estatísticos foram analisados usando o t de Student teste. P <0,05 foi definido como estatisticamente significativo e P <0,01 foi considerado altamente significativo.
Resultados e discussão
Caracterização de COS, COS-S-S-CUR, Biotina-COS e BCSC
As principais ressonâncias características de CUR e CH 2 -S-S-CH 2 apareceu no 1 Espectro H-NMR de COS-S-S-CUR, comprovando a conjugação bem-sucedida de CUR às cadeias COS. Comparado com os picos de COS na Fig. 3 (A), os sinais característicos de CUR apresentados na Fig. 3 (B) foram observados na região entre 6,7 e 7,5 ppm e em 3,75 ppm (−OCH 3 ), enquanto a ressonância de CH 2 -S-S-CH 2 a 2,5 ppm permaneceu inalterado. Conforme mostrado na (Fig. 3 (C), a, b), os picos de biotina no 1 O espectro de H-NMR da Biotina-COS foi de 0,99 ppm (−CH 2 -) e 3,39 ppm (−CH – S–). 1 O espectro de H-NMR de BCSC é mostrado na Fig. 3 (D). As ressonâncias de CUR (Fig. 3 (D), a, e) foram vistas nas posições correspondentes, e o pico característico de CH 2 -S-S-CH 2 (Fig. 3 (D), b) foi novamente observada a 2,5 ppm. Além disso, o aparecimento de sinais no pico de 0,09 ppm e 3,39 ppm (Fig. 3 (D), c, d) verificou a existência de biotina ligada às cadeias COS-S-S-CUR. As ressonâncias características de CUR, CH 2 -S-S-CH 2 , e biotina como mostrado na Fig. 3 (D) são consistentes com aqueles na Fig. 3 (B) e Fig. 3 (C), indicando que o material anfifílico BCSC foi sintetizado com sucesso.
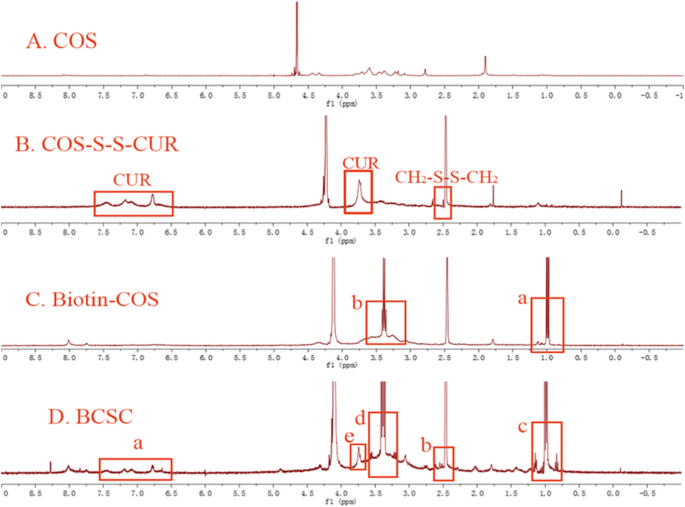
O 1 Espectro de H-NMR de COS ( A ), COS-S-S-CUR ( B ), Biotina-COS ( C ), e BCSC ( D )
Caracterização de CUR-BCSCs e CUR-BCSC @ PCs
As morfologias de CUR-BCSCs e CUR-BCSC @ PCs foram estudadas por microscopia eletrônica de transmissão (TEM) (Fig. 4 (A, B)). Os CUR-BCSCs mostraram uma forma esférica lisa (Fig. 4 (A), a) sob microscopia eletrônica, enquanto os CUR-BCSC @ PCs possuíam uma forma aproximadamente esférica com a camada de florescimento circundando os CUR-BCSC @ PCs (Fig. 4 (B ), b). Isso indicou que o PC formou uma estrutura corona de proteína cobrindo as superfícies dos CUR-BCSCs. Um claro efeito Tyndall de CUR-BCSC @ PCs foi observado devido à existência de nanopartículas generosas (Fig. 4 (C)). O tamanho de partícula, PI, potencial zeta, DL (%) e EE (%) de CUR-BCSCs e CUR-BCSC @ PCs são ilustrados na Tabela 1. Na Fig. 5, o tamanho médio de CUR-BCSCs e CUR- BCSC @ PCs foi 97,8 ± 4,2 nm e 160,3 ± 9,0 nm, respectivamente. Já os valores de IP dos CUR-BCSCs e CUR-BCSC @ PCs foram 0,181 ± 0,014 e 0,114 ± 0,024, respectivamente, menores que 0,2, indicando a uniformidade de seus tamanhos. Os potenciais zeta de CUR-BCSCs e CUR-BCSC @ PCs foram 21,57 ± 0,53 e 12,90 ± 1,93 mV, respectivamente. Devido ao revestimento eletronegativo de PC, o potencial zeta dos CUR-BCSCs era maior do que o dos CUR-BCSC @ PCs. O EE do CUR-BCSC @ PCs foi maior do que o dos CUR-BCSCs.

A As imagens TEM de CUR-BCSCs e um único CUR-BCSC. B As imagens TEM de CUR-BCSC @ PCs e um único CUR-BCSC @ PC. C Efeito Tyndall e a fotografia de CUR-BCSC @ PCs na água
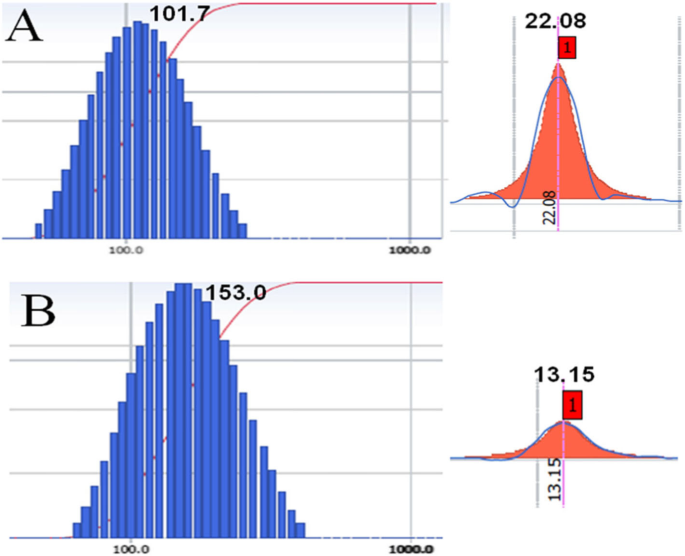
a A distribuição de tamanho e o potencial zeta de CUR-BCSCs; b A distribuição de tamanho e o potencial zeta de CUR-BCSC @ PCs
Estabilidade de CUR-BCSC @ PCs
Como mostrado na Fig. 6a, devido à natureza redutiva da ligação dissulfeto, a ligação foi clivada em PBS contendo GSH 10 mM e CUR-BCSC @ PCs foram desintegrados em fragmentos de polímero, que se aglomeraram para aumentar o tamanho de partícula das nanopartículas . No entanto, em PBS contendo 20 μM de GSH, as mudanças no tamanho das partículas foram menores, o que mostrou um resultado semelhante ao PBS sem GSH. Conforme ilustrado na Fig. 6b, o tamanho de partícula foi medido em momentos diferentes para estudar a estabilidade de CUR-BCSC @ PCs em PBS, e os resultados mostraram que o tamanho de partícula de CUR-BCSC @ PCs aumentou lentamente ao longo do tempo [14].
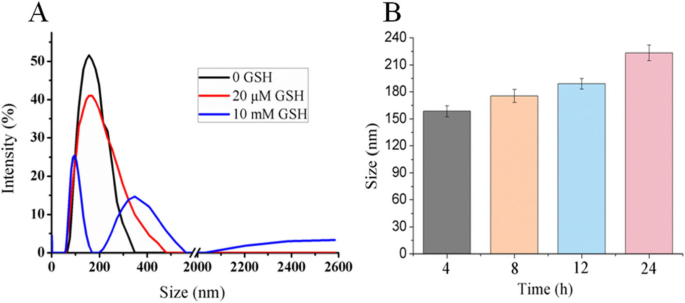
A estabilidade do CUR-BCSC @ PCs. a Mudanças de tamanho de CUR-BCSC @ PCs em diferentes concentrações de GSH. b Mudanças de tamanho de CUR-BCSC @ PCs em PBS em momentos diferentes
Resposta de redução de CUR-BCSC @ PCs
Está bem estabelecido que as ligações dissulfeto são instáveis em um ambiente de redução de tumor. Os pesquisadores usaram ligações dissulfeto para conectar polímeros hidrofílicos e drogas hidrofóbicas para preparar fragmentos anfifílicos, que podem se automontar em água para formar nano-micelas. Então, de acordo com as diferenças no ambiente fisiológico e no ambiente do tumor, as ligações dissulfeto se quebram no local do tumor para liberar drogas [34]. No presente estudo, a liberação do fármaco in vitro foi realizada para verificar se o CUR-BCSC @ PCs poderia apresentar uma propriedade de liberação esperada. A capacidade de resposta de redução de CUR-BCSC @ PCs contendo ligações dissulfeto foi investigada após a ativação de GSH. Conforme mostrado na Fig. 7, a liberação de CUR de CUR-BCSC @ PCs no meio com 20 μM de GSH em pH 7,4, que simulou o ambiente extracelular, foi extremamente lenta em comparação com um ambiente com 10 mM de GSH em pH 7,4. Além disso, em comparação com o meio GSH 20 μM, o GSH 1, 5 e 10 mM mostrou diferenças significativas no comportamento de liberação. Com o aumento da concentração de GSH, também foi promovida a liberação de CUR dos CUR-BCSC @ PCs, indicando que a liberação do fármaco foi em resposta à concentração de GSH.
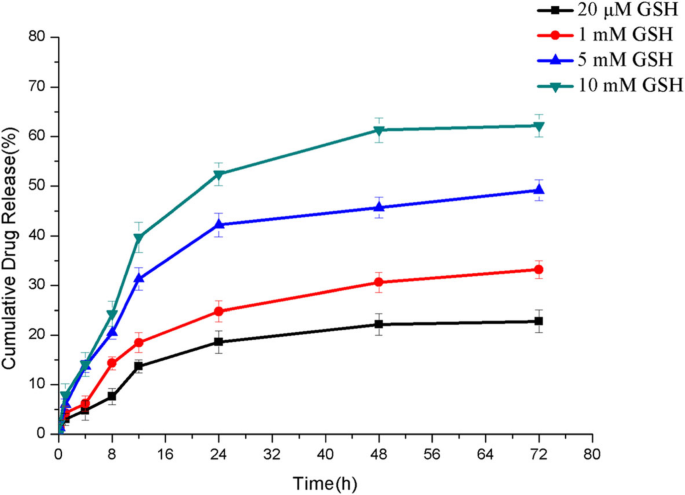
Liberação cumulativa de CUR de CUR-BCSC @ PCs em diferentes condições GSH
Citotoxicidade in vitro
O ensaio de MTT foi conduzido para investigar os efeitos citotóxicos de CUR, BCSCs, CUR-BCSCs e CUR-BCSC @ PCs livres em linhas celulares A549 [35]. Os dados de viabilidade celular estão resumidos na Fig. 8. Todas as preparações de CUR mostraram dependência da dose em termos de inibição da proliferação celular. Como mostrado na Fig. 8, CUR livre teve ligeiramente menos capacidade para inibir a proliferação celular contra todas as células A549 em comparação com CUR-BCSC @ PCs e CUR-BCSCs, após incubação por 24 h. Para células A549, a atividade anticancerígena de CUR-BCSC @ PCs foi melhor do que a de BCSCs e CUR-BCSCs, o que foi provavelmente devido à excelente absorção celular. Além disso, CUR-BCSC @ PCs mostraram uma propriedade de citotoxicidade mais elevada do que CUR-BCSCs, indicando que PC tem um potencial efeito inibidor na proliferação de células A549.
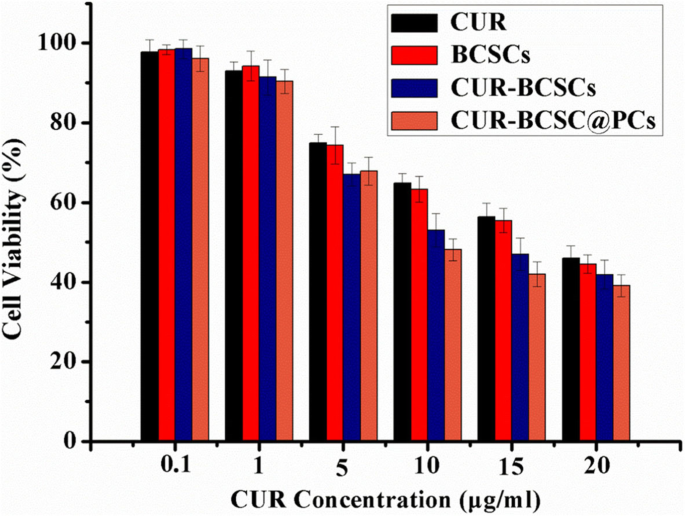
Citotoxicidade in vitro de diferentes formulações em 24 h em células A549
Estudo de captação celular in vitro
Conforme mostrado na Fig. 8, os sinais de fluorescência de CUR foram observados em células A549 tratadas com CUR-BCSCs e CUR-BCSC @ PCs (CUR:20 μg / mL) em 1, 2 e 4 h, usando o microscópio de fluorescência invertido . CUR, como uma sonda de fluorescência verde, também era uma droga anticâncer, que era freqüentemente usada como um modelo hidrofóbico para desenvolver novos e eficientes sistemas de distribuição de drogas. Tal como ilustrado na Fig. 9a, tanto CUR-BCSCs como CUR-BCSC @ PCs foram absorvidos em linhas celulares A549 e a eficiência de captação era dependente do tempo. Devido aos receptores de biotina superexpressos na superfície das células cancerosas, as nanomicelas carregadas de biotina tinham uma afinidade para as células A549. Os sinais de fluorescência de CUR-BCSC @ PCs eram elevados às 4 horas, indicando uma elevada taxa de absorção celular de CUR-BCSC @ PCs. Os sinais de fluorescência dos CUR-BCSC @ PCs foram mais elevados às 4 h do que às 1 h ou 2 h; isso provou que a captação celular era dependente do tempo.
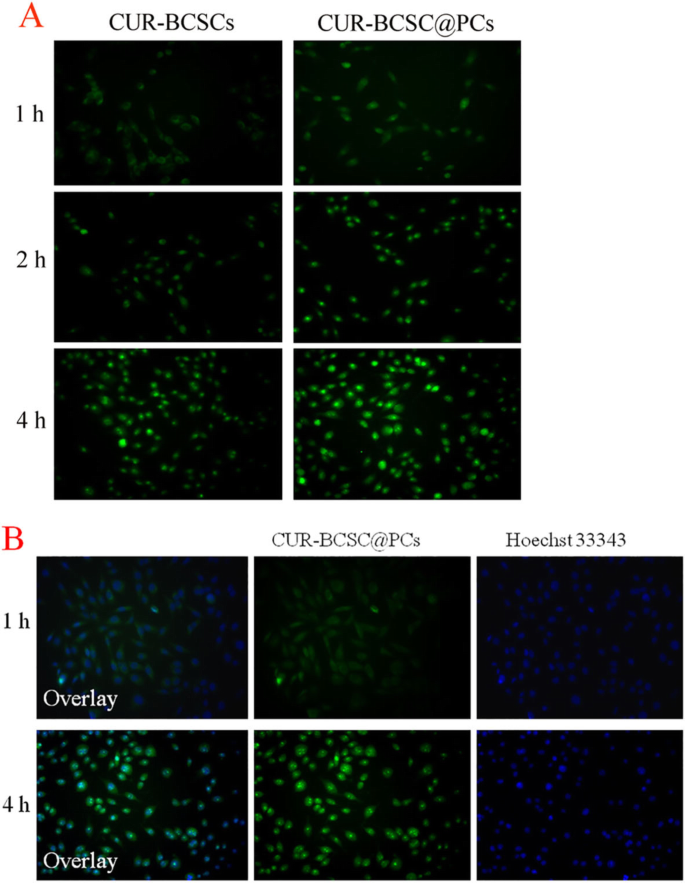
a Imagem fluorescente da captação celular de CUR-BCSCs e CUR-BCSC @ PCs em momentos diferentes. b A localização da célula de CUR-BCSC @ PCs em 1 he 4 h
Os núcleos das células A549 foram corados por Hoechst 33342. Como mostrado na Fig. 9b, sinais de fluorescência verde foram vistos no citoplasma do grupo de 1 h de CUR-BCSC @ PCs, e a fluorescência ocorreu gradualmente nos núcleos de 4 h grupo de CUR-BCSC @ PCs, que demonstrou captação celular por endocitose mediada por caveolae.
Conclusões
Neste estudo, um tipo de nanopartícula de COS funcionalizada com proteína foi preparada por meio de reações de condensação, comportamento de automontagem e a interação entre PC e CUR-BCSCs. Após a investigação preliminar, os materiais carreadores anfifílicos (BCSCs) com sensibilidade redox foram sintetizados com sucesso e verificados usando 1 H-NMR. As superfícies dos CUR-BCSCs foram modificadas com uma camada de corona de ficocianina, o que poderia melhorar a eficiência de captação celular e proteger os CUR-BCSC @ PCs da adsorção de proteínas plasmáticas. A citotoxicidade celular e a análise de absorção indicaram que CUR-BCSC @ PCs podem transportar CUR para as células A549 e tem uma excelente propriedade antiproliferativa. Considerando o efeito PDT do PC e CUR, avaliaremos as propriedades fotodinâmicas e a atividade anticâncer do CUR-BCSC @ PCs sob fototerapia na próxima fase desta pesquisa. Este estudo abriu o caminho para a melhoria da eficácia do medicamento anticâncer e a introdução de uma proteína corona funcional. Em resumo, o biomaterial carreador de nanomedicina do CUR-BCSC @ PCs baseado em COS com múltiplas funções forneceu uma nova estratégia para o tratamento de tumores e exibiu grandes perspectivas de aplicação.
Disponibilidade de dados e materiais
As conclusões feitas neste manuscrito são baseadas nos dados que são apresentados e mostrados neste artigo.
Abreviações
- BCSC:
-
Biotina-quitosana oligossacarídeo-ácido ditiodipropiônico-curcumina
- COS:
-
Oligossacarídeo de quitosana
- COS-S-S-CUR:
-
Oligossacarídeo de quitosana-ácido ditiodipropiônico-curcumina
- CUR:
-
Curcumina
- CUR-BCSC @ PCs:
-
Funcionalizadas com ficocianina e carregadas com curcumina, oligossacarídeo-quitosana-oligossacarídeo-ácido ditiodipropiônico-micelas de curcumina
- CUR-BCSCs:
-
Micelas de curcumina carregadas com curcumina-oligossacarídeo-ácido ditiodipropiônico
- EPR:
-
Permeabilidade e retenção aprimoradas
- PC:
-
Ficocianina
- PDT:
-
Terapia fotodinâmica
Nanomateriais
- Nanofibras e filamentos para entrega aprimorada de drogas
- Nanopartículas de FePO4 biocompatíveis:entrega de drogas, estabilização de RNA e atividade funcional
- Síntese biogênica, caracterização e avaliação do potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
- Nanopartículas lipídicas de PLGA rastreadas com 131I como transportadores de administração de drogas para o tratamento quimioterápico direcionado do melanoma
- Síntese fácil de compósito CuSCN colorido e condutor revestido com nanopartículas de CuS
- Nanopartículas de sílica para entrega de proteína intracelular:uma nova abordagem de síntese usando proteína fluorescente verde
- Síntese e desempenho in vitro de nanopartículas de ferro-platina revestidas com polipirrole para terapia fototérmica e imagem fotoacústica
- Fabricação, caracterização e citotoxicidade de nanopartículas de carbonato de cálcio derivadas de casca de ouro conjugada em forma esférica para aplicações biomédicas
- Novela dupla mitocondrial e nanopartículas de direcionamento do receptor CD44 para liberação desencadeada por estímulos redox
- Platycodon saponins from Platycodi Radix (Platycodon grandiflorum) para a síntese verde de nanopartículas de ouro e prata



