Um Novo Mecanismo Subjacente à Formação de Raiz Lateral de Tomate Disparada por Nanotubo de Carbono Multifurdado:o Envolvimento do Óxido Nítrico
Resumo
Estudos abundantes revelaram que os nanotubos de carbono de paredes múltiplas (MWCNTs) são tóxicos para as plantas. No entanto, se ou como os MWCNTs influenciam a formação da raiz lateral (LR), que é um componente importante da adaptabilidade do sistema radicular a vários sinais ambientais, permanece controverso. Neste relatório, descobrimos que MWCNTs podem entrar nas raízes de mudas de tomate. A administração com MWCNTs promoveu a formação de LR do tomate de uma forma aproximadamente dependente da dose. A produção de óxido nítrico (NO) endógeno foi desencadeada por MWCNTs, confirmada pelo método de reagente de Greiss, ressonância paramagnética eletrônica (EPR) e microscopia confocal de varredura a laser (LSCM), juntamente com o eliminador de NO. Existe uma relação de causa-efeito entre MWCNTs e NO na indução do desenvolvimento de LR, uma vez que a síntese de NO desencadeada por MWCNT e a formação de LR foram obviamente bloqueadas pela remoção de NO endógeno com seu eliminador. A atividade da enzima nitrato redutase (NR) geradora de NO foi aumentada em resposta aos MWCNTs. A inibição de NR por tungstato não apenas prejudicou a produção de NO, mas também aboliu a formação de LR desencadeada por MWCNTs. A adição de N G O éster metílico de -nitro-l-arginina (l-NAME), um inibidor da enzima semelhante à óxido nítrico sintase (NOS) de mamíferos, não influenciou a formação de LR. Coletivamente, propusemos que o NO pode atuar como uma molécula de sinalização a jusante no controle MWCNT do desenvolvimento de LR, pelo menos parcialmente via NR.
Introdução
Existem muitas aplicações biológicas e biomédicas de nanotubos de carbono [1, 2]. Devido à capacidade única de penetrar facilmente nas membranas celulares, a biossegurança dos nanotubos de carbono é sempre um tópico de debate [3, 4]. Enquanto isso, como a produção e o uso de nanotubos de carbono crescem rapidamente, torna-se importante caracterizar detalhadamente os mecanismos de sua citotoxicidade em seres humanos e mamíferos, e recentemente em plantas [3,4,5,6,7,8,9]. É bem sabido que as plantas e suas comunidades são muito importantes para os humanos e o meio ambiente, e também estão sob risco de exposição aos nanotubos de carbono, devido ao acúmulo nos solos por meio da aplicação de fertilizantes biossólidos [6, 10, 11]. Como membros importantes dos nanotubos de carbono, a toxicidade dos nanotubos de carbono de paredes múltiplas (MWCNTs), consistindo em múltiplas camadas laminadas de grafeno, tem sido amplamente investigada. Estudos em mamíferos revelaram que a exposição tanto com MWCNTs quanto com nanotubo de carbono de parede única induziu dano oxidativo e ativação de NF-κB em queratinócitos humanos e células A549 [9, 12]. MWCNTs e nanotubos de carbono de parede simples podem se fundir com a membrana plasmática, causando danos às células através da peroxidação lipídica e estresse oxidativo [9, 11, 13, 14]. Citotoxicidade e estresse oxidativo desencadeados por MWCNTs, bem como respostas inflamatórias modestas, foram observados em células endoteliais da veia umbilical humana [15]. Estudo anterior sugeriu que a toxicidade primária de MWCNTs no espinafre vermelho era principalmente derivada da superprodução de espécies reativas de oxigênio (ROS), e os efeitos tóxicos poderiam ser revertidos pelo ácido ascórbico suplementado [7]. Nesse sentido, os MWCNTs são considerados um novo fator estressante para os organismos, tanto em animais quanto em plantas.
A formação da raiz lateral (LR), um importante determinante da arquitetura da raiz, tem sido considerada como um indicador de resposta adaptativa a várias tensões [16]. Em plantas superiores, a formação de LR é influenciada por fitormônios e uma ampla gama de sinais ambientais, incluindo disponibilidade de água, nutrientes e estresse abiótico, como hipóxia e estresse por metais pesados [17,18,19]. Enquanto isso, ampla evidência confirmou que a formação de RL não atua apenas como um suporte físico, mas também contribui para a absorção de água e nutrientes para o crescimento e desenvolvimento das plantas [19,20,21]. Diferentes pistas ambientais podem desencadear vários fenótipos específicos de resposta morfogênica induzida por estresse (SIMR), incluindo a promoção da formação de LR e uma inibição do alongamento da raiz [17]. A regulação da formação de LR também é rigidamente controlada por fitormônios, como auxina, e a ativação de genes reguladores do ciclo celular em resposta à auxina foi sugerida [19, 22]. Enquanto isso, o envolvimento de algumas moléculas pequenas na organogênese da raiz desencadeada por auxina foi confirmado em pepino, tomate, soja e plantas de colza [23,24,25,26,27]. Essas pequenas moléculas incluem peróxido de hidrogênio (H 2 O 2 ), óxido nítrico (NO), monóxido de carbono (CO) e gás hidrogênio (H 2 )
Entre estes, o NO, um gás radical livre, demonstrou ter múltiplas funções fisiológicas nas plantas [28, 29]. Além do aumento da adaptação da planta contra estresses, as funções do NO incluem a promoção do desenvolvimento do cabelo da raiz, enraizamento adventício e formação lateral da raiz [30,31,32,33], embora o (s) recurso (s) enzimático (s) da biossíntese de NO nesses processos supracitados permanece indescritível. Em animais, a síntese de NO a partir de l-arginina é catalisada pela enzima óxido nítrico sintase contendo heme (NOS) [34]. Embora o (s) gene (s) que codificam as enzimas NOS não tenham sido identificados em plantas, a atividade semelhante a NOS em mamíferos é amplamente detectada [35, 36], e os inibidores de NOS em mamíferos, tais como N G cloridrato de éster metílico de -nitro-l-arginina (l-NAME), pode inibir a geração de NO em plantas [25, 33, 36,37,38,39]. É importante ressaltar que ampla evidência genética revelou que o NO pode ser produzido pela nitrato redutase (NR), uma enzima bem conhecida responsável pelo metabolismo do nitrogênio nas plantas [28]. O envolvimento da produção de NO mediada por NR no fechamento estomático e aclimatação ao frio foi demonstrado geneticamente [37, 38]. Nosso estudo anterior mostrou que a síntese de NO dependente de NR está envolvida na formação da raiz lateral mediada por gás hidrogênio induzida por auxina [39].
Até agora, diferentes respostas na formação, promoção ou inibição de LR foram relatadas respectivamente em várias espécies de plantas quando suplementadas com nanomateriais, incluindo MWCNTs [40,41,42,43], nanopartículas de ouro (Au NP, [44]), óxido de zinco nanopartículas (ZnO NP [45, 46];), nanopartículas de dióxido de titânio (TiO 2 NP [46];) e óxido de grafeno (GO [47,48,49];) (Tabela 1), e nenhum estudo ainda forneceu prova definitiva de um papel do NO nas respostas acima. Neste estudo, a detecção de NO endógeno pelo método de reagente de Greiss, microscopia confocal de varredura a laser (LSCM) e análises de ressonância paramagnética eletrônica (EPR) revelaram que o nível de NO foi aumentado em mudas de tomate tratadas com MWCNT. Posteriormente, foi observada a formação de LR. Nós ainda estudamos o envolvimento de NO na formação de LR desencadeada por MWCNTs, pela manipulação dos níveis de NO endógeno usando NO scavenger e antagonistas que inibem NR e atividade de NOS semelhante a mamíferos. Experimentos adicionais revelaram que o NO dependente de NR pode ser, pelo menos parcialmente, essencial para a formação de LR em resposta a MWCNTs. Este trabalho abre assim uma nova janela para a compreensão dos efeitos biológicos dos nanomateriais nas plantas.
Materiais e métodos
Químicos
Salvo indicação em contrário, todos os outros produtos químicos foram obtidos na Sigma-Aldrich (St Louis, MO, EUA). MWCNTs, adquiridos da Sigma-Aldrich, foram caracterizados como descrito anteriormente [50]. O diâmetro externo, diâmetro interno e o comprimento dos MWCNTs foram de 6–12 nm, 2,5–5 nm e 1–9 μm, respectivamente. Após o tratamento com sonicação, a suspensão coloidal homogeneizada obtida foi esterilizada e utilizada.
Outras nanopartículas de carbono foram obtidas da Nanjing XFNANO Materials Tech Co., Ltd., incluindo nanotubos de carbono de parede única (SWCNTs, XFS22; pureza> 95%, diâmetro de 1–2 nm, comprimento de 5–30 μm, área de superfície especial> 1075 m 2 / g), grafeno (XF001W; pureza ~ 99%, diâmetro 0,5–5 μm, espessura ~ 0,8 nm, proporção de camada única ~ 80%, área de superfície BET 500 ~ 1000 m 2 / g; resistividade elétrica ≦ 0,30 Ω.cm) e carbono ativo (AC, XFP06; pureza> 95%, tamanho de partícula 5 ± 1 μm, volume de poro 1–1,2 cm 3 / g, abertura 2,0–2,2 nm, área de superfície especial ~ 1500–1700 m 2 / g).
Além disso, nitroprussiato de sódio (SNP) foi usado como um composto de liberação de NO [30,31,32,33]. O sal de potássio de 2- (4-carboxifenil) -4,4,5,5-tetrametilimidazolina-1-oxil-3-óxido (cPTIO) foi considerado um eliminador de NO [51,52,53,54]. Tungstate (Tg; um inibidor de NR [28, 33, 37, 55,56,57];) e N G cloridrato de éster metílico de -nitro-L-arginina (NAME; um inibidor da enzima semelhante a NOS de mamífero [25, 33, 36,37,38,39];) também foram aplicados. Neste estudo, as concentrações dos produtos químicos acima foram determinadas nos experimentos piloto, a partir dos quais as respostas significativas foram observadas.
Material vegetal e condições de crescimento e determinação da formação LR
Tomate ( Solanum lycopersicum L.) as sementes “Jiangshu 14” foram gentilmente fornecidas pelos Institutos Agrícolas de Jiangsu, Nanjing, Província de Jiangsu, China. Sementes selecionadas de tamanho idêntico foram germinadas em água destilada a 25 ± 1 ° C no escuro por 3 dias. As mudas idênticas selecionadas com radículas de 2–3 mm foram então transferidas para soluções de tratamento de 6 mL contendo as concentrações indicadas de MWCNTs, ácido 1-naftilacético 200 nM (NAA; uma auxina bem conhecida), SNP 0,1 mM, cPTIO 0,2 mM, 20 μM de tungstato (Tg), 0,2 mM de NOME e outras nanopartículas de carbono, incluindo 5 mg / mL de nanotubos de carbono de parede única (SWCNTs), grafeno e carbono ativo (AC), sozinho ou em combinação para os pontos de tempo indicados. As mudas foram cultivadas em uma incubadora iluminada (25 ± 1 ° C) com uma intensidade de luz de 200 μmol m −2 s −1 em 14/10 h (claro / escuro) fotoperíodo.
Após os tratamentos, as fotos foram tiradas e o número e o comprimento da raiz lateral emergida (> 1 mm) por muda foram determinados usando o software Image J (http://rsb.info.nih.gov/ij/) [39 , 58]. Conforme descrito anteriormente, apenas os segmentos induzíveis pela raiz lateral foram usados para a análise subsequente.
Imagem da distribuição MWCNT por microscopia eletrônica de transmissão
A distribuição de MWCNTs na raiz de mudas de tomate foi caracterizada por microscopia eletrônica de transmissão (TEM; JEOL, JEM-200CX, Tóquio, Japão). A preparação da amostra para análise TEM foi de acordo com o protocolo anterior [59].
Imagem de NO endógeno por microscópio confocal de varredura a laser
A imagem de NO foi realizada usando uma sonda fluorescente de NO razoavelmente específica 4-amino-5-metilamino-2 ', 7'-difluorofluoresceína diacetato (DAF-FM DA). Depois que a sonda foi completamente lavada, as imagens foram obtidas usando o microscópio confocal Zeiss LSM 710 (Carl Zeiss, Oberkochen, Alemanha, excitação em 488 nm, emissão em 500-530 nm para análise de NO). Em nosso experimento, 20 amostras individuais foram selecionadas aleatoriamente e medidas por tratamento. As fotografias são representativas de resultados idênticos.
Nenhum conteúdo determinado pelo ensaio de reagente Griess
De acordo com os métodos descritos anteriormente [50], o teor de NO foi determinado com o ensaio de reagente de Griess. É importante ressaltar que, para escapar da interferência causada pelos conteúdos de nitrato e nitrito concentrados nas plantas, as amostras idênticas pré-incubadas em 200 μM cPTIO (o eliminador de NO) por 30 min foram consideradas como amostras em branco. Após a adição do reagente de Griess por 30 min, a absorbância foi registrada a 540 nm, e o conteúdo de NO foi determinado por comparação com uma curva padrão de NaNO 2 .
Determinação de NO com Ressonância Paramagnética Eletrônica (EPR)
De acordo com nossos métodos anteriores [39, 55, 60], a determinação do nível de NO usando ressonância paramagnética eletrônica (RPE) foi realizada. A camada de solvente orgânico foi utilizada para determinar o NO num espectrómetro Bruker A300 (Bruker Instrument, Karlsruhe, Germany) nas seguintes condições:temperatura ambiente; frequência de microondas, 9,85 GHz; potência de microondas, 63,49 mW; e frequência de modulação, 100,00 kHz.
Determinação da atividade da nitrato redutase (NR)
A atividade NR foi detectada espectrofotometricamente em 540 nm de acordo com o método anterior [57]. O nitrito produzido foi determinado espectrofotometricamente a 540 nm pela adição de 1 mL de 1% (p / v) sulfenilamida em HCl 3 M junto com 1 mL de 0,02% (v / v) n- (1-naftil) -etilenodiamina.
Análise estatística
Onde indicado, os resultados foram expressos como os valores médios ± SE de três experiências independentes com três réplicas biológicas para cada. A análise estatística foi realizada com o software SPSS Statistics 17.0. Para análise estatística, teste múltiplo de Duncan ( p <0,05) foi escolhido como apropriado.
Resultados
MWCNTs não apenas entram nas células raiz, mas também promovem a formação de LR
A formação de LR é um dos principais determinantes da arquitetura de sistemas de raiz. Para investigar o efeito dos MWCNTs na formação de LR, mudas de tomate com 3 dias de idade foram incubadas com uma gama de concentrações de MWCNTs (0,05, 0,5, 5 e 50 mg / mL) por 3 dias. A aplicação de ácido 1-naftilacético (ANA) foi considerada um controle positivo. Em nosso experimento, o número e o comprimento do LR foram determinados como dois parâmetros de formação do LR. Como mostrado na Fig. 1, em comparação com as amostras de controle, MWCNTs exógenos induziram significativamente a formação de LR de uma maneira aproximadamente dependente da dose, com um efeito máximo em 5 e 50 mg / mL. Resposta induzível semelhante foi observada quando 200 nM NAA foi administrado. Considerando o custo de MWCNTs e a resposta induzível na formação de LR, 5 mg / mL de MWCNTs foram aplicados nos experimentos a seguir.
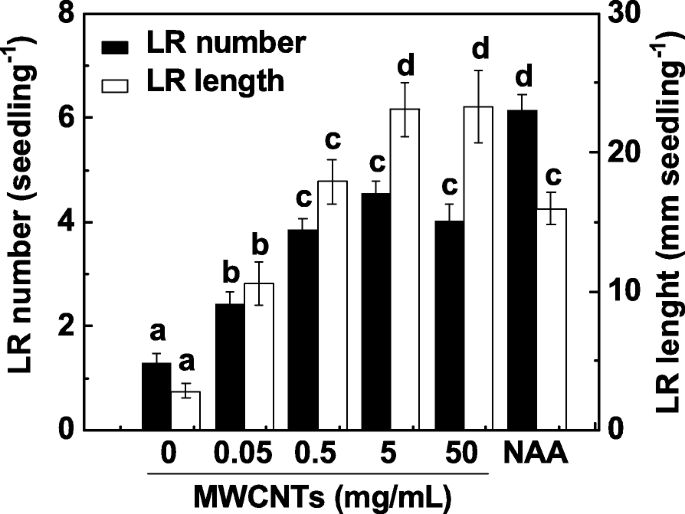
A formação de LR de tomate induzida por MWCNT foi de uma maneira aproximadamente dependente da dose. Mudas de tomate com três dias de idade foram tratadas com 200 nM NAA e as concentrações indicadas de MWCNTs, respectivamente. O número e o comprimento da raiz lateral emergida (> 1 mm) por muda foram então determinados após 3 dias de tratamento. Havia 30 (10 × 3) plantas em três repetições biológicas e os experimentos foram conduzidos por 3 vezes. Os dados são as médias ± SE. Dentro de cada conjunto de experimentos, as barras denotadas pela mesma letra não diferiram significativamente em p Nível <0,05 de acordo com o teste múltiplo de Duncan
Para validar a função específica de MWCNTs na indução da formação de LR, investigamos ainda se as outras alotropias de MWCNTs também têm tais efeitos indutíveis. Conforme mostrado na Fig. 2a, todos esses nanomateriais de carbono exibiram efeitos tóxicos no crescimento de rebentos (dados não mostrados). Curiosamente, a aplicação de MWCNTs, nanotubos de carbono de parede única (SWCNTs), grafeno e carbono ativo com concentração idêntica (5 mg / mL) pode resultar diferencialmente no aumento do número e comprimento LR, em comparação com as plantas de controle livres de produtos químicos (Fig. 2b). Entre esses produtos químicos, a resposta induzível máxima foi descoberta em mudas de tomate incubadas com MWCNT.
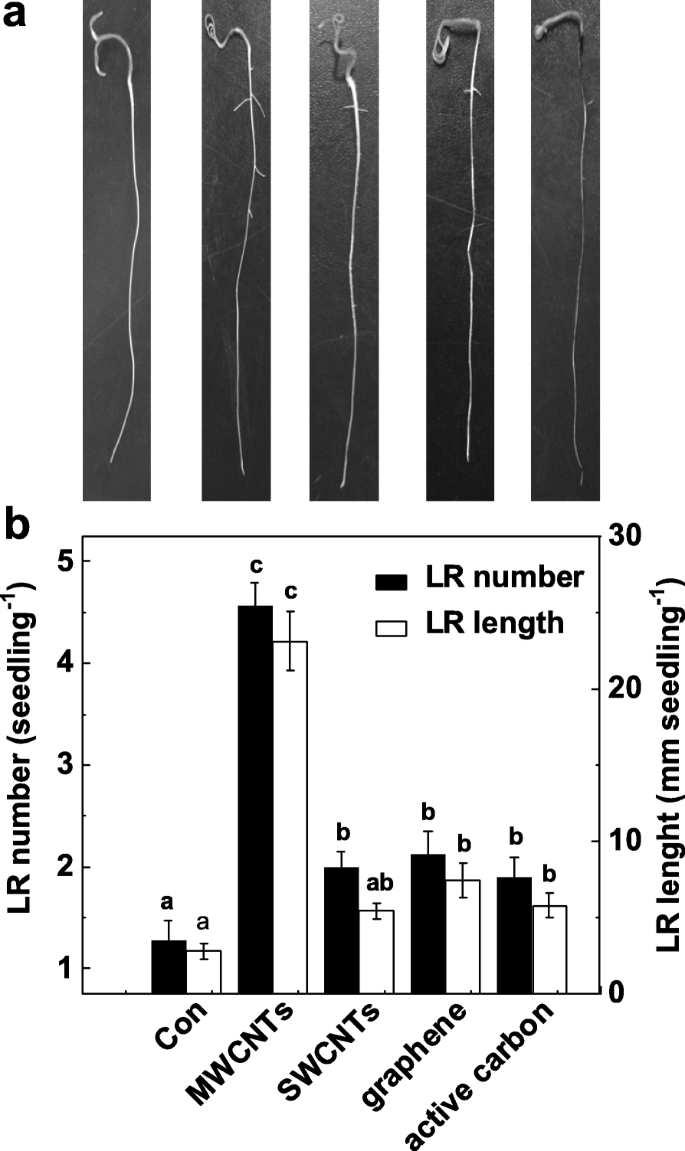
Mudanças na formação da raiz lateral em resposta a diferentes nanopartículas de carbono. Mudas de tomate com três dias de idade foram tratadas com água destilada (Con), 5 mg / mL MWCNT, nanotubos de carbono de parede simples (SWCNTs), grafeno e carbono ativo (AC), respectivamente, por mais 3 dias. a Fotos representativas foram então tiradas. b O número e o comprimento da raiz lateral emergida (> 1 mm) por muda também foram determinados. Barra de escala =50 mm. Havia 30 (10 × 3) plantas em três repetições biológicas e os experimentos foram conduzidos por 3 vezes. Os dados são as médias ± SE. Dentro de cada conjunto de experimentos, as barras denotadas pela mesma letra não diferiram significativamente em p Nível <0,05 de acordo com o teste múltiplo de Duncan
Com o auxílio da microscopia eletrônica de transmissão (TEM), a distribuição de MWCNTs pode ser avaliada facilmente. Os resultados mostrados na Fig. 3 revelaram que MWCNTs, quando aplicados exogenamente, podem ser absorvidos por mudas de tomate, e a distribuição de MWCNTs foi encontrada nas células da raiz. Esse resultado pode ser entendido, uma vez que as raízes das mudas são cultivadas diretamente em solução líquida contendo MWCNTs.
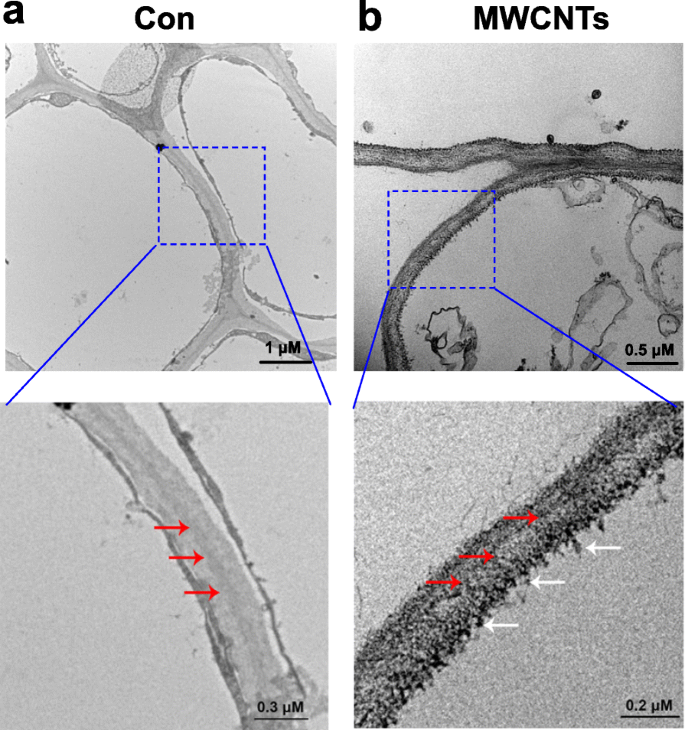
Distribuição de MWCNTs em raízes de tomate. Imagens TEM de mudas de tomate com 3 dias de idade tratadas com água destilada (Con; a ) ou 5 mg / mL MWCNTs ( b ) durante 1 dia. A seta vermelha indica parede celular, enquanto a seta branca indica MWCNTs
Síntese de NO induzida por MWCNT e posteriormente a formação de LR eram sensíveis a cPTIO, um eliminador de NO
Para investigar se o NO também está envolvido na formação de LR induzida por MWCNT, a função de NO na formação de LR induzida por MWCNTs foi avaliada pela manipulação dos níveis de NO endógeno usando composto de liberação de NO e o eliminador. Semelhante aos resultados anteriores [31], a administração de nitroprussiato de sódio (SNP) poderia resultar na indução da formação de LR, e uma resposta aditiva foi observada quando SNP e MWCNTs foram aplicados juntos (Fig. 4). Quando o sal de potássio de 2- (4-carboxifenil) -4,4,5,5-tetrametilimidazolina-1-oxil-3-óxido (cPTIO; um eliminador de NO) foi adicionado, as respostas de promoção na formação de LR causadas por MWCNTs foram significativamente prejudicada. Sozinho, o cPTIO poderia inibir o desenvolvimento do LR, em comparação ao controle livre de produtos químicos, indicando o importante papel do NO endógeno na organogênese da raiz.
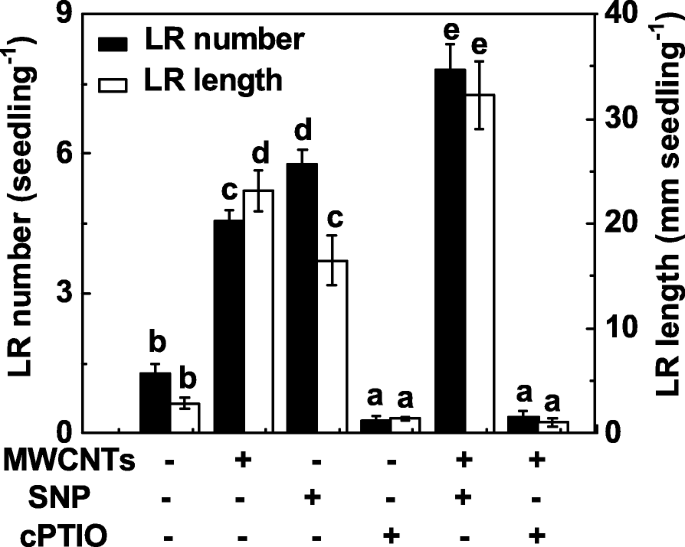
A formação de LR induzida por MWCNT foi sensível à remoção de NO endógeno com cPTIO, seu eliminador. Mudas de tomate com três dias de idade foram tratadas com água destilada, 5 mg / mL MWCNT, SNP 0,1 mM, cPTIO 0,2 mM, sozinha ou em combinação por 3 dias. Posteriormente, foram determinados o número e o comprimento da raiz lateral emergida (> 1 mm) por muda. Havia 30 (10 × 3) plantas em três repetições biológicas e os experimentos foram conduzidos por 3 vezes. Os dados são as médias ± SE. Dentro de cada conjunto de experimentos, as barras denotadas pela mesma letra não diferiram significativamente em p Nível <0,05 de acordo com o teste múltiplo de Duncan
A fim de avaliar ainda mais o importante papel do NO endógeno na resposta de MWCNT, um curso de tempo de produção de NO in vivo foi detectado pela primeira vez com o método de reagente de Greiss. Durante a determinação acima, o filtrado idêntico pré-tratado com cPTIO foi considerado um branco para os resultados precisos. Foi observado que a produção de NO nas raízes das mudas de tomate aumentou dramaticamente até 24 h após o tratamento com MWCNT e, em seguida, voltou aos níveis iniciais (48 h; Fig. 5a). Acima do nível máximo de NO endógeno desencadeado por MWCNTs por 24 h foi obviamente abolido por cPTIO, um eliminador de NO, sugerindo o papel específico do NO.
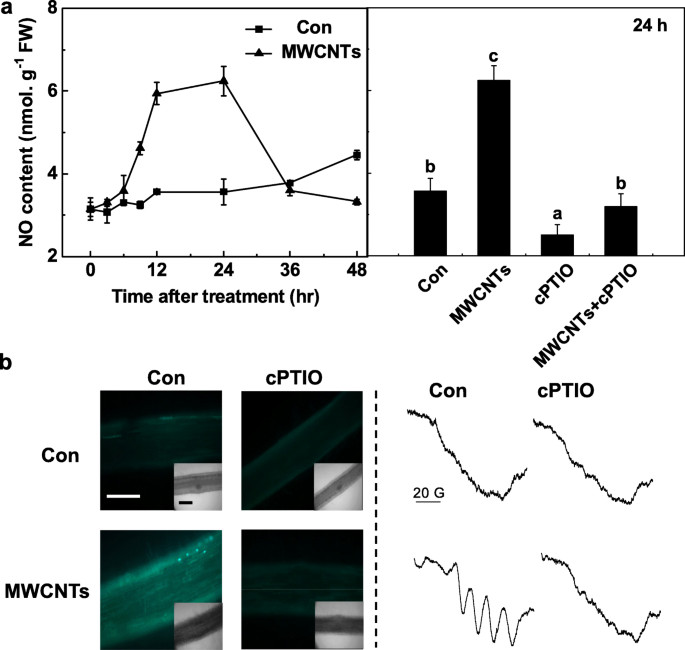
A produção de NO induzida por MWCNT foi bloqueada por cPTIO, o eliminador de NO. Mudas de tomate com três dias de idade foram tratadas com água destilada e 5 mg / mL MWCNTs com ou sem 0,2 mM de cPTIO, respectivamente. a Mudanças na atividade de NR (esquerda) e produção de NO (direita) determinadas usando o método de reagente Greiss. b Após 24 h, o sinal de NO foi analisado por LSCM (esquerda) e EPR (direita). Barra de escala =0,1 mm. Os dados são as médias ± SE. Barras denotadas pela mesma letra não diferiram significativamente em p Nível <0,05 de acordo com o teste múltiplo de Ducan
Para confirmar os resultados acima, ambos LSCM e ESR foram adotados. Em primeiro lugar, as mudanças nos níveis de NO endógeno nas raízes de mudas de tomate foram monitoradas por meio da marcação de NO usando a sonda fluorescente DAF-FM DA, bastante permeável às células e bastante específica para NO, e imagem com LSCM. Semelhante aos resultados anteriores (Fig. 5a), na presença de cPTIO, o aumento da intensidade de fluorescência dependente de DAF-FM desencadeada por MWCNTs foi amplamente abolida (Fig. 5b). Esses resultados implicaram que a fluorescência desencadeada por DAF-FM está relacionada aos níveis de NO endógeno em raízes de plântulas de tomate.
A produção de NO induzida por MWCNT foi confirmada por espectroscopia EPR. Como esperado, raízes de mudas tratadas por 24 h com MWCNTs apresentaram o tripleto de estrutura hiperfina típico do complexo NO. No entanto, a adição de cPTIO aboliu o sinal acima, indicando que a exposição a MWCNT resultou em uma forte produção de NO (Fig. 5b). Coletivamente, esses dados sugeriram que a síntese de NO pode ser necessária para a formação de LR desencadeada por MWCNT em mudas de tomate.
NR pode ser responsável pela produção de NO induzida por MWCNT e, posteriormente, pela formação de LR
Uma vez que NR e NOS de mamífero são duas enzimas principais relacionadas à síntese de NO em plantas, tanto o tungstato (um inibidor de NR) quanto o NAME (um inibidor de NOS de mamífero) foram aplicados no experimento subsequente. Aqui, o tratamento com tungstato suprimiu substancialmente a promoção da formação de LR em raízes de mudas de tomate tratadas com MWCNT (Fig. 6). Comparativamente, a indução da formação de LR desencadeada por MWCNTs não foi fortemente inibida pela adição de NAME, indicando que NOS semelhante a mamífero pode não ser a enzima sintética de NO alvo responsável pela produção de NO induzida por MWCNTs. Também foi observado que uma ligeira, mas não significativa diminuição na formação de LR foi observada em mudas de tomate quando tungstato ou NAME foram aplicados separadamente.
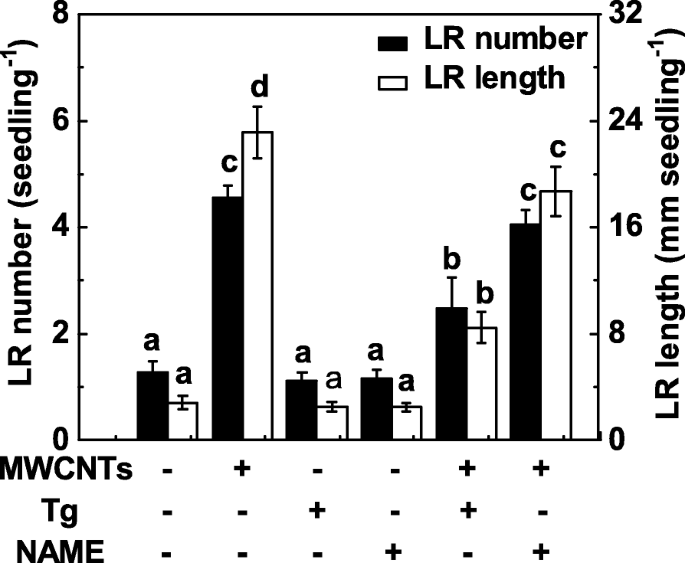
Mudanças na formação de LR em resposta a MWCNTs e dois inibidores da síntese de NO. Mudas de tomate com três dias de idade foram tratadas com 5 mg / mL de MWCNT, 20 μM de tungstato (Tg), 0,2 mM de NOME, sozinho ou em combinação por 3 dias. Posteriormente, foram determinados o número e o comprimento da raiz lateral emergida (> 1 mm) por muda. Havia 30 (10 × 3) plantas em três repetições biológicas e os experimentos foram conduzidos por 3 vezes. Os dados são as médias ± SE. Dentro de cada conjunto de experimentos, as barras denotadas pela mesma letra não diferiram significativamente em p Nível <0,05 de acordo com o teste múltiplo de Duncan
O papel do NR na formação de LR desencadeado por MWCNT foi ainda examinado pelo monitoramento da produção de NO em resposta a MWCNTs aplicados com ou sem tungstato. Em comparação com as mudanças na produção de NO endógeno (Fig. 5a), a análise do curso do tempo na atividade de NR mostrou a tendência semelhante (Fig. 7a), também com pico 24 h após o tratamento com MWCNTs. Estes resultados sugeriram que o aumento induzido por MWCNT na produção de NO pode resultar principalmente da atividade aumentada de NR. Consistentemente, a inibição da produção de NO dependente de NR por tungstato foi confirmada usando o método de reagente Greiss (Fig. 7b), LSCM e EPR (Arquivo adicional 1:Figura S1).
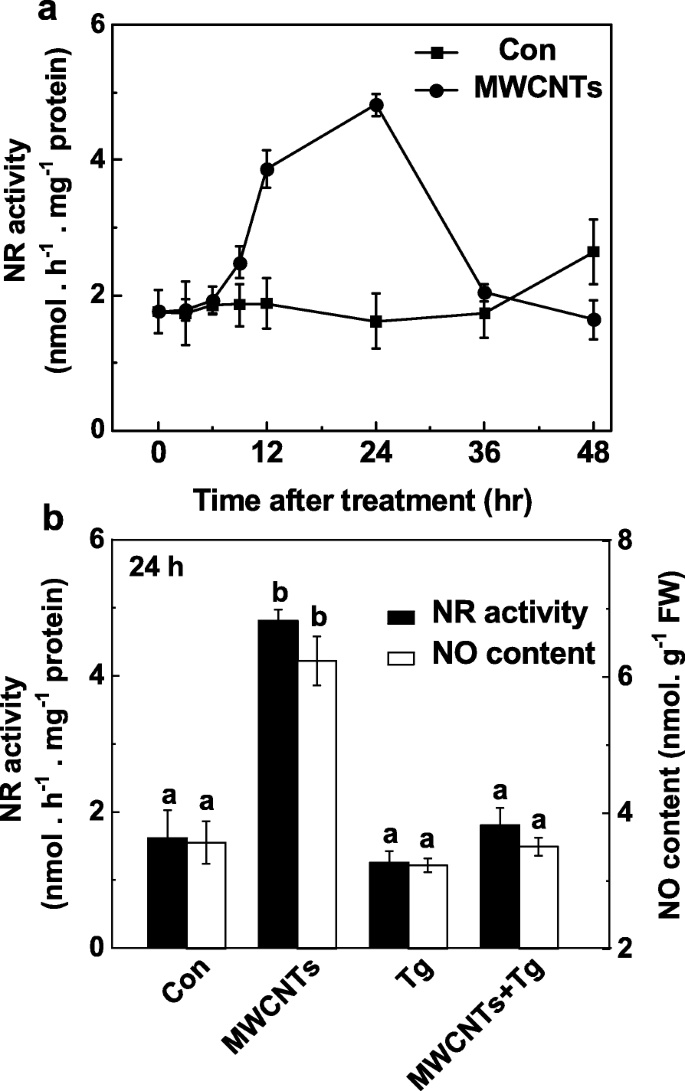
A produção de NO induzida por MWCNT foi bloqueada por tungstato, um inibidor de NR. Mudas de tomate com três dias de idade foram tratadas com água destilada e 5 mg / mL MWCNTs com ou sem 20 μM de tungstato (Tg). Mudanças na atividade NR ( a ) e SEM produção ( b ) determinado usando o método de reagente Greiss. Os dados são as médias ± SE. Barras denotadas pela mesma letra não diferiram significativamente em p Nível <0,05 de acordo com o teste múltiplo de Ducan
Discussão
A fitotoxicidade é uma consideração significativa na compreensão do potencial impacto ambiental das nanopartículas [4, 7, 61,62,63]. Evidências abundantes revelaram que MWCNTs são tóxicos para as plantas, incluindo indução de dano oxidativo, inibição da germinação de sementes, crescimento de raízes e desenvolvimento [11, 63, 64]. No entanto, sendo um fenótipo de SIMR, a ramificação da raiz através da formação da raiz lateral é um componente importante da adaptabilidade do sistema radicular a vários sinais ambientais [17]. Neste trabalho, integramos análises biológicas, farmacológicas e bioquímicas para mostrar o envolvimento da produção de NO mediada por NR na formação de LR induzida por MWCNT, pelo menos parcialmente em nossas condições experimentais. Além disso, a função do NO na organogênese da raiz estimulada por MWCNTs enfatizou os papéis centrais desse segundo mensageiro envolvido no processo de desenvolvimento da planta e adaptação contra o estresse [29,30,31,32,33, 37, 38].
Primeiro, confirmamos que 5 mg / mL MWCNTs (OD 6-12 nm) podem entrar nos tecidos radiculares (Fig. 3). Posteriormente, foi observada a indução da formação de LR do tomate (Fig. 1), mimetizando os papéis de indução de NAA e SNP (Fig. 4), um conhecido composto liberador de NO [30, 31]. Respostas indutoras semelhantes foram descobertas em árvores resinosas [41], alface [42] e Arabidopsis [43] quando desafiadas com MWCNTs (OD 6–13 nm, cerca de 9,5 nm e 30–40 nm, respectivamente). Por exemplo, a aplicação com MWCNT puro (p-MWCNT) ou MWCNT funcionalizado com carboxila (c-MWCNT) (diâmetro médio de 9,5 nm) poderia promover o desenvolvimento de LR em mudas de alface [42]. Em contraste, a inibição da raiz primária e até mesmo a formação de LR foram encontradas simultaneamente em plantas de soja quando submetidas a MWCNTs (OD 20-70 nm [40];). Comparando com os dados de diâmetro externo de MWCNTs (Tabela 1), supomos que os efeitos exibidos por MWCNT na formação de LR variaram com seus diâmetros, mostrando a promoção com diâmetro menor e a inibição com diâmetro maior. Certamente, o mecanismo relacionado deve ser investigado cuidadosamente. Fenômeno semelhante foi confirmado na tolerância à salinidade da planta [50]. Combinado com os resultados acima, foi ainda deduzido que a função dos nanomateriais pode variar de espécie, e vice-versa, diferentes tipos de nanomateriais podem causar vários efeitos biológicos. No entanto, outros fatores de influência, como diferentes doses de MWCNTs [48] e até mesmo as condições de crescimento da planta, não poderiam ser facilmente descartados.
Em comparação com outros nanomateriais, incluindo SWCNT, grafeno e AC com uma concentração idêntica, a indução máxima na formação de LR e até mesmo efeitos tóxicos no crescimento de rebentos foram observados em MWCNTs (Fig. 2). Isso pode estar relacionado às características físicas especiais dos MWCNTs, um tipo de nanomateriais que possuem alta condutividade elétrica, grande área de superfície específica, alta razão de aspecto e notável estabilidade térmica [65]. Os efeitos tóxicos dos nanomateriais foram amplamente relatados em pepino, repolho, cenoura, cebola, etc. [66, 67].
Amplas evidências mostraram que o NO, agindo como uma molécula de sinalização, pode regular uma ampla gama de processos da planta, desde a adaptação ambiental ao desenvolvimento e este último inclui a germinação da semente e organogênese da raiz [29, 68,69,70,71,72,73 ] Nosso experimento subsequente revelou que o NO pode estar envolvido na formação de LR induzida por MWCNT. Embora vários métodos para geração de imagens de NO em células vegetais tenham sido aplicados, as desvantagens, incluindo a falta de sensibilidade e a interferência por moléculas independentes de NO, podem existir em cada método [74]. Assim, três métodos responsáveis pela imagem e determinação de NO, incluindo o método de reagente Greiss, LSCM e EPR, juntamente com a aplicação de cPTIO, um eliminador de NO, foram aplicados em nossas condições experimentais. Usando três métodos, observamos que um aumento da produção endógena de NO induzida por MWCNTs em mudas de tomate foi abolida por cPTIO (Fig. 5), um eliminador de NO [30,31,32]. É importante ressaltar que este processo foi correlacionado à resposta biológica do desenvolvimento de LR induzido por MWCNT, que foi severamente bloqueado quando cPTIO foi aplicado simultaneamente (Fig. 4).
Uma avaliação adicional dessas respostas e da (s) fonte (s) potencial (is) de NO induzida (s) por MWCNTs aplicados exogenamente revelou que a produção de NO e, posteriormente, a formação de LR poderiam ser atribuídas à atividade de NR. Em plantas, a produção de NO é gerada principalmente a partir de NR e proteína semelhante a NOS de mamíferos [28]. No entanto, o gene da planta NOS ainda não foi identificado [35, 75, 76], embora alguns experimentos usando os inibidores da enzima NOS de mamífero tenham fornecido alguma evidência da via dependente de l-arginina na produção de NO [36, 76]. O NR é confirmado como a fonte mais importante de NO nas plantas [28]. Estudos anteriores mostraram que a produção de NO dependente de NR funciona como um sinal relacionado ao nitrato envolvido na regulação da arquitetura da raiz [32, 33]. Além disso, a produção de NO dependente de NR foi intimamente associada com aclimatação ao frio [38], tolerância à salinidade [50] e fechamento estomático induzido por ácido abscísico [77]. Nossos resultados revelaram ainda que o tungstato (um inibidor de NR) obviamente prejudicou a formação de LR induzida por MWCNT, especialmente no comprimento de LR (Fig. 6). Em contraste, houve apenas uma ligeira diminuição no comprimento LR, e nenhuma diferença significativa observada no número LR quando l-NAME (um inibidor de NOS de mamífero) foi usado. De forma consistente, o ensaio bioquímico mostrou que a atividade de NR foi aumentada obviamente por MWCNTs (Fig. 7a), paralelamente às mudanças na produção de NO (Fig. 5a). As respostas acima podem ser totalmente bloqueadas por tungstate (Fig. 7a, Arquivo Adicional 1:Figura S1). Assim, deduzimos que o aumento da produção endógena de NO induzida por MWCNTs foi atribuída principalmente à via NR. Certamente, mais evidências genéticas devem ser investigadas.
Conclusion
In summary, we provide evidence to show that MWCNT-induced NO production via NR might be required for tomato lateral root formation and this was summarized in Fig. 8. Importantly, above findings provide insights into the intricate molecular mechanism of MWCNTs functions in plants.
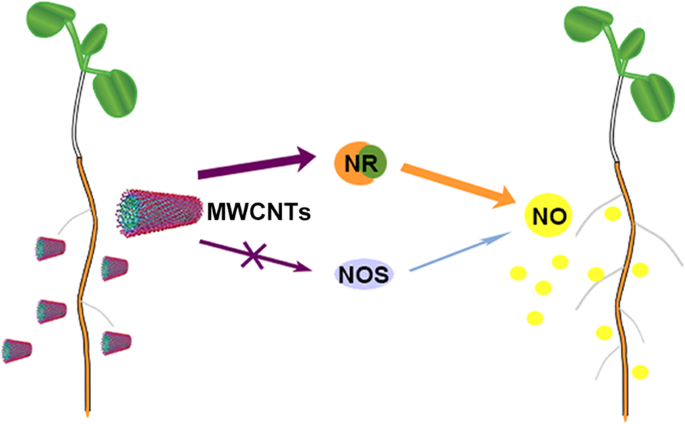
Schematic representation of the proposed MWCNT-induced tomato lateral root formation mainly via NR-dependent NO production. The role of mammalian NOS-like enzyme was preliminarily ruled out
Disponibilidade de dados e materiais
Todos os dados estão totalmente disponíveis sem restrição.
Abreviações
- CO:
-
Monóxido de carbono
- cPTIO:
-
2-(4-Carboxyphenyl)-4,4,5,5-tetramethylimidazoline-1-oxyl-3-oxide potassium salt
- DAF-FM DA:
-
4-Amino-5-methylamino-2′,7′-difluorofluorescein diacetate
- EPR:
-
Electron paramagnetic resonance
- GO:
-
Óxido de grafeno
- H 2 :
-
Hydrogen gas
- H 2 O 2 :
-
Peróxido de hidrogênio
- l-NAME:
-
N G -Nitro-l-arginine methyl ester
- LR:
-
Lateral root
- LSCM:
-
Laser scanning confocal microscopy
- MWCNTs:
-
Multi-walled carbon nanotubes
- NAA:
-
1-Naphthylacetic acid
- NO:
-
Nitric oxide
- NOS:
-
Nitric oxide synthase
- NR:
-
Nitrate reductase
- ROS:
-
Espécies que reagem ao oxigênio
- SIMR:
-
Stress-induced morphogenic response
- SNP:
-
Sodium nitroprusside
- SWCNTs:
-
Nanotubos de carbono de parede única
- TEM:
-
Microscopia eletrônica de transmissão
- Tg:
-
Tungstate
Nanomateriais
- Nanotubos de carbono ultrapassam o limite da eletrônica flexível
- Carbono oceânico gerado na escala atômica
- As vantagens de uma prótese de fibra de carbono
- Oxinitreto de carbono de boro como um novo fotocatalisador livre de metal
- Revelando a estrutura atômica e eletrônica das nanofibras de carbono de copo empilhado
- A detecção fotoeletroquímica aprimorada de ácido úrico em nanopartículas de Au Eletrodo de carbono vítreo modificado
- O estudo de um novo sistema micelar em forma de verme aprimorado por nanopartículas
- Óxido de grafeno hibridizado nHAC / PLGA Scaffolds facilitam a proliferação de células MC3T3-E1
- Estudo comparativo das propriedades eletroquímicas, biomédicas e térmicas de nanomateriais naturais e sintéticos
- Reduza a sensibilidade do CL-20 melhorando a condutividade térmica por meio de nanomateriais de carbono



