Fosfeto de cobalto (Co2P) com notável atividade eletrocatalítica projetado para bioanálise sensível e seletiva sem enzima de peróxido de hidrogênio
Resumo
Neste trabalho, nanopartículas de fosfeto de cobalto (Co 2 P NPs) foram preparados por método hidrotérmico simples e leve, sem o uso de fonte de fósforo prejudicial. A estrutura morfológica e o componente de superfície de Co 2 Os P foram caracterizados por microscopia eletrônica de transmissão, difração de raios-X e medidas de espectroscopia de fotoelétrons de raios-X. Considerando a excelente atividade de redução eletrocatalítica e a boa condutividade elétrica do fosforeto de metal de transição, fabricamos Co 2 P NPs em substrato de óxido de índio e estanho (ITO) (Co 2 P / ITO) para H 2 O 2 detecção. O Co 2 O transdutor P / ITO exibiu uma resposta amperométrica rápida inferior a 5 s, uma faixa de resposta mais ampla de 0,001 a 10,0 mM e um limite de detecção baixo de 0,65 μM. Além disso, o Co 2 não enzimático O sensor P / ITO mostrou excelente seletividade, reprodutibilidade, repetibilidade e estabilidade, todos os quais qualificaram o Co 2 Eletrodo P / ITO para um biossensor bastante confiável e promissor para H 2 O 2 de detecção.
Introdução
Peróxido de hidrogênio (H 2 O 2 ) é uma espécie reativa representativa de oxigênio em organismos vivos e desempenha um papel crítico na função fisiológica normal [1]. A concentração de H 2 O 2 em células vivas está intimamente relacionado com o equilíbrio fisiológico celular [2]. Numerosos estudos também foram relatados que câncer, doenças de Alzheimer, doenças de Parkinson e algumas doenças graves podem ser causados por concentração anormal de H 2 O 2 [3,4,5]. Desenvolvimento de métodos precisos, sensíveis, rápidos e seletivos para detectar a concentração de H 2 O 2 , um biomarcador normal de estresse oxidativo, será, sem dúvida, benéfico para o diagnóstico precoce. Até agora, uma série de métodos analíticos como espectroscopia [6], colorimetria [7], fluorescência [8, 9] e métodos eletroquímicos [10,11,12] foram aplicados em H 2 O 2 determinação. O método eletroquímico, especialmente o teste amperométrico, está gradualmente se tornando um dos métodos de detecção mais simples e eficazes para H 2 O 2 análise biológica entre diversos métodos de sensoriamento devido às suas vantagens como alta sensibilidade, excelente seletividade e baixo custo.
Sensores eletroquímicos enzimáticos provaram ser instrumentos eficazes para detectar H 2 O 2 . No entanto, a aplicação prática em larga escala de sensores baseados em enzimas é limitada pela complicada imobilização, instabilidade ambiental e baixa reprodutibilidade. Portanto, o desenvolvimento eletroquímico não enzimático H 2 O 2 sensores é altamente indispensável.
Nos últimos anos, um número crescente de sensores baseados em metal nobre [13,14,15], metal não nobre e seus compostos correspondentes [16,17,18,19] ou materiais de carbono [20, 21] têm sido usados para eletroquímico H 2 O 2 detecção. Como materiais eletroquímicos ativos para a fabricação de biossensores não enzimáticos, os compostos de metais de transição têm recebido um interesse crescente. Fosfetos de metal de transição (TMPs) são uma classe de materiais recentemente desenvolvidos com excelente atividade eletrocatalítica, boa condutividade elétrica e uma abundância de propriedades excelentes. Assim, eles têm sido extensivamente estudados para aplicações em separação de água [22, 23], hidrodessulfurização [24] e eletrodos de supercapacitores [25]. Pesquisas recentes indicam que CoP, Ni 2 P e Cu 3 P [26,27,28] também pode ser usado como eletrocatalisador eficiente para H 2 não enzimático O 2 detecção. No entanto, o número de pesquisas sobre a aplicação de TMPs em bioanálise ainda é limitado nos dias de hoje. Além disso, o uso de trifenilfosfina [29, 30], fósforo branco [31, 32] ou outra fonte de fósforo prejudicial ao meio ambiente [33] pode aumentar o risco operacional na preparação de TMPs. Portanto, alguns trabalhos de pesquisa para o desenvolvimento do método verde na preparação de TMP devem ser complementados nesta área.
Neste trabalho, nanopartículas de fosfeto de cobalto (Co 2 P NPs) foram preparados pelo método hidrotérmico de uma etapa utilizando acetato de cobalto e fósforo vermelho como matérias-primas. Aqui, nós fabricamos Co 2 P NPs em substrato de óxido de índio e estanho (ITO) pelo método de drop-casting para H 2 O 2 detecção. Co 2 P exibiu excelente atividade eletrocatalítica para H 2 O 2 redução. Além disso, revelou seletividade favorável, excelente reprodutibilidade e boa estabilidade, o que, portanto, exibiu sua aplicação potencial como uma plataforma sensível para H 2 O 2 detecção.
Seção Experimental
Reagentes e materiais
Todos os reagentes eram de grau analítico e usados sem purificação adicional. Tetra-hidrato de acetato de cobalto (II) (Co (Ac) 2 · 4H 2 O), cloreto de cobalto hexa-hidratado (CoCl 2 · 6H 2 O), D - (+) - glicose, L-Glicina (L-Gly), ácido ascórbico (AA), ácido úrico (UA), ureia, NaCl, KCl, NaH 2 PO 4 , Na 2 HPO 4 , peróxido de hidrogênio (30% H 2 O 2 ), etanol e acetona foram adquiridos de Sinopharm Chemical Reagent Co., Ltd. China. D - (-) - frutose, L-arginina (L-Arg), L-lisina (L-Lys), dopamina (DA), acetaminofeno (APAP), ácido amino trimetileno fosfônico (ATMP, 50% em peso) foram adquiridos de Aladdin Ltd. Fósforo vermelho comercial (98,5%, malha 100) foi adquirido da Energy Chemical Technology (Shanghai) Co., Ltd. A dispersão de polímero Nafion PFSA (5%) foi adquirida da Beijing Honghaitian technology Co., Ltd. Foi usada água desionizada em todos os experimentos. O vidro de óxido de índio e estanho (ITO) (10 × 20 × 1,1 mm com um filme ITO de 185 ± 2 nm e uma resistência de folha de 6,6 ± 0,1 Ω) foi fornecido por Shenzhen South Xiangcheng Technology Co., Ltd.
Síntese de Co 2 Nanopartículas P
Fósforo vermelho comercial (2 g) foi disperso em 15 mL de H 2 O sob sonificação e hidrotermicamente tratado a 200 ° C por 12 h em uma autoclave de aço inoxidável revestida com Teflon de 50 mL para limpar as camadas de óxido [34]. Em seguida, o fósforo vermelho tratado hidrotérmicamente foi seco em um forno a vácuo. Depois de terminar o pré-tratamento do fósforo vermelho, 1 mmol Co (Ac) 2 · 4H 2 O foi dissolvido em 30 mL de água destilada para obter uma solução aquosa. Em seguida, o fósforo vermelho tratado hidrotérmicamente foi adicionado à solução sob ultra-som por 15 min com a razão molar de Co / P 1/10. A suspensão preparada foi rapidamente vertida para uma autoclave revestida com Teflon de 50 mL. Em seguida, a autoclave foi colocada em forno eletrônico e tratada hidrotermicamente a 160, 200, 240 ° C por 12 h, respectivamente. Em seguida, o produto foi coletado por centrifugação e lavado três vezes com água destilada e etanol, respectivamente. Finalmente, Co 2 P NPs foram secos a 60 ° C durante 3 h ao ar.
Síntese de Co (PO 3 ) 2
O método de preparação de Co (PO 3 ) 2 foi remetido para o relatório anterior [35]. CoCl 0,1 M 2 · 6H 2 A solução de O metanol foi preparada primeiro. Em seguida, 2 mL ATMP (50 w t%) foi adicionado gota a gota a 20 mL da solução roxa acima e agitada durante 30 min. O polímero insolúvel de coordenação de cobalto-metafosfato formado na solução subsequentemente. O pó rosa obtido foi ainda aquecido a 900 ° C sob fluxo de Ar com uma taxa de aquecimento de 5 ° C · min -1 e então mantido por 2 h. Após resfriamento até a temperatura ambiente, o produto preto foi coletado e reaquecido a 650 ° C por 4 h ao ar para remover o ligante orgânico carbonizado. Finalmente, o pó roxo claro de Co (PO 3 ) 2 foi obtido.
Fabricação de Co 2 Eletrodo P / ITO
Primeiramente, o vidro ITO (1 cm × 2 cm) foi limpo em acetona, etanol e água deionizada por 10 min, respectivamente, por sonicação. Depois disso, o ITO tratado foi seco sob varredura de nitrogênio. Para a modificação do eletrodo, 5 mg do Co 2 P NPs foi disperso em 1 mL de água desionizada para formar 5 mg mL −1 Co 2 Suspensão P. Em seguida, 5 μL de solução de Nafion a 5% foram adicionados à suspensão e a mistura foi submetida a ultrassom por 15 min para obter uma suspensão uniforme semelhante a tinta. O Co 2 O eletrodo P / ITO foi preparado por lançamento de gota 100 μL de Co 2 Suspensão de P na superfície do ITO e seca ao ar como eletrodo de trabalho. O processo de preparação esquemática de Co 2 O eletrodo P / ITO é mostrado no Esquema 1.
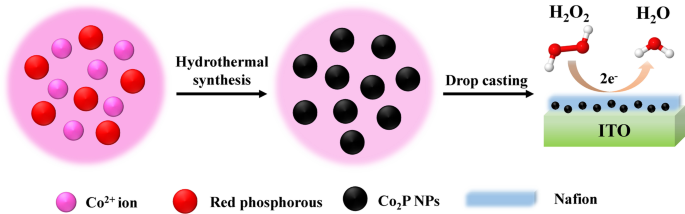
Preparação esquemática de Co 2 Eletrodo P / ITO e H 2 O 2 de detecção
Caracterizações
Os dados de difração de raios X (XRD) foram analisados por um difratômetro D8 ADVANCE com radiação Cu Kα. A medição por microscopia eletrônica de transmissão (TEM) foi realizada em um Tecnai G2 F20 com detector de espectro de energia dispersa. Os espectros de espectroscopia de fotoelétrons de raios X (XPS) foram medidos em um espectrômetro Thermo ESCALAB 250XI.
Medições eletroquímicas
As medições de voltametria foram realizadas por estação de trabalho eletroquímica CHI 660E em um sistema de três eletrodos, empregando Co 2 Eletrodo P / ITO como eletrodo de trabalho, uma folha de platina (1 cm × 1 cm) como contra-eletrodo e Ag / AgCl com solução de KCl 3 M como eletrodo de referência para estudar as atividades eletroquímicas das amostras sintetizadas para H 2 O 2 detecção. O tampão fosfato salino (PBS; 0,1 M, pH 7,4) foi usado como eletrólito para simular o meio fisiológico no corpo humano. Os desempenhos sensoriais de Co 2 Eletrodo P / ITO em direção a H 2 O 2 a detecção foi investigada por voltametria cíclica (CV) e amperometria (I-t). Todos os experimentos de detecção foram realizados sob agitação de 100 rpm à temperatura ambiente. Os testes de impedância eletroquímica foram realizados na estação de trabalho eletroquímica VersaSTAT 3F e a solução de ferricianeto foi usada como eletrólito para a medição da impedância.
Resultados e discussão
Caracterização de Co 2 P NPs
A estrutura cristalina de Co 2 P NPs foi confirmado por medição de XRD. A Figura 1a mostra os padrões de XRD de Co 2 Amostras P preparadas a 160, 200 e 240 ° C por 12 h. O Co 2 A amostra P preparada a 200 ° C mostra picos de difração em torno de 40,7 °, 40,9 °, 52,0 ° e 56,2 ° que correspondem aos planos de difração característicos em (121), (201), (002) e (320) para a fase ortorrômbica de Co 2 P (JCPDS no. 32-0306). Quando a temperatura variou de 160 a 200 ° C, as intensidades dos picos de difração aumentaram e os picos tornaram-se mais estreitos e nítidos, indicando que os produtos apresentaram maior cristalinidade a 200 ° C. No entanto, quando a temperatura atingiu 240 ° C, algumas impurezas foram formadas e os picos de difração em 29,7 ° foram atribuídos ao plano de difração em (-222) de Co (PO 3 ) 2 (JCPDS no. 27-1120). A influência do tempo sintético na preparação de Co 2 P abaixo de 200 ° C é mostrado no arquivo adicional 1:Fig. S1. Quando o tempo de duração foi controlado dentro de 12 h, o Co 2 obtido P NPs exibiram o valor mais baixo de largura total na metade do máximo de (121) pico, sugerindo melhor cristalinidade. Além disso, nenhuma impureza existia na amostra quando o tempo de reação variou de 6 a 24 h. De acordo com a fórmula de Scherrer, o tamanho de grão calculado de Co 2 P NPs preparados a 200 ° C durante 12 h foi de 14,2 nm.
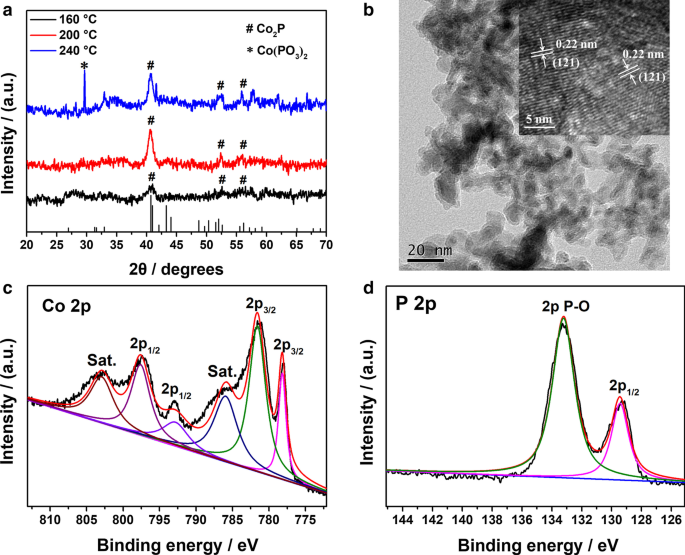
a Padrões de XRD de Co 2 P NPs preparados em diferentes temperaturas por 12 h. b Imagem microscópica eletrônica de transmissão e imagem microscópica eletrônica de transmissão de alta resolução (inserção) de Co 2 P NPs. Espectros XPS de Co 2 P no c Co 2 p região e d P 2 p região
A morfologia de Co 2 P NPs foi avaliado por medições TEM. Conforme mostrado na Fig. 1b, o produto preparado a 200 ° C é composto de nanopartículas irregulares com o diâmetro em torno de 10–20 nm e duas franjas de rede podem ser vistas claramente na imagem TEM de alta resolução (HRTEM) (inserção na Fig. 1b). A distância entre os planos vizinhos é de 0,22 nm, correspondendo às (121) facetas de Co 2 P, que confirma ainda que a formação de TMP é Co 2 P.
A técnica XPS foi empregada na análise das composições químicas na superfície do Co 2 P. Arquivo adicional 1:Fig. S2 mostra o espectro de pesquisa XPS de Co 2 Elementos P. Co, P e O são detectados na amostra, confirmando a existência de Co 2 P e alguns produtos oxidados. Espectroscopia de energia dispersiva de raios-X (EDX) de Co 2 P (Arquivo adicional 1:Fig. S3) confirma ainda mais a coexistência de três elementos (Co, P, O) na amostra. Os espectros XPS de alta resolução de Co 2p e P 2p são mostrados na Fig. 1c, d, respectivamente. No espectro de Co 2p, os picos em 781,1 e 797,6 eV podem ser atribuídos às energias de ligação (BEs) de Co 2+ 2 p 3/2 e Co 2+ 2 p 1/2 , respectivamente [26, 36]. Os picos em 786,0 e 803,1 eV são dois picos de satélite de agitação aparente. O Co 2p BE de 778,2 eV muda positivamente daquele do Co metálico (777,9 eV), o que sugere que Co em Co 2 P tem uma carga parcial positiva ( δ + ) com um valor pequeno (0 < δ <2) [37]. Pelo contrário, o P 2 p BE de 129,4 eV muda negativamente daquele de P elementar (130,2 eV) de modo que o P tem uma carga negativa parcial ( δ - ) em Co 2 P. As mudanças de BE no elemento Co e P em comparação com sua substância elementar, respectivamente, revelam que a direção de transferência da densidade do elétron em Co 2 P é de Co a P [38]. Oxidação superficial de Co 2 P gera algumas espécies de P oxidadas na amostra. Portanto, os picos em 133,2 eV na faixa de BE alto são atribuídos aos óxidos [39].
Detecção eletroquímica de H 2 O 2 em Co 2 Eletrodo P / ITO
Para investigar a atividade eletrocatalítica de Co 2 P NPs em H 2 O 2 redução, projetamos um H 2 não enzimático O 2 eletrodo por drop-casting Co 2 Suspensão de NPs de P em uma superfície ITO nua. A Figura 2a mostra as curvas CV de ITO e Co 2 nuas P / ITO em PBS 0,1 M a pH 7,4 com e sem H 5,0 mM 2 O 2 , respectivamente. As linhas tracejadas indicam que a resposta do ITO simples para H 2 O 2 a redução é insignificante. No entanto, o Co 2 O eletrodo P / ITO exibe um pico de redução notável em - 0,5 V na presença de H 2 O 2 , que demonstra a atividade eletrocatalítica proeminente de Co 2 P NPs em direção a H 2 O 2 redução. A Figura 2b apresenta as curvas CV de Co 2 P / ITO em diferentes taxas de varredura (de 30 a 100 mV s −1 ) com 2,5 mM H 2 O 2 . Ao aumentar a taxa de varredura, a redução da corrente de pico aumentou e o potencial de pico mudou para o lado do potencial mais negativo, indicando a redução em H 2 O 2 no Co 2 P / ITO foi uma reação irreversível. A curva de calibração correspondente (inserção, Fig. 2b) mostra que as densidades de corrente de pico de redução aumentam linearmente proporcional à taxa de varredura, sugerindo que a redução eletroquímica de H 2 O 2 na superfície de Co 2 O eletrodo P / ITO é um processo de superfície controlada [40].
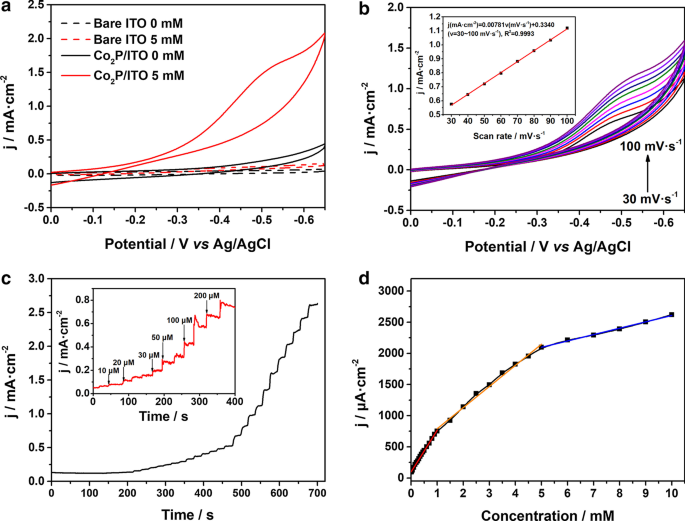
a Curvas de CV de ITO e Co 2 simples Eletrodo P / ITO em PBS 0,1 M com e sem H 5,0 mM 2 O 2 a uma taxa de varredura de 100 mV s −1 . b Curvas CV de Co 2 Eletrodo P / ITO em 2,5 mM H 2 O 2 em taxas de varredura de 30 a 100 mV s −1 . Inserção:O gráfico correspondente da corrente versus a taxa de varredura. c Respostas amperométricas de Co 2 Eletrodo P / ITO com adição sucessiva de H 2 O 2 em 0,1 M PBS. d A curva de calibração da corrente constante versus a concentração de H 2 O 2
A Figura 2c, d mostra a resposta amperométrica e a curva de calibração de Co 2 Eletrodo P / ITO após a adição sucessiva de H 2 O 2 no PBS 0,1 M a -0,5 V com agitação. O Co 2 Eletrodo P / ITO exibiu resposta rápida à adição de H 2 O 2 e atingiu a corrente de estado estacionário em 5 s. A curva de calibração na Fig. 2d mostra que o transdutor exibe uma faixa multilinear de H 2 O 2 concentração de 0,001 a 1,0 mM, 1,0–5,0 mM e 5,0–10,0 mM. A sensibilidade do sensor altera com o aumento da concentração de H 2 O 2 , devido à mudança da cinética de redução eletrocatalítica de H 2 O 2 na superfície do eletrodo. De acordo com relatórios anteriores, a etapa determinante da taxa de H 2 O 2 a redução é dominada por H 2 O 2 adsorção em baixa concentração, enquanto a ativação de H 2 O 2 é o principal determinante em alta concentração. Na região intermediária, a cinética de redução de H 2 O 2 é controlado por adsorção e ativação ao mesmo tempo [10]. Uma multidão de analistas será adsorvida na superfície de Co 2 P e cobrem os sítios ativos na concentração elevada, que levam à diminuição da sensibilidade [41].
A comparação em H 2 O 2 detectar desempenhos do Co 2 preparado A amostra P em várias temperaturas de reação e tempo é mostrada no arquivo adicional 1:Fig. S4, S5 e Tabela S1, indicando que o Co 2 A amostra P preparada a 200 ° C por 12 h exibe o melhor H 2 O 2 desempenho de detecção. Quando a temperatura da reação subiu para 240 ° C, o Co formado (PO 3 ) 2 em Co 2 P pode ser considerado impureza. Para esclarecer ainda mais a influência de Co (PO 3 ) 2 em H 2 O 2 detecção, as propriedades eletroquímicas do Co (PO 3 ) 2 foram investigados. Conforme mostrado no arquivo adicional 1:Fig. S6, Co (PO 3 ) 2 exibe resposta eletroquímica desprezível para H 2 O 2 e sua condutividade é inferior a Co 2 P, que diminui o sinal atual de Co 2 P / ITO em teste amperométrico. Portanto, quanto maior a pureza e a melhor cristalinidade do Co 2 A amostra P pode contribuir para a melhoria do desempenho de detecção. Assim, escolhemos o Co 2 Amostra P preparada a 200 ° C e 12 h como o melhor H 2 O 2 material de detecção. A calibração I - t curva também apresenta uma boa relação linear na concentração de 1,0-50 μM, a faixa fisiológica de H 2 O 2 concentração em biossistema (Fig. S7) [28], o que poderia ser útil para melhorar a possibilidade de aplicações práticas deste sensor. Além disso, o limite de detecção (LOD) do H 2 O 2 o sensor pode ser calculado como 0,65 μM a uma razão sinal-ruído de 3. Comparado com o H 2 relatado anteriormente O 2 sensor, o desempenho eletroquímico abrangente de nosso Co 2 Os transdutores P / ITO são superiores àqueles com sensibilidade favorável, faixa linear e LOD, conforme mostrado na Tabela 1.
Depois de detectar H 1,0 mM 2 O 2 repetidamente por 35 vezes (Fig. 3a, b), os espectros de XPS em Co 2 p e P 2 p região de Co 2 P são analisados para investigar melhor o mecanismo de detecção. Não há mudança significativa na posição dos picos em P 2 p região antes e depois de H 2 O 2 detecção. No entanto, os picos em 778,2 e 793,0 eV em Co 2 p espectro desapareceu após múltiplas medições. Como o pico em 778,2 eV indica a existência de espécies reduzidas de Co em Co 2 Amostra P [37], o desaparecimento desses dois picos demonstra que a espécie de Co reduzida com baixa valência em Co 2 P pode ser oxidado por H 2 O 2 durante o processo de detecção, especialmente com alta concentração de H 2 O 2 . Os picos remanescentes em Co 2 p região (782,1 e 798,3 eV) são atribuídos a Co 2+ 2 p 3/2 e Co 2+ 2 p 1/2 , respectivamente, sugerindo a existência exclusiva de espécies de Co (II) em Co 2 P após várias medições. De acordo com relatórios anteriores sobre a utilização de eletrocatalisador à base de cobalto em H 2 O 2 detecção, Co 2+ espécies são demonstradas como os locais ativos catalíticos para H 2 O 2 redução [46,47,48]. Geralmente, a redução eletroquímica em H 2 O 2 passa por duas etapas no PBS [49, 50], conforme mostrado abaixo.
$$ {\ text {H}} _ {{2}} {\ text {O}} _ {{2}} + {\ text {e}} ^ {-} \ to {\ text {OH}} _ {{{\ text {ad}}}} + {\ text {OH}} ^ {-} $$ (1) $$ {\ text {OH}} _ {{{\ text {ad}}}} + {\ text {e}} ^ {-} \ to {\ text {OH}} ^ {-} $$ (2) $$ (2) $$ {\ text {2OH}} ^ {-} + {\ text {2H}} ^ {+} \ para {\ text {2H}} _ {{2}} {\ text {O}} $$ (3)
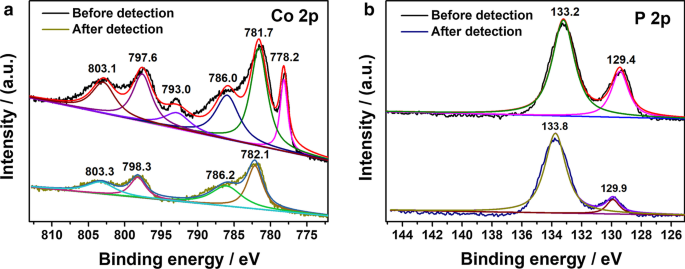
A comparação dos espectros de XPS em a Co 2 p região e b P 2 p região de Co 2 P antes e depois da detecção
Na primeira etapa, H 2 O 2 obtém um elétron para formar OH adsorvido - (OH anúncio ) Quando o intermediário OH ad obtém um elétron adicional, o produto final da redução de H 2 O 2 , H 2 O, é gerado. Como o potencial redox de H 2 O 2 / H 2 O é maior do que Co 3+ / Co 2+ , a espécie Co (II) em Co 2 P pode ser oxidado a Co (III) no processo de transferência de elétrons e H 2 O 2 é reduzido a H 2 O irreversivelmente. Durante o teste amperométrico, a polarização aplicada é - 0,5 V versus Ag / AgCl (igual a 0,14 V vs . NHE), que é inferior ao potencial redox padrão de Co 3+ / Co 2+ . Como resultado, o Co (III) oxidado pode ser reduzido a Co (II) e esses sítios ativos catalíticos do Co (II) são regenerados novamente. Portanto, pode-se concluir que o ciclo catalítico de espécies de Co (II) ocorre durante a detecção eletroquímica de H 2 O 2 e as espécies reduzidas de Co com baixa valência são oxidadas por H 2 O 2 após medições repetitivas.
Seletividade, estabilidade, reprodutibilidade e repetibilidade de Co 2 Eletrodo P / ITO
O desempenho anti-interferência é outra propriedade importante do biossensor. O nitrogênio de alta pureza foi utilizado para evitar a influência do oxigênio dissolvido em solução porque o oxigênio poderia ser reduzido em potencial semelhante ao que foi aplicado no teste amperométrico [51]. Comparando as curvas CV de Co 2 P / ITO em PBS 0,1 M com ou sem purga de nitrogênio, o potencial de redução e a resposta de corrente de H 2,5 mM 2 O 2 são semelhantes, como mostrado na Fig. S8, o que, portanto, sugere que a interferência do oxigênio dissolvido pode ser desprezada. Seletividade de Co 2 P / ITO também foi testado com substâncias comuns e outras pequenas moléculas em fluidos corporais, como alguns sais inorgânicos, sacarídeos, aminoácidos e biomoléculas redutoras. Conforme mostrado na Fig. 4a, a resposta atual após a adição dos interferentes acima pode ser desprezada em comparação com a resposta de 1,0 mM H 2 O 2 . Como dois átomos de O de H 2 O 2 poderia ser ligado com um ou dois átomos de Co [52], o H 2 O 2 molécula seria adsorvida quimicamente em espécies de Co (II) em Co 2 P especificamente. Além disso, a interferência da oxidação indiscriminada de alguns compostos redutivos em amostras biológicas reais em alto potencial também pode ser reduzida significativamente em potencial de polarização inferior [53]. Portanto, a seletividade favorável de Co 2 P em direção a H 2 O 2 beneficia principalmente das espécies Co (II) como locais de adsorção específicos e do potencial de polarização negativa aplicada durante o processo de detecção.
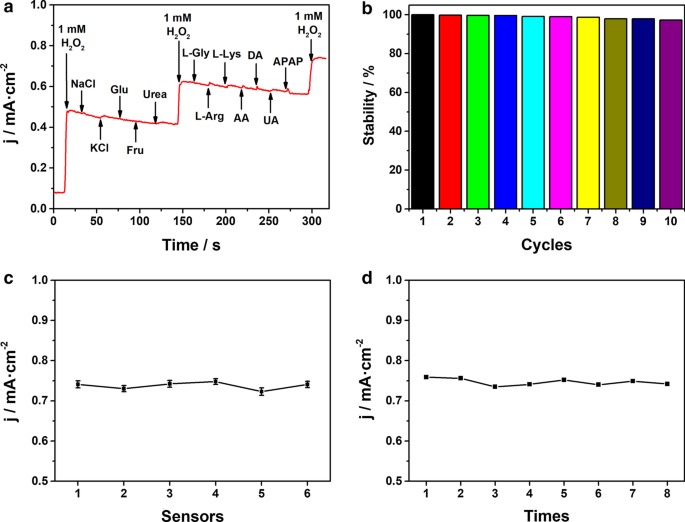
a Respostas amperométricas de Co 2 Eletrodo P / ITO com a adição de 1 mM H 2 O 2 e outras espécies interferentes (NaCl 10 mM, KCl, Glu, Fru, ureia, L-Gly, L-Arg, L-Lys, AA; DA 1 mM, UA; APAP 0,5 mM) em PBS 0,1 M. b As correntes de pico catódico de dez curvas CV de varredura sucessivas em 50 μM H 2 O 2 . c Reprodutibilidade de seis Co 2 Eletrodos P / ITO para detecção de H 1,0 mM 2 O 2 . d Repetibilidade de Co 2 Eletrodo P / ITO para detecção de H 1,0 mM 2 O 2 oito vezes
Além disso, a estabilidade, reprodutibilidade e repetibilidade do Co 2 O transdutor P / ITO também foi avaliado. As correntes de pico de redução de dez curvas CV de varredura sucessivas em 50 μM H 2 O 2 é mostrado na Fig. 4b. Após dez ciclos, a corrente de pico do eletrodo caiu apenas 2,7%. Além disso, o sensor permaneceu cerca de 98,2% de sua resposta de corrente inicial após ser armazenado no ar por um mês (Fig. S9), demonstrando estabilidade de detecção ideal e excelente durabilidade de longo prazo. A reprodutibilidade eletrodo para eletrodo é investigada calculando o desvio padrão relativo (RSD) de H 2 O 2 respostas atuais. Para eliminar o erro potencial da fabricação do eletrodo, tanto quanto possível, a densidade de corrente constante na presença de H 2 O 2 é subtraído pelo sinal de fundo inicial do eletrodo individual e o valor de diferença obtido é considerado como a resposta eletroquímica de cada eletrodo. Seis Co 2 Eletrodos P / ITO foram fabricados sob as mesmas condições para experimentos controlados e o RSD das respostas de corrente foi de 1,24%, como mostrado na Fig. 4c, indicando a reprodutibilidade relativamente excelente de Co 2 P / ITO. Enquanto isso, a repetibilidade foi medida em um eletrodo detectando 1,0 mM H 2 O 2 oito vezes, e o RSD de 1,14% foi alcançado (fig. 4d). Os resultados acima ilustram a estabilidade satisfatória, reprodutibilidade e repetibilidade do eletrodo para detecção eletroquímica não enzimática de H 2 O 2 .
Conclusão
Em resumo, Co 2 P NPs foram sintetizados com sucesso pelo método hidrotérmico. Além disso, o Co 2 P NPs preparados a 200 ° C por 12 h provaram ser um catalisador eficiente para a redução eletroquímica de H 2 O 2 em pH 7,4 PBS. Como um H não enzimático 2 O 2 sensor, o Co 2 O eletrodo P / ITO exibiu uma resposta amperométrica rápida inferior a 5 s, uma faixa de resposta mais ampla de 0,001 a 10,0 mM e um limite de detecção baixo de 0,65 μM, bem como seletividade, reprodutibilidade e estabilidade satisfatórias. Este trabalho tem como objetivo ampliar a pesquisa sobre a aplicação do fosforeto de metal de transição na detecção eletroquímica de pequenas biomoléculas e nosso Co 2 O sensor P / ITO pode ser projetado como uma nova plataforma não enzimática para H 2 O 2 detecção.
Disponibilidade de dados e materiais
Todos os dados e materiais estão totalmente disponíveis sem restrições.
Abreviações
- NPs:
-
Nanopartículas
- ITO:
-
Óxido de índio estanho
- TEM:
-
Microscopia eletrônica de transmissão
- HRTEM:
-
Microscopia eletrônica de transmissão de alta resolução
- XRD:
-
Difração de raios X
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- EDX:
-
Espectroscopia de raios-X de dispersão de energia
- CV:
-
Voltametria cíclica
- I-t:
-
Amperometria
- Gly:
-
Glicina
- AA:
-
Ácido ascórbico
- UA:
-
Ácido úrico
- Arg:
-
Arginina
- Lys:
-
Lisina
- DA:
-
Dopamina
- APAP:
-
Paracetamol
- ATMP:
-
Ácido trimetileno fosfônico
- PBS:
-
Tampão Fosfato
- LOD:
-
Limite de detecção
- RSD:
-
Desvio padrão relativo
Nanomateriais
- Demonstração de um biossensor flexível à base de grafeno para detecção sensível e rápida de células cancerosas do ovário
- MoS2 com Espessura Controlada para Evolução Eletrocatalítica de Hidrogênio
- Nanodots de carbono como nanosensores de modo duplo para detecção seletiva de peróxido de hidrogênio
- Fabricação, Caracterização e Atividade Biológica de Sistemas de Nanotransmissão de Avermectina com Diferentes Tamanhos de Partículas
- Cascas de diatomáceas de sílica adaptadas com nanopartículas de Au permitem a análise sensível de moléculas para aplicações biológicas, de segurança e ambientais
- Um método fácil para preparação de heterojunção Cu2O-TiO2 NTA com atividade fotocatalítica visível
- Uma nova microestrutura de cluster de nanocônios com propriedades anti-reflexo e superhidrofóbicas para dispositivos fotovoltaicos
- Plasmonic ELISA para detecção sensível de biomarcadores de doenças com um leitor baseado em telefone inteligente
- A influência dos materiais, heteroestrutura e orientação para nanohíbridos na atividade fotocatalítica
- Torno projetado para precisão e velocidade



