Propriedades fotocatalíticas de pós de TiO2 revestidos com Co3O4 preparados por deposição de camada atômica aprimorada com plasma
Resumo
Co 3 O 4 de TiO comercial revestido 2 pós (P25) fotocatalisadores de junção p-n foram preparados pela técnica de deposição de camada atômica intensificada por plasma (PEALD). A estrutura, morfologia, bandgap e propriedades fotocatalíticas sob luz ultravioleta foram investigadas sistematicamente. Embora a deposição de Co 3 O 4 não altera a estrutura anatase e o tamanho do cristalito dos pós P25, a atividade fotocatalítica ultravioleta foi melhorada evidentemente. Para o Co 3 O 4 revestidos com P25, os vestígios de Co ions existem como Co 3 O 4 nanopartículas anexadas a TiO 2 superfície do pó em vez da ocupação de Ti 4+ posição no TiO 2 treliça. O Co 3 O 4 os pós P25 revestidos exibem eficiência de degradação fotocatalítica aprimorada de quase 100% para azul de metileno em 1,5 h sob luz ultravioleta, em comparação com P25 de 80%. Os gráficos de Mott-Schottky dos pós fotocatalisadores confirmam a formação da heterojunção p-n em Co 3 O 4 –TiO 2 materiais nanocompósitos, o que é benéfico para aumentar a eficiência da separação elétron-buraco fotogerada. Além disso, o Co 3 O 4 o revestimento também promove a adsorção de corantes orgânicos de azul de metileno em pós P25.
Histórico
Com o rápido desenvolvimento da indústria moderna, a contaminação da água surgiu como um problema sério [1, 2]. Os corantes orgânicos apresentam efeitos tóxicos e reduzem a penetração da luz na água contaminada [3]. Além disso, a maioria dos corantes têxteis mostra recalcitrância em relação à oxidação química e outros tratamentos tradicionais de águas residuais. Felizmente, TiO 2 fotocatalisadores à base de exibem excelente degradação para corantes orgânicos [4]. TiO 2 tem sido extensivamente e intensamente estudado como um dos materiais fotocatalíticos populares devido à sua baixa toxicidade, alta estabilidade química e atividade catalítica na eliminação de uma grande variedade de poluentes orgânicos [5,6,7]. No entanto, sua eficiência quântica geral é relativamente baixa devido à rápida taxa de recombinação dos pares elétron-buraco fotogerados [8]. Além disso, o grande gap intrínseco do TiO 2 limita sua absorção óptica à região do UV, que representa apenas menos de 4% da radiação solar total [9, 10]. Essas falhas impedem suas aplicações práticas. Assim, diferentes abordagens têm sido exploradas para melhorar suas atividades fotocatalíticas, incluindo dopagem metal / não-metal [11, 12], sensibilização por corante [13] e formação de heterojunção [14, 15].
Foi demonstrado que construir a heterojunção p-n entre TiO tipo n 2 e semicondutor do tipo p, como NiO ou Ag 2 O, é benéfico para reduzir a taxa de recombinação de elétrons fotogerados e lacunas [16,17,18]. Em primeiro lugar, a junção p-n pode produzir um potencial embutido na interface do semicondutor. Sob iluminação, o campo elétrico interno promoverá a separação e o transporte dos pares elétron-buraco fotogerados [19]. Em segundo lugar, semicondutores com bandgap menor podem aumentar a absorção de luz do catalisador com bandgap maior [20]. Além disso, alguns semicondutores também podem ser empregados para melhorar a estabilidade do catalisador e facilitar as reações eletroquímicas de superfície [21]. Como resultado, a atividade fotocatalítica poderia ser melhorada dramaticamente pela formação de hetero-junção semicondutor / semicondutor. Chen et al. relataram que a junção p-n NiO / TiO 2 o fotocatalisador mostrou fotoatividade melhorada na degradação do azul de metileno (MB) [22].
Co 3 O 4 , um dos óxidos de metal de transição mais versáteis, é amplamente aplicado em muitos campos, como degradação de corantes [23, 24], sensores de gás [25], baterias de íon de lítio [26], oxidação de CO em baixa temperatura [27] , e H 2 geração [28]. Co 3 O 4 , como NiO e Ag 2 O, pertence a semicondutores do tipo p. Seu bandgap (2,1 eV) é relativamente mais estreito em comparação com o de NiO (3,5 eV). Além disso, mostra melhor estabilidade química do que Ag 2 O porque Ag 2 O tende a absorver CO 2 no ar para formar Ag 2 CO 3 ou se decompõe em Ag quando usado em uma temperatura comparativamente alta [28]. Foi relatado que p-n Co 3 O 4 / BiVO 4 ou Co 3 O 4 / TiO 2 junção exibiu atividade fotocatalítica mais alta do que semicondutor único de BiVO 4 ou TiO 2 na remoção de corantes orgânicos [29, 30].
Vários métodos foram usados para sintetizar Co 3 O 4 nanosistemas baseados em plasma, como deposição química de vapor (CVD) [31,32,33], spray de plasma [34] e processos de CVD assistido por plasma (PECVD) [35,36,37]. O Co 3 O 4 / TiO 2 A junção p-n também foi fabricada pelo método de impregnação-deposição-decomposição [30]. A calcinação e excitação subsequentes foram necessárias, o que pode produzir emissão de exaustão.
A deposição de camada atômica (ALD) é uma nova técnica de deposição de filme fino baseada em reações sequenciais de quimissorção de superfície autolimitada e complementar usando vapor precursor. Comparado ao CVD, PECVD e método de solução química, apresenta vantagens únicas, incluindo grande uniformidade de área, excelente conformalidade tridimensional, controle preciso e simples da espessura do filme, modificação de superfície flexível e baixa temperatura de processamento [38]. A deposição de camada atômica intensificada por plasma (PEALD), onde espécies de plasma são empregadas como gás reativo durante uma etapa do processo de deposição cíclica, mostra alguns méritos sobre ALD térmico, como mais liberdade para a temperatura do substrato e precursores. Recentemente, ALD tem mostrado perspectivas crescentes e amplas aplicações em vários campos, como semicondutor [39], nova energia [40] e fotocatálise [41], especialmente na modificação de superfície de nanomateriais [42].
Aqui, trace Co 3 O 4 com revestimento de TiO 2 O fotocatalisador de junção p-n foi fabricado pelo método ALD. Comparado com o método de impregnação-deposição-decomposição com procedimentos de várias etapas [30], a técnica ALD tem apenas uma etapa de deposição e baixa temperatura de processamento de 200 ° C sem recozimento subsequente. A estrutura cristalina, morfologia, composição e bandgap de Co 3 O 4 os pós P25 revestidos foram caracterizados por várias técnicas analíticas. A atividade fotocatalítica de Co 3 O 4 Os pós P25 revestidos com 100 e 200 ciclos na degradação do corante azul de metileno (MB) sob irradiação de luz ultravioleta (UV) foram investigados profundamente. Pode-se descobrir que, em contraste com os pós P25 puros, o Co 3 de 100 ciclos O 4 a amostra de junção P25 p-n revestida exibe uma eficiência fotocatalítica de UV nitidamente melhorada. O possível mecanismo fotocatalítico de Co 3 O 4 com revestimento de TiO 2 pós também é proposto.
Métodos
TiO comercial 2 pós (P25) foram usados como apoiadores para Co 3 O 4 deposição. Os pós P25 foram carregados uniformemente em um recipiente poroso e colocados na câmara PEALD (SUNALE R-200, Picosun). Dicarbonil ciclopentadienil cobalto (CoCp (CO) 2 , Strem Chemicals, 96%) mantido a 45 ° C e plasma de oxigênio em temperatura ambiente foi usado como precursor de cobalto e fonte de oxigênio para Co 3 O 4 deposição, respectivamente. Oxigênio de alta pureza (99,999%) foi usado como fonte de plasma de oxigênio com argônio (99,999%) como gás de arraste, e a potência do plasma e O 2 a taxa de fluxo de gás foi de 2500 W e 160 sccm, respectivamente. Em seguida, 100 e 200 ciclos Co 3 O 4 foram depositados em pós P25 a 200 ° C por PEALD, onde um ciclo consistia em 0,2 s CoCp (CO) 2 dosagem, 6 s N 2 purga, 21,5 s O 2 dosagem de plasma e 6 s N 2 purgando. Para o Co 3 de 600 ciclos O 4 Uma amostra P25 revestida, fluxo de oxigênio (130 sccm) em vez de plasma de oxigênio foi usada como fonte de oxigênio. O precursor de Co e a temperatura do reator permaneceram inalterados. Portanto, 600 ciclos Co 3 O 4 foram depositados em pós P25 por ALD térmico, onde um ciclo consistia em 2 s CoCp (CO) 2 dosagem, 8 s N 2 purga, 5 s O 2 dosagem e 10 s N 2 purgando. Em nosso trabalho anterior, foi demonstrado que PEALD Co 3 O 4 em nanotubos de carbono mostrou uma baixa taxa de deposição e modo de crescimento em ilha [43]. A espessura de 800 e 2400 ciclos de Co 3 O 4 foi de 5 e 20 nm, respectivamente. A superfície de deposição áspera foi coberta por Co 3 O 4 nanopartículas. Portanto, 100 e 200 ciclos Co 3 O 4 deposição em P25 pode ainda estar em seu estágio de nucleação, podendo levar à formação de Co 3 O 4 nanopartículas revestidas de TiO 2 estrutura de junção p-n.
A estrutura cristalina de Co 3 O 4 Os pós P25 revestidos foram caracterizados por difração de raios-X (XRD, Rigaku-D / max 2000) com radiação Cu Kα (λ =0,15418 nm). O ângulo de varredura variou de 10 ° a 80 ° operado a 40 kV e 40 mA. A característica química da superfície foi analisada por espectroscopia de fotoelétrons de raios-X (XPS, Thermo ESCALAB-Thermo fisher K-alpha) usando radiação Al Kα (1486,6 eV) como fonte de excitação. Todas as energias de ligação foram referenciadas ao pico C 1s em 284,6 eV. A espectrometria de massa com plasma indutivamente acoplado (ICP-MS, Thermo X Series 2 ICP-MS) foi realizada para medir o conteúdo do elemento Co de pós fotocatalisadores.
A microestrutura e a morfologia da superfície dos pós foram caracterizadas usando microscopia eletrônica de varredura por emissão de campo (FESEM, Ultra 55, ZRISS) e microscopia eletrônica de transmissão (TEM, FEI Tecnai G 2 F20 S-Twin). Os pós do catalisador foram dispersos totalmente em etanol por 20 min de vibração ultrassônica antes de pingar na grade de cobre com folha de carbono ultrafina para observação TEM. As áreas superficiais específicas de Brunauer-Emmett-Teller (BET) foram realizadas em aparelho de adsorção de nitrogênio (Micromeritics Tristar-3000).
A atividade fotocatalítica de Co 3 O 4 com revestimento de TiO 2 pós na decomposição do azul de metileno (MB) foram avaliados sob irradiação de uma lâmpada LED UV de 100 W (UVEC-411). Água de resfriamento circulante foi empregada para manter a temperatura do sistema em ~ 25 ° C. A lâmpada estava localizada a 15 cm de distância da solução de reação. Cinquenta miligramas de catalisador foram adicionados a 50 mL de solução aquosa MB (37,4 mg / L). Antes da iluminação, a solução misturada foi agitada por 3 h na ausência de luz para atingir o equilíbrio de adsorção. Após cada tempo de irradiação determinado, cerca de 4 mL da mistura foram retirados e separados por centrifugação para remover o catalisador sólido suspenso. O processo de degradação foi monitorado por um espectro de absorção de UV-vis (UV-3600, Shimadzu, Japão), e a concentração do MB residual foi analisada quantitativamente medindo a absorção máxima em 664 nm.
A atividade fotocatalítica de luz visível de Co 3 O 4 com revestimento de TiO 2 os pós também foram avaliados por meio da degradação da laranja de metila (MO) em solução aquosa. Um simulador solar (lâmpada Xe de 300 W, MircoSolar300, PerfectLight) com um filtro de corte de 420 nm fornece a irradiação de luz visível. A concentração de MO residual foi determinada medindo a absorção máxima de MO a 464 nm.
Os gráficos de Mott-Schottky foram medidos usando estação de trabalho eletroquímica (CHI Instruments CHI760E) nas frequências de 1 e 2 kHz no escuro. Cinquenta e dois miligramas de P25 ou 200 ciclos de Co 3 O 4 pós revestidos de P25 juntamente com 18 mg de iodo foram dispersos em 50 mL de acetona por meio de vibração ultrassônica. Em seguida, a lama misturada foi galvanizada em óxido de estanho dopado com flúor (FTO), conduzindo vidro sob 15 V por 2 min. A medição eletroquímica foi conduzida em eletrólito de NaOH 1 M em temperatura ambiente usando uma configuração de três eletrodos. O vidro FTO preparado com fotocatalisador foi adotado como o eletrodo de trabalho. Uma tela de platina (1 cm × 2 cm) e Ag / AgCl foram usados como contra-eletrodo e eletrodo de referência, respectivamente. O ponto isoelétrico (IEP) de MB, P25 e Co de 200 ciclos 3 O 4 P25 revestido em soluções aquosas foi determinado usando a medição do potencial Zeta (Malvern Zetasizer, Nano ZS 90 zeta).
Resultados e discussão
O XRD foi usado para determinar a estrutura de fase das amostras. A Figura 1 exibe os padrões de XRD de P25 puro e Co de 200 ciclos 3 O 4 P25 revestido em pó. Ambas as amostras exibem os picos característicos semelhantes de anatase TiO padrão 2 (Cartão JCPDS nº:21–1272), sugerindo que não há nenhuma mudança óbvia na estrutura do cristal após Co 3 O 4 Revestimento. Além disso, o tamanho do cristalito de ambas as amostras pode ser estimado em 20 ± 2 nm pela fórmula de Scherrer.
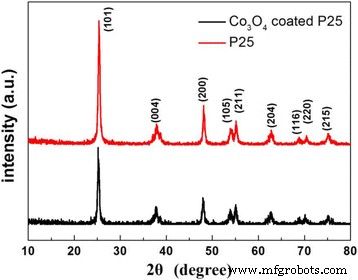
Padrões de XRD de P25 e Co de 200 ciclos puros 3 O 4 -pós P25 revestidos
SEM e TEM foram utilizados para observar a morfologia e microestrutura de P25 puro e Co de 200 ciclos 3 O 4 P25 revestido com pó, conforme mostrado na Fig. 2a-d. P25 puro e Co de 200 ciclos 3 O 4 As amostras P25 revestidas mostram morfologia semelhante e tamanho de cristalito de 15-30 nm (Fig. 2a, b). A distribuição do tamanho das nanopartículas também foi contada, conforme mostrado na Fig. 2e, f, que pode ser ajustada às curvas gaussianas. O valor médio calculado dos tamanhos de cristalito de P25 puro e Co de 200 ciclos 3 O 4 os pós P25 revestidos são ~ 25,8 e ~ 26,2 nm, respectivamente, o que é ligeiramente maior do que o resultado de XRD devido à fácil negligência de nanopartículas menores em observações de SEM. Essas nanopartículas se aglomeram para formar alguns aglomerados maiores de 50-100 nm. Na imagem TEM de alta resolução (HRTEM) da Fig. 2c, um TiO bem cristalizado de ampliação local 2 nanocristais com franjas de rede transparentes podem ser vistos em pós P25 puros. Após 200 ciclos PEALD Co 3 O 4 , podemos discernir notavelmente algumas pequenas nanopartículas amorfas localizadas no TiO cristalino maior 2 superfície com o diâmetro de 2–3 nm, conforme marcado pelas setas na Fig. 2d. Com base em nosso trabalho anterior [43], essas pequenas nanopartículas devem ser Co 3 derivado de PEALD O 4 com o modo de crescimento da ilha. Combinado com os resultados de TEM e XRD, pode-se deduzir que os Co ions existem como Co 3 O 4 nanopartículas amorfas anexadas a TiO 2 superfície do pó em vez da ocupação de Ti 4+ posição no TiO 2 treliça.
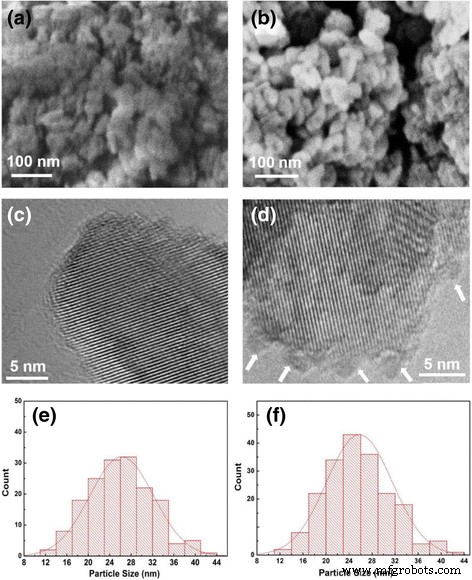
SEM ( a , b ) e HRTEM ( c , d ) imagens de puro P25 e 200 ciclos Co 3 O 4 P25 revestido com pós juntamente com a distribuição de tamanho de partícula ( e , f ) a , c , e Pós P25 puros. b , d , f 200 ciclos Co 3 O 4 -pós P25 revestidos
Além disso, a influência de PEALD Co 3 O 4 na área de superfície específica de P25 também foi examinada. A área de superfície BET é 112,6 e 104,0 m 2 / g para P25 e Co 3 puros O 4 pó P25 revestido, respectivamente, então Co 3 O 4 a deposição em pós de P25 tem um leve efeito na área de superfície específica de P25.
O XPS foi realizado para investigar a composição química das amostras com e sem PEALD 100-cycle Co 3 O 4 Revestimento. Ambas as amostras mostram quase os mesmos sinais para espectros de Ti 2p e O 1s. Na Fig. 3a, o dupleto em 464,6 e 458,9 eV pode ser atribuído a Ti 4+ 2p 1/2 e Ti 4+ 2p 3/2 picos de ligações Ti – O com a energia de divisão da órbita de spin de 5,7 eV, consistente com os valores de TiO 2 . Os espectros de O 1s podem ser deconvoluídos em dois picos, como mostrado na Fig. 3b. O pico forte em 529,9 eV pode ser atribuído à ligação O – Ti. O pico fraco com maior energia de ligação em 532,2 eV é atribuído às espécies OH absorvidas nas superfícies da amostra [44]. O pico O1s de Co 3 O 4 deve localizar-se em ~ 529,8 eV [43], que é difícil de ser distinguido da ligação O – Ti. A razão atômica calculada de Ti:O é de cerca de 1,00:2,13, basicamente consistente com a composição de TiO 2 . No entanto, o sinal de Co de 100 ciclos Co 3 O 4 os pós P25 revestidos são muito fracos para serem detectados. Isso pode ser atribuído ao fato de que o conteúdo de Co pode estar abaixo do limite de detecção de XPS. Portanto, ICP-MS foi utilizado para determinar o teor de Co em P25 puro e Co de 100 ciclos 3 O 4 P25 revestido em pó. Verificou-se que o conteúdo de Co no P25 puro e no Co de 100 ciclos 3 O 4 P25 revestido é 0,13 e 3,63 ppm, respectivamente. Portanto, trace Co 3 O 4 é de fato depositado nos pós P25 por PEALD. Além disso, o XPS também foi usado para analisar Co 3 de 600 ciclos O 4 P25 revestido com amostras preparadas por ALD térmico. Os espectros fracos de Co 2p podem ser reconhecidos com o teor de porcentagem atômica de Co de ~ 0,6%.
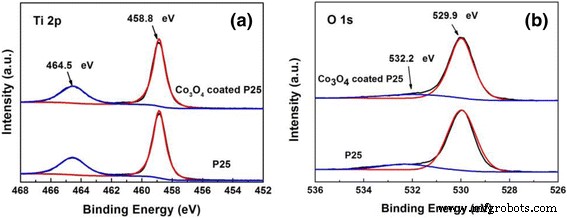
Espectro XPS de 100 ciclos Co 3 O 4 P25 revestido e pós P25 puro. a Ti 2p. b O 1s
A Figura 4a registra os espectros de reflexão difusa de UV-visível à temperatura ambiente de P25 e Co 3 puros O 4 amostras P25 revestidas com 200 e 600 ciclos. P25 puro e Co de 200 ciclos 3 O 4 as amostras P25 revestidas mostram quase os mesmos espectros de absorção óptica, no entanto, 600 ciclos de Co 3 O 4 As amostras P25 revestidas derivadas de ALD térmico exibem absorção relativamente mais forte na faixa visível de 400 a 700 nm, especialmente na região de 400–500 nm, que se origina da transição d-d para Co 3+ ou Co 2+ íons.
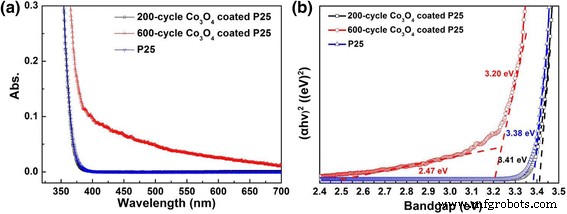
a Espectros de reflexão difusa UV-visível e ( b ) gráficos de determinação de band gaps de P25 puro, 200 ciclos e 600 ciclos de Co 3 O 4 -pós P25 revestidos
Para o semicondutor de bandgap direto, a relação entre a borda de absorção e a energia do fóton ( hν ) pode ser escrito da seguinte forma [45]:
( αhν ) 2 = A ( hν - E g ) onde A é a constante de absorção do semicondutor de gap direto. O coeficiente de absorção (α) é determinado a partir dos espectros de espalhamento e refletância de acordo com a teoria de Kubelka-Munk. As energias diretas do bandgap podem ser estimadas a partir da interceptação das tangentes aos gráficos, conforme apresentado na Fig. 4b. O bandgap de 200 ciclos Co 3 O 4 o pó P25 revestido tem cerca de 3,41 ± 0,02 eV, quase o mesmo que TiO puro 2 pós (3,38 ± 0,02 eV), devido à quantidade de carga de Co extremamente baixa (~ ppm por ICP-MS). Co 3 de seiscentos ciclos O 4 As amostras P25 revestidas mostram dois bandgaps devido ao carregamento de Co relativamente maior (~ 0,6% atômico por XPS). O bandgap maior de 3,20 ± 0,03 eV vem do TiO 2 pós, enquanto o bandgap muito menor de 2,47 ± 0,03 eV pode estar relacionado ao Co 3 O 4 Revestimento. CO derivado de ALD 3 O 4 revestimento tem bandgap ligeiramente maior do que o valor da literatura de 2,3 eV de Co 3 O 4 nanoesferas (~ 20 nm) por síntese baseada em solução [46].
O MB é comumente usado como sonda para avaliação de fotocatalisadores e seu mecanismo de degradação foi bem esclarecido. A Figura 5a-c ilustra a decomposição fotocatalítica de MB sob luz ultravioleta na presença de Co puro de P25, 100 ciclos e 200 ciclos 3 O 4 fotocatalisadores P25 revestidos, respectivamente. A absorção máxima de MB está localizada em 664 nm. A intensidade de absorção diminui com o tempo sob irradiação de luz ultravioleta para todas as amostras, correspondendo à degradação do MB. A Figura 5d traça as curvas de degradação fotocatalítica para todas as amostras. P25 puro e Co 3 O 4 Os pós P25 revestidos podem degradar MB sob luz ultravioleta. Enquanto isso, quase nenhuma degradação do MB é observada na luz ultravioleta sem catalisador, demonstrando que o MB é estável sob a luz ultravioleta. No entanto, 100 ou 200 ciclos Co 3 O 4 os pós P25 revestidos apresentam uma atividade fotocatalítica muito maior em comparação com os pós P25 puros. A eficiência de degradação de Co 3 O 4 O P25 revestido pode atingir quase 100% em 1,5 h, enquanto que o P25 puro é apenas cerca de 80%.
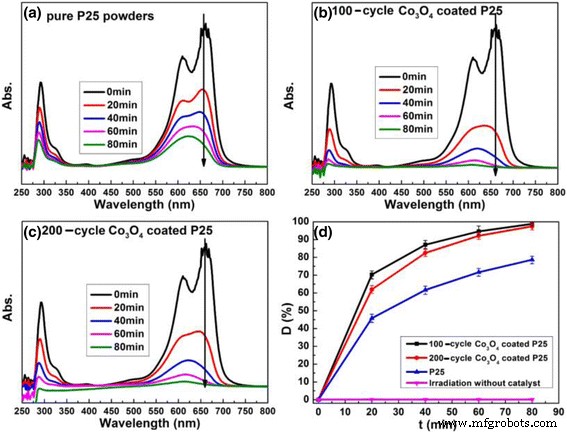
Absorção UV-visível e curvas de degradação da solução MB com vários catalisadores. a P25 puro. b 100 ciclos Co 3 O 4 . c 200 ciclos Co 3 O 4 P25 revestido com catalisador. d Curvas de degradação de MB
Os testes de reciclagem também foram realizados para determinar a estabilidade dos catalisadores compostos de Co 3 O 4 P25 revestido em pó. Nenhuma decadência da eficiência fotocatalítica é observada em 200 ciclos de Co 3 O 4 revestidas com P25 depois de usadas repetidamente na fotodegradação MB por três vezes.
A atividade fotocatalítica aprimorada de Co 3 O 4 Os pós P25 revestidos podem ser atribuídos à formação de junção p-n entre Co 3 O 4 e TiO 2 . A Figura 6 registra os gráficos de Mott-Schottky de P25 com ou sem Co de 200 ciclos 3 O 4 Revestimento. Amostras de P25 puro exibem o gráfico de Mott-Schottky com inclinação positiva, sugerindo o semicondutor do tipo n com portadores de elétrons. O gráfico de Mott-Schottky com inclinação negativa implica o semicondutor do tipo p com portadores de orifício. Para 200 ciclos Co 3 O 4 No catalisador P25 revestido, a coexistência de inclinações positivas e negativas com valores semelhantes no gráfico de Mott-Schottky pode ser observada simultaneamente, indicando a formação da junção p-n em nossas amostras. Isso ajudará na separação dos pares elétron-buraco fotogerados [18, 22, 47].
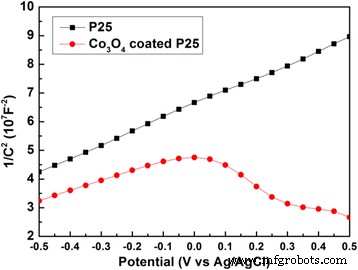
Gráficos de Mott-Schottky de P25 e Co 3 puros O 4 revestido com P25 em solução aquosa de NaOH 1 M com frequências de 1 e 2 kHz no escuro
A Figura 7 ilustra o esquema do nível de energia e do movimento do buraco do elétron em Co 3 O 4 –TiO 2 estrutura de junção p-n. Co 3 O 4 exibe uma lacuna de banda muito menor (~ 2,4 eV) do que TiO 2 (~ 3,4 eV). Após a irradiação de luz ultravioleta, pares elétron-buraco podem ser gerados em ambos Co 3 O 4 e TiO 2 . De acordo com a estrutura do nível de energia na Fig. 7, os elétrons fotogerados se moveriam da banda de condução de Co 3 O 4 ao de TiO 2 . Em contraste, os orifícios são injetados da banda de valência do TiO 2 ao de Co 3 O 4 . Como resultado, uma alta concentração de elétrons e lacunas são formadas na banda de condução de TiO 2 e banda de valência de Co 3 O 4 , respectivamente. A recombinação do par elétron-buraco é efetivamente prejudicada devido à separação de elétrons fotogerados e buracos. Os elétrons e lacunas separados ficam então livres para sofrer reações com os reagentes adsorvidos na superfície do fotocatalisador e aumentar a atividade fotocatalítica. Portanto, o Co 3 O 4 –TiO 2 A estrutura da junção p-n exibe a melhor propriedade fotocatalítica do que o TiO puro 2 .
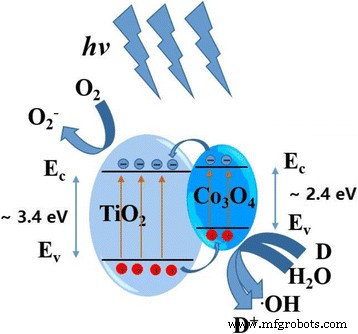
Esquema do nível de energia e movimento do buraco do elétron em Co 3 O 4 –TiO 2 Estrutura de junção p-n sob irradiação de luz ultravioleta
Além disso, para avaliar a influência do ponto isoelétrico (IEP) na absorção de MB, o IEP foi detectado por meio da medição do potencial Zeta, conforme mostrado na Fig. 8. O IEP de MB, P25 puro e 200- ciclo Co 3 O 4 P25 revestido em soluções aquosas são determinados como sendo 5,37, 6,74 e 7,42, respectivamente. O valor de pH do corante MB e P25 ou Co 3 O 4 A suspensão aquosa revestida de P25 é avaliada como 6,68. De acordo com os resultados do IEP, o corante MB carrega carga negativa líquida, enquanto ambos os catalisadores carregam carga positiva. Além disso, Co 3 O 4 os pós P25 revestidos têm mais cargas positivas do que o P25 puro. Portanto, o Co 3 O 4 o revestimento pode promover a adsorção de MB em P25, o que é benéfico para o aumento da atividade fotocatalítica.
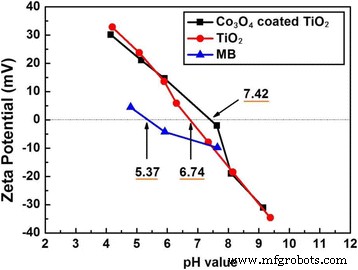
Potencial Zeta de MB, P25 e Co 3 O 4 revestido com P25 em soluções aquosas em função dos valores de pH
Finalmente, o teste de fotodegradação de laranja de metila (MO) usando Co 3 O 4 P25 revestido com pó também foi conduzido sob iluminação de luz visível. Os 200 ciclos Co 3 O 4 A amostra P25 revestida não mostra atividade fotocatalítica para degradação de MO. Pode ser atribuído ao fato de que existe apenas vestígios Co 3 O 4 na superfície P25. O traço Co 3 O 4 não consegue absorver luz visível suficiente para estimular as reações catalíticas. Portanto, preparamos 600 ciclos de Co 3 O 4 - amostra P25 revestida por ALD térmico para introduzir mais Co 3 O 4 nanopartículas em pós P25. A atividade fotocatalítica na decomposição do corante MO foi examinada sob irradiação de luz visível ( λ ≥ 420 nm), conforme registrado na Fig. 9. Seiscentos ciclos de Co 3 O 4 P25 revestido mostra atividade fotocatalítica visível com degradação de ~ 26% MO em 120 min. Isso pode ser explicado considerando o Co 3 O 4 atividade das nanopartículas sob luz visível devido ao seu estreito bandgap (~ 2,4 eV), conforme confirmado pela Fig. 4d [28].
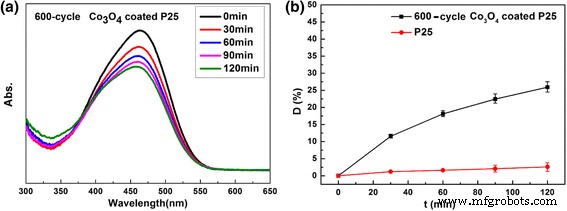
Atividade fotocatalítica visível de 600 ciclos de Co 3 O 4 P25 revestido em pó. a Absorção UV-visível e b curvas de degradação da solução de MO sob irradiação de luz visível
Conclusões
Em resumo, Co 3 O 4 os fotocatalisadores de pó de junção P25 p-n revestidos foram preparados com sucesso por PEALD. A estrutura, morfologia, composição e bandgap destes pós P25 modificados foram caracterizados sistematicamente. A atividade fotocatalítica da degradação do MB sob luz ultravioleta foi explorada profundamente. A estrutura anatase e o tamanho do cristalito dos pós P25 não mudam após 100 e 200 ciclos de Co 3 O 4 deposição. No entanto, sob luz ultravioleta, o Co 3 O 4 os pós P25 revestidos exibem uma taxa de degradação de quase 100% em 1,5 h. A atividade fotocatalítica de UV foi evidentemente melhorada em comparação com os pós P25 puros. Os gráficos de Mott-Schottky de pós fotocatalisadores confirmam a formação da heterojunção p-n em Co 3 O 4 –TiO 2 materiais nanocompósitos, que são benéficos para a separação de pares elétron-buraco fotogerados. Além disso, os resultados do IEP também indicam que o Co 3 O 4 o revestimento pode promover a adsorção de corantes orgânicos de azul de metileno em pós P25. Acima de tudo, ALD é uma tecnologia promissora e poderosa para construir fotocatalisador de junção p-n eficaz por meio de modificação de superfície.
Nanomateriais
- Tecnologias de Deposição de Camada Atômica Avançada para Micro-LEDs e VCSELs
- Em direção aos nanofluidos de TiO2 - Parte 1:Preparação e propriedades
- S, N Co-dopado de grafeno Quantum Dot / TiO2 Compósitos para geração eficiente de hidrogênio fotocatalítico
- Características de chaveamento resistivo bipolar de dispositivos RRAM de estrutura tricamada de HfO2 / TiO2 / HfO2 em substratos revestidos com Pt e TiN fabricados por deposição de camada atômica
- Características interfaciais, elétricas e de alinhamento de banda de pilhas de HfO2 / Ge com camada intermediária de SiO2 formada in situ por deposição de camada atômica aprimorada com plasma
- Alto desempenho fotocatalítico de dois tipos de fotocatalisadores compostos de TiO2 modificados com grafeno
- Características ópticas e elétricas de nanofios de silício preparados por corrosão eletrolítica
- As Nanofibras Hierárquicas de Poliamida 6-ZnO Antibacteriana Fabricadas por Deposição de Camada Atômica e Crescimento Hidrotérmico
- Ajustando as morfologias de superfície e propriedades dos filmes ZnO pelo projeto da camada interfacial
- Ajuste de nível de Fermi de filmes ZnO por meio de deposição de camada atômica superciclada



