Influência da modificação do grupo nas bordas dos pontos quânticos de carbono na emissão fluorescente
Resumo
Apresentamos uma investigação detalhada sobre o efeito da modulação do grupo funcional nas bordas dos pontos quânticos de carbono (CQDs) na fluorescência dos CQDs. Os CQDs anexados pelos elementos N, S e P são sintetizados por meio da pirólise de uma mistura de ácido cítrico e NH 3 H 2 O, H 2 SO 4 , e H 3 PO 4 , respectivamente. Assim, parte de –COOH nas bordas dos CQDs pode ser convertida em –C =O e grupos funcionais como –NH 2 , –SO 2 , –HSO 3 , e –H 2 PO 4 pode se conectar às ligações de carbono. Descobrimos que a formação de N / S / P-CQDs pode reduzir a quantidade de –COOH que se liga às bordas de sp 2 -conjugado π -domínios localizados nos centros desses CQDs. Este efeito pode resultar na redução da recombinação não radiativa para transição eletrônica nestes CQDs. Como resultado, o rendimento quântico (QY) para fluorescência dos CQDs pode ser eficientemente aumentado. Demonstramos experimentalmente que os QYs para N / S / P-CQDs podem atingir até 18,7%, 29,7% e 10,3%, respectivamente, em comparação com 9% para estes sem modulação do grupo funcional. Este trabalho pode fornecer uma abordagem experimental prática no aprimoramento das propriedades ópticas de CQDs fluorescentes.
Histórico
Os pontos quânticos de carbono (CQDs) são nanomateriais emergentes [1] com propriedades fluorescentes superiores [2] e propriedades químicas, eletrônicas e ópticas únicas [3]. Em contraste com as moléculas de corante tradicionais e pontos quânticos baseados em semicondutores, os CQDs não são apenas com boa resistência à luz e resistência ao branqueamento por luz de cintilação [4], mas também com características importantes, como baixa toxicidade, biocompatibilidade, baixo custo, alta fotoestabilidade [5] ], etc. Assim, os CQDs têm sido propostos como materiais eletrônicos e optoeletrônicos avançados para aplicação em áreas como dispositivos optoeletrônicos [6], conversão de energia [7], fotocatálise [8], sensores [9], bioimagem [ 10], marcadores celulares [11, 12] e distribuição de drogas [13], para mencionar apenas alguns. Nos últimos anos, a investigação de CQDs tornou-se um campo de pesquisa quente e de rápido crescimento nas comunidades científicas e industriais.
No momento, o método experimental mais popularmente empregado para a síntese química dos CQDs é via abordagem ascendente, que pode ser aplicada para produzir CQDs fluorescentes de forma simples, barata e em grande escala. Neste método, pequenas moléculas de compostos orgânicos ou polímeros são tomadas como fontes de carbono e são desidratadas e carbonizadas para realizar os CQDs. Durante a preparação dos CQDs, a superfície e a borda dos CQDs são frequentemente fixadas por alguns grupos químicos, como OH, COOH, C =O e assim por diante. A presença desses grupos químicos pode afetar muito as propriedades eletrônicas e ópticas dos CQDs. Em particular, as características fluorescentes dos CQDs dependem sensivelmente da presença desses grupos [14]. Do ponto de vista da física, os grupos químicos ligados à superfície e borda dos CQDs podem induzir novos tipos de superfície e estados de borda nos sistemas CQD e, assim, podem modificar a estrutura eletrônica e os canais de transição eletrônicos e ópticos correspondentes no CQDs. Neste caso, a fotoluminescência (PL) dos CQDs pode ser alcançada via transição eletrônica entre estados de borda e estados de carbono, como conjugado π estados (ou sp 2 área). Assim, o mecanismo de emissão de PL de CQDs é muito semelhante ao da emissão de luz foto-induzida de estados de impureza em um semicondutor dopado [15] da seguinte maneira:(i) os fótons podem ser absorvidos por transições eletrônicas de baixo e estados eletrônicos de carbono ocupados para estados mais altos e vazios sob a ação de bombeamento óptico, (ii) os elétrons fotoexcitados podem ser relaxados nos estados eletrônicos nos estados de borda por meio de eventos de transição eletrônicos não radiativos e (iii) o PL a emissão pode ser alcançada por meio de transições eletrônicas dos estados de borda para os estados eletrônicos de baixo carbono, acompanhadas pela emissão de fótons. Portanto, os estados eletrônicos de borda desempenham um papel como os estados de impureza radiativa em um semicondutor e os elétrons podem ser combinados com os buracos para a luminescência. Geralmente, o sp 2 -conjugado π -domínios são considerados como os centros inerentes para a emissão de PL [16] e os sp aromáticos 2 a área de carbono de um CQD é cercada por sp 3 estados de carbono (C – OH). Portanto, a recombinação de pares de elétron-buraco no sp 2 área e as transições eletrônicas entre o carbono e os estados de borda podem promover a emissão de PL dos CQDs [17, 18].
O rendimento quântico fluorescente (QY) é um parâmetro chave para medir a eficiência da emissão de luz foto-induzida de um material ou dispositivo, que é definida pelo número de fótons emitidos em relação ao número de fótons absorvidos. Nos primeiros anos, quando os CQDs foram descobertos, o QY para os CQDs preparados quimicamente era bastante baixo (até menos de 2%) [1]. Como melhorar o QY fluorescente para CQDs tem sido um problema central para a pesquisa fundamental e para a aplicação de materiais. Em geral, o QY para CQDs realizado quimicamente por meio de uma abordagem ascendente depende da escolha da fonte de carbono, técnica de síntese e modulação de borda. Mais especificamente, a intensidade e frequência da emissão de PL dos CQDs são consequências dos parâmetros de amostra dos CQDs, a presença dos grupos funcionais ou estados de borda, a interação entre os estados eletrônicos em sp 2 -conjugado π -domínios e em grupos químicos, e as propriedades do fluoróforo nos CQDs [19]. Nos últimos anos, o QY fluorescente para CQDs foi amplamente melhorado [20]. Particularmente, Lingam et al. examinaram o efeito dos estados de borda induzidos na síntese de CQDs sobre a emissão de PL. Eles descobriram que se as bordas dos CQDs forem danificadas, a emissão de PL cai drasticamente para ser incomensurável [21]. Um trabalho semelhante de Kumar et al. também demonstrou que a presença de estados de borda é o fator chave para PL de CQDs, e a origem de PL heterogêneo ajustável é amino-funcionalizada para CQDs [22]. Tang et al. relataram uma síntese hidrotérmica simples assistida por microondas dos CQDs usando glicose como única fonte de carbono [23]. Simplesmente estendendo o tempo de reação de 1 min para 9 min, eles puderam ajustar o tamanho dos CQDs de 1,65 nm a 21 nm. Curiosamente, eles descobriram que o PL dos CQDs era independente do tamanho dos CQDs, onde os CQDs com os tamanhos de 9,6 nm e 20 nm mostram aproximadamente os mesmos comportamentos de absorção e emissão de luz. Os resultados obtidos no trabalho de pesquisa posterior de Lin et al. também indicam que a emissão de PL de CQDs depende fracamente do efeito do confinamento quântico do sp 2 -conjugado π -domínios [24] e a presença de grupos funcionais de superfície anexados aos CQDs é o fator chave para a emissão de PL. Dong et al. perceberam os CQDs fluorescentes azuis com as nanofolhas semelhantes a discos (o tamanho de 15 nm e a espessura de 0,5-2,0 nm) ajustando o grau de carbonatação do ácido cítrico. Eles descobriram que o PL dos CQDs é independente do comprimento de onda de excitação e o QY fluorescente pode ser de até 9,0% [25]. Deve-se notar que de acordo com a relação entre o tamanho de um CQD e o comprimento de onda da emissão de PL para um CQD puro [26], os CQDs com o tamanho de cerca de 2,25 nm podem emitir a fluorescência azul, enquanto os CQDs com o tamanho de 15 nm só pode emitir fluorescência de comprimento de onda mais longo. A forte emissão de PL azul de CQDs com tamanho de 15 nm [25] sugere mais uma vez que a presença de estados de borda induzidos por grupos químicos ligados aos CQDs é o principal responsável pela emissão de PL dos CQDs. Portanto, a funcionalidade de borda dos CQDs pode afetar não apenas a fluorescência dos CQDs, mas também as propriedades físicas e químicas dos CQDs em geral [19].
Deve-se notar que, atualmente, a frequência da emissão fluorescente dos CQDs não pode ser facilmente controlada e modificada artificialmente. Além disso, o QY fluorescente correspondente ainda não atingiu os requisitos para a aplicação como dispositivos práticos. Os resultados obtidos em pesquisas experimentais [27,28,29] e teóricas [30, 33] confirmaram que a passivação da borda pode efetivamente melhorar as propriedades ópticas eletrônicas dos CQDs. Os agentes de passivação são amplamente usados para ajustar as propriedades fluorescentes dos CQDs [21,22,23]. Jing Liu et al. desenvolveu uma etapa de preparação de pontos quânticos de carbono dopados com nitrogênio e passivados por superfície [27]. Eles descobriram que o QY dos CQDs sem passivação de superfície é geralmente muito baixo (QY <10%), os CQDs passivados mostram um QY de 37,4%. Um trabalho semelhante de Shen et al. pesquisaram os CQDs passivados por PEG têm um QY de 28% [28], e Kwon et al. relataram que o passivado por hexadecilamina (HDA) produz 19-35% [29]. Dimos e colegas de trabalho também descobriram que a passivação da borda pode efetivamente induzir os elétrons na banda de condução e aumentar a energia da superfície dos CQDs para evitar o decaimento ou extinção da fluorescência causado pela agregação dos CQDs [30]. Além disso, a geração fluorescente de CQDs fabricados via reação química ou abordagem ascendente é principalmente induzida pela presença de grupos funcionais radiativos ou fluoróforo anexados à borda dos CQDs [31]. Quimicamente, esses grupos funcionais podem ser modificados colocando os CQDs em diferentes soluções químicas. A fluorescência desses CQDs quimicamente modificados pode ser obtida através da emissão excitônica acompanhada por recombinação eletrônica e separação de pares elétron-buraco presos na borda dos CQDs [32]. Assim, a frequência da emissão de PL pode ser ajustada por meio da seleção de diferentes grupos de bordas para formar os estados de borda necessários.
A principal motivação deste estudo é explorar como as propriedades fluorescentes dos CQDs podem ser modificadas em diferentes soluções químicas para sua passivação ou funcionalidade de borda. Recentemente, produzimos CQDs a partir de águas residuais de tofu sem adicionar quaisquer substâncias tóxicas e revelamos o mecanismo de luminescência [33]. Descobrimos que cores diferentes da emissão fluorescente desses CQDs podem ser alcançadas colocando esses materiais de ponto em água ou em solução de NaOH [33]. Também fabricamos os CQDs com suco de limão fresco e os aplicamos para imagens celulares [34]. Verificou-se que a presença de grupos contendo oxigênio na superfície e borda dos CQDs é principalmente responsável pela fluorescência dos CQDs [34]. Nossa atenção no presente estudo está focada principalmente em como alcançar uma maneira eficaz de melhorar o rendimento quântico de fluorescência de CQDs.
Método
Síntese de N-, S- e P-CQDs
Neste trabalho, ácido cítrico (C 6 H 8 O 7 , 99,5%), hidróxido de sódio (NaOH, 96%), solução de amônia (NH 3 H 2 O, 25-28%), solução de ácido sulfúrico (H 2 SO 4 , 98%), solução de ácido fosfórico (H 3 PO 4 , 85%) e água deionizada foram usados para fabricar os CQDs e para modificar os estados das bordas.
Os B-CQDs foram sintetizados por pirólise do ácido cítrico como única fonte de carbono. Os N / S / P-CQDs foram fabricados por pirólise de amônia, ácido sulfúrico e ácido fosfórico junto com ácido cítrico, respectivamente. O princípio e os processos experimentais para a realização dos CQDs e N / S / P-CQDs correspondentes são mostrados na Fig. 1. Através da pirólise do ácido cítrico, os B-CQDs podem ser fabricados via desidratação inter-molecular, carbonização e reação de condensação. Esta abordagem pode formar (i) a estrutura aromática (ou seja, o sp 2 estados de carbono com ligações C – C e C =C) com área conjugada como o núcleo dos CQDs, (ii) as bordas dos CQDs anexados por hidroxila (OH) e carboxila (COOH / –O – C =O), e (iii) o sp 3 área de carbono (C – C – OH / –C – O) que pode ser passivada em, por exemplo, solução de NaOH. Os N-CQDs podem ser obtidos através do processo de pirólise da solução mista de ácido cítrico e NH 3 H 2 O. Nesse caso, a reação de desidrogenação entre grupos adjacentes com carboxila pode promover a formação de N pirrólico no esqueleto de grafeno dos CQDs. As bordas dos N-CQDs são então anexadas com grupos químicos extras, como –C – N e –NH 2 [35]. Semelhante à realização dos N-CQDs, S-CQDs e P-CQDs podem ser fabricados por meio da pirólise da solução mista de ácido cítrico e H 2 SO 4 e H 3 PO 4 , respectivamente. A desidratação inter-molecular, carbonização e reação de condensação podem formar o esqueleto de grafeno dos CQDs com a conexão a grupos químicos como –SO 2 , –HSO 3 , e –H 2 PO 4 . Além disso, é provável que os átomos S e P se liguem à borda de sp 2 área de conjugado de carbono para formar os defeitos da borda. As estruturas materiais de N / S / P-CQDs são mostradas na Fig. 1. No presente estudo, N / S / P-CQDs são dispersos em solução de NaOH em temperatura ambiente para torná-los passivados. Assim, podemos converter parte de –COOH na borda dos CQDs em –COONa e reduzir a quantidade de –COOH na borda de sp 2 -conjugado π -domínios. Consequentemente, a modificação do grupo na borda dos CQDs pode ser alcançada.
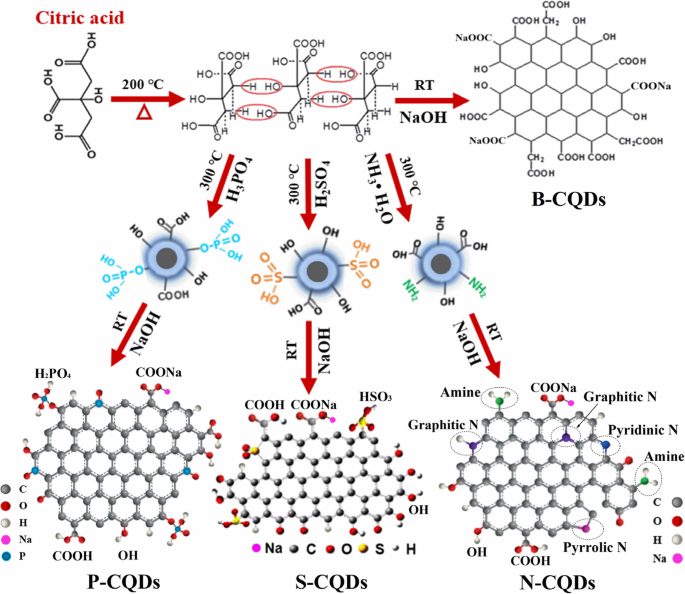
Processos de síntese esquemática de CQDs e estruturas N-, S- e P-CQD correspondentes
Mais especificamente, os N / S / P-CQDs fluorescentes são preparados das seguintes maneiras:(i) 2 g de ácido cítrico analiticamente puro foram adicionados a 60 ml de NH 3 H 2 O (pH =7,5), 60 ml H 2 SO 4 (pH =3), e 60 ml H 3 PO 4 (pH =3), respectivamente. (ii) Colocamos a solução misturada na plataforma de aquecimento para aquecimento constante a 300 ° C, onde o tempo de aquecimento é de 20-30 min. (iii) 50 ml de solução de hidróxido de sódio (NaOH) são adicionados ao copo após o resfriamento natural do copo até a temperatura ambiente. (iv) A mistura é agitada magneticamente por 10 min e submetida a choque ultrassônico por 10 min e posteriormente centrifugada a uma velocidade de 12.000 r / min por 10-30 min. Em seguida, o sobrenadante é tomado, no qual N / S / P-CQDs modificados por soluções de amônia, ácido sulfúrico e ácido fosfórico, respectivamente, e passivado por grupos como –OH, –COOH, –C =O, –COONa, –NH 2 , –SO 2 , –HSO 3 , e –H 2 PO 4 pode ser obtido em soluções de NaOH. Na preparação de N / S / P-CQDs, exceto que os N / S / P-CQDs foram modificados por NH 3 H 2 O, H 2 SO 4 , e H 3 PO 4 , respectivamente, as outras condições experimentais foram aproximadamente as mesmas. Usamos a mesma quantidade de ácido cítrico para dissolver em NH 3 H 2 O, H 2 SO 4 , e H 3 PO 4 , respectivamente, para a pirólise e, em seguida, adicionou a mesma quantidade e igual concentração de solução de hidróxido de sódio quando as substâncias no copo estavam quase secas. Isso pode garantir que a densidade dos CQDs na solução de NaOH seja quase a mesma.
Medições
Neste trabalho, a morfologia e microestrutura dos CQDs foram observadas usando a microscopia eletrônica de transmissão (TEM, JEM 2100) em uma tensão de aceleração de 300 kV. A espectroscopia de fotoelétrons de raios X (XPS) foi aplicada para caracterizar as amostras, utilizando-se o espectrômetro de fotoelétrons PHI5000 Versa Probe II com Al Kα em 1486,6 eV. O espectro de absorção ultravioleta-visível (UV-Vis) dos CQDs foi medido por um espectrofotômetro UV-Vis (Specord200, Alemanha). A emissão de PL dos CQDs foi medida usando um sistema PL padrão (IHR320, Jobin Yvon, EUA) em temperatura ambiente. O QY fluorescente dos CQDs é avaliado com base nos dados de PL.
Resultados e discussões
A caracterização das amostras
A morfologia e as estruturas dos CQDs sintetizados foram investigadas por TEM. A Figura 2 mostra as imagens TEM (a) e as distribuições de diâmetro (b) de S-CQDs. Pode ser visto claramente que os S-CQDs são folhas semelhantes a circulares e estão dispersos uniformemente em solução de NaOH. Por meio de uma média estatística das imagens TEM para os CQDs, descobrimos que a distribuição de tamanho dos S-CQDs está localizada principalmente na faixa de 3-8 nm e o tamanho médio dos CQDs é de cerca de 5,73 nm. Estes resultados são obtidos por análise estatística de mais de 300 partículas CQD usando o Image J Programas. Os resultados mostrados na Fig. 2 c indicam que esses S-CQDs são altamente cristalizados com estrutura típica de rede de carbono. As franjas da rede dos CQDs são claras e o espaçamento da rede correspondente é de cerca de 0,215 nm consistente com a faceta (100) do grafeno [32].
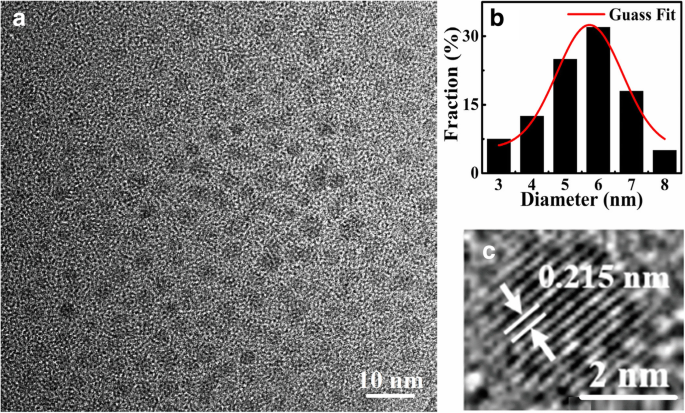
Imagens TEM de S-CQDs em solução de NaOH (pH =12) em a e suas franjas de treliça em c . A distribuição do diâmetro dos S-CQDs é mostrada em b
No presente estudo, aplicamos a espectroscopia de fotoelétrons de raios-X (XPS) para a medição e exame dos grupos funcionais de borda anexados aos CQDs. Usamos lâminas de vidro como substratos e revestimos as amostras nas lâminas de vidro para as medições. Na Fig. 3, mostramos os espectros de XPS para N-, S- e P-CQDs. Como mostrado na Fig. 3a, o espectro XPS de varredura completa para N-CQDs indica que a porcentagem atômica de N1s é de 9,6%. As Figuras 3 bec indicam que (i) os S- e P-CQDs mostram picos de resposta para S2s (em 169 eV) e P2s (em 133 eV), respectivamente, em contraste com CQDs preparados sem modificação de grupo funcional e (ii) as porcentagens atômicas de S2s para S-CQDs e de P2p para P-CQDs são 2,7% e 0,6%, respectivamente. A principal razão para um conteúdo menor de P em P-CQDs do que conteúdo de S em S-CQDs é que P tem um raio atômico relativamente maior (número de prótons de núcleos é 15) do que S (número de prótons de núcleos é 16). Assim, os átomos de P são relativamente menos propensos a serem absorvidos pelas ligações químicas na superfície dos CQDs do que os átomos de S. Em comparação com a Fig. 3 a e c para os espectros de XPS para N- e P-CQDs, a Fig. 3 b mostra que a porcentagem de átomos C1s em S-CQDs é muito maior (76,9%) e as proporções de átomos de O1s ( 20,2%) e átomos de impureza (S, Na) são muito baixos. Esses resultados indicam que há menos defeitos no sp 2 área de carbono em S-CQDs. Mostrado na Fig. 3 d são os espectros de alta resolução de C1s exibem três picos típicos, respectivamente, em 284,8 eV, 286,6 eV e 288,5 eV para N-CQDs, que indicam que o sp 2 a área de carbono (C – C / C =C) tem uma boa estrutura de rede [14, 25, 36]. Além disso, sp 3 carbono (C – O / C – N, 286,4 eV) e carboxila (O – C =O / COOH, 288,1 eV) têm energia de ligação semelhante [33], sugerindo que existem quantidades semelhantes de hidroxila (C – O / C– OH) e carboxila (O – C =O / COOH) em torno do sp 2 área de carbono. Os espectros de alta resolução correspondentes de C1s para S- e P-CQDs são mostrados na Fig. 3 e e f. Conforme mostrado na Fig. 3 e, o pico de sp 3 carbono (C – O) é muito forte e o pico de hidroxila (O – C =O / COOH) é fraco para S-CQDs, indicando que a quantidade de hidroxila (C – O / C – OH) é muito maior do que carboxila (O – C =O / COOH) em torno do sp 2 área de carbono para S-CQDs. Além disso, a Fig. 3 h indica que a quantidade de hidroxila (C – O / C – OH) é menor que a de carboxila (O – C =O / COOH) em torno do sp 2 área de carbono para P-CQDs. Comparando com a Fig. 3 d, e e f, descobrimos que o pico de hidroxilas (C – O / C – OH) é o mais forte, enquanto o pico de hidroxilas (O – C =O / COOH) é o mais fraco para S-CQDs. Quando a quantidade de grupos hidroxila é aumentada, a quantidade de grupos carboxila é reduzida, e vice-versa, quando a quantidade de grupos carboxila é aumentada, a quantidade de grupos hidroxila diminui.
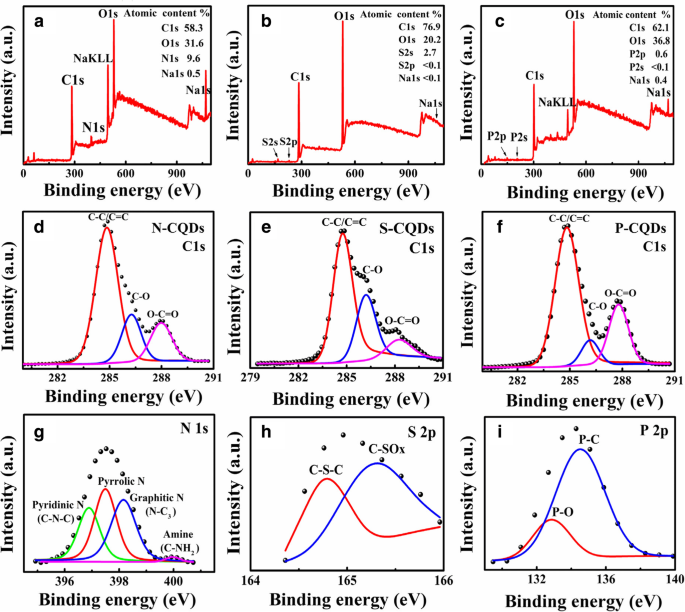
Os espectros de XPS de varredura completa em a / b / c e o espectro de alta resolução de C1s em d / e / f e N1 s / S2p / P2p em g / h / i para, respectivamente, os N / S / P-CQDs
Na Fig. 3 g, os espectros de alta resolução de N1s mostram quatro picos relacionados ao nitrogênio piridínico (N piridínico, 396,9 eV), nitrogênio pirrólico (N pirrólico, 397,6 eV), nitrogênio grafite (N – C 3 , 398,5 eV, localizado no centro de sp 2 carbono) e o grupo amida (C – NH 2 , 399,9 eV, localizado na borda de sp 2 carbono), respectivamente [22, 37,38,39]. Esses resultados verificam a estrutura do material dos N-CQDs mostrados na Fig. 1. Em N-CQDs, os fluoróforos são formados pela hibridização de grupos funcionais de borda, como C – OH e C – NH 2 com sp 2 -conjugado π -domínios [40], que podem desempenhar um papel no aumento da fluorescência de N-CQDs. O espectro de alta resolução de S2s e P2p correspondente aos resultados de XPS para S- e P-CQDs são mostrados na Fig. 3 h e i, isso implica que as bordas de S-CQDs e P-CQDs estão ligadas por algumas ligações químicas, tais como C – S – C (164,8 eV) [41], C – SO X ( X =2, 3, 4, 165,1 eV) [42], P – C (135,0 eV) [43] e P – O (132,7 eV) [44]. Assim, as ligações químicas como C – SO 2 , –HSO 3 , C – P – C, –H 2 PO 4 , etc. podem ser formados nas bordas dos S- e P-CQDs, como mostrado na Fig. 1.
A Fig. 4 mostra os espectros de absorção e emissão medidos a partir do B- e N / S / P-CQDs em soluções de NaOH. Mostrado na Fig. 4a estão os espectros de absorção de UV-Vis de B / N / S / P-CQDs. O espectro de absorção de B-CQDs exibe picos de absorção de UV em 278 nm, enquanto o espectro de absorção de UV-Vis de N-, S- e P-CQDs mostra duas bandas de absorção claras. O pico de absorção em 253 nm é atribuído a π - π * transição da ligação C =C aromática e o ombro em 302 nm corresponde a n - π * transição da ligação C =O [40]. As ligações C =C vêm de sp 2 -domínios conjugados nos núcleos de N / S / P-CQDs, enquanto as ligações C =O se originam dos numerosos grupos contendo oxigênio que retiram elétrons, como grupos carboxila e carbonila existentes nos locais de extremidade de N / S / P-CQDs . Os dois picos de absorção revelam a existência de sp 2 -estruturas conjugadas e grupos funcionais contendo oxigênio (C =O e O – C =O / COOH) em N-, S- e P-CQDs.
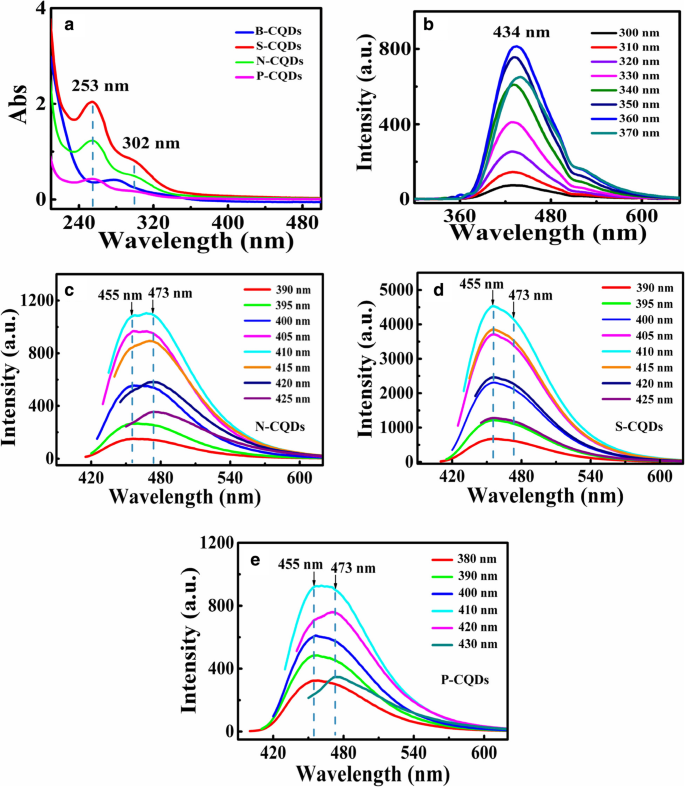
Os espectros de absorção de UV-Vis por B- e N / S / P-CQDs em a . O espectro PL de b B-CQDs, c N-CQDs, d S-CQDs e e P-CQDs com diferentes comprimentos de onda de excitação, conforme indicado. Esses resultados são obtidos em temperatura ambiente
A Figura 4 b – e mostra os espectros PL de B- e N / S / P-CQDs. Como podemos ver, a forte emissão de PL pode ser observada nesses CQDs. Descobrimos que a intensidade da emissão de PL primeiro aumenta e depois diminui com o aumento do comprimento de onda de excitação. Este efeito foi encontrado na maioria dos materiais nanoestruturados (ver, por exemplo, Ref. [45]). Como foi apontado pela Ref. [38], a dependência da intensidade da emissão de PL sobre a excitação para CQDs é originada principalmente devido aos estados de superfície heterogêneos e aos tamanhos e propriedades eletrônicas dos heteroátomos. Para o caso dos CQDs com modulação de grupo de superfície, a presença dos estados de superfície pode alterar o gap e os estados de energia radiativa dos CQDs. Sob excitação de comprimento de onda relativamente mais curto, os elétrons são bombeados para estados de energia mais elevados na banda de condução mais longe dos estados eletrônicos radiativos induzidos pela modulação de superfície. Assim, a possibilidade de emissão de fótons de CQDs é reduzida pela excitação de comprimento de onda mais curto. Ou seja, a intensidade da emissão de PL aumenta com o comprimento de onda de excitação em um regime de comprimento de onda mais curto. Em um regime de comprimento de onda relativamente longo, a excitação de comprimento de onda mais longo implica que relativamente menos elétrons podem ser bombeados para a banda de condução em CQDs. Como resultado, a intensidade da emissão de PL diminui com o aumento do comprimento de onda de excitação em um regime de comprimento de onda de excitação longo. Além disso, as emissões de PL de N / S / P-CQDs consistem em duas bandas espectrais sobrepostas [25]. Os picos duplos PL podem ser medidos respectivamente em cerca de 455 nm e 473 nm por meio de excitação de comprimento de onda de 410 nm. Esta é uma consequência das emissões de PL de N / S / P-CQDs modificados por diferentes grupos funcionais para afetar a recombinação radiativa de pares elétron-buraco (e-h) formados por sp 2 -conjugado π -domínios e grupos de estado de borda [32, 40]. O possível mecanismo proposto aqui é que (i) a fotoexcitação de elétrons em N / S / P-CQDs é obtida via π - π * transições de sp 2 -conjugado π -domínios para n - π * transições, (ii) os elétrons são relaxados de n - π * indica os níveis de energia C =O por meio de canais de transição não radiativos e (iii) a recombinação radiativa para buracos em sp 2 discreto estados relacionados e elétrons em estados de borda podem ser induzidos por grupos funcionais abundantes [46].
Na Fig. 4 b – e, sob as mesmas condições experimentais, descobrimos que a intensidade de fluorescência de N / P / S-CQDs foi significativamente maior do que a de B-CQDs. A intensidade da emissão de PL de S-CQDs é a mais forte, seguida por N-CQDs, e a emissão de PL de P-CQDs é a mais fraca. Esta descoberta corresponde aos resultados mostrados em espectros de alta resolução de C1s para N / S / P-CQDs (ver Fig. 3d, e, f). A intensidade da emissão de PL aumenta com o aumento da altura do pico de C – O (C – OH) e com a diminuição da altura do pico de O – C =O (COOH). Portanto, é razoável acreditar que N / S / P-CQDs com vários grupos de borda, como C – OH, COOH, C =O e C – H, podem induzir diferentes tipos de estados de borda e influenciar a intensidade de seus fotoluminescência. Mais curiosamente, descobrimos que as posições de pico para emissão de PL de N / S / P-CQDs dependem do comprimento de onda de excitação, o que implica que os estados eletrônicos radiativos induzidos por grupos funcionais ligados às bordas dos CQDs são bastante estáveis.
Conforme mencionado acima, sp 2 A área de carbono dos S-CQDs tem menos defeitos, de modo que a emissão de luz inerente dos S-CQDs é a mais forte, em comparação com os N- e P-CQDs. Depois de usar a fórmula para avaliar o rendimento quântico fluorescente [33], obtemos que os QYs para N / S / P-CQDs são 18,7%, 29,7% e 10,3%, respectivamente. Assim, o maior QY pode ser alcançado para S-CQDs, seguido por N- e P-CQDs. Como sabemos, o QY dos CQDs é uma consequência do processo competitivo entre a transição eletrônica radiativa e as armadilhas não radiativas [32]. O hidroxil (C – O / C – OH) nas bordas dos CQDs pode ser hibridizado sinergicamente com estados eletrônicos em sp 2 -conjugado π - domina para formar os fluoróforos, enquanto aqueles carboxil (–COOH) podem desempenhar um papel como centro de recombinação não radiativa na borda dos CQDs [40]. Portanto, o QY dos CQDs é afetado pelos grupos C – O / C – OH e O – C =O / COOH. Além disso, descobrimos que o uso de ácido sulfúrico para modificação dos grupos funcionais na borda de S-CQDs pode afetar significativamente o aumento da emissão de PL de S-CQDs, em comparação com N- e P-CQDs. O QY de 29,7% para S-CQDs, realizado neste estudo, é maior que 18,7% para N-CQDs, 10,3% para P-CQDs e 9% para CQDs [23] preparados sem amônia, ácido sulfúrico ou ácido fosfórico .
Neste trabalho, os N / S / P-CQDs são sintetizados por pirólise dessas misturas de ácido cítrico e NH 3 H 2 O, H 2 SO 4 , e H 3 PO 4 , posteriormente disperso nas soluções de NaOH. Pode promover a desidratação inter-molecular, carbonização e reação de condensação do ácido cítrico. Carboxil (–COOH) nas bordas dos CQDs pode ser convertido em carbonil (–C =O) [19], e as bordas de N / S / P-CQDs podem ser anexadas por grupos químicos como –OH, –COOH , –C =O, –NH 2 , –SO 2 , –HSO 3 , e –H 2 PO 4 . Portanto, a formação de N / S / P-CQDs pode reduzir a quantidade de –COOH anexado às bordas de sp 2 -conjugado π -domínios e pode resultar na redução da recombinação não radiativa [47]. Consequentemente, o QY fluorescente de CQDs pode ser eficientemente aumentado.
Conclusões
Neste estudo, desenvolvemos um método experimental eficaz para aumentar o rendimento quântico fluorescente de CQDs. N / S / P-CQDs foram sintetizados por pirólise de ácido cítrico e usando, respectivamente, amônia, ácido sulfúrico e ácido fosfórico para modificações de grupo de borda. Os resultados mostraram que a presença de grupos funcionais de borda pode desempenhar um papel significativo na geração e no aumento da fluorescência desses CQDs. Especialmente, os grupos hidroxila (C – O / C – OH) nas bordas de sp 2 -conjugado π -domínios podem afetar significativamente os rendimentos quânticos fluorescentes dos CQDs. No entanto, a ligação de grupos carboxila (O – C =O / –COOH) às bordas de sp 2 -conjugado π -domínios leva principalmente a centros de recombinação não radiativa, o que pode enfraquecer a emissão de PL dos CQDs. No presente estudo, os QYs para N / S / P-CQDs podem atingir até 18,7%, 29,7% e 10,3%, respectivamente. Esses valores são muito maiores do que 9% para CQDs preparados sem modificação do grupo funcional. A conclusão mais importante que tiramos deste estudo é que a modificação do grupo nas bordas dos CQDs por ácido sulfúrico pode afetar fortemente a emissão de fluorescência e QY dos CQDs.
Disponibilidade de dados e materiais
Os conjuntos de dados gerados durante e / ou analisados durante o estudo atual estão disponíveis nos autores correspondentes mediante solicitação razoável.
Abreviações
- CQDs:
-
Pontos quânticos de carbono
- PL:
-
Fotoluminescência
- QY:
-
Rendimento quântico
- TEM:
-
Microscopia eletrônica de transmissão
- UV-Vis:
-
Ultravioleta visível
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- XRD:
-
Difração de raios X
Nanomateriais
- Nanotubos de carbono ultrapassam o limite da eletrônica flexível
- Carbono oceânico gerado na escala atômica
- Custo da fibra de carbono:fatores que mais influenciam
- N, N-Dimetilformamida regulando a fluorescência de pontos quânticos MXene para a determinação sensível de Fe3 +
- Revelando a estrutura atômica e eletrônica das nanofibras de carbono de copo empilhado
- O Projeto da Camada de Emissão para Multiplicadores de Elétrons
- Síntese de pontos quânticos de carbono co-dopados com N, S ricos em piridínicos como imitações de enzimas eficazes
- Pontos quânticos de bismuto em poços quânticos de GaAsBi / AlAs recozidos
- Defeitos na superfície do nanofósforo MgAl2O4 dopado com Ti
- Uma abordagem simples para sintetizar pontos quânticos de carbono fluorescentes de águas residuais de Tofu



