Nova detecção por fluorescência de imunossensor do fragmento de citoqueratina-19 do marcador tumoral (CYFRA 21-1) por meio de pontos quânticos de carbono / nanocompósito de óxido de zinco
Resumo
A detecção rápida do câncer de pulmão em estágios iniciais utilizando o fragmento do antígeno citoqueratina-19 (CYFRA 21-1) como marcador tumoral no soro humano desempenha um papel importante na sobrevida dos pacientes e na realização de uma rápida reação cirúrgica. Este estudo teve como objetivo empregar o nanocompósito de óxido de zinco conjugado com pontos quânticos de carbono sintetizado como uma solução imunossensora de fluorescência altamente sensível para a determinação rápida do antígeno CYFRA 21-1 em soro humano. O método sugerido foi conduzido aplicando um método hidrotérmico para preparar pontos quânticos de carbono usando limão cítrico pericarpo. Os pontos quânticos de carbono formados foram usados na redução e estabilização do acetato de zinco para sintetizar nanocompósitos de pontos quânticos de carbono-óxido de zinco. Para formar um sistema imunossensível de anticorpo-antígeno-anticorpo de cobertura sanduíche, um antígeno CYFRA 21-1 foi capturado imobilizando um anticorpo monoclonal não conjugado BM 19.21 na superfície de pontos quânticos de carbono-nanocompósito de óxido de zinco e outro anticorpo monoclonal KS 19.1, que foi revestido na superfície do poço de microtitulação. Este sistema possui um recurso sintonizável de fluorescência registrado na excitação e emissão de λ ex =470 e λ em =520 nm, respectivamente. O sistema imunossensível de fluorescência nanocompósito sugerido exibiu uma relação linear de 0,01–100 ng mL −1 com um limite de detecção de 0,008 ng mL −1 . O sistema de imunossensor sugerido com base em nanocompósitos de óxido de zinco de pontos quânticos de carbono fornece uma abordagem promissora para diagnósticos rápidos de câncer de pulmão pela detecção de CYFRA 21-1 em soro humano.
Introdução
O câncer de pulmão é o tipo de câncer mais público e agressivo, com grandes desafios no tratamento médico. A recorrência tumoral e metástases são consideradas as principais causas de morte em pacientes com câncer de pulmão [1]. O fragmento de citoqueratina 19 do marcador tumoral (CYFRA 21-1) é um fragmento que existe em muitas células epiteliais normais e também malignas [2]. Ele pode ser estimado usando um ensaio imunorradiométrico em sanduíche. Os primeiros estudos esclareceram que nos estágios malignos do câncer de pulmão, o CYFRA 21-1 é liberado na circulação sanguínea dos pacientes e elevado em seu soro [3]. Portanto, é possível melhorar a sobrevida dos pacientes com câncer de pulmão pela detecção precoce e, consequentemente, rápida reação cirúrgica [4].
Poucas técnicas foram relatadas anteriormente para a detecção de CYFRA 21-1, incluindo imunoensaio enzimático [5], imunoensaio eletroquimioluminescente [6] e ensaio imunorradiométrico [7] . Uma estratégia vantajosa para aumentar e melhorar a sensibilidade do CYFRA 21-1 no soro humano ainda é uma preocupação.
Nos últimos anos, grandes progressos e crescimento explosivo da nanotecnologia foram alcançados em quase todos os campos de vida [8]. Entre esses campos estão os sistemas de entrega de drogas [9], análise farmacêutica [10], reações de atividade catalítica [11], aplicações medicinais [12], marcadores de tumor de câncer [13] e imagens de tecidos [14].
Hoje em dia, as técnicas de detecção baseadas em fluorescência (FL) têm atraído muitos pesquisadores devido ao seu design simples e excelente sensibilidade. Vários materiais sensoriais FL foram projetados e sintetizados para monitoramento biológico. Os sistemas FL para determinação biológica são altamente luminescentes, dispersíveis em água, quimicamente estáveis e não tóxicos [15]. Existem várias sondas imunossensíveis baseadas em fluorescência para detecção de biomarcadores. O ensaio competitivo heterogêneo é conduzido imobilizando moléculas de captura na superfície e, em seguida, incubado com biomarcadores conjugados com fluoróforo. A competição entre os biomarcadores livres e conjugados pela ligação às moléculas de captura diminui a intensidade da fluorescência com a concentração do biomarcador [16]. O ensaio sanduíche heterogêneo é baseado na incubação de moléculas de captura e solução de interesse formando um complexo com biomarcadores. Consequentemente, a intensidade da fluorescência aumenta com a concentração do biomarcador [17].
No ensaio competitivo homogêneo, duas moléculas de captura conjugadas com fluoróforo A diferentes conjugadas com biomarcadores conjugados com fluoróforo B e a solução aumentando a fluorescência com concentrações de biomarcadores [18]. No entanto, essas técnicas mostraram certas desvantagens, incluindo seu longo tempo experimental, falta de detecção multiplexada, complexidade e, às vezes, resultados relativamente falsos. O avanço na nanotecnologia permitiu aos pesquisadores desenvolver novas sondas de imunossensibilidade de fluorescência com características ópticas únicas [19]. Desde o primeiro uso de pontos quânticos na detecção de biomoléculas, eles ganharam um grande interesse, pois suas características ópticas fornecem alta flexibilidade na seleção do comprimento de onda adequado, excelentes rótulos para detecção multiplexada, biocompatibilidade e capacidade de direcionamento [20].
Os pontos quânticos de carbono (CQDs) demonstraram excelentes propriedades químicas, físicas, ópticas, magnéticas e elétricas. Os CQDs podem ser sintetizados usando diferentes técnicas, incluindo hidrotermal, eletro-oxidação, ablação a laser e métodos de microondas [21,22,23,24]. Devido às suas características de baixa toxicidade, os pesquisadores científicos consideraram os CQDs como candidatos poderosos em muitas sondas fluorescentes. Além disso, eles têm uma forte capacidade de manipulação por meio de diferentes reações químicas controláveis em várias demandas, como bioquímica, fotoquímica, biossensor, bioimagem e sistemas de entrega de drogas [25,26,27], bem como na detecção de imunoensaios [28]. Estudos anteriores sobre a síntese de CQDs revelaram certas desvantagens pelo uso de fontes de carbono caras, produtos químicos tóxicos e reagentes, ou usando processos não seletivos [29]. Para restringir essas desvantagens, os pesquisadores começaram a usar sucos de frutas como uma nova e barata fonte de carbono [30]. Uma vez que o uso de sucos de frutas não fornece o objetivo ideal de utilização de recursos, CQDs fluorescentes foram recentemente obtidos de cascas de frutas [31]. O uso de cascas de frutas fornece uma rota promissora para a síntese ecológica e verde de CQDs.
O óxido de zinco (ZnO) é um dos mais importantes óxidos metálicos potencialmente ativos, estáveis e de baixa toxidade, amplamente utilizado em dispositivos de laser ultravioleta, campo biomédico, vários tipos de sensores e fotocatálise [32,33,34,35]. Nanopartículas de ZnO (ZnONPs) exibiram propriedades fotoluminescentes próximas às faixas de espectro de UV e Vis. Isso pode ser atribuído à emissão excitônica que é baseada na recombinação direta de pares elétron-buraco [36] ou devido à emissão verde-amarela em 520 nm como resultado da transição eletrônica da borda da banda de condução para um nível de armadilha [37].
Geralmente, os pontos de carbono são nanopartículas quase esféricas amorfas ou nanocristalinas contendo sp 2 e sp 3 carbono, grupos baseados em O / N e grupos químicos pós-modificados. Além disso, CQDs têm a capacidade de excitar com comprimentos de onda mais elevados e podem alterar a eficácia das superfícies combinadas dos pares elétron-buraco e trata a extinção nos sistemas analisados, o que pode facilitar a determinação quantitativa de biomoléculas [38]. Eles podem ser decorados com óxidos de metal, como TiO 2 e ZnO para formar nanocompósitos opticamente ativos que podem ser explorados na detecção de biomarcadores em soro humano. O ZnO é um material de largo band gap (3,37 eV), que pode ser luminescente nas regiões de UV e azul da luz visível devido à presença de uma grande densidade de níveis de defeito no band gap [39]. A formação de nanocompósitos CQDs / ZnO aumenta a absorção de luz visível devido à hibridização de ZnO com CQDs, e o desvio para o azul na absorção de luminescência para 520 nm pode ser atribuído à recombinação radiativa de vacâncias de O ionizado. Além do aumento na absorção de luz visível, uma melhor separação elétron-buraco e redução do tempo de transferência de elétron interfacial podem ser consideradas para o maior desempenho óptico dos CQDs hibridizados com nanopartículas de ZnO [40]. Além disso, o aumento significativo de radicais –OH *, gerado a partir do nanocompósito CQDs / ZnO na interface de água, pode causar uma elevação significativa nos sinais de fluorescência do sistema de análise. Assim, o nanocompósito CQDs / ZnO combinado aumenta a modificação das propriedades optoeletrônicas e fotoluminescência da superfície de ZnO e produz um defeito de superfície forte com fotoluminescência ajustável [41]. Além disso, os CQDs imobilizados com anticorpos de bio-reconhecimento que formam o sistema de detecção de FL de anticorpo-antígeno-anticorpo fornecem uma sonda viável com alta especificidade e sensibilidade para o analito alvo [42].
O estudo sugerido propôs um novo sistema de detecção de fluorescência de imunoensaio simples e ultrassensível baseado em CQDs decorados com nanocompósito de ZnO para determinar o marcador de tumor CYFRA 21-1 em soro humano. Pericarpo de limão cítrico foi empregado como um precursor de carbono para derivar CQDs usando condições hidrotérmicas. Além disso, foi utilizado como agente redutor e estabilizador para a síntese de nanocompósitos de ZnO conjugados com CQDs. O nanocompósito CQDs / ZnO preparado foi imobilizado por um anticorpo monoclonal BM 19.21 não conjugado (mAb) e os poços de microtitulação foram revestidos com outro anticorpo monoclonal KS 19.1 para formar um sistema imunossensível de cobertura em sanduíche.
Métodos
Instrumentos
Os espectros espectrofotométricos de ambos os CQDs e também do nanocompósito CQDs / ZnO foram registrados usando um espectrofotômetro Ultrospec 2100-Biochrom (Biochrom Ltd., Cambium, Cambridge, UK). A morfologia da superfície e a distribuição do tamanho de partícula dos CQDs verdes sintetizados e do nanocompósito CQDS / Zn foram avaliadas usando um microscópio eletrônico de transmissão (TEM) JEOL 1200EX modelo de instrumento (JEOL Ltd., Freising, Alemanha) e microscópio eletrônico de varredura (SEM) modelo JSM-7610F (JEOL, EUA). Os espectros de fluorescência e infravermelho de transformada de Fourier (FT-IR) do sistema de imunossensibilidade sugerido foram verificados usando o leitor multimodo Biotek Synergy H1 (Biotek, Tóquio, Japão) e espectrofotômetro Perkin Elmer FT-IR (PerkinElmer Ltd., Yokohama, Japão) , respectivamente. Os espectros Raman, espectroscopia de fotoelétrons de raios-X (XPS) e difração de raios-X em pó (XRD) foram medidos usando espectrômetro micro-Raman (CRAIC Technologies, CA, EUA), sistema de espectroscopia de raios-X Kratos Axis Ultra (Kratos Analytical Ltd. , Manchester, Reino Unido) e difratômetro Siemens D-5000 (Siemens, Erfurt, Alemanha), respectivamente.
Produtos Químicos e Reagentes
O instrumento SG-2000-10090 (Barsbuttel, Alemanha) foi usado para adquirir a água desionizada usada em todos os experimentos. Os anticorpos monoclonais não conjugados CYFRA 21-1 (mAb) BM 19.21 e KS 19.1 para formar o sistema de imunossensibilidade de cobertura em sanduíche foram obtidos da Abcam (Cambridge, UK). Limão cítrico as frutas eram fornecidas pelos mercados locais. A solução salina tamponada com fosfato (PBS) de pH =7,4 foi preparada usando cloreto de sódio, cloreto de potássio, hidróxido de sódio, fosfato monopotássico e fosfato dissódico (BHD Ltd. Co. Poole, Reino Unido). Randox Laboratories (Northern Ireland-UK) gentilmente forneceu os soros normais comerciais. Amostras de sangue aleatórias foram coletadas de voluntários saudáveis e, antes do início deste estudo, foi obtido um consentimento informado. Além disso, a Sigma-Aldrich (Hamburgo, Alemanha) forneceu um grau puro de cloridrato de carbodiimida (EDC) e N-hidroxissuccinimida (NHS). O comitê de ética em pesquisa da King Saud University, KSA (KSU-REC-002-E, 2019) aprovou o estudo.
Preparação hidrotérmica verde de pontos quânticos de carbono (CQDs)
Limão cítrico pericarpo foi empregado para sintetizar CQDs em condições hidrotérmicas. Aproximadamente 20 g de limão cítrico pericarpo e 200 mL de água desionizada foram transferidos para um frasco redondo e refluxados a 100 ° C sob agitação magnética contínua por 6 h. Após resfriamento à temperatura ambiente, o extrato resultante foi centrifugado a 3500 rpm e 20 mL da solução extraída superior foi autoclavado e aquecido em condições hidrotérmicas na faixa de temperatura de 100 a 200 ° C por diferentes intervalos de 6-120 h. Após o resfriamento à temperatura ambiente, o licor superior representa os CQDs (Esquema 1).
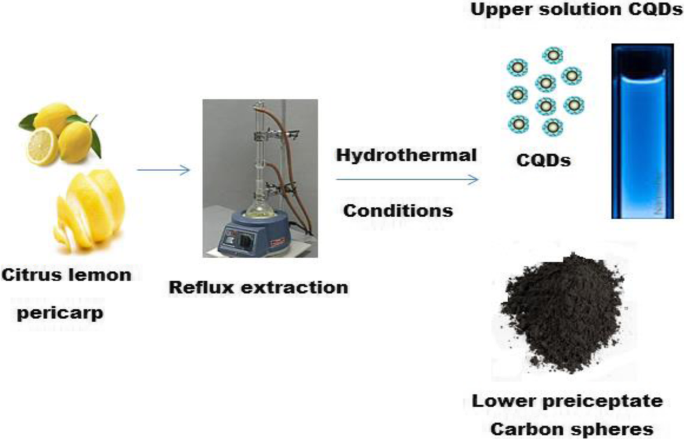
Síntese verde de CQDs usando limão cítrico pericarpo para solução fluorescente CQD e esferas de carbono
Preparação de nanocompósitos de pontos quânticos de carbono-óxido de zinco
Para preparar o nanocompósito CQDs / ZnO, uma reação de redução química simples foi realizada usando CQDs como um agente de redução e estabilização. Nanocompósito CQDs / ZnO foi obtido pela adição de 20 mL dos CQDs a 50 mL de 5,0 × 10 −2 mol L −1 de acetato de zinco a 60 ° C sob agitação contínua durante 10 min. Quando a cor da mistura mudou de amarelado para cremoso, a mistura foi deixada de lado por 30 min para completar o processo de redução e armazenada a 4 ° C. Para garantir a estabilidade e verificar a aglomeração dos nanocompósitos CQDs / ZnO preparados, a espectrometria UV-Vis foi empregada para registrar a absorbância em 20 dias a 390 nm. Os resultados dos resultados revelaram alta estabilidade e nenhuma mudança significativa na absorbância do nanocompósito CQDs / ZnO.
Caracterização de pontos quânticos de carbono-nanocompósito de óxido de zinco
Para garantir a formação do nanocompósito CQDs / ZnO, diferentes técnicas microscópicas e espectroscópicas foram utilizadas. A uniformidade e a morfologia da superfície dos nanocompósitos CQDs e CQDs / ZnO foram estudadas usando microscópio eletrônico de transmissão de alta resolução (HRTEM) e MEV. Os espectros ópticos foram estudados usando espectroscopia UV-Vis, FT-IR, XPS e Raman. A estrutura cristalina dos CQDs preparados foi avaliada usando o padrão de XRD.
Processo de imobilização
Um anticorpo monoclonal BM 19.21 não conjugado foi imobilizado na superfície do nanocompósito CQDs / ZnO sintetizado por uma ligação amida peptídica simples entre a amina e os grupos carboxílicos ativos. O processo de imobilização foi conduzido adicionando 5,0 mL de cada equimolar 3,0 × 10 −3 mol L −1 NHS e EDC para 5,0 mL de solução de nanocompósito CQDs / ZnO sob agitação contínua por 1 h. Aproximadamente 5 mg de anticorpo monoclonal BM 19.21 não conjugado foi dissolvido em 1,0 mL de 0,01 mol L −1 solução salina tamponada com fosfato (pH =7,4) e adicionada à solução de detecção acima. O anticorpo monoclonal BM 19.21 não conjugado foi imobilizado na superfície de uma solução de nanocompósito CQDs / ZnO após incubação a 37 ° C por 12 h (Esquema 2). A espectrofotometria foi utilizada para confirmar o sucesso do processo de imobilização.
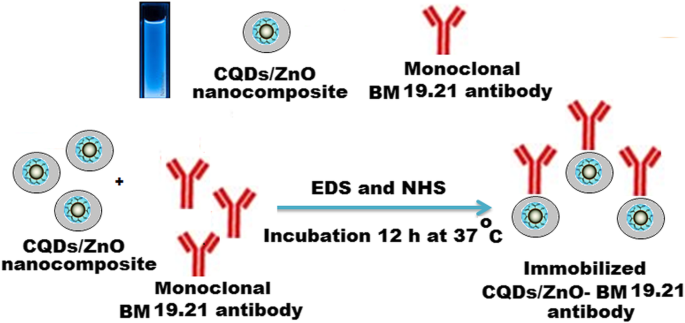
Imobilização do anticorpo monoclonal BM 19.21 na superfície do nanocompósito CQDs / ZnO
Princípio geral do método de imunoensaio
Uma reação de capeamento em sanduíche anticorpo-antígeno-anticorpo foi obtida usando outro anticorpo monoclonal KS 19.1 revestindo a superfície de poços de microtitulação (Esquema 3). Em condições ideais de imunoensaio, a concentração do antígeno CYFRA 21-1 foi determinada em função de um aumento na intensidade do sinal de fluorescência.
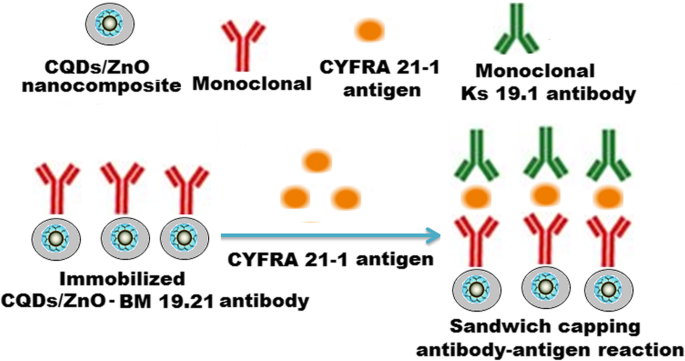
Esquema ilustrado representa uma reação de imunossensibilidade de capeamento de sanduíche anticorpo-antígeno-anticorpo
O procedimento de imunossensibilidade
A coleta de amostras de soros humanos foi fornecida por voluntários aleatórios. A coagulação completa foi assegurada antes da centrifugação à temperatura ambiente e armazenada a 4 ° C. A técnica de spiking foi usada para preparar amostras padrão contendo antígeno CYFRA 21-1 na faixa de concentração de 0,01–500 ng mL −1 . Aproximadamente 50 μL das amostras enriquecidas foram dispensados em poços de microtitulação e misturados com 50 μL de anticorpo monoclonal KS 19.1 recém diluído usando solução salina tamponada com fosfato de pH =7,4 por 30 min e depois incubados sem cobrir a placa por 1 h a 37 ° C. O conteúdo dos poços foi agitado vigorosamente e os poços foram enxaguados três vezes com água desionizada (300 μL) para cada poço. Aproximadamente 50 μL da solução de nanocompósito CQDs / ZnO-BM 19.21 imobilizado foi adicionado a cada poço, suavemente misturado e incubado por 30 min a 37 ° C. As amostras preparadas foram submetidas à análise de fluorescência em leitor de microtitulação para registro das intensidades.
Resultados e discussão
Avaliação morfológica de pontos quânticos de carbono e seu nanocompósito
Um microscópio eletrônico de transmissão (TEM) foi usado para caracterizar a morfologia da superfície e a distribuição dos CQDs nas amostras. Para realizar o exame sob TEM, aproximadamente 4 μL da suspensão de CQDs preparada foi descartada na superfície da grade de carbono de TEM. Na imagem HRTEM (Fig. 1a), os pontos pretos uniformes observados com espaçamento de rede (0,36 nm) indicaram a formação de CQDs. Um gráfico de distribuição de tamanho de partícula foi traçado e o tamanho médio de partícula variou de 1,5 ± 0,5 a 5,0 ± 0,5 nm (Fig. 1b). O tamanho de partícula obtido provou que os CQDs formados são de fato os nanomateriais de tamanho quântico. Além disso, um espalhamento dinâmico de luz (DLS) foi realizado, e o tamanho médio de partícula foi de ~ 20 ± 0,2 nm. Foi observada uma diferença entre as duas medições anteriores. Estudos anteriores revelaram que HRTEM não mostra a estrutura de rede cristalina dos CQDs formados em ampliações maiores devido à sua natureza amorfa [43]. Da mesma forma, neste estudo, o precursor natural do carbono é o limão cítrico pericarpo e os CQDs derivados também exibiram natureza amorfa. Portanto, a diferença nas medições de tamanho de partícula pode ser atribuída à aglomeração dos CQDs formados, à natureza amorfa dos pontos de carbono formados, ao mecanismo envolvido em cada experimento e à dinâmica de hidratação das partículas.
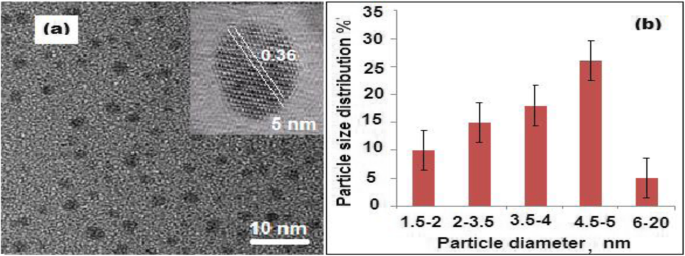
a Imagem de microscópio eletrônico de transmissão de alta resolução (HRTEM) de CQDs com diâmetro de 5 nm e b gráfico de distribuição de tamanho dos CQDs com base no TEM
O nanocompósito CQDs / ZnO preparado foi investigado usando TEM e SEM. Na imagem TEM (Fig. 2a), a presença de partículas hexagonais ligadas a CQDs indicou a formação de nanocompósitos CQDs / ZnO. No MEV, a amostra do nanocompósito foi revestida com ouro para evitar a absorção de elétrons pela amostra e o acúmulo de carga. A tensão acelerada aplicada foi de 15 kV com ampliação de 30.000 × (Fig. 2b).

a e b representam o microscópio eletrônico de transmissão e as imagens do microscópio eletrônico de varredura do nanocompósito CQDs / ZnO
Os espectros de UV-Vis e fluorescência de CQDs foram estudados, e os espectros registrados mostraram dois picos significativos a 224 e 280 nm que podem ser atribuídos a p ~ p * e n ~ P * transição de C =C e C =O, respectivamente. Além disso, o espectro de fluorescência de CQDs exibiu dois sinais no máximo λ ex =360 e λ em =453 nm (Fig. 3a, b). Além disso, o espectro UV-Vis do nanocompósito CQDs / ZnO foi estudado. Um pico de absorção significativo foi observado em 370 nm exibindo desvio para o azul e verde (Fig. 4a). As propriedades de fotoluminescência (PL) dos nanocompósitos CQDs / ZnO foram estudadas. O tamanho e os defeitos de superfície dos CQDs afetam muito suas propriedades de luminescência. Em função do comprimento de onda de excitação, a emissão (PL) dos CQDs foi variada [38]. Além disso, as partículas nanométricas de ZnO exibiram uma emissão relacionada ao defeito na região visível de absorção de azul a verde [41]. Portanto, ZnONPs decorados com CQD produziram um excelente nanocompósito para emissão de PL. Como mostrado na Fig. 4b, o espectro de PL de CQDs / ZnO exibiu um desvio para o azul com um pico significativo a 520 nm após comprimento de onda de excitação 470 nm. O deslocamento observado pode ser atribuído à sobreposição entre as bandas de energia de CQDs e ZnONPs. O deslocamento para o azul exibido estava no nível de emissão de defeito 2,1 eV.
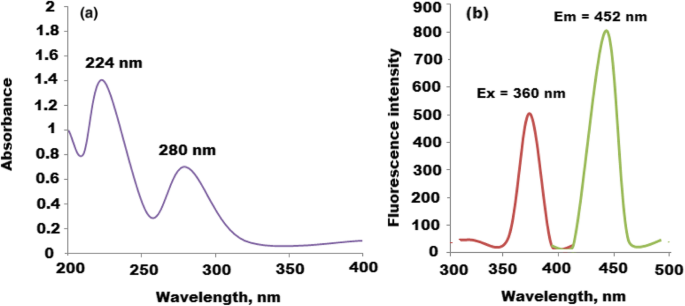
Espectros espectroscópicos de CQDs ( a ) Espectro UV-Vis a 224 e 280 nm e ( b ) espectro de fluorescência de CQDs em λ ex =360 e λ em =452 nm
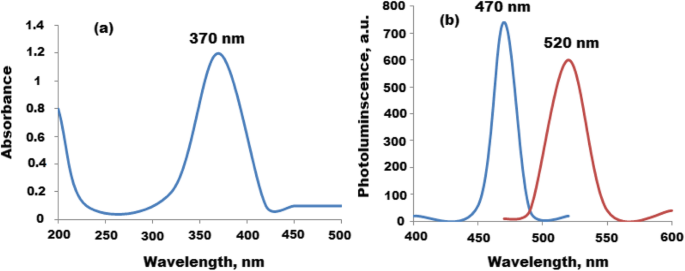
Espectros espectroscópicos de CQDs / ZnONPs a Espectro UV-Vis no pico de absorção em 370 nm e b espectro de fotoluminescência de CQDs / ZnONPs em λ ex =470 e λ em =520 nm
Para confirmar a formação do nanocompósito CQDs / ZnO e do nanocompósito CQDs / ZnO imobilizado com o anticorpo monoclonal BM 19.21 não conjugado, foi realizado um estudo comparativo de FT-IR. O espectro FT-IR registrado de CQDs revelou a presença de diferentes picos distintos correspondentes a certos grupos funcionais, incluindo alongamento de picos vibracionais a 3462 cm −1 e 2932 cm −1 para os grupos C – OH e C – H, respectivamente. Além disso, três bandas de absorção de vibração foram observadas em 1749 cm −1 , 1375 cm −1 e 1246 cm −1 correspondendo à presença de grupos funcionais C =O, C – N e C – O – C, respectivamente (Fig. 5a). Um novo pico em 436 cm −1 correspondente a uma banda de vibração de alongamento de Zn – O foi observada. As propriedades de redução e estabilização dos CQDs foram obtidas com a presença de grupos –OH e COOH em sua superfície. Esses grupos funcionais atuam como doadores de elétrons e possuem forte afinidade para a formação de nanocompósitos CQDs / ZnO. Portanto, os CQDs reduziram e estabilizaram o nanocompósito formado (Fig. 5b). Conforme representado na Fig. 5c, foi notado que dois novos picos foram formados a 3254 cm −1 e 1675 cm −1 . Esses picos foram atribuídos ao alongamento da vibração de N – H e C =O, respectivamente, e confirmando a imobilização de CQDs / ZnO-BM 19,21 por meio de ligações peptídicas.
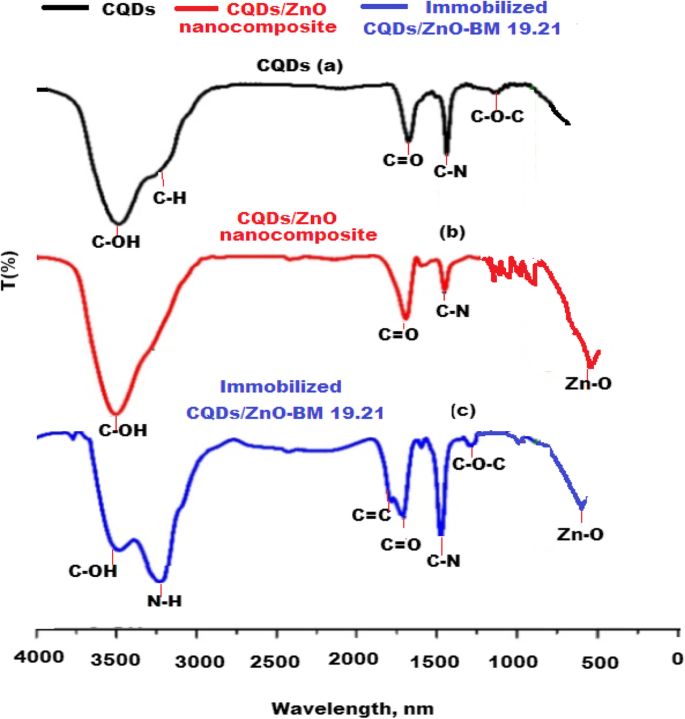
Espectros FT-IR de a CQDs, b Nanocompósito CQDs / ZnO e c nanocompósito CQDs / ZnO-BM 19.21 imobilizado
Os espectros de espectroscopia de fotoelétrons de raios-X (XPS) dos CQDs verdes sintetizados foram examinados. O espectro de CQDs obtido (Fig. 6a) mostrou diferentes grupos funcionais em 288 e 286 eV para C =O e COOH, respectivamente. Além disso, dois picos de energia de ligação significativos foram observados em 1044,4 e 1021,5 eV para Zn 2p 1/2 e Zn 2p 3/2 , respectivamente (Fig. 6b). Além disso, o espectro XPS de alta resolução do nanocompósito CQDs / ZnO confirmou a presença de diferentes picos de energia de ligação em 560, 385, 350, 246 e 200 eV para O 1s, C 1s, Zn 3s, Zn 3p e Zn 3d, respectivamente (Fig. 6c). Todos os dados mencionados anteriormente comprovaram a presença de ZnO na superfície de CQDs formando nanocompósitos de CQDs / ZnO.
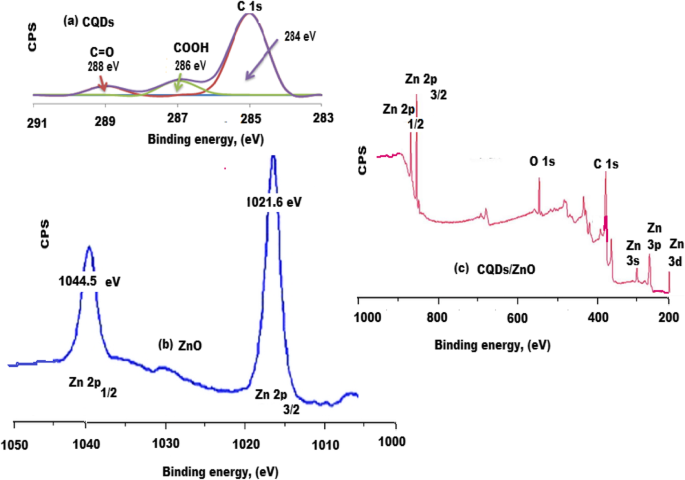
Espectroscopia de fotoelétrons de raios-X (XPS) de a CQDs, b ZnO e c Nanocompósito CQDs / ZnO
Um estudo comparativo entre os padrões de XRD de CQDs e nanocompósitos CQDs / ZnO foi realizado. Um pico largo a 20 ° (2Ɵ) para pontos de carbono foi observado no padrão de XRD de CQDs (Fig. 7a). No entanto, diferentes picos agudos foram reconhecidos em 27 °, 32 °, 34 °, 45 °, 57 °, 64 °, 67 °, 70 °, 73 °, 78 ° e 80 ° (2Ɵ) para Zn (100), (002), (101), (102), (110), (103), (200), (112), (201), (004) e (202), respectivamente. Os picos observados refletiram a distribuição de ZnO na superfície de CQDs formando nanocompósitos de CQDs / ZnO (Fig. 7b).
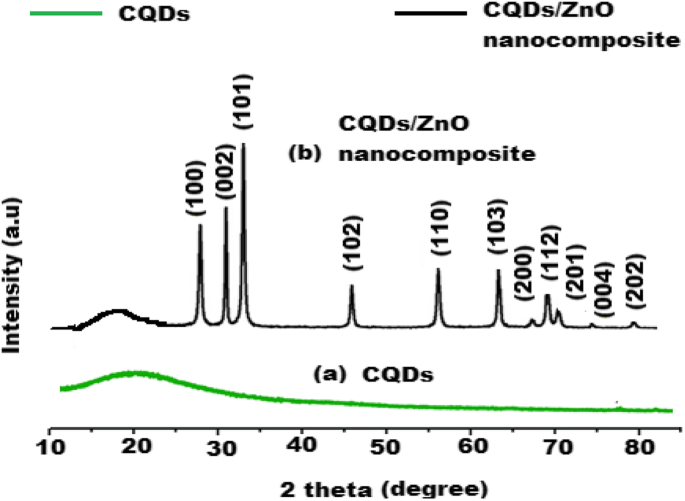
Padrão de difração de raios-X de a CQDs e b Nanocompósito CQDs / ZnO
Os espectros Raman dos CQDs preparados, CQDs / ZnO e nanocompósitos de CQDs / ZnO-BM 19,21 imobilizados foram estudados. Os sinais Raman são comumente usados para estudar a estrutura do cristal e seus defeitos. A Figura 8a, mostrou duas bandas D e G típicas em 1300 e 1520 cm −1 para nanopartículas de carbono, respectivamente. Conforme relatado anteriormente, a banda D geralmente representa sp 3 defeitos, e a banda G é uma característica da vibração plana de sp 2 carbonos ligados [44]. O eu D / eu G a proporção foi calculada para os CQDs preparados e verificou-se que era 1,02 ± 0,03. Novos picos agudos foram observados em 440 e 520 cm −1 para nanopartículas de ZnO e os picos típicos de CQDs foram observados em 1364 e 1595 cm -1 . A proporção de I D / eu G verificou-se ser 1,2 ± 0,01 indicando a formação de nanocompósitos CQDs / ZnO (Fig. 8b). O espectro Raman do nanocompósito CQDs / ZnO-BM 19.21 imobilizado exibiu vários picos que podem ser facilmente reconhecidos como sinais de confirmação de estruturas secundárias e terciárias. Os picos observados na região 1007-1128 cm −1 foram atribuídos para representar a estrutura secundária principal do anticorpo monoclonal. O Raman atinge o pico em 550-682 cm −1 região foram designados para representar conformações dissulfeto, enquanto o 867-797 cm −1 alguns foram atribuídos para representar o estado de ligação de hidrogênio de resíduos de tirosina. Além disso, a mudança significativa no pico do espectro Raman para 1630 cm −1 pode ser atribuída à presença de estrutura terciária do anticorpo imobilizado [45] (Fig. 8c). A proporção de I D / eu G foi aumentado para 1,4 ± 0,04 revelando melhor estrutura cristalina devido à formação de nanocompósitos CQDs / ZnO-BM 19,21 imobilizados.
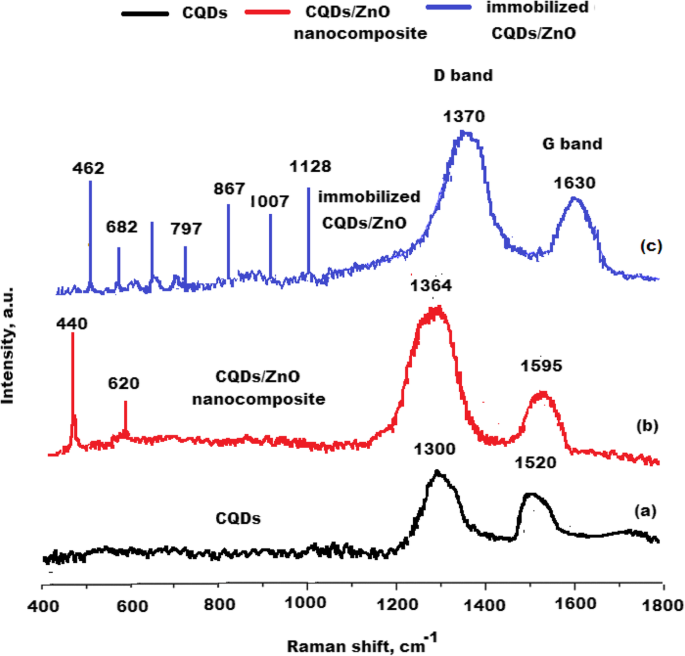
Mudança de espectro Raman de a CQDs, b Nanocompósito CQDs / ZnO e c nanocompósito CQDs / ZnO-BM 19.21 imobilizado
Otimização das condições de imunossensibilidade por fluorescência
A seleção e otimização das condições de imunossensibilidade de fluorescência sugeridas foram conduzidas através do estudo de vários parâmetros. Geralmente, a quantidade de nanocompósito imobilizado, pH e concentração do tampão usado, tempo de incubação entre o analito alvo nas amostras de soro e os reagentes de imunossensor devem ser investigados e otimizados. A fim de selecionar a quantidade adequada de nanocompósitos CQDs / ZnO-BM 19.21 imobilizados, diferentes quantidades na faixa de 10–100 μL foram testadas. A intensidade máxima de fluorescência foi observada pela adição de 50 μL do nanocompósito CQDs / ZnO-BM 19.21 imobilizado (Fig. 9a). Quatro soluções salinas tamponadas com fosfato de valores de pH 7,2-7,5 foram preparadas e testadas em função da intensidade de fluorescência. Uma ligeira mudança na intensidade do sinal de fluorescência foi observada alterando os valores de pH. Em pH 7,2 e 7,3, o sinal de fluorescência foi diminuído devido à instabilidade química do nanocompósito CQDs / ZnO imobilizado. O sinal de fluorescência foi aumentado em pH 7,4 a 7,5 devido à excelente interação entre as moléculas monoclonais na superfície do nanocompósito (Fig. 9b). Verificou-se que 7,4 é o valor de pH mais adequado para manter a atividade do antígeno alvo que pode ser decomposto aumentando o pH para mais de 7,5. Portanto, pH 7,4 foi selecionado para estudos posteriores.
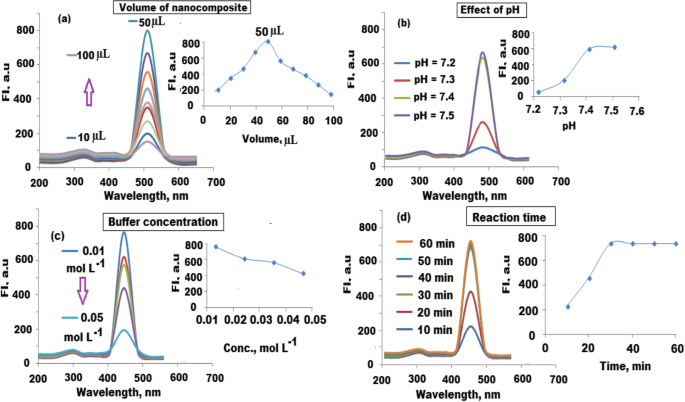
Otimização da determinação de fluorescência do antígeno CYFRA 21-1 em λ ex =470 e λ em =520 nm. a Efeito da adição de CQDs / ZnO-BM 19.21 nanocompósito imobilizado, b efeito da solução salina tampão de fosfato de intervalo de pH 7,3-7,5, c efeito da concentração do tampão usando PBS na faixa de concentração de 0,01–0,05 mol L −1 , e d efeito do tempo de imunorreação usando 10-60 min
A influência da concentração de solução salina tamponada com fosfato na intensidade de fluorescência foi estimada usando uma faixa de concentração de 0,01–0,05 mol L −1 . O sinal de intensidade máxima de fluorescência foi obtido usando a concentração de tampão de 0,01 mol L −1 . Em concentrações de tampão mais altas, o nanocompósito CQDs / ZnO-BM 19.21 imobilizado foi agregado e a instabilidade da solução de imunossensibilidade pode causar uma diminuição na intensidade de fluorescência (Fig. 9c). Para calcular o tempo de imunorreação, o procedimento analítico foi repetido usando o tempo de reação variando de 10 a 60 min. O sinal de intensidade máxima de fluorescência foi observado mantendo a reação entre o antígeno testado e a solução de imunossensor por pelo menos 30 min (Fig. 9d).
Quantificação Analítica
Em condições otimizadas, o método de imunoensaio sugerido foi realizado usando 12 amostras de soro contendo antígeno CYFRA 21-1 na faixa de concentração de 0,01–500 ng mL 1 . Os resultados dos resultados foram plotados para construir o gráfico de calibração que era linear ao longo de uma faixa de concentração de 0,01–100 ng mL −1 com um limite de detecção de 0,008 ng mL −1 . A equação calculada foi I F =7,933C + 181,24 ( r 2 =0,9992). Após seis repetições, a porcentagem do desvio padrão relativo (% RSD) foi de 1,3%. Os resultados aceitáveis revelaram uma alta sensibilidade do método de imunossensibilidade por fluorescência para a quantificação do antígeno CYFRA 21-1 em amostras de soro.
Adequação do sistema
A adequação do sistema foi investigada através da realização de um estudo comparativo entre o método de imunossensibilidade CQDs / ZnO-BM 19.21 imobilizado sugerido e os métodos previamente tratados. O sistema de fluorescência sugerido forneceu vantagens significativas, como simplicidade, ecologicamente correto e fácil de detectar o analito alvo em amostras de soro. Os resultados registrados revelaram alta sensibilidade com uma ampla faixa de detecção linear de 0,01–100 ng mL 1 e limite de detecção inferior de 0,008 ng mL 1 (Tabela 1).
Exatidão, precisão e seletividade do sistema de imunossensor imobilizado
Para garantir a precisão do sistema imunossensível de fluorescência de CQDs / ZnO-BM 19.21 imobilizado sugerido para a determinação do antígeno CYFRA 21-1 em amostras de soro, 12 amostras de soro foram testadas. Os dados do resultado foram comparados com outra técnica relatada anteriormente [6], que foi baseada no ensaio de eletroquimioluminescência usando o complexo tris 2,2′-bipiridil rutênio (II) para ser excitado por tripropilamina. Resultados aceitáveis foram obtidos conforme indicado na Tabela 2. Ensaios intra-dia e inter-dias foram usados para investigar a precisão do método sugerido. O teste foi realizado com uma amostra de soro contendo 10 ng mL - 1 do antígeno CYFRA 21-1. Os desvios padrão relativos médios foram 1,1% e 1,3% para os ensaios intra e inter-dia, respectivamente, o que revelou alta precisão. Além disso, a seletividade do método sugerido para a determinação do antígeno CYFRA 21-1 foi avaliada usando algumas espécies de possível interferência, como aminoácidos (cisteína, lisina, serina, tirosina e glicina), alguns cátions (K + , Na + , Ca 2+ , Mg 2+ e Zn 2+ ) e alguns outros biomarcadores, como CA 15-3, CA 27-29, CA 19-9 e CA 125. O teste foi realizado em condições ideais usando soro humano contendo 10 ng mL −1 Antígeno CYFRA 21-1 na presença de 10 ng mL −1 espécies coexistentes. Os dados do resultado foram calculados como erro percentual relativo (Er%) e o resultado correspondente não excedeu ± 5% para cada espécie interferente (Tabela 3). Os valores de tolerância calculados (F-F 0 / F 0 ) estavam dentro dos limites de tolerância (<5%). Portanto, o sistema de imunossensibilidade de fluorescência CQDs / ZnO-BM 19.21 imobilizado sugerido exibiu alta seletividade para a determinação do antígeno CYFRA 21-1 em soro humano.
Análise de espécimes reais
Em espécimes humanos reais, o sistema de fluorescência de imunossensibilidade sugerido com base na solução imobilizada de CQDs / ZnO-BM 19.21 estava explorando para detectar e quantificar a porcentagem (%) de recuperações do antígeno marcador de tumor CYFRA 21-1. Conforme mencionado anteriormente no procedimento de imunossensibilidade, o sistema sugerido foi usado para determinar o antígeno CYFRA 21-1, encontrando a relação entre a intensidade de fluorescência e a concentração do antígeno CYFRA 21-1 em amostras de soro. Certas quantidades do antígeno alvo (0,5, 1,0 e 2,0 ng mL −1 ) foram adicionados às amostras estimadas, e o aumento nas intensidades de sinal foi avaliado. Após seis determinações, os desvios padrão relativos percentuais (% RSD) foram calculados. Os resultados percentuais de recuperação encontrados variaram de 96,7 ± 0,7 a 100,0 ± 1,3%. O% RSD calculado estava na faixa de 0,2-1,4%. As amostras de soro testadas foram analisadas usando um método relatado anteriormente [6] e as recuperações percentuais foram encontradas na faixa de 96,1 ± 1,6 a 100,0 ± 0,4% com% RSD 0,3–1,7%. A fim de garantir a adequação da técnica de fluorescência de imunossensibilidade sugerida usando uma solução imobilizada de CQDs / ZnO-BM 19.21, um estudo estatístico comparativo usando t de Student teste e F teste [46] foi realizado entre os resultados presentes e aqueles obtidos por outros métodos previamente realizados (Tabela 4). O t obtido teste e F os valores de teste variaram de 0,354 a 2,181 (2,228) * e 1,16 a 4,0 (5,05) * em relação aos valores tabulados de P =0,05, respectivamente. Os resultados revelaram boa concordância entre o método sugerido e os procedimentos publicados anteriormente. Além disso, todas as quantidades detectadas de antígeno CYFRA 21-1 em amostras de soro estavam dentro do limite normal, indicando que nenhum câncer de pulmão foi diagnosticado nas amostras de soro investigadas.
Conclusão
O presente estudo refere-se à preparação de CQDs de síntese verde conjugados com nanocompósito de ZnO usando limão cítrico como um precursor. O nanocompósito CQDs / ZnO foi empregado para formar um novo sistema de imunossensibilidade de fluorescência por meio da imobilização de um anticorpo monoclonal BM 19.21 através de ligações peptídicas simples. O sistema de fluorescência altamente sensível foi usado para determinar o marcador tumoral de câncer de pulmão (CYFRA 21-1) em soro humano. O antígeno CYFRA 21-1 foi determinado por meio da reação anticorpo-antígeno-anticorpo de capeamento de sanduíche usando outro anticorpo monoclonal KS 19.1 revestindo os poços de microtitulação. As características únicas e a alta sensibilidade do sistema sugerido facilitam a determinação do marcador tumoral alvo com alta estabilidade e reprodutibilidade. Um estudo comparativo foi realizado e os resultados dos resultados confirmaram a adequação e alta sensibilidade do sistema de imunossensor sugerido, e os resultados estavam de acordo com uma técnica convencional previamente relatada.
Disponibilidade de dados e materiais
Os únicos dados de desfecho deste estudo foram apresentados no manuscrito.
Abreviações
- % RSD:
-
Desvio padrão relativo percentual
- BM 19-21:
-
Anticorpo monoclonal específico
- CQDs:
-
Pontos quânticos de carbono
- CQDs / ZnO:
-
Pontos quânticos de carbono / óxido de zinco
- CYFRA-21-1:
-
Fragmento de Cytikeratin-19
- DLS:
-
Espalhamento de luz dinâmico
- EDC:
-
Cloridrato de carbodiimida
- eV:
-
Elétron volt
- FT-IR:
-
Transformada de Fourier Infra-vermelho
- HRTEM:
-
Microscópio eletrônico de transmissão de alta resolução
- KS 19-1:
-
Anticorpo monoclonal específico para citoqueratina 19
- Ltd. Co:
-
Companhia limitada
- mAb:
-
Anticorpo monoclonal
- NHS:
-
N-hidroxisuccinimida
- P:
-
Grau de confiança
- PBS:
-
Salina tamponada com fosfato
- SEM:
-
Microscópio eletrônico de varredura
- TEM:
-
Microscopia eletrônica de transmissão
- Reino Unido:
-
Reino Unido
- EUA:
-
Estados Unidos da América
- UV-Vis:
-
Visível por ultravioleta
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- XRD:
-
Difração de pó de raios-x
- ZnO:
-
Óxido de zinco
- ϴ:
-
Grau Theta
- λ max :
-
Comprimento de onda
Nanomateriais
- Pontos de carbono luminescente azul independente de excitação de alta eficiência
- Síntese de pontos quânticos de carbono co-dopados com N, S ricos em piridínicos como imitações de enzimas eficazes
- Nanodots de carbono como nanosensores de modo duplo para detecção seletiva de peróxido de hidrogênio
- Pontos quânticos de bismuto em poços quânticos de GaAsBi / AlAs recozidos
- Fabricação e caracterização de novo composto de suporte de catalisador anódico de nanofibra de carbono Tio2 para célula de combustível de metanol direto via método de eletrofiação
- Uma abordagem simples para sintetizar pontos quânticos de carbono fluorescentes de águas residuais de Tofu
- Síntese de pontos quânticos de sulfeto de antimônio solúvel em água e suas propriedades fotoelétricas
- Material e propriedades ópticas de pontos quânticos de carbono fluorescente fabricados a partir de suco de limão via reação hidrotérmica
- Propriedades das nanopartículas de óxido de zinco e sua atividade contra micróbios
- Ajuste do modo de movimento deslizante de nanotubos de carbono por meio de grupos hidroxila



