Efeito de álcalis no processo de fabricação de ferro em um alto-forno
Efeito de álcalis no processo de fabricação de ferro em um alto-forno
Um dos principais objetivos durante a operação de um alto-forno (BF) é maximizar a produção de metal quente (HM) da composição química desejada a custos mínimos. Isso requer uma base de matéria-prima de alta qualidade e uma operação regular e suave do alto-forno. A qualidade dos materiais de carga é muito importante para evitar problemas no processo causados pela entrada de elementos indesejados no forno. Nesta área, também é necessário prestar atenção ao conteúdo de elementos indesejados na carga de entrada. Esses elementos indesejados causam uma série de problemas tecnológicos no BF. Além disso, eles afetam significativamente o custo de produção do HM. Os principais elementos indesejados presentes na carga que podem ser problemáticos em relação à remoção e ao desempenho do BF são os compostos alcalinos dos metais potássio (K) e sódio (Na).
No processo BF, sabe-se que a presença de álcalis tem influências negativas no processo. Os álcalis causam maior reatividade do coque, amolecimento prematuro da carga do minério, decomposição do sinter, inchamento das pelotas e estão envolvidos na formação de depósitos no revestimento refratário do BF que aceleram o desgaste do revestimento. Os efeitos negativos dos álcalis são devidos ao efeito catalítico na gaseificação do coque, destruição da estrutura do carbono (C) devido à inserção de álcalis, formação de andaimes e ataque refratário. Os álcalis são introduzidos com as matérias-primas e devido à circulação do álcali (Fig 1) os álcalis são recolhidos no caminho para a zona de temperatura mais alta no BF.
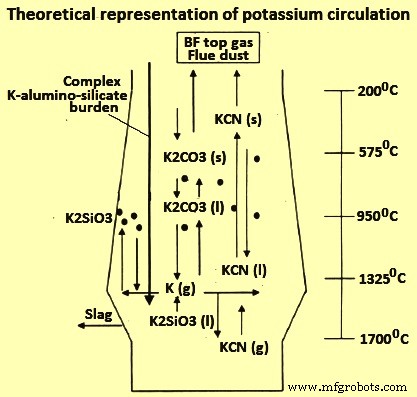
Fig1 Representação teórica da circulação K
A presença de álcalis leva a uma menor produção e maior consumo de coque no BF, em torno de 4,5% e 2,3% respectivamente para cada kg/tHM de álcali adicionado com a carga máxima de matéria-prima. O álcali diminui a produção devido à diminuição do limiar para a reação reversível de Boudouard, C(s) + CO2 (g) =2CO (g), aumento do gás de coque e redução da resistência do coque. A permeabilidade ao gás é diminuída devido à degradação do coque e podem ocorrer andaimes nas paredes reduzindo assim o volume do BF.
Reações alcalinas no BF
Em todas as reações alcalinas apresentadas neste artigo, K pode ser substituído por Na. A redução de silicatos alcalinos por C pode ocorrer de acordo com as reações reversíveis K2SiO3 (escória) + C (s) =2K (g) + SiO2 (escória) + CO (g), e K2SiO3 (escória) + 3C (s) =2K (g) + Si (HM) + 3CO (g). A extensão dessas reações depende da temperatura e da pressão parcial de CO (monóxido de carbono). Os óxidos alcalinos podem ser reduzidos por C no coque ou pelo CO conforme as reações reversíveis K2O + C (s) =2 K (g) + CO (g), e K2O + CO (g) =2 K (g) ) + CO2 (g).
Os álcalis são volatilizados como elementos ou reagem com C e N2 (nitrogênio) na região bosh do BF formando vapores de cianeto de potássio (KCN) ou cianeto de sódio (NaCN) conforme reação reversível 2K (g) + N2 (g) =2KCN (g). Os vapores são transportados junto com o gás do forno e não se dissolvem no HM ou na escória. O ponto de fusão e o ponto de ebulição para K são 63,4 graus C e 759 graus C, respectivamente, enquanto as temperaturas de fusão e ebulição correspondentes para Na são 97,7 graus C e 883 graus C, respectivamente. Os pontos de fusão de KCN e NaCN são 622 graus C e 562 graus C, respectivamente, e os pontos de ebulição são 1625 graus C e 1530 graus C, respectivamente. O estado desses compostos é líquido no eixo inferior e gasoso na pista e na zona da fornalha, dependendo da temperatura. O gás é transportado pelos gases em movimento rápido no BF.
No poço onde o potencial de oxigênio (O2) aumenta (em torno de 1100°C), K e KCN não são mais estáveis e são oxidados pelo dióxido de carbono (CO2) a carbonatos alcalinos (K2CO3, Na2CO3) de acordo com as reações 2K ( g) + 2CO2 (g) =K2CO3 + CO (g), e 2KCN (g) + 4CO2 (g) =K2CO3 (s) + N2 (g) + 5CO (g) respectivamente e óxidos alcalinos pelo CO de acordo com o reação reversível 2KCN (g) + CO (g) =K2O + 3C + N2 (g). Os carbonatos alcalinos gerados saem na forma de finos brancos, que são distribuídos na superfície do material de carga ou localizados no revestimento do tijolo.
Componentes alcalinos adsorvidos no material de carga e coque formam novos compostos de acordo com sua relativa estabilidade. O carbonato de potássio (K2CO3) e o carbonato de sódio (Na2CO3) são sólidos em temperaturas abaixo de 891°C e abaixo de 851°C, respectivamente. Os compostos alcalinos descem com os materiais de carga e são reduzidos e vaporizados novamente atingindo a zona de alta temperatura, de acordo com a reação reversível K2CO3(l) + 2C =2K (g) =3CO (g).
A maior parte do álcali é drenada do BF com a escória. No entanto, uma parte do álcali na escória é reduzida gerando vapor alcalino que ascende com o gás circundante. O vapor alcalino condensa na parte superior do BF, onde uma parte sai com o gás de topo, enquanto o restante condensa nas paredes internas ou no material de alimentação. Devido à volatilização e condensação do álcali nas diferentes zonas térmicas, o álcali tende a circular dentro do BF, levando a um acúmulo e interações com outros materiais de alimentação. Isso pode ter um impacto significativo no processo, mesmo quando o álcali é carregado em pequenas quantidades, geralmente inferiores a 5 quilogramas por tonelada de metal quente (kg/tHM). Uma visão simplificada da circulação alcalina no BF é mostrada na Figura 2. Estudos de BFs escavados mostraram que o nível de álcali é mais alto onde a temperatura está acima de 1000 graus C, o que significa que há uma concentração de álcali aumentada na parte inferior do o BF.
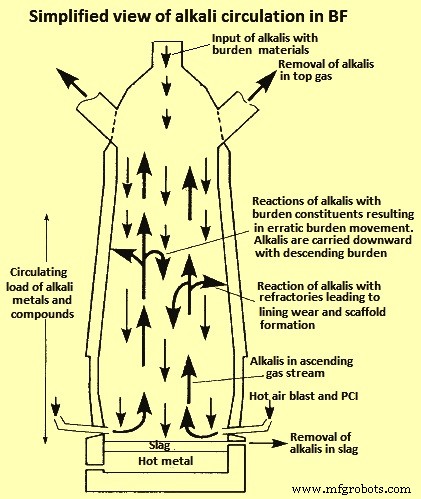
Fig 2 Uma visão simplificada da circulação alcalina no BF
Ciclo alcalino no BF
Os álcalis normalmente entram no BF com o material ferroso e com o coque na forma de silicatos. Para uma operação de BF suave e eficiente, é desejável limitar a quantidade de álcali em cerca de 1,5 kg/tHM a 5 kg/tHM, mas normalmente varia de 2,5 kg/tHM a 7,5 kg/tHM em diferentes plantas. Das duas substâncias alcalinas Na e K, K é normalmente o principal composto que entra no BF. A maioria dos álcalis sai com a escória, enquanto alguns se tornam parte do gás de topo e saem do forno com o gás de topo. O álcali recirculante pode ser removido pela escória ou pelo gás. O K vai para o gás de topo em maior grau, pois é mais volátil em comparação com o Na, que sai mais com a escória.
Os álcalis entram no BF na forma de silicatos (K2SiO3). Estudos do ciclo alcalino mostraram que os silicatos descem com a carga e o ciclo começa com o silicato alcalino sendo reduzido pelo C do coque na zona de fusão conforme a equação K2SiO3 + C (s) =2K (g) + SiO2 + CO (g). As reações ocorrem em torno de 1550 graus C conforme os dados termodinâmicos para as reações. Quaisquer óxidos alcalinos que entram ou são formados no BF reagem mais acima no BF em temperaturas mais baixas de acordo com a equação K2O + CO (g) =2K (g) + CO2 (g), uma vez que não são estáveis. O K2O também pode se dissolver na escória primária.
Além disso, os vapores de K produzidos no nível da lareira no BF, reagem com o carvão pulverizado injetado e o N2 do jato de ar quente conforme a equação 2K (g) + 2C (s) + N2 (g) =2KCN (g , eu). O ponto de ebulição para KCN é 1625 graus C, de modo que o cianeto de potássio (KCN) sobe do jato de ar quente das ventaneiras, ele se transforma em uma fase líquida quando a temperatura cai. O tempo na zona da ventaneira é muito curto devido ao alto fluxo de gás, de modo que os cianetos alcalinos têm tempo de subir o BF antes de se transformarem na fase líquida. Mais acima no BF, os cianetos alcalinos reagem com CO2 (dióxido de carbono) para formar carbonatos mais estáveis em temperaturas abaixo de 1100 graus C conforme a equação 2KCN (l) + 4CO2 (g) =K2CO3 + N2 (g) + 5CO ( g). Os carbonatos seguem o gás superior como gás ou são depositados na carga quando começam a condensar abaixo de 900 graus C.
Em comparação com os silicatos alcalinos, os cianetos alcalinos são instáveis, de modo que qualquer SiO2 presente na parte da lareira do BF pode reagir com os cianetos alcalinos para formar novamente silicatos alcalinos. O processo de redução de silicatos alcalinos em vapor alcalino, que ascende no BF, sai com o gás de topo ou reage com CO2 para formar carbonatos, é conhecido como ciclo alcalino. Existem algumas visões diferentes que têm um resumo ligeiramente diferente do processo, diferindo exatamente sobre quais reações ocorrem. Há dúvidas se os carbonatos realmente são formados no topo do BF, uma vez que os carbonatos não são encontrados durante a escavação dos BFs. No entanto, o principal processo pelo qual os cianetos alcalinos são formados e que o álcali circula no BF é acordado em todas as visões.
A Fig. 3 mostra a circulação de álcalis no BF. O material carregado desce para a zona de alta temperatura antes que os silicatos alcalinos se decomponham em vapores alcalinos ou sejam absorvidos pela fase de escória primária na forma de K2O ou Na2O. O ciclo também indica quando o vapor alcalino reage com os silicatos para formar novamente silicatos. A distribuição de vapores alcalinos através do BF depende dos caminhos do fluxo de gás e da extensão do fluxo central de gás. Os fluxos de gás têm um grande efeito em como o calor é distribuído em um BF. Fluxo mais central significa mais fusão no meio e menos na periferia do BF.
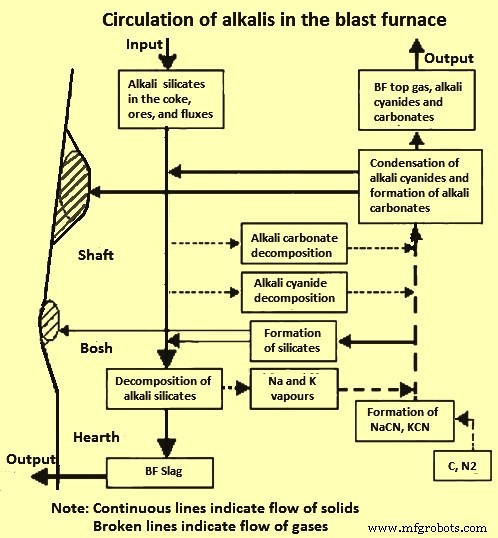
Fig 3 Circulação de álcalis no BF
Formação de amônia e cianeto de hidrogênio no BF
Acredita-se que a amônia (NH3) seja formada no BF. As reações básicas por trás da formação de NH3 e cianeto de hidrogênio (HCN) no BF são 2KCN + 3H2O =K2CO3 + 2NH3 + C e NH3 + CO =HCN + H2O. A razão entre essas reações depende de vários parâmetros como (i) a quantidade de umidade disponível, (ii) a quantidade de KCN disponível no topo e (ii) a temperatura durante as reações. O limiar de temperatura para NH3 é em torno de 600 graus C e a formação de NH3 diminui exponencialmente continuamente até 500 graus C e depois não é detectada. Mais NH3 que é formado é oxidado por Fe2O3 ou CO2 e a quantidade de NH3 formada diminui. A oxidação de NH3 por Fe2O3 ou MnO2 depende da temperatura. Em temperaturas mais baixas o MnO2 é um oxidante mais forte e em temperaturas mais altas o Fe2O3 é o oxidante mais forte.
Como HCN e NH3 podem ser encontrados no gás de topo, a cinética de oxidação do NH3 não é rápida o suficiente para removê-lo completamente. A maior quantidade de água encontrada no gás de topo significa que há mais formação de NH3 que pode ocorrer de acordo com a reação acima. A formação de NH3 no BF é complexa, pois vários parâmetros, conforme indicado abaixo, afetam sua formação.
Temperatura máxima do gás – A temperatura de topo do gás depende da relação entre as reações endotérmicas / exotérmicas no BF. A temperatura afeta o teor de umidade. A temperatura mais baixa também pode levar ao aumento da solubilidade do NH3 em água e o HCN é miscível em água, portanto, a presença de água pode diminuir sua presença no gás de topo.
Temperatura da chama – A temperatura da chama tem um efeito menor na quantidade de vapor alcalino produzido e na carga alcalina total. Uma alta temperatura é necessária para reduzir os silicatos alcalinos em gás alcalino que inicia a circulação alcalina. A diminuição da temperatura da chama leva, portanto, a mais álcali deixando o BF através da escória.
Basicidade – Uma basicidade mais baixa leva a uma maior absorção de álcali na escória, portanto, há menos álcali circulante no BF e menos NH3 é produzido.
Conteúdo de umidade – Menos umidade introduzida com a carga ou por outras vias no BF dá menos água para que a reação de formação de NH3 aconteça.
Efeito do álcali e remoção
A concentração de álcalis na matéria-prima aumentou nos últimos anos devido à diminuição da disponibilidade de carvão metalúrgico de alta qualidade. O álcali é prejudicial à operação do BF, pois causa um aumento da reatividade do coque devido ao efeito catalítico na reação de perda de solução (reação de Boudouard).
Um dos principais efeitos negativos do álcali é que ele catalisa a reação reversível de Boudouard, baixando a temperatura da reação de 900°C para 950°C até cerca de 750°C a 850°C e aumentando a reatividade do coque dependendo da qualidade do coque. Também afeta negativamente a estrutura do coque. O limiar reduzido para a reação de Boudouard significa que mais C está sendo consumido no BF em uma reação fortemente endotérmica. Assim, é necessário aumentar a adição de coque no BF para manter uma operação estável com 2 kg a 10 kg de coque por kg de álcali ou com 6 kg a 11 kg de coque dependendo das fontes utilizadas.
O álcali que entrou na estrutura do coque diminui a resistência do coque na parte inferior do BF devido ao aumento da reatividade do coque e, portanto, ao aumento da degradação. A taxa de reação aparente do coque no nível da ventaneira mostrou ser dez vezes a taxa de reação do coque de alimentação, que está relacionada à quantidade total de presença de K. K é conhecido por aumentar a reatividade do coque com CO2 e pode resultar na fratura do coque devido ao inchamento dos grãos de coque pela inserção de K. Um aumento na reatividade pode ser vantajoso, pois reduz a temperatura de operação do BF, a temperatura na zona de reserva térmica e, assim, abaixando a temperatura para redução do óxido de ferro. No entanto, o objetivo do coque também é atuar como suporte de carga dentro do forno e, portanto, a fratura do coque precisa ser minimizada.
Estudos sobre a penetração do vapor de K no coque confirmaram que a estrutura dos minerais do coque pode ser quebrada devido à expansão do volume dos minerais alcalinizados, especialmente a calsilita. A área de superfície entre os minerais e a matriz C aumenta devido à quebra dos minerais no coque. Isso facilita a interação da matéria mineral com os gases C e BF acelerando a gaseificação do coque. Uma expansão no coque também pode ocorrer quando os vapores alcalinos penetram nas camadas cristalinas do coque para formar compostos intercamadas. A resistência do coque e o suporte da carga durante a operação de BF são críticos, pois um colapso da carga reduz a permeabilidade a gases e líquidos, o que reduz a eficiência tanto em relação à produção de HM quanto ao aumento das emissões de CO2.
Pequenas partículas de coque de diferentes tamanhos diminuem os vazios no leito de coque na zona úmida e a área de superfície do coque aumenta. A quebra do coque também promove inundações, asfixia da fornalha e aumento da queima de ventaneiras e entalhes de escória, os quais limitam a produção do forno. A tendência do gás ascendente ser transportado próximo às paredes aumenta quando a permeabilidade é reduzida, o que diminui a utilização do gás e, portanto, aumenta a taxa de coque.
Outro efeito do álcali é o aumento da chance de formação de andaimes no eixo, pois o álcali se condensa no revestimento e pode ligar o material fino a ele. Os andaimes são um acúmulo de material sólido na parede do forno e se projetam em direção ao centro do forno. Os andaimes podem ocorrer em qualquer lugar do meio para a parte superior do eixo. O efeito da formação do andaime é que a descida da carga é retardada ou interrompida e, em casos extremos, levando a suspensão, deslizamento e carregamento descontrolado. Os andaimes também reduzem o volume de trabalho do BF. A velocidade do gás é aumentada nas partes não afetadas no poço, o que resulta em um aumento da temperatura do gás de topo e diminuição da utilização do CO. Quando os andaimes se separam da parede do forno, muitas vezes resulta em uma fornalha resfriada. Os andaimes podem ser removidos por aumento temporário da temperatura do forno ou são removidos quando um fluxo de gás de alta temperatura atinge a área.
O material de carga também pode ser colado por cianetos e carbonatos líquidos condensados, o que reduz a permeabilidade do leito. Além disso, os álcalis podem atacar o material refratário, principalmente os refratários à base de C normalmente utilizados na parte inferior do forno. Os compostos alcalinos penetram nos blocos C que são consumidos formando vapor alcalino. Isso resulta em uma vida útil mais curta do revestimento refratário e na necessidade de um reembasamento mais frequente.
A remoção de álcalis é feita principalmente com a escória e é melhor realizada em valores de basicidade mais baixos. Do álcali removido, mais de 90% é removido através da escória. Aqui a basicidade é considerada como CaO/SiO2. Os resultados de vários estudos mostraram que a menor basicidade da escória aumenta a quantidade de álcali na escória. No entanto, o problema com basicidade muito baixa é que um nível mais alto de enxofre (S) permanece no HM, pois o S pode ser neutralizado pelo CaO presente na escória de BF e o CaO é menor quando a basicidade é menor. O limite inferior da basicidade para manter a qualidade do LH sob controle difere de planta para planta. O limite depende dos parâmetros de BF e da qualidade da matéria-prima utilizada. Um valor de basicidade um pouco acima ou em torno de 1 pode ser visto como o limite se o álcali deve ser removido e a qualidade do HM deve ser mantida.
Para impedir a gaseificação de silicatos alcalinos, a pressão parcial de CO deve ser mantida alta. A alta temperatura para a reação a 1550°C significa que uma temperatura de chama mais baixa também pode ser usada para retardar a redução e a gaseificação e, assim, diminuir a circulação alcalina. A remoção de álcalis precisa diminuir a recirculação de materiais contendo álcalis para o BF, pois o álcali é apenas reintroduzido no BF.
A redução do efeito catalisador do álcali na gaseificação do coque pode ser feita por adições de cinzas de coque que podem ligar o álcali existente em formas mais estáveis. Foi tentado com certa adição mineral antes. À medida que o álcali se difunde através do coque, um revestimento da adição de minerais pode estabilizar o álcali na superfície do coque, impedindo-o de degradar as partes internas do coque.
Controle de carga alcalina
Para controlar a carga alcalina no BF, a entrada alcalina deve ser mantida o mais baixa possível. Se houver uma variação no material de entrada, a mistura de minério deve ser bem misturada para minimizar o risco de seções de alto teor alcalino no BF. Outra precaução é evitar a recirculação de pó de combustão com altos níveis de álcalis. Uma forma de minimizar o risco de formação de andaimes é aumentar a resistência da carga ferrosa e do coque para evitar a formação de finos.
O BF pode ser operado com um fluxo de gás central. Por causa disso, a temperatura do gás superior no centro é aumentada a tal nível que parte do álcali deixa o forno como vapor com o gás superior. No entanto, temperaturas de gás superiores mais altas resultam em maiores perdas de calor.
O álcali recirculado pode ser diminuído e, em vez disso, deixar o BF através da escória operando o BF com uma escória ácida. Quanto menor a basicidade da escória, mais facilmente o K e o Na básicos são absorvidos pela escória, uma vez que a cal (CaO) e a magnésia (MgO) ocupam os mesmos locais na rede de sílica que os óxidos alcalinos. Uma basicidade diminuída pode ser alcançada diminuindo a basicidade na carga ferrosa e nas adições de fluxo. No entanto, uma basicidade mais baixa também resulta em aumento do teor de S (enxofre) no HM, pois o S se liga ao Ca na escória.
Outra possibilidade de diminuir a carga alcalina é aumentar o volume da escória, o que diminui a atividade dos óxidos alcalinos na escória e, portanto, aumenta a absorção de álcali e a saída através da escória, mas um volume aumentado de escória também aumenta a taxa de coque.
Uma temperatura mais baixa no BF resulta em diminuição da redução e vaporização do álcali. Operar o BF com temperatura de chama mais baixa resulta em uma carga alcalina diminuída, mas também em produtividade diminuída e taxa de coque mais alta. A carga alcalina também pode ser diminuída operando o BF com alta pressão parcial de CO, uma vez que se opõe à reação de gaseificação alcalina. Isso pode ser alcançado pelo enriquecimento de O2 da explosão ou alta pressão de topo.
Processo de manufatura
- Sistema de automação, medição e controle de processos de alto forno
- Uso de Nut Coke em um Alto Forno
- Processo HIsmelt de fabricação de ferro
- Processo HIsarna para fabricação de ferro
- Irregularidades do alto-forno durante a operação
- Sistema de resfriamento do alto-forno
- Química da Ferragem por Processo de Alto Forno
- Revestimento refratário do alto-forno
- Alto-forno e seu projeto
- Fabricação de ferro por alto-forno e emissões de óxido de carbono



