Preparação in situ fácil e atividade antibacteriana in vitro de micelas de copolímero com prata à base de PDMAEMA
Resumo
Micelas de polímero bem definidas com estrutura núcleo-casca são uma boa plataforma de entrega para estabilizar nanopartículas de prata (AgNPs) no campo de doenças que visam antimicrobianos. A construção racional da estrutura do polímero, uma abordagem de preparação eficiente, fácil e ecológica e a exploração abrangente dos AgNPs derivados são necessárias, como tamanho, estabilidade de partícula, atividade antibacteriana e outras propriedades. Aqui, projetamos e avaliamos a atividade antimicrobiana in vitro de micelas de copolímero decoradas com AgNPs com diferentes topologias de copolímero. Em primeiro lugar, foram obtidos copolímeros tribloco em estrela linear ou de quatro braços com peso molecular e grau de polimerização semelhantes, que consistiam em DMAEMA para redução in situ de íons de prata para formar AgNPs sem agente redutor externo. HEMA e PEGMA em concha micelar proporcionaram maior estabilidade de AgNPs durante a circulação sanguínea. A combinação de modelagem computacional e resultados experimentais indicou que ambos os tipos de micelas poderiam fabricar AgNPs com morfologia monodispersa e esférica. AgNPs estabilizados de micelas de copolímero em estrela apresentaram tamanho médio menor, melhor estabilidade e maior atividade antibacteriana do que aquelas com estrutura linear, o que pode ser devido à maior estabilidade de micelas de copolímeros em estrela. Além disso, o teste de avaliação de citotoxicidade mostrou que os AgNPs estabilizados com micelas de copolímeros lineares ou estrela alcançados tinham boa biocompatibilidade. Este trabalho fornece uma abordagem fácil e universal no projeto racional de AgNPs estabilizados por micelas com topologia adequada para o combate a uma ampla gama de infecções bacterianas.
Introdução
Nas últimas décadas, uma série de agentes antimicrobianos tradicionais tem sido amplamente usada para tratar doenças infecciosas. De acordo com a Organização Mundial da Saúde, o rápido surgimento de microrganismos multirresistentes tem se tornado um problema global cada vez mais sério, que está classificado entre os três primeiros na lista das principais ameaças à saúde humana [1,2,3,4,5]. Portanto, é necessário o desenvolvimento de novos agentes antimicrobianos com boa segurança, capacidade antibacteriana eficaz sem produzir resistência bacteriana. Nanopartículas de prata (AgNPs) como um dos melhores agentes antimicrobianos desde os tempos antigos, foram amplamente utilizadas em bens de consumo devido ao seu desempenho superior contra vários patógenos bacterianos e fúngicos, toxicidade relativamente baixa para células de mamíferos e resistência bacteriana limitada [6,7, 8,9,10]. AgNPs são capazes de melhorar a permeabilidade da membrana de bactérias, permear no citoplasma, desnaturalizar proteínas bacterianas e interromper a replicação de bactérias, resultando na morte de bactérias [11,12,13]. Um grande número de formulações de prata foi empregado para elucidar a atividade antibacteriana de AgNPs [14,15,16,17], por exemplo, um curativo através de um hidrogel de policarboxibetaína zwitteriônica juntamente com AgNPs antibacterianos como componente principal proposto por Zhang et al . [18], as superfícies multifuncionais obtidas via revestimento multicomponente para co-imobilização de AgNPs propostas por Moreno-Couranjou et al., Etc. [19] .
No entanto, grande área de superfície específica e alta energia de superfície levaram à agregação de AgNPs, que se tornou um grande gargalo para sua aplicação. Assim, a matriz polimérica ou estabilizador externo é necessária para estabilizar os AgNPs. Como se sabe, a matriz polimérica é o método mais comum para resolver o problema de agregação. Atualmente, vários métodos são usados para estabilizar AgNPs com matriz polimérica, tais como método de redução química, método eletroquímico, método fotoquímico e método de microondas. Entre eles, a redução química é um método comum e eficaz. O nitrato de prata é reduzido em AgNPs pela adição de redutores como o hidrato de hidrazina (N 2 H 4 ), boro-hidreto de sódio (NaBH 4 ), citrato de sódio e ácido ascórbico em solução [20,21,22,23]. Por exemplo, Hoda et al. ácido poliacrílico em bloco de poliestireno fabricado (PS- b -PAA) reverter micelas carregadas com os AgNPs de 20 nm sob a influência do agente redutor N 2 H 4 , e os blocos PS jogaram a camada externa em tolueno [24]. O grupo de Liu relatou que nanotemplacas de micelas automontadas foram preparadas a partir de poli (ε-caprolactona) -bloco-poli (ácido aspártico) (PCL- b -PAsp). AgNPs bem dispersos foram preparados com AgNO 3 como o precursor e NaBH 4 como redutor [25]. No entanto, os métodos acima não eram amigáveis ao meio ambiente e a adição de redutores em excesso produz subprodutos, dificultando a purificação de AgNPs e restringindo sua aplicação de antimicrobianos voltados para doenças infecciosas.
Nesse ínterim, foi relatado que os polímeros contendo o grupo amina poderiam ser usados como redutor e estabilizador para preparar AgNPs in situ. Por exemplo, Lang et al. polímeros em estrela de seis braços sintetizados consistindo em PCL, metacrilato de 2- (dimetilamino) etil (DMAEMA) e metacrilato de éter metílico de poli (etilenoglicol) (PEGMA). O sistema reduziu diretamente o nitrato de prata em AgNPs sem adicionar qualquer outro redutor na fase aquosa [26]. Embora os AgNPs mencionados acima apresentem modificação superficial fácil sem redutor adicional, em relação às nanopartículas de ouro [27, 28], o efeito das topologias do polímero na redução e estabilidade das nanopartículas de prata junto com sua aplicação na atividade antibacteriana baseada em micelas é menor estudou.
Neste trabalho, uma abordagem suave, fácil e ecológica foi projetada para lutar contra infecções bacterianas, aproveitando as vantagens de micelas poliméricas automontadas a partir de copolímeros tribloco lineares ou de quatro braços com peso molecular e grau de polimerização semelhantes aos da nanoplataforma para decorar AgNPs (Esquema 1). Nessa abordagem, os copolímeros tribloco, compostos por DMAEMA, 2-hidroxietil metacrilato (HEMA) e PEGMA, poderiam gerar micelas automontadas em meio aquoso, o que é um bom molde para a preparação e estabilização de AgNPs. Os blocos PDMAEMA com grupos de amina terciária poderiam facilmente absorver o Ag + íons por meio de interação de coordenação e, em seguida, in situ geram AgNPs sem qualquer agente redutor. Os blocos HEMA e PEGMA com alta hidrofilicidade podem ser usados como estabilizadores na fase aquosa para melhorar ainda mais a estabilidade dos AgNPs. Portanto, o nitrato de prata pode coordenar espontaneamente e desoxidar no núcleo de micelas de copolímero auto-montadas para formar AgNPs. Eles estavam embutidos no núcleo micelar e podem resultar na destruição da membrana bacteriana. Aqui, como as topologias de copolímero em estrela linear ou de quatro braços afetam o comprimento de onda de absorção máximo, morfologia, tamanho de partícula, potencial zeta, estabilidade, bem como a eficiência antibacteriana de AgNPs foram totalmente investigados. Portanto, o estudo da relação entre estrutura e propriedades pode encontrar uma explicação detalhada das nanopartículas de híbridos de prata para o tratamento de infecções bacterianas. Além disso, forneceria idéias de design e base técnica para a preparação de AgNPs com estrutura mais estável e tamanho de partícula controlável.
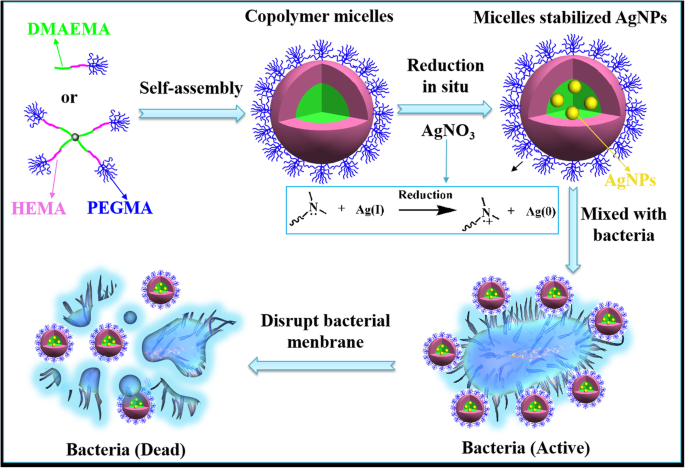
Ilustração esquemática da formação de micelas de copolímeros lineares / estrela estabilizou AgNPs para excelente atividade antibacteriana
Material e métodos
Materiais
Pentaeritritol ( J&K Scientific Ltd.) foi seca por meio de pressão reduzida por 24 h antes do uso. Metacrilato de 2- (Dimetilamino) etil (DMAEMA,> 98%), metacrilato de 2-hidroxietil (HEMA, 99%) e metacrilato de éter metílico de poli (etilenoglicol) (PEGMA, M n =300 Da, 99%), todos da Aldrich, foram purificados por meio de passagem por uma coluna contendo alumina neutra para remover o inibidor. Pela utilização de hidreto de cálcio (CaH 2 ), tetra-hidrofurano (THF) e tolueno da Aldrich foram secos e, em seguida, destilados sob pressão reduzida antes do uso. 2-bromoisobutirato de etila (EBiB, 98%, Alfa Aesar), brometo de 2-bromoisobutirila (BIBB, 98%, Alfa Aesar), 1,1,4,7,10,10-hexametiltrietilenotetramina (HMTETA, 99%), nitrato de prata (AgNO 3 , 99,9%), brometo cúprico (CuBr 2 ), metanol, trietilamina (TEA), diclorometano (DCM), acetona, n -hexano, dimetilsulfóxido (DMSO), octoato estanoso (Sn (Out) 2 ), carbonato de sódio (Na 2 CO 3 ), bicarbonato de sódio (NaHCO 3 ), cloreto de sódio (NaCl), sulfato de sódio (Na 2 SO 4 ), e todos os outros reagentes obtidos de J&K Chemical Company foram usados como recebidos.
Caracterização geral e instrumentação
Ressonância magnética nuclear de prótons ( 1 H NMR) espectros dos copolímeros tribloco linear ou de quatro braços foram detectados em CDCl 3 e D 2 O a 25 ° C através de um espectrômetro Bruker ADVANCE 400 MHz (Madison, WI, EUA). Medições de espectros de espectroscopia de infravermelho com transformada de Fourier (FTIR) de copolímeros lineares, copolímeros de estrelas e seus AgNPs estabilizados por micelas foram conduzidas usando um espectrofotômetro FT IR (Nicolet Nexus para Euro, EUA) equipado com um modo de transmissão a 25 ° C. Amostras granulares foram preparadas após trituração com brometo de potássio (KBr) e compactação. Para obter um espectro, as condições espectrais foram definidas previamente com comprimento de onda de 4000 a 400 cm −1 (32 varreduras) e uma resolução de 8 cm −1 . Os potenciais zeta de micelas de copolímeros lineares e em estrela estabilizadas com AgNPs em diferentes razões molares foram medidos usando medição eletroforética com o instrumento Malvern Zetasizer Nano S (Malvern, WR, UK) em que cada amostra foi testada três vezes a 25 ° C. Microscopia eletrônica de transmissão (TEM, FEI Tecnai-G20) operando a 200 kV foi conduzida para observar morfologias de micelas de copolímeros lineares e estrela estabilizadas AgNPs em diferentes razões molares. O processo de preparação do produto para TEM foi o seguinte:10 μL de solução de amostra foram primeiro colocados em uma grade de cobre revestida com carbono e depois secos ao ar. Os espectros de UV-Vis de micelas de copolímeros lineares e em estrela estabilizadas com AgNPs em diferentes razões molares foram determinados usando um espectrofotômetro de UV-Vis (UV-2450, Shimadzu, Kyoto, Japão). A análise termogravimétrica (TGA) foi realizada em um equipamento NETZSCH (STA409PC, Alemanha). Todas as amostras de pó seco (copolímeros lineares, copolímeros em estrela e seus AgNPs estabilizados por micelas) foram aquecidas de 25 a 600 ° C a uma taxa de 10 ° C / min sob condição de nitrogênio.
Síntese de PDMAEMA- b -PHEMA- b -PPEGMA
Os ativadores contínuos regenerados por polimerização de radical de transferência de átomo de transferência de elétrons (AGERT ATRP) de DMAEMA, HEMA e PEGMA foram realizados seguindo o procedimento modificado de Zhang et al. [29, 30]. Em resumo, após a adição de CuBr 2 (10 mg, 0,045 mmol), o balão de três tubuladuras seco de 100 mL foi evacuado e enxaguado com árgon três vezes. Com o auxiliar de seringa desgaseificada, tolueno anidro (25 mL), EBiB (88 μL, 0,24 mmol), DMAEMA (5,15 mL, 30,5 mmol) e ligante HMTETA (62 μL, 0,24 mmol) foram injetados ordenadamente no recipiente, a seguir Agitação de 10 min. Após injetar Sn (Out) 2 (78 μL, 0,24 mmol) com tolueno (2 mL) como solução, a reação foi realizada a 70 ° C em um banho de óleo por 8 h. O bloco sucessivo HEMA (2,32 mL, 18,4 mmol) foi injetado para as próximas 8 horas de reação após a solução se tornar muito mais espessa. Por fim, com a participação do terceiro monômero PEGMA (8,89 g, 55,6 mmol), testemunhamos uma reação contínua de 72 horas antes de resfriar o frasco quase à temperatura ambiente. THF (30 mL) foi injetado no recipiente e a mistura de reação foi então passada através de uma coluna de alumina neutra para remover o catalisador. O produto PDMAEMA- b -PHEMA- b -PPEGMA foi precipitado em excesso dez vezes maior de frio n -hexano, filtrado e finalmente seco sob vácuo durante 48 h a 35 ° C.
Síntese de (PDMAEMA- b -PHEMA- b -PPEGMA) 4
Iniciador terminado com bromo do tipo estrela (Br) 4 foi sintetizado pela esterificação dos grupos hidroxila terminais presentes no pentaeritritol com brometo de 2-bromoisobutirila usando THF como solvente e TEA como agente de ligação de ácido. Normalmente, após carregar com pentaeritritol (2,72 g, 2 mmol), o frasco de três gargalos de 100 mL foi evacuado e enxaguado com argônio três vezes, após injeção sequencial gota a gota de THF anidro (120 mL) e TEA (12,51 mL, 90 mmol) . Sob a circunstância de gelo / água, brometo de 2-bromoisobutiril (11,12 mL, 90 mmol) foi injetado gota a gota na solução vigorosamente agitada, após reação de 4 h a 0 ° C e, em seguida, 20 h a 25 ° C. Para purificar o produto, a mistura foi primeiro passada por uma coluna de alumina neutra. O produto bruto foi lavado sucessivamente com água, 10% Na 2 CO 3 , NaHCO saturado 3 , e NaCl saturado, então sucessivamente seco através de Na 2 SO 4 durante a noite, filtrada e concentrada antes de despejar no excesso dez vezes maior de frio n -hexano para precipitar o produto e, finalmente, secar sob vácuo por 24 h para receber o produto.
As rotas sintéticas e as quantidades de alimentação de (PDMAEMA- b -PHEMA- b -PPEGMA) 4 foi realizado usando o mesmo procedimento do PDMAEMA- b -PHEMA- b -PPEGMA.
Preparação de AgNPs usando micelas de copolímero linear ou em forma de estrela
O PDMAEMA- b -PHEMA- b -PPEGMA ou (PDMAEMA- b -PHEMA- b -PPEGMA) 4 solução aquosa (pH 7,0) foram obtidos primeiro, para o qual o AgNO 3 solução foi adicionada ao disparar a reação de redução de DMAEMA com Ag + para formar AgNPs in situ no núcleo micelar. Pegando a razão molar de DMAEMA e AgNO 3 é igual a 9 como exemplo, em primeiro lugar, PDMAEMA- b -PHEMA- b -PPEGMA ou (PDMAEMA- b -PHEMA- b -PPEGMA) 4 com a mesma quantidade de [DMAEMA] =4,8 mM agitado em acetona (5 mL) por 4 h seguido pela adição de água destilada (20 mL) sob agitação durante a noite para formar micelas estáveis. Então AgNO 3 solução (220 μL, 48 mM) foi injetada gota a gota na solução acima e agitada a 25 ° C no escuro por 48 h. Finalmente, os AgNPs estabilizados com micelas poliméricas lineares ou em estrela foram preparados por coleta e liofilização antes do armazenamento a -20 ° C para os experimentos seguintes.
Ensaio antibacteriano
As investigações antibacterianas nas micelas de polímero estabilizadas AgNPs foram realizadas contra Escherichia coli DH5alpha ( E . coli DH5α) cepas usando meio Luria-Bertani (LB) como transportador para preparar diferentes concentrações das soluções de AgNPs estabilizadas de micelas de polímero por ultrassom. O monoclonal E . coli DH5α foram cultivados durante a noite em meio LB (5 mL) a 37 ° C em um agitador a 200 rpm antes da suspensão bacteriana ser diluída para 1 × 10 5 CFU / mL por meio LB. Depois de misturar um volume igual de bactérias diluídas com diferentes concentrações de micelas de copolímero ou AgNPs estabilizados de micelas e incubação a 37 ° C por 16 h, a mudança na densidade óptica no comprimento de onda de 600 nm foi caracterizada por um leitor de microplaca (Multiskan Spectrum, Thermo Scientific, Vantaa, Finlândia). Cada ensaio foi repetido seis vezes.
Avaliação de viabilidade celular
Para avaliar a viabilidade celular, foi realizado o ensaio do brometo de 3- (4,5-dimetiltiazol-2-il) -2,5-difeniltetrazólio (MTT) com células de carcinoma hepatocelular hepático (HepG2). Antes da semeadura das células, as células HepG2 foram primeiro incubadas em uma atmosfera umidificada de 5% de CO 2 a 37 ° C em meio Eagle modificado por Dulbecco (DMEM) suplementado com 10% de soro fetal bovino (FBS), penicilina (100 μL / mL) e estreptomicina (0,1 mg / mL). Em seguida, as células HepG2 foram semeadas em um meio DMEM fresco em uma placa de 96 poços a uma densidade de 1 × 10 4 por poço e cultivadas por 1 dia. Depois de substituir o meio DMEM em micelas de copolímero pré-preparadas ou soluções de AgNPs estabilizadas por micelas (100 μL) em várias concentrações, as células continuaram a ser cultivadas nas 24 horas seguintes. Depois de lavado com tampão PBS três vezes, os 20 μL de reagente MTT (5 mg / mL) e 180 μL de DMEM fresco foram então adicionados e incubados por mais 4 h. Finalmente, a solução foi alterada para 200 μL de DMSO e a placa foi agitada suavemente por 10 min. A absorvância a 570 nm foi medida com o leitor de microplacas mencionado acima. Os dados de seis experimentos paralelos foram calculados.
Simulação de Dinâmica de Partículas Dissipativas
A fim de analisar o processo de crescimento de AgNPs, simulação de dinâmica de partículas dissipativas (DPD), que foi baseada em modelos de granulação grossa, foi realizada usando o módulo mesocito do Materials Studio 8.0 (Accelrys Inc., San Diego, CA, EUA). Conforme mostrado no arquivo adicional 1:Figura S1, seis tipos de grânulos constituíram os copolímeros PDMAEMA- b -PHEMA- b -PPEGMA ou (PDMAEMA- b -PHEMA- b -PPEGMA) 4 :laranja representa o centro, verde claro para MAA1 (metacrilato próximo à cadeia lateral de etilamina), verde para DMA (cadeia lateral de aminoetil), rosa para HEMA, azul claro para MAA2 (metacrilato próximo à cadeia lateral de PEG) e azul para PEG. Um pequeno aglomerado com cristal de célula unitária (comprimento da rede:3,87 Å) consistia em quatro átomos de prata, marcados como uma conta de prata (cor dourada). Ao mesmo tempo, cada conta de água (W) na cor preta continha cinco moléculas de água. De acordo com nosso trabalho anterior, Arquivo adicional 1:Tabela S1 mostrou o resultado dos parâmetros de interação computacional [31, 32]. A 30 × 30 × 30 r c 3 A caixa de simulação cúbica com condições de contorno periódicas foi utilizada em todas as direções com 100.000 etapas de simulação total e etapa de tempo de integração de 0,05 ns.
Análise estatística
A análise estatística foi realizada usando um Student’s t de duas amostras teste com variância desigual. p <0,05 foi considerado estatisticamente significativo.
Resultados e discussão
Síntese e caracterização de copolímeros lineares / estrela
Copolímeros lineares PDMAEMA- b -PHEMA- b -PPEGMA e copolímeros estrela (PDMAEMA- b -PHEMA- b -PPEGMA) 4 foram sintetizados por ARGET ATRP polimerização de DMAEMA, HEMA e PEGMA com CuBr 2 / HMTETA como catalisador, Sn (outubro) 2 como agente redutor, e EBiB ou pentaeritritol que foi previamente acilado com BIBB como iniciador em tolueno (Esquema 2). A estrutura e composição dos polímeros alvo foram verificadas por 1 H NMR. Micelas poliméricas foram automontadas a partir de PDMAEMA- b -PHEMA- b -PPEGMA ou (PDMAEMA- b -PHEMA- b -PPEGMA) 4 com o DMAEMA como bloco funcional, onde o Ag + íons foram atraídos e reduzidos em AgNPs sem a participação de agente redutor extra. Os efeitos das estruturas topológicas dos copolímeros nos AgNPs foram discutidos e avaliados a partir das propriedades físico-químicas e atividades antibacterianas e anticâncer.
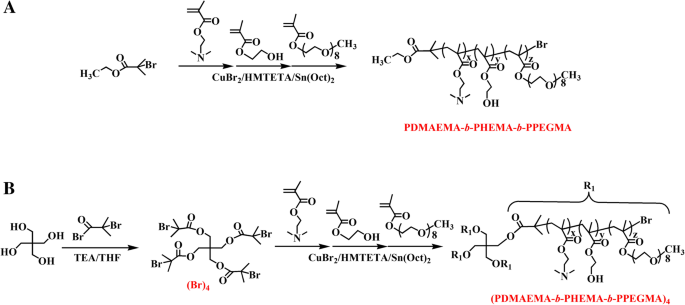
Rotas sintéticas de a PDMAEMA- b -PHEMA- b -PPEGMA e b (PDMAEMA- b -PHEMA- b -PPEGMA) 4
As estruturas químicas dos copolímeros lineares / estrela foram confirmadas por 1 H NMR. Primeiro, os grupos hidroxila finais do pentaeritritol foram inteiramente transferidos para o grupo bromo terminal (Br) 4 , conforme mostrado em 1 Espectro de H NMR (arquivo adicional 1:Figura S2). O pico a 4,33 ppm foi atribuído ao -C H 2 O- em pentaeritritol, enquanto o novo - (C H 3 ) 2 - o sinal apareceu em 1,94 ppm. E os valores da razão de integração dos picos em 1,94 ppm a 4,33 ppm foram em torno de 3. Como mostrado no arquivo adicional 1:Figura S3 e S4, o pico de -C (C H 3 ) 2 - apareceu a 1,94 ppm. Os sinais a 1,83 ppm, 1,00 ppm foram atribuídos a -C H 2 - e -CC H 3 - nas cadeias principais do metacrilato de metila, respectivamente. Os picos a 2,58 ppm e 4,08 ppm pertenciam às ressonâncias características dos dois prótons de metileno contíguos -C H 2 C H 2 - no bloco DMAEMA, e o pico em 2,29 ppm foi atribuído a prótons de metila -C H 3 -, que estava ligado a um grupo amina terciária. A presença de -C H 2 C H 2 - prótons de metileno conectados ao grupo hidroxila terminal na unidade HEMA apareceram em 4,08 ppm e 3,57 ppm, respectivamente. Os picos PEG característicos de -OC H 2 C H 2 - e terminal -C H 3 os prótons apareceram a 3,67 e 3,39 ppm, respectivamente. Picos de ligação dupla em 5,5–6,1 ppm desapareceram no 1 Espectro de H NMR. Calculado a partir dos valores da razão de integração do sinal (f) para (a) ( I f / eu a ), sinalizar (g) para (a) ( I g / eu a ), e sinalizar (h) para (a) ( I h / eu a ), respectivamente, PDMAEMA 19.3 - b -PHEMA 12,5 - b -PPEGMA 24,6 e (PDMAEMA 5.0 - b -PHEMA 5,6 - b -PPEGMA 5.0 ) 4 foram obtidos.
Preparação e caracterização das micelas de copolímero linear / estrela AgNPs estabilizados
O processo de formação de AgNPs foi mostrado no Esquema 1. Um único par de elétrons no átomo N que pertence ao grupo amina terciária na cadeia molecular de PDMAEMA, possuindo capacidade de coordenação e redução, podendo ser utilizado tanto como agente de aprisionamento e um agente redutor. Primeiro, os íons de prata foram capturados por PDMAEMA por causa da complexação entre Ag + e átomo de N, formando (Ag + ) Complexo -PDMAEMA. Posteriormente, Ag + foram reduzidos in situ para formar átomos de prata no estágio de nucleação. Posteriormente, a nucleação do Ag continuou com o crescimento do cristal de Ag, resultando na formação de AgNPs [26]. O bloco hidrofílico PPEGMA atuou como casca micelar, que forneceu uma camada protetora estável e melhorou ainda mais a estabilidade dos AgNPs. O efeito de estabilização estérica das micelas auto-organizadas dentro do sistema foi determinado pelo equilíbrio termodinâmico das micelas na estabilização dos AgNPs e a aglomeração entre os AgNPs. No caso de uma pequena quantidade de AgNPs, a estabilização estérica do copolímero pode impedir a agregação adicional dos AgNPs. Com o aumento do número de Ag, a estabilidade das micelas aos AgNPs seria enfraquecida e então a possibilidade de colisão entre as partículas aumentaria, resultando no aumento do tamanho dos AgNPs. Aproveitando a estabilização espacial das micelas, os AgNPs que preparamos possuem tamanho de partícula controlado, o que é de grande potencial para aplicações antibacterianas.
A simulação DPD foi realizada para investigar o processo de crescimento e distribuição de AgNPs, com as mesmas concentrações do experimento real (PDMAEMA / AgNO 3 razão molar =1/1, as frações de volume de copolímeros lineares, grânulos de Ag e água sendo 10%, 0,23% e 89,77%, respectivamente). A Figura 1 revelou que as contas de PDMAEMA- b -PHEMA- b -PPEGMA e AgNPs mostraram inicialmente um estado irregularmente distribuído em solução aquosa. Com o passar do tempo, oito micelas de copolímero automontadas foram finalmente formadas e dispersas uniformemente, enquanto todas as contas de Ag foram carregadas nas micelas. Pode-se observar que AgNPs em equilíbrio podem ser estabilizados nas micelas do copolímero sem mais agregação, indicando que as micelas automontadas foram capazes de prevenir a agregação adicional de AgNPs e então atingir o objetivo de controlar seu tamanho de partícula e distribuição.
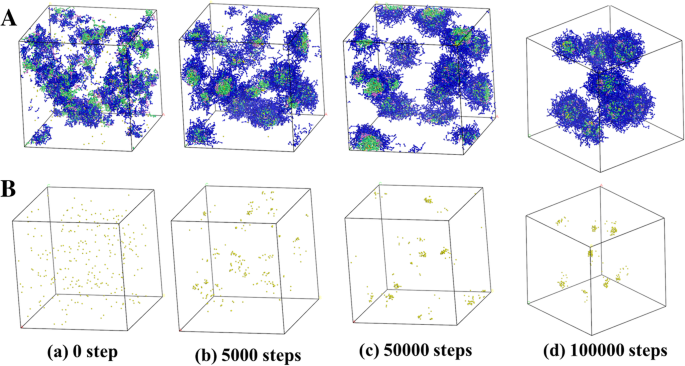
Simulação DPD do processo de crescimento e distribuição de AgNPs com PDMAEMA- b -PHEMA- b -PPEGMA em PDMAEMA / AgNO 3 razão molar =1/1 em diferentes tempos de simulação. a As moléculas de água foram escondidas para maior clareza. b Apenas os AgNPs foram mostrados
A caracterização de FT IR de copolímeros lineares / estrela e seus AgNPs estabilizados por micelas foram mostradas no arquivo adicional 1:Figura S5. Obviamente, em comparação com os copolímeros lineares / estrela simples, a vibração de alongamento -COOR em 1730 cm −1 e a vibração de flexão da ligação C-N em PDMAEMA em 1457 cm −1 diminuiu após a formação de AgNPs, indicando que os AgNPs foram carregados com sucesso nas micelas de copolímero. A natureza cristalina de AgNPs estabilizados com micelas de copolímeros lineares / estrela foi confirmada por espectro de difração de raios-X (arquivo adicional 1:Figura S6). Os valores dos picos de difração de 38,5 °, 44,8 °, 64,2 ° e 78,0 ° corresponderam às faces cristalinas (111), (200), (220) e (311) da estrutura cristalina cúbica de face centrada (fcc) de nanopartículas contidas em Ag [33, 34]. Os potenciais zeta de AgNPs estabilizados com micelas de copolímeros lineares / estrela foram medidos. Como mostrado na Fig. 2, os potenciais zeta desses AgNPs estabilizados de micelas de copolímero estavam em torno de 15,0-23,2 mV. Além disso, com o aumento da quantidade de AgNO 3 , o potencial zeta de AgNPs estabilizados de micelas aumentou notavelmente por causa da decoração de mais AgNPs. Para investigar melhor a dispersão de AgNPs e o efeito estabilizador de micelas em AgNPs, as simulações DPD de micelas de copolímeros lineares / estrela estabilizaram AgNPs em diferentes PDMAEMA / AgNO 3 relações molares foram realizadas. Conforme mostrado na Fig. 2, os resultados também demonstraram que os tamanhos dos AgNPs foram proporcionais às razões em que o número de pequenos AgNPs agregados aumentou e a distância entre eles diminuiu, levando ao aumento da probabilidade de colisão e aglomeração.
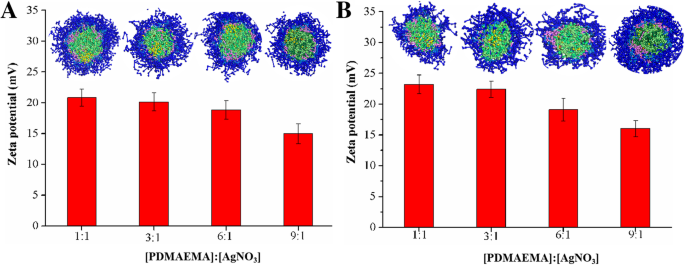
Os potenciais zeta e as visualizações em corte transversal de a linear e b micelas de copolímeros estrela estabilizaram AgNPs. Os dados foram coletados com diferentes PDMAEMA / AgNO 3 razões molares de (a) 1/1, (b) 3/1, (c) 6/1, (d) 9/1
Os espectros para AgNPs estabilizados de micelas de quatro copolímeros lineares possuíam uma pequena diferença no pico de absorção máximo localizado em torno de 437 nm, que era o pico de absorção de ressonância plasmônica de superfície (SPR) característico de AgNPs esféricos / quase esféricos, relacionados tanto à excitação de ressonância quanto à transição entre bandas de eles (Fig. 3a). O resultado provou que o grupo amina terciária nos copolímeros lineares poderia reagir com o nitrato de prata e a formação de AgNPs dificilmente dependia do impedimento estérico das micelas dos copolímeros lineares. Posteriormente, os copolímeros em estrela com o bloco e grau de polimerização semelhantes nas mesmas condições, o tamanho de partícula de AgNPs diminuiu quando o PDMAEMA / AgNO 3 razão molar aumentada. Foi refletido através do deslocamento hipsocrômico nos espectros de UV-Vis, onde os picos máximos de absorção foram em 429 nm, 426 nm, 421 nm e 414 nm, respectivamente, devido à quantidade diferente de AgNPs formados pela redução da coordenação na amina terciária de micelas de copolímero em estrela (Fig. 3b). Em outras palavras, a estabilização estérica dos copolímeros estrela poderia estabilizar melhor os AgNPs e prevenir sua agregação adicional em pequenas quantidades de AgNPs. Em contraste, o aumento na quantidade de AgNPs enfraqueceu o efeito estabilizador, o que forneceu mais oportunidades para a colisão de AgNPs e, finalmente, resultou em AgNPs maiores. Comparando a Fig. 3a com a Fig. 3b, os picos de absorção em 437 nm de AgNPs dentro de micelas de copolímero linear possuíam uma distribuição de comprimento de onda mais ampla, enquanto AgNPs dentro de micelas de copolímero em estrela estavam em cerca de 422 nm. Aqui, não houve deslocamento para o azul mostrado nos espectros dos copolímeros lineares, o que poderia ser explicado pelo fato de que os blocos de micelas de copolímeros lineares têm efeito mais fraco sobre o impedimento estérico para AgNPs, o que resultou no aumento da probabilidade de aglomeração colisional entre AgNPs.
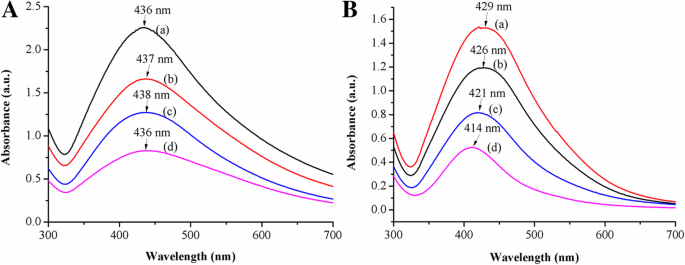
Espectros UV-Vis de a linear e b micelas de copolímeros em estrela estabilizaram AgNPs em diferentes PDMAEMA / AgNO 3 razões molares de (a) 1/1, (b) 3/1, (c) 6/1, (d) 9/1
Medições de TEM foram então realizadas para determinar o tamanho, distribuição de tamanho e morfologia dos AgNPs. As imagens TEM de AgNPs dependiam de AgNO 3 as taxas de alimentação foram mostradas na Fig. 4. Quando o PDMAEMA / AgNO 3 as razões molares foram 6 e 1, calculadas usando o software ImageJ, o tamanho de partícula de AgNPs estabilizados de micelas de copolímeros lineares foram 11,1 nm e 25,7 nm, enquanto o diâmetro de AgNPs estabilizados de micelas de copolímeros em estrela foram 3,7 nm e 6,4 nm, respectivamente. O aumento de AgNO 3 o conteúdo levou a mais átomos de prata nas micelas, maior energia de superfície e o número de AgNPs agregados aumenta de acordo com um tamanho de AgNPs maior. Ficou claro que os AgNPs estabilizados por micelas eram monodispersos e esféricos com um pouco irregular de AgNPs estabilizados de micelas de copolímero linear. Os tamanhos de AgNPs estabilizados por micelas complementaram ainda mais os resultados de UV-Vis.

Imagem TEM de a , b copolímeros lineares e c , d micelas de copolímeros em estrela estabilizaram AgNPs em diferentes PDMAEMA / AgNO 3 razões molares: a , c 1/6, b , d 1/1
Estabilidade das micelas de copolímeros lineares / estrela AgNPs estabilizados
The stability of the linear/star copolymers micelles stabilized AgNPs is of great influence for the development of biomedical field. Obviously, the SPR peak in UV-Vis spectra (Fig. 5) of star copolymer micelles stabilized AgNPs did not display any significant changes for at least 1 month even after further diluted by one time, three times, and six times, indicating that the prepared AgNPs appeared well long-term colloidal stability within the experimental concentration range. However, the results of linear copolymer micelles stabilized AgNPs showed that the UV absorption wavelength decreased slightly as the increase of dilution ratios. And the micelles concentration of linear copolymer decreased after 1 month of placement may lead to insufficient provision of steric hindrances to stabilize AgNPs.
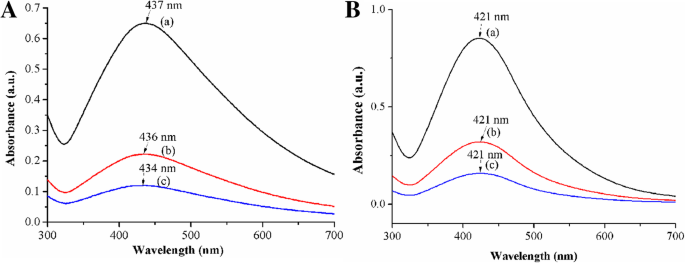
UV-Vis spectra of a linear copolymers and b star copolymers micelles stabilized AgNPs solution at PDMAEMA/AgNO3 molar ratio =6/1 after 1 month at the diluted times of 1 (a), 3 (b), and 6 (c), respectively
From the thermogravimetric analysis curves in Fig. 6, it was shown that the initial decomposition temperature (T início ) of linear copolymers micelles was 217 °C, which shifted to 172 °C after silver loading, suggesting that the linear copolymer micelles stabilized AgNPs showed lower thermal stability than the pure linear copolymers micelles. It may be due to the fact that the chemical structure of PDMAEMA in the molecular chain changes and the catalytic effect of AgNPs in the thermal degradation process cannot be ignored [35]. As for star copolymers and their stabilized AgNPs, T início were around 213 °C. The two Tonset of star copolymers micelles and their micelles stabilized AgNPs showed very few gaps, which could be speculated that the more stable star-shaped copolymers have better effect on stabilizing AgNPs than the linear copolymers. Combined the results of UV-Vis, TEM, and TGA measurements, it could be inferred that compared to the linear copolymers, the star copolymers have superior advantages in topology for stabilizing AgNPs, such as better stability, more uniform dispersion, slower nucleation rate during reduction, and the better product with a smaller and more uniform size of AgNPs.
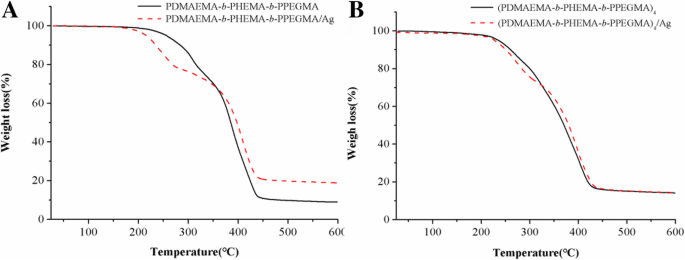
TGA curves of a linear copolymers and b star copolymers micelles and their micelles stabilized AgNPs at PDMAEMA/AgNO3 molar ratio =6/1
Antibacterial Activity and Cell Viability
To evaluate the antibacterial activities of the linear/star copolymers micelles stabilized AgNPs by optical density (OD600 ) measurements, E . coli DH5α was selected as the Gram-negative bacterial model. The absorbance at 600 nm after incubation was tested by incubating the bacteria with the eight different concentrations of micelles and micelles stabilized AgNPs at 37 °C. Results shown in Fig. 7a illustrated that the bacterial growth curves were highly correlated with the AgNPs concentration in the LB medium. The inhibition of linear/star copolymers micelles on the growth of bacteria was weak, which was not fatal to bacteria. However, as the concentration of linear/star copolymers micelles stabilized AgNPs increased, the survival rate of E . coli DH5α was significantly inhibited, indicating a strong antibacterial efficacy of AgNPs against E . coli DH5α. The concentrations of linear copolymers micelles stabilized AgNPs preventing the bacterial growth in the experiments were relatively higher than those of star copolymers micelles stabilized AgNPs, which might due to the fact that bigger size of AgNPs could lead to a lower antibacterial performance because of the inefficient exposure of bacteria to AgNPs and relatively slow release behavior of AgNPs.
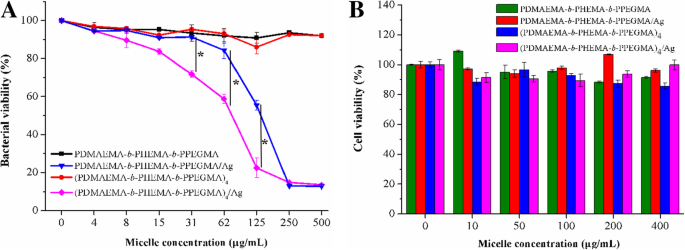
a Antibacterial activity and b cell viability of linear copolymers and star copolymers micelles stabilized AgNPs at PDMAEMA/AgNO3 molar ratio =6/1. * p <0.05, two-tailed Student t teste
Cancer is an uncontrollable disease of cell growth that can occur in any part of the body. The most common cancers are liver cancer, breast cancer, colorectal cancer, and lung cancer. Among them, the liver cancer has the much higher prevalence in both developed and developing countries. Therefore, the toxicity experiments of the linear/star copolymers micelles stabilized AgNPs on HepG2 cells were carried out, in which HepG2 cells were incubated with linear/star copolymers micelles stabilized AgNPs at different concentrations (10, 50, 100, 200, 400 mg/L, respectively) for 48 h and the cell viability with MTT assay was the most intuitive data to evaluate the biocompatibility of the composite material. As shown in Fig. 7b, the percentage of viable cells for the linear/star copolymers micelles stabilized AgNPs exhibited negligible cytotoxicity, and was about 90% viability even at the highest concentration applied (400 μg/mL) after 48-h incubation, indicating the advantageous cytocompatibility of the micelles stabilized AgNPs within a relatively wide range of concentration.
Conclusão
In conclusion, PDMAEMA-based linear and star copolymer micelles as effective delivery carriers for silver-bearing antimicrobials were developed, and their in vitro antimicrobial efficacy and cell viability were investigated. Being a reducing agent and a stabilizer simultaneously, the micellar PDMAEMA core acted as loading platform for AgNPs in situ translated from the precursor silver nitrate. In silico simulation and experimental results indicated that both types of the copolymer micelles could generate monodisperse and spherical AgNPs. Compared with linear copolymers sliver-bearing micelles, the fabricated star copolymers micelles stabilized AgNPs exhibited smaller average size, better stability against dilution and pyrogenic decomposition, and enhanced antibacterial activities against E . coli DH5α due to the serious damage of bacterial membrane caused by loaded AgNPs. Moreover, both types of copolymer micelles stabilized AgNPs possessed great cytocompatibility toward HepG2 cells. Therefore, these studies may provide some guidance for the construction of more effective AgNPs weapon with well-defined and feasible polymer topology for combating the multiple bacteria-induced infections.
Disponibilidade de dados e materiais
Os conjuntos de dados usados e / ou analisados durante o estudo atual estão disponíveis junto ao autor correspondente, mediante solicitação razoável.
Abreviações
- AgNPs:
-
Nanopartículas de prata
- DMAEMA:
-
2-(dimethylamino) ethyl methacrylate
- HEMA:
-
2-hydroxyethyl methacrylate
- PEGMA:
-
Poly (ethylene glycol) methyl ether methacrylate
- CuBr2 :
-
Cupric bromide
- 1 H NMR:
-
Proton nuclear magnetic resonance
- FTIR:
-
Fourier-transform infrared spectroscopy
- KBr:
-
Potassium bromide
- UV-Vis:
-
Visível por ultravioleta
- MTT:
-
3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide
- HepG2:
-
Liver hepatocellular carcinoma
- DPD:
-
Dissipative particle dynamics
- SPR:
-
Ressonância de plasmon de superfície
- XRD:
-
Difração de raios X
Nanomateriais
- Preparação e propriedades magnéticas de nanopartículas de espinélio FeMn2O4 dopadas com cobalto
- Em direção aos nanofluidos de TiO2 - Parte 1:Preparação e propriedades
- Síntese fácil e propriedades ópticas de pequenos nanocristais de selênio e nanorods
- Preparação e atividade de hidrogenação catalítica aprimorada de nanopartículas de Sb / Palygorskite (PAL)
- Estudo in vitro da influência das nanopartículas de Au nas linhas celulares HT29 e SPEV
- Biossegurança e capacidade antibacteriana do grafeno e do óxido de grafeno in vitro e in vivo
- Preparação e desempenho fotocatalítico de fotocatalisadores de estrutura oca LiNb3O8
- Nanocompósitos de poli (N-isopropilacrilamida) magnético:efeito do método de preparação nas propriedades antibacterianas
- Síntese de um vaso de nanoplacas Cu2ZnSnSe4 e sua atividade fotocatalítica orientada por luz visível
- Atividade antibacteriana de solução de nanopartículas de prata / quitosana preparada in situ contra cepas de Staphylococcus aureus resistentes à meticilina



