Síntese seletiva de fase de nanopartículas de CIGS com fases metaestáveis por meio do ajuste da composição do solvente
Resumo
I-III-VI 2 compostos têm mostrado grande interesse na aplicação de semicondutores funcionais. Entre eles, Cu (In, Ga) S 2 tem sido um candidato promissor devido às suas excelentes propriedades optoeletrônicas. Embora os polimorfos de Cu (In, Ga) S 2 têm atraído atenções extensas, os esforços para desenvolver as metodologias para a síntese deles controlada por fase são raros. Neste artigo, relatamos uma síntese seletiva de fase de nanopartículas de CIGS com fases metaestáveis por meio da simples alteração da composição dos solventes. Para a síntese química úmida, a microestrutura dos núcleos iniciais é decisiva para a estrutura cristalina dos produtos finais. Na formação de Cu (In, Ga) S 2 , o ambiente solvente é o fator chave, o que pode afetar a coordenação de monômeros e influenciar as condições termodinâmicas de nucleação de Cu-S. Além disso, wurtzita e zincblende Cu (In, Ga) S 2 nanopartículas são preparadas seletivamente escolhendo en puro ou sua mistura com água desionizada como solvente de reação. O wurtzite Cu (In, Ga) S 2 sintetizado possuem uma lacuna de banda de 1,6 eV e uma mobilidade de portadora de 4,85 cm 2 / Vs, que indica seu potencial para construir uma heterojunção com CdS hexagonal estruturado para células solares.
Introdução
I-III-VI 2 semicondutores compostos apresentam grandes promessas para as aplicações de dispositivos fotoelétricos, devido às suas propriedades ópticas e elétricas vantajosas [1,2,3,4,5]. Especialmente, as células solares de película fina baseadas em Cu (In, Ga) Se 2 (CIGSe) alcançaram eficiência de conversão de energia superior a 22% [6]. No entanto, em comparação com as tecnologias fotovoltaicas baseadas em silício, o custo das células solares baseadas em semicondutores compostos ainda precisa ser reduzido significativamente [7]. Recentemente, CuInS 2 (CIS) e Cu (In, Ga) S 2 (CIGS), em que o selênio (Se) é substituído pelo enxofre menos tóxico e mais barato (S), atraiu grandes interesses como alternativas atraentes ao CIGSe [8,9,10]. Além da escolha dos materiais, geralmente acredita-se que o processo a vácuo baseado na suspensão de nanopartículas (NPs) também é promissor na redução do custo das células solares baseadas em CIGS [7, 11]. Portanto, CIGS NPs desempenham um papel vital no desenvolvimento de células solares de filme fino de baixo custo [12,13,14].
Nas últimas duas décadas, muitos esforços têm sido feitos para sintetizar os calcogenetos NPs com as propriedades desejadas para aplicação fotovoltaica [15,16,17,18,19,20,21]. O controle de fase é um dos pontos mais importantes para a síntese de NPs de calcogeneto, pois suas propriedades optoeletrônicas dependem da estrutura cristalina [22,23,24,25,26]. De acordo com a literatura [27,28,29], CIGS pode ter três polimorfos:uma fase termodinamicamente estável com estrutura de calcopirita tetragonal (CH) e duas fases metaestáveis com estrutura de zincblenda cúbica (ZB) e estrutura wurtzita hexagonal (WZ), respectivamente. Os estudos anteriores focaram principalmente no CIS e CIGS estruturados em CH [18, 30, 31]. NPs CIS estruturados com ZB e WZ metaestáveis preparados por meio de abordagem de injeção a quente foram relatados pela primeira vez por Pan et al. em 2008 [32]. Depois disso, NPs CIS com fase metaestável também foram obtidos por síntese solvotérmica [33, 34] e decomposição térmica de precursores [35, 36]. No entanto, até onde sabemos, todos esses relatórios anteriores sobre a síntese da fase metaestável CIS ou CIGS envolvem aditivos indutíveis [37, 38], ligantes caros [32, 39] ou precursores complexos [34,35,36]; uma síntese de baixo custo e fácil de CIGS NPs ainda permanece um desafio.
A formação de NPs geralmente inclui duas etapas, a saber, a etapa de nucleação e a etapa de crescimento cristalino [40, 41]. Estudos anteriores [26, 42, 43] indicam consistentemente que CIGS NPs foram formados em duas etapas:(1) a formação de núcleos de cristal Cu-S por meio da reação rápida entre Cu + e S 2− ; e (2) a incorporação de índio e gálio nos núcleos de cristal de Cu-S por meio da difusão e / ou troca catiônica. Além disso, a estrutura cristalina dos CIGS NPs finais pode depender principalmente da estrutura dos núcleos Cu-S [25, 35, 44]. Aqui, relatamos uma síntese solvotérmica em um único recipiente de NPs CIGS com fases metaestáveis, sem a necessidade de aditivos, ligantes caros ou preparação de precursores complexos. Simplesmente alterando a composição de solventes para a reação solvotérmica, o ambiente termodinâmico de nucleação Cu-S pode ser ajustado, por sua vez CIGS NPs estruturados em ZB ou WZ podem ser obtidos seletivamente. Além da discussão do mecanismo de síntese seletiva de fase, as propriedades elétricas e ópticas dos produtos com diferentes estruturas cristalinas também são comparadas neste estudo.
Métodos Experimentais
Materiais
CuCl 2 · 2H 2 O (99,9%), enxofre em pó (99,9%), etilenodiamina anidra (en, 99%) e etanol anidro (99,7%) foram adquiridos de Chengdu Kelong Chemical Co., Ltd. InCl 3 (99,9%) foi adquirido da Aladdin. Ga (acac) 3 (99,99%) foi adquirido da Sigma-Aldrich. Todos os produtos químicos foram usados conforme recebidos.
Síntese solvotérmica de NPs CIGS
Para a síntese de CIGS NPs estruturados em WZ, uma solução de precursor de metal foi preparada pela dissolução de CuCl 2 · 2H 2 O (0,164 g, 0,96 mmol), InCl 3 (0,192 g, 0,868 mmol) e Ga (acac) 3 (0,068 g, 0,186 mmol) em 5 ml de etilenodiamina. Pó de enxofre (0,0826 g, 2,58 mmol) foi disperso em 5 ml de etilenodiamina através de um tratamento ultrassônico a 60 ° C por 15 min. A solução de precursor de metal foi misturada com a dispersão de enxofre em uma autoclave forrada de Teflon de 20 ml. Cerca de 6 ml de etilenodiamina foram então adicionados para fazer com que o volume da solução de reação fosse 80% do volume da autoclave revestida com Teflon. A autoclave foi selada e tratada com sonicação a 60 ° C durante 15 min. Em seguida, a autoclave foi levada ao forno. A temperatura no forno foi elevada da temperatura ambiente para 200 ° C e mantida por 24 h, sendo então resfriada até a temperatura ambiente naturalmente. O precipitado foi separado por centrifugação, lavado com um solvente misto de etanol e água desionizada por cinco vezes e seco em vácuo a 60 ° C por 4 h.
Para a síntese de CIGS NPs estruturados em ZB, a solução de precursor de metal foi preparada por dissolução de sais de metal em 5 ml de água desionizada. Outros procedimentos e condições sintéticas permaneceram inalterados.
Caracterização
A fase dos NPs sintetizados foi identificada por difração de raios-X (XRD) em um difratômetro Bruker D8 Advance equipado com radiação monocromatizada Cu-Kα (λ =1,5418 Å). Os dados de difração foram coletados com um incremento de ângulo de 0,02 ° a uma taxa de varredura de 0,1 s / etapa. Imagens de microscopia eletrônica de varredura (SEM) foram obtidas usando um ZEISS EVO @ LS15 SEM operou sob 15 kV. O ZEISS EVO @ LS15 SEM é equipado com um Bruker Nano GmbH XFlash Detector 5010, que foi usado para estimar a proporção estequiométrica por espectroscopia de energia dispersiva de raios-X (EDS). As propriedades ópticas dos produtos preparados foram caracterizadas por um espectrofotômetro Agilent Cary5000 UV-Vis-IR. As propriedades elétricas foram calculadas com base nas medições do efeito Hall usando o sistema Swin Hall 8800. Os CIGS NPs sintetizados foram depositados em substratos de vidro via spray coating, e os contatos elétricos foram formados por pasta de prata para medições de efeito Hall. As espécies em soluções precursoras foram estudadas por espectrofotômetro UV-Vis-IR (Agilent Cary5000) e espectrofotômetro Raman (Renishaw Invia).
Resultados e discussão
Para a síntese dos CIGS NPs, o enxofre (S) disperso em etilenodiamina (en) foi misturado com os sais metálicos que se dissolveram em en ou água desionizada. Em seguida, as misturas com diferentes composições de solventes foram tratadas por ultrassom a 60 ° C por 15 min, seguido de reação a 200 ° C por 24 h sob a condição solvotérmica. pt com um grupo amina duplo e uma cadeia de carbono curta foi usado para estabilizar a fase metaestável CIGS. Como mostrado na Fig. 1, os picos de XRD dos NPs sintetizados são bem idênticos ao padrão CIS wurtzite relatado [32,33,34], indicando que o cristal dos NPs fabricados derivados de solvente en puro é uma estrutura wurtzita hexagonal . Enquanto isso, para NPs preparados no solvente de mistura de água desionizada e en e, o padrão de XRD é bem consistente com o do CIS estruturado por ZB [32, 34, 39]. Assim, a síntese de fase seletiva de CIGS NPs com fase metaestável pode ser alcançada simplesmente alterando a composição do solvente da reação.
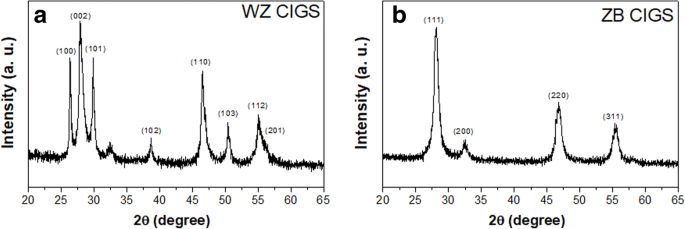
Padrões de XRD de CIGS NPs sintetizados em solvente en puro ( a ) e solvente de mistura en / água ( b )
Como mencionado acima, a nucleação de aglomerados de Cu-S é cineticamente favorável e decisiva para a estrutura cristalina dos produtos quaternários finais. O ambiente de solvente pode afetar a reatividade do sal de metal e precursores de calcogênio, por sua vez, influenciar a microestrutura dos aglomerados de Cu-S. Sabe-se que en é um bom agente de ataque e pode reduzir parcialmente o precursor de calcogênio [35, 45]. Para investigar o impacto da composição do solvente no status do enxofre, os espectros Raman do solvente en, mistura en / água, solução de S em en e a solução de mistura S em en / água foram coletados. Conforme mostrado na Fig. 2, um pico dividido em 811 cm −1 pode ser observada no espectro da solução de S em en, embora esteja ausente nas outras três contrapartes. Este pico de divisão pode indicar que o status do precursor do enxofre no en puro é diferente daquele na mistura en / água. Parece que a introdução de H 2 O enfraqueceria a interação entre S e o grupo amino (veja a linha azul na Fig. 2). Além disso, o en pode atuar como um forte agente quelante para íons metálicos devido à sua característica de grupo amina dupla. A coordenação da amina para Cu 2+ difere no en puro e na mistura de água en e desionizada, o que é indicado pelo fato de que a cor da solução en de CuCl 2 é verde escuro, enquanto o da solução aquosa de CuCl 2 é azul. Com base na constante de estabilidade e no equilíbrio de dissociação dos complexos, a concentração molar de Cu 2+ livre no en puro e na água são avaliados como 3,12 × 10 −22 M e 0,192 M, respectivamente (consulte os detalhes do cálculo no arquivo Adicional 1). Espectros Raman das soluções de CuCl 2 em en puro e a mistura de en e água parecem ser semelhantes (Arquivo adicional 1:Figura S1). Isso deve ser atribuído às vibrações de Cu – NH 2 ligação quelante existe em ambas as soluções. A Figura 3 mostra os espectros de absorção das soluções de CuCl 2 em en puro, água e sua mistura. A ampla absorção em 250-350 nm de CuCl 2 no solvente da mistura implica que o status de coordenação de Cu 2+ pode ser uma combinação equilibrada daquela em en puro e água. Pegue a concentração avaliada de Cu 2+ livre em consideração, é razoável propor que haja um maior número de monômeros livres prontos para reagir com o precursor S a uma temperatura relativamente baixa no en / H 2 O mistura do que naquele puro en. Para a reação na mistura de solvente, o Cu 2+ livre pode reagir com S elementar a partir de núcleos Cu-S em temperatura moderada. Enquanto isso, a nucleação de Cu-S em puro en pode acontecer em temperatura elevada entre Cu 2+ e \ ({S} _n ^ {2-} \), uma vez que a alta temperatura facilita a dissociação de Cu [en] 2+ complexo e a redução do S elementar por en puro [45]. Assim, os diferentes ambientes de solvente resultam em diferentes condições termodinâmicas e espécies reagentes para nucleação de Cu-S, por sua vez levando a diferentes microestruturas de aglomerados de Cu-S. Após a incorporação de In e Ga nos aglomerados Cu-S, CIGS NPs com diferentes estruturas cristalinas podem ser obtidos a partir de en puro e sua mistura com água, respectivamente. De acordo com o mecanismo apresentado aqui, o pico menor em ~ 32 ° na Fig. 1a, que pode ser indexado a CIGS estruturados com ZB, deve ser atribuído ao traço de água existente em solventes.
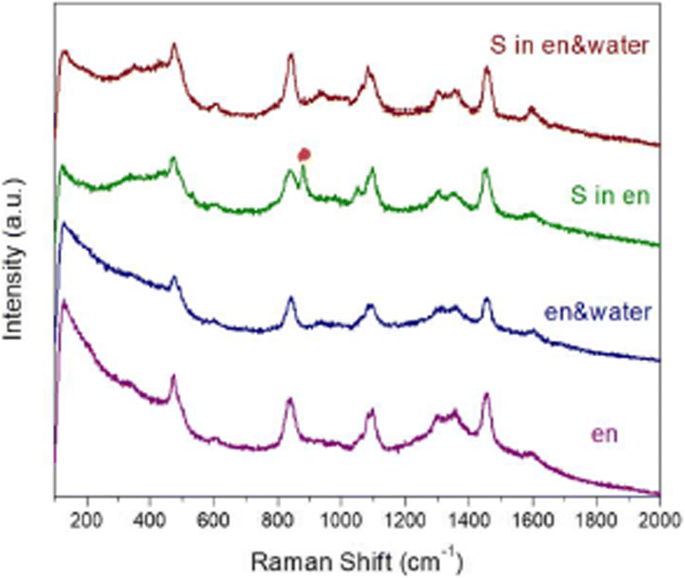
Espectros Raman de en puro (linha roxa), a mistura de en e água deionizada (linha azul), as soluções do precursor S em en puro (linha verde) e as soluções do precursor S na mistura de en e deionizada água (linha vermelha)
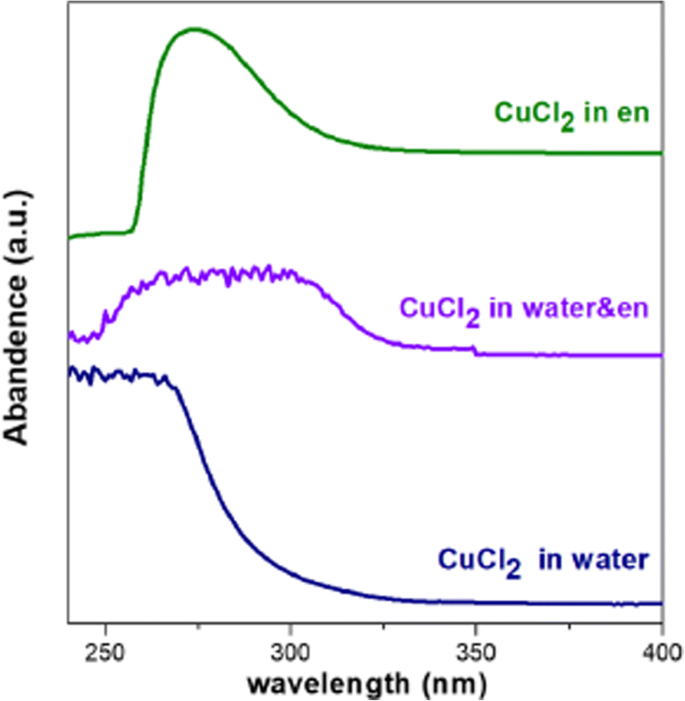
Espectros de absorção das soluções do precursor Cu em en (linha verde), água deionizada (linha azul) e a mistura de en e água deionizada (linha violeta)
A composição dos solventes da reação também pode afetar as morfologias dos CIGS NPs preparados. Os NPs CIGS estruturados em WZ, que são derivados de en puro, exibem uma morfologia particulada uniforme com um diâmetro de 50 nm e são bastante monodispersos (Fig. 4a, b). No entanto, a monodispersidade de NPs CIGS estruturados em ZB é pobre e sua morfologia é muito mais complexa. Os pellets, flocos e hastes em nanoescala podem ser observados na Fig. 4c, d. Essa diferença morfológica é consistente com o mecanismo de reação dependente de solvente proposto acima. Para a síntese de NPs CIGS estruturados por WZ em en puro, a nucleação é difícil em uma temperatura baixa por causa da ligação quelante entre en e Cu 2+ . Em uma temperatura elevada, monômeros metálicos livres são fornecidos pela dissociação de compostos complexos, e o precursor S está em uma forma reativa e solúvel de \ ({S} _n ^ {2-} \). A alta concentração de monômeros e o ambiente de reação homogêneo tendem a gerar numerosos núcleos Cu-S. Assim, a maioria dos monômeros é consumida pela nucleação, e o crescimento dos aglomerados é limitado. Este processo é benéfico para a morfologia uniforme e fina dos NPs resultantes. Enquanto isso, a nucleação de Cu-S é possível ocorrer a uma temperatura baixa durante a síntese de CIGS estruturados em ZB, porque considerável quantidade de Cu 2+ livre existem na mistura de en e água em uma temperatura ambiente, e eles podem reagir com o elementar sólido S. Os monômeros reativos suplementares fornecidos em alta temperatura tenderiam a facilitar o crescimento de aglomerados, mas não a gerar novos núcleos, por meio da reação na solução interfaces sólidas [40, 41]. Além disso, en molecular não pode fornecer um forte efeito de confinamento espacial para os aglomerados durante seu crescimento, porque os segmentos de en molecular são curtos. Assim, os NPs CIGS estruturados em ZB apresentam vários formatos, como pelotas, flocos e hastes. O ligeiro agrupamento dos NPs observados em imagens SEM pode ser causado pela evaporação do solvente durante o teste de preparação da amostra.

Imagens representativas de SEM da estrutura WZ ( a , b , c ) e estruturado em ZB ( c , b , d ) CIGS NPs
A composição dos CIGS NPs preparados foi determinada usando EDS e os resultados foram resumidos na Tabela 1. A composição do elemento em CIGS NPs estruturados WZ e ZB é aproximadamente consistente com a composição química estequiométrica. No entanto, ambos mostram uma característica pobre em enxofre, ou seja, [0,5Cu + 1,5 (In + Ga)]:S =1:0,96 e 1:0,91 para GIGS estruturados WZ e ZB respectivamente, embora ~ 35 % de enxofre em excesso foi aplicado nos materiais de partida. Este desvio da estequiometria pode ser corrigido por um tratamento térmico em atmosfera de enxofre durante a fabricação de camadas absorvedoras de CIGS por meio de abordagens sem vácuo baseadas em NPs. Pode-se ver que os NPs CIGS estruturados em WZ possuem uma característica pobre em cobre (Cu:(In + Ga) =1:1,16) que é desejável para aplicações fotovoltaicas [46], enquanto o estruturado em ZB é ligeiramente rico em cobre (Cu:(In + Ga) =1:0,96). Isso indica que a composição do solvente pode ter uma influência cinética na incorporação de In e Ga em aglomerados de Cu-S. O ambiente en puro pode induzir uma cinética favorável à incorporação de In e Ga.
As propriedades ópticas e elétricas de NPs CIGS sintetizados com diferentes estruturas cristalinas foram investigadas e comparadas. A energia do intervalo de banda (E g ) de NPs CIGS estruturados com WZ e ZB foi estimado com base nos espectros de absorção de UV-vis-IR [47]. Ambos exibem E g em torno de 1,6 eV (Arquivo adicional 1:Figura S2), o que é atraente para os dispositivos fotovoltaicos [48]. De acordo com a medição do efeito Hall, todos os CIGS NPs sintetizados apresentam um comportamento de condução do tipo N, que deve ser atribuído à sua característica pobre em enxofre. Os valores de resistividade da folha, concentração de portador e mobilidade listados na Tabela 2 são comparáveis aos valores relatados [49, 50]. Estes resultados sugerem ainda que os CIGS estruturados com WZ sintetizados possuem propriedades elétricas superiores em relação aos estruturados com ZB. É relatado que uma interface rica em enxofre entre CuInSe 2 e o CdS melhoraria a eficiência das células solares por causa da estrutura bandgap otimizada [51]. As excelentes propriedades ópticas e elétricas tornam os NPs WZ-CIGS muito atraentes para a construção de heterojunções com WZ-CdS. Além da otimização do bandgap, as heterojunções WZ-CIGS / WZ-CdS também podem se beneficiar de uma melhor correspondência de rede, pois ambas são hexagonais estruturadas. É importante notar que a mobilidade da portadora medida do WZ-CIGS é tão alta quanto 4,85 cm 2 / Vs, que é comparável ao do óxido de índio, gálio e zinco (IGZO) (~ 5–10 cm 2 / Vs) [52]. Geralmente, acredita-se que o IGZO é um dos candidatos mais promissores para painel de exibição de próxima geração [53]. Portanto, acreditamos que o CIGS também é uma grande promessa para aplicações optoeletrônicas.
Para verificar a viabilidade da estratégia apresentada para a síntese seletiva de fase de calcogenetos multinários à base de cobre, CIS e CuGaS 2 (CGS) também foram preparados usando en puro ou a mistura de en e água como solventes. Os padrões de XRD dos produtos demonstram que as estruturas cristalinas CIS e CGS com WZ e ZB foram sintetizadas seletivamente (Arquivo adicional 1:Figura S3). A síntese bem-sucedida de CIS, CGS e CIGS com seletividade de fase indica que a abordagem apresentada também possui a capacidade de ajustar a razão In / Ga dos produtos facilmente, por sua vez, o E g dos semicondutores compostos podem ser projetados, o que é valioso para a preparação de materiais absorventes para células solares [54].
Conclusão
Em resumo, a síntese de fase seletiva de CIGS NPs com fases metaestáveis é obtida simplesmente mudando a composição dos solventes da reação. A coordenação da amina aos monômeros metálicos difere no en puro e na mistura de en e água desionizada. E assim, a condição termodinâmica de nucleação do Cu-S, que é cineticamente preferida durante a síntese solvotérmica, pode ser influenciada pelo ambiente do solvente. Os NPs CIGS estruturados com WZ e ZB são preparados seletivamente através do controle da microestrutura de núcleos Cu-S pré-formados. Os NPs CIGS WZ-estruturados resultantes exibem uma morfologia uniforme e excelentes propriedades ópticas e elétricas. Além de fornecer uma abordagem alternativa para a síntese de NPs CIGS de alta qualidade de uma maneira controlada por fase, a estratégia apresentada neste estudo também pode contribuir para o desenvolvimento de metodologias para a síntese seletiva de fase de outros sistemas polimórficos.
Abreviações
- CIGS:
-
Cu (In, Ga) S 2
- CIGSe:
-
Cu (In, Ga) Se2
- CIS:
-
CuInS2
- en:
-
Etilenodiamina
- NPs:
-
Nanopartículas
- WZ:
-
Wurtzite
- ZB:
-
Blenda de zinco
Nanomateriais
- Síntese fácil e propriedades ópticas de pequenos nanocristais de selênio e nanorods
- Nanopartículas de albumina carregadas de resveratrol com circulação sanguínea prolongada e biocompatibilidade aprimorada para terapia de tumor pancreático direcionada altamente eficaz
- Síntese fácil de compósito CuSCN colorido e condutor revestido com nanopartículas de CuS
- Células endoteliais de segmentação com nanopartículas de GaN / Fe multifuncionais
- Método de pós-tratamento para a síntese de nanopartículas FePt-Fe3O4 binárias monodispersas
- Efeitos sinérgicos de nanopartículas de Ag / BiV1-xMoxO4 com atividade fotocatalítica aprimorada
- Síntese e desempenho in vitro de nanopartículas de ferro-platina revestidas com polipirrole para terapia fototérmica e imagem fotoacústica
- Efeito do método de síntese de La1 - xSr x MnO3 nanopartículas de manganita em suas propriedades
- Toxicidade de nanopartículas de CoFe2O4 revestidas com PEG com efeito de tratamento da curcumina
- Síntese Verde de Nanopartículas de Metal e Óxido de Metal e Seu Efeito na Alga Unicelular Chlamydomonas reinhardtii



