Decoração de Nanovesículas com Peptídeo de Inserção de pH (Baixo) (pHLIP) para Entrega Almejada
Resumo
A acidez na superfície das células cancerosas é uma marca registrada dos microambientes tumorais, que não depende da perfusão tumoral, portanto, pode servir como um biomarcador geral para direcionar as células tumorais. Usamos o peptídeo de inserção de pH (baixo) (pHLIP) para decoração de lipossomas e niossomas. O pHLIP detecta o pH na superfície das células cancerosas e se insere na membrana das células-alvo, trazendo o nanomaterial para a proximidade da membrana celular. Lipossomas DMPC e niossomas Tween 20 ou Span 20 com e sem pHLIP em seu revestimento foram totalmente caracterizados a fim de obter um entendimento fundamental sobre as características dos nanocarreadores e facilitar o projeto racional de nanovetores sensíveis à acidez. A estabilidade das amostras ao longo do tempo e na presença de soro foi demonstrada. O tamanho, potencial ζ e morfologia dos nanovetores, bem como sua capacidade de aprisionar uma sonda hidrofílica e modular sua liberação foram investigados. As vesículas decoradas com pHLIP podem ser úteis para obter uma liberação prolongada (modificada) de substâncias ativas biológicas para o direcionamento de tumores e outros tecidos com doenças ácidas.
Introdução
Cerca de um século atrás, Paul Ehrlich lançou a ideia de realizar “balas mágicas” para uma distribuição específica e mais eficaz de drogas [1]. As “balas mágicas” devem ser capazes de proteger o medicamento administrado de um ambiente hostil, diminuir os efeitos colaterais, direcionando o medicamento para o tecido doente, melhorando a farmacocinética e a farmacodinâmica do medicamento e modulando a liberação do medicamento [2].
Em 1965, Bangham observou vesículas baseadas em fosfolipídios pela primeira vez [3] e, nos anos seguintes, Gregory Gregoriadis estabeleceu o conceito de que os lipossomas poderiam encapsular drogas e, então, ser usados como sistemas de liberação de drogas. Em particular, eles são compostos por bicamadas fechadas de fosfolipídios (lamelas), onde as cadeias lipídicas hidrofóbicas são fechadas entre duas camadas de grupos de cabeça hidrofílicos. A bicamada fechada envolve um núcleo aquoso, permitindo assim a localização de drogas lipofílicas ou hidrofílicas, respectivamente [4, 5].
O tamanho do lipossoma é um parâmetro crítico para influenciar o destino do portador após a administração, em termos de absorção de proteínas plasmáticas, reconhecimento pelo sistema reticuloendotelial (RES), meio tempo de circulação e tráfego celular. Carreadores nanométricos podem favorecer a internalização celular e o direcionamento do tumor, portanto, muitos pesquisadores têm se concentrado na “nanonização” [6,7,8,9].
A fim de obter nanocarreadores mais versáteis e econômicos, surfactantes sintéticos têm sido empregados para a obtenção de sistemas de liberação de fármacos semelhantes a lipossomas. Os surfactantes não iônicos são amplamente utilizados para esta finalidade, e são capazes de se automontar em vesículas unilamelares ou multilamelares ( não - lipossomas iônicos , niossomas ou vesículas de surfactante não iônico). Os surfactantes de ésteres de sorbitano (Spans®) são substâncias lipofílicas amplamente utilizadas na preparação de niossomas. A fim de prolongar o tempo de circulação das vesículas e obter nanocarreadores “furtivos”, a incorporação de polietilenoglicol (PEG) é uma abordagem padrão ouro:por meio dessa conjugação, são obtidos surfactantes de ésteres de etoxietiladosorbitano (Tweens®). Tanto o Span quanto o Tween são caracterizados por um valor de balanço hidrofílico / lipofílico (HLB) diferente e a escolha do surfactante permite a preparação de niossomas com as propriedades desejadas [10]. Além disso, a adição de colesterol é usada para o aumento da estabilidade da bicamada alongando as caudas do surfactante, afetando a temperatura de transição do gel do surfactante para a fase líquida e conferindo rigidez da bicamada lipofílica [11, 12]. O nanotransportador "otimizado" é projetado para melhorar a formulação e / ou aumentar o direcionamento [10].
Atualmente, o câncer é uma das principais causas de morte no mundo. As abordagens terapêuticas atuais têm uma série de limitações, incluindo a entrega não eficiente de drogas a tumores e a falta de direcionamento de tumor associada a efeitos colaterais indesejáveis e perigosos, que as abordagens da nanotecnologia podem ajudar a superar [13].
Atualmente, várias abordagens de segmentação estão em desenvolvimento. A maioria deles é baseada no direcionamento de biomarcadores específicos superexpressos na superfície das células cancerosas. No entanto, devido ao fato de que os tumores humanos são muito heterogêneos, abordagens mais gerais de direcionamento de tumor serão muito mais vantajosas. A acidez na superfície das células cancerosas é uma marca registrada dos microambientes tumorais e não depende da perfusão tumoral, portanto, pode servir como um biomarcador geral para direcionar as células tumorais [14]. A tecnologia de peptídeo de inserção de pH (baixo) (pHLIP) está se desenvolvendo rapidamente para direcionar imagens e pequenas moléculas terapêuticas, bem como nanomateriais para tumores. O pHLIP detecta o pH na superfície das células cancerosas e se insere na membrana das células-alvo [15, 16]. O mecanismo de inserção do pHLIP é desencadeado pela protonação de resíduos carregados negativamente do peptídeo em pH baixo (pH <7,0). Isso leva a um aumento da hidrofobicidade do peptídeo, mudando, assim, o equilíbrio em direção à partição do peptídeo na bicamada [17]. Nanocarriers decorados com pHLIPs são biocompatíveis, podem ter como alvo tumores e demonstrar captação celular aumentada pelas células cancerosas. Entre as nanopartículas revestidas com pHLIP investigadas estão lipídios, polímeros e nanomateriais à base de metal [18,19,20,21].
O objetivo do presente trabalho é caracterizar completamente novos nanocarreadores vesiculares decorados por pHLIP, a fim de obter um entendimento fundamental sobre as características dos nanocarreadores e facilitar o projeto racional de nanovetores sensíveis à acidez.
Materiais e métodos
Materiais
Monolaurato de polioxietilenossorbitano (Tween 20), monolaurato de sorbitano (Span 20), colesterol (Chol), sal de Hepes { N - (2-idroxietil) piperazina- N ′ - (ácido 2-etanossulfônico)}, soro humano, Sephadex G-75, calceína e difenilhexatrieno (DPH) foram adquiridos na Sigma-Aldrich. 1,2-Dimiristoil- sn -glicero-3-fosfocolina (DMPC) e 1,2-dioleoil-sn-glicero-3-fosfoetanolamina- N O sal de sódio de - [4- (p-maleimidofenil) butiramida] (DSPE-maleimida) foi adquirido na Avanti Polar Lipids e o pireno foi obtido na Fluka. O peptídeo pHLIP (ACEQNPIYWARYADWLFTTPLLLLDLALLVDADEGT) foi sintetizado e purificado por CS Bio. Todos os outros produtos e reagentes eram de qualidade analítica.
Síntese de DSPE-pHLIP
pHLIP foi conjugado com DSPE lipídios em metanol pela conjugação covalente de DSPE-maleimida com o único resíduo de cisteína no N-terminal de pHLIP, como foi descrito anteriormente [18, 21, 22]. Resumidamente, 5 mg de peptídeo dissolvido em 250 μL de metanol (soprado com argônio) e DSPE-maleimida (de solução estoque 9,9 mM) dissolvido em clorofórmio foram misturados a uma razão molar de 1:1. A mistura de reação foi mantida em temperatura ambiente por cerca de 2–6 h até que a conjugação fosse concluída. O progresso da reação na conjugação de DSPE-malemida com pHLIP foi monitorado pelo RP-HPLC usando um gradiente de 25 a 80% de acetonitrila em água contendo 0,05% de TFA, monitorando uma diminuição do pico correspondente ao pHLIP não marcado na mistura de reação. A construção sintetizada foi caracterizada por espectrometria de massa SELDI-TOF. A concentração do conjugado DSPE-pHLIP foi determinada por absorbância usando o coeficiente de extinção molar para pHLIP: ε 280 =13.940 M −1 cm −1 .
Preparação e purificação das vesículas
O método de evaporação em camada delgada foi usado para preparar vesículas de surfactante não iônico (de Tween 20 ou Span 20) e fosfolipídeo (de DMPC), com e sem pHLIP. Em cada formulação de vesícula, o colesterol foi adicionado em diferentes razões molares (Tabela 1) [23].
A composição da amostra foi otimizada escolhendo estruturas previamente bem caracterizadas [24, 25] nas quais a mesma quantidade de pHLIP foi adicionada.
Os componentes lipofílicos foram primeiro dissolvidos em CHCl 3 :CH 3 Mistura OH (3:1); o solvente orgânico foi então removido sob vácuo a diferentes temperaturas dependendo da amostra. O filme obtido foi hidratado com 5 mL de tampão Hepes (0,01 M pH 7,4) ou solução de calceína de sódio 10 −2 M. A suspensão foi misturada com vórtice por cerca de 5 min, seguida por sonicação (consulte o arquivo adicional 1:Tabela S1, informações de apoio) usando uma microssonda operando a 20 kHz (VibraCell-VCX 400-Sonics, Taunton, MA, EUA). A sonicação LipoDMPC foi conduzida sob atmosfera inerte para prevenir a oxidação.
A suspensão de vesículas foi então purificada por cromatografia de permeação em gel usando Sephadex G-75 (coluna de vidro de 50 x 1,2 cm) e tampão Hepes como eluente. A seguir, a suspensão de vesículas purificada foi filtrada por meio de filtros de celulose com o diâmetro de poro adequado.
O mesmo método de preparação foi usado para preparar niossomas e lipossomas revestidos com pHLIP.
Medições dinâmicas de dispersão de luz
O tamanho médio e a distribuição do tamanho das vesículas foram medidos em T =25 ° C por espalhamento dinâmico de luz (DLS), usando um Malvern NanoZetaSizer ZS90, equipado com um laser HeNe 5 mW (comprimento de onda λ =632,8 nm) e um correlacionador digital. As funções de autocorrelação normalizadas da intensidade espalhada em ângulo de 90 ° foram analisadas pelo algoritmo de Contin para obter a distribuição do coeficiente de difusão das partículas D , daí a distribuição do raio hidrodinâmico efetivo R H das vesículas através da relação de Stokes-Einstein R H = K B T / 6πη D , onde K B T é a energia térmica e η é a viscosidade do solvente. A largura da distribuição de tamanhos de niossomas / lipossomas é bastante pequena, mas não negligenciável. Os valores relatados na Tabela 2 correspondem ao diâmetro hidrodinâmico médio ponderado pela intensidade das partículas [26].
ζ-Medições de potencial
As medidas de mobilidade eletroforética foram realizadas pela técnica de eletroforese a laser Doppler, no aparelho Malvern NanoZetaSizer ZS90. A mobilidade u foi convertido no ζ -potencial usando a relação de Smoluchowski ζ =uη / є, onde η e є são a viscosidade e a permissividade da fase solvente, respectivamente [27].
Dispersão de raios-X em pequeno ângulo
Experimentos de espalhamento de raios X a baixo ângulo (SAXS) foram realizados na European Synchrotron Radiation Facility (ESRF, Grenoble, França). O uso da linha de luz de alto brilho ID02 permitiu realizar medidas em soluções diluídas na região de transferência de momento 0,1 nm −1 ≤ q ≤ 6 nm −1 , q =(4π / λ) sin (θ / 2), onde θ é o ângulo de espalhamento e λ =0,1 nm o comprimento de onda dos raios-X. A escala de comprimento investigada correspondente está entre 1 e 60 nm, adequada para acessar a estrutura interna de vesículas niossômicas e lipossomais. Todos os experimentos foram realizados em T =25 ° C com tempo de irradiação curto, 0,1 s, para evitar danos por radiação. Para cada amostra, a intensidade espalhada em diferentes ângulos de espalhamento foi capturada em um detector 2D, então angularmente reagrupada, subtraída para as contribuições de fundo e solvente e analisada para obter informações sobre a forma e estrutura interna das vesículas em solução.
No caso das vesículas unilamelares, a bicamada fechada foi modelada com três conchas concêntricas correspondentes aos grupos de cabeça externos, as cadeias hidrofóbicas e os grupos de cabeça internos. Uma distribuição de Schulz para o tamanho da vesícula foi assumida.
Cryo-TEM
A solução da vesícula (gota de 5 μL) foi espalhada em uma grade de formar Lacey / microscopia eletrônica de carbono e preservada em um estado hidratado congelado por um congelamento rápido em etano líquido. O processo de vitrificação foi realizado no sistema FEI Vitrobot com configuração de um único blot de 3 s, deslocamento de 1 e drenagem e tempo de espera de 1 s. Microscopia eletrônica de transmissão (TEM) (JEOL 2100) com uma tensão de aceleração de 200 kV em ampliações na faixa de × 10.000 a × 150.000 foi usada para imagens de vesículas.
Estudos de estabilidade
Os estudos de estabilidade física de niossomas e lipossomas, preparados com e sem pHLIP, foram realizados a duas temperaturas de armazenamento diferentes (25 ° C e 4 ° C). O objetivo foi avaliar se mudanças significativas no tamanho e potencial ζ da dispersão das vesículas ocorrem ao longo de um período de 90 dias. Amostras de cada lote foram retiradas em intervalos de tempo definidos (1, 30, 60 e 90 dias) e o tamanho das vesículas e o potencial ζ foram determinados conforme descrito anteriormente.
Da mesma forma, a estabilidade das vesículas foi investigada também na presença de fluidos biológicos, como soro humano. As suspensões foram postas em contato com 45% de soro humano a 37 ° C. Em intervalos de tempo definidos (0, 30 min, 1 h, 2 h e 3 h), as variações no tamanho da vesícula e no potencial ζ foram determinadas conforme descrito.
Caracterização bicamada
Fluidez e microviscosidade-polaridade de bicamadas niossômicas e lipossomais foram acessadas por medidas de fluorescência de duas sondas fluorescentes, difenilhexatrieno (DPH) e pireno, respectivamente, localizadas na região hidrofóbica da membrana de bicamada. Tanto DPH (2 mM) quanto pireno (4 mM), 220 μL e 2,5 mg respectivamente, foram adicionados ao surfactante ou à mistura de fosfolipídeo / colesterol antes da preparação da vesícula [28]. Posteriormente, as vesículas carregadas com pireno foram purificadas conforme descrito anteriormente, enquanto as vesículas carregadas com DPH foram filtradas por tamanhos de poro progressivamente menores (de 5,0 a 0,22 μm).
As medições de anisotropia de fluorescência foram realizadas à temperatura ambiente usando um espectrofluorômetro LS55 (PerkinElmer, MA, EUA) em λ exc =400 nm e λ em =425 nm e a anisotropia de fluorescência ( A ) de amostras foi calculado de acordo com a seguinte equação [29]:
$$ A =\ frac {I_ {vv} - {I} _ {vh \ kern0.5em} x \ G} {I_ {vv} +2 {I} _ {vh} \ x \ G} $$
onde eu vv e eu vh são as intensidades da fluorescência emitida (unidades arbitrárias), respectivamente, paralela e perpendicular à direção da luz de excitação polarizada verticalmente. O fator de correção G =I hv / I hh é a razão entre os componentes de emissão polarizados verticalmente e horizontalmente quando a luz de excitação é polarizada horizontalmente. Os valores de anisotropia de fluorescência são inversamente proporcionais à fluidez da membrana. Portanto, alto valor de anisotropia de fluorescência corresponde a uma alta ordem estrutural e / ou baixa fluidez de membrana [30].
A fim de avaliar a microviscosidade e a micropolaridade da bicamada da vesícula, experimentos de fluorescência com pireno foram realizados com um espectrofluorômetro Perkin-Elmer LS55 em λ exc =330 nm, registrando o espectro de emissão na faixa 350 <λ em <550 nm [28]. A estrutura fina da fluorescência do pireno apresenta cinco picos. A razão entre as intensidades da primeira (372 nm) e da terceira (382 nm) bandas vibracionais do espectro de fluorescência do pireno, I 1 / eu 3 , está relacionado à polaridade do ambiente pireno [31]. Na verdade, valores baixos do eu 1 / eu 3 a proporção corresponde a um ambiente apolar. Além disso, as moléculas de pireno incorporadas na bicamada da vesícula podem formar excímeros intramoleculares e este processo é sensível à viscosidade do microambiente da sonda [32]. Portanto, a razão de intensidade de fluorescência de excímero / monômero, I E / eu M , está relacionado à microviscosidade.
Esses estudos foram realizados nas vesículas preparadas com e sem pHLIP e os resultados obtidos foram comparados.
Estudos de liberação de Calcein
Surfactante não iônico ou vesículas de fosfolipídios foram carregadas com calceína na concentração de 10 −2 M. Nesta concentração, a fluorescência da calceína é autoextinguida [33]. Medições de extinção foram então usadas para determinar a liberação de calceína do núcleo aquoso da vesícula. A sonda fluorescente foi carregada nas vesículas durante a hidratação do filme fino pela adição de 5 mL da solução aquosa de calceína. As suspensões de vesículas foram purificadas por cromatografia de permeação em gel, colocadas em contato com soro humano a 45% ou Hepes e, em seguida, carregadas dentro de um saco de diálise de membrana de celulose (peso molecular de corte 8,000 Da de Spectra / Por®). Os experimentos de liberação foram realizados a 37 ° C, sob agitação magnética em tampão Hepes (10 mM, pH 7,4) como meio externo. Alíquotas do meio externo foram retiradas em momentos diferentes ao longo de 0–24 h. De vez em quando, as alíquotas retiradas eram reintroduzidas no sistema [34].
A liberação de calceína foi monitorada por medições da fluorescência do meio usando um espectrofluorômetro Perkin-Elmer LS50B com λ ex =492 e λ em =520 nm. O valor de referência F ∞ (unidades arbitrárias), correlacionada à quantidade total de calceína aprisionada nas vesículas [35], foi determinada após a ruptura das vesículas usando álcool isopropílico (1:1 v / v ) As porcentagens de liberação ( F %) em cada ponto de tempo foram obtidos usando a seguinte equação:
$$ F \% ={F} _t / {F} _ {\ infty} x \ 100 $$
onde F t (unidades arbitrárias) é a fluorescência lida em um ponto de tempo específico t .
Análise estatística
Uma ANOVA unilateral foi usada para análise estatística. A posteriori Bonferroni t teste foi realizado para avaliar a significância estatística do teste ANOVA. A p valor <0,05 foi considerado estatisticamente significativo. Os resultados são a média de três experimentos ± desvio padrão.
Resultados e discussão
Tween20-, Span20- e DMPC-vesículas, preparadas com e sem DSPE-pHLIP, foram caracterizadas quanto ao tamanho e potencial ζ (Tabela 2).
De acordo com os resultados apresentados na Tabela 2, as amostras analisadas não apresentam variações significativas de tamanho e potencial ζ, independentemente da presença de pHLIP.
As faixas de tamanho relatadas acima foram confirmadas por meio de uma técnica de análise diferente, como o crio-TEM (Fig. 1).
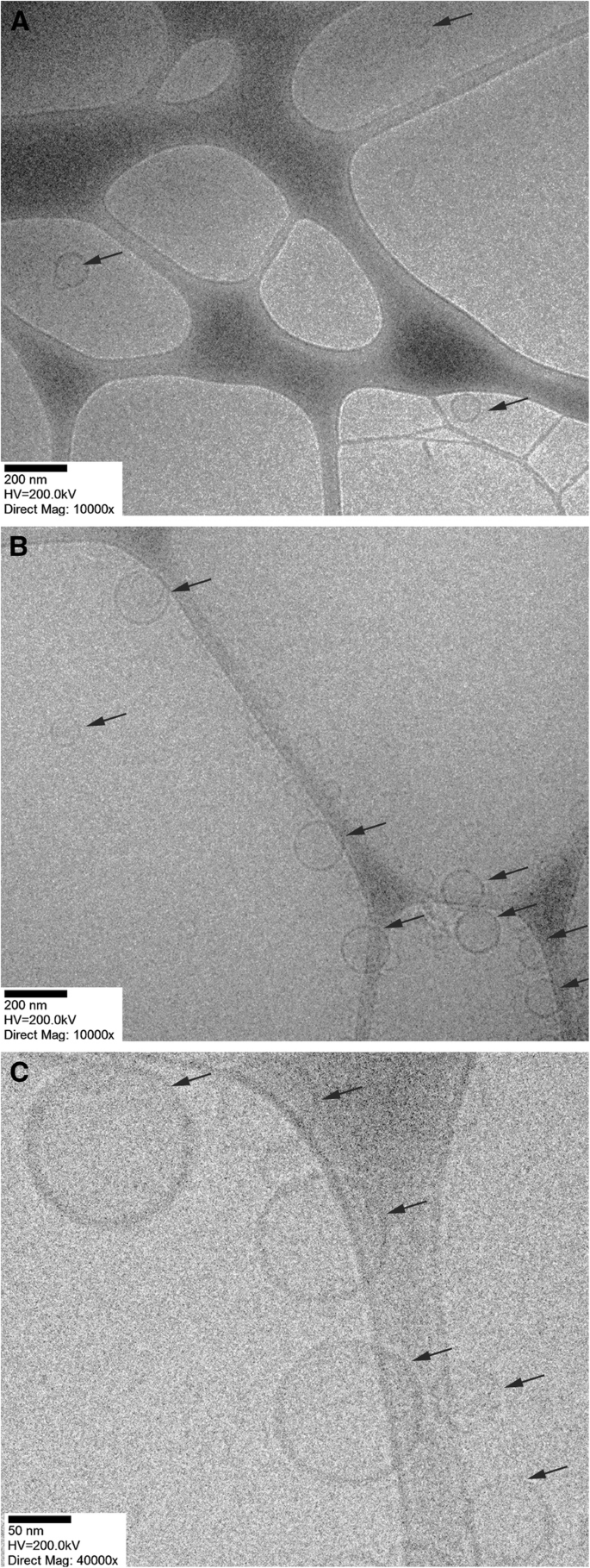
Imagens representativas de crio-TEM de niossomas e lipossomas revestidos com pHLIP. Imagens de niossomas NioSpan20-pHLIP ( a ) e lipossomas LipoDMPC-pHLIP ( b ) obtido com aumento de × 10.000 e lipossomas LipoDMPC-pHLIP ( c ) obtido com uma ampliação de 40.000 ×
A estrutura interna dos niossomas / vesículas com e sem DSPE-pHLIP foi determinada por experimentos SAXS. Os espectros de intensidade SAXS, apresentados na Fig. 2, são diferentes, indicando que cada sistema possui características peculiares.
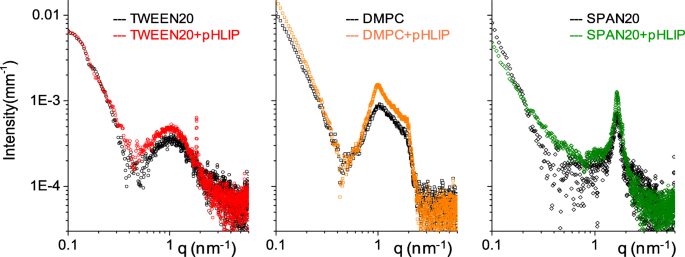
Espectros SAXS. Espectros de intensidade de niossomas / vesículas sem (símbolos pretos abertos) e com DSPE-pHLIP (símbolos coloridos)
Os niossomas baseados em Tween20 são unilamelares, enquanto as vesículas DMPC exibem um certo grau de multilamelaridade (como lipossomas), conforme mostrado pela presença do pico característico em q ≅ 1 nm −1 , correspondendo a uma distância interlamelar de 6 nm (cerca de 5 nm de bicamada lipídica e 1 nm de água). As vesículas baseadas em Span20 são definitivamente multilamelares, com um pico característico em q =1,6 nm −1 correspondendo a uma distância interlamelar de 3,8 nm, correspondendo ao dobro do comprimento da molécula Span20. Os resultados indicam que a camada de múltiplas camadas das vesículas Span20 é composta de bicamadas adjacentes com quase nenhuma água interlamelar.
A presença de DSPE-pHLIP (menos de 1% da fração molar) não afeta dramaticamente os sistemas. A intensidade dispersa em todos os q investigados -faixa é bastante semelhante, indicando fração comparável de material estruturado e tamanho total comparável das partículas vesiculares.
As vesículas baseadas em DMPC mostram um ligeiro aumento no número de bicamadas dentro do lipossoma, como dedutível pelo aumento da intensidade do pico de Bragg em q =1 nm −1 . A inserção de uma baixa fração de cadeias DSPE C18, ligada a cada molécula de peptídeo, não altera a espessura da bicamada lipídica e é principalmente ditada pela grande fração de colesterol em relação ao DMPC (cerca de 40-50%). Nesta concentração de colesterol, as cadeias lipídicas são organizadas na fase de ordenação líquida (Lo), e caracterizadas pelo desacoplamento da ordem posicional lateral fraca das cadeias em relação à ordem orientacional elevada ao longo das cadeias e capazes de hospedar poucos C18- cadeias sem qualquer mudança estrutural [36]. Além disso, as vesículas de múltiplas camadas baseadas em Span20 não exibem alterações em sua estrutura interna.
No sistema Tween20 + pHLIP, uma pequena quantidade de cristalitos de colesterol está presente, como mostrado pelo pico agudo típico em q =1,84 nm −1 (distância característica de 3,41 nm), e a estrutura da vesícula não é afetada. A presença de poucos microcristalitos foi frequentemente encontrada associada a niossomas baseados em Tween [37] em quantidade dependendo da composição, procedimento de preparação e purificação. Na Fig. 2, os dois espectros experimentais das vesículas Tween20 e Tween20 + pHLIP são mostrados junto com as curvas de ajuste obtidas pela modelagem da bicamada esférica fechada com três camadas concêntricas:os grupos de cabeças externos, as cadeias e os grupos de cabeças internos. O tamanho médio de ajuste das vesículas é de cerca de 168 nm em ambos os sistemas, de acordo com os resultados do DLS. Os parâmetros estruturais são os mesmos para as duas bicamadas fechadas (ver arquivo adicional 1:Figura S1 e Tabela S2), exceto para a camada externa:na presença de DSPE-pHLIP, uma ligeira diminuição (5%) da densidade de elétrons dos grupos de cabeças é observada (de 0,42 a 0,40 e / Å 3 ), juntamente com um aumento da rugosidade da camada. Este resultado indica que a adição de DSPE-pHLIP afeta principalmente a casca externa das vesículas. Isso é consistente com uma imagem em que as cadeias DSPE C18 se inserem na bicamada e ancoram o peptídeo à superfície da vesícula, entre os grupos principais de polietilenoglicol estendido e ramificado. Notamos que a capacidade do próprio peptídeo pHLIP (não ligado às moléculas de lipídios) de interagir com a superfície externa das vesículas em pH alto e se inserir na bicamada em pH baixo foi recentemente observada por SAXS no caso de bicamadas de fosfolipídios insaturados [38 ] No presente estudo, a fração molar do peptídeo é significativamente menor e o peptídeo está ligado a lipídeos, pois o objetivo é projetar nanovetores de fármacos sensíveis ao pH revestidos com pHLIP. A associação pHLIP é conduzida pela interação hidrofóbica das cadeias DSPE C18 conjugadas que se inserem na região hidrofóbica do nanovetor. O peptídeo pHLIP é ancorado e fica na região externa do grupo principal, propenso a interagir com as membranas alvo em pH ácido e / ou a liberar o conteúdo do nanovetor após o rearranjo da bicamada em ambiente de baixo pH.
Para investigar se a presença de pHLIP pode afetar as propriedades micro-reológicas da bicamada (fluidez, microviscosidade e polaridade), foi realizada uma caracterização de casca lipofílica. Os estudos de caracterização foram realizados utilizando-se a sonda fluorescente pireno, adicionada às amostras no início do procedimento de preparo. Devido à sua natureza lipofílica, ele se insere na bicamada da vesícula e fornece informações sobre a polaridade e a microviscosidade do ambiente da membrana.
Conforme mostrado na Tabela 3, em todos os três conjuntos de amostras, os valores de polaridade diminuem apenas ligeiramente na presença de pHLIP em comparação com a vesícula de contrapartida sem pHLIP, enquanto os valores de microviscosidade mostram um aumento de três vezes, para todas as vesículas.
A bicamada foi ainda caracterizada por medidas de anisotropia de fluorescência de outra sonda fluorescente lipofílica, DPH, incorporada a lipídios. Essas medidas refletem o movimento da sonda e sua orientação dentro da bicamada que fornece informações sobre a fluidez da bicamada que pode afetar a capacidade das vesículas de liberar seu conteúdo [29]. Os valores de anisotropia de fluorescência são inversamente proporcionais à fluidez da membrana. Assim, alto valor de anisotropia de fluorescência corresponde a uma alta ordem estrutural e / ou baixa fluidez de membrana, como na fase ordenada de líquido [30].
Os valores de anisotropia para cada amostra são apresentados na Tabela 3. Os dados indicam que a presença do DSPE-pHLIP nas vesículas aumenta a fluidez da membrana, visto que a anisotropia de fluorescência diminuiu. É bem conhecido que a fluidez da bicamada é afetada não apenas pela ordem e organização lateral das cadeias apolares, mas também pelos grupos de cabeças polares [31]. Os resultados do SAXS nos três sistemas diferentes mostram que as moléculas DSPE-pHLIP afetam principalmente a região do grupo de cabeça, eventualmente causando um empacotamento diferente das cabeças polares. Os resultados estruturais parecem corresponder às propriedades micro-reológicas das bicamadas na presença de DSPE-pHLIP associado, conforme revelado pela inserção de duas sondas diferentes. Os resultados mostram um aumento da microviscosidade revelado pelo pireno, uma sonda que poderia se inserir perto da região externa (o log P do pireno é 4,88). Por outro lado, presume-se que o DPH esteja embutido no núcleo das bicamadas, orientado paralelamente ao eixo da cadeia de acila lipídica ou restrito no centro da bicamada, paralelo à superfície. É amplamente sensível à reorientação angular das cadeias acil anfifílicas [39]. O aumento da fluidez, conforme revelado pelo DPH, pode estar relacionado tanto ao efeito da inserção das cadeias DSPE entre as demais cadeias acil quanto ao efeito da partição do pHLIP na região dos grupos polares, alterando as propriedades de empacotamento dos surfactantes. (Fig. 3).
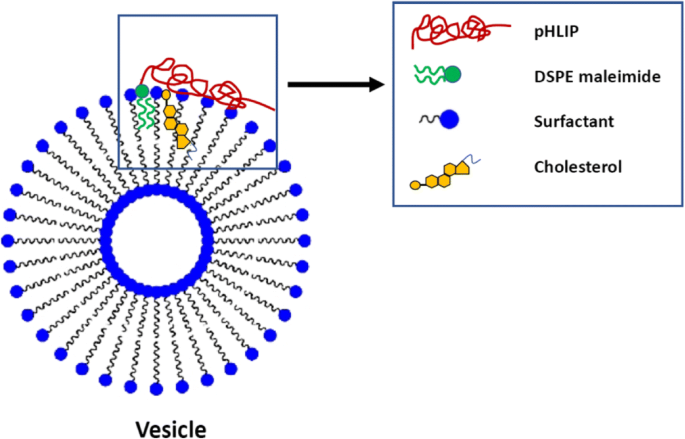
Representação das interações de pHLIP com a membrana da vesícula
Outros estudos de caracterização foram conduzidos nas preparações examinadas. Todas as amostras, preparadas com e sem pHLIP, foram armazenadas por 90 dias a 4 ° C de temperatura para avaliar a estabilidade das vesículas ao longo do tempo, medindo seu tamanho e variações do potencial ζ (Arquivo adicional 1:Figura S2). Nenhuma variação significativa no tamanho e potencial ζ foi observada ao longo do experimento; portanto, todas as preparações examinadas resultaram estáveis se armazenadas a 4 ° C de temperatura.
Além disso, a estabilidade das amostras foi examinada na presença de 90% ( v / v ) soro humano e armazenado a 37 ° C por 3 h (arquivo adicional 1:Figura S3).
Em contato com soro humano, as vesículas Tween20 apresentaram aumento de tamanho, embora tenham permanecido abaixo de 300 nm. O tamanho e os valores de PDI foram medidos para serem constantes ao longo do experimento de 3 h, sugerindo que as vesículas em suspensão permaneceram intactas ao longo de todo o experimento.
Ambas as amostras de Span20 em contato com soro humano apresentaram aumento de tamanho, principalmente na preparação com pHLIP, enquanto os valores de PDI sugerem distribuição homogênea de tamanho (dados não mostrados). Esse evento pode ser devido à absorção de proteínas plasmáticas na superfície niossômica, como resultado de interações eletrostáticas, porém, sem incorrer no rompimento das vesículas. Esta hipótese é sustentada pela diminuição do potencial ζ após o contato das vesículas com o soro humano. Esse fenômeno ocorre quando o potencial ζ atinge valores levemente negativos, em torno da região de neutralidade, tornando o sistema instável, e as vesículas começam a se agregar.
Assim como Tween20, as vesículas DMPC mostram um aumento de tamanho em comparação com a amostra pré-contato. No entanto, esta variação revelou-se não significativa e os valores de tamanho mantidos abaixo de 280 nm (DMPC) ou abaixo de 240 nm (DMPC + pHLIP).
A capacidade de liberação foi avaliada para as amostras preparadas com e sem pHLIP seguindo a quantidade de calceína (sonda hidrofílica) liberada das vesículas ao longo do tempo.
Os estudos foram realizados à temperatura de 37 ° C por um período de 24 h, por exposição das amostras purificadas com tampão HEPES ou soro humano. Conforme mostrado na Fig. 4, os perfis de liberação de calceína revelaram-se muito semelhantes para Tween20 e Tween20-pHLIP em tampão HEPES ou soro humano.
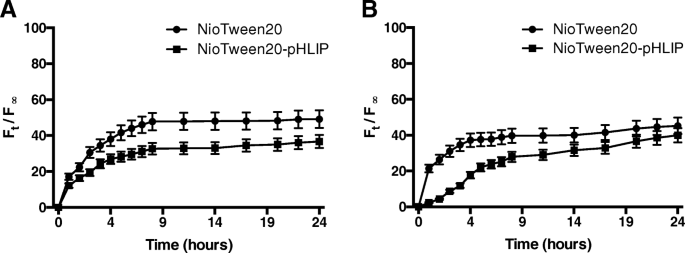
Perfil de liberação de Calcein. NioTween20 e NioTween20-pHLIP contataram com tampão HEPES ( a ) ou soro humano ( b )
A quantidade liberada de calceína estava entre 30 e 50%, indicando que não há diferenças nas capacidades de liberação entre as amostras preparadas com e sem pHLIP.
Os mesmos resultados foram obtidos para amostras Span e DMPC (dados não mostrados).
Perfis de liberação comparáveis foram relatados para diferentes nanocarreadores responsivos a estímulos, tais como cubossomos termossensíveis [40] ou nanotransportadores automontados poliméricos (SANs) [41, 42].
Em conclusão, as diferenças físico-químicas observadas em termos de microviscosidade e fluidez para as amostras preparadas com e sem pHLIP (Tabela 3) não afetam suas capacidades de liberação (Fig. 4), de acordo com as evidências de que a inserção do DSPE-pHLIP as moléculas afetam principalmente a região do grupo de cabeça. Esses dados estão de acordo com os resultados relatados anteriormente, mostrando que em pHs neutros e altos, o pHLIP se liga à superfície dos lipossomas feitos por 1-Palmitoil-2-oleoil- sn -glicero-3-fosfocolina (POPC) e não induz fusão ou vazamento da membrana.
Conclusão
Este estudo confirma a possibilidade de preparação de vesículas decoradas com pHLIP. As amostras são estáveis se armazenadas à temperatura de 4 ° C por pelo menos 3 meses e na presença de soro. Além disso, os nanovetores propostos são capazes de aprisionar uma sonda hidrofílica e modular sua liberação.
pHLIP vesicles were fully characterized in order to obtain fundamental understanding on nanocarrier features and facilitate the rational design of acidity sensitive nanovectors.
The pHLIP association is driven by the hydrophobic interaction of the conjugated DSPE C18-chains inserting in the hydrophobic region of the nanovector. The pHLIP peptide is anchored and lies in the external headgroup region, prone to interact with target membranes at acidic pH and/or to release the nanovector content after bilayer rearrangement in low pH environment.
According to these findings, proposed pHLIP decorated vesicles could be useful to obtain a prolonged (modified) release of biological active substances for targeting tumors and other acidic diseased tissues.
Abreviações
- Chol:
-
Colesterol
- Cryo-TEM:
-
Cryo-transmission electron microscopy
- DLS:
-
Dynamic light scattering
- DMPC:
-
1,2-Dimyristoyl-sn-glycero-3-phosphocholine
- DPH:
-
Diphenylhexatriene
- pHLIP:
-
pH (low) insertion peptide
- SAXS:
-
Small angle X-ray scattering
- Span20:
-
Sorbitan monolaurate
- Tween20:
-
Polyoxyethylenesorbitan monolaurate
Nanomateriais
- Nanofibras e filamentos para entrega aprimorada de drogas
- Estruturas Metálicas-Orgânicas de Meio Ambiente como Sistema de Administração de Medicamentos para Terapia de Tumor
- Administração de medicamentos baseados em células para solicitações de câncer
- MoS2 com Espessura Controlada para Evolução Eletrocatalítica de Hidrogênio
- Nanopartículas lipídicas de PLGA rastreadas com 131I como transportadores de administração de drogas para o tratamento quimioterápico direcionado do melanoma
- Nanopartículas de albumina carregadas de resveratrol com circulação sanguínea prolongada e biocompatibilidade aprimorada para terapia de tumor pancreático direcionada altamente eficaz
- Células endoteliais de segmentação com nanopartículas de GaN / Fe multifuncionais
- Eletrodo de porta de prata impresso a jato de tinta curado por UV com baixa resistividade elétrica
- Nanocarriers à base de nucleosídeo-lipídio para entrega de sorafenibe
- Novos caminhos para terapias relacionadas a nanopartículas



