Uso de Nanocages de Au altamente biocompatíveis @ PEG Nanopartículas como um novo agente de contraste para imagens de tomografia computadorizada in vivo
Resumo
Nos últimos anos, os agentes de contraste têm sido amplamente usados na tecnologia de imagem para melhorar a qualidade. As nanopartículas têm melhor capacidade de detecção in vivo do que os agentes de contraste convencionais em escala molecular. Neste estudo, um novo tipo de nanocages de Au @ nanopartículas de PEG (AuNC @ PEGs) com um forte coeficiente de absorção de raios-X foi sintetizado como um agente de contraste para imagens de tomografia computadorizada (TC). Os resultados mostraram que AuNC @ PEGs tinha boa dispensação aquosa, baixa citotoxicidade e forte capacidade de absorção de raios-X. Além disso, estudos in vivo demonstraram que os AuNC @ PEGs sintetizados têm um aumento de contraste evidente, um longo tempo de circulação no sangue e uma toxicidade insignificante in vivo. Portanto, os AuNC @ PEGs funcionalizados sintetizados neste estudo têm grande potencial para aplicação clínica em imagens de tomografia computadorizada.
Introdução
Nos últimos anos, a tomografia computadorizada (TC) tem sido a técnica de diagnóstico por imagem mais comumente usada em ambientes clínicos e tem ampla aplicação no estudo de vários tecidos humanos. Devido à forte capacidade de penetração e alto contraste e processamento de imagem relativamente simples da tomografia computadorizada, é considerada a técnica de diagnóstico por imagem não invasiva mais poderosa no sistema médico moderno [1, 2]. No entanto, no processo de imagem, não há contraste natural entre a lesão e algumas estruturas circundantes. Assim, um agente de contraste, que é uma substância com uma densidade relativamente maior ou menor, deve ser usado para distinguir a estrutura alvo ou tecido e órgãos. Além disso, essa substância tem capacidades de absorção variadas em diferentes tecidos e pode ser observada por meio de irradiação de raios-X nos tecidos moles. O uso de algumas moléculas e vários agentes de contraste de micropartículas em imagens de tomografia computadorizada tem sido avaliado [3,4,5].
Atualmente, o agente de contraste mais comumente usado para tomografia computadorizada é uma molécula orgânica contendo iodo. Moléculas iodadas, como íon iodeto ou preparação não iônica, são amplamente utilizadas como agente de contraste para tomografias em ambientes clínicos. Embora as moléculas iodadas possam fornecer um bom aumento de contraste na tomografia computadorizada, elas têm uma taxa de depuração renal rápida, um curto tempo de circulação no corpo e propriedades alergênicas, o que limita significativamente outras aplicações [6, 7]. Devido à rápida remoção do revelador de iodo, a janela de tempo efetiva da imagem do pool de sangue é seriamente limitada e uma imagem de alto contraste é difícil de obter. Além disso, a rápida eliminação de uma grande dose de medicamentos pode ter efeitos colaterais potenciais no rim [8, 9].
Na última década, a aplicação de nanopartículas em biomedicina, particularmente em diagnóstico por imagem, tem recebido considerável atenção [10]. Em comparação com os agentes de contraste à base de iodo, as nanopartículas têm cargas úteis de características de contraste que as moléculas pequenas não possuem, e também têm um tamanho, formato e superfície específicos [11, 12]. Geralmente, as nanopartículas com um grande número atômico, como ouro, prata e outras nanopartículas de metal, têm um excelente coeficiente de absorção de raios-X; assim, eles têm uma capacidade de realce de contraste notável [13, 14]. Entre essas nanopartículas, as nanopartículas de ouro foram rapidamente desenvolvidas no campo da biomedicina e consideradas um substituto para os agentes de imagem à base de iodo devido à sua significativa inércia biológica e facilidade de síntese e modificação de superfície [15,16,17]. As nanopartículas de ouro têm maior tempo de circulação sanguínea, menor risco de nefrotoxicidade e coeficiente de absorção de raios-X mais forte do que os compostos de iodo. Portanto, uma dosagem reduzida pode ser fornecida e o risco de efeitos colaterais é baixo [18]. Várias nanopartículas de ouro, incluindo nanoesferas, nanobastões e nanostars, têm sido amplamente utilizadas como agente de contraste para imagens de tomografia computadorizada [19, 20], e tem um efeito promissor. Entre as várias nanoestruturas de ouro, os nanocages de Au têm um interior oco e uma parede porosa fina; assim, eles têm uma área de superfície maior e capacidade de imagem de tomografia computadorizada mais eficaz do que outras nanopartículas de ouro com morfologias diferentes [21, 22]. Nos últimos anos, os nanocages de Au têm sido usados como intensificadores de contraste para tomografia de coerência óptica e tomografia fotoacústica e têm demonstrado bom desempenho. Enquanto isso, devido à grande área de absorção dos nanocages de Au, eles também são transdutores fototérmicos eficazes [23, 24]. Até onde sabemos, apenas alguns estudos avaliaram o uso de nanocages de Au como agente de contraste para imagens de tomografia computadorizada. Com base nos estudos mencionados acima, exploramos ainda mais o uso de nanocages de Au como agente de contraste de tomografia computadorizada. A aplicação de nanopartículas em imagens de tomografia computadorizada requer superfícies com biocompatibilidade e atividades biológicas. O polietilenoglicol (PEG) é um polímero biodegradável e biocompatível, que também é o material furtivo usado para prevenir a captura por RES e para melhorar a biocompatibilidade, a capacidade de eliminação dos rins e o tempo de circulação sanguínea; assim, as nanopartículas PEGuiladas podem ser retidas no sangue por um longo período [15, 25,26,27,28].
Neste estudo, novos AuNC @ PEGs foram preparados e caracterizados. Em seguida, a biocompatibilidade in vitro de AuNC @ PEGs foi avaliada por colorimetria MTT, método de vazamento de lactato desidrogenase (LDH), ensaio de concentração de espécies reativas de oxigênio intracelular (ROS), Calceína-AM / PI e outras técnicas experimentais. Além disso, análises hematológicas e histológicas foram realizadas para determinar a toxicidade de AuNC @ PEGs in vivo. Os resultados mostraram que AuNC @ PEGs tinha grande biocompatibilidade in vitro e in vivo. Além disso, descobriu-se que AuNC @ PEGs tem uma capacidade mais forte de imagens de tomografia computadorizada in vitro e in vivo. Esses resultados experimentais mostraram que os AuNC @ PEGs sintetizados têm vantagens óbvias, como forte contraste, longo tempo de circulação sanguínea e baixo risco de nefrotoxicidade. Portanto, os AuNC @ PEGs funcionalizados sintetizados neste estudo têm grande potencial para aplicação clínica em imagens de tomografia computadorizada.
Métodos
Todos os protocolos experimentais, incluindo quaisquer detalhes relevantes, foram aprovados pelo Comitê de Ética Regional da Jinzhou Medical University na Província de Liaoning, China.
Materiais e instrumentos
Os kits de teste de LDH e ROS foram adquiridos do Nanjing Institute of Bioengineering, China, e os kits de coloração Calcein-AM / PI da Shanghai Dongren Chemical Technology Co., Ltd., China. Outros agentes químicos e solventes foram adquiridos da Sigma-Aldrich. Todas as seções foram avaliadas usando um microscópio de fluorescência (DMI4000B, Leica, Wetzlar, Alemanha). As características das nanopartículas sintetizadas foram avaliadas com um microscópio eletrônico de transmissão (TEM). Foi utilizada uma tomografia computadorizada em espiral de 256 linhas e 512 cortes (Philips, Alemanha), e os parâmetros de imagem foram os seguintes:espessura de corte, 0,625 mm; tensão do tubo, 100 Kvp; e a corrente do tubo, 100 mA.
Síntese de AuNC @ PEGs
Os nanocages de Au foram preparados usando uma reação de substituição galvânica simples entre nanocubos de Ag e HAuCl 4 solução, de acordo com um estudo anterior [29, 30]. Normalmente, os nanocubos de 25 nm de Ag foram preparados em dietilenoglicol e foram usados como modelos para a síntese de nanocubos de Au de 30 nm. Em seguida, SH-PEG (MW ≈ 2000, 10 mg dissolvidos em 5 mL de solução salina tamponada com fosfato (PBS)) foi adicionado à solução AuNC (pH 8,0, 6,55 nM, 6 mL) e foi agitado durante a noite no escuro sob nitrogênio proteção. Depois de lavar os AuNC @ PEGs por mais três vezes, eles foram dispersos em solução aquosa.
Avaliação da toxicidade in vitro
Neste estudo, colorimetria MTT, método de vazamento de LDH, ensaio de concentração de ROS intracelular e coloração com Calcein-AM / PI foram usados para detectar a toxicidade dos AuNC @ PEGs sintetizados in vitro. As células HUVEC foram inoculadas em placas de 96 poços com uma densidade de 1 × 10 4 /Nós vamos. Foi utilizado o meio RPMI-1640 suplementado com 10% de soro fetal bovino e penicilina (100 μg / mL) e estreptomicina. Em seguida, as células foram cultivadas a 37 ° C e 5% de dióxido de carbono em incubadora por 12 h. Em seguida, o meio com AuNC @ PEGs em diferentes concentrações (10, 20, 50, 100, 200, 500 e 1000 μg / mL) foi adicionado para posterior cultura. Após 24 h, o ensaio MTT foi obtido. O meio de cultura sem nanopartículas foi utilizado como controle em cada grupo.
Em seguida, o conteúdo de lactato desidrogenase (LDH) liberado de células HUVEC tratadas com AuNC @ PEGs em diferentes concentrações foi determinado para avaliar a toxicidade in vitro. As células foram inoculadas de forma semelhante ao MTT e, então, tratadas com AuNC @ PEGs em diferentes concentrações (10, 20, 50, 100, 200, 500 e 1000 μg / mL) por 24 h. Em seguida, o sobrenadante foi separado, centrifugado e transferido para uma placa de 96 poços limpa. A atividade de LDH no meio de cultura foi avaliada de acordo com as instruções do fabricante, e a absorbância foi determinada usando um instrumento de marcação de enzima (450 nm).
Com base no princípio de medição da concentração de ROS intracelular usando o kit ROS, DCFH foi oxidado a diclorofluoresceína (DCF), que é uma substância fluorescente verde forte DCF, na presença de 2 ', 7'-diclorofluoresceína (DCFH-DA). As células HUVEC foram cultivadas em placas de 24 poços por 12 h, tratadas com AuNC @ PEGs em diferentes concentrações (50, 100, 200 e 500 μg / mL) por 24 h e incubadas com DCFH-DA a 37 ° C por 40 min. As células tratadas com peróxido de hidrogênio (H 2 O 2 ) foram usados como controle positivo. A intensidade de fluorescência das células foi observada usando um microscópio de fluorescência (λex, 485 nm; λem, 525 nm). Antes da avaliação, um meio sem soro e gelo foi usado três vezes para a lavagem.
Para coloração viva / morta, as células HUVEC foram inoculadas em placas de 24 poços e foram cultivadas por 12 h. Em seguida, as células foram tratadas com AuNC @ PEGs em diferentes concentrações (10, 20, 50, 100, 200, 500 e 1000 μg / mL) por 24 h. Após digestão com tripsina-EDTA via centrifugação, as células foram lavadas com PBS (pH =7,4); em seguida, a suspensão de células preparada foi misturada com o reagente Calcein-AM / PI pré-configurado e foi cultivada a 37 ° C por 15 min. Para detectar a toxicidade de AuNC @ PEGs, o número de células mortas foi avaliado por meio de microscopia de fluorescência.
Modelo Animal
Todos os procedimentos de experimentos com animais foram realizados de acordo com os critérios estabelecidos pelo Comitê de Proteção e Uso de Animais da Universidade Médica de Jinzhou. Após o experimento, os animais foram sacrificados de acordo com os princípios humanitários. Neste estudo, ratos Sprague Dawley adultos pesando 250–300 g (adquiridos no Animal Center da Jinzhou Medical University) foram usados. Neste experimento, todos os animais foram divididos aleatoriamente em grupos. Solução de hidrato de cloral (10% em peso) foi administrada através da cavidade abdominal; em seguida, todos os materiais foram injetados pela veia da cauda.
Imagens de tomografia computadorizada in vitro e in vivo
Para imagens de tomografia computadorizada in vitro, AuNC @ PEGs em diferentes concentrações e soluções de iodo foram colocadas em tubos de EP e foram organizadas na ordem adequada, e uma tomografia computadorizada foi realizada de frente para trás. Na tomografia computadorizada in vivo, após a administração da anestesia, os animais foram digitalizados da cabeça à cauda, sendo o centro da cavidade abdominal o ponto de referência. A posição dos animais não mudou todas as vezes. Todos os dados originais (imagem de 0,625 mm) foram transmitidos para a estação de trabalho Philips para análise por tomografia computadorizada.
Avaliação da toxicidade in vivo
A análise hematológica foi realizada usando a técnica padrão de coleta de sangue da veia safena. Os tecidos do coração, fígado, baço, pulmão e rim dos ratos foram fixados com paraformaldeído 4% por 48 he foram incluídos em parafina após a desidratação. A seção de parafina tinha 5 µm de espessura e foi montada em lâmina de vidro. A coloração com hematoxilina e eosina (H&E) foi então realizada, e a análise foi conduzida ao microscópio.
Análise estatística
Os dados foram analisados usando análise de variância unilateral e P valor foi usado como o índice. A P valor <0,05 foi considerado estatisticamente significativo, expresso pelo valor médio do DP.
Resultados e discussão
Síntese e caracterização do AuNC @ PEGs
Funcionalização de superfície e controle de tamanho são dois fatores-chave para o desenvolvimento de agente de nano-contraste de alto desempenho [ 15]. A estrutura e os caracteres de AuNC @ PEGs foram determinados por TEM e DLS. A Fig. 1a mostrou os resultados de que o tamanho dos AuNC @ PEGs era de cerca de 40 nm com alta uniformidade; entretanto, o raio de hidratação de AuNC @ PEGs também foi usado para testar a dispersão na solução, como mostrado na Fig. 1b, o raio de hidratação de AuNC @ PEGs foi de cerca de 50 nm, mostrando que AuNC @ PEGs eram muito estáveis sem qualquer agregação . AuNC @ PEGs têm um tamanho menor e uma inércia biológica relativamente boa, que são melhores para aplicações de nanomedicina. Além disso, a estrutura de gaiola oca indica grandes áreas de superfície específicas internas e externas e melhor capacidade de imagem de tomografia computadorizada, e as paredes metálicas circundantes forneceram proteção adicional para cargas úteis durante seu processamento, transporte e armazenamento. Com sua óbvia estrutura de núcleo-casca, a parte externa foi coberta com PEG de aplicabilidade biológica, que pode efetivamente aumentar a biocompatibilidade e escapar da captura de macrófagos.
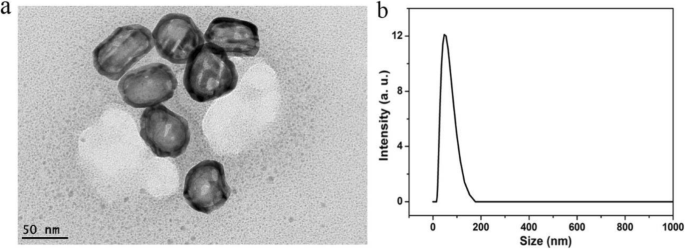
Imagens TEM de AuNC @ PEGs ( a ) e DLS de AuNC @ PEGs ( b )
Segurança e estabilidade de AuNC @ PEGs in vitro
Antes de usar AuNC @ PEGs para imagens in vivo, avaliamos sua segurança e estabilidade. O efeito de AuNC @ PEGs na viabilidade de células HUVEC foi detectado usando o ensaio MTT (Fig. 2a). As células foram tratadas com AuNC @ PEGs em diferentes concentrações (10, 20, 50, 100, 200, 500 e 1000 μg / mL) por 24 h. Os resultados do ensaio MTT mostraram que a taxa de sobrevivência celular dos AuNC @ PEGs foi semelhante à do grupo controle e apresentou biocompatibilidade favorável quando a concentração de AuNC @ PEGs atingiu 200 μg / mL. A taxa de sobrevivência celular a uma concentração de 1000 μg / mL ainda era> 75%.
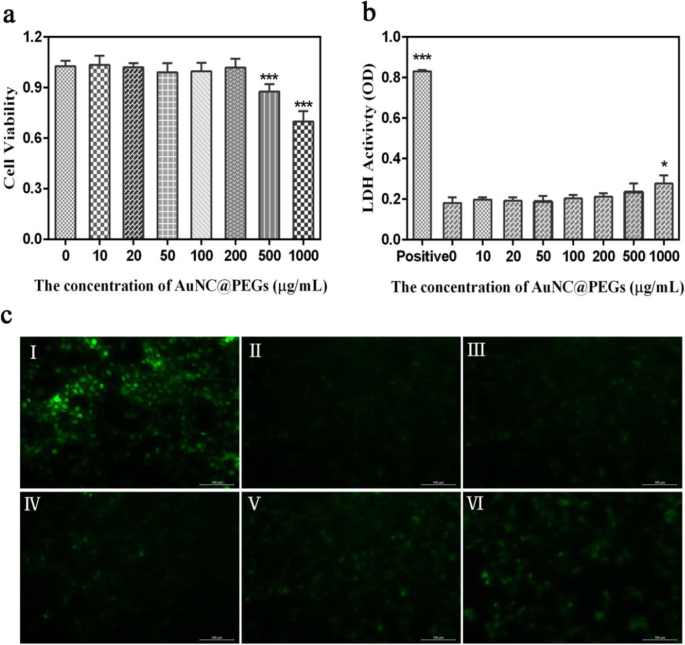
Avaliação de MTT da viabilidade de células HUVEC cultivadas com diferentes concentrações de AuNC @ PEGs por 24 h ( a ) Avaliação da lactato desidrogenase no sobrenadante induzido por AuNC @ PEGs com LDH ( b ) Exame de imagens de fluorescência de 24 h de células cultivadas com AuNC @ PEGs em diferentes concentrações (H 2 O 2 (I), 0 μg / mL (II), 50 μg / mL (III), 100 μg / mL (IV), 200 μg / mL (V) e 500 μg / mL (VI)) pelo método ROS ( c ) * P <0,05, *** P <0,001. Barras de escala são 100 μm
Além disso, o ensaio de LDH também foi usado para avaliar a biocompatibilidade de AuNC @ PEGs in vitro. Em células normais, o LDH não pode passar através da membrana celular. Quando a membrana celular é danificada, o LDH é liberado através da membrana celular [ 31]. Assim, avaliamos a segurança de AuNC @ PEGs medindo o teor de LDH no sobrenadante da célula (Fig. 2b) tratando células com AuNC @ PEGs em diferentes concentrações por 24 h. Os resultados mostraram que o nível de LDH liberado pelas células aumentou ligeiramente em comparação com as células de controle não expostas quando a concentração de AuNC @ PEGs foi <200 μg / mL, e foi significativamente menor do que o do grupo de controle positivo (H 2 O 2 ), que foi consistente com os resultados do ensaio de MTT, e 200 μg / mL de AuNC @ PEGs como concentração ideal apresentaram boa citocompatibilidade.
Além disso, testes de estresse oxidativo e avaliação da coloração por imunofluorescência de células vivas / mortas (Calcein-AM / PI) foram realizados para detectar a toxicidade de AuNC @ PEGs in vitro. O estresse oxidativo é uma condição prejudicial para todos os sistemas vitais, e as espécies reativas de oxigênio em excesso (ROS) podem causar estresse oxidativo [32, 33]. Portanto, medimos o nível de ROS nas células. Após 24 h de indução por AuNC @ PEGs em diferentes concentrações, a intensidade de fluorescência verde das células induzidas em uma concentração de 50-200 μg / mL não diferiu significativamente daquela do grupo de controle, e foi significativamente menor do que a de o grupo de controle positivo (Fig. 2c). A intensidade da fluorescência foi proporcional ao nível de ROS. Conforme mostrado na Fig. 3, a taxa de sobrevivência das células HUVEC em uma concentração de 0–200 μg / mL foi> 90% (Fig. 3a – f). Os resultados citados acima validaram que AuNC @ PEGs na concentração de 200 μg / mL são estáveis e têm boa compatibilidade celular, podendo ser agentes de contraste clínicos promissores.
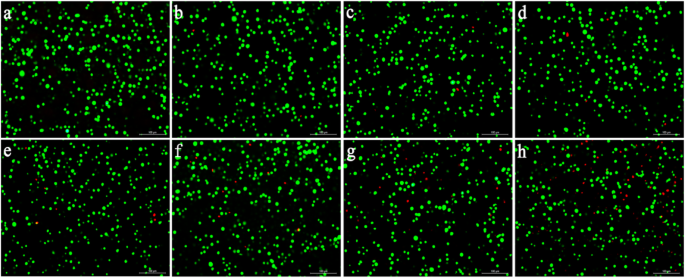
Imagens de microscopia de fluorescência de coloração viva e morta. Taxa de sobrevivência de células HUVEC tratadas com AuNC @ PEGs em diferentes concentrações (0 μg / mL ( a ), 10 μg / mL ( b ), 20 μg / mL ( c ), 50 μg / mL ( d ), 100 μg / mL ( e ), 200 μg / mL ( f ), 500 μg / mL ( g ), e 1000 μg / mL ( h )) por 24 h. A fluorescência verde representa as células vivas e a fluorescência vermelha representa as células mortas. As barras de escala são 100 μm
Imagem de tomografia computadorizada in vitro e determinação do valor de TC
Para avaliar a viabilidade do AuNC @ PEGs em imagens de tomografia computadorizada, comparamos os aumentos de contraste de diferentes concentrações molares (AuNC @ PEGs) com o uso clínico de um agente de contraste (iodo). Imagens de tomografia computadorizada foram obtidas e os valores tomográficos foram medidos. AuNC @ PEGs foram comparados com agentes de imagem de iodo em concentrações semelhantes (50, 100, 200, 500 e 1000 μg / mL). Os resultados mostraram que o valor de CT aumentou com o aumento da concentração (Fig. 4a), e de acordo com a análise dos valores de CT de AuNC @ PEGs e agente de contraste de iodo (Fig. 4b), o coeficiente de absorção de AuNC @ PEGs foi melhor do que os agentes de contraste à base de iodo em concentrações semelhantes, indicando que o uso de AuNC @ PEGs para imagens de tomografia computadorizada é melhor.
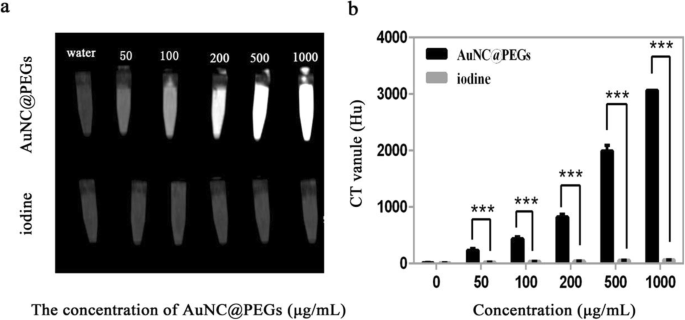
Comparação de resultados de tomografia computadorizada in vitro entre AuNC @ PEGs e agente de contraste à base de iodo. Conforme a concentração aumenta, a intensidade da atenuação de raios-X aumenta ( a ) Comparação dos valores de Hu entre AuNC @ PEGs e agentes de contraste à base de iodo ( b ) *** P <0,001
Imagens de tomografia computadorizada ao vivo
Devido à capacidade de alto contraste do AuNC @ PEGs, comparamos ainda a qualidade de imagem do AuNC @ PEGs com a dos agentes de iodo in vivo. Duzentos microlitros de AuNC @ PEGs (200 μg / mL) foram injetados através da veia da cauda dos ratos. O tempo de angiografia do pool de sangue em AuNC @ PEGs foi avaliado por meio de varredura de ponto de tempo contínua pré-injeção (0 min) e pós-injeção (10, 20, 30, 40, 60 e 90 min). Em seguida, os ratos do grupo controle foram injetados com meio de contraste iodo em concentração adequada. A dose de injeção e o tempo de varredura foram semelhantes aos do AuNC @ PEGs. Após a injeção de um agente de contraste, observamos simultaneamente o aumento do contraste no rim (fig. 5) e o enchimento da bexiga (SI fig. 1). Os resultados mostraram que o rim no grupo AuNC @ PEGs atingiu o pico em 30 min e foi completamente excretado em 90 min e que no grupo de agente de contraste à base de iodo atingiu o pico em 20 min e foi completamente excretado em 60 min. Em seguida, observamos que a bexiga foi sendo preenchida gradativamente com agente de contraste ao longo do tempo. Este achado mostrou que o tempo de angiografia do pool de sangue de AuNC @ PEGs foi melhor do que o do agente de contraste à base de iodo. O maior tempo de circulação sanguínea do AuNC @ PEGs pode fornecer um melhor diagnóstico, e o AuNC @ PEG tem uma melhor perspectiva de desenvolvimento.
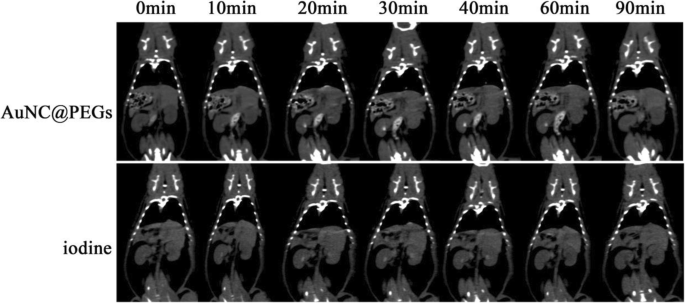
Imagens de TC in vivo dos ratos em diferentes pontos de tempo após a pós-injeção de AuNC @ PEGs
Segurança de AuNC @ PEGs In Vivo
Como mostrado na Fig. 6a, os parâmetros padrão das análises de rotina de sangue e função hepática e renal foram refletidos pelo nível de hemoglobina, concentração de hemoglobina corpuscular média, volume corpuscular médio, contagem de plaquetas, contagem de glóbulos vermelhos, contagem de leucócitos, concentração de albumina, nível de alanina aminotransferase, nível de aspartato aminotransferase e nível de creatinina. Na análise estatística, nenhuma diferença significativa foi observada entre o AuNC @ PEG, agente de contraste de iodo e grupos de controle ( P > 0,05). Além disso, os órgãos (coração, fígado, baço, pulmão e rim) dos ratos foram analisados histologicamente, conforme mostrado na Fig. 6b, 24 h após a injeção de AuNC @ PEGs (200 μg / mL); fatiado; e corado (H&E). Em comparação com o grupo de controle (não injetado com nanomateriais), nenhuma alteração morfológica óbvia e lesões foram encontradas, conforme mostrado ao microscópio. Os resultados acima mencionados confirmaram ainda a segurança e confiabilidade dos AuNC @ PEGs in vivo.
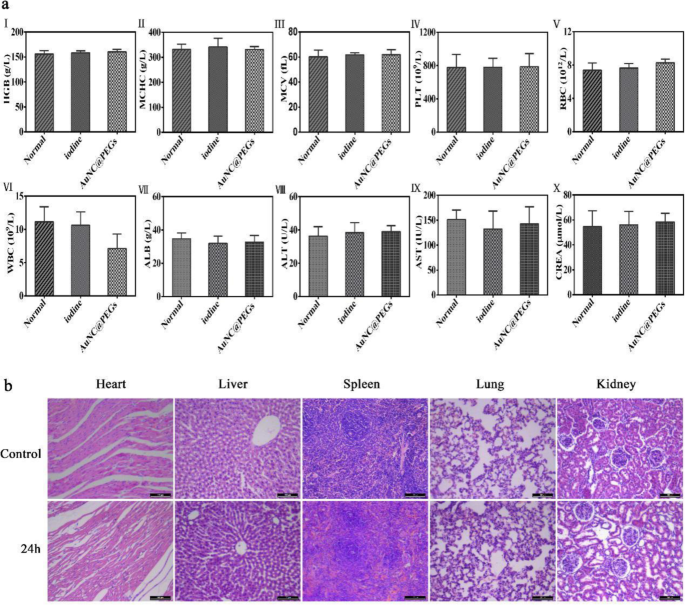
Avaliação da toxicidade in vivo de AuNC @ PEGs. Rotina sanguínea e função hepática e renal:nível de hemoglobina (I), concentração média de hemoglobina corpuscular (II), volume corpuscular médio (III), plaquetas (IV), contagem de glóbulos vermelhos (V), contagem de leucócitos (VI), concentração de albumina (VII), nível de alanina aminotransferase (VIII), nível de aspartato aminotransferase (IX) e nível de creatinina (X) ( a ) A coloração H&E foi realizada nos órgãos (coração, fígado, baço, pulmão e rim) de ratos normais e aqueles injetados com AuNC @ PEGs por 24 h ( b ) As barras de escala de b são 100 μm
Conclusão
Desenvolvemos AuNC @ PEG, um novo tipo de agente de contraste para tomografia computadorizada, com características como tamanho pequeno, alto contraste, longo tempo de retenção de sangue e baixo risco de toxicidade. Avaliações de toxicidade in vitro e in vivo mostraram que AuNC @ PEGs tinha boa biocompatibilidade e baixo risco de efeitos colaterais. O desempenho de imagem da tomografia computadorizada in vitro e in vivo mostrou que AuNC @ PEGs tem um coeficiente de absorção de raios-X mais alto e um tempo mais longo de angiografia de pool de sangue do que os agentes de imagem tradicionais à base de iodo. Além disso, AuNC @ PEGs são superiores aos agentes de imagem à base de iodo, e o uso de AuNC @ PEGs é prático. Todos esses resultados mostraram que AuNC @ PEGs tem um coeficiente de absorção de raios-X mais alto do que os agentes de contraste tradicionais à base de iodo e que o desempenho de imagem do AuNC @ PEGs foi superior ao dos agentes de contraste tradicionais à base de iodo. Portanto, os AuNC @ PEGs funcionalizados sintetizados neste estudo têm grande potencial para aplicação clínica em imagens de tomografia computadorizada.
Disponibilidade de dados e materiais
Os dados brutos / processados necessários para reproduzir essas descobertas não podem ser compartilhados neste momento, pois os dados também fazem parte de uma pesquisa e desenvolvimento em andamento.
Abreviações
- CT:
-
Tomografia computadorizada
- DCF:
-
Diclorofluoresceína
- DCFH:
-
Diclorofluorescina
- H 2 O 2 :
-
Peróxido de hidrogênio
- LDH:
-
Lactato desidrogenase
- MTT:
-
Brometo de 3- (4,5-dimetiltiazol-2-il) -2,5-difeniltetrazólio
- PBS:
-
Salina tamponada com fosfato
- PEG:
-
Polietileno glicol
- ROS:
-
Espécies que reagem ao oxigênio
- TEM:
-
Microscopia eletrônica de transmissão
Nanomateriais
- Nova Certificação para a Elite de Lubrificação
- Um Novo Legado para AM:Capacitando a Escolha pela Sustentabilidade
- IBM &Warwick Image Molécula Triangular Altamente Reativa pela Primeira Vez
- Nanotecnologia:do Sistema de Imagem In Vivo à Entrega Controlada de Medicamentos
- Novel Biocompatible Au Nanostars @ PEG Nanopartículas para imagens In Vivo CT e propriedades de depuração renal
- Método de pós-tratamento para a síntese de nanopartículas FePt-Fe3O4 binárias monodispersas
- Emissão de infravermelho próximo Cr3 + / Eu3 + Co-dopado com galogermanato de zinco Nanopartículas luminescentes de persistência para imagem celular
- Síntese de nanopartículas carbonáceas dopadas com cério inspirada na biomineralização para atividade de eliminação de radical hidroxila elevada
- Nanopartículas de albumina conjugada com corante próximo ao infravermelho e carregadas com artesunato como agente fotoquimo teranóstico direcionado a tumor de alta eficiência
- AI:encontre o uso certo para a inteligência artificial



