Síntese fácil em um vaso de pontos de carbono de polidopamina para terapia fototérmica
Resumo
Pontos de carbono (CDs) são um membro de nanomateriais de carbono fluorescentes que são amplamente aplicados em bioimagem, terapia fototérmica (PTT) e biossensores por sua fluorescência sintonizável, propriedade de conversão fototérmica e excelente biocompatibilidade. Passivação de superfície e dopagem, especialmente a dopagem de átomos de N, são fatores críticos para aumentar a intensidade fluorescente dos CDs. Até agora, uma variedade de moléculas ricas em nitrogênio tem sido aplicada para a passivação de superfície de CDs, como L-Dopa, aminoácidos e polietilenimina (PEI). Aqui, relatamos a síntese de pontos de carbono passivados por polidopamina fluorescente (PDA) (CD-PDA) por meio de pirólise assistida por micro-ondas em um único recipiente em 5 min, simplificando drasticamente o processo de reação em comparação com o tratamento hidrotérmico relatado antes. DLS, FT-IR, UV-Vis e espectroscopia de fluorescência foram usados para confirmar os componentes do CD-PDA e iluminar o mecanismo de sua fotoluminescência sintonizável (PL). Devido à dopagem de átomos de N por PDA, o rendimento quântico (QY) do CD-PDA foi medido em 5%, o que foi quase o triplo dos CDs originais sem adição de PDA. O rendimento do CD-PDA foi cerca de 1,5 vezes o dos CDs devido ao aumento do local de nucleação para a formação do ponto de carbono com o grupo fenólico fornecido pelo PDA. Enquanto isso, a eficiência de conversão fototérmica do CD-PDA foi determinada em 35% devido à excelente propriedade de conversão luz-térmica NIR do PDA. No geral, fornecemos uma abordagem extremamente eficiente para fabricar o CD-PDA fluorescente dopado com N com eficiência de conversão fototérmica estável e excelente biocompatibilidade. Mais importante ainda, a passivação do PDA permitiu que o CD-PDA sintetizado em nossa pesquisa fosse compatível para modificações posteriores por meio da adição de Michael ou da reação à base de Schiff.
Histórico
Como um membro de materiais de carbono de baixa dimensão, o vasto SP misturado 2 e SP 3 átomos, bem como elétrons π em pontos de carbono (CDs) aumentam significativamente os defeitos e heteroátomos dos sistemas fotoativos, desencadeando assim a energia da luz absorvida em calor ou a liberação de fótons estimulados. Os CDs têm sido amplamente aplicados em bioimagem, terapia fototérmica (PTT) e biossensores por sua fluorescência sintonizável, propriedade de conversão fototérmica e excelente biocompatibilidade. Os pontos quânticos de carbono magnetofluorescentes carregados com drogas (MCQDs) sintetizados por meio de tratamento hidrotérmico e reação de reticulação relatados antes realizaram a combinação de PTT e terapia fotodinâmica (PDT) através da fabricação de uma plataforma de terapia de câncer quimio-foto eficiente [1]. Até agora, métodos extensivos foram explorados para aumentar a intensidade fluorescente de CDs desde sua primeira descoberta durante a purificação de nanotubos de carbono de parede única descarregados por arco (SWCNTs) em 2004 [2], apesar das rotas sintetizadas para atingir certo grau de oxidação sendo geral complicado. O tratamento de cima para baixo e de baixo para cima são duas vias comuns para sintetizar os CDs, incluindo ablação a laser [3, 4], tratamento com ácido oxidativo [5, 6], tratamento hidrotérmico [7, 8], pirólise assistida por micro-ondas [9, 10,11], oxidação eletroquímica [12, 13], irradiação ultrassônica [14] e tratamento com plasma [15].
Pesquisas mostram que a dopagem de átomos de N é de grande importância para o aumento da fluorescência dos CDs [16,17,18]. Liu et al. usou polietilenimina (PEI) fornecendo os átomos de N para fabricar CDs funcionalizados com PEI por pirólise de glicerol assistida por microondas (700 W) em uma etapa e PEI ramificado; o rendimento quântico (QY) do sistema foi medido até 15,3%, e foi aplicado para imagens de células e entrega de genes [19]. Zhou et al. relataram o desenvolvimento de pontos de carbono co-dopados com fósforo e nitrogênio (CDs dopados com N-P) para bioimagem por meio do tratamento hidrotérmico do nucleotídeo adenosina-5′-trifosfato (ATP) a 180 ° C por 10 h. Normalmente, ATP foi a única fonte de material para a dopagem de ambos os átomos de N e P para aumentar os defeitos na superfície do sistema, levando ao aumento de QY dos CDs dopados com N-P (calculado em 9,8%) [20]. Além disso, foi relatado que os compostos fenólicos podem servir como uma semente catalítica para o crescimento de pontos de carbono. Lee et al. descobriram que os pontos de carbono aumentaram dramaticamente com a adição de uma pequena quantidade de ácido ferúlico [21].
A polidopamina (PDA) é um tipo de polímero semelhante à melanina derivado da polimerização do monômero de dopamina (DA), que tem sido amplamente aplicado para modificação de superfície de vários materiais desde que foi inicialmente estudado como um agente adesivo de modificação de superfície [22]. Como todos sabemos, grandes quantidades de grupos funcionais hidroxila fenólicos e ricos em N, como a catecolamina no PDA, tornam-no um passivante e catalisador potencialmente excelente para os CDs.
Inspirados por isso, relatamos uma via de pirólise assistida por micro-ondas fácil e eficiente para a síntese de CDs funcionalizados com PDA ao longo de 5 min. Espalhamento de luz dinâmico (DLS), espectroscopia de infravermelho com transformada de Fourier (FT-IR), microscopia eletrônica de transmissão (TEM), espectroscopia ultravioleta e visível (UV-Vis) e espectroscopia de fluorescência foram usados para definir os componentes dos pontos de carbono de polidopamina (CD- PDA) e sua fotoluminescência ajustável (PL). Viabilidades celulares relativas de células HeLa tratadas por CD-PDA com e sem irradiação NIR foram medidas pelo ensaio de brometo de 3- (4,5-dimetiltiazol-2-il) -2,5-difeniltetrazólio (MTT) padrão.
Resultados e discussão
Síntese e caracterização de CD-PDA
Nesta pesquisa, sintetizamos os pontos de carbono funcionalizados com polidopamina (PDA) (CD-PDA) por meio de pirólise de glicerina e PDA assistida por micro-ondas em um único recipiente. Os pontos de carbono (CDs) fabricados através da mesma abordagem de pirólise assistida por micro-ondas sem adicionar PDA foram definidos como um grupo de controle. A ilustração esquemática do processo de síntese de CD-PDA foi descrita conceitualmente no Esquema 1. O rendimento do CD-PDA foi quase 1,5 vezes maior que o dos CDs, devido ao aumento do local de nucleação para a formação de pontos de carbono com o grupo fenólico fornecido por PDA [21].
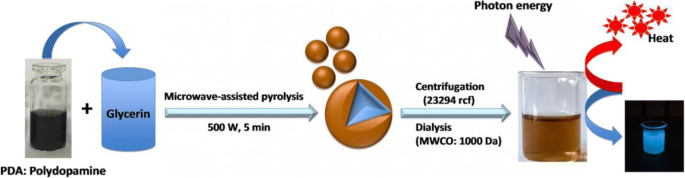
Ilustração esquemática do processo de síntese de CD-PDA
Perfis de espalhamento dinâmico de luz (DLS) revelaram o tamanho de partícula e o potencial zeta de CD-PDA. O tamanho de partícula hidrodinâmica de CD-PDA foi de 51,5 ± 19,5 nm (inserção da Fig. 1a) e o potencial zeta foi determinado como sendo - 27,5 ± 0,4 mV, indicando grupos carregados negativamente na superfície dos nanopontos, o que demonstrou ainda mais a superfície modificação por PDA. O tamanho de partícula hidrodinâmica de CDs dispersos em água DI foi de 5,5 ± 2,5 nm (inserção da Fig. 1b). Imagens de microscopia eletrônica de transmissão (TEM) caracterizaram as nanopartículas esféricas monodispersas e distribuídas por tamanho uniforme (Fig. 1a, b); o diâmetro do CD-PDA foi de ~ 25 nm (Fig. 1c) e o dos CDs (Fig. 1d) foi medido a ~ 5 nm. Após a modificação da superfície por PDA, o crescimento do diâmetro do CD-PDA foi de cerca de 20 nm em comparação com o dos CDs.
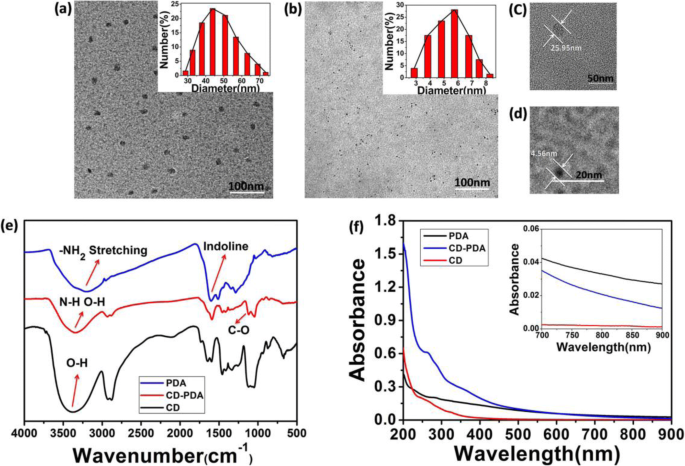
Morfologia, espectros de FT-IR e espectros de UV-Vis de CD-PDA e CDs. a Imagem TEM de CD-PDA (barra de escala 100 nm, inserção:distribuição de tamanho determinada por DLS). b Imagem TEM de CDs (barra de escala 100 nm, inserção:distribuição de tamanho determinada por DLS). c Imagem ampliada de um único CD-PDA (barra de escala 50 nm). d Imagem ampliada de um único CD (barra de escala 20 nm). e Espectros FT-IR de CD-PDA, CDs e PDA. f Espectros de UV-Vis de CD-PDA, CDs e PDA (inserção:a absorbância de 600 a 900 nm)
A passivação do PDA nos pontos de carbono foi registrada por espectros FT-IR. Aqui, o PDA foi sintetizado por meio da polimerização de 20 mg de cloridrato de DA em 10 mL de tampão Tris (pH 8,5, 10 mM) à temperatura ambiente por 12 he depois foi centrifugado a 23.294 rcf. Conforme as informações do espectro de picos característicos de CD-PDA, CDs e PDA observados na Fig. 1e, o pico de 3400 cm −1 e 1600 cm −1 sugeriu os grupos catecol –OH e anéis aromáticos de PDA, que também existiam no CD-PDA [23, 24]. Novos picos aparecendo em 1642 cm −1 , 1588 cm −1 e 1640 cm −1 referido a C =O, N – H e C – N enquanto o pico em 3400 cm −1 indicou a existência de –OH e N – H no sistema, o que ilustrou ainda mais a modificação de superfície do PDA nos CDs. O N – H, C =O e C – N emergentes nos pontos de carbono durante a oxidação assistida por micro-ondas demonstraram os mecanismos da passivação de superfície para os nanopontos:durante a oxidação assistida por micro-ondas de 5 minutos ocorreu a polimerização da dopamina e a desidratação do sistema para formar o núcleo dos nanopontos, após o que foi o crescimento dos pontos de carbono.
Os espectros de absorção de UV-Vis de CD-PDA, CDs e PDA com a mesma concentração são mostrados na Fig. 1f (concentração da amostra inserida na Fig. 1f, 12,5 μg / mL). Como passivante de superfície do sistema, o PDA exibiu absorção de amplo espectro de 200 a 900 nm, especialmente na região do infravermelho próximo, o que foi essencial para a excelente propriedade de conversão fototérmica do CD-PDA. A absorção em 220 nm e 280 nm representou a transição de elétrons entre o forte π-stacking do anel fenil como um sistema conjugado, verificando a modificação do PDA. Particularmente, a redução óbvia de absorção em 280 nm indicou a barreira espacial entre as fortes interações de empilhamento π no sistema conjugado após a passivação de PDA [25], enquanto os espectros de absorção de UV-Vis de CD-PDA mostram os picos característicos ao redor 274 nm e 370 nm, e o dos CDs foi medido a 260 nm e 330 nm. O deslocamento batocrômico de 330 para 370 nm foi responsável pela introdução do amidogênio do PDA, que também foi caracterizado pela quelação da glicerina e do PDA [26, 27]. A inserção é a absorbância de CD-PDA, CDs e PDA do comprimento de onda de 600 a 900 nm.
Fotoluminescência de CD-PDA
Como relatado antes, a modificação da superfície dos pontos de carbono pode afetar seu processo de conversão de fótons em grande medida, levando a uma enorme diversidade nos espectros de fluorescência [28, 29]. Em nossa pesquisa, o pico de emissão do CD-PDA mudou para o vermelho de 450 para 500 nm com o comprimento de onda de excitação alterado de 350 para 420 nm (Fig. 2a). Consequentemente, observamos imagens de microscopia fluorescente vermelha, azul e verde mergulhando gotas em uma lâmina de vidro, esclarecendo ainda mais a enorme diversidade de fluorescência para CD-PDA (inserção da Fig. 2a). Além disso, detectamos as imagens macroscópicas do CD-PDA, CDs e água DI sob a iluminação de luz ultravioleta (365 nm), confirmando que a intensidade fluorescente do CD-PDA era muito mais forte do que a dos CDs (Fig. 2b). A Figura 2c ilustra ainda o aumento da intensidade fluorescente após a modificação da superfície de PDA; o rendimento quântico (QY) de CD-PDA foi quase o triplo dos CDs (sulfato de quinina foi selecionado como a amostra padrão [19]), verificando o efeito da dopagem de átomos de N de PDA. Testamos a estabilidade da intensidade fluorescente de CD-PDA; não mostrou uma mudança clara sob a irradiação de 2100 s (365 nm), exibindo, portanto, propriedade de fotoluminescência estável (Fig. 2d).
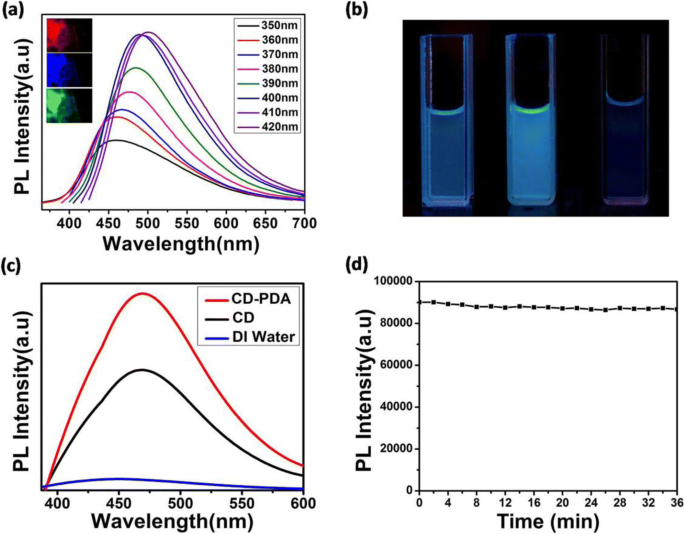
Propriedades ópticas de CD-PDA e CDs. a Espectros de fotoluminescência de CD-PDA (os comprimentos de onda de excitação variam de 350 a 420 nm com 10 incrementos, inserção:imagens de microscopia fluorescente de CD-PDA). b Da esquerda para a direita:CDs, CD-PDA e água DI sob irradiação de luz ultravioleta (365 nm). c Espectros de fotoluminescência de CD-PDA, CDs e água DI. d Curva de estabilidade da intensidade fluorescente de CD-PDA
Para estudar mais a influência do PDA no aumento da intensidade fluorescente do CD-PDA, medimos primeiramente a intensidade fluorescente contra a duração da polimerização da dopamina em tampão Tris. O gradiente de fotoluminescência na Fig. 3a ilustrou que CD-PDA com dopamina polimeriza em tampão Tris por 2 h exibiu a maior intensidade fluorescente, indicando a influência da extensão da pré-polimerização de dopamina. Exploramos ainda mais a intensidade fluorescente de CD-PDA com várias concentrações originais de PDA em tampão Tris (3, 5, 7 e 9 mg / mL). Como as concentrações originais de DA variam de 3 a 9 mg / mL, a fluorescência do CD-PDA apresentou tendência de primeiro aumentar e depois diminuir (Fig. 3b).
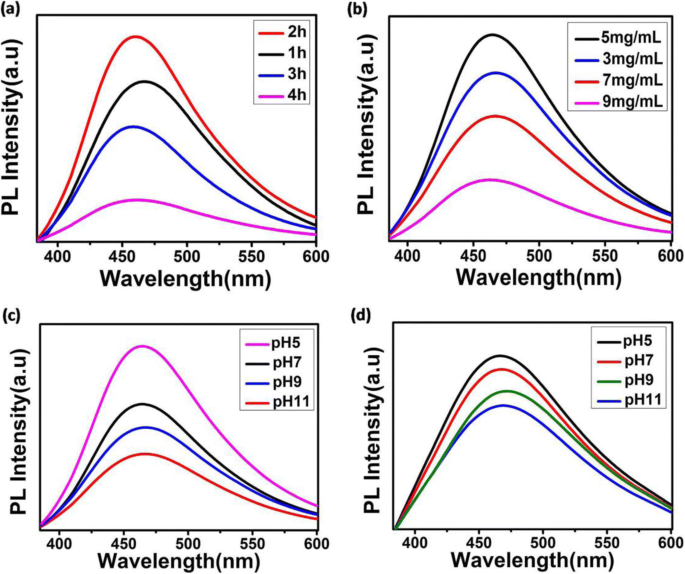
Espectros de fotoluminescência de CD-PDA. a Intensidade fluorescente de CD-PDA com várias durações de polimerização de dopamina em tampão Tris. b Intensidade fluorescente de CD-PDA com várias concentrações originais de dopamina. c Intensidade fluorescente de CD-PDA com diferentes pH antes da pirólise assistida por microondas. d Intensidade fluorescente de CD-PDA com pH diferente após a pirólise assistida por microondas
Além disso, investigamos a intensidade fluorescente de CD-PDA com vários pH iniciais; a intensidade fluorescente diminuiu à medida que o pH do tampão Tris aumentou de 5 para 11 (Fig. 3c). A Figura 3d exibiu a influência do pH após a oxidação assistida por microondas. O pH do sistema após a oxidação assistida por microondas foi mediado de 5 a 11, e comparamos a intensidade fluorescente do CD-PDA; meio ácido (pH 5,0) levou a fluorescência mais forte, o que também indicou fluorescência mais forte de CD-PDA no microambiente tumoral ácido.
Desempenho fototérmico e citotoxicidades de CD-PDA
Medição de eficácia fototérmica
Para demarcar a análise da eficiência de conversão fototérmica de CD-PDA e CDs, avaliamos quantitativamente o incremento de temperatura em função do tempo sob irradiação; PDA foi selecionado como um grupo de controle adicional. Sob irradiação de 10 min (808 nm, 2 W / cm 2 ), o incremento de temperatura do CD-PDA foi de 27 ° C, enquanto o do PDA foi de cerca de 30 ° C a 200 μg / mL. Enquanto isso, o incremento de temperatura dos CDs (200 μg / mL) sob irradiação durante os 10 min foi de cerca de 7,5 ° C e o da água DI não foi superior a 5 ° C (Fig. 4a). Além disso, medimos a elevação da temperatura do CD-PDA em várias concentrações em função do tempo sob uma densidade de potência de 2 W / cm 2 Irradiação de laser NIR durante 10 minutos. No geral, o aumento da temperatura cresceu com o aumento da concentração do CD-PDA, e a temperatura aumentou mais rapidamente à medida que a concentração de CD-PDA aumentou de 25 para 200 μg / mL (Fig. 4b). Com isso, desenhamos a curva do incremento de temperatura contra várias concentrações de CD-PDA, entre as quais o incremento de temperatura de CD-PDA a 200 μg / mL, 100 μg / mL, 50 μg / mL e 25 μg / mL foi de cerca 27 ° C, 18 ° C, 13 ° C e 10 ° C, respectivamente (Fig. 4d). Normalmente, a fim de estudar a influência na eficiência de conversão fototérmica de CD-PDA contra várias concentrações iniciais de DA em tampão Tris, medimos a mudança de temperatura de CD-PDA (200 μg / mL) com várias concentrações originais de DA em Tris tampão (Fig. 4c). A temperatura aumentou conforme a concentração de DA melhorou de 3 para 9 mg / mL. O aumento da temperatura foi de 27 ° C quando a concentração original de DA foi de 9 mg / mL, enquanto o incremento de temperatura foi de apenas 10 ° C quando a concentração original de DA foi de 3 mg / mL. A curva de resfriamento natural de CD-PDA é apresentada na Fig. 4e (200 μg / mL, 808 nm, 2 W / cm 2 , 20 min), e os dados mais enxutos de - lnθ calculados a partir do período de resfriamento são observados na Fig. 4f. A eficiência de conversão fototérmica de CD-PDA foi medida em 35%, maior do que a dos nanobastões de Au relatados antes (valor da literatura, 22% [30]).
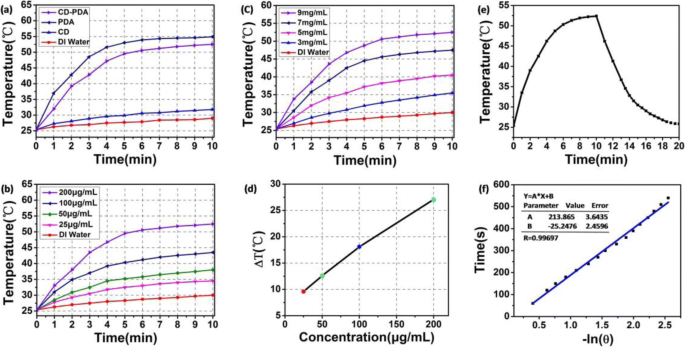
Propriedades de conversão fototérmica de CD-PDA e CDs. a Curvas de aquecimento fototérmico de CD-PDA, CDs, PDA e água DI sob uma densidade de potência de 2 W / cm 2 Irradiação com laser NIR por 10 min. b Curvas de aquecimento fototérmico de CD-PDA em várias concentrações durante 10 min. c Curvas de aquecimento fototérmico de CD-PDA (200 μg / mL) com várias concentrações originais de DA em tampão Tris. d Incremento de temperatura do CD-PDA em várias concentrações. e Curva de resfriamento de CD-PDA (sob uma densidade de potência de 2 W / cm 2 Irradiação NIR nos primeiros 10 min e resfriamento natural à temperatura ambiente). f Dados de tempo mais enxutos versus - lnθ calculado de acordo com a curva de resfriamento do CD-PDA
Viabilidade celular in vitro
As citotoxicidades de CD-PDA, CDs e PDA foram analisadas por um ensaio MTT padrão. Para avaliar as diferenças de viabilidade celular entre CD-PDA, CDs e PDA, células HeLa foram incubadas com essas nanopartículas na mesma concentração em cada grupo. Os resultados do MTT (Fig. 5a) revelaram que a viabilidade celular das células HeLa exibiu uma relação dependente da dose com o CD-PDA, CDs e PDA. Foi relatado que a superfície modificada com PDA rica em quinonas foi ativa na atividade de proliferação celular [31]. É notável em nosso estudo que o CD-PDA poderia obviamente promover a viabilidade celular de células HeLa mesmo na concentração de 50 μg / mL devido à modificação da superfície por PDA e a viabilidade celular não foi dramaticamente inibida a 100 μg / mL, que basicamente compartilhou a mesma tendência com os resultados do PDA, enquanto a viabilidade das células HeLa que foram incubadas com os CDs reduziu para 80% e 70% a 100 μg / mL e 200 μg / mL, respectivamente.
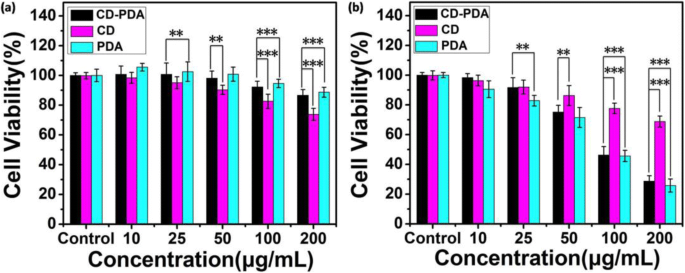
Citotoxicidade in vitro contra células HeLa. a Viabilidade celular in vitro de células HeLa incubadas com CD-PDA, CDs e PDA em várias concentrações por 24 h. b Viabilidade celular in vitro de células HeLa incubadas com CD-PDA, CDs e PDA em várias concentrações sob irradiação (808 nm, 2 W / cm 2 , 5 min; média ± DP, n =6). * p <0,05, ** p <0,01, *** p <0,001
O ensaio MTT padrão foi ainda avaliado em células HeLa para determinar a eficiência de morte fototérmica de CD-PDA, CDs e PDA. As células HeLa foram incubadas com essas nanopartículas na mesma concentração em cada grupo. Enquanto sob irradiação (808 nm, 2 W / cm 2 , 5 min), o ensaio de MTT (Fig. 5b) mostrou que a eficácia de eliminação fototérmica de CD-PDA, CDs e PDA foi aumentada em função de sua concentração. No geral, a viabilidade celular de células HeLa incubadas com CD-PDA foi reduzida para 30% a 200 μg / mL, manifestando a eficácia de eliminação fototérmica do sistema. Enquanto isso, é digno de nota que a diferença de viabilidade celular entre CD-PDA e PDA diminuiu progressivamente conforme sua concentração aumentou de 25 para 200 μg / mL graças ao óbvio incremento de temperatura de CD-PDA sob irradiação NIR juntamente com a melhoria de sua concentração (Fig. 4b, 4d). Além disso, a viabilidade celular de células HeLa incubadas com CDs sob irradiação NIR foi de 68% a 200 μg / mL, o que não foi uma variação significativa em comparação com aquela na mesma concentração sem laser NIR devido à sua fraca absorção de luz na região do infravermelho próximo (Fig. 1e).
Conclusões
Neste trabalho, relatamos a síntese de pontos de carbono passivados por polidopamina fluorescente (PDA) (CD-PDA) por meio de pirólise assistida por micro-ondas em 5 min, simplificando drasticamente o processo de reação, promovendo sua intensidade fluorescente devido ao doping de Átomos de N de PDA, e melhorando seu rendimento devido ao aumento do local de nucleação para a formação de pontos de carbono com o grupo fenólico fornecido por PDA. Após a passivação do PDA, o rendimento do CD-PDA foi de quase 1,5 vezes o dos CDs; o rendimento quântico de CD-PDA foi de ~ 5%, o triplo dos CDs originais. A eficiência de conversão fototérmica do sistema foi medida em 35%, maior do que os nanobastões de Au relatados antes (22%). Durante o teste in vitro, o CD-PDA exibiu excelente biocompatibilidade e desempenho do PTT; poderia até promover a viabilidade celular de células HeLa com a concentração chegando a 50 μg / mL. Durante a irradiação, a viabilidade celular das células HeLa reduziu para 30%. Mais importante ainda, a passivação do PDA permitiu que o sistema fosse compatível para modificações posteriores por meio da adição de Michael ou da reação de base de Schiff.
Métodos / Experimental
Materiais
Todos os reagentes químicos eram de grau analítico e usados sem purificação adicional, a menos que indicado de outra forma. O cloridrato de dopamina (DA) foi adquirido da Sigma-Aldrich (EUA); sulfato de quinina (98%, adequado para fluorescência) foi obtido da Fluka (EUA); e glicerina (> 99%), Tris, dimetilsulfóxido (DMSO,> 99,8%) e membranas de diálise (MWCO 1000 Da) foram fornecidos pela Sangon Biotech (Shanghai, China). Brometo de 3- (4, 5-Dimetiltiazol-2-il) -2, 5-difeniltetrazólio (MTT), tripsina e solução de estreptomicina-penicilina foram obtidos de Beyotime Biotechnology (Shanghai, China). O meio Eagle de modificação de Dulbecco (DMEM) foi obtido da Hyclone (EUA). O soro fetal bovino (FBS) foi adquirido na Biological Industries (Israel). As células HeLa foram fornecidas pela American Type Culture Collection (ATCC).
Instrumentação e caracterização
A composição elementar foi confirmada por espectroscopia de infravermelho com transformada de Fourier conduzida no espectrômetro Nicolet 380 (FT-IR, Thermo Nicollet, Instruments, Ltd., América). Os espectros de UV-Vis foram caracterizados por espectrofotômetro de infravermelho próximo Perkin Elmer Lambda 750 UV-vis (UV-vis-NIR, Perkin-Elmer, Norwalk, CT). Os espectros de fotoluminescência (PL) foram medidos por Infinite 200PRO Fluorometer (Tecan, Instruments, Ltd., Suíça). A distribuição do diâmetro e o potencial zeta foram realizados por Mastersizer2000 (DLS, Nano-ZS, Malvern, Instruments, Ltd., UK). A morfologia e o diâmetro foram representados por microscopia eletrônica de transmissão (TEM, Tecnai G, Spirit, FEI, Hong Kong). O forno de micro-ondas doméstico foi servido como fonte de micro-ondas (500 W) e ainda de reação (Galanz, Instruments, Ltd., China).
Preparação de CD-PDA e CDs
Em primeiro lugar, 50 mg de cloridrato de dopamina foram completamente dissolvidos em 10 mL de tampão Tris (10 mM, pH 8,5) e autopolimerizados à temperatura ambiente durante 2 h sob agitação magnética. Em seguida, o CD-PDA foi sintetizado pela mistura direta de 6 mL de solução de PDA pré-polimerizada acima e 20 mL de glicerina (> 99%) antes de 5 min de oxidação assistida por microondas (500 W) e da etapa de purificação de acompanhamento. Enquanto os CDs foram preparados por 5 min de oxidação assistida por microondas (500 W) de 20 mL de glicerina, ele foi definido como um grupo de controle. Posteriormente, tanto o CD-PDA quanto os CDs foram purificados por diálise contra água DI por 48 h (MWCO 1000 Da) e finalmente coletados por centrifugação (23.294 rcf, 10 min) e liofilização.
Medição de rendimentos quânticos fluorescentes
O rendimento quântico (QY) de CD-PDA foi medido através do método colorimétrico relatado antes [19], sulfato de quinina (em 0,1 M H 2 SO 4 ) foi selecionada como amostra padrão (literatura QY 54%), e a emissão de fotoluminescência (PL) foi medida pelo Fluorômetro Infinite 200PRO. No geral, o valor específico para intensidade fluorescente de CD-PDA e quinino representou o QY de CD-PDA (comprimento de onda de excitação 350 nm) na condição de que eles compartilhavam o mesmo valor de densidade óptica (OD) inferior a 0,02 (comprimento de onda 350 nm). A intensidade fluorescente integrada foi a área abaixo da curva PL com o comprimento de onda variando de 380 a 700 nm. Basicamente, sulfato de quinina dissolvido em H 0,1 M 2 SO 4 foi servido como a amostra padrão (valor OD 0,02, comprimento de onda 350 nm); O CD-PDA foi disperso em água DI, e medimos seu valor OD para 0,02 a fim de excluir a influência da absorção de luz. Em seguida, medimos a intensidade fluorescente de CD-PDA e quinino para calcular a área das curvas PL. Os CDs foram configurados como um grupo de controle. O valor absoluto do QY foi calculado de acordo com a fórmula:
$$ {F} _X ={F} _ {ST} \ left (\ frac {{\ mathrm {Grad}} _ X} {{\ mathrm {Grad}} _ {ST}} \ right) \ left (\ frac {R_X ^ 2} {R_ {ST} ^ 2} \ direita) $$
Portanto, F é o QY, Grad é o gradiente da curva PL, ST e X representam o padrão e o grupo de teste, respectivamente, e R é o índice de refração do solvente.
Medição do desempenho fototérmico
CD-PDA, CDs e PDA foram todos dispersos em água DI e suas concentrações foram mediadas a 200 μg / mL. Em seguida, adicionamos 1 mL de solução acima na célula de quartzo padrão, respectivamente, e configuramos a fonte de diodo laser (STL 808CFS-10W, China) acima do nível do líquido cerca de 1 cm para cobrir completamente a solução. Medimos as mudanças de temperatura de CD-PDA e CDs a cada minuto sob uma densidade de potência de 2 W / cm 2 Irradiação com laser NIR; PDA e água DI foram definidos como grupos de controle. Em seguida, encerramos a irradiação e registramos as mudanças de temperatura à medida que o CD-PDA esfria naturalmente até a temperatura ambiente para traçar a curva de resfriamento. A eficiência de conversão fototérmica do CD-PDA foi calculada de acordo com a fórmula relatada antes [30].
Cultura de células
As células HeLa foram cultivadas em meio Eagle modificado por Dulbecco (DMEM, HyClone) contendo alta glicose com 10% de soro fetal bovino (FBS), penicilina (100 U / mL) e estreptomicina (100 μg / mL) na temperatura de 37 ° C e 5% CO 2 atmosfera umidificada. Mudamos o meio de cultura uma vez por dia.
Ensaio de viabilidade celular
A citotoxicidade do CD-PDA foi medida através do ensaio MTT padrão. As células HeLa foram semeadas em placas de 96 poços com uma densidade de 2 × 10 4 células por poço e cultivadas por 24 h a 37 ° C, 5% CO 2 atmosfera umidificada. Em seguida, limpamos as células HeLa três vezes com PBS fresco, após o que o CD-PDA disperso em DMEM com várias proporções de peso (10, 25, 50 e 100 μg / mL) foi adicionado a cada poço. Depois, foi incubado por mais 24 h a 37 ° C, 5% CO 2 atmosfera umidificada. O meio de cultura foi substituído por 200 μL de DMEM contendo 20 μL de MTT (5 mg / mL em PBS) e incubado por mais 4 h a 37 ° C, 5% de CO 2 atmosfera umidificada. Finalmente, removemos completamente o meio e adicionamos 200 μL de DMSO em cada poço, agitando por mais 15 min. A absorvância de cada poço foi medida a 490 nm. As células HeLa não tratadas (cultivadas em DMEM) foram definidas como um grupo de controle. As viabilidades celulares relativas das células HeLa foram calculadas de acordo com a fórmula Abssample / Abscontrol × 100%. Para isso, o Abssample é a absorbância de células HeLa tratadas por CD-PDA enquanto o Abscontrol representa a absorbância de células HeLa não tratadas.
Abreviações
- CD-PDA:
-
Pontos de carbono de polidopamina
- CDs:
-
Pontos de carbono
- DA:
-
Dopamina
- DLS:
-
Espalhamento de luz dinâmico
- DMEM:
-
Meio Eagle de modificação de Dulbecco
- DMSO:
-
Dimetilsulfóxido
- FBS:
-
Soro fetal bovino
- FT-IR:
-
Espectroscopia de infravermelho com transformada de Fourier
- MTT:
-
Brometo de 3- (4, 5-Dimetiltiazol-2-il) -2, 5-difeniltetrazólio
- NIR:
-
Região do infravermelho próximo
- OD:
-
Densidade ótica
- PDA:
-
Polidopamina
- PEI:
-
Polietilenimina
- PL:
-
Fotoluminescência
- PTT:
-
Terapia fototérmica
- QY:
-
Rendimento quântico
- SWCNTs:
-
Nanotubos de carbono de parede única
- TEM:
-
Microscopia eletrônica de transmissão
- UV-Vis:
-
Espectroscopia ultravioleta e visível
Nanomateriais
- Nanorods de ouro revestidos com BSA para terapia fototérmica NIR-II
- Pontos de carbono luminescente azul independente de excitação de alta eficiência
- Síntese de pontos quânticos do tipo II / tipo I suprimida por reabsorção / CdS / ZnS Core / Shell Quantum Dots e sua aplicação para ensaio de imunossorvente
- Síntese de pontos quânticos de carbono co-dopados com N, S ricos em piridínicos como imitações de enzimas eficazes
- Síntese fácil de nanopartículas de SiO2 @ C ancoradas em MWNT como materiais de ânodo de alto desempenho para baterias de íon-lítio
- Uma abordagem simples para sintetizar pontos quânticos de carbono fluorescentes de águas residuais de Tofu
- Síntese e desempenho in vitro de nanopartículas de ferro-platina revestidas com polipirrole para terapia fototérmica e imagem fotoacústica
- Síntese sonoquímica fácil de uma etapa e propriedades fotocatalíticas de compostos de pontos quânticos de grafeno / Ag3PO4
- Síntese fácil de nanocompósitos magnéticos funcionalizados por superfície para adsorção efetivamente seletiva de corantes catiônicos
- Síntese fácil de pontos quânticos bidimensionais de perovskita de Ruddlesden-Popper com propriedades ópticas ajustáveis



