Carbono poroso hierárquico com poros solicitados interconectados de resíduos biológicos para eletrodos supercapacitores de alto desempenho
Resumo
Usar biorresíduos como precursores para a preparação de nanomateriais de valor agregado é fundamental para o desenvolvimento sustentável de dispositivos. Os lignosulfonatos são subprodutos das indústrias de celulose e papel e geralmente descartados como resíduos. No presente estudo, o lignosulfonato é usado como o precursor para preparar carbono poroso ordenado hierárquico com poros interconectados para a aplicação de armazenamento de energia eletroquímica. A estrutura molecular única e as propriedades do lignosulfonato garantem a aquisição de carbono poroso de alta qualidade com uma estrutura de poro controlável e propriedades físicas aprimoradas. Como resultado, o carbono poroso de ordem hierárquica conforme preparado mostra excelente desempenho de armazenamento de energia quando usado para montar o supercapacitor simétrico, que exibe capacitância específica alta de 289 F g −1 a uma densidade de corrente de 0,5 A g −1 , com a densidade de energia de 40 Wh kg −1 na densidade de potência de 900 W kg −1 . O presente estudo fornece uma estratégia promissora para a fabricação de dispositivos de armazenamento de energia de alto desempenho e baixo custo.
Introdução
Os supercapacitores são promissores como dispositivos de armazenamento de energia para sistemas de backup e diversos eletrônicos devido à sua alta densidade de potência, ciclo de vida longo, peso leve em comparação com baterias e capacitores convencionais [1,2,3,4,5,6]. Os nanomateriais à base de carbono são conhecidos por seu excelente desempenho de armazenamento de energia como materiais de eletrodo ativo em supercapacitores que armazenam eletricidade por meio da camada dupla eletroquímica. Seu desempenho de armazenamento de energia é determinado pelas propriedades físicas dos materiais ativos do eletrodo, especialmente a estrutura porosa [7,8,9]. Os macroporos (maiores que 50 nm) servem como reservatórios de tampão de íons, mesoporos (2–50 nm) como canais de transporte de íons de eletrólito e microporos geralmente como locais de armazenamento de carga [10]. Nosso trabalho anterior baseado na investigação de correlação linear indica que a capacitância específica e a capacidade de taxa estão altamente relacionadas ao volume de ambos os microporos e mesoporos [11, 12], respectivamente. Espera-se que os supercapacitores baseados em nanomateriais de carbono tenham uma estrutura porosa hierárquica com a distribuição equilibrada de macroporos, mesoporos e microporos que estão interconectados.
Esforços consideráveis foram feitos para preparar carbono poroso hierárquico para melhor desempenho de armazenamento de energia [13,14,15,16]. Os pesquisadores desenvolveram vários modelos rígidos, incluindo zeólita, MCM-41, MCM-48, SBA-15, SBA-16 e KIT-6 para preparar carbono poroso com mesoporos ordenados [17, 18]. Tratamentos de ativação química e física também são amplamente empregados, os quais geralmente resultam em poros fechados distribuídos aleatoriamente [13] e, portanto, apresentam baixa controlabilidade sobre a estrutura dos poros.
Biomassa e resíduos biológicos têm sido química e fisicamente ativados a temperaturas elevadas para a preparação de carbono poroso [19]. Poucos deles têm sido usados nos métodos de template para a síntese de carbono poroso com estrutura de poros ordenada [11, 12, 20]. Muitos carbonos porosos são preparados a partir de surfactantes e copolímeros em bloco caros e não renováveis. A lignina é o segundo material orgânico mais abundante e o polímero aromático mais abundante existente nas espécies vegetais [21]. Na indústria de fabricação de papel, a lignina é convertida em lignosulfonatos durante o processo de polpação e geralmente descartada como resíduo, resultando em sérios problemas ambientais [22]. Os lignosulfonatos são normalmente moléculas pequenas com um anel aromático e grupos contendo oxigênio. Eles normalmente têm peso molecular muito menor do que a lignina e exibem excelente solubilidade em água devido aos grupos contendo oxigênio [23]. Esses méritos fazem dos lignosulfonatos os precursores ideais que podem ser empregados no método de molde para a síntese de carbono poroso de valor agregado com estrutura de poros ordenada.
No presente estudo, usamos o KIT-6 como o modelo rígido por sua boa interconectividade de poros ordenados e controlabilidade sobre o tamanho dos poros para preparar carbono mesoporoso ordenado combinado com a pós-ativação química para criar microporos na estrutura mesoporosa. O lignosulfonato de sódio tem sido empregado como precursor. O carbono poroso ordenado hierárquico conforme preparado (HOPC) foi usado para montar o supercapacitor simétrico que mostra um excelente desempenho de armazenamento de energia.
Métodos
Preparação do KIT-6
O molde de sílica mesoporosa ordenada (KIT-6) foi sintetizado de acordo com a referência [24]. Em um procedimento modificado, 5,53 g de Pluronic P123 (EO 20 PO 70 EO 20 , MW =5800, Aldrich) foi primeiramente dissolvido em 200 g de água desionizada contendo 10,9 g de HCl concentrado (35%) em uma garrafa de vidro de 250 mL. 5,53 g de butanol foram então adicionados à garrafa sob agitação a 35 o C. Após agitação durante 1 h, 11,9 g de TEOS (tetraetil ortossilicato, Aldrich) foram adicionados à solução acima e, em seguida, a mistura foi agitada durante 24 h a 35 ° C. C. A garrafa foi posteriormente envelhecida por mais 24 horas a 100 o C em condições estáticas. O produto sólido foi recolhido por filtração e seco a 100 o C sem lavar. O resíduo orgânico foi removido por extração na mistura de etanol e HCl, seguido de calcinação a 550 o C por 6 h.
Preparação do carbono mesoporoso pedido
O carbono mesoporoso ordenado (OMC) foi preparado usando o KIT-6 como o modelo rígido e lignosulfonato de sódio como fonte de carbono. O modelo de sílica KIT-6 sintetizado acima foi usado para carregar lignosulfonato. Normalmente, 0,6 g de lignosulfonato de sódio adquirido na Lanyi Reagent (Pequim, China) foi dissolvido em 15 mL de água desionizada, seguido pela adição de 0,6 g de molde KIT-6. A mistura foi mantida em agitação por 24 h em temperatura ambiente, seguida por secagem a 70 ° C C. O compósito seco contendo sílica e lignosulfonato de sódio foi usado como o precursor para a carbonização. O processo de carbonização foi conduzido em 900 o C por 2 h em Ar com uma taxa de fluxo de gás de 30 sccm. Após a carbonização, o molde de sílica foi removido por imersão do compósito em solução aquosa de NaOH 2,5 M durante 12 h à temperatura ambiente. Após um tratamento de lavagem com solução diluída de HCl e água desionizada, carbono mesoporoso ordenado (abreviado como OMC) foi obtido e registrado como OMC-900 (o número digital refere-se à temperatura de carbonização). OMC-700, OMC-800 e OMC-1000 referem-se às amostras obtidas carbonizadas em 700 o C, 800 o C e 1000 o C, respectivamente.
Preparação de carbono poroso ordenado hierárquico
Para preparar o carbono poroso ordenado hierárquicamente (abreviado como HOPC), um processo de ativação pós-química foi empregado. Resumidamente, o OMC-900 como preparado foi homogeneamente misturado com ZnCl 2 solução com uma proporção em peso de carbono para ZnCl 2 de 1:1 e seco a 110 o C por 6 h. O tratamento de ativação foi realizado aquecendo os compósitos a 900 o C por 3 h em Ar com uma taxa de fluxo de gás de 30 sccm. Para investigar o efeito da temperatura de carbonização, os modelos KIT-6 impregnados com lignosulfonato de sódio também foram carbonizados a 700 o C e 800 o C, marcado como OMC-700 e OMC-800. Para comparação, lignosulfonato de sódio puro sem qualquer tratamento foi carbonizado diretamente nas mesmas condições e o carbono obtido foi registrado como carbono-lignina.
Caracterização
A morfologia do modelo KIT-6 sintetizado e as amostras de carbono poroso foram caracterizadas usando uma microscopia eletrônica de varredura Hitachi SU8020 (SEM). A estrutura porosa fina foi posteriormente examinada em uma microscopia eletrônica de transmissão (TEM) JEOL 2100F. O padrão de difração de XRD de baixo ângulo foi registrado em um difratômetro de raios-X de pó avançado XD-2 / XD-3. A estrutura química foi investigada usando uma espectroscopia de fotoelétrons de raios-X ESCALAB250Xi (XPS). A caracterização Raman foi conduzida usando uma espectroscopia Raman da HORIBA Science. Os espectros de infravermelho transformado de Fourier (FTIR) foram registrados usando uma espectroscopia NEXUS 670 FTIR. As características porosas do modelo KIT-6 e do carbono poroso foram analisadas por N 2 experimentos de adsorção / dessorção a 77 K usando um ASAP2020 V3.02 H. Micromerítico. A área de superfície específica foi medida de acordo com o método Brunauer-Emmett-Teller (BET), e a distribuição de tamanho de poro foi calculada usando uma densidade não local de poro de fenda modelo de teoria funcional (NLDFT).
Medição eletroquímica
O desempenho eletroquímico das amostras de carbono poroso preparadas foi examinado usando uma configuração de três eletrodos. O HOPC otimizado foi finalmente investigado usando uma configuração de dois eletrodos. O eletrodo de trabalho no sistema de três eletrodos foi fabricado misturando fisicamente o carbono poroso conforme preparado e PVDF que foi dissolvido em solvente NMP antecipadamente com uma proporção em peso de carbono para PVDF de 9:1. A pasta homogênea foi fundida em uma folha de níquel com a área de cobertura de cerca de 1 cm 2 , seguido de secagem a 80 o C por 12 h para remover o solvente residual. No teste de três eletrodos, uma placa de platina (1 cm 2 ) e Ag / AgCl foram usados como contra-eletrodo e eletrodo de referência, respectivamente. O eletrodo de trabalho no sistema de dois eletrodos foi preparado pelo mesmo procedimento ao substituir a folha de níquel por espuma de níquel. Espumas de níquel com a mesma quantidade de carga de materiais de eletrodo ativo foram usadas para montar o supercapacitor simétrico no qual o papel de filtro foi usado como separador. Em ambas as configurações de três eletrodos e dois eletrodos, soluções aquosas 6 M de KOH foram empregadas como eletrólito.
Voltametria cíclica (CV), espectroscopia de impedância eletroquímica (EIS) e carga / descarga galvanostática constante foram conduzidas em um instrumento Gamry referência 3000. A medição de CV na configuração de três eletrodos foi realizada em uma janela de potencial de - 1 a 0 V versus Ag / AgCl, enquanto a janela de potencial no supercapacitor simétrico foi de 0 a 1 V. A caracterização EIS foi conduzida na amplitude AC de 5 mV na faixa de frequência de 1 MHz a 0,01 Hz. A capacitância específica das curvas CV coletadas do teste de três eletrodos foi calculada pela equação C =ʃ eu dt / mV . A capacitância específica derivada da curva CV no teste de dois eletrodos e no teste galvanostático foi determinada via C =4ʃ eu dt / MV e C =v4 I t / MV , respectivamente, onde eu é a corrente de descarga, t é o tempo de descarga, V é a janela de tensão de trabalho, m é a massa do material ativo no eletrodo de trabalho na configuração de três eletrodos, e M é a massa total do material ativo nos dois eletrodos do supercapacitor simétrico. A densidade de energia ( E ) e a densidade de potência ( P ) foram calculados a partir de teste de carga / descarga galvanostática via E = CV 2 / 2 e P = E / t , respectivamente, onde C é a capacitância específica do teste de dois eletrodos e t é a hora da alta.
Resultados e discussão
A amostra HOPC foi sintetizada através de cinco etapas conforme ilustrado na Fig. 1. (a) O modelo de sílica KIT-6 foi preparado por um método modificado na literatura [24]; (b) o lignosulfonato de sódio foi impregnado no molde KIT-6 por imersão do molde de sílica KIT-6 na solução aquosa de lignossulfonato de sódio; (c) o KIT-6 carregado com lignosulfonato de sódio foi carbonizado por 2 h em gás Ar. Para otimizar o processo de carbonização, realizamos a carbonização em 700 o C, 800 o C, 900 o C e 1000 o C. (d) após a carbonização, o modelo de sílica KIT-6 foi então removido em solução quente de NaOH 2,5 M para obter o carbono mesoporoso ordenado (OMC); (e) a amostra de carbono OMC foi ainda quimicamente ativada usando ZnCl 2 em 900 o C por 3 h para preparar HOPC.
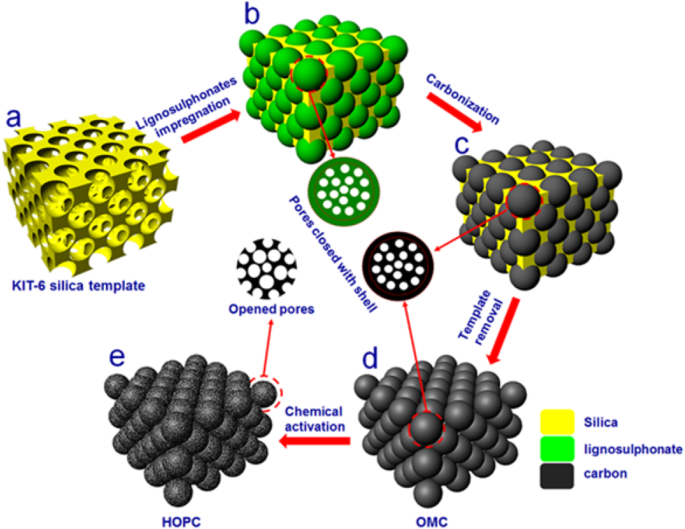
Ilustração dos processos sintéticos de carbono poroso ordenado hierárquico (HOPC) usando o método de molde rígido combinado com pós-ativação química
O modelo de sílica KIT-6 conforme preparado foi analisado em primeiro lugar usando padrão de difração de raios-X de pó de baixo ângulo (XRD) como mostrado na Fig. 2a. A sílica KIT-6 como sintetizada pertence ao cúbico Ia3d com dois picos de difração característicos em 1 o e 1.2 o dos (211) e (220) planos da estrutura mesoporosa cúbica ordenada [24]. Os resultados do N 2 A análise de adsorção / dessorção mostra que o modelo de sílica KIT-6 é constituído pela maioria dos mesoporos e poucos microporos, com boa interconectividade (Fig. 2b). A distribuição do tamanho dos poros está centrada em 2,5 nm e 7,5 nm (Fig. 2c). A área de superfície BET (Brunauer-Emmett-Teller) é de 1481 m 2 g −1 e o volume total do poro é 2,62 cm 3 g −1 . Investigamos ainda mais a micromorfologia e a estrutura de poros do modelo KIT-6 sintetizado por microscopia eletrônica de transmissão (TEM), como mostrado na Fig. 2d. Os pontos brilhantes representam os poros e a área escura das paredes (sílica). A espessura da parede e o tamanho médio dos poros são medidos em 3,1 nm e 6,4 nm, respectivamente. A imagem inserida do padrão FFT na Fig. 2d confirma a estrutura de poros periodicamente ordenada.
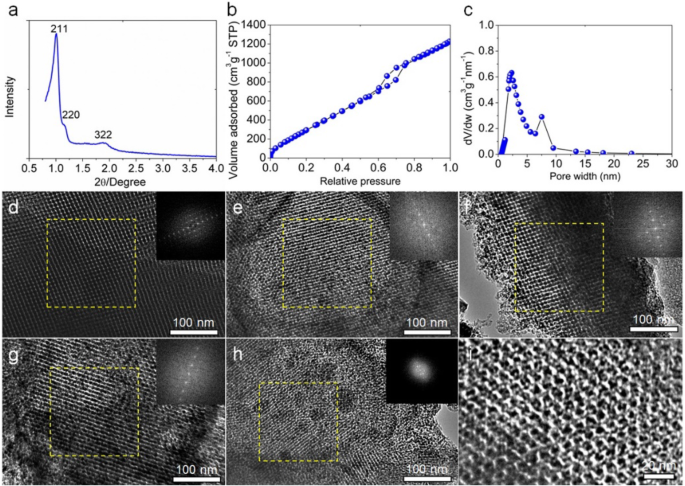
Caracterização do modelo de sílica KIT-6 preparado, a Padrão de XRD de baixo ângulo do gabarito de sílica KIT-6. b N 2 isoterma de adsorção / dessorção do modelo KIT-6. c A distribuição de tamanho de poro correspondente para N 2 calculado usando um modelo NLDFT de poro com fenda. Imagens TEM de ( d ) Sílica KIT-6, as amostras de carbono OMC preparadas em ( e ) 700 o C, ( f ) 800 o C, e ( g ) 900 o C, e a amostra HOPC ( h - i ) As imagens inseridas são os padrões de Transformação Rápida de Fourier correspondentes das áreas selecionadas
As amostras de carbono OMC foram caracterizadas por SEM e TEM. Na Figura S1, as amostras de carbono OMC preparadas em diferentes temperaturas de carbonização exibem a morfologia semelhante a favo de mel com poros ordenados. Além disso, usamos TEM para investigar a estrutura microporosa, conforme mostrado na Fig. 2e-g. As imagens TEM mostram nanodomínios ordenados. As partes escuras são o carbono isolado e as partes brilhantes são poros interconectados. As imagens FFT exibem pontos nítidos e brilhantes para todas as amostras de carbono OMC, confirmando ainda mais a estrutura de poros ordenada. O tamanho do poro é de 2,9 nm, 2,1 nm e 2,4 nm para OMC-700, OMC-800 e OMC-900, respectivamente, o que é muito próximo da espessura da parede do molde de sílica. Em contraste, a amostra preparada a partir da carbonização do lignosulfonato de sódio sem o uso do molde de sílica não apresenta estrutura porosa (Figura S2). Conclui-se que o carbono mesoporoso ordenado é preparado com sucesso usando lignosulfonato de sódio e o modelo de sílica KIT-6 nas temperaturas de carbonização selecionadas.
Os experimentos de adsorção / dessorção de nitrogênio foram conduzidos para investigar as propriedades físicas e químicas das amostras de carbono OMC sintetizadas, conforme mostrado na Figura S3. Todas as curvas isotérmicas têm intermediários semelhantes e o volume adsorvido aumenta na pressão relativa muito baixa e aumenta rapidamente com a pressão relativa, sugerindo a coexistência de microporos e mesoporos com o alto volume de poros para todas as amostras de OMC preparadas. A distribuição do tamanho dos poros para as amostras OMC é centrada em 0,6 nm e 2,3 nm. Aumentamos ainda mais a temperatura de carbonização para 1000 o C e a curva de isotérmica da amostra OMC-1000 mostrada na Figura S4 exibe um perfil semelhante, indicando uma estrutura de poro semelhante. A Figura 3a mostra a área de superfície específica, o volume total do poro, o volume do microporo e o volume do mesoporo em função da temperatura de carbonização. O aumento da área superficial específica está relacionado ao aumento do volume total dos poros. Aumentando ainda mais a temperatura de carbonização para 1000 o C, a área de superfície específica diminui para 1948 m 2 g −1 , com diminuição do volume do microporo e aumento do volume do mesoporo. É sugerido que a temperatura ideal de carbonização é 900 o C. A Tabela S1 resume as propriedades físicas das amostras de carbono OMC preparadas. Verificou-se que a amostra OMC-900 mostra a maior área de superfície específica de 2201 m 2 g −1 e um volume total de poro de 3,74 cm 3 g −1 .
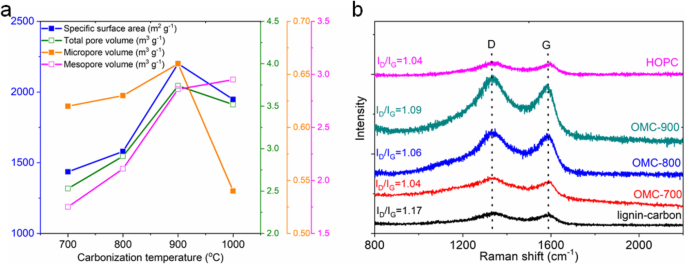
Caracterização do carbono OMC preparado e das amostras HOPC. a A área de superfície específica, o volume total do poro, o volume do microporo e o volume do mesoporo em função da temperatura de carbonização. b Espectros Raman
Portanto, conduzimos a ativação química usando ZnCl 2 como o reagente de ativação usando a amostra OMC-900 para criar ainda mais uma estrutura porosa hierárquica. Como visto a partir da imagem SEM na Figura S5, a rede de poros tridimensional ordenada foi parcialmente destruída após a ativação química para formar numerosas nanopartículas isoladas. A imagem TEM na Fig. 2e mostra claramente poros ordenados e o padrão FFT correspondente exibe pontos brilhantes, indicando a existência de nanodomínios ordenados. A imagem HRTEM na Fig. 2f mostra que microporos são formados nas paredes dos mesoporos após a ativação química. Os resultados de N 2 adsorção / dessorção indicam após a ativação química que a amostra HOPC mostra uma área de superfície específica significativamente aumentada de 2602 m 2 g −1 , com o volume do micropore de 1,03 cm 3 g −1 e mesoporos volume de 3,49 cm 3 g −1 (Tabela S1 e Figura S6a e b).
As propriedades dos lignosulfonatos facilitam a formação de carbono mesoporoso ordenado. A Figura S7 mostra a estrutura molecular representativa do lignosulfonato, e os grupos hidroxila permitem que as moléculas de lignosulfonato ocorram a reação de reticulação [25]. No presente estudo, é proposto que as moléculas de lignosulfonato sejam adsorvidas nas paredes de sílica hidrofílica através dos grupos hidroxila e reticuladas entre si por meio de ligações de hidrogênio para formar redes tridimensionais. Os espectros de FTIR do molde KIT-6, lignosulfonato de sódio e lignosulfonatos impregnados do molde KIT-6 são mostrados na Figura S8. Os picos de lignosulfonato de sódio localizados a 3429 cm −1 , 2950 cm −1 , 1635 cm −1 , 1514 cm −1 , 1041 cm −1 pode ser atribuído ao alongamento O – H, alongamento C – H, alongamento C =O, alongamento C – C e alongamento C – O [26], respectivamente. Os picos do modelo de sílica KIT-6 localizados em 463 cm −1 , 802 cm −1 e 1090 cm −1 são atribuídos ao balanço de Si – O – Si. O pico localizado em 967 cm −1 é devido à vibração de Si – O dos silanóis de superfície [27]. Nos espectros de lignosulfonato-sílica, os picos característicos de lignosulfonato e sílica coexistiram, confirmando a impregnação de lignosulfonato em molde de sílica. Além disso, o pico localizado em 3429 cm −1 no lignosulfonato, a sílica é alargada, indicando a formação de ligações de hidrogênio entre as moléculas de lignosulfonato por meio de uma reação de reticulação. As moléculas de lignosulfonato adsorvidas e orientadas são convertidas em camadas de carbono sólidas durante o processo de carbonização, o que pode induzir vários poros fechados, conforme ilustrado na etapa b e c na Fig. 1. A ativação química ajuda a abrir esses poros fechados para melhorar ainda mais as propriedades físicas .
A caracterização Raman foi usada para investigar o grau de grafite das amostras de carbono preparadas e os resultados são mostrados na Fig. 3b. Todos os espectros Raman exibem banda D e banda G características localizadas a 1340 cm −1 e 1590 cm −1 , respectivamente. A relação de intensidade da banda D (o carbono desordenado) e da banda G (carbono ordenado) para as amostras OMC e a amostra HOPC é em torno de 1,06, inferior a 1,17 da amostra de carbono preparada pela carbonização do lignosulfonato sem o uso de sílica modelo. Este resultado indica que as amostras de carbono OMC têm um grau de grafite mais alto do que a amostra de carbono da carbonização direta do lignosulfonato. A razão é provavelmente atribuída à reação de reticulação acima mencionada entre as moléculas de lignosulfonato que ajuda na orientação dos anéis aromáticos. O resultado da análise XPS na Figura S9 mostra que todas as amostras contêm principalmente carbono e oxigênio. Não há sinal detectável de impureza nos produtos finais de carbono. A decomposição do lignosulfonato de sódio pode dar origem à formação de CO 2 e Na 2 CO 3 [28], que pode ser completamente removido durante o tratamento de lavagem subsequente com água deionizada. O nível do núcleo C1s pode ser deconvoluído em quatro componentes para todas as amostras de carbono preparadas. Ou seja, C – O (286,7 eV), C =O (288,0 eV) [29], o sp 2 carbono (284,8 eV, carbono ordenado) e o sp 3 carbono (285,4 eV, carbono desordenado) [30].
O desempenho eletroquímico das amostras de carvão OMC preparadas e da amostra de HOPC ativado foram avaliados por meio de uma configuração de três eletrodos em eletrólito aquoso 6 M KOH. A amostra de carbono da carbonização direta de lignosulfonato mostra desempenho insignificante de armazenamento de energia (Figura S10). As amostras de carbono OMC exibem perfis CV retangulares indicando o desempenho eletroquímico aprimorado (Figura S11 e Figura 4a). A 2 mV s −1 , a capacitância específica é 59 F g −1 , 93 F g −1 , 130 F g −1 , e 120 F g −1 para OMC-700, OMC-800, OMC-900 e OMC-1000 (Fig. 4b). O eletrodo OMC-900 apresenta o melhor desempenho eletroquímico entre todas as amostras de carbono OMC. Após a ativação química, a capacitância específica aumenta ainda mais para 243 F g −1 para a amostra HOPC, quase duas vezes maior do que a amostra OMC-900 antes da ativação. A capacitância específica de HOPC neste estudo é muito maior do que a do carbono derivado de fungos (196 F g −1 a 5 mV s −1 ) [31], e também superior ao do carbono mesoporoso à base de aerogel de grafeno preparado a partir de um molde de sílica dura (226 F g −1 a 1 mV s −1 ), que diminui para 83 F g −1 a 100 mV s −1 [32]. Para o carbono derivado de fungos, a capacitância específica diminui para 90 F g −1 a 100 mV s −1 . No entanto, a capacitância específica de HOPC ainda é tão alta quanto 128 F g −1 na mesma taxa de varredura.
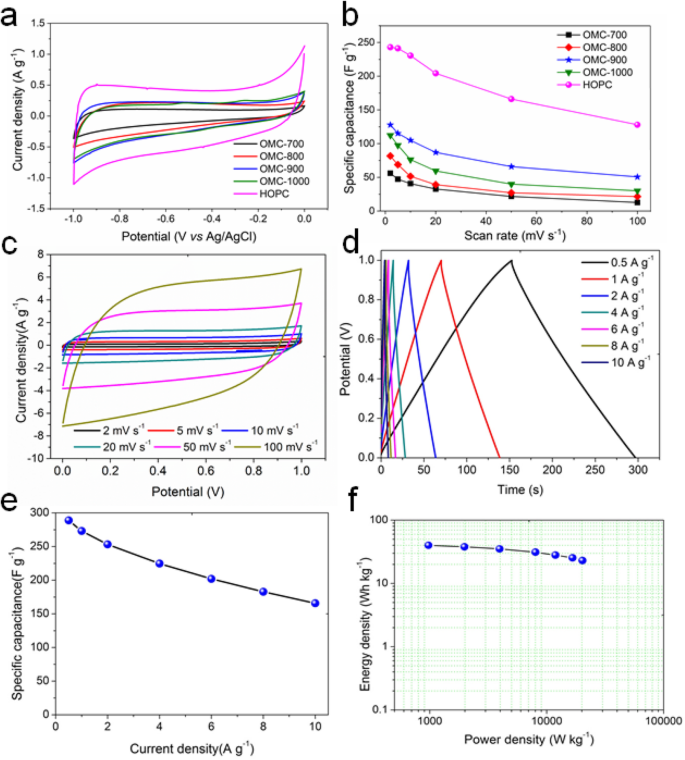
a Perfis de voltametria cíclica (CV) dos eletrodos OMC-700, OMC-800, OMC-900, OMC-1000 e HOPC a uma taxa de varredura de 2 mV s −1 usando a configuração de três eletrodos e b capacitância específica correspondente. c Perfis de CV do eletrodo HOPC no supercapacitor simétrico de dois eletrodos em taxas de varredura que variam de 2 mV s −1 a 100 mV s −1 em eletrólito aquoso 6 M KOH. d Curvas de carga-descarga em diferentes densidades de corrente de 0,5 A g −1 a 10 A g −1 . e Capacitância específica calculada a partir das curvas de descarga do teste de carga-descarga. f Gráficos de Ragone mostrando a densidade de energia em função da densidade de potência
As medições de impedância foram realizadas para investigar a condutividade das amostras. A Figura S12 revela os espectros de impedância de Nyquist na faixa de frequência de 1 MHz – 0,01 Hz, e o circuito equivalente correspondente que consiste na resistência em série equivalente ( R s ), resistência à transferência de carga ( R ct ) e a capacitância eletroquímica de camada dupla. A resistência de série equivalente R s é 0,7 Ω cm −2 para todos os eletrodos, indicando a alta condutividade elétrica das amostras e a alta qualidade dos eletrodos. Os gráficos de Nyquist indicam que o eletrodo HOPC mostra a resistência de transferência de carga mais baixa de 5 Ω.
A energia entregável e a densidade de potência estão altamente relacionadas com a capacitância dependente da frequência [33, 34], que pode ser expressa da seguinte forma
$$ C =\ frac {1} {jwZ} =\ frac {- {Z} _ {\ mathrm {imagem}}} {W {\ esquerda | Z \ direita |} ^ 2} -j \ frac {- { Z} _ {\ mathrm {real}}} {W {\ left | Z \ right |} ^ 2} ={C} _ {\ mathrm {real}} - j {C} _ {\ mathrm {imagem}} $$
onde C e Z são a capacitância e a resistência, respectivamente. Z real e Z imagem referem-se às partes reais e imaginárias de Z . C real é a parte real da capacitância que representa a capacitância distribuível dos materiais do eletrodo, e C imagem é a capacitância imaginária relacionada à perda de resistividade irreversível no dispositivo. A Figura S13a mostra que a amostra HOPC teve a resposta mais rápida. A frequência ƒ é a frequência de caracteres em que C imagem atinge o máximo e t =1 / ƒ é a constante de tempo do supercapacitor. Ambos f e t são a capacidade de taxa característica. Supercapacitores de alta densidade de potência geralmente têm alta frequência de caracteres ƒ e pequeno t . A Figura S13b mostra os gráficos de C imagem em função da frequência. A frequência de caractere da amostra OMC-700, OMC-800, OMC-900, OMC-1000 e HOPC é 0,01 Hz, 0,1 Hz, 0,01 Hz, 0,01 Hz e 0,5 Hz, e a constante de tempo correspondente é 100 s, 10 s, 100 s, 100 s e 2 s. A amostra HOPC mostra a frequência de caracteres mais alta e a constante de tempo mais baixa, indicando a resposta mais rápida à saída de energia.
Foi demonstrado que HOPC exibe alto desempenho eletroquímico. No entanto, para aplicações práticas, o teste de configuração de três eletrodos não pode revelar a capacidade real de armazenamento de energia [33, 35]. Portanto, usamos amostra HOPC para preparar eletrodos para montar supercapacitores simétricos. A Figura 4c ilustra as curvas CV do eletrodo HOPC. Os perfis CV apresentam formato quase retangular com boa simetria em todas as taxas de varredura de 2 mV s −1 a 100 mV s −1 , indicando as boas propriedades eletroquímicas e estabilidade de taxa do eletrodo HOPC. As medições de carga-descarga galvanostática em densidades de corrente constantes também foram realizadas no supercapacitor simétrico montado e os resultados são mostrados na Fig. 4d. Os perfis de tensão linear versus tempo durante o processo de carga e descarga mostram uma forma de triângulo ideal com boa simetria, representando a excelente capacidade de armazenamento de energia do eletrodo HOPC. Quando a densidade da corrente era 0,5 A g −1 , o tempo de descarga é tão longo quanto 150 s, o que corresponde à capacitância específica de cerca de 289 F g −1 . A capacitância específica de HOPC de lignosulfonato em 10 A g −1 ainda é tão alto quanto 166 F g −1 , conforme mostrado na Fig. 4e. O desempenho do HOPC neste estudo é melhor do que os valores de amostras de carbono em literaturas [3, 36,37,38,39].
A alta capacitância específica de HOPC contribui para a baixa resistência ôhmica e resistência de transferência de carga, que é cerca de 0,6 Ω cm −1 e 2,4 Ω cm −1 , respectivamente, conforme mostrado na Figura S14. O ângulo de fase do supercapacitor simétrico na frequência mais baixa de 0,01 Hz é cerca de 81,7 o (Figura S15), que está muito próximo do valor do supercapacitor ideal (90 o ) A frequência do caractere é de cerca de 0,2 Hz, correspondendo à constante de tempo de 5 s. Isso significa que o eletrodo HOPC tem uma boa capacidade de entrega de energia. A capacitância distribuível é de até 290 mF (Figura S16). A Figura 4f ilustra o gráfico de Ragone do supercapacitor simétrico. A densidade de energia está na faixa de 40 Wh kg −1 a 23 Wh kg −1 com a densidade de potência de cerca de 0,9 kW kg −1 a 20 kW kg −1 .
A alta capacitância específica e densidade de energia de HOPC podem contribuir para a estrutura de poros otimizada. A amostra HOPC contém alto volume de poros de ambos os microporos e mesoporos. Como demonstrado na literatura anterior por análise de correlação [40, 41], os microporos são altamente relacionados ao armazenamento de energia e os mesoporos são altamente relacionados à retenção de capacitância, uma vez que os mesoporos são os principais responsáveis pelo transporte de íons. Conclui-se também que os mesoporos contribuem para o armazenamento de carga. Mantenha a instrução acima em mente, nós empregamos dedicadamente o método de modelo rígido e ativação química para preparar a amostra HOPC. Os presentes resultados não apenas demonstram mais as conclusões acima, mas também mostram o projeto para a preparação de materiais de armazenamento de energia de alto desempenho. A fim de medir a ciclabilidade, o supercapacitor simétrico de usar HOPC como o material do eletrodo é repetidamente carregado e descarregado a 2 A g −1 para 3000 ciclos (Figura S17). Verificou-se que após 3.000 ciclos, a capacitância específica é 218 F g −1 com uma ligeira diminuição de 253 F g −1 inicial com retenção de capacitância de 86,2%. A capacitância específica de nossa amostra HOPC do sistema de dois eletrodos é maior e comparável após 3000 ciclos com os valores relatados na Tabela S2. Portanto, o presente estudo fornece uma rota potencial para o desenvolvimento de materiais ativos com eletrodo supercapacitor de alto desempenho a partir de resíduos industriais.
Conclusão
Neste estudo, preparamos com sucesso materiais de carbono mesoporoso ordenados usando lignosulfonato de biorresíduos como fonte de carbono usando a técnica de fundição de molde com base no modelo KIT-6. Durante o processo de fundição do molde, o lignosulfonato pode ser facilmente fundido nos poros do KIT-6. The crosslinking reaction of lignosulphonate molecules not only increases the pore volume, but also bridges the aromatic rings to promote the graphitization. The as-synthesized ordered mesoporous carbons exhibit high electrical conductivity, high-specific surface area, and pore volume, which are highly dependent on the carbonization temperature. The results of Raman analysis and N2 adsorption/desorption experiments show that the OMC-900 sample has the best physical properties. The pore structure of OMC-900 was further optimized through ZnCl2 chemical activation to prepare HOPC. The specific capacitance of HOPC in the symmetric supercapacitor was about 289 F g −1 with the energy density as high as 40 Wh kg −1 . The present study indicates lignosulphonate is very suitable to prepare hierarchical ordered porous carbon at low cost with high-performance supercapacitors.
Disponibilidade de dados e materiais
All data generated or analyzed in this study are included in the manuscript and the supplementary information files. All the materials are available from the corresponding author on request.
Abreviações
- HOPC:
-
Hierarchical ordered porous carbon
- KIT-6:
-
The ordered mesoporous silica template
- OMC:
-
The ordered mesoporous carbon
- NMP:
-
N-methyl pyrrolidone
- PVDF:
-
Fluoreto de polivinilideno
- CV:
-
Voltametria cíclica
- EIS:
-
Espectroscopia de impedância eletroquímica
- AC:
-
Alternating current
Nanomateriais
- Compostos de grafeno e polímero para aplicações de supercapacitor:uma revisão
- Fibras de carbono ativado com nanoestrutura hierárquica derivada de luvas de algodão como eletrodos de alto desempenho para supercondensadores
- Síntese fácil de nanofios de prata com diferentes proporções de aspecto e usados como eletrodos transparentes flexíveis de alto desempenho
- Nanoesferas de carbono monodispersas com estrutura porosa hierárquica como material de eletrodo para supercapacitor
- Microesferas de carbono magnético como um adsorvente reutilizável para remoção de sulfonamida da água
- Uma abordagem simples para sintetizar pontos quânticos de carbono fluorescentes de águas residuais de Tofu
- Avaliação de estruturas de grafeno / WO3 e grafeno / CeO x como eletrodos para aplicações de supercapacitor
- Composto de aerogel de carbono ativado revestido com polianilina para bateria de lítio-enxofre de alto desempenho
- Síntese e desempenho do supercapacitor de compostos de carbono mesoporosos ordenados com polianilina / nitrogênio dopado
- Microarranjos mesoporosos de VO2 bidimensional para supercapacitor de alto desempenho



