Uma nova preparação hidrotérmica de uma etapa de catalisadores de oxidação de diesel Ru / SnxTi1-xO2 e seu desempenho em baixa temperatura
Resumo
O rutilo Sn x Ti 1− x O 2 ( x =0, 0,33, 0,5, 0,67, 1) solução sólida foi sintetizada por um método hidrotérmico de uma etapa, em que titanato de tetrabutila e cloreto de estanho (IV) penta-hidratado foram usados como matérias-primas. Uma série de Ru / Sn x Ti 1− x O 2 foram então preparados pelo processo de impregnação em RuCl 3 para investigar o desempenho e a estabilidade de CO e C 3 H 8 oxidação. Esses catalisadores foram caracterizados por meio de XRD, N 2 adsorção-dessorção, FT-IR, TEM, XPS, H 2 -TPR e O 2 Técnicas -TPD. O efeito da razão molar Sn / Ti e da condição hidrotérmica no desempenho oxidado catalítico de baixa temperatura e na estabilidade de Ru / Sn x Ti 1− x O 2 foram investigados. Os resultados indicaram que Ru / Sn 0,67 Ti 0,33 O 2 o catalisador apresentou excelente atividade e estabilidade em baixas temperaturas. A conversão de CO atingiu 50% a 180 ° C e 90% a 240 ° C. Além disso, o C 3 H 8 a conversão atingiu 50% a 320 ° C, a conversão completa de C 3 H 8 realizada a 500 ° C, e nenhuma desativação ocorre após 12 h de reação catalítica. A excelente atividade em baixa temperatura e estabilidade do Ru / Sn 0,67 Ti 0,33 O 2 foram atribuídos aos seguintes fatores. Em primeiro lugar, os resultados de XRD mostraram que Sn 4+ foi introduzido com sucesso na rede de TiO 2 para substituir Ti 4+ formando uma solução sólida homogênea (contendo –Sn 4+ –O – Ti 4+ - espécie), que era consistente com TEM e N 2 resultados de adsorção-dessorção. A introdução de Sn pode suprimir o crescimento do cristal de anatase e promover a formação da fase rutilo, e esta transição de fase foi útil para melhorar a atividade de baixa temperatura dos catalisadores. Em segundo lugar, as imagens TEM mostraram que nanopartículas de Ru ultrafinas (~ 5 nm) foram dispersas em Sn 0,67 Ti 0,33 O 2 suporte, sugerindo que a formação de Sn x Ti 1− x O 2 solução sólida foi benéfica para a dispersão de partículas de Ru.
Histórico
Os motores a diesel são amplamente aplicados na área de transporte, mineração e máquinas de engenharia devido a essas vantagens de baixo consumo de combustível, alta eficiência térmica e boa estabilidade [1]. No entanto, monóxido de carbono (CO), hidrocarbonetos não queimados (HCs), vários óxidos de nitrogênio (NO x ), e o material particulado (PM) no escapamento de veículos a diesel tem causado uma séria ameaça ao meio ambiente ecológico e à saúde humana [2, 3]. Além disso, leis e regulamentos ambientais rigorosos conduziram a avanços recentes nas tecnologias de controle de emissão de diesel. Um sistema integrado de pós-tratamento de exaustão consistindo de catalisador de oxidação de diesel (DOC), redução catalítica seletiva (SCR) e filtro de partículas de diesel catalisado (DPF) tem sido amplamente utilizado para purificar exaustores de diesel. As funções do DOC no sistema de pós-tratamento são a conversão de CO, HCs e NO em CO 2 , H 2 O, e NÃO 2 , o NÃO 2 sendo usado como matéria-prima para subsequente de-NO x reação para promover a reação SCR. Além disso, também pode oxidar a fração orgânica solúvel (SOF) para diminuir as emissões de PM. A emissão excessiva de HCs será causada devido à combustão incompleta dos HCs durante a partida a frio dos veículos a diesel. Portanto, os catalisadores precisam inflamar rapidamente em baixas temperaturas [4]. Atualmente, catalisadores de metal nobre (como Pt, Pd e Rh) suportados em materiais ou óxidos de carbono (como TiO 2 , Al 2 O 3 , CeO 2 , e ZrO 2 ) são catalisadores de oxidação de diesel comercializados com bom desempenho para oxidação catalítica de CO, NO e HCs. No entanto, existem desvantagens para os catalisadores comercializados, como baixa estabilidade térmica, forte autoinibição por CO e alto custo [5].
Ru e RuO x os catalisadores são amplamente aplicados na oxidação de CO [6], metano [7] e clorobenzeno [8]. É importante ressaltar que os catalisadores Ru têm excelente atividade em baixa temperatura e resistência a venenos [8,9,10,11]. Mas Ru e RuO x são facilmente sinterizados, resultando em diminuições de exposição dos locais ativos [12]. Portanto, os catalisadores Ru devem ser suportados em um carreador para evitar sua sinterização e melhorar a atividade catalítica.
TiO 2 tem sido amplamente utilizado para purificar escapamentos de diesel. RuO x e fase rutilo TiO 2 têm uma constante de rede semelhante, e o rutilo TiO 2 em Ru / TiO 2 catalisadores desempenham um papel importante na estabilização de RuO x partículas durante o processo de calcinação em comparação com RuO suportado por anatase x catalisadores. Portanto, RuO x pode ser altamente disperso na superfície do TiO 2 . Além disso, há um efeito sinérgico entre RuO x e TiO 2 , que é benéfico para melhorar a capacidade redox de Ru / TiO 2 [13,14,15,16,17,18]. A fim de melhorar ainda mais a estabilidade térmica, a dispersão dos componentes ativos e a transformação da fase anatase em rutilo, muitos estudos introduziram Sn 4+ em TiO 2 para formar Sn x Ti 1− x O 2 solução sólida. Huang et al. [16] descobriram que a introdução do Sn 4+ em TiO 2 a rede pode melhorar a estabilidade do CuO / Ti x Sn 1− x O 2 catalisadores e dispersão de CuO. Bai et al. [17] indicou Sn 4+ melhorou significativamente a estabilidade térmica do TiO 2 . Mehraz et al. [18] encontrado doping Sn 4+ promoveu a transição de fase do TiO 2 de anatásio a rutilo.
Pesquisas anteriores se concentraram na preparação de catalisadores de oxidação de diesel pelo método de co-precipitação, método sol-gel e reação em fase sólida [5, 6, 15, 19, 20]. Yang et al. [19] preparou o Pt / TiO 2 catalisadores através do método de co-precipitação e descobriram que a conversão de CO e C 3 H 6 atinge apenas 50% a 232 ° C. Li et al. [15] TiO sintetizado 2 –SnO 2 nanocompósito pelo método sol-gel e sugeriu que a conversão de TiO 2 –SnO 2 para CO foi de 90% a 260 ° C. Sharif et al. [6] preparou Ru / [Ca 24 Al 28 O 64 ] 4+ (O 2− ) 2 através da reação de estado sólido e mostrou que a conversão de Ru / [Ca 24 Al 28 O 64 ] 4+ (O 2− ) 2 para CO foi de apenas 82% a 240 ° C devido à menor dispersão de Ru. Portanto, existem desafios críticos que permanecem na atividade de baixa temperatura dos catalisadores de oxidação do diesel e muitos esforços ainda são necessários para remover CO e HCs causados na partida a frio do diesel. Além disso, a pesquisa atual [8, 16, 19, 21, 22] está focada principalmente na preparação de catalisadores DOC por métodos de co-precipitação e sol-gel, que tem um tamanho de grão pequeno, mas as amostras têm cristalinidade pobre e múltiplas fases do cristal; além disso, é necessário o subsequente processo de tratamento térmico da mistura pelo método de co-precipitação. O tratamento hidrotérmico é adotado no processo de preparação para evitar os processos de calcinação tradicionalmente seguidos e a formação de agregação dura dos catalisadores, o que poderia melhorar a atividade catalítica em baixa temperatura [23]. No entanto, há uma falta de estudos sistemáticos e abrangentes sobre o método hidrotérmico de uma etapa [24, 25].
Portanto, relatamos que RuO x partículas com suporte no Sn 4+ -modificado TiO 2 pelo método hidrotérmico de uma etapa foram excelentes catalisadores de oxidação de CO e HC com atividade e estabilidade em baixa temperatura promissoras. Uma série de Sn x Ti 1− x O 2 ( x =0, 0,33, 0,5, 0,67, 1) solução sólida foram preparadas pelo método hidrotérmico de uma etapa. Ru / Sn x Ti 1− x O 2 foram então preparados por impregnação do Sn x Ti 1− x O 2 com RuCl 3 para oxidar CO e C 3 H 8 . O efeito das temperaturas hidrotérmicas, do tempo hidrotérmico, das temperaturas de calcinação e das razões molares de Sn / Ti de Ru / Sn x Ti 1− x O 2 catalisadores foram investigados a fim de melhorar a atividade e estabilidade em baixa temperatura.
Método
Materiais
Cloreto de estanho (IV) pentahidratado (SnCl 4 · 5H 2 O) foi adquirido da Guangdong Kehua Stock Corporation, titanato de tetrabutila (C 16 H 36 O 4 Ti) foi adquirido da Tianjin Kemiou Chemical Reagent Factory e cloreto de Rutênio (III) anidro, RuCl 3 , (37% Ru p / p) foi adquirido da Aladdin.
Preparação de catalisadores
Sn x Ti 1− x O 2 solução sólida foi preparada pelo método hidrotérmico de uma etapa. As quantidades certas de SnCl 4 · 5H 2 O e C 16 H 36 O 4 Ti foram dissolvidos em 200 mL de água desionizada e 10 mL de etanol anidro, respectivamente; então, C 16 H 36 O 4 Solução de etanol de Ti e SnCl 4 · 5H 2 A solução aquosa foi misturada enquanto se agitava à temperatura ambiente durante 0,5 h. A mistura homogênea foi colocada em uma autoclave de 250 mL a 180 ° C por 24 h. Depois disso, a solução misturada foi centrifugada lavando com água desionizada e etanol várias vezes até que não houvesse resíduos de Cl - e depois foi seca a 80 ° C durante a noite no forno. Posteriormente, produtos sólidos amarelos claros foram obtidos, denominados Sn x Ti 1− x O 2 . SnO 2 e TiO 2 foram obtidos por métodos de preparação semelhantes, respectivamente.
Ru / Sn x Ti 1− x O 2 catalisadores foram preparados por impregnação de Sn x Ti 1− x O 2 com uma solução aquosa incluindo 1,0% em peso de RuCl 3 . Essas amostras foram agitadas por ultrassom por 2 he secas a 80 ° C por 12 h, e foram então calcinadas a 400 ° C por 3 h (a taxa de aquecimento é de 3 ° C / min). O pó obtido foi denominado Ru / Sn x Ti 1− x O 2 .
Desempenho catalítico
As atividades dos catalisadores foram avaliadas em um reator de quartzo de leito fixo com aquecedor elétrico. Os gases reagentes simulados continham uma mistura de 3000 ppm CO, 600 ppm C 3 H 8 , 600 ppm NÃO, 50 ppm SO 2 , 7% O 2 , e N 2 equilíbrio a uma velocidade espacial do gás de 60.000 mL g −1 h −1 . A taxa de fluxo de gás foi regulada por controladores de fluxo de massa. A temperatura do leito fixo foi testada por um termopar K de 0,5 mm que foi colocado no meio dos canais centrais. A saída CO e C 3 H 8 foram medidos por um analisador de gases de combustão KM9106 (Kane International Limited, Grã-Bretanha). A conversão ( X ) de CO e C 3 H 8 foi calculado usando a seguinte equação:
$$ X =\ frac {c _ {\ mathrm {in}} - {c} _ {\ mathrm {out}}} {c _ {\ mathrm {in}}} \ times 100 \% $$
onde c em é a concentração inicial de CO ou C 3 H 8 e c fora é o instantâneo de CO ou C 3 H 8 na temperatura de reação; T 50 é denotado como o índice de atividade catalítica de baixa temperatura.
Caracterização do catalisador
Os padrões de difração de raios-X (XRD) das amostras foram realizados por difração de raios-X de potência em um difratômetro BRUKER D8 ADVANCE equipado com uma câmara de alta temperatura usando radiação Cu Kα (0,15418 nm). O tubo de raios X foi operado com uma fonte de alimentação de 40 kV × 40 mA.
As áreas de superfície Brunauer-Emmett-Teller (BET) foram testadas por adsorção de nitrogênio a 77 K em um aparelho de adsorção Micromeritics ASAP2020; a área superficial específica e a distribuição dos poros foram calculadas pelos métodos BET e BJH, respectivamente. Estas amostras foram desgaseificadas sob vácuo a 300 ° C por 4 h antes de cada análise.
A espectroscopia de infravermelho com transformada de Fourier (FT-IR) foi examinada usando um espectrômetro Nicolet is5 a uma resolução espectral de 4,0 cm −1 . Os pós foram prensados em um wafer autossustentável (cerca de 15 mg, 12 mm de diâmetro). O wafer foi pré-tratado com N 2 a 300 ° C durante 1 h. Após resfriamento à temperatura ambiente, o espectro das amostras foi registrado.
As imagens de microscopia eletrônica de transmissão (TEM) dessas amostras foram obtidas por um instrumento Tecnai G2 F20 a uma tensão de aceleração de 200 kV. As amostras foram moídas, dispersas em etanol e depositadas em grades de cobre revestidas de carbono antes da observação.
A análise da espectroscopia de fotoelétrons de raios-X (XPS) foi realizada em um espectrômetro ESCALAB250Xi, usando radiação monocromática Al Kα (1486,6 eV) a uma potência de aceleração de 15 kW. Os espectros de amostra obtidos foram corrigidos usando C1s (284,6 eV) como o padrão de referência interno.
H 2 -redução programada de temperatura (H 2 -TPR) experimentos foram realizados em um reator de quartzo conectado a um detector de condutividade térmica (TCD) com H 2 (6,9% vol.%) - mistura de Ar (30 mL / min) como redutor. Antes da reação, a amostra (50 mg) foi pré-tratada em N 2 a 300 ° C por 1 h e, em seguida, resfriado à temperatura ambiente. O TPR começou a partir da temperatura ambiente até a temperatura alvo a uma taxa de 10 ° C / min.
Dessorção de oxigênio programada por temperatura (O 2 -TPD) os experimentos foram realizados usando o mesmo dispositivo que H 2 -TPR. O catalisador gasto (50 mg) foi pré-tratado a 300 ° C durante 1 h sob fluxo de Ar a 30 mL / min. Então, a adsorção de oxigênio foi conduzida sob um O 2 –Mistura de Ar (20% O 2 vol. %) a 500 ° C por 0,5 h. Após arrefecimento até à temperatura ambiente, o sistema foi purgado em Ar (30 mL / min) durante 1 h. Após o tratamento, a temperatura foi elevada até a temperatura alvo (10 ° C / min).
A espectroscopia de infravermelho (IR) in situ de adsorção de CO foi coletada em um espectrômetro Nicolet 5700 FT-IR a uma resolução espectral de 4,0 cm −1 . A adsorção de CO foi realizada expondo uma pastilha autossustentada de catalisador (cerca de 15 mg) e montada em uma câmara de ambiente comercial controlado (HTC-3). As amostras foram expostas a um fluxo controlado de CO-Ar (10% de CO por volume) a uma taxa de 5,0 mL / min por 40 min. Os espectros foram registrados em várias temperaturas alvo a uma taxa de 10 ° C / min desde a temperatura ambiente até 300 ° C.
Resultados e discussão
Atividade catalítica e estabilidade
A Figura 1 mostra as atividades catalíticas de CO e C 3 H 8 oxidação no Ru / Sn x Ti 1− x O 2 catalisadores nas condições ideais de preparação (Fig. S1, S2 e S3) de temperatura hidrotérmica a 180 ° C, tempo hidrotérmico a 24 h e temperatura de calcinação a 400 ° C. Pode ser visto que desempenhos catalíticos de Ru / Sn x Ti 1− x O 2 os catalisadores aumentaram primeiro e depois tenderam a se estabilizar com o aumento da temperatura de reação. Quando a razão molar de Sn / Ti é 2/1, o T 50 de Ru / Sn 0,67 Ti 0,33 O 2 para oxidar CO e C 3 H 8 é 180 ° C e 320 ° C, respectivamente, que é a temperatura de reação mais baixa do que outras razões molares Sn / Ti. A conversão de CO atingiu 90% a 240 ° C, e a conversão completa de C 3 H 8 poderia ser alcançado a 500 ° C no Ru / Sn 0,67 Ti 0,33 O 2 catalisador. O desempenho catalítico para cada amostra foi normalizado em relação aos átomos de Ru na superfície e expresso em termos de frequência de rotação (TOF), conforme mostrado na Fig. 2. O valor TOF para Ru / Sn 0,67 Ti 0,33 O 2 foi a mais alta entre todas as amostras em qualquer temperatura de reação. É atribuído ao Ru altamente disperso na superfície de Sn 0,67 Ti 0,33 O 2 , e o componente ativo Ru tem uma forte interação com o portador Sn 0,67 Ti 0,33 O 2 [22, 26]. Sharif et al. [6] relatou que a conversão de Ru / [Ca 24 Al 28 O 64 ] 4+ (O 2− ) 2 para CO foi de apenas 82% a 240 ° C. Murayama et al. [27] relatou que a conversão de Au / Nb 2 O 5 e Au / SiO 2 para CO foi de 55% e 38%, respectivamente, a 250 ° C. Comparado com outras literaturas [27, 28], quando a razão molar de Sn / Ti é 2/1, maior conversão de CO pode ser alcançada em temperatura mais baixa neste estudo. Okal et al. [29] relatou que o T 50 de CH 4 oxidado por Ru / ZnAl 2 O 4 os catalisadores eram 480, 500 e 540 ° C, quando a carga de Ru era de 0,5% em peso, 1,0% em peso e 4,5% em peso, respectivamente. Wilburn et al. [30] relatou que o T 50 de CH 4 oxidação acima de 0,3Pd – 0,7Pt / γ – Al 2 O 3 o catalisador era 360 ° C. As atividades catalíticas de diferentes catalisadores para CO e C 3 H 8 a oxidação é mostrada na Tabela S1 e na Tabela S2. Transformação completa de C 3 H 8 pode ser alcançado em uma temperatura mais baixa neste trabalho. A razão molar ótima de Sn / Ti é 2/1, que é consistente com a atividade de CO. A partir da análise acima, pode-se concluir que a conversão de CO e C 3 H 8 é muito afetado pela razão molar de Sn / Ti. Quando a razão molar de Sn / Ti é 2/1, o T 50 de Ru / Sn 0,67 Ti 0,33 O 2 para CO e C 3 H 8 é 180 ° C e 320 ° C, respectivamente. Quando a temperatura da reação é 240 ° C, a conversão de CO pode chegar a 90% e a conversão completa de C 3 H 8 pode ser alcançado quando a temperatura de reação é de 500 ° C.
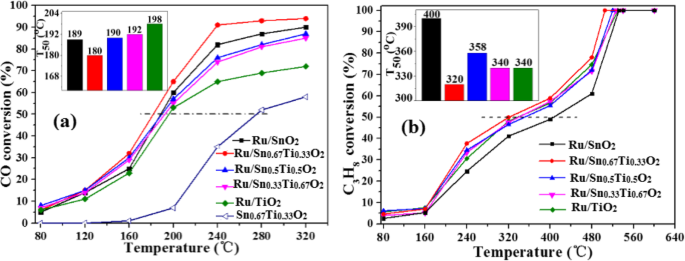
Efeito de diferentes razões molares Sn / Ti em Ru / Sn x Ti 1− x O 2 oxidação catalítica de CO ( a ) e C 3 H 8 ( b )
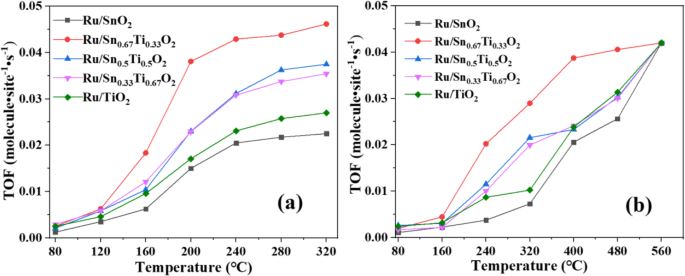
TOF de temperatura de reação para CO ( a ) e C 3 H 8 ( b ) oxidação sobre vários catalisadores
A estabilidade de CO e C 3 H 8 foi investigado na Fig. 3, sob temperatura hidrotérmica de 180 ° C, tempo hidrotérmico de 24 h e temperatura de calcinação de 400 ° C (Fig. S1, S2 e S3). A conversão de CO atingiu 90% a 240 ° C, e a conversão completa de C 3 H 8 poderia ser alcançado a 500 ° C. Curiosamente, Ru / Sn 0,67 Ti 0,33 O 2 o catalisador é basicamente inativado após uma reação catalítica de 12 h; no entanto, a atividade de Ru / TiO 2 e Ru / SnO 2 os catalisadores diminuíram ligeiramente com o aumento do tempo quando oxidaram o CO. O fenômeno indica que a formação de Sn x Ti 1− x O 2 a solução sólida pode não apenas melhorar a atividade dos catalisadores, mas também aumentar a estabilidade. É atribuído que Ru está altamente disperso na superfície de Sn 0,67 Ti 0,33 O 2 ; há uma forte interação entre o componente ativo Ru e o portador Sn 0,67 Ti 0,33 O 2 [26].
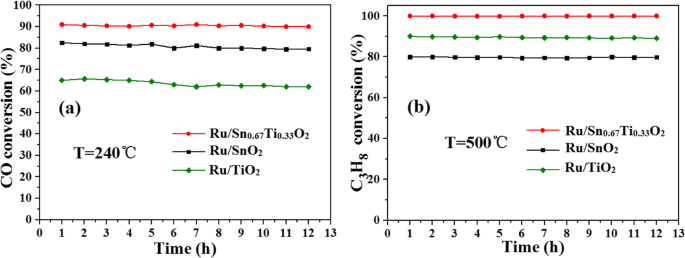
A estabilidade de Ru / Sn x Ti 1− x O 2 CO catalítico ( a ) e C 3 H 8 ( b )
Caracterização do catalisador
Propriedades de textura de Sn x Ti 1− x O 2 Suporta e Ru / Sn x Ti 1− x O 2 Catalisadores
A Figura 4 mostra os padrões de XRD de ambos Sn x Ti 1− x O 2 solução sólida e Ru / Sn x Ti 1− x O 2 catalisadores. Picos típicos da estrutura anatase são observados no TiO 2 (25,78 °) e Ru / TiO 2 (25,67 °) amostras com tamanhos de grão de cerca de 4 nm e 5,5 nm (Tabela 1), respectivamente. Uma transição de fase de anatásio para rutilo apareceu com a introdução de Sn. Os picos de difração de Ru não são observados, indicando que Ru está altamente disperso em Sn x Ti 1− x O 2 superfície ou além da limitação de detecção de XRD [31]. Além disso, os picos de difração de Sn x Ti 1− x O 2 e Ru / Sn x Ti 1− x O 2 mover gradualmente para ângulos mais baixos com o aumento do conteúdo de Sn, sugerindo que o espaçamento interplanar d aumenta de acordo com a equação de Bragg, 2 d sin θ = nλ . Isso é consistente com o aumento nos parâmetros da rede tetragonal ( a e c ) na Tabela 1, que é atribuída à substituição de raio iônico maior Sn 4+ (0,071 nm) para Ti 4+ (0,068 nm). Os resultados sugerem o Sn 4+ foi dopado com sucesso no TiO 2 rede para formar um uniforme (–Sn 4+ –O – Ti 4+ -) solução sólida mantendo a estrutura da fase rutílica, o que está de acordo com alguns estudos anteriores [5, 18].
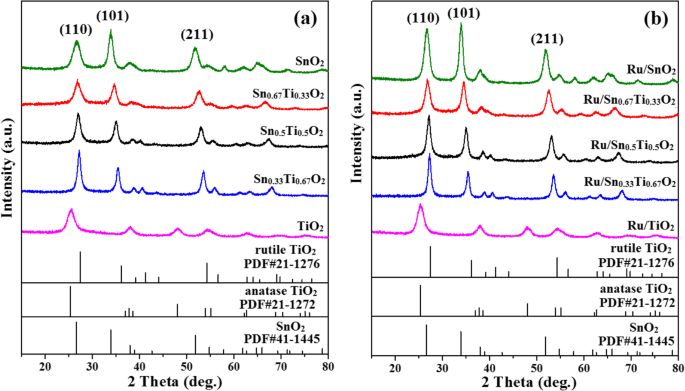
Padrões de XRD de Sn x Ti 1− x O 2 suporta ( a ) e Ru / Sn x Ti 1− x O 2 catalisadores ( b )
Para determinar as propriedades de textura das amostras, o N 2 técnica de adsorção-dessorção foi usada. O N 2 As isotermas de adsorção-dessorção e as curvas de distribuição do diâmetro dos poros correspondentes dessas amostras são mostradas na Fig. 5. O N 2 isotermas de adsorção-dessorção de SnO 2 pertencem distintamente ao tipo II; outros são clássicos do tipo IV de acordo com a classificação IUPAC e apresentam um ciclo de histerese complexo H2 em um p / p 0 faixa de 0,4-0,95, que é uma característica comum do material mesoporoso (Fig. 5a, c) [17, 32]. A existência desses mesoporos é uma razão importante para a grande área de superfície específica dos catalisadores [33]. Todos Sn x Ti 1− x O 2 suporta e Ru / Sn x Ti 1− x O 2 os catalisadores exibiram uma distribuição estreita de poros de pequeno porte (3-8 nm), especialmente o Sn 0,67 Ti 0,33 O 2 suporte e Ru / Sn 0,67 Ti 0,33 O 2 catalisadores, com o diâmetro dos poros principalmente distribuído uniformemente em torno de 5 nm (Fig. 5b, d). Este fenômeno sugeriu que uma quantidade adequada de Sn pode enfraquecer o coeficiente de difusão da superfície catalítica e indiretamente impedir a aglomeração dos cristalitos [17].
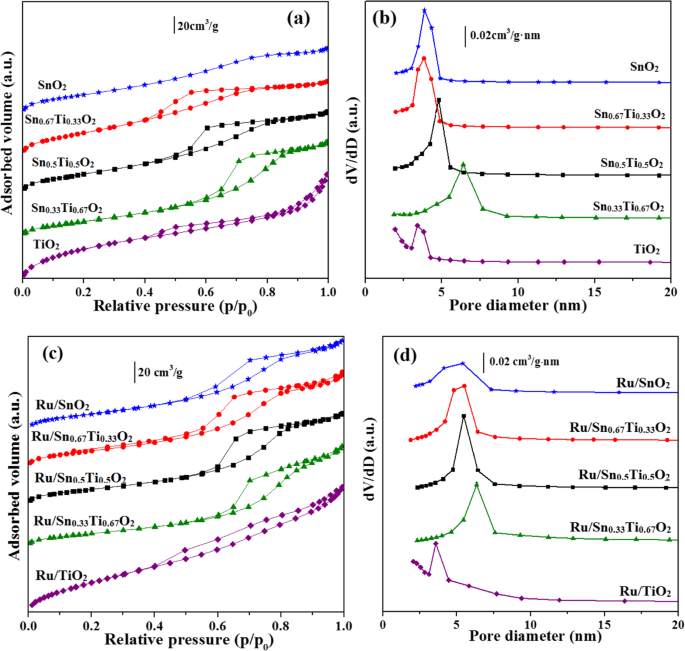
N 2 isotermas de adsorção-dessorção de Sn x Ti 1− x O 2 ( a ) e Ru / Sn x Ti 1− x O 2 ( c ) a distribuição de tamanho de poro de Sn x Ti 1− x O 2 ( b ) e Ru / Sn x Ti 1− x O 2 ( d )
As propriedades de textura de Sn x Ti 1− x O 2 suporta e Ru / Sn x Ti 1− x O 2 os catalisadores estão listados na Tabela 1. A área de superfície específica e a distribuição dos poros foram calculadas pelo método BET e BJH. Tanto a área de superfície específica quanto o volume de poro de Sn 0,67 Ti 0,33 O 2 são 156,5 m 2 g −1 e 0,17 cm 3 g −1 , respectivamente. Mas tanto a área de superfície específica quanto o volume de poro do Ru / Sn 0,67 Ti 0,33 O 2 catalisador são diminuídos em comparação com o Sn 0,67 Ti 0,33 O 2 suporte, o que indica que Ru carregado no Sn 0,67 Ti 0,33 O 2 superfície. Além disso, o Ru / Sn 0,67 Ti 0,33 O 2 o catalisador é sinterizado e a estrutura de poros abertos colapsou para formar poros obstruídos durante o processo de calcinação de alta temperatura [31]. No entanto, Ru / Sn 0,67 Ti 0,33 O 2 ainda mantém uma área de superfície específica maior (83,3 m 2 g −1 ) e diâmetro de poro menor (5,3 nm) em comparação com outras amostras de rutilo, como Ru / Sn 0,33 Ti 0,67 O 2 , Ru / Sn 0,5 Ti 0,5 O 2 e Ru / SnO 2 .
A Figura 6 mostra os espectros FT-IR de Sn x Ti 1− x O 2 suporta e Ru / Sn x Ti 1− x O 2 catalisadores. Todas as amostras apresentam picos de vibração semelhantes em posições de número de onda análogas. A adsorção em cerca de 3223,68 cm −1 é devido aos grupos hidroxila da superfície vizinhos aos locais de vacância de oxigênio [34, 35]. As bandas de 1501,86–1618,18 cm −1 pertencem ao pico de vibração angular da água. O pico de vibração de alongamento simétrico do oxigênio da rede aparece em 1028,17 cm −1 . A banda de 527,27-681,2 cm −1 pode ser atribuído ao pico de vibração de alongamento do TiO 2 ou SnO 2 [34]. Comparado com Sn x Ti 1− x O 2 suporta, Ru / Sn x Ti 1− x O 2 o espectro se amplia, indicando que o componente ativo Ru e suporta Sn x Ti 1− x O 2 têm alguma interação, resultando em defeitos de superfície dos catalisadores [36, 37].
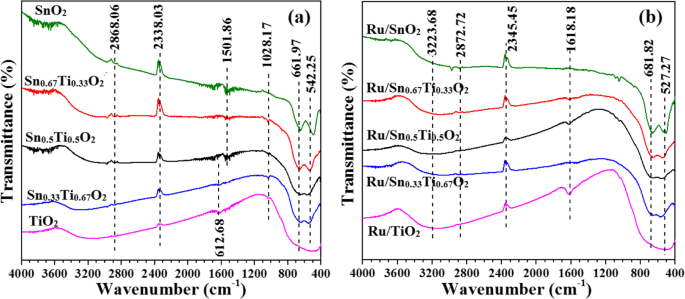
Espectros FT-IR do Sn x Ti 1− x O 2 suporta ( a ) e Ru / Sn x Ti 1− x O 2 catalisadores ( b )
Morfologia dos catalisadores
TEM de baixa e alta resolução, imagens HRTEM e a distribuição de tamanho de partícula de Ru / Sn x Ti 1− x O 2 são exibidos na Fig. 7. Com base na observação das imagens TEM apresentadas na Fig. 7a, d, g, j e m, descobrimos que todas as amostras são compostas por partículas bem definidas com formas irregulares e estrutura mesoporosa desordenada, que é formado pela aglomeração das nanopartículas [38]. Além disso, pode ser visto que o Ru / Sn 0,67 Ti 0,33 O 2 amostra tem o maior grau de aglomeração devido ao menor tamanho de grão entre essas amostras. A partir das imagens HRTEM (Fig. 7b, e, h, k, n), existe apenas um tipo de franjas de rede com 0,327 nm, que é compatível com o plano (110) dessas amostras. Além disso, descobrimos que as franjas da rede de TiO 2 e SnO 2 não são observados, o que é atribuído a Sn 4+ tendo sido dopado com sucesso na rede de TiO 2 para formar um Sn x homogêneo Ti 1− x O 2 solução sólida [39]. Os resultados são consistentes com o XRD. A distribuição do tamanho das partículas Ru (Fig. 7c, f, i, l, o) mostra que os tamanhos aproximados das partículas Ru variaram de 3 a 20 nm. A introdução do Sn 4+ poderia efetivamente diminuir os tamanhos das partículas de Ru e alcançar uma maior dispersão no Sn x Ti 1− x O 2 superfície. Comparando com outras amostras, a distribuição de tamanho de partícula Ru de Ru / Sn 0,5 Ti 0,5 O 2 amostra era mais ampla (<13 nm), o que pode ser causado pela interação entre (–Sn 4+ –O – Ti 4+ -) espécies e Ru [26]. O Ru / Sn 0,67 Ti 0,33 O 2 o catalisador tem melhor dispersão de Ru e menor tamanho de partícula (5,49 nm) entre todas as amostras.
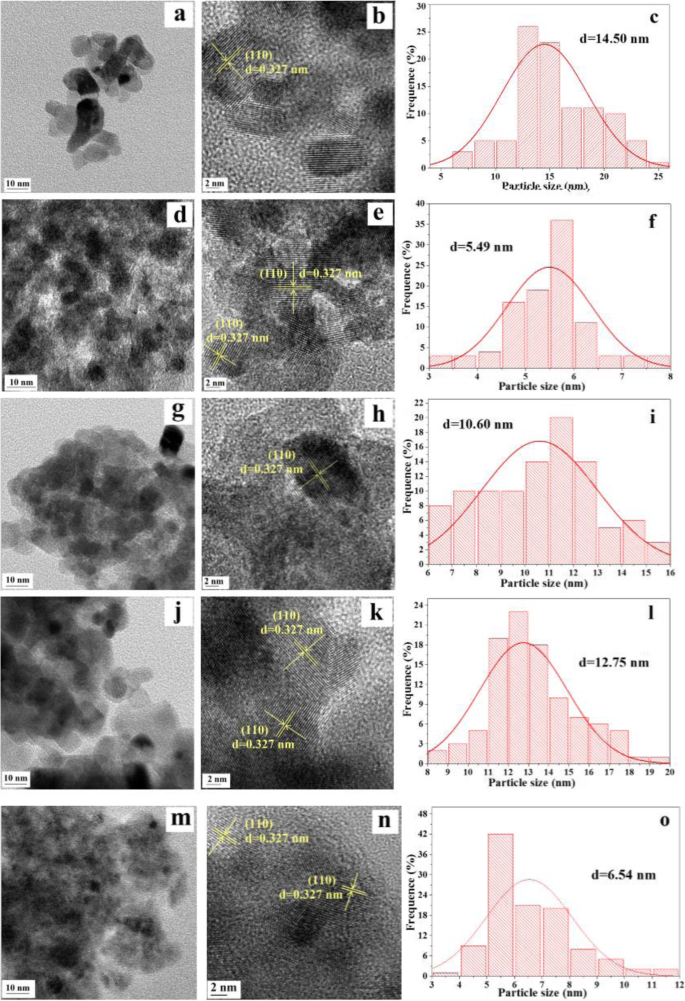
TEM, imagens HRTEM e a distribuição de tamanho de partícula de a , b , c Ru / SnO 2 ; d , e , f Ru / Sn 0,67 Ti 0,33 O 2 ; g , h , i Ru / Sn 0,5 Ti 0,5 O 2 ; j , k , l Ru / Sn 0,33 Ti 0,67 O 2 ; e m , n , o Ru / TiO 2
Propriedades de superfície dos catalisadores
Para determinar ainda mais os estados elementares e a composição da superfície, a análise XPS foi realizada. A Figura 8 mostra os espectros de XPS de Sn 3d, Ti 2p, O 1s e Ru 3d para o Sn x Ti 1− x O 2 suporta e Ru / Sn x Ti 1− x O 2 catalisadores. Os valores de energia de ligação XPS do Sn 3d 3/2 e Sn 3d 5/2 são observados em 486,6-487,5 eV e 494,9-496,1 eV, respectivamente, que são característicos de Sn 4+ espécies em Sn x Ti 1− x O 2 suporta ou Ru / Sn x Ti 1− x O 2 catalisadores. Curiosamente, a energia de ligação de Sn 3d 3/2 e Sn 3d 5/2 alterado para valores mais altos após a introdução de Sn 4+ , indicando alguns dos Sn 4+ substitua o Ti 4+ sites e têm uma forte interação com TiO 2 , que está de acordo com XRD. Além disso, as vagas de oxigênio podem ser criadas pelo valor inferior Sn δ + [5]. Dois picos correspondentes a Ti 2p 3/2 e Ti 2p 1/2 são observados em 458,7-459,9 eV e 464,3-465,8 eV nos espectros XPS de Ti 2p, sugerindo que Ti 4+ e Ti 3+ existia nas amostras, e os valores de energia de ligação de Ti 2p 3/2 e Ti 2p 1/2 alterado para valores de energia de ligação mais altos com o aumento de Sn 4+ , comprovando ainda mais a existência de lacunas de oxigênio. Pode-se observar na Tabela 3 que a razão molar Sn / Ti por XPS é observada ligeiramente superior ao cálculo teórico, indicando que o Sn é enriquecido na superfície dos catalisadores, o que leva a mais vacâncias de oxigênio. Como a eletronegatividade do Sn (1,96) é maior que a do Ti (1,62), em outras palavras, a capacidade de captura de elétrons do Sn é mais forte do que a do Ti, o que causa o equilíbrio redox (Sn 4 + + Ti 3+ → Sn δ + + Ti 4+ ) mudando para a direita [32].
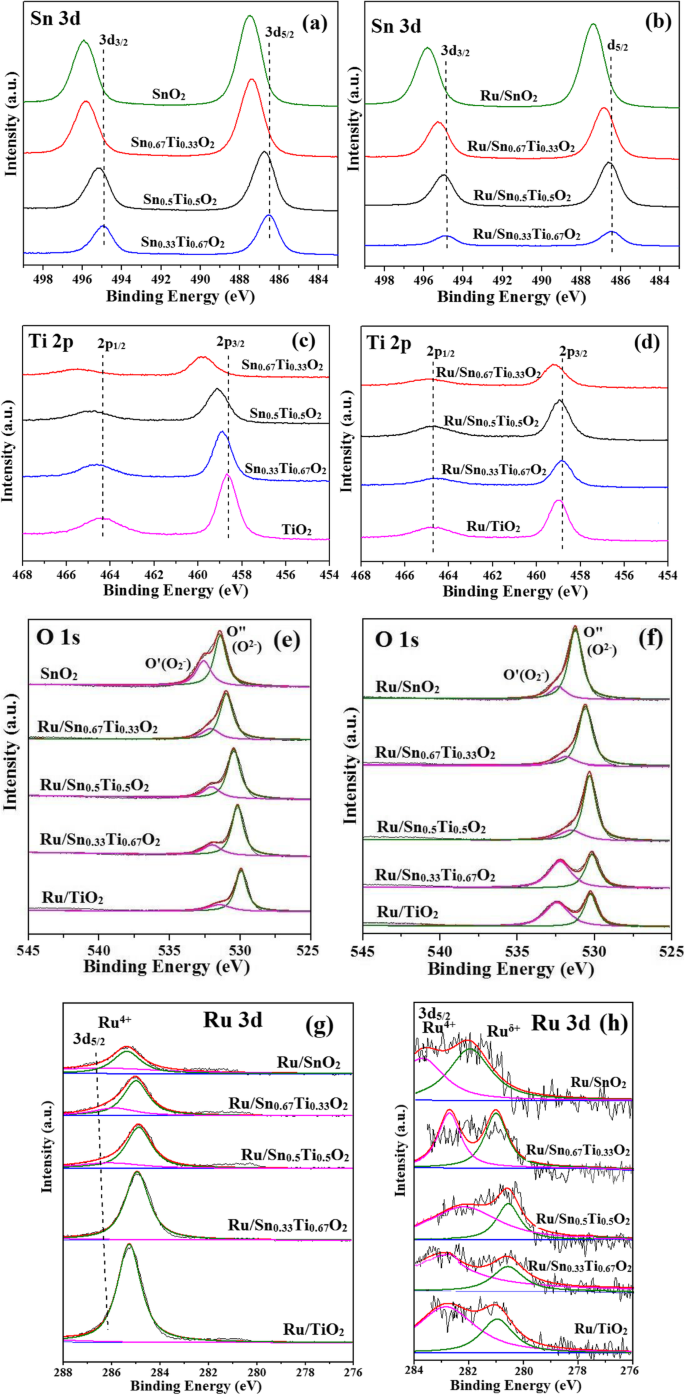
Espectro XPS (Sn3d ( a , b ), Ti2p ( c , d ), O1s ( e , f ) e Ru3d ( g , h )) de Sn x Ti 1− x O 2 suporta e Ru / Sn x Ti 1− x O 2 catalisadores
Os espectros de alta resolução do recurso de ionização O 1s são numericamente consistentes com o recurso Gaussiano e deconvoluídos em dois picos [5]. A energia de ligação mais alta (O ’, 532,1 eV) é causada pelo oxigênio adsorvido quimicamente que formou o (O 2 - , O - , ou O 2 2− ) espécies. No entanto, o O ”(529,9 eV) é o pico característico de O 2− na superfície dos óxidos de metal. Curiosamente, a energia de ligação de O 1s mudou para valores mais altos após a adição de Sn 4+ .
Os espectros de Ru 3d apresentam Ru 4+ e menor valor Ru δ + . O sinal de Ru 3d 5/2 é frequentemente usado para analisar o estado de carga das espécies Ru, uma vez que outro Ru 3d 3/2 sobrepõe-se com C 1s em cerca de 284,0 eV [40]. A energia de ligação de 282,0-283,5 eV é atribuída a Ru 3d 5/2 , que correspondia a Ru 4+ . A energia de ligação inferior em cerca de 280,2-281,7 eV é atribuída ao estado inferior Ru δ + , e o Ru δ + razão relativa em Ru / Sn 0,67 Ti 0,33 O 2 atinge 53,9%, o que é maior do que outros catalisadores. Pode-se explicar que a forte interação entre Sn 0,67 Ti 0,33 O 2 e Ru causou uma maior quantidade de espécies reativas de oxigênio na superfície [26].
As análises XPS e EDS são realizadas para determinar a superfície e a composição da massa das amostras, conforme mostrado na Tabela 2. A análise da superfície e da massa Ru mostra que Ru / Sn 0,67 Ti 0,33 O 2 tem o maior Ru superficial (0,69% em peso) e Ru bruto (0,40% em peso) entre todos os catalisadores, indicando que o componente ativo Ru está mais uniformemente distribuído no Sn 0,67 Ti 0,33 O 2 suporte, e mais espécies de Ru entram no interno de Sn 0,67 Ti 0,33 O 2 para formar uma interação forte.
A fim de investigar melhor o desempenho de redução do Ru / Sn x Ti 1− x O 2 catalisadores, são realizados estudos de redução com temperatura programada (Fig. 9). As formas desses H 2 Os perfis -TPR são quase idênticos. Os picos de redução de Ru / Sn x Ti 1− x O 2 são divididos em duas partes:os picos de redução de baixa temperatura 80–270 ° C estão associados ao estado inferior Ru δ + reduzido de RuO 2 e uma quantidade significativa de Sn 4+ que poderia ser reduzido para menor valor Sn δ + ou pode ser atribuído à redução do oxigênio da superfície [41], enquanto os picos de redução de alta temperatura 600-640 ° C estão associados a Sn 0 reduzido de Sn δ + ou a redução do oxigênio em massa dos catalisadores [26, 42], que é consistente com os resultados de XPS. A redução da temperatura de Ru / Sn x Ti 1− x O 2 move-se em direção à temperatura mais baixa, os picos aumentam e H 2 aumento de consumo com a adição de Sn, e consumo de hidrogênio do H 2 As medidas de -TPR são apresentadas na Tabela 3. A dispersão dos componentes ativos na superfície das amostras tem efeito significativo na redução do oxigênio superficial, e o hidrogênio poderia ser mais facilmente ativado com maior dispersão de Pd, resultando no aumento de H 2 consumo [43]. Portanto, podemos inferir que a introdução de Sn aumentou significativamente a dispersão de Ru no portador, o que pode ter resultado da formação de Sn x Ti 1− x O 2 solução sólida. Os resultados estão de acordo com XRD e TEM. Porque a redução do TiO 2 geralmente é difícil de conduzir em baixa temperatura, não há picos de TiO 2 redução observada durante o H 2 -TPR de 50 a 800 ° C [15]. No entanto, o Ru / Sn 0,67 Ti 0,33 O 2 ainda exibe um H 2 mais alto consumo.
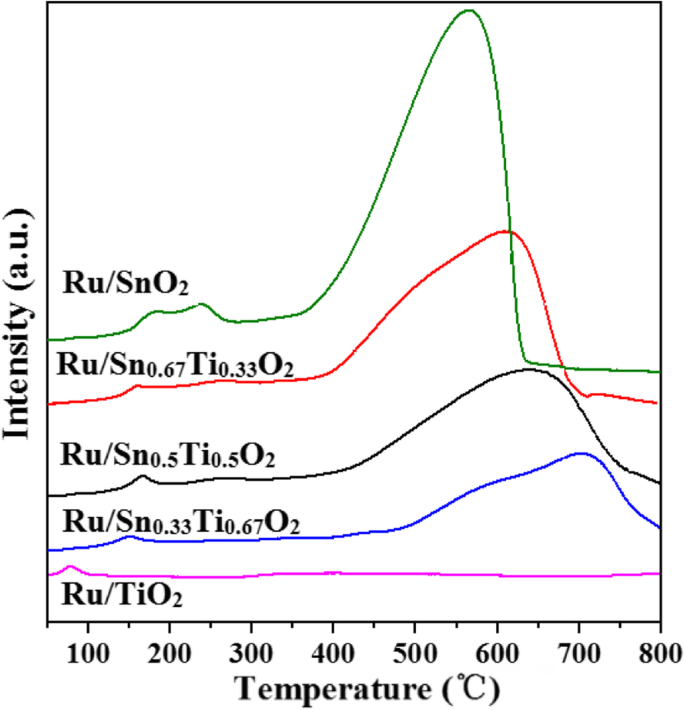
H 2 -TPR espectros de Ru / Sn x Ti 1− x O 2 catalisadores
O 2 Experimentos -TPD (Fig. 10) de Ru / Sn x Ti 1− x O 2 as amostras são impostas para obter informações sobre a mobilidade do oxigênio da superfície e da rede. O sinal em baixa temperatura (<200 ° C) é atraído pela dessorção do oxigênio adsorvido na superfície (O 2 - , O 2 2− , ou O - espécies); o pico principal centrado em 280 ° C ou 500 ° C, que é atribuído à dessorção das espécies de oxigênio da estrutura, e os picos acima de 600 ° C são atribuíveis à dessorção do oxigênio da rede (O 2 - ) espécies [44]. A incorporação de Sn aumentou as espécies de oxigênio adsorvidas e mudou para uma temperatura mais baixa [45]. Os resultados indicam que a incorporação de Sn melhorou a capacidade de ativação de oxigênio do Ru / Sn x Ti 1− x O 2 amostras e a interação entre os portadores Sn x Ti 1− x O 2 e componente ativo Ru [46, 47].
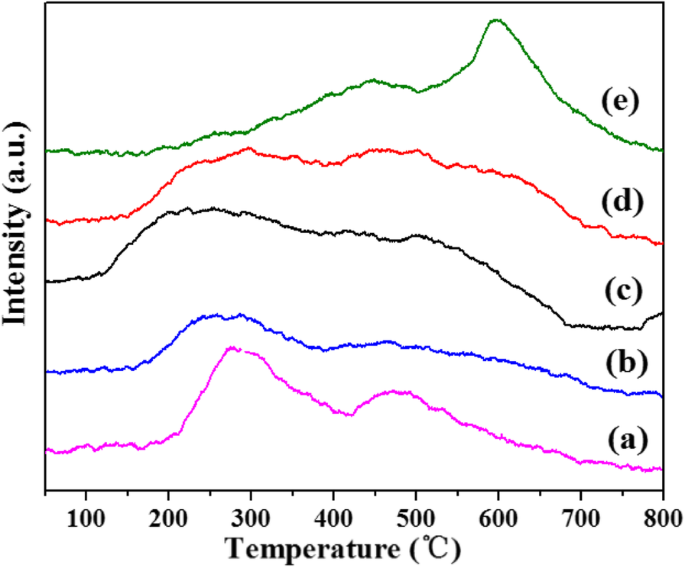
O 2 -TPD espectros de Ru / TiO 2 ( a ), Ru / Sn 0,33 Ti 0,67 O 2 ( b ), Ru / Sn 0,5 Ti 0,5 O 2 ( c ), Ru / Sn 0,67 Ti 0,33 O 2 ( d ), e Ru / SnO 2 catálise
CO e / ou O 2 Interação com essas amostras
Os espectros de FI-IR in situ de adsorção de CO são registrados para investigar melhor o efeito das espécies de óxido de rutênio, como mostrado na Fig. 11. A banda localizada a 2052 cm −1 é atribuído ao CO linear adsorvido em cristalitos de Ru reduzidos (Ru δ + –CO), a banda em 2140 cm −1 e 2075 cm −1 pode ser atribuído a dois tipos diferentes de espécies multicarbonil em sítios Ru parcialmente oxidados (Ru n + (CO) x ), e a banda em 1765 cm −1 é atribuído a (Sn x Ti 1− x O 2 ) Espécies Ru – CO [48, 49]. O Ru δ + –Os picos de adsorção de CO à temperatura ambiente indicam a presença de algum estado inferior Ru δ + espécies. Isso está de acordo com os resultados do XPS. No entanto, a temperatura de dessorção do Ru δ + –O pico de CO está relacionado à razão Sn / Ti e à temperatura. À medida que a temperatura aumenta, o pico de intensidade aumenta primeiro e depois diminui gradualmente. Simultaneamente, o pico de adsorção de CO se move para um número de onda mais alto (2052 cm −1 a 25 ° C e 2060 cm −1 em temperaturas mais altas). Este desvio para o vermelho indica que Sn 4+ tem maior capacidade de doação de elétrons [50]. Para o Ru / SnO 2 , Ru / Sn 0,5 Ti 0,5 O 2 , Ru / Sn 0,33 Ti 0,67 O 2 e Ru / TiO 2 amostras, o pico máximo de adsorção de CO em Ru δ + aparece a cerca de 200 ° C e desaparece basicamente a 300 ° C. Para o Ru / Sn 0,67 Ti 0,33 O 2 amostra, o pico máximo de adsorção de CO em Ru δ + aparece a cerca de 200 ° C, o que pode ser observado claramente mesmo a 300 ° C. Pode-se concluir que Ru δ + é muito mais estável em Ru / Sn 0,67 Ti 0,33 O 2 amostra, que pode fornecer mais locais de adsorção de CO do que nas outras amostras.
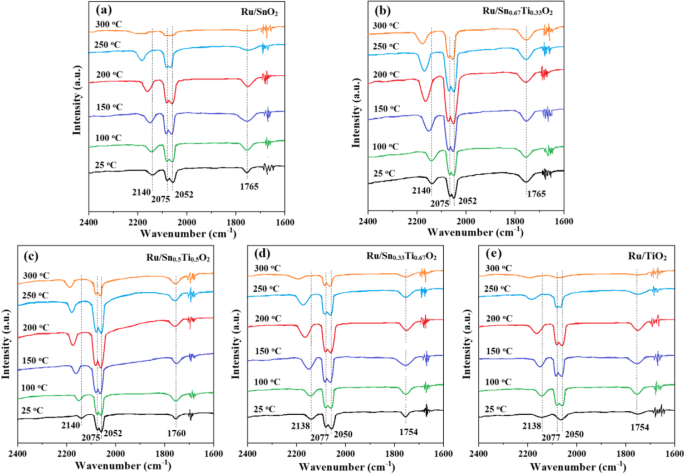
Espectros FI-IR in situ da interação CO / Ar de 10% com a Ru / SnO 2 , b Ru / Sn 0,67 Ti 0,33 O 2 , c Ru / Sn 0,5 Ti 0,5 O 2 , d Ru / Sn 0,33 Ti 0,67 O 2 , e Ru / TiO 2 em diferentes temperaturas
Possível mecanismo de reação sobre Ru / Sn x Ti 1− x O 2 Catalisadores
De acordo com as caracterizações mencionadas acima, um possível mecanismo de reação de CO e C 3 H 8 a oxidação é proposta e esquematizada na Fig. 12. Com base nos resultados de XPS, os elétrons migram entre Ru e Sn x Ti 1− x O 2 solução sólida; porque a eletronegatividade de Ru (2.22) é maior que a de Ti (1.62) e Sn (1.96), os elétrons serão transferidos do Sn x Ti 1− x O 2 solução sólida para Ru 4+ , em que estado inferior Ru δ + será gerado. Enquanto isso, –Ti 4+ –O – Sn 4+ - as espécies são oxidadas e mais oxigênio será absorvido na superfície de Sn x Ti 1− x O 2 solução sólida, que pode fornecer oxigênio para a reação de oxidação de CO e C 3 H 8 . Ao mesmo tempo, os subprodutos produzidos no processo de oxidação também serão adsorvidos na superfície do Sn x Ti 1− x O 2 solução sólida, que não irá deteriorar a atividade de Ru δ + espécies. É também a razão da alta estabilidade dos catalisadores. Além disso, o estado inferior Ru δ + espécies têm mais propriedades de metal, que desempenham um papel crucial na ativação de CO e C 3 H 8 [40]. Comparado com Ru / TiO 2 e Ru / SnO 2 , alta dispersão de Ru em Sn x Ti 1− x O 2 a solução sólida também é uma causa importante para sua excelente atividade e estabilidade. Baseado em O 2 -TPD analysis, O 2 é primeiro adsorvido na superfície dos catalisadores para formar O 2 - espécies e CO e C 3 H 8 adsorvido em Ru δ + espécies reagem com O 2 - espécies para produzir CO 2 e H 2 O, que é um mecanismo de Langmuir-Hinshelwood.
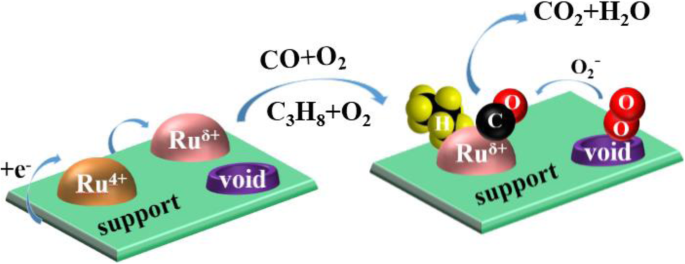
Possível mecanismo de reação de CO e C 3 H 8 sobre Ru / Sn x Ti 1− x O 2
Conclusões
Uma série de Ru / Sn x Ti 1− x O 2 os catalisadores foram preparados por um método hidrotérmico de uma etapa para a oxidação catalítica de CO e C 3 H 8 . As condições de preparação de Ru / Sn x Ti 1− x O 2 os catalisadores foram otimizados para a reação de oxidação do CO. Ru / Sn 0,67 Ti 0,33 O 2 o catalisador mostra melhor atividade catalítica de CO e estabilidade em baixa temperatura sob a condição de temperatura hidrotérmica a 180 ° C, tempo hidrotérmico em 24 h e temperatura de calcinação em 400 ° C.
Os efeitos de diferentes razões molares de Sn / Ti nas propriedades catalíticas de Ru / Sn x Ti 1− x O 2 catalisadores para CO e C 3 H 8 foram investigados sob as melhores condições de preparação. Os resultados mostram que Ru / Sn 0,67 Ti 0,33 O 2 o catalisador exibe melhor atividade e estabilidade em baixa temperatura. A conversão de CO atingiu 90% a 240 ° C, e T 50 dos quais se mantém a 180 ° C. A conversão completa de C 3 H 8 poderia ser alcançado a 500 ° C, e seu T 50 permanece a 320 ° C. A excelente atividade catalítica de Ru / Sn 0,67 Ti 0,33 O 2 catalisador é atribuído aos fatores listados a seguir.
- (1)
A incorporação bem-sucedida de Sn 4+ no TiO 2 estrutura para substituir Ti 4+ forma uma solução sólida homogênea (–Sn 4+ –O – Ti 4+ - espécie), que aumenta a interação entre o componente ativo Ru e o portador Sn x Ti 1− x O 2 . O crescimento do cristal da fase anatase pode ser inibido pela introdução de Sn 4+ , que resulta na presença da fase rutilo.
- (2)
Nanopartículas ultrafinas de Ru (~ 5 nm) são altamente dispersas em Sn x Ti 1− x O 2 suporte, sugerindo que a introdução de Sn 4+ poderia não apenas evitar a aglomeração de grãos e induzir um tamanho de grão menor, mas também produzir mais defeitos, como lacunas de oxigênio.
- (3)
CO e C 3 H 8 espécies podem ser absorvidas em Ru δ + sites; O 2 - é formado pela adsorção de O 2 sobre as vagas de oxigênio. O CO e C adsorvidos 3 H 8 reage com O 2 - para produzir CO 2 e H 2 O.
Disponibilidade de dados e materiais
Todos os dados gerados ou analisados durante este estudo estão incluídos neste artigo publicado e informações de apoio.
Abreviações
- XRD:
-
Difração de raios X
- BET:
-
Brunauer-Emmett-Teller
- FT-IR:
-
Transformada de Fourier Infra-vermelho
- TEM:
-
Microscopia eletrônica de transmissão
- XPS:
-
espectroscopia de fotoelétrons de raios-X
- H 2 -TPR:
-
H 2 -redução programada de temperatura
- O 2 -TPD:
-
Dessorção de oxigênio programada por temperatura
- DOC:
-
Catalisadores de oxidação de diesel
- SCR:
-
Redução Catalítica Seletiva
- DPF:
-
Filtro de partículas diesel
- SOF:
-
Fração orgânica solúvel
Nanomateriais
- Preparação e propriedades magnéticas de nanopartículas de espinélio FeMn2O4 dopadas com cobalto
- Em direção aos nanofluidos de TiO2 - Parte 1:Preparação e propriedades
- Rota de eletrofiação em uma etapa de nanofibras de Rutilo TiO2 modificadas com SrTiO3 e suas propriedades fotocatalíticas
- Preparação e atividade de hidrogenação catalítica aprimorada de nanopartículas de Sb / Palygorskite (PAL)
- Os efeitos da relação Li / Nb na preparação e desempenho fotocatalítico de compostos Li-Nb-O
- A preparação da nanoestrutura de casca de gema de Au @ TiO2 e suas aplicações para degradação e detecção de azul de metileno
- Preparação e desempenho fotocatalítico de fotocatalisadores de estrutura oca LiNb3O8
- Preparação de micrromateriais híbridos MnO2 revestidos com PPy e seu desempenho cíclico aprimorado como ânodo para baterias de íon-lítio
- Um romance fotocatalisador de heterojunção Bi4Ti3O12 / Ag3PO4 com desempenho fotocatalítico aprimorado
- Preparação de nanoesferas poliméricas impressas com íons de paládio (II) e sua remoção de paládio (II) da solução aquosa



