Uma síntese hidrotérmica de nanopartículas híbridas de Fe3O4 @ C e desempenho adsortivo magnético para remover íons de metais pesados em solução aquosa
Resumo
O material com núcleo avançado com uma área específica elevada tem sido considerado um material eficaz para remover metais pesados de soluções aquosas. Um Fe 3 com núcleo shell O 4 Agregados de nanopartículas híbridas @C com canal ambientalmente correto no estudo. Além disso, a maior exposição dos locais de adsorção pode ser alcançada para a configuração especial em que a área de superfície de Brunauer-Emmet-Teller (BET) mais alta alcance até 238,18 m 2 g −1 . Assim, uma remoção mais eficiente de íons de metal pesado é obtida, Pb (II), Cd (II), Cu (II) e Cr (VI) até 100, 99,2, 96,6 e 94,8%, respectivamente. Além disso, os produtos são facilmente separados das soluções aquosas após a adsorção, devido ao tamanho submicrométrico relativamente grande e aos campos magnéticos externos aprimorados introduzidos pelos núcleos à base de ferro. Fornecemos um modo ideal para remover íons de metais pesados usando Fe 3 revestido com núcleo O 4 @C sob a condição de tratamento de água. Uma nova abordagem é esclarecida que os materiais nano / micro-funcionais do núcleo-shell podem ser bem sintetizados em grandes escalas que são usadas em muitos campos, como remediação ambiental, catalisador e energia.
Histórico
Com a voz da proteção ambiental sendo constante e crescente, há cada vez mais atenção ao seu efeito tóxico que se refere à saúde humana e à poluição ambiental por contaminação por metais pesados [1,2,3]. A remoção de elementos de metal pesado de águas residuais industriais antes da descarga torna-se crucial [4]. Até o momento, troca iônica, precipitação de coagulação e uma série de tecnologias tradicionais foram aplicadas para remover metais pesados de águas residuais durante as últimas décadas [5, 6]. A compreensão de que as técnicas convencionais trazem benefícios significativos para o ser humano e também expõe desvantagens caracterizadas tanto do ponto de vista administrativo quanto técnico, que são custos operacionais caros, geração adicional de lodo tóxico e remoção incompleta de metal [7,8,9]. Por outro lado, controlar o tamanho das partículas, a morfologia dos materiais adsorventes, tem se mostrado uma das soluções eficientes e inovadoras para contornar esse tipo de problema. Esferas ocas, nanofios e nanotubos têm melhor desempenho de adsorção para contribuir com a remoção de metais pesados nas Referências [10,11,12,13]. Além disso, as pesquisas estão focadas no novo material que contém a estrutura core-shell com o recurso core-void-shell. Provou-se por suas vantagens em comparação com o mesmo tamanho de contrapartes sólidas, como a validade daquele nas mudanças de áreas superficiais, índice de refração, menor densidade e volume de acomodação, o que leva a uma grande contribuição tanto do ponto de vista de propriedades e funções [14, 15]. Assim, esta estrutura única com forma, composição e arquitetura interior ajustáveis é uma direção estimulante para buscar a remediação ambiental.
Muitas literaturas tratam de materiais de estrutura núcleo-casca. Guo [16] fez gaiola-sino Ag @ TiO 2 materiais, e o estudo expressou melhores propriedades fotocatalíticas e eletroquímicas. Liu [17] preparou núcleo-shell Fe 3 O 4 nanopartículas de polidopamina que exibiram bom potencial no campo de suporte de medicamentos, transportador de catalisador e adsorvente de carbono. Até onde sabemos, a assistência de moldes removíveis ou sacrificais (por exemplo, sílica polimérica [18], esferas [19], carbono [20] e líquidos iônicos [21]) das cascas desejáveis são importantes na síntese geral de núcleos estruturas de nanopartículas híbridas de casca. No entanto, os materiais de estrutura core-shell mais disponíveis são sintetizados por processos multi-template que se concentram principalmente nas configurações relativamente simples, como uma composição em partículas de camada única. Além disso, ainda faltam métodos de remoção de íons de metais pesados com uma abordagem geral que acompanhe ainda mais o fortalecimento da viabilidade de preparação dos materiais avançados com estruturas núcleo-casca, incluindo tempo e custo no processo de construção de nanoestruturas complexas que foram limitadas por modelos de síntese e rotas com vários modelos, que se tornaram um desejo tanto do ponto de vista técnico quanto de benefício ecológico.
A síntese do nanocompósito magnético funcional é uma forma eficaz e prática de resolver a separação entre o adsorvente e a solução para expandir a separação magnética [22]. O polímero cada vez mais imobilizado covalentemente, a nova molécula e o material inorgânico são colocados na superfície da nanopartícula magnética neste processo; eles são rotas técnicas úteis para o tratamento de águas residuais com íons de metais pesados tóxicos também [23]. Por exemplo, novos nanocompósitos magnéticos modificados com quitosana sintetizados [24] e Fe monodisperso 3 O 4 @silica core-shell structure compósito nanopartículas magnéticas core-shell microesferas [25] são relatadas. Apesar desses nanocompósitos magnéticos serem facilmente separados da solução por meio do processo de adsorção baseado no magnético externo, ainda é necessário considerar as condições especiais, como a aplicabilidade de águas residuais de ácido forte.
Recentemente, existem muitos estudos sobre materiais nanoestruturados à base de carbono. Wildgoose [26] apresentou que esses tipos de materiais apresentam vantagens óbvias em termos de custo, resistência à corrosão alcalina, área de superfície específica e capacidade de adsorção. Uchida [27] apontou que os grupos funcionais carboxílicos podem ser facilmente gerados na superfície do carbono, aumentando ainda mais a capacidade de adsorção de íons de metais pesados. Porém, a falha fatal da dificuldade de removê-los de uma solução, causada pelo pequeno tamanho das partículas de carbono, limitou sua aplicação no tratamento de efluentes de metais pesados. Considerando que a nanopartícula magnética revestida com carbono é um meio voltado para o tratamento de águas residuais, ela apresentou impactos avançados na capacidade de adsorção e na propriedade de separação no campo magnético externo. Muito mais atenção aumentou [28,29,30,31,32,33,34,35]. Zhang [36] preparou nanoesferas ocas magnéticas de carbono, usadas na remoção de íons de cromo. Para remover o metal pesado, os grupos de Wang [37] relataram um estudo de caso de materiais com nanopartículas de Fe. Esses estudos anteriores indicaram que o trabalho futuro correspondente deve se referir a adsorventes de íon de metal pesado altamente eficientes com fácil separação e grande capacidade de adsorção. Nesse ínterim, deve ser apontado que existem estudos raros sobre Fe 3 core-shelled O 4 Agregados de nanopartículas híbridas @C até agora.
Neste estudo, preparamos microesferas de carbono com núcleos magnéticos. Além disso, uma estratégia concisa foi proposta para sintetizar Fe 3 com núcleo shell O 4 Agregados de nanopartículas híbridas @C, que é um material avançado para remoção de íons de metais pesados com pureza de força, áreas de superfície e capacidade de adsorção. Comparado com a tecnologia de produção tradicional de Fe 3 O 4 materiais, os benefícios são óbvios. Ele não apenas expressou uma área de superfície maior e configuração estável, mas também o modelo de remoção que não é afetado pela morfologia do produto. Nossa pesquisa fornece um maior grau de sítios ativos [38, 39]. O adsorvente pode ser facilmente separado quando os campos magnéticos externos são introduzidos, que são causados pelas nanopartículas à base de ferro [40, 41]. Portanto, o Fe 3 de núcleo-shell obtido O 4 Os agregados de nanopartículas híbridas @C mostram capacidade de adsorção superior para íons de metais pesados com uma rota ecologicamente correta, produção em massa e benefícios de custo.
Experimental
Materiais e Síntese
Síntese de Fe com núcleo com casca 3 O 4 Agregados de nanopartículas híbridas
Em etapas de síntese típicas, 0,72 g de Fe (NO 3 ) 3 · 9H 2 O, 0,0086 g de NH 4 H 2 PO 4 , 0,008 g de Na 2 SO 4 · 10H 2 O e 3 g de glicose foram dissolvidos em água destilada, respectivamente, misturados todos juntos em um volume de 90 mL, adicionada água destilada à mistura e continuamente misturada por 10 min com um agitador magnético básico. Em seguida, a mistura mudou para 100 mL de autoclave de aço inoxidável forrada com Teflon a 180 ° C, 48 h. Após a reação ser completada e resfriada à temperatura ambiente naturalmente, o pé preto foi adquirido e lavado várias vezes com água desionizada e etanol absoluto, em seguida, o pé preto foi dessecado a 65 ° C a noite inteira sob a condição de vácuo e, por último, obtido precursores calcinados a 450 ° C com a taxa de 3 ° C min −1 em seguida, reteve o aquecimento com um fluxo sequencial de monóxido de carbono / gás argônio (4 h) e resfriou até a temperatura ambiente. The Fe 3 O 4 Amostra @C foi obtida. Conforme descrito no Esquema 1, a hidrólise de Fe 3+ leva à camada de óxido de Fe com precisão nanométrica. Enquanto isso, a sacarose é carbonizada. Depois disso, microesferas de material composto de Fe-C-O serão criadas in situ durante a reação de aquecimento do banho por meio de seções de calcinação e, em seguida, ganharão Fe 3 revestido com núcleo O 4 Nanopartícula híbrida @C.
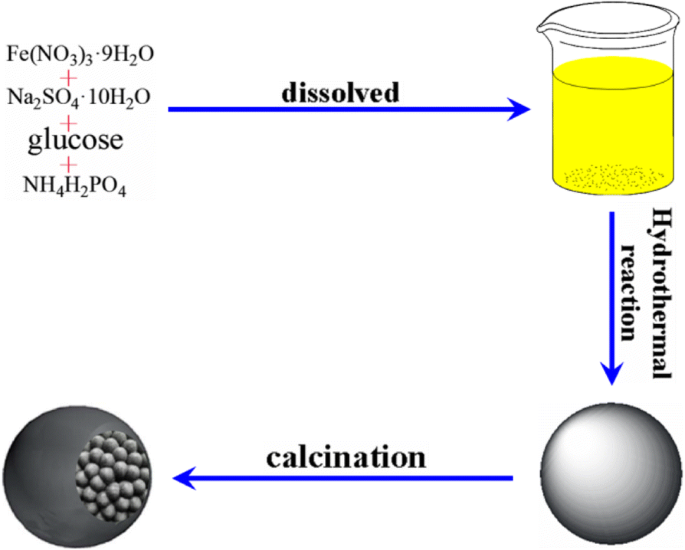
Rota de síntese do Fe 3 com casca central O 4 Nanopartícula híbrida @C
Caracterização
A composição de fase do material preparado foi analisada por difração de raios-X (XRD), que foi tomada a 2 θ =20 ° –90 ° por difratômetro Rigaku D / max-A com radiação Co Kα. FTIR (espectroscopia de infravermelho com transformada de Fourier, Thermo Nicolet AVATARFTIR 360) foi realizada para registrar os caracteres FTIR das amostras dentro do intervalo 400-4000 cm -1 também. AMRAY 1000B SEM (microscópio eletrônico de varredura), HR-TEM (microscópio eletrônico de transmissão de alta resolução, JEOL JEM-2100) (200 Kv) e difração de elétrons de área selecionada (SAED) foram implementados para descrever a morfologia da amostra, o recurso de microestrutura, e a estrutura da rede. Além disso, o aparelho Micromeritics Tristar a 350,15 ° C foi levado para medir os processos de adsorção e dessorção de nitrogênio; Brunauer-Emmet-Teller (BET) foi usado para discutir as áreas de superfície específicas; A análise quantitativa da espectroscopia de absorção atômica (AAS) será implementada pelo espectrofotômetro Hitachi Z2000, que possui lâmpadas catódicas ocas e chama de ar de acetileno. O desempenho magnético do material preparado foi medido por magnetômetro de amostra vibratória (VSM).
Experimentos de remoção de íons de metal pesado
Em temperatura ambiente, a realização de uma série de experimentos foi considerada para remover íons de metais pesados. Em primeiro lugar, o Pb (II), o Cd (II), o Cu (II) e o Cr (VI) são adicionados em quatro recipientes fechados; depois disso, HCl 0,1 M e NH 0,1 M 3 • H 2 O são usados para ajustar o pH para 3, e então, as soluções de adsorção com o volume final de 50 mL e concentração de 10 mg L −1 foram obtidos. Posteriormente, sob uma condição de agitação contínua, 20 mg de Fe 3 como preparado O 4 A amostra @C foi adicionada às soluções acima. Durante o processo de reação de adsorção, quase 1,0 mL de cada solução acima mencionada foi lixiviado ao longo dos vários períodos (0, 0,5, 1, 1,5, 2, 4, 6, 10 e 24 h, respectivamente) por meio da utilização de um tubo de pino que equipado com filtro de membrana, enfim atenuado para ser aplicado na medida AAS.
Resultado e discussão
Características Físico-Químicas do Core-Shelled Fe 3 O 4 @C Nanosphere
Os padrões de XRD do Fe 3 com núcleo-shell sintetizado O 4 Agregados de nanopartículas híbridas @C e seu precursor foram mostrados na Fig. 1, que evidenciou que o processo de produção é de maior cristalinidade do que o precursor através de calcinações a 450 ° C. As amostras preparadas exibiram materiais compostos correspondentes a cúbico de face centrada (f c c) Fe 3 O 4 (JCPDS (Joint Committee on Powder Diffraction Standards), cartão nº 75-0033). O pico de difração em 21,5 °, conforme mostrado nos padrões, deve ser atribuído ao plano (002) do carbono grafítico, que também pode ser encontrado diretamente por SEM e TEM.
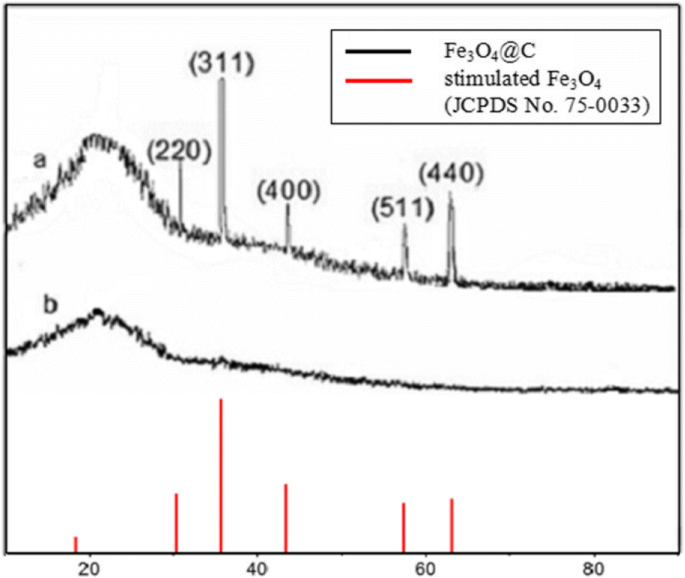
Padrões de XRD de Fe 3 com núcleo shell O 4 Agregados de nanopartículas híbridas @C e seu precursor (a — Fe 3 O 4 @C agregados de nanopartículas híbridas; b - o precursor)
Imagens SEM do precursor e do Fe 3 com núcleo-shell O 4 A síntese de nanopartículas híbridas @C produzida por calcinação a 450 ° C em diferentes ampliações foi exibida na Fig. 2a-c. Obviamente, além de um pouco menor em tamanho, o Fe 3 sintetizado O 4 @C reteve a morfologia do precursor preparado que são microesferas ca. com o tamanho de 700 nm uniformemente. A Figura 2b, c descreveu claramente a estrutura de núcleo-casca híbrida do Fe 3 O 4 @C; pode ser evidenciado pelas mesosferas. A Figura 2c também mostra que o pó sintetizado é feito de nanopartículas com base nos resultados das partículas parciais com a casca parcialmente quebrada. As microesferas fissuradas acima provavelmente vêm do rápido transporte de massa que passa pelas conchas. A Figura 2d, e também descreveu a estrutura de Fe 3 O 4 @C. Há uma estrutura interna de núcleo-casca visível na Fig. 2d, iluminando que o Fe 3 O 4 nanopartículas são distribuídas no carbono amorfo, obviamente. Isso é consistente com o resultado SEM. Por outro lado, HRTEM (Fig. 2e) e XRD também estão em uma boa concordância, o que mostra que o espaçamento da rede (0,297 nm) concorda com (220) espaçamento plano de Fe cúbico de face centrada 3 O 4 . Seu resultado SAED revelou que o Fe 3 O 4 as nanopartículas eram monocristais altamente cristalinos. Assim, a amostra de núcleo-casca híbrida única pode conter uma maior eficiência de resposta do local de adsorção para os adsorbatos alvo, que podem ser usados no campo da proteção ambiental.

Imagem SEM do precursor preparado ( a ) Imagens SEM ( b , c ), Imagem TEM ( d ), Micrografia HRTEM ( e ), e difração de elétrons de área selecionada ( f ) de Fe 3 com núcleo-shell sintetizado O 4 Agregados de nanopartículas híbridas @C produzidos por calcinações a 450 ° C
As propriedades magnéticas do como-preparado foram avaliadas usando VSM, e os resultados são mostrados na Fig. 3. O valor de saturação magnética é alcançado 53 emu / g em comparação com Fe puro 3 O 4 microesferas (67,55 emu / g). O alto valor de magnetização do material preparado pode ser visto claramente. A inserção na Fig. 3 mostra quando um campo magnético externo foi aplicado, as partículas são atraídas pelo ímã, deixando a solução aquosa límpida e transparente.
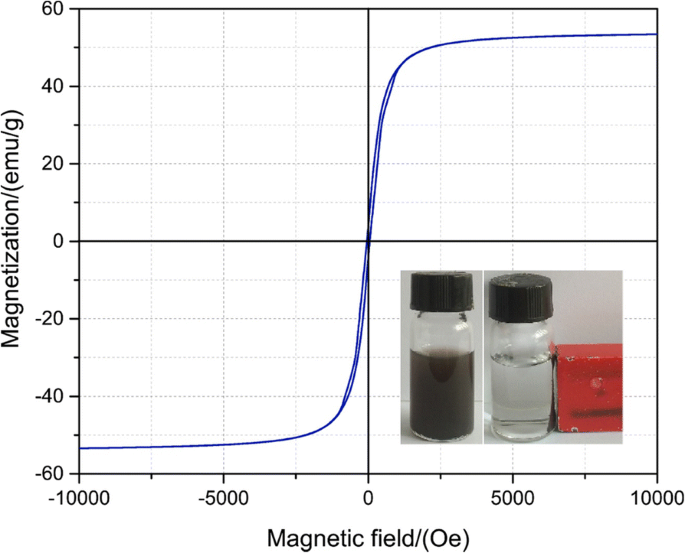
Medições de loop de magnetização
A Figura 4a exibiu a isoterma de adsorção e dessorção das amostras, enquanto a Fig. 4b mostra a distribuição do tamanho dos poros das amostras obtidas, ambas vieram de antes e depois da calcinação, respectivamente. A isoterma é uma isoterma representativa de material mesoporoso com base no tipo clássico IV. A distribuição do tamanho dos poros através da calcinação mostrou claramente os diâmetros médios dos poros de 7,5 a 9,1 nm, menores que o precursor. Enquanto isso, a área de superfície BET da amostra aumentou significativamente de 9,74 para 238,18 após calcinações, que é maior do que a maioria dos relatórios [36, 37]. O acima também indicou que o Fe 3 se absteve O 4 As amostras @C eram um material de estrutura mesoporosa solta, o que é um benefício para o desempenho de adsorção aprimorado.
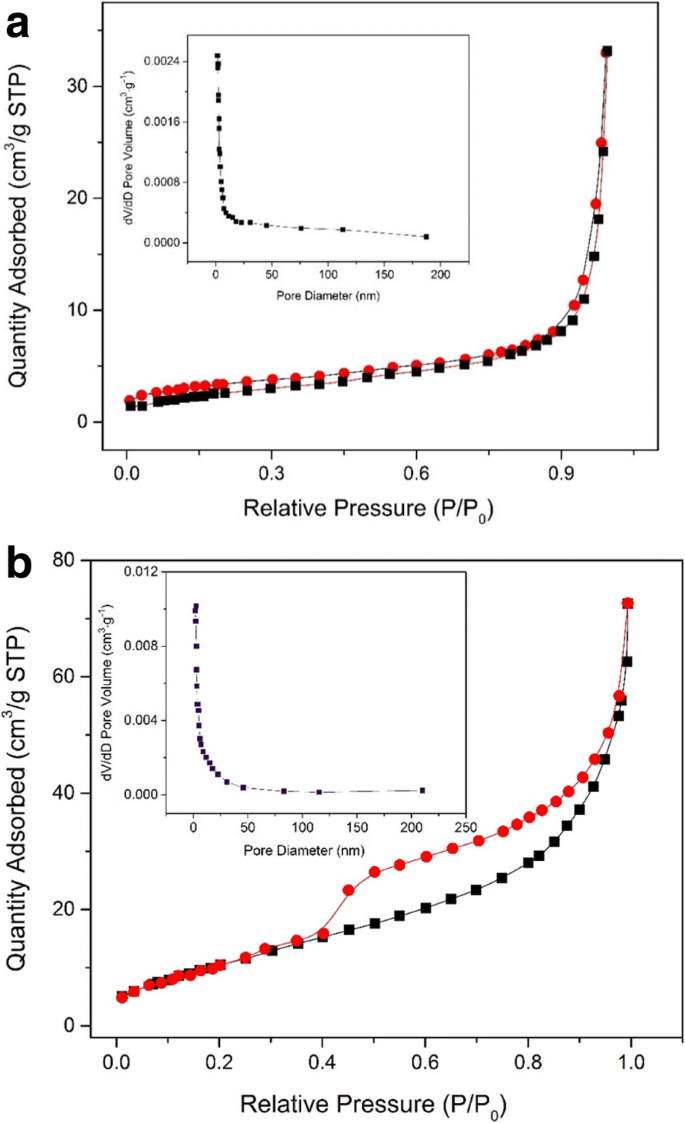
Isoterma de adsorção-dessorção de nitrogênio e gráfico de distribuição de tamanho de poro de Barrett-Joyner-Halenda (BJH) da amostra preparada antes ( a ) e depois ( b ) calcinações
Absorção de íons de heavy metal pelo Fe 3 O 4 @C
Pb (II), Cd (II), Cu (II) e Cr (VI) foram escolhidos como adsorbatos para estudar a capacidade de absorção do Fe 3 preparado O 4 @C, e eles foram colocados em pH =3 em temperatura ambiente para conduzir experimentos cinéticos. Como mostrado na Fig. 5, todos os íons de adsorção foram adsorvidos com sucesso pela amostra preparada, a eficiência alcançada em 100% para Pb (II), 99,2% para Cd (II), 96,6% para Cu (II) e 94,8% para Cr (VI), respectivamente. Possui uma aplicação mais ampla e maior eficiência de remoção do que o estudo anterior [42]. Esta alta eficiência de absorção pode ser atribuída às vantagens intrínsecas das estruturas híbridas núcleo-casca com altas áreas de superfície específicas, que forneceram o Fe 3 O 4 Amostra @C com mais sites ativos para o processo de remoção. Além disso, pode ser facilmente recuperado após a adsorção devido às estruturas de partículas submicrométricas relativamente grandes. Também pode ser facilmente percebido que o Pb (II) apresentou a maior taxa que é razoável devido à adsorção geralmente por troca iônica, e existe interação eletrostática dos íons metálicos livres e da superfície do adsorvente. Assim, Cd, Cu e Cr são desorpções leves e fáceis após a troca iônica, Pb (II) é o oposto [43,44,45,46,47,48,49].
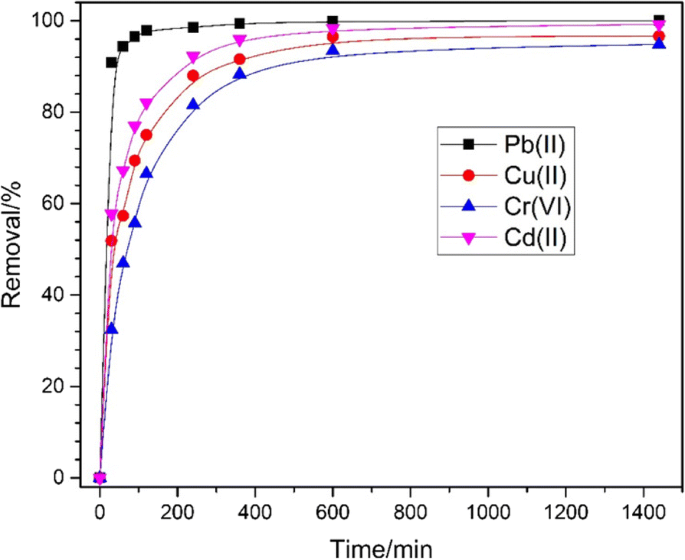
Relação entre a eficiência de remoção e o tempo de adsorção de Pb (II), Cd (II), Cu (II) e Cr (VI) pelo Fe 3 O 4 @C (400 mg L −1 ) amostra em concentrações iniciais de íons de metais pesados como 10 mg L −1 , respectivamente
Espectros FTIR do Heavy Metal Carregado com Fe 3 O 4 @C
A Figura 6 mostra a amostra com o Pb mais alto 2+ absorção no início e no final da adsorção, que foi usada no estudo para descobrir a interação entre Fe 3 O 4 @C e íons de metais pesados. Além disso, a vibração para frente e para trás do grupo −OH de H 3 O + via troca iônica ou moléculas de fisissorção de água, o que levou a uma ampla banda vibracional em 3475,26 cm −1 . O pico em 2304,20 cm −1 é atribuído à extensão de vibração de CO 2 , enquanto o pico em ca. 1625 cm −1 geralmente era causado pela curva O-H. O pico em 1605,45 cm −1 era de grupos carboxila (−C =O−). A principal contribuição dos outros picos na faixa de 400-1000 cm - 1 estava normalmente associado a ligações de metal O. A diferença da posição do pico e da intensidade do metal O no início e no final da adsorção de Pb 2+ está implicando que Pb 2+ é carregado no Fe 3 O 4 @C amostra fortemente.
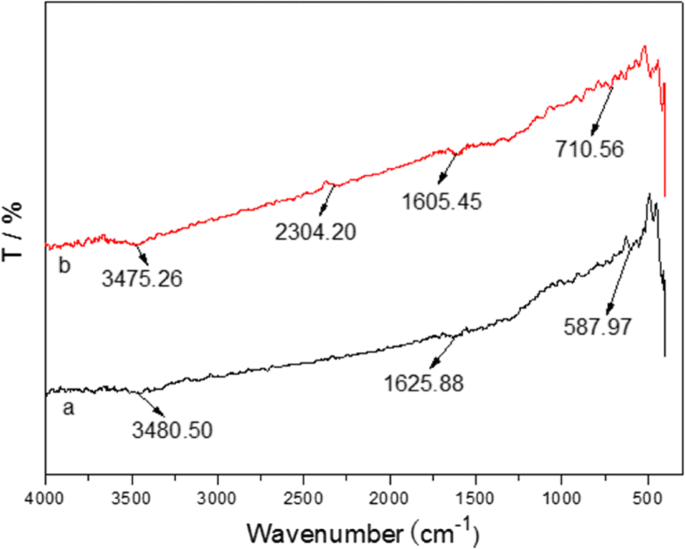
Espectros de FTIR do Fe 3 preparado O 4 Amostra @C antes ( a ) e depois ( b ) adsorção de Pb (II)
Cinética de Adsorção
Uma variedade de textos foi realizada para discutir a capacidade de adsorção e cinética do Fe 3 O 4 Agregados de nanopartículas híbridas @C nesta seção. Pb 2+ foi preparado para o experimento de remoção das soluções aquosas em pH =3. Em seguida, preparou-se o volume de 50 mL de 10, 30 e 50 mg L −1 soluções iniciais, adsorventes de 20 mg, que foram adicionados ao Pb 2+ soluções em frascos cônicos de 100 mL na adsorção de 30 ° C respectivamente. Com os diferentes períodos (0, 7, 14, 21, 28, 35, 60, 180, 480 e 1440 min), foi extraído aproximadamente 1 mL de cada solução, que será utilizada para análise de AAS. Eq. (1) mostra o modelo de taxa cinética de pseudo-segunda ordem [50]:
$$ \ frac {t} {q_t} =\ frac {1} {k_2 {q} _e ^ 2} + \ frac {1} {q_e} t $$ (1)
onde q e é Pb 2+ adsorvido por unidade de massa quando o adsorvente está em equilíbrio, q t (mg g −1 ) significa o Pb 2+ adsorvido na massa unitária durante o tempo t (min); k 2 (g mg −1 min −1 ) é a constante de velocidade do modelo cinético, que é uma pseudo-segunda ordem. A Figura 7a mostra o tempo de reação do Fe 3 O 4 Amostra @C em Pb 2+ remoção nas diferentes concentrações iniciais (10, 30 e 50 mg L −1 ), então a diferença de eficiência pode ser facilmente descoberta. O resultado indicou o Fe 3 O 4 As amostras @C expressaram desempenho de adsorção superior, além de serem facilmente separáveis. A Figura 7b descreveu a taxa de adsorção nas diferentes concentrações de Pb 2+ (10, 30 e 50 mg L −1 ) A taxa de adsorção foi negativamente relacionada com a concentração inicial. Esta tendência pode ser revelada da seguinte forma, havia apenas parte do sítio tensoativo usado durante a adsorção. Ou seja, com a concentração de Pb 2+ aumentando, a adsorção começou a partir dos locais de alta energia em primeiro lugar, seguido pelos locais de baixa energia saturados que causaram a diminuição da taxa de adsorção, finalmente [51]. A Tabela 1 mostra o coeficiente de correlação ( R 2 ) atingiu 0,999 neste estudo; indica claramente que o processo de adsorção está em conformidade com o modelo de pseudo-segunda ordem.
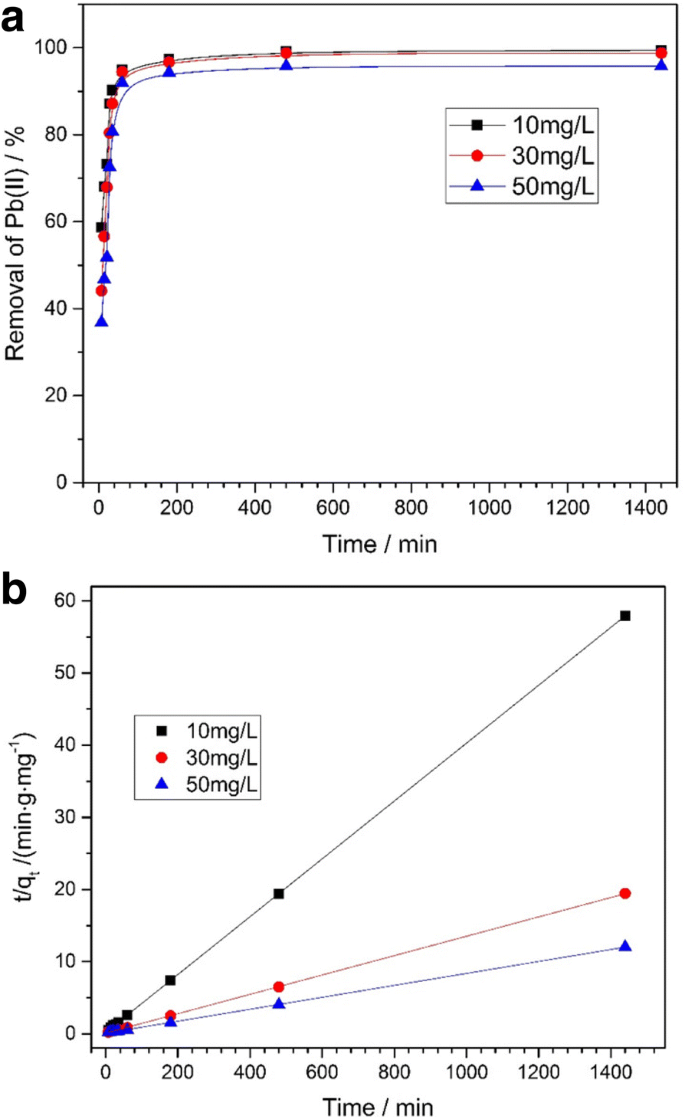
a Relação entre a eficiência de remoção e o tempo de adsorção de Pb (II) pelo Fe 3 O 4 @C (20 mg) nas concentrações iniciais de Pb2 + de 10, 30 e 50 mg L −1 , respectivamente. b Cinética de pseudo-segunda ordem para adsorção de Pb2 + no Fe 3 O 4 Amostra @C ( T =30 ° C; dose absorvente =400 mg L −1 ; Concentrações de Pb2 +: a =10 mg L −1 , b =30 mg L −1 , c =50 mg L −1 )
Isoterma de Adsorção
Nesta parte, 20 mg de adsorvente foi adicionado aos 100 mL dos frascos cônicos e Pb 2+ amostras de solução também foram preparadas (10-60 mg L −1 , 50 mL, pH =3). A 30 ° C, as amostras do frasco cônico acima foram mantidas em estado lacrado e colocadas em agitador termostático (24 h, 150 rpm) e, a seguir, por centrifugação para obtenção da solução sobrenadante medida por AAS. A Figura 8a mostra o Fe 3 preparado O 4 Capacidade de adsorção @C para Pb 2+ . As isotermas de Langmuir e Freundlich foram implementadas para explicar o curso de adsorção no estudo. O processo ocorreu em uma monocamada localizada, sem interação entre as moléculas de adsorbato [52]. Além disso, o local para a molécula de adsorvato é o primeiro a chegar, primeiro a ser servido, sem mais adsorção no mesmo local. A isoterma de Langmuir descrita a seguir:
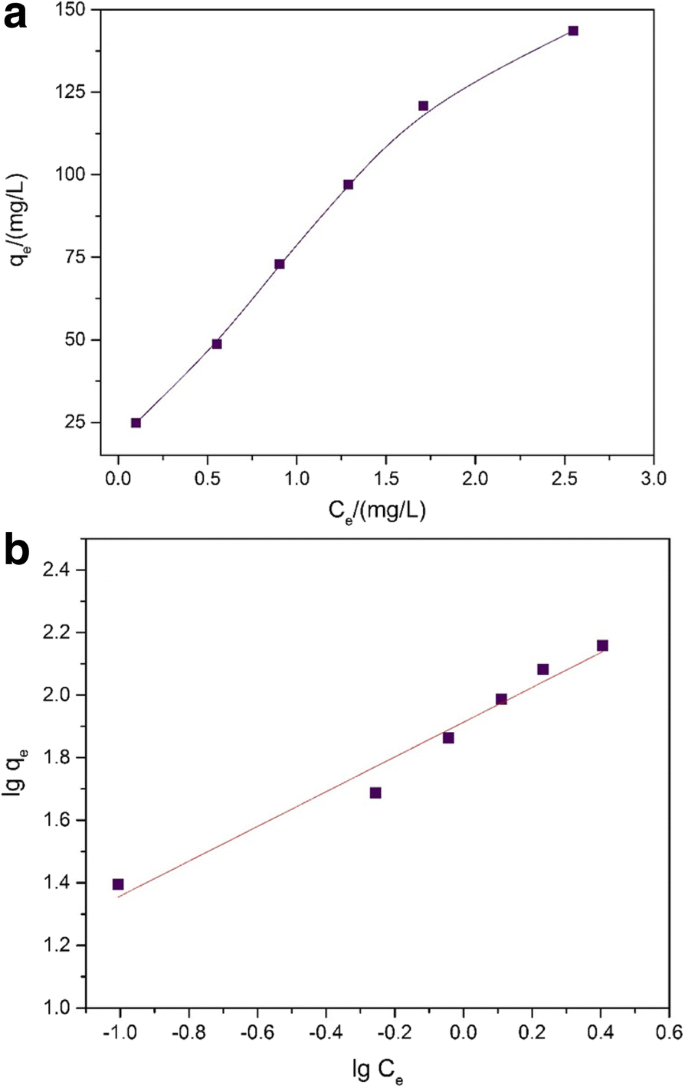
a Isoterma de adsorção para Pb2 + no Fe 3 O 4 Amostra @C ( T =30 ° C; dose adsorvente =400 mg L −1 ; Concentração de Pb2 + =10–60 mg L −1 ) b Gráficos lineares de Freundlich para isoterma de adsorção do Fe 3 O 4 @Camostra na remoção de Pb2 + a 30 ° C
$$ \ frac {C_e} {q_e} =\ frac {C_e} {q _ {\ mathrm {max}}} + \ frac {1} {k_L {q} _ {\ mathrm {max}}} $$ (2 )
onde a capacidade máxima teórica de sorção em monocamada é representada como q máximo (mg g −1 ), levando k L para expressar a constante de Langmuir (L mg −1 ), e C e é a concentração de Pb (II) inicialmente. Enquanto as isotermas de Langmuir não atingem a consequência ideal para nosso estudo, isso significa que não são bem adequadas. Correspondendo à forma linear como Eq. (3) é outro modelo empírico comum como a isoterma de Freundlich, que tem a hipótese de que, acompanhando o aumento do grau de ocupação do sítio, sítios de ligação mais resistentes são amarrados antecipadamente e sua intenção diminui correspondentemente [52].
$$ \ lg {q} _e =\ lg {k} _F + \ frac {1} {n} \ lg {C} _e $$ (3)
Aqui, k F significa a constante de Freundlich (mg g −1 ) (L mg −1 ) 1 / n , e 1 / n expressa o fator de heterogeneidade. O conteúdo específico de k F e 1 / n , identificado com um gráfico de lg q e versus lg C e , é mostrado na Fig. 8b. A Tabela 2 mostra uma condição de adsorção favorável [52, 53]. Indicou o motivo pelo qual o expoente de Freundlich n é maior que 1. Pode-se concluir que o efeito de adsorção do Pb 2+ era dependente das estruturas híbridas núcleo-casca ou heterogeneidade para as superfícies do Fe 3 O 4 Amostra @C. Nesse ínterim, R 2 , o coeficiente de correlação da amostra, chega a 0,9712, o que significa que o modelo de isoterma de Freundlich foi bem adequado para a análise de equilíbrio experimental.
Análise Termodinâmica
Considerando um sistema isolado como suposição relevante, a equação de Arrhenius (Eq. (4)) foi usada para conduzir a análise termodinâmica. Normalmente, sob algumas condições especiais do agitador termostático, a concentração original era de 30 mg L −1 e o volume de adsorção foi de 50 ml, então, foram colocados 20 mg de adsorvente nos frascos cônicos com capacidade de 100 ml e também Pb 2+ soluções em cinco condições de temperatura de classificação, incluindo 30, 40, 50, 60 e 70 ° C. No processo de adsorção, as amostras aquosas foram conduzidas amostragem após vários intervalos de tempo; durante este período, as concentrações consistentes de Pb 2+ também deveriam ser medidos com base no AAS que foi usado para analisar sua cinética de adsorção de acordo com a situação de temperatura diferente acima. Além disso, a equação de Arrhenius dada no item anterior é utilizada para avaliar a energia de ativação que foi a pré-condição para a pesquisa de adsorção.
$$ \ ln {k} _2 =1n \ kern0.5em A- \ frac {E_a} {RT} $$ (4)
Aqui, E a é a energia de ativação de Arrhenius (kJ mol −1 ) A representa o fator de Arrhenius; a constante do gás (8.314 J mol −1 K −1 ) é expresso com R , e T refere-se à temperatura absoluta (K). A inclinação correspondente é - Ea / R , com base em um gráfico de ln k 2 contra 1 / T (Fig. 9) para obter a linha reta.
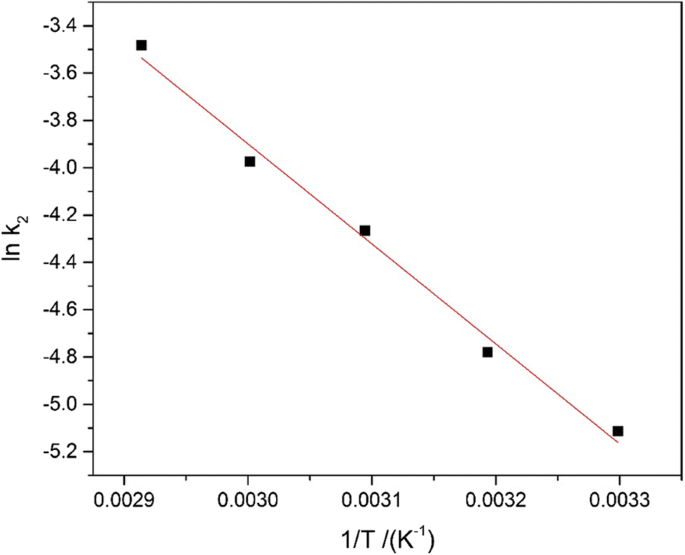
Trama de lnk2versus 1 / T para adsorção de Pb2 + no Fe 3 O 4 Amostra @C (TOC)
As dimensões da energia de ativação foram tomadas para determinar a forma de adsorção. Normalmente tendo um escopo específico (0-40 kJ mol −1 ) para a energia de ativação no processo de fisissorção [54], um intervalo maior foi necessário no processo de quimissorção, em contraste. A energia de ativação foi de 34,92 kJ mol −1 aqui. Indicou que o processo de adsorção de Pb 2+ no Fe 3 O 4 @C é classificado em fisiossorção.
Conclusões
O composto de Fe 3 revestido com núcleo O 4 Os agregados de nanopartículas híbridas @C são alcançados através da adoção de etapas pacíficas e moderadas ambientalmente baseadas no método de síntese solvotérmica e obtidas as calcinações a 450 ° C. Por meio das nanoestruturas núcleo-concha híbridas à base de carbono, um maior grau de eficiência de exposição dos locais de adsorção pode ser realizado de forma eficiente para o adsorbato quando comparado a um sólido, o que entregará propriedades de adsorção para eliminar os íons de metais pesados. Além disso, os núcleos à base de ferro fazem com que os adsorventes sejam facilmente separados das soluções aquosas. Sob este dispositivo (mais barato, menos cumplicidade e maior produtividade), uma nova abordagem é esclarecida que materiais nano / micro-funcionais do núcleo-shell podem ser bem sintetizados em grande escala que são usados em muitos campos, como remediação ambiental, catalisador, e energia.
Abreviações
- AAS:
-
Espectroscopia de absorção atômica
- BET:
-
Brunauer-Emmet-Teller
- FTIR:
-
Espectroscopia de infravermelho com transformada de Fourier
- HR-TEM:
-
Microscópio eletrônico de transmissão de alta resolução
- JCPDS:
-
Comitê Conjunto de Padrões de Difração de Pó
- SAED:
-
Difração de elétrons de área selecionada
- SEM:
-
Microscópio eletrônico de varredura
- TEM:
-
Microscopia eletrônica de transmissão
- VSM:
-
Magnetômetro de amostra vibratória
- XRD:
-
Difração de raios X
Nanomateriais
- Vodcast:OEE e gerenciamento de desempenho em tempo real
- Remoção adsortiva de íons de cobre (II) de solução aquosa usando um nanoadsorvente de magnetita de resíduos de escala de moinho:Síntese, caracterização, adsorção e modelagem cinética Estud…
- Composto Híbrido de Sílica Nanoestruturada / Ouro-Celulose Ligado Amino-POSS via Processo Sol-Gel e Suas Propriedades
- Investigações da sorção de íons de metal pesado usando nanocompósitos de biocarvão modificado com ferro
- Síntese de nanofibra de sílica condutora elétrica / nanopartícula composta de ouro por pulsos de laser e técnica de pulverização catódica
- O efeito do plasma sem equilíbrio de contato nas propriedades estruturais e magnéticas de Mn Х Fe3 - X О4 Spinels
- Síntese hidrotérmica de nanopartículas de In2O3 híbridos gêmeos heteroestruturas de ZnO de disco hexagonal para atividades fotocatalíticas aprimoradas e estabilidade
- Hidrozincita com suporte de aerogel de sílica e hidrotalcita intercalada com carbonato para remoção de alta eficiência de íons de Pb (II) por reações de transformação de precipitação
- Preparação de nanoesferas poliméricas impressas com íons de paládio (II) e sua remoção de paládio (II) da solução aquosa
- Síntese e desempenho in vitro de nanopartículas de ferro-platina revestidas com polipirrole para terapia fototérmica e imagem fotoacústica



