Progresso dos eletrocatalisadores à base de carbono para baterias flexíveis de zinco-ar nos últimos 5 anos:estratégias recentes para design, síntese e otimização de desempenho
Resumo
A crescente popularidade dos dispositivos eletrônicos vestíveis levou ao rápido desenvolvimento de sistemas flexíveis de conversão de energia. As baterias recarregáveis de zinco-ar (ZABs) flexíveis com altas densidades de energia teóricas demonstram um potencial significativo como dispositivos de energia flexível de próxima geração que podem ser aplicados em produtos eletrônicos vestíveis. O projeto de catodos altamente eficientes e estáveis ao ar que podem catalisar eletroquimicamente a reação de redução de oxigênio (ORR) e a reação de evolução de oxigênio (OER) são altamente desejáveis, mas desafiadores. Catalisadores flexíveis à base de carbono para catálise ORR / OER podem ser amplamente categorizados em dois tipos:(i) catalisadores autossustentados baseados na modificação in situ de substratos flexíveis; (ii) catalisadores não autossustentáveis baseados em revestimentos de superfície de substratos flexíveis. Os métodos usados para otimizar o desempenho catalítico incluem dopagem com átomos e regulação da estrutura eletrônica e ambiente de coordenação. Esta revisão resume as estratégias propostas mais recentemente para a síntese de eletrocatalisadores projetados à base de carbono e a otimização de seus desempenhos eletrocatalíticos em eletrodos de ar. E nos concentramos significativamente na análise dos sítios ativos inerentes e seus mecanismos eletrocatalíticos quando aplicados como catalisadores ZABs flexíveis. Os resultados desta revisão podem ajudar no projeto de eletrodos de ar baseados em carbono mais valiosos e seus ZABs flexíveis correspondentes para aplicação em dispositivos eletrônicos vestíveis.
Introdução
O atual uso excessivo de energia não renovável levantou preocupações em relação à crise energética. Portanto, para aliviar a atual escassez de energia, dispositivos de fornecimento de energia mais eficientes e ecológicos precisam ser estabelecidos. Além disso, o surgimento e popularização de dispositivos eletrônicos vestíveis extensíveis, dobráveis e dobráveis instigaram o rápido crescimento e desenvolvimento de sistemas de armazenamento de energia flexíveis [1,2,3]. As baterias de zinco-ar (ZABs) exibem uma densidade de energia teórica de 1086 Wh kg −1 , que é aproximadamente cinco vezes maior do que as baterias recarregáveis de íon de lítio amplamente utilizadas. Além disso, o zinco tem as vantagens de reservas abundantes e ampla disponibilidade [4, 5]. ZABs típicos utilizam zinco como eletrodo negativo, oxigênio como eletrodo positivo e hidróxido de potássio como eletrólito. Devido à introdução de ânodos de zinco altamente estáveis e eletrólitos à base de água, os ZABs não são tóxicos, são ecologicamente corretos e seguros e têm recebido grande atenção como sistemas promissores de armazenamento de energia [6]. O princípio básico de funcionamento dos ZABs envolve uma reação eletroquímica entre o zinco no eletrodo negativo da bateria e o OH - na solução eletrolítica, resultando na liberação de elétrons. Simultaneamente, os catalisadores no eletrodo de difusão de gás ou na camada de reação do cátodo de ar entram em contato com o eletrólito e o oxigênio do ar e, em seguida, ocorre a transferência de carga. Durante a operação de ZABs recarregáveis, a conversão entre oxigênio e água ocorre no eletrodo de ar; isso inclui o ORR e OER, ambos os quais são processos de recombinação de múltiplos elétrons. As reações específicas que ocorrem em soluções alcalinas são as seguintes:
$$ {\ text {ORR}}:\, {\ text {O}} _ {2} \ left ({\ text {g}} \ right) + 2 {\ text {H}} _ {2} { \ text {O}} \, \ left ({\ text {l}} \ right) + 4 {\ text {e}} ^ {-} \ a 4 {\ text {OH}} ^ {-} $$ (1) $$ {\ text {OER}}:\, 4 {\ text {OH}} ^ {-} \ to {\ text {O}} _ {2} \ left ({\ text {g}} \ right) + 2 {\ text {H}} _ {2} {\ text {O}} \ left ({\ text {l}} \ right) + 4 {\ text {e}} ^ {-} $ $ (2)
Vários modelos cinéticos foram desenvolvidos para compreender as vias de reação envolvidas durante a ORR. O primeiro modelo, desenvolvido por Damjanovic et al. [7, 8], envolve a formação de peróxido de hidrogênio em uma via de reação paralela àquela em que O 2 é reduzido a água sem a formação de peróxido de hidrogênio como intermediário. Isso é esquematicamente representado pela Eq. 1 e 2.
$$ {\ text {O}} _ {{2}} \ to ^ {{{\ text {I}} _ {{1}}}} {\ text {H}} _ {{2}} {\ texto {O}} $$ (1) $$ \ begin {array} {* {20} c} {{\ text {O}} _ {{2}} \ mathop {\ longrightarrow} \ limits ^ {{{ \ text {I}} _ {{2}}}} {\ text {H}} _ {{2}} {\ text {O}} _ {{2}} \ mathop {\ longrightarrow} \ limits ^ { {{\ text {I}} _ {{3}}}} {\ text {H}} _ {{2}} {\ text {O}}} \\ {\ downarrow {\ text {I}} _ {4}} \\ {{\ text {to}} \, {\ text {solução}} \, {\ text {e}} \, {\ text {anel}} \, {\ text {eletrodo}} } \\ \ end {array} $$ (2)
O peróxido de hidrogênio, formado como um intermediário de reação na via 2, é parcialmente reduzido no mesmo eletrodo de disco que a água e parcialmente transferido do eletrodo de disco para a solução e para o eletrodo de anel por difusão convectiva. I 1 , I 2 e eu 3 representam as respectivas correntes. I 4 representa a taxa na qual o peróxido de hidrogênio se difunde para longe do eletrodo do disco como uma corrente. Porém, o intermediário peróxido gerado é instável, o que pode complicar o processo de reação, danificar a membrana eletrolítica e reduzir a atividade do catalisador, bem como a tensão de saída e a taxa de conversão de energia da célula a combustível [9]. Portanto, o 4e direto - caminho (Eq. 1) é considerado o caminho ideal para o ORR, pois tem uma tensão de saída e conversão de energia mais altas do que o 2e - via (Eq. 2).
Como um potencial excessivo considerável do ORR é necessário para superar as barreiras de energia associadas à transferência de elétrons em várias etapas [10], o principal desafio enfrentado no desenvolvimento de ZABs recarregáveis flexíveis que podem ser aplicados em grande escala é o uso de cátodos de ar nas ZABs que exibem potencial excessivo [11] e reversibilidade do oxigênio pobre causada pela ORR lenta e OER durante a carga e descarga [12]. Os eletrodos Pt / C demonstram o melhor desempenho catalítico para o ORR, enquanto IrO 2 / RuO 2 demonstra um excelente desempenho catalítico no REA. No entanto, esses catalisadores também apresentam várias desvantagens, como reservas escassas, alto custo, atividade catalítica única e baixa estabilidade, que dificultam seriamente sua aplicação em larga escala [13]. Assim, o desenvolvimento de um catalisador com excelentes desempenhos catalíticos bifuncionais ORR / OER que seja acessível é vital para a comercialização de ZABs flexíveis. Metais não nobres, particularmente metais de transição, têm atraído grande atenção devido à sua alta atividade e excelente estabilidade térmica. Além disso, os catalisadores à base de carbono possuem vantagens significativas, incluindo flexibilidade estrutural, excelente condutividade elétrica, boa estabilidade química e térmica e simples funcionalização química, além de serem leves. Portanto, eles são considerados materiais candidatos promissores para uso em produtos eletrônicos vestíveis. Existem vários cátodos de ar à base de CC (tecido de carbono) excelentes; entretanto, um dos principais desafios é a identificação de materiais com excelente condutividade que podem crescer uniformemente no CC. Se os materiais crescem de forma desordenada no CC, o número de locais ativos no catalisador é reduzido. Os ZABs tradicionais usam uma solução aquosa como eletrólito, que não pode atender aos requisitos dos ZABs flexíveis de estado sólido. Assim, a maioria dos ZABs de estado sólido que exibem excelentes desempenhos usam eletrólitos em gel para conduzir eletricidade, como álcool polivinílico, óxido de polietileno (PEO), poliacrilamida (PAM) e ácido poliacrílico (PAA). Esses eletrólitos em gel são cada vez mais usados em ZABs, pois possuem forte plasticidade e boa condutividade. Especificamente, o poliacrilato de sódio é estável na aplicação prática de eletrólitos em gel à base de água, devido ao seu efeito tampão em eletrólitos alcalinos. [1]
Nos últimos anos, o número de estudos sobre ZABs flexíveis tem aumentado, fornecendo algumas bases teóricas para a produção e aplicação prática de ZABs flexíveis. Embora Zhu et al. publicou uma revisão detalhada de baterias unidimensionais [14] e Shi et al. introduziu catalisadores bifuncionais em detalhes [15], o progresso recente, particularmente nos últimos cinco anos, de ZABs flexíveis contendo catalisadores à base de carbono não foi relatado. Portanto, este trabalho resume as estratégias para a síntese de catalisadores à base de carbono e a otimização de seus desempenhos eletrocatalíticos em eletrodos de ar, com um foco significativo na análise de seus sítios ativos inerentes e seu mecanismo eletrocatalítico quando aplicados como catalisadores ZABs flexíveis.
Eletrocatalisadores à base de carbono de designer
Os materiais à base de carbono são amplamente usados em catalisadores ZABs devido às suas excelentes propriedades. Esses materiais são principalmente materiais à base de grafeno (incluindo grafeno funcionalizado e perfis de grafeno); entretanto, grafite, fulereno e nanotubos de carbono (CNTs) também são usados [16]. No entanto, os materiais à base de carbono ainda sofrem de muitos defeitos durante a aplicação prática dos ZABs. Assim, é necessário otimizar o tratamento aplicado aos materiais de carbono. Um exemplo disso são os materiais de carbono poroso dopados com N, que exibem desempenhos eletrocatalíticos bifuncionais excepcionais no ORR e OER [17, 18]. Dentre a variedade de métodos usados para modificar materiais de carbono, a dopagem com átomos únicos, como N, P e S, pode melhorar significativamente a atividade do catalisador. Diante disso, alguns pesquisadores têm utilizado a co-dopagem com N e P e constatado que o catalisador co-dopado tem excelente atividade. Além disso, outros métodos, como dopagem de metal único, dopagem bimetálica e nanomateriais, têm um efeito positivo definitivo na otimização do desempenho do catalisador de materiais de carbono. No entanto, os métodos para desenvolver eletrocatalisadores de alto desempenho para ZABs têm sido pouco explorados. Estudos têm mostrado que a modificação de materiais de carbono, como grafeno e CNTs, por meio de dopagem pode otimizar as propriedades de superfície dos materiais de carbono. A estratégia mais típica para otimizar o desempenho do catalisador é combinar nanomateriais de carbono dopados com heteroátomo com material à base de metal de transição (óxidos, calcogenetos, como sulfetos à base de Ni, etc. [19,20,21], fosfetos de metal de transição (TMP [ 22]) e compostos de nitreto). Como os eletrocatalisadores ZABs ainda apresentam inúmeras deficiências, é vital otimizar sua estrutura catalítica. Atualmente, o ajuste da estrutura eletrônica, defeitos de oxigênio, ligações metal-oxigênio, deformação de interface e dopagem atômica têm sido amplamente utilizados no projeto de catalisadores ZABs.
Desenvolvimento de catalisadores de alta eficiência em eletrodos flexíveis
O eletrodo flexível é representado pela camada de difusão de gás em ZABs flexíveis. O cátodo de ar é formado pelo crescimento direto de um catalisador de alta eficiência no eletrodo flexível, que tem as vantagens de ser autossustentável e ter uma grande área de contato do eletrodo e forte dobrabilidade. Autossustentável indica que nenhum adesivo não condutor é necessário, evitando assim a deterioração do desempenho do eletrodo e a perda do catalisador durante a deformação repetida do eletrodo. Além disso, a redução dos sítios ativos e o aumento da impedância da interface são evitados com o uso de adesivos não condutores. O crescimento do catalisador no eletrodo expansível pode ser combinado com outros métodos, como eletrodeposição, o método hidrotérmico e vulcanização à temperatura ambiente. Eletrodos flexíveis comumente usados incluem espuma de carbono dopada com nitrogênio, tecido de fibra de carbono, papel carbono e feltro de carbono, que possuem excelente condutividade elétrica.
Crescimento de catalisadores de alta eficiência em tecido de fibra de carbono
O pano de fibra de carbono, um tecido feito de fibras de carbono, é o material de substrato flexível mais comumente usado. O cultivo de catalisadores de alta eficiência diretamente em tecido de fibra de carbono é um método simples e eficaz, que pode ser obtido por meio de reações de solução (Fig. 1a-c), eletrodeposição e uma combinação de outros métodos, como espaço confinado, tratamento térmico [2] (Fig. 1d, e), carbonização-oxidação CC e calcinação assistida por ligante (preparação de um CoO X ultrafino camada [23]). Um exemplo de carbonização-oxidação inclui o crescimento de diferentes estruturas de cristais, morfologias e tamanhos de partícula de MOFs 3D e 2D à base de cobalto em CC para a preparação de um cátodo livre de aglutinante, seguido pela ancoragem do Co 3 O 4 nanopartículas em nanomatrizes de carbono dopados com nitrogênio [24]. A rede de nanofibras está enraizada no CC em uma atmosfera de nitrogênio para obter um cátodo de ar bifuncional com um excelente desempenho catalítico e notável flexibilidade [25]. Embora o método de eletrodeposição tenha sido amplamente utilizado para preparar materiais de eletrodo, devido à condutividade inerentemente pobre de Co 3 O 4 , os métodos convencionais de eletrodeposição apresentam limitações na formação de um Co 3 O 4 camada com uma grande área de contato em uma portadora condutiva. Co 3 O 4 pode ser cultivado in situ no tecido de fibra de carbono para formar um Co 3 ultrafino crescido uniformemente O 4 camada. Em particular, o ultrafino Co 3 O 4 as camadas possuem uma área de contato máxima no suporte condutor, facilitando o transporte rápido de elétrons e evitando a agregação das camadas ultrafinas durante o processo de preparação do eletrodo [26]. Além disso, Co 3 O 4 pode ser convertido em um nano-microarray com uma estrutura em camadas [24], conforme ilustrado na Fig. 1f. Esta camada ultrafina de óxido de cobalto também pode ser usada como um eletrocatalisador em ZABs [23], conforme ilustrado na Fig. 1g.
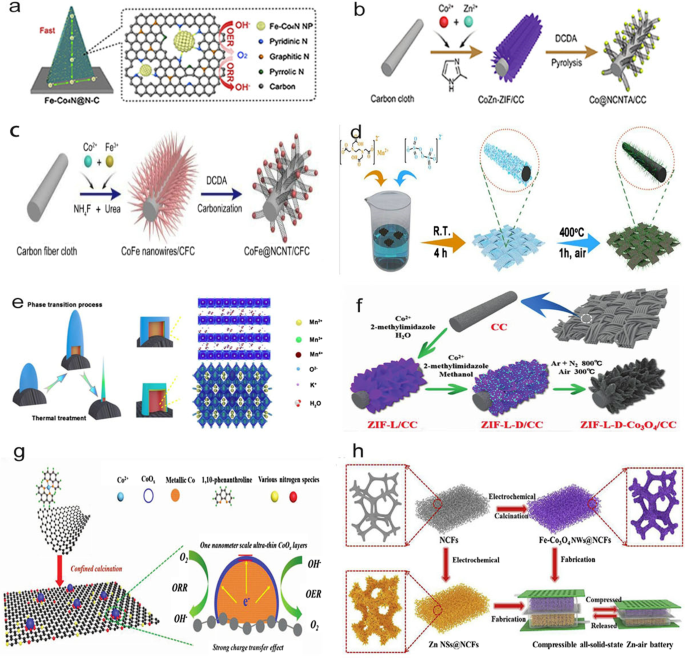
a Esquema do Fe-Co 4 Nanofolha N @ N – C crescida em CC para aplicação na reação bifuncional de oxigênio [56]. b Esquema que descreve o processo sintético para Co @ NCNTAs [85]. c Esquema do processo de síntese para CoFe @ NCNT / CFC [98]. d Esquema da preparação de MnO x -CC-400 [2]. e Proposta de transição de fase de óxido de manganês em CC via tratamento térmico [2]. f Esquema do ZIF-L-D-Co 3 O 4 / Processo de formação do CC [24]. g Esquema de um 1 nm-CoO x camada sobre o substrato metálico de Co / N-RGO [23]. h Esquema dos processos de fabricação para os ZABs de estado sólido compressíveis e recarregáveis [27]
Crescimento de catalisadores eficientes em materiais de espuma feitos pelo próprio
Os materiais de espuma feitos pelo próprio se referem principalmente a espuma de carbono e espuma de níquel. Pan et al. usou uma esponja de melamina recozida a uma temperatura de 800 ° C para formar um material de espuma de carbono flexível, que foi então usado como um eletrodo de trabalho para eletrodepositar o precursor de Fe-Co 3 O 4 NWS @ NCFs por meio de um método de eletrodeposição escalonável. Consequentemente, o material de espuma de carbono flexível pode ser aplicado em baterias de esponja totalmente sólidas [27], como mostrado na Fig. 1h. O material de espuma de níquel é um tipo de esponja de metal reticulada. Jiang et al. indicaram que o crescimento de eletrodos de catalisador in situ em um substrato flexível causaria desordem e formaria áreas irregulares densas, o que reduziria a atividade catalítica. Portanto, eles construíram um arranjo multidimensional ordenado de CNTs 1D decorado com nanopartículas de cobalto 0D (chamadas MPZ-CC @ CNT) e nano-cristas de carbono 2D em um material de espuma de níquel. Durante a pirólise da estrutura de coordenação bimetálica 2D ZnCo, os CNTs contendo um alto teor de N-doping foram cultivados in situ a partir do cobalto altamente disperso, formando assim um arranjo aberto e ordenado [28], conforme ilustrado na Fig. 2a.
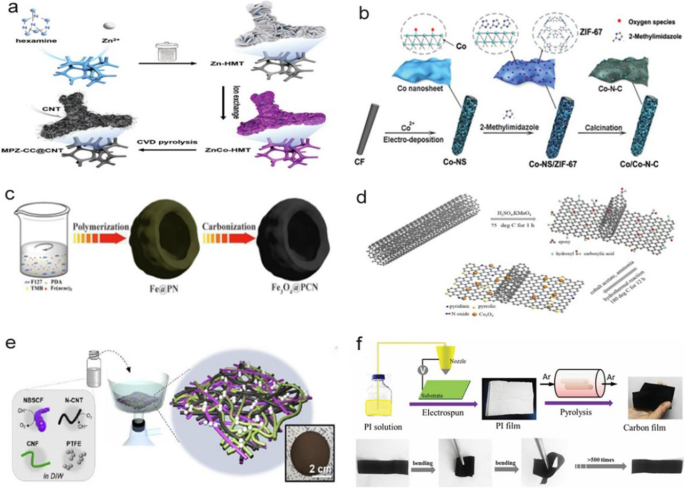
a Esquema do processo de preparação para MPZ-CC @ CNT [28]. b Síntese do catalisador Co / Co – N-C [29]. c Esquema da preparação do Fe 3 O 4 Catalisadores @PCN [40]. d Esquema que descreve o Co 3 O 4 / Síntese de catalisador composto N-p-MCNTs [41]. e Esquema do procedimento de fabricação do cátodo de ar de papel MH, juntamente com sua fotografia [43]. f Representação esquemática do procedimento de fabricação para o NCNF e fotografias do NCNF flexível resultante [44]
Síntese de catalisadores de alta eficiência em feltro de carbono
O feltro de carbono é um tecido não tecido. Yu et al. [29] desenvolveram uma nova estratégia para sintetizar nanofolhas de Co-N-C suportadas em feltro de carbono (Co / Co-N-C), contendo nano-ilhas de Co com uma estrutura em camadas 3D, conforme ilustrado na Fig. 2b. Esta estrutura incomum resulta em um bom contato entre as nano-ilhas Co e as nanofolhas Co – N-C. Além disso, a coexistência de Co 0 e Co 2+ melhorou o desempenho eletrocatalítico do catalisador bifuncional (ORR / OER). Portanto, a estrutura em camadas única geral pode promover ainda mais o transporte eficaz de elétrons / íons em ORR e OER [29]. Além de crescer nanoeletrodos 3D em feltro de carbono, uma camada de óxido de cobalto ultrafina (CoOx) em nanoescala também pode ser fabricada em feltro de carbono (isto é, um substrato de grafeno dopado com Co / N de metal) [23]. Essa estrutura ultrafina oferece condições favoráveis para aplicação em ZABs.
Síntese de catalisadores de alta eficiência em papel carbono
O papel de fibra de carbono (CFP) é composto de fibra de carbono e produzido por meio do processo de fabricação de papel. O CFP pode ser usado para melhorar o desempenho de ORR e OER de eletrocatalisadores não metálicos, como g- C 3 N 4 . G-C 3 N 4 tem um alto conteúdo de nitrogênio e pode, portanto, fornecer um número suficiente de sítios ativos para reações eletrocatalíticas e reduzir o potencial de ORR [30]. No entanto, seu desempenho eletrocatalítico é significativamente limitado devido à sua não condutividade levando a uma baixa capacidade de transferência de elétrons [30]. G-C 3 N 4 com diferentes morfologias podem ser preparadas usando diferentes métodos de tratamento térmico [30]. Os desempenhos de ORR e OER do catalisador podem ser otimizados pela aplicação de tratamentos a g-C 3 N 4 , como 1) sintetizar um catalisador de alta eficiência usando g-C 3 N 4 como um modelo [31, 32], 2) aplicando um g-C 3 N 4 estratégia de pirólise assistida [33,34,35], ou 3) introdução de g-C 3 N 4 em carbono. G-C dopado com fósforo 3 N 4 pode crescer diretamente em CFP, que pode ser projetado como um eletrodo de oxigênio flexível. Este é o primeiro eletrocatalisador bifuncional ORR / OER não metálico formado pela combinação de Pg-C semelhante a uma flor 3 N 4 composto de nanofolhas finas de g-C 3 N 4 e CFP. O eletrocatalisador contém uma rede híbrida 3D com um alto conteúdo de N e uma grande quantidade de P-doping, que produz uma excelente atividade e durabilidade de ORR e OER [36], e um bom desempenho de carga e descarga, mesmo no caso de deformação por flexão .
Síntese de catalisadores de alta eficiência em espaços confinados
A síntese de catalisadores de alta eficiência em espaços confinados pode aumentar a eficiência de dopagem, reduzir a perda de calor e aumentar as propriedades mesoporosas, melhorando assim seu desempenho de ORR. Os espaços confinados podem ser nanocanais de peneira molecular, como montmorilonita, 2-4-6 tripiridil triazina, CNTs, nanofolhas de carbono e camadas de carbono dopadas. Numerosos experimentos também demonstraram que os catalisadores preparados em espaços confinados exibem um efeito catalítico melhorado. Elementos de transição de dopagem e elementos não metálicos em espaços confinados podem aumentar significativamente a eficiência catalítica. Foram relatados co-dopagem N e S [13], co-dopagem N e P [12], dopagem bidimensional com nitrogênio [37, 38], etc. Além disso, foi estabelecido que, se uma estratégia assistida por plasma for usada para dopagem em um espaço confinado, o efeito de corrosão do plasma pode conferir porosidade ao espaço confinado, expondo assim mais locais ativos, o que é favorável a longo prazo durabilidade e transporte efetivo de elétrons do eletrocatalisador [39]. Zhang et al. usou um método de membrana macia para preparar Fe 3 O 4 envolto em uma nano-tigela de carbono poroso, demonstrando excelente desempenho catalítico e durabilidade de longo prazo [40], como mostrado na Fig. 2c. O Co 3 O 4 nanopartículas foram ancoradas nos CNTs parcialmente esfoliados de paredes múltiplas dopados com nitrogênio, resultando em um excelente desempenho catalítico [41], conforme mostrado na Fig. 2d.
Combinação de catalisadores flexíveis de alta eficiência
Um catalisador combinado compreende um único catalisador funcional composto do mesmo material em diferentes formas ou um catalisador bifuncional composto de diferentes materiais. Xu et al. alcançou um catodo de ar ORR de função única ao projetar folhas de CNT alinhadas, cruzadas e porosas, em que as folhas de CNT funcionavam como uma camada de difusão de gás, uma camada de catalisador e um coletor de corrente e sintetizavam um novo ZABs fibroso, flexível e extensível [42]. O catalisador de catodo de ar em ZABs flexíveis exibe tipicamente atividade catalítica ORR / OER insuficiente e requer condições de síntese severas, incluindo altas temperaturas / altas pressões e soluções ácidas (ou alcalinas). Além dos problemas dos catalisadores de ar bifuncionais, as propriedades mecânicas do cátodo de ar dependem fortemente das propriedades mecânicas de seu substrato, resultando em uma falta de diversidade de formas e deformabilidade na folha de cátodo de ar. Com base nisso, Lee et al. usou um catalisador flexível combinado de alta eficiência para o OER e CNTs dopados com nitrogênio para o ORR [43], como mostrado na Fig. 2e. O cátodo de ar de papel hetero-nano-tapete monolítico compreende uma mistura de catalisador bifuncional 1D, nanofibras de celulose e nanopartículas de politetrafluoroetileno, sem a necessidade de coletores de corrente convencionais e camadas de difusão de gás [43]. Zhang et al. sintetizou um novo tipo de NiCo 2 O 4 / Eletrocatalisador bifuncional de nano-malha de carbono dopado com N composto de NiCo 2 oco O 4 nanoesferas e nano-mesh de carbono dopado com N [40]. O eletrocatalisador bifuncional foi sintetizado através de uma síntese em fase líquida e posteriormente tratado termicamente, após o qual foi montado em uma bateria.
Filme de cátodo flexível caseiro
Liu et al. preparou um filme de nanofibra de carbono nanoporoso (NCNF) por pirólise de um filme de poliimida eletrofiado (PI) sob uma atmosfera de Ar. Conforme mostrado na Fig. 2f, o NCNF possui flexibilidade e alta resistência mecânica e à tração. A resistência à tração do NCNF é de 1,89 MPa e o módulo de tração é de 0,31 GPa. NCNF exibe uma estrutura de rede de carbono nanoporosa 3D e uma grande área de superfície específica, que pode fornecer caminhos curtos e rápidos de elétrons / íons e canais de difusão de gás abundantes. Mais importante, o projeto do eletrodo também tem as vantagens de eliminar aglutinantes de polímero e simplificar o processo de fabricação, minimizando o tamanho e o custo da bateria. Os ZABs recarregáveis totalmente sólidos flexíveis contendo o cátodo de ar NCNF exibem uma alta tensão de descarga (~ 1,0 V @ 2 mA cm −2 ), baixa tensão de carga (~ 1,8 V @ 2 mA cm −2 ), alta densidade de energia de 378 Wh kg −1 e excelente estabilidade mecânica e cíclica. Esses resultados sugerem a possibilidade de aplicações em larga escala dos ZABs [44].
Estratégias de otimização para desempenho do catalisador ZABs
Nos últimos anos, a pesquisa sobre eletrocatalisadores baratos e altamente eficientes para ORR e OER se desenvolveu rapidamente. Embora existam muitas controvérsias a respeito do processo catalítico específico que ocorre durante a eletrocatálise, é certo que um maior número de sítios ativos eficazes no catalisador leva a uma melhor atividade catalítica. No processo de otimização do desempenho dos catalisadores ZABs, a dopagem atômica sobre o carbono pode levar à sinergia e defeitos estruturais, bem como ao ajuste da estrutura eletrônica, ambiente de coordenação e estrutura do catalisador. Portanto, o efeito eletrocatalítico do catalisador pode ser melhorado dopando os materiais de carbono com átomos específicos. A dopagem atômica pode ser categorizada em dopagem com um único átomo e dopagem com vários átomos, em que os átomos podem ser átomos de metal ou heteroátomos. Tanto a dopagem de átomo único quanto a dopagem de vários átomos podem melhorar o desempenho eletrocatalítico do catalisador.
Dopagem atômica
Por meio da análise composicional e do cálculo da teoria funcional da densidade, Yu et al. estabeleceu que o N-doping pode efetivamente melhorar a condutividade e a capacidade de absorção de oxigênio do catalisador; entretanto, o N-doping excessivo causa uma diminuição na cinética da reação [45]. Efeito sinérgico e defeitos estruturais podem ser alcançados por dopagem de heteroátomo.
Dopagem de átomo único
Heteroátomos (N, P, S, etc.) e metais (Fe, Co, Mn, etc.) podem ser usados para dopagem de átomo único. Entre eles, o N-dopagem é o dopagem de átomo único mais comumente usado no carbono. O N-doping pode aumentar a eficiência de transporte de elétrons e a força de adsorção de oxigênio, bem como melhorar a cinética de reação do catalisador, resultando em defeitos e exposição de locais mais ativos. Por exemplo, Yu et al. demonstrou que N-doping pode melhorar significativamente a condutividade eletrônica e O 2 capacidade de adsorção de Co 3 O 4 nanofios através de investigações experimentais e cálculos da teoria funcional da densidade (DFT) [45]. Devido à lacuna entre as folhas, metais de transição, como Co [5], Ni, Mn [46, 47] (como mostrado na Fig. 3b, c), Fe e Cu, podem ser dopados em materiais de substrato ativo, como como materiais de carbono (grafeno, CNTs, etc.). Também foi confirmado que os heteroátomos 2D exibindo estruturas únicas e propriedades físicas e químicas, como N, P, S [22, 48] e B [49,50,51,52,53,54] (como mostrado na Fig. 3d, e), pode melhorar os desempenhos eletroquímico e eletrocatalítico dos catalisadores.
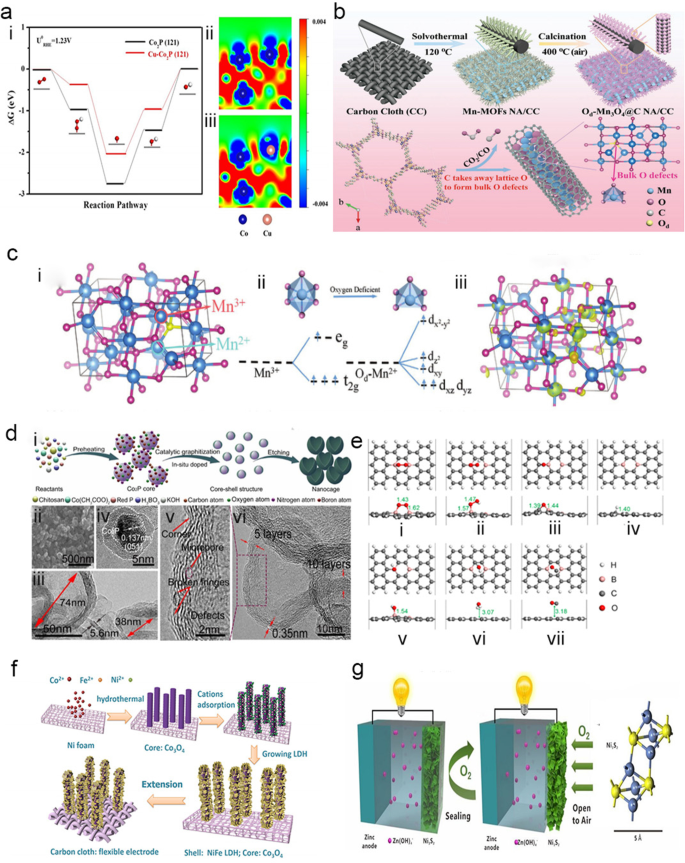
a (i) Diagrama de energia livre do ORR sobre Co 2 Co dopado com P e Cu 2 Superfícies P. As diferentes densidades de carga de (ii) Co 2 P (121) e (iii) Co dopado com Cu 2 P (121). As regiões azul e vermelha separadamente indicam o esgotamento e o acúmulo de elétrons [22]. b Ilustração do procedimento de síntese do Od-Mn 3 O 4 @ Nanoestrutura CNA / CC e seus mecanismos de formação em escala atômica. As esferas azul, rosa, cinza e amarela representam os átomos Mn, O, C e Od, respectivamente [46]. c (i) Modelo Supercell de Mn 3 O 4 . (ii) Mn-O octaédricos e campos de cristal piramidal e as configurações de divisão orbital d. (iii) Diferenças de densidade de elétrons de Od-Mn 3 O 4 (o círculo rosa representa Mn 3+ , o círculo azul celeste representa Mn 2+ ) [47]. d Síntese e caracterização morfológica de NB-CN [52]. (i) Ilustração do mecanismo de formação da nanocage de carbono grafítico. (ii) imagem SEM e (iii) imagem TEM de NB-CN. (iv) imagem HR-TEM de NB-CN antes da lavagem com ácido e (v) imagem HR-TEM de NB-CN. e Estruturas de adsorção otimizadas dos intermediários ORR e CO no BGNR [54]:(i) O 2 , (ii) OOH, (iii) O, (iv) H, (v) OH, (vi) H 2 O e (vii) CO. f Diagrama esquemático do processo de síntese do Co 3 O 4 Matrizes de nanofios híbridos @NiFe LDH em espuma de Ni e tecido de carbono flexível, respectivamente [24]. g Ilustração esquemática de Zn- Ni 3 S 2 bateria e bateria de zinco-ar e diagrama de estrutura de Ni 3 S 2 molecular, respectivamente [23]
Dopagem multi-átomo
Dopagem multi-átomo inclui co-dopagem de heteroátomo (NS, NP, NB, etc.), e heteroátomo e co-dopagem de metal [55] (Fe-Co-N [56], Mn-N [57], Fe- N [58], Co-Fe-NP [12], Co-Fe-N [39], Co-Mn-NP [59], Co-Cu-N [60, 61], Co-Cu-P, etc. .). Por outro lado, a dopagem com heteroátomo pode efetivamente gerar efeitos de defeito sinérgico no catalisador, levando a uma maior atividade catalítica [62, 63]. Por outro lado, foi confirmado que a co-dopagem com átomos e heteroátomos de metais de transição pode efetivamente melhorar o desempenho de redução de oxigênio do catalisador [64, 65]. Além disso, existe um efeito sinérgico entre multi-metais e heteroátomos que aumenta a atividade eletrocatalítica do catalisador. Os multi-metais podem melhorar a condutividade e o estado de oxidação do catalisador, aumentando assim a quantidade de transferência de carga do catalisador [66] e o desempenho eletrocatalítico do catalisador [60]. Por exemplo, Diao et al. estabeleceu através do DFT que o dopagem com Cu pode levar a locais mais positivos adjacentes ao Co e enfraquecer a força de ligação entre os locais ativos de superfície e os intermediários adsorvidos, aumentando assim as taxas de transferência de massa e carga e a exposição dos locais ativos [61]. Conforme mostrado na Fig. 3a, em Co dopado com Cu 2 P, a depleção clara de elétrons ocorre nos sítios de Co vizinhos aos átomos de Cu, indicando que o dopagem de Cu pode alterar a distribuição de elétrons de Co 2 P [22].
Efeito sinérgico
Um efeito sinérgico na catálise pode ser definido como um aumento significativo na atividade catalítica quando vários elementos (metais ou não metais) ou compostos são combinados, em comparação com quando esses elementos ou compostos são usados por conta própria. O efeito sinérgico pode auxiliar na regulação da estrutura eletrônica do substrato do catalisador, aumentando a atividade eletrocatalítica [37, 67], e pode produzir uma forte coordenação para produzir mais sítios ativos [56]. Esta colaboração pode ser classificada nas seguintes categorias:
-
Os grupos metal / não metal altamente ativos experimentam sinergismo com os substratos de carbono / nitrogênio dopados condutores. Um exemplo desta categoria são compostos de metal-nitrogênio-carbono (M – N-C) [68,69,70], como compostos Co – N-C. Sítios ativos Co – N-C podem existir na interface entre Co e o carbono dopado com N, o que pode facilitar a formação / deposição de O *. Além disso, foi demonstrado que o Co-N x sítios e o N embutido na matriz de carbono são sítios ativos em catalisadores híbridos ORR de metal não nobre [68]. Outros exemplos incluem metais de transição (Co e Fe) em carbono dopado com N [39, 71, 72], piridina-N [58], grafitização-N [71], espécies Co-azo [71], N, P co- materiais dopados, nanofibras de carbono heteroporosas dopadas com N em camadas que possuem excelentes caminhos de transporte de elétrons e uma área de superfície específica elevada [10] e nanocompósitos de grafeno. Nanocompósitos de grafeno foram sintetizados através do crescimento hidrotérmico in situ de CoSe e nanopartículas de seleneto de níquel em nanofolhas de grafeno (GNs). O efeito sinérgico entre as nanopartículas compostas e o grafeno aumenta o desempenho eletroquímico do catalisador [73, 74]. Mais importante ainda, foi provado que a forte coordenação entre o centro de metal e piridina-N pode promover a formação de sítios ativos de piridina-NM, e a piridina-N rica em elétrons pode efetivamente acelerar a transferência de carga para o centro de metal, desse modo melhorando significativamente a atividade ORR [75, 76].
-
A sinergia entre os metais confere aos catalisadores um efeito de liga que ajusta a estrutura eletrônica do sistema e otimiza a combinação de oxigênio [74, 77]. O efeito sinérgico dos sítios ativos bimetálicos na eletrocatálise de oxigênio foi previamente estudado. Para o NiCo 2 S 4 @ g-C 3 N 4 Eletrodo flexível integrado -CNT, elétrons são transferidos do sítio ativo bimetálico de Ni / Co para a abundante piridina-N em g-C 3 N 4 e coopere com o CNT condutor acoplado para promover a eletrocatálise reversível de oxigênio. Cálculos teóricos indicam que as espécies de piridina metal-N (Ni, Co-N 2 ) tem um efeito de coativação único no átomo bimetálico de Ni / Co. Reduz o centro da banda d e facilita a adsorção / dessorção de intermediários de oxigênio, acelerando assim a cinética da reação. Em um Fe-O co-dopado 4 Matriz de nanofolhas N @ NC, o centro de metal pode gerar um forte efeito de coordenação com a piridina-N, e a co-dopagem com Fe e N promove significativamente a formação de um grande número de sítios ativos de piridina-NM no ORR [78,79 , 80,81]. Em Co poroso hibridizado 3 O 4 ancorado em MnO 2 , Co e Mn geram um efeito de acoplamento, acelerando assim a taxa de transporte de elétrons, formando uma zona tampão e acelerando a separação dos produtos de superfície do catalisador [82]. Outro exemplo são as GNs dopadas com N-dopadas com Cu e Co-modificadas com nanopartículas de Co [60]. Além disso, a excelente atividade eletrocatalítica de Co 2 P @ CNF pode ser explicado pela forte interação entre o Co 2 Nanocristais de P e o revestimento de carbono poroso co-dopado com CoNx e N e P, resultando em um transporte de carga interfacial aprimorado e regulação do Co 2 Atividade eletrocatalítica de P [83]. Um novo MoSe 2D 2 -Ni (OH) 2 o material também foi preparado por meio de uma síntese hidrotérmica simples de uma etapa. O MoSe 2D 2 -Ni (OH) 2 nanohíbrido, com uma estrutura de nano folha de orientação vertical única, fornece uma grande quantidade de área de superfície específica eletroativa, encurtando o comprimento de difusão dos íons de eletrólito e, portanto, melhorando a cinética da reação eletroquímica [84].
Defeitos estruturais
Defeitos, incluindo distorção de rede, listras quebradas e locais de borda nos cantos, são considerados como tendo um efeito positivo na atividade catalítica. Foi estabelecido que defeitos nas bordas da GD (grafeno defeituoso) podem reduzir as mudanças de energia livre da ORR e REA, melhorando assim a atividade catalítica e a condutividade da GD [85]. Por exemplo, a introdução de átomos de P na matriz de carbono dopada com N pode produzir efetivamente um efeito de defeito sinérgico e estrutura N-P, otimizando assim o desempenho catalítico no OER e no ORR [12]. Enquanto isso, H 2 [86] e o condicionamento por plasma Ar também podem ser usados para formar materiais com estruturas de defeitos ricos.
Ajustando a estrutura eletrônica e o ambiente de coordenação
Com relação à estrutura eletrônica do catalisador, tem sido amplamente estimado que a distribuição de carga superficial do catalisador pode ser ajustada pela introdução de defeitos, como cátions heterometálicos dopados. Os defeitos, incluindo vacâncias de oxigênio (VO) [77], podem aumentar o número de sítios ativos catalíticos ou fornecer ao catalisador nova atividade catalítica [87]. VO pode ser alcançado por condicionamento de plasma Ar [88]. Em meios alcalinos, um catalisador ORR eficiente deve ser capaz de reduzir completamente o oxigênio a hidróxido através do processo de redução de quatro elétrons, enquanto um catalisador ORR mais fraco termina a sequência de reação no meio do processo de transferência de dois elétrons. Por exemplo, Lian et al. provou que uma configuração orbital 3D do centro metálico promove o ORR ajustando o estado de oxidação e o estado eletrônico do centro metálico. Além disso, a coordenação local pode acelerar ainda mais a taxa de conversão das substâncias redox alvo [10]. Os átomos de co também têm excelente atividade devido aos seus diferentes estados de valência possíveis. Co 2+ e Co 3+ ocupar os sítios tetraédricos e octaédricos de Co 3 O 4 , respectivamente, o que auxilia na promoção da transferência de elétrons no OER [11]. Além disso, a deposição de hidróxidos duplos em camadas de NiFe ultrafinos (LDHs de NiFe) na superfície de Co 3 O 4 pode ajustar a valência química de superfície de Co, Ni e Fe alterando o efeito do doador de elétrons e / ou absorção de elétrons, resultando no equilíbrio e na otimização do desempenho de ORR e REA [89], como mostrado na Fig. 3f.
Aumentando o número de estruturas de poros
Materiais nanoestruturados possuem estruturas de poros ricas e grande número de canais mesoporosos, que desempenham um papel vital na modificação dos canais de transmissão de oxigênio [11], estendendo o tempo de captura das moléculas de oxigênio e aumentando sua interação com os sítios ativos catalíticos. Alguns materiais nanoestruturados exibem uma estrutura 2D / 3D [90], que possui uma área de superfície específica maior e aumenta o número de interfaces trifásicas. Por design racional, um material poroso nanoestruturado com uma grande área de superfície e alta condutividade pode ser construído para garantir que mais nanopartículas estejam em contato direto com o eletrólito, resultando em uma menor resistência entre o material ativo e o eletrólito [83]. Uma estrutura de poros rica pode acelerar a transferência de carga e a difusão entre as cargas e aumentar a transferência de massa, melhorando assim o desempenho do catalisador [11, 39]. As superfícies de materiais nanoestruturados têm um baixo índice de refração estável e podem exibir energias de adsorção de oxigênio semelhantes à superfície de Pt [91]. Esse recurso faz parte das condições necessárias para o desempenho catalítico altamente eficiente do catalisador. Materiais nanoestruturados que podem ser usados como cátodo de ar de ZABs incluem Ni 3 Nanofolhas C / NC (2D), Ni 3 S 2 / Matrizes de nanofolhas de Ni [1] (como mostrado na Fig. 3g), Co poroso uniforme 3 O 4 nanopartículas / nanofolhas [11, 45], CNTs dopados com N (geralmente usados como um substrato ativo), NiCo oco 2 O 4 nanoesferas, CNTs dopados com N [92] e MoSe 2 / G nano-híbridos [93].
Ajustando a estrutura do catalisador
Um catalisador com uma estrutura razoável é necessário para catalisar uma reação. Os óxidos de metal de transição com uma estrutura espinélica podem ajudar a reduzir os sobrepotenciais, melhorando assim a eficiência de conversão de energia do catalisador [82, 94]. A estrutura 2D / 3D do catalisador pode resultar em uma excelente atividade catalítica devido à área de contato ampliada entre o sítio ativo e o eletrólito. Por exemplo, flores nanoporosas Co-dopadas com NiO, nas quais o efeito sinérgico entre a estrutura hexagonal 2D e um grande número de nanoporos no lado da nanofolha aumenta o número de sítios ativos catalíticos eficazes para O 2 adsorção / difusão [5]; e a estrutura única do sistema Co / Co-NC em camadas 3D que pode fornecer um número eficiente de sites ativos [29]. Outros exemplos incluem um novo material composto de pontos quânticos dopado com grafeno / hidrogênio / B que tem uma estrutura 3D única, alta porosidade e grande área de superfície específica, que exibe uma abundância de locais cataliticamente ativos e transporte de massa de eletrólito aprimorado e difusão de íons [95], e um Co-MOF 2D que é desenvolvido diretamente em CC, fornecendo ao crescimento de 3D Co-MOF espaço suficiente para formar uma estrutura de sistema MOF 3D em 2D em camadas. Em comparação com um MOF exclusivamente 3D ou 2D, locais mais cataliticamente ativos são expostos [24]. Além disso, a estrutura 3D facilita a penetração total do eletrólito e promove o transporte de elétrons na estrutura da rede porosa [41]. Além disso, a miniaturização do volume do material catalítico também pode melhorar a eficiência catalítica. Por exemplo, em escala atômica, um CoO ultrafino x camada acelera efetivamente a condução de elétrons e fornece locais ativos abundantes. Isso se deve à introdução da oxidação de Co nas nanofolhas, que podem aumentar o número de centros ativos expostos [23]. Outro exemplo inclui um 2D La (OH) 3 -grafeno nanohíbrido, preparado por uma técnica de redução solvotérmica simples e econômica, que é eletrostaticamente ancorado em GNs 2D para evitar a agregação de hidróxido de lantânio e fornecer vários centros eletroativos para a reação [96].
Conclusões e perspectivas futuras
Embora a pesquisa atual sobre ZABs tenha feito algum progresso substancial, ainda existem grandes desafios, incluindo o desenvolvimento de novos métodos para sintetizar catodos flexíveis autossuficientes, explorando mecanismos eletrocatalíticos e identificando materiais adequados para sintetizar catodos flexíveis com excelente desempenho catalítico. Como um dos materiais catalisadores importantes para ZABs, os catalisadores à base de carbono têm atraído atenção significativa devido à sua grande área de superfície específica, centros ativos abundantes e boa condutividade elétrica. No entanto, os materiais de carbono ainda sofrem de algumas desvantagens, como a toxicidade incerta dos CNTs, custo mais alto do que outros materiais eletrocatalisadores flexíveis e baixa repetibilidade em diferentes substratos; materiais de carbono derivados de biomateriais naturais têm flexibilidade e condutividade relativamente pobres, o que limita o desempenho dos dispositivos eletrônicos vestíveis nos quais são aplicados. Espera-se que um extenso estudo sobre a microestrutura do catalisador e o efeito da dopagem atômica, bem como a relação interna entre a distribuição eletrônica do catalisador e seu desempenho de redução de oxigênio eletrocatalítico, desempenhe um papel vital na identificação eficaz do real papel dos íons metálicos, N, S e P, e outros elementos de dopagem nos sítios ativos e aprofundar a compreensão do processo ORR de eletrocatálise do catalisador de carbono. Esperávamos contribuir para o desenvolvimento de catalisadores ORR de metal não nobre à base de carbono e de alto desempenho a preços acessíveis. Produtos eletrônicos flexíveis baseados em carbono têm sido usados para detectar o pulso humano e a taxa de respiração [97]. Acredita-se que mais dispositivos eletrônicos flexíveis multifuncionais baseados em catalisadores ZAB flexíveis à base de carbono serão comercializados no futuro.
Disponibilidade de dados e materiais
Não aplicável. Todas as fotos do artigo foram citadas.
Abreviações
- ZABs:
-
Baterias de zinco-ar
- ORR:
-
Reação de redução de oxigênio
- REA:
-
Reação de evolução de oxigênio
- CC:
-
Pano de carbono
- PEO:
-
Óxido de polietileno
- PAM:
-
Poliacrilamida
- PAA:
-
Ácido poliacrílico
- CNTs:
-
Nanotubos de carbono
- TMP:
-
Fosfetos de metal de transição
- CFP:
-
Papel de fibra de carbono
- DFT:
-
Teoria da densidade funcional
- DG:
-
Grafeno defeituoso
- VO:
-
Vagas de oxigênio
- NiFe LDHs:
-
Hidróxidos duplos com camada de NiFe
Nanomateriais
- Projeto higiênico para as indústrias de alimentos e processamento
- Nanopartículas para terapia do câncer:progresso e desafios atuais
- Avanços e desafios dos nanomateriais fluorescentes para aplicações biomédicas e de síntese
- O Projeto da Camada de Emissão para Multiplicadores de Elétrons
- Engenharia de processo de revestimento por imersão e otimização de desempenho para dispositivos eletrocrômicos de três estados
- Síntese e propriedades eletroquímicas de materiais catódicos de LiNi0,5Mn1,5O4 com dopagem composta Cr3 + e F− para baterias de íon-lítio
- Preparação de micrromateriais híbridos MnO2 revestidos com PPy e seu desempenho cíclico aprimorado como ânodo para baterias de íon-lítio
- Um Projeto Eficiente e Eficaz de Nanofios InP para Captação Máxima de Energia Solar
- Efeito de diferentes ligantes no desempenho eletroquímico do ânodo de óxido de metal para baterias de íon-lítio
- Seis Estratégias de Cadeia de Suprimentos para Petróleo e Gás na Era do Coronavírus



