Nanocompósitos à base de óxido de grafeno decorados com nanopartículas de prata como agente antibacteriano
Resumo
Um dos métodos mais promissores contra bactérias resistentes a medicamentos pode ser materiais modificados por superfície com nanopartículas biocidas e nanocompósitos. Aqui, apresentamos um nanocompósito com nanopartículas de prata (Ag-NPs) na superfície de óxido de grafeno (GO) como um novo material antibacteriano e antifúngico multifuncional. As tecnologias ultrassônicas têm sido usadas como um método eficaz de revestimento de folhas de poliuretano. Toxicidade em bactérias gram-negativas ( Escherichia coli ), bactérias gram-positivas ( Staphylococcus aureus e Staphylococcus epidermidis ) e levedura patogênica ( Candida albicans ) foi avaliada pela análise da morfologia celular, avaliação da viabilidade celular pelo ensaio PrestoBlue, análise da integridade da membrana celular pelo ensaio da lactato desidrogenase e produção de espécies reativas de oxigênio. Em comparação com Ag-NPs e GO, que têm sido amplamente usados como agentes antibacterianos, nosso nanocompósito mostra uma eficiência antimicrobiana muito maior para bactérias e células de levedura.
Histórico
O desenvolvimento de antibióticos tem desempenhado um papel significativo no controle do número de infecções bacterianas. No entanto, o uso indevido e o uso excessivo de antibióticos levaram ao desenvolvimento de multirresistência em muitas espécies bacterianas. Algumas cepas se tornaram resistentes a praticamente todos os agentes comumente disponíveis:beta-lactâmicos, tetraciclinas e aminoglicosídeos [1]. Os principais patógenos resistentes são Staphylococcus aureus resistentes à meticilina , Enterococcus resistente à vancomicina , e produtora de β-lactamase de espectro estendido Klebsiella pneumoniae e Escherichia coli [2, 3]. As bactérias, com suas populações muito grandes e rápido tempo de proliferação, são capazes de desenvolver rapidamente mecanismos de resistência aos antibióticos quando um subconjunto da população de bactérias sobrevive ao tratamento com antibióticos. Além disso, as bactérias resistentes a antibióticos são capazes de transferir cópias de DNA que codificam um mecanismo de resistência para outras bactérias distantemente relacionadas, que são então capazes de transmitir os genes de resistência para as gerações subsequentes. Assim, o surgimento de bactérias resistentes a antibióticos representa um sério problema que pode ser superado pelo desenvolvimento de novos agentes antimicrobianos. Os agentes antibacterianos são muito importantes na indústria têxtil, desinfecção de água, medicamentos e embalagens de alimentos. Nanopartículas e nanomateriais podem ser usados como alternativa aos antibióticos [4]. O mecanismo de atividade antibacteriana das nanopartículas varia entre os diferentes tipos de nanopartículas. Enquanto alguns mecanismos propostos se relacionam com a estrutura físico-química das nanopartículas, outros se relacionam com o aumento da liberação de íons antibacterianos das superfícies das nanopartículas. Múltiplos mecanismos simultâneos de ação contra micróbios exigiriam uma variedade de mutações síncronas de DNA na mesma célula microbiana para o desenvolvimento de resistência; portanto, é difícil para as células bacterianas se tornarem resistentes a nanopartículas e nanomateriais. Nanomateriais antimicrobianos, como prata, cobre, fulerenos e nanotubos de carbono de parede simples, podem oferecer várias vantagens devido às suas propriedades físico-químicas únicas e altas áreas de superfície [5,6,7,8]. Os mecanismos exatos da toxicidade das nanopartículas (NP) contra várias bactérias não são completamente compreendidos. De acordo com a pesquisa atual, os principais processos subjacentes aos efeitos antibacterianos dos NPs são a ruptura da membrana celular bacteriana, liberação de íons metálicos, geração de ROS, penetração da membrana celular bacteriana e indução de efeitos antibacterianos intracelulares, incluindo interações com DNA e proteínas [9, 10]. NPs são capazes de se anexar à membrana da bactéria por interação eletrostática e interromper a integridade da membrana bacteriana. A carga positiva da superfície das NPs é essencial para a adesão. A carga positiva permite a adição eletrostática entre NPs e a membrana celular carregada negativamente dos microrganismos [11]. A conexão eletrostática entre NPs com as proteínas contendo enxofre presentes na superfície das células bacterianas causa mudanças irreversíveis na estrutura da parede celular, resultando em danos na parede celular e na membrana [12]. A membrana bacteriana é crucial, independentemente do estado metabólico da célula, pois fornece permeabilidade seletiva para a homeostase celular e transdução de energia metabólica. A segunda atividade antibacteriana e antifúngica dos NPs é devido à sua capacidade de produzir ROS e espécies de radicais livres [13]. Aumento do nível de ROS induziu hiperoxidação de lipídios, proteínas e DNA [14].
Além disso, as estruturas de muitos tipos de NPs são adequadas para o transporte de agentes antimicrobianos [15, 16]. Os transportadores podem ajudar a proteger os medicamentos da resistência das bactérias alvo. Um sistema de administração de medicamentos baseado em nanopartículas pode ajudar a direcionar os antibióticos para um local de infecção e, assim, minimizar os efeitos colaterais sistêmicos. Outras vantagens incluem melhor solubilidade de drogas hidrofóbicas, tempo prolongado de circulação sistêmica e meia-vida da droga e liberação sustentada da droga [4].
Recentemente, foi demonstrado que o grafeno, um novo alótropo de carbono, tem atividade antibacteriana. O grafeno é um material feito de átomos de carbono que são unidos em um padrão repetitivo de hexágonos. Uma característica única dos flocos de grafeno é a proporção de sua espessura em relação à superfície. A superfície do grafeno é coberta por uma nuvem de elétrons, o que provavelmente predispõe esse material a ser um doador de elétrons e lhe dá a capacidade de fazer ligações especiais. As bordas do grafeno possuem outras ligações (característica para ligações do tipo diamante sp3), e esses locais podem ter diferentes características físico-químicas [17]. Essas características sugerem que o grafeno pode ser exposto à adesão plástica a diferentes estruturas intercelulares, incluindo células bacterianas [18,19,20]. Além disso, por ter dois lados ativos (superfície e bordas), o grafeno pode anexar moléculas biológicas às suas bordas e aderir à superfície celular. Uma forma oxidada do grafeno, o óxido de grafeno (GO), é facilmente dispersível em água e outros solventes orgânicos devido à presença das funcionalidades de oxigênio. Os grupos oxigenados permitem a funcionalização química direta das folhas GO por meio de interações covalentes e não covalentes. A forte atividade antibacteriana do GO foi relatada. A atividade antibacteriana do GO foi atribuída ao estresse da membrana induzido por bordas afiadas das nanofolhas de óxido de grafeno, que podem resultar em danos físicos às membranas celulares, levando à perda da integridade da membrana bacteriana [21]. Recentemente, nanopartículas antimicrobianas funcionalizadas com grafeno têm sido utilizadas como materiais antibacterianos promissores [22, 23]. Os nanocompósitos podem superar as limitações dos componentes individuais. Por exemplo, nanomateriais antibacterianos anexados ao substrato de grafeno são mais estáveis e bem dispersos [24]. Esses nanocompósitos podem conter metais, óxidos de metal e polímeros.
Um dos métodos mais promissores contra bactérias resistentes a medicamentos pode ser materiais modificados por superfície com nanopartículas biocidas. As tecnologias ultrassônicas foram confirmadas como um método eficaz de revestimento de vários materiais com substâncias antibacterianas e fungicidas [25,26,27,28]. Muitos pesquisadores classificam o método de ultrassom como uma “tecnologia verde” [29, 30]. O método é baseado no uso de fenômenos de cavitação, que é a formação, crescimento e colapso de bolhas de cavitação no meio líquido [31, 32]. Bolhas que explodem geram imensas quantidades de energia em microrregiões de até 5000 K e pressão de até 2.000 atm em um curto período de tempo [33, 34]. Consequentemente, ondas de choque e os chamados microjatos direcionados à superfície sólida são gerados [35]. Localizadas em meio líquido, as NPs são impulsionadas pelo efeito de implosão e jatos em alta velocidade (> 100 m / s) na superfície sólida e formam uma camada [36]. A cavitação acústica também pode levar a alterações nas propriedades físicas de objetos sonicados, por exemplo, redimensionamento de flocos GO [37, 38] .
Obtivemos resultados promissores em nossos estudos anteriores com Salmonella enterica e Listeria monocytogenes tratado com grafeno puro, GO e GO reduzido [20]. Dos diferentes tipos de grafeno, o GO também apresentou a maior atividade antibacteriana em baixa concentração. As células bacterianas foram distribuídas por toda a superfície do GO. Neste estudo, hipotetizamos que o GO decorado com nanopartículas de prata (GO-Ag) terá uma influência tóxica mais forte nas células microbianas do que o GO nu ou nanopartículas de prata (Ag-NPs). Por ter dois lados ativos (superfície e bordas), o óxido GO pode anexar Ag-NPs às bordas e aderir à superfície da célula. A atividade antibacteriana dos nanocompósitos à base de grafeno pode ser devido ao rompimento da membrana celular e ao estresse oxidativo. O objetivo deste estudo foi avaliar a atividade antimicrobiana de nanocompósitos à base de GO decorados com Ag-NPs em comparação com GO e Ag-NPs nus usando bactérias gram-negativas ( Escherichia coli ), bactérias gram-positivas ( Staphylococcus aureus e Staphylococcus epidermidis ) e levedura patogênica ( Candida albicans ) usando um modelo in vitro. A investigação consistiu na análise estrutural de nanocompósitos utilizando difração de raios-X, transmissão de espectroscopia Raman, FT-IR, microscopia eletrônica (TEM), microscopia eletrônica de varredura (MEV) e microscopia de força atômica (AFM), avaliação da morfologia celular microbiana, avaliação de viabilidade celular pelo ensaio PrestoBlue ™, investigação da integridade da membrana celular pelo ensaio da lactato desidrogenase (LDH) e avaliação da produção de espécies reativas de oxigênio (ROS).
Métodos
Síntese, modificação e caracterização do óxido de grafeno
Neste estudo, um pó de grafite disponível comercialmente (Acros Organics, New Jersey, EUA) foi oxidado pelo método Hummers modificado [39]. Dez gramas de pó de grafite foram misturados com 230 mL de ácido sulfúrico concentrado (98%) abaixo de 10 ° C. Em seguida, 4,7 g de nitrato de sódio e 30 g de permanganato de potássio foram adicionados gradualmente à mistura de ácido sulfúrico e grafite, mantendo a temperatura abaixo de 10 ° C. Em seguida, a mistura foi aquecida a 30 ° C e agitada durante 2 h. Na etapa seguinte, foram adicionados 100 mL de água e a temperatura da mistura atingiu ~ 100 ° C. Finalmente, a mistura foi tratada com 10 mL de peróxido de hidrogênio. Para purificação, a pasta foi filtrada e lavada com água desionizada até o pH do filtrado atingir 6,5.
Os padrões de difração de raios-X de GO foram coletados à temperatura ambiente dentro da faixa de ângulo 2 teta de 10 ° a 100 ° com a etapa de 0,02 ° usando o difratômetro de pó de raios-X ( CuK α1 ) (X’Pert PRO, PANalytical, Almelo, Holanda).
A análise do teor de carbono, hidrogênio, nitrogênio e enxofre em peso no GO foi realizada usando o aparelho Vario EL III produzido pela Elementar Analysensysteme GmbH (Langenselbold, Alemanha). Antes de realizar medições de análises químicas de GO, as amostras foram submetidas a dessorção de 24 horas em uma estação de dessorção (VcPrep 061, Micromeritics, Norcross, GA, EUA) sob vácuo (0,05 mbar) a 50 ° C. O conteúdo de oxigênio foi calculado subtraindo o conteúdo determinado de carbono, hidrogênio, nitrogênio e enxofre de 100% do peso.
A espectroscopia Raman foi realizada usando um microscópio InVia Raman (Renishaw, Reino Unido). O óxido de grafeno foi analisado com o comprimento de onda do laser de 514 nm com 5% de sua potência inicial. Os espectros foram coletados em cinco pontos diferentes da amostra. O tempo de exposição foi de 10 se duas varreduras foram coletadas.
As medições de FT-IR foram realizadas usando o espectrômetro Nicolet iS10 (Thermo Fisher Scientific, EUA) no modo de refletância total atenuada em um cristal de diamante. Cinco microlitros de suspensão aquosa de óxido de grafeno foram gotejados na superfície do cristal de diamante e este foi deixado secar. Depois de seco, o espectro foi coletado na faixa de 400–4000 cm −1 .
As medidas de tamanho médio de partícula e potencial zeta foram realizadas usando Zetasizer Nano-ZS ZEN 3600 produzido por Malvern Instruments Ltd. (Malvern, Reino Unido) usando o modo de espalhamento dinâmico de luz (DLS) e eletroforese laser Doppler, respectivamente, em temperatura ambiente (23 ° C).
Análise TEM / SEM / AFM de nanomateriais
A morfologia dos pós e folhas foi determinada usando o microscópio eletrônico de transmissão (TEM; JEM-1220 JEOL, Tóquio, Japão, voltagem de aceleração de 80 kV) e microscópio eletrônico de varredura (SEM; Zeiss, Ultra Plus, Oberkochen, Alemanha). As amostras para observações de TEM foram preparadas colocando gotículas de hidrocolóides em grades de TEM (Formvar em 3 mm 200 Mesh Cu Grids, Agar Scientific, Stansted, Reino Unido). Imediatamente após secar as gotas ao ar, as grades foram inseridas no microscópio.
Para a análise de MEV, as amostras foram revestidas com uma fina camada de carbono usando o aplicador sputter (SCD 005 / CEA 035, BAL-TEC, Pfäffikon, Suíça). Um procedimento de medição laboratorial interno foi aplicado (P5.10, edição 6 de 26.08.2015).
A imagem AFM (microscopia de força atômica) foi realizada usando o software Asylum Research MFP3D Bio (versão:Asylum Research MFP3D 15.106.09). Imagens de topografia de superfície e detecção de GO nas superfícies de folha testadas foram realizadas usando dois modos de imagem, modo AC para imagem de contraste de fase e microscopia de força lateral (LFM) para detecção de GO, uma vez que GO reduz as forças de atrito [40] . b>
Preparação de folhas de poliuretano revestidas com GO e Ag-NPs
Para cobertura de folhas de poliuretano, foram utilizadas suspensões de Ag-NPs (HydroSilver1000, Amepox, Łódź, Polônia) e GO. Suspensões de GO, Ag-NPs e GO-Ag (GO (200 μg / mL), Ag-NPs (100 μg / mL), GO (200 μg / mL) + Ag-NPs (100 μg / mL)) foram preparado em água desionizada (condutância 0,09 μS / cm, deionizador:HLP 20UV, Hydrolab, Staszyn, Polônia). As suspensões foram utilizadas sem purificação e filtração adicionais.
O revestimento ultrassônico de folhas de poliuretano (15 × 15 × 0,05 mm) foi realizado em frasco de vidro com volume de 50 ml. Amostras de folhas foram fixadas em um suporte (Teflon) e posteriormente imersas nas suspensões preparadas. O processo de revestimento foi realizado utilizando uma corneta ultrassônica (corneta de Ti, Ø13 mm, eficiência de 60%, 20 kHz, Sonics &Materials, Inc., Newtown, CT, EUA) colocada em quadrado com as amostras de folha presentes na suspensão. A temperatura do processo era de 30 ± 1 ° C. As amostras cobertas foram lavadas em água deionizada e secas em câmara laminar e posteriormente acondicionadas em embalagens estéreis.
Energia Livre de Superfície
Os testes de molhabilidade foram realizados com o goniômetro Data Physics OCA - 20 (DataPhysics Instruments GmbH, Filderstadt, Alemanha). A energia livre de superfície (SFE) foi calculada usando o método Owens, Wendt, Rabel e Kaelble (OWRK) usando dois líquidos de teste:água deionizada e diiodometano [41].
Cultivo e preparação bacteriana e de fermento
Staphylococcus aureus (ATCC 25923) e Staphylococcus epidermidis (ATCC 14990), Escherichia coli (ATCC 25922) e Candida albicans (90028) foram obtidos de LGC Standards (Lomianki, Polônia). As cepas foram armazenadas como suspensões de esporos em 20% ( v / v ) glicerol a -20 ° C. Antes do seu uso em experimentos, as cepas foram descongeladas e o glicerol removido por lavagem das células bacterianas com água destilada. A bactéria e a levedura foram então cultivadas nos seguintes meios de nutrientes:ágar de soja tríptica para S . aureus e E . coli , ágar cérebro e coração para S . epidermidis e ágar de Sabouraud para C . albicans (Merck Millipore, Darmstadt, Alemanha). As bactérias e leveduras cultivadas em placas de ágar foram colhidas lavando suavemente as placas com solução salina destilada estéril. Para calcular o número de bactérias na suspensão de células, a densidade óptica das suspensões a 600 nm (OD 600 ) foi medido usando um espectrofotômetro (Helios Epsilon, Unicam, Milwaukee, WI, EUA). As curvas de calibração para cada um dos microrganismos foram preparadas realizando diluições seriadas de dez vezes (até 10 - 5 ) de suspensões de bactérias e leveduras de densidade óptica conhecida. Um mililitro de cada diluição foi espalhado em placas de Petri contendo o meio nutriente. Após 24 h de incubação a 37 ° C, o número de colônias formadas nas placas de Petri foi contado. Com base nos resultados das enumerações (conduzidas em triplicata), foi calculada a densidade da suspensão bacteriana original em unidades formadoras de colônias (UFC) / mL.
Ensaio Antimicrobiano
O inóculo para o ensaio antibacteriano foi preparado a partir de organismos em crescimento ativo (fase logarítmica). Os inóculos de todos os microrganismos foram preparados a partir de uma cultura crescida aerobicamente durante a noite em caldo Mueller-Hinton (MH) a 37 ° C. A concentração de bactérias e leveduras foi determinada medindo a densidade óptica a 600 nm (OD 600 ) Resumidamente, as suspensões de bactérias e leveduras foram preparadas a partir de culturas durante a noite e ajustadas para 10 6 CFU / ml. O inoculo foi inoculado uniformemente na superfície do ágar MH em placas de Petri por esfregaço. Folhas estéreis revestidas com GO, Ag-NPs e GO-Ag foram depositadas na superfície do ágar. Folhas sem nanopartículas foram utilizadas como grupo controle. O crescimento de bactérias e leveduras sob as folhas foi medido após 24 h de incubação a 37 ° C.
Ensaio de viabilidade
A viabilidade celular foi avaliada usando o Ensaio de Viabilidade Celular PrestoBlue ™ (Life Technologies, Taastrup, Dinamarca). O reagente PrestoBlue ™ é rapidamente reduzido por células metabolicamente ativas, fornecendo uma medida quantitativa de viabilidade e citotoxicidade. As células bacterianas e de levedura foram cultivadas em folhas revestidas com GO, Ag-NPs e GO-Ag localizadas em inserções inseridas em placas de 6 poços (200 μL de caldo MH com 5 × 10 3 células por folha) e incubadas por 24 h. Na próxima etapa, 90 μL de cada amostra foram transferidos para placas de 96 poços e 10 μL de reagente PrestoBlue ™ foram adicionados a cada poço e incubados por mais 2 h a 37 ° C. A densidade óptica de cada poço foi registrada a 570 nm em um leitor de ensaio imunoenzimático (ELISA) (Infinite M200, Tecan, Durham, NC, EUA). A viabilidade celular foi expressa como a porcentagem (OD teste - OD em branco ) / (OD controle - OD em branco ) × 100%, onde OD teste é a densidade óptica das células expostas às folhas testadas, OD controle é a densidade óptica da amostra de controle, e OD em branco é a densidade óptica de poços sem células bacterianas e de levedura.
Integridade da membrana
Um teste de LDH (In Vitro Toxicology Assay Kit, à base de desidrogenase láctica, Sigma-Aldrich, Hamburgo, Alemanha) foi usado para avaliar a integridade da membrana celular. O NAD reduzido resultante (NADH + ) foi utilizado na conversão estequiométrica de um corante de tetrazólio. Quando alíquotas livres de células do meio de culturas foram testadas, a quantidade de atividade de LDH pode ser usada como um indicador da integridade da membrana. Se a membrana foi danificada, as moléculas de LDH intracelulares foram liberadas no meio de cultura. Células bacterianas e de levedura foram cultivadas em folhas (GO, Ag-NPs e GO-Ag) localizadas em inserções inseridas em placas de 6 poços (200 μL de caldo MH com 5 × 10 3 células por folha) e incubadas por 24 h. As células cultivadas em folha sem nanopartículas foram utilizadas como controle. Após esse tempo, as amostras foram transferidas para tubos de microcentrífuga e centrifugadas a 1200 rpm por 5 min. Cem microlitros de sobrenadante foram transferidos para placas de 96 poços e 100 μL da mistura de ensaio de LDH foram adicionados a cada poço. A placa foi coberta e incubada por 30 min em temperatura ambiente. A densidade óptica de cada poço foi registrada a 450 nm em um leitor de ELISA (Infinite M200, Tecan, Männedorf, Suíça). O vazamento de LDH foi expresso como a porcentagem {(OD teste - OD em branco ) - (OD controle - OD em branco ) / (OD controle - OD em branco )} × 100%, onde OD teste é a densidade óptica das células expostas às folhas testadas, OD controle é a densidade óptica da amostra de controle, e OD em branco é a densidade óptica de poços sem células.
Análise SEM de Microorganismos
Antes da análise SEM, foram preparadas amostras de bactérias e leveduras incubadas em folhas com GO-Ag e bactérias não tratadas. Resumidamente, uma gota de cultura de bactérias e leveduras (10 6 CFU / ml) foi incubado em folhas com nanocompósito GO-Ag, ou bactérias não tratadas foram depositadas na superfície de uma lamela de vidro estéril e incubadas por 24 h a 37 ° C dentro de uma placa de Petri vazia. Todas as amostras foram secas e cobertas com ouro. Finalmente, as amostras foram fotografadas com SEM (FEI Quanta 200, Tóquio, Japão) em uma tensão de aceleração de 15 kV.
Produção ROS
A produção de ROS foi avaliada usando DCFDA, Cellular Reactive Oxygen Species Detection Assay Kit (Abcam, Cambridge, UK). DCFDA usa o reagente permeante celular 2 ′, 7′-diacetato de diclorofluoresceína, um corante fluorogênico que mede hidroxila, peroxila e outras atividades ROS dentro da célula. Após a difusão na célula, o DCFDA é desacetilado pelas esterases celulares em um composto não fluorescente, que é posteriormente oxidado por ROS em 2 ′, 7′-diclorofluoresceína (DCF). Células bacterianas e de levedura foram cultivadas em folhas (GO, Ag-NPs e GO-Ag) localizadas em inserções inseridas em placas de 6 poços (200 μL de caldo MH com 5 × 10 3 células por folha) e incubadas por 24 h. As células cultivadas em folha sem nanopartículas foram utilizadas como controle. Após esse tempo, as amostras foram transferidas para tubos de microcentrífuga e centrifugadas a 1200 rpm por 5 min. Cem microlitros de sobrenadante foram transferidos para placas de 96 poços e 100 μL de DCFDA diluído foram adicionados a cada poço e incubados por mais 45 min a 37 ° C no escuro. A produção de DCF foi medida por espectroscopia de fluorescência com um comprimento de onda de excitação a 485 nm e um comprimento de onda de emissão a 535 nm em um leitor de ELISA (Infinite M200, Tecan, Durham, NC, EUA).
Resultados
Características de GO e Ag-NPs
A análise química revelou a presença de nitrogênio, carbono, enxofre, hidrogênio e oxigênio (Tabela 1).
A análise de fase da amostra GO (Fig. 1) revelou a presença de impurezas provenientes de traços de grafite, nitrato de sódio e provavelmente uma forma reduzida de óxido de grafeno.
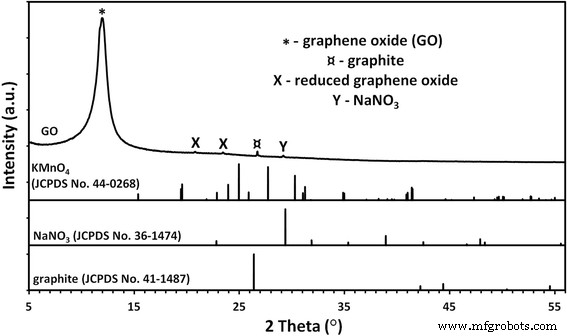
Padrões de difração de raios-X de pós GO. A análise de fase da amostra GO revelou a presença de impurezas provenientes de traços de grafite, nitrato de sódio e provavelmente uma forma reduzida de óxido de grafeno
A espectroscopia Raman pode fornecer informações sobre as características estruturais do óxido de grafeno. A banda D é atribuída à desordem estrutural, enquanto a banda G vem do alongamento da ligação do carbono sp 2 átomos [42]. As bandas adicionais (incluindo D ′, 2D e D + G) surgem dos defeitos presentes na estrutura grafítica do material de carbono. eu D / eu G razão (calculada a partir da intensidade das bandas D e G) pode ser usada para caracterizar a desordem da estrutura grafítica em materiais de carbono. Como pode ser visto na Fig. 2, GO possui uma estrutura altamente desordenada devido a muitos grupos funcionais na estrutura formada durante a oxidação do pó de grafite. A posição da banda D é 1351 cm −1 e a banda G 1590 cm −1 ; o eu D / eu G a proporção é 1,15.
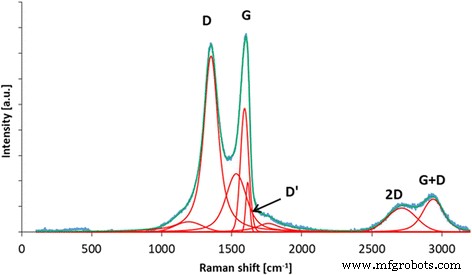
Espectro Raman de óxido de grafeno com deconvolução proposta das bandas D, G, D ′, 2D e D + G. GO possui uma estrutura altamente desordenada devido a muitos grupos funcionais na estrutura formada durante a oxidação do pó de grafite. A posição da banda D é 1351 cm −1 e a banda G 1590 cm −1 ; o eu D / eu G proporção é 1,15
O espectro FT-IR do óxido de grafeno coletado no modo ATR revelou que GO possui muitos grupos funcionais presentes na estrutura. O pico mais notável pode ser observado em ~ 3500 cm −1 , que é atribuído principalmente aos grupos água e hidroxila (Fig. 3). Um pico muito intenso em torno de 1080 cm −1 também pode ser atribuído a grupos hidroxila. O pico em torno de 1600 cm −1 geralmente é atribuído a ligações C =C presentes no carbono grafítico. No entanto, nossos estudos anteriores de XPS mostram que existem algumas ligações C =C no óxido de grafeno [43]; portanto, atribuímos esse pico principalmente à água ainda presente no óxido de grafeno. Outros picos observados no espectro FT-IR mostram que GO é rico em grupos contendo ligações C =O (principalmente grupos carboxila), com pico em torno de 1720 cm -1 , epóxi (C – O – C) com o pico visível em torno de 1200 cm −1 , e ligações C – H (pico em torno de 2.800 cm −1 ) A análise FT-IR está de acordo com as medições XPS realizadas para óxido de grafeno, onde também grupos hidroxila, carboxila, epóxi e carbonila foram identificados [44]. GO e GO após uma homogeneização ultrassônica de 10 min foram comparados (Figs. 4 e 5), e da mesma forma, Ag-NPs com Ag-NPs após uma homogeneização ultrassônica de 10 min (Figs. 4 e 6) foram comparados. Para evitar alterações na morfologia do composto, todos os compostos foram resfriados rapidamente com nitrogênio líquido e secos em um liofilizador. A Figura 5a, b apresenta flocos de GO, enquanto a Figura 5c, d mostra os efeitos de ultrassons em flocos de GO, que sofrem dobramento parcial e fragmentação. A Figura 6 também mostra um efeito semelhante para Ag-NPs, onde uma mudança na morfologia do material é visível. A Figura 6a, b exibe poli (álcool vinílico) seco, que foi usado para estabilizar a suspensão de água de Ag-NPs. O efeito destrutivo da homogeneização ultrassônica foi notável, pois a estrutura do álcool polivinílico foi quebrada em longas partes heterogêneas com pequenas aberturas esféricas (Fig. 6c, d).
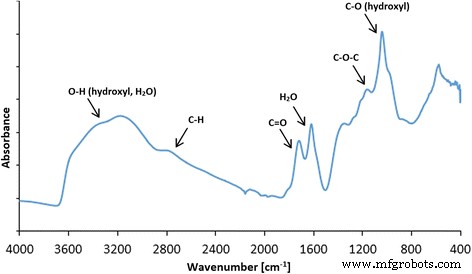
Espectro FT-IR (ATR, refletância total atenuada) de óxido de grafeno com atribuição proposta de grupos funcionais presentes em GO. Os picos mais notáveis foram observados em ~ 3500 cm −1 , (atribuído a grupos de água e hidroxila), ~ 1080 cm −1 (grupos hidroxila), ~ 1600 cm −1 (atribuído a ligações C =C presentes no carbono grafítico). Outros picos observados no espectro FT-IR mostram que GO é rico em grupos contendo C =O (principalmente grupos carboxila), com pico em torno de 1720 cm −1 , epóxi (C – O – C) com o pico visível em torno de 1200 cm −1 , e ligações C – H (pico em torno de 2.800 cm −1 )
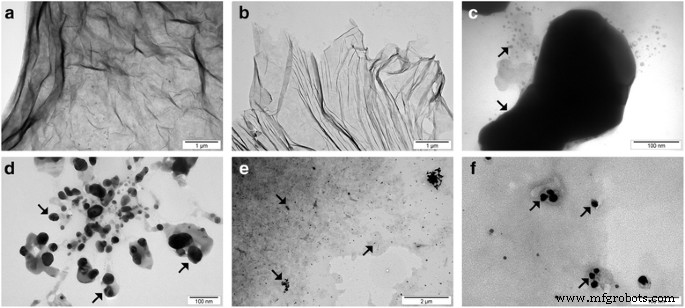
Imagens TEM de flocos GO aglomerados ( a ), Flocos GO após tratamento ultrassônico ( b ), Ag-NPs aglomerados ( c ), Ag-NPs após tratamento ultrassônico ( d ), e GO-Ag ( e , f ) A diminuição do tamanho médio das partículas GO após o tratamento ultrassônico foi causada pela desfragmentação ou dobramento dos flocos GO. A diminuição do tamanho médio do Ag após o tratamento ultrassônico foi causada pela desfragmentação dos aglomerados de Ag. Nota:As setas apontam para Ag-NPs / aglomerados

Comparação da morfologia de flocos liofilizados GO ( a , b ) e flocos GO após tratamento ultrassônico ( c , d ) usando microscopia eletrônica de varredura. A diminuição do tamanho médio das partículas GO após o tratamento ultrassônico foi causada pela desfragmentação ou dobramento dos flocos GO

Comparação da morfologia da mistura de Ag-NP liofilizada ( a , b ) e mistura Ag-NP após tratamento ultrassônico ( c , d ) usando microscopia eletrônica de varredura
Tamanho médio e potencial Zeta
Os resultados do tamanho médio de partícula / aglomerado em suspensões de água são apresentados na Tabela 2. As análises de tamanho médio foram realizadas para suspensões concentradas que não foram submetidas à homogeneização ultrassônica (conforme recebido) e para suspensões diluídas. As suspensões diluídas antes do teste foram submetidas à homogeneização ultrassônica, com parâmetros de homogeneização idênticos aos usados durante o revestimento ultrassônico da folha com camadas de nanomateriais (Ag-NPs, GO). Para a suspensão de Ag-NP, a ação dos ultrassons causou um aumento no tamanho médio das partículas de 80 para 218 nm. A principal causa do aumento no tamanho médio de partícula após a homogeneização ultrassônica na suspensão (além do processo de aglomeração de Ag-NP) foi que os Ag-NPs foram conduzidos para o poli (álcool vinílico) que foi usado para estabilização da suspensão. O grande desvio padrão da amostra Ag-NP homogeneizada por ultrassom resultou da presença de Ag-NPs soltos e Ag-NPs direcionados para o poli (álcool vinílico) na suspensão. In the case of GO suspension, the average particle size of the sample subject to ultrasonic homogenization was 263 nm and was ca 7.7 times smaller than the average particle size of the sample that was not subject to homogenization. The obtained results are convergent with the SEM tests (Fig. 5), which show the destructive effect of ultrasounds on GO flakes. The decrease of the average GO particle size was caused by defragmentation or folding of the GO flakes. However, it should be emphasized that the results of the average particle size of GO suspension samples involve an error related to the nanomaterial shape. The results obtained by the DLS method are a hydrodynamic average that is calculated based on the shape of a sphere that has the same diffusion coefficient as the measured particles; however, the shape of GO was flakes, which was confirmed by SEM images.
Test results of the zeta potential analysis of samples are provided in Table 3. The zeta potential of Ag-NPs in a water suspension was merely − 5.9 mV, which resulted in a lack of electrostatic stability of the sample. The sample of Ag-NP suspension was stabilized sterically by preserving Ag-NP distances through poly(vinyl alcohol) addition, which prevented agglomeration/aggregation of Ag-NPs. The zeta potential of the GO suspension sample, in turn, was − 41 mV, which gave a moderate electrostatic stability to the sample. A moderate electrostatic stability of a sample is characterized by slow sedimentation with virtually negligible change of particle size in the period of declared fitness of the suspension. The zeta potential result of the mixture of Ag-NPs and GO was − 7.1 mV, which potentially means that during the action of the ultrasounds, the GO flakes were coated by poly(vinyl alcohol) and Ag-NPs. The obtained zeta potential result of the mixture of Ag-NPs and GO sample in the water suspension implied that electrostatic stability was not present.
Foil Characteristics
In order to determine the morphology of the created layers, four types of foil samples were compared (Fig. 7):pure polyurethane foil (A, B), GO-coated polyurethane foil (C, D), Ag-NP-coated polyurethane foil (E, F), and GO-Ag mixture-coated polyurethane foil (G, H).

Scanning electron microscopy images of a , b non-coated polyurethane foil with a smooth surface with single impurities; c , d foil coated with GO, the broken-down GO flakes deposited on the polyurethane foil surface; e , f foil coated with Ag-NPs on which grid structures composed of polyvinyl alcohol and Ag-NPs are observed; and g , h foil coated with GO-Ag, which was mixed under the influence of ultrasounds and deposited on the foil surface
Figure 7a, b shows an uncoated polyurethane foil with a smooth surface with single impurities. In Fig. 4c, d, the broken-down GO flakes deposited on the polyurethane foil surface are noticeable. Figure 7e, f shows the foil surface coated with Ag-NPs on which grid structures composed of polyvinyl alcohol and Ag-NPs are observable. Figure 7g, h presents a mixture of GO-Ag composition, which was mixed under the influence of ultrasounds and deposited on the foil surface.
AFM Analysis and Surface Free Energy
AFM and LFM were used to complement the information about the surface morphology investigated by SEM. The investigation confirmed evolution of surface morphology by sonication of the polyvinyl alcohol with Ag-NP, GO, and GO-Ag NP solutions on the foils. Pure polyurethane foil was used as a reference foil in relation to foils coated by the ultrasonic method. The images in Fig. 8 are the AFM phase contrast images made in AC; additionally, cross sections of the GO flakes are attached under the corresponding images. Figure 8a is an image of pure polyurethane film; Fig. 7b depicts the Ag-NP-coated film, where characteristic and homogeneous grid structures are observable, being similar to those in Fig. 8e, f. Figure 8c, d shows GO-Ag-NP-coated film. Figure 8e shows the surface of the foil almost entirely covered with GO flakes; the phase contrast image helps to observe these two phases, the darker area is GO and the lighter area is polymer foil. It was noticed that the morphology of the foils has changed after Ag-NP coating comparing to the not-coated foils. The GO-Ag-NP coating differs from the previous one because it contains also small amounts of GO flakes seen as small black spots on the image, as it was mentioned earlier. Figure 8f depicts magnification of one GO flake made in LFM. The reduced friction confirms that it is, in fact, a GO flake.
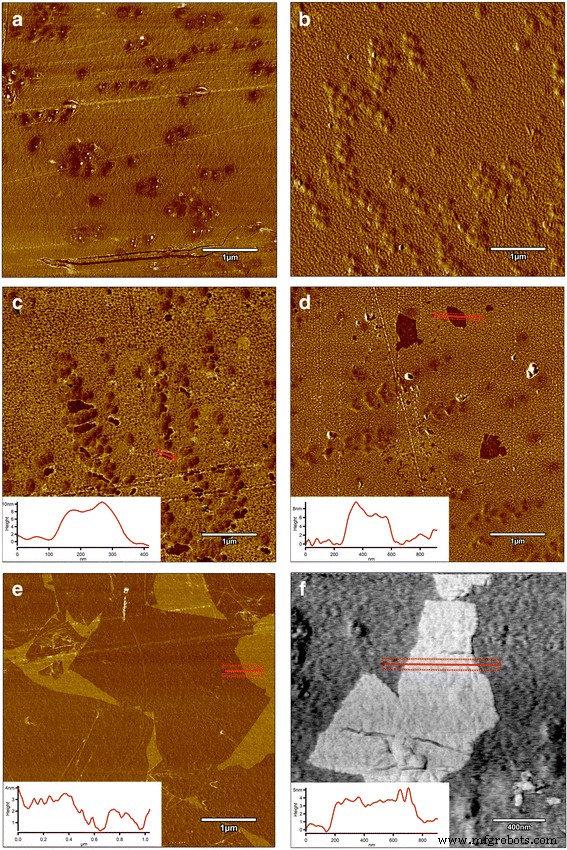
AFM phase contrast images and cross sections topographic images of graphene flakes:a non-coated foil polyurethane foil; b Ag-NPs coated foil where characteristic and homogeneous grid structures are observed; c , d GO-Ag-coated foil; e GO-coated foil, the surface of the foil almost entirely covered with GO flakes; the phase contrast image helps to observe these two phases, the darker area is GO and the lighter area is polymer foil; f LFM image of graphene flake. Red marks, area of cross section
The polar component for the GO-coated foil increased in relation to pure foil, from 2.3 ± 0.6 to 68.9 ± 2.8 mJ/m 2 , while the dispersion component decreased from 34.4 ± 1.3 to 8.2 ± 1.2 mJ/m 2 . SFE increased from 36.7 ± 1.4 to 77.0 ± 3.4 mJ/m 2 . A similar effect was not observed on foil surfaces coated with Ag-NPs and GO-Ag mixture. SFE of foil samples coated with Ag-NPs and GO-Ag mixture does not differ statistically (Table 4).
Antibacterial Properties
The antibacterial activity of the different foils coated with GO, Ag-NPs, and GO-Ag were tested with E . coli , S . aureus , S . epidermidis e C . albicans. Results showed that after co-incubation with bacteria at 37 °C for 24 h, foils inhibited the growth of all tested microorganisms but to various degrees. The maximum antibacterial effect against all tested microorganisms was with foil coated with the GO-Ag nanocomposite. The bacterial growth of the cells treated with foils coated with GO and Ag-NPs was slightly lower than that of cells in the control group whereas the growth of bacterial cells treated with foils coated with GO-Ag was greatly inhibited, 88.6% of E . coli , 79.6% of S . aureus , 76.5% of S . epidermidis , and 77.5% of C . albicans (Figs. 9, 10, and 11).
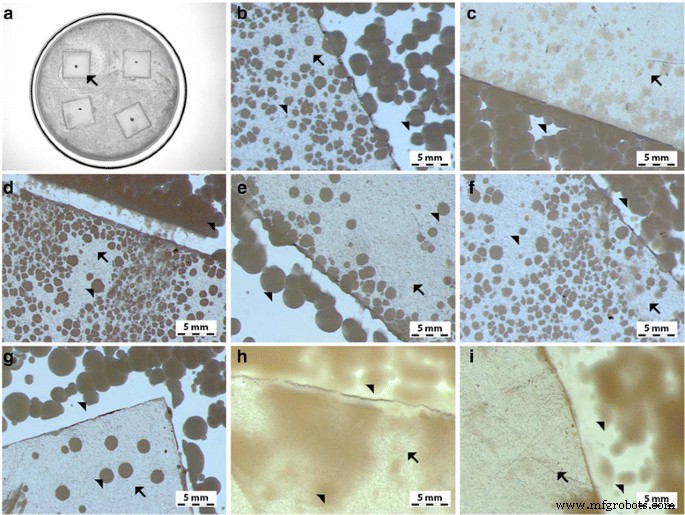
Antimicrobial properties of GO-Ag coated foils. The growth of E . coli ( b , c ), S . aureus ( c , d ), S . epidermidis ( e , f ), and C . albicans (g - i ) colonies is reduced after co-incubation with GO-Ag-coated foils at 37 °C for 24 h. a Representative agar plate with GO-Ag-coated foils. Notes:Black arrows point to GO-Ag coated foils; arrowheads point to colonies of microorganisms

Morphology of microorganisms after co-incubation with GO-Ag-coated foils. Scanning electron microscopy images of bacteria and yeast in the control foils (a , c , e , g ) and foils coated with GO-Ag (b , d , f , h ) after incubation at 37 °C for 24 h. E . coli ( a , b ), S . aureus ( c , d ), S . epidermidis ( e , f ), and C . albicans (g , h ) show decreased growth and deformed morphology after co-incubation with GO-Ag-coated foils
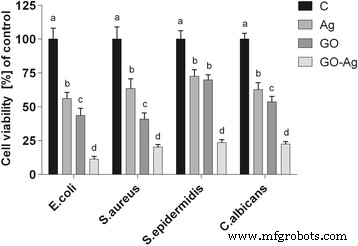
Foils coated with nanomaterials decrease E . coli , S . aureus , S . epidermidis e C . albicans viability. Viability of bacteria and yeast after incubation on foils coated with Ag-NPs, GO, and GO-Ag at 37 °C for 24 h was assessed with Presto Blue assay. C control group (foil without nanoparticles), Ag foil coated with silver nanoparticles, GO foil coated with graphene oxide, GO-Ag foil coated with composite of graphene oxide and silver nanoparticles. Note:The columns with different letters (a–d) indicate significant differences between the concentrations (P = 0.001); error bars are standard deviations
Membrane Integrity
In cases where the cell membrane is damaged, intracellular LDH molecules could be released into the culture medium. The LDH level outside the cells demonstrates the cell membrane integrity. Foils coated with GO, Ag-NPs, and GO-Ag disrupted cell membrane functionality and integrity with significant differences between control groups and the Ag-NPs and GO-Ag groups (Fig. 12). The highest disruption of cell membranes was observed in the GO-Ag groups, 66.3% of E . coli , 59.4% of S . aureus , 54.8% of S . epidermidis , and 48.5% of C . albicans .
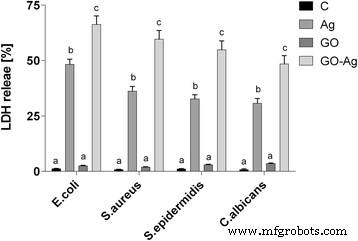
Foils coated with nanomaterials decreased E . coli , S . aureus , S . epidermidis e C . albicans membrane integrity. Membrane integrity of bacteria and yeast after incubation on foils coated with Ag-NPs, GO, and GO-Ag at 37 °C for 24 h was assessed with LDH assay. C control group (foil without nanoparticles), Ag foil coated with silver nanoparticles, GO foil coated with graphene oxide, GO-Ag foil coated with composite of graphene oxide and silver nanoparticles. Note:The columns with different letters (a–c) indicate significant differences between the concentrations (P = 0.000); error bars are standard deviations
ROS Production
Low levels (or optimum levels) of ROS play an important role in signaling pathways. However, when ROS production increases and overwhelms the cellular antioxidant capacity, it can induce macromolecular damage (by reacting with DNA, proteins, and lipids) and disrupt thiol redox circuits. Foils coated with Ag-NPs and GO-Ag (P < 0.05) increased the ROS production of all tested microorganisms compared to the control group. Foils coated with GO only increased the ROS production of C . albicans . The highest ROS production was observed in the GO-Ag group (Fig. 13).
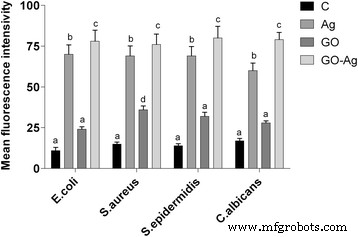
Effect of foils coated with nanomaterials on the production of reactive oxygen species. E . coli , S . aureus , S . epidermidis e C . albicans were cultured on foils coated with Ag-NPs, GO, and GO-Ag at 37 °C for 24 h. Production of reactive oxygen species was assessed with DCFDA, Cellular Reactive Oxygen Species Detection Assay Kit. C control group (foil without nanoparticles), Ag foil coated with silver nanoparticles, GO foil coated with graphene oxide, GO-Ag foil coated with composite of graphene oxide and silver nanoparticles. Note:The columns with different letters (a–d) indicate significant differences between the concentrations (P = 0.000); error bars are standard deviations
Discussion
The discovery of antibiotics, natural products produced by microorganisms that are able to prevent the growth of bacteria and thus cure infectious diseases, revolutionized medical therapy; however, the overuse and misuse of antibiotics have been key factors contributing to antibiotic resistance. Now, the era of antibiotics is coming to an end, and new antibacterial agents are needed. In recent years, studies have reported nanoparticles as a promising alternative to antibacterial reagents because of their antibacterial activity in several biomedical applications [19, 45]. Nanoparticles can be an effective way to control many pathogenic and antibiotic-resistant microorganisms. Among many metal nanoparticles, Ag-NPs have been intensely studied because of the distinct properties of their antibacterial activity [7]. Ag-NPs have been proved effective against over 650 microorganisms including bacteria (both gram-positive and negative), fungi, and viruses; however, the precise mechanism of antimicrobial action is not understood completely [46]. Ag-NP exposure to microorganisms could cause adhesion of nanoparticles to the peptidoglycan and the cell membrane [47], penetration inside the cell [48], induction of ROS [49], and damaging of intracellular structures [50]. However, bare Ag-NPs aggregate when they come into contact with bacteria; thus, they lose their active surface area and show weaker antibacterial activity [51]. To overcome this problem, nanocomposites composed of graphenic materials and Ag-NPs or other metal nanoparticles could be fabricated. GO with oxygen-containing functional groups is water soluble and therefore more biocompatible than pristine graphene. As a result, Ag-based GO nanocomposites may be used as antibacterial agents. However, the information about antimicrobial properties of graphene-based composites is limited, and mechanisms of toxicity or lack of toxicity are not fully explained.
The aim of this work was to study the action of graphene oxide-based nanocomposites decorated with Ag nanoparticles on S . aureus , S . epidermidis , E . coli e C . albicans growth; membrane integrity; and ROS production. After co-incubation with the bacterial and yeast cells for 24 h, foils coated with GO-Ag nanocomposite inhibited the growth of all tested microorganisms with varying degrees, 88.6% of E . coli , 79.6% of S . aureus , 76.5% of S . epidermidis , and 77.5% of C . albicans . This action is most probably due to an increase in cell membrane and wall penetration by the nanoparticles. Some researchers suggest that the antimicrobial activity of graphene-based nanocomposites may be due to the disruption of cell membrane integrity and oxidative stress [52].
Foils coated with GO, Ag-NPs, and GO-Ag disrupted cell membrane functionality and integrity with significant differences between the control group and the Ag-NPs and GO-Ag groups. The highest disruption of cell membranes was observed in the GO-Ag groups, 66.3% of E . coli , 59.4% of S . aureus , 54.8% of S . epidermidis , and 48.5% of C . albicans . However, foils coated with bare Ag-NPs also disrupted cell membranes. It has been proposed that Ag-NPs are able to interact with bacterial membranes by increasing permeability and changing the structure of membranes, which finally leads to cell death [50]. Ag-NPs can cause direct damage to the bacterial cell membrane. Bacteria may be killed by the combined bactericidal effects of the released Ag + ions and Ag nanoparticles. Additionally, the antimicrobial potential of Ag-NPs is also influenced by the thickness of the cell wall of the microorganisms [53]. The wall of gram-positive cells contains a thick layer (20–80 nm) of peptidoglycan, which is attached to teichoic acids. In gram-negative bacteria, the cell wall comprises a thin (7–8 nm) peptidoglycan layer and contains an outer membrane. The thicker peptidoglycan layer in gram-positive bacteria, such as S . aureus e S . epidermidis , may explain why these bacteria are more resistant to the antibacterial effects of GO-Ag.
Many studies have sought to establish a mechanism of action of antibacterial activity exhibited by silver in both its colloidal and ionic form. A disruption of membrane functionality from an interaction between released Ag + ions and the cell membrane and extensive cell membrane damage caused by the formation of ROS ultimately causes damage to the cell due to oxidative stress. Additionally, Ag + ions could cause dysfunction of the respiratory electron transport chain by uncoupling it from oxidative phosphorylation by inhibiting respiratory chain enzymes [54]. Foils coated with Ag-NPs and GO-Ag increased the ROS production of all tested microorganisms compared to the control group. The biological targets are DNA, RNA, proteins, and lipids. Lipids are one major target during oxidative stress. Free radicals can directly attack polyunsaturated fatty acids in bacterial and yeast membranes and activate peroxidation of lipids. A fundamental effect of lipid peroxidation is a decrease in membrane fluidity, which can significantly disrupt membrane-bound proteins. DNA is also a main target. Mechanisms of DNA damage involve abstractions and addition reactions by free radicals leading to carbon-centered sugar radicals and OH- or H-adduct radicals of heterocyclic bases. The sugar moieties producing single- and double-strand breaks in the backbone, adducts of base and sugar groups, and cross-links to other molecules can block replication. Foils coated with GO increased the ROS production at very low levels. However, Hu et al. [55] demonstrated that GO had a detrimental effect on E . coli due to decreased production of ATP and increased ROS production. Zhao et al. [56] reported the antibacterial activity of GO and reduced GO. Also, Gurunathan et al. [57] presented that GO and reduced GO showed significant antibacterial activity in a concentration- and time-dependent manner. Their results demonstrated that oxidative stress is a key mechanism for the antibacterial activity of GO and reduced GO through ROS generation. Nanda et al. [53] reported the effect of cystamine-conjugated GO against E . coli , S . typhimurium , E . faecalis , and B . subtilis with ROS production and high antibacterial activity.
Kurantowicz et al. [20] confirmed that bacteria could adhere to the GO surface, which results in the highest antibacterial activity. GO is characterized by a high degree of oxygenated functional groups:carbonyl, carboxylate, and hydroxyl. We hypothesize that these groups can be attractive groups for bacterial and yeast attachment. These groups are present on a large range of nutrients (amino acids, fatty acids) which are commonly recognized by microorganisms. In the present study, foils coated with GO induced membrane disruption and ROS production at a lower level than the Ag-NP and Ag-GO groups; however, cell viability was decreased, which is likely connected to the smaller active surface of GO after ultrasonic modifications.
Conclusões
Ag-NPs, GO, and Ag-GO nanocomposites demonstrated the antibacterial activity that is stronger against gram-negative bacteria (E . coli ) versus gram-positive bacteria (S . aureus e S . epidermidis ) and yeast (C . albicans ) The results showed that the decoration of GO with Ag-NPs promotes a synergistic effect and reduces dramatically the concentrations required to inhibit all tested bacterial and yeast strains. The antimicrobial potential of Ag-GO is also influenced by the thickness of the cell wall of the microorganisms. The thicker peptidoglycan layer in gram-positive bacteria, such as S . aureus e S . epidermidis , may explain why these bacteria are more resistant to the antibacterial effects of GO-Ag. A disruption of membrane functionality from an interaction between released Ag nanoparticles/Ag + ions and the cell membrane and extensive cell membrane damage caused by the formation of ROS ultimately caused damage to the cell due to oxidative stress. In order to explain the mechanism of ROS production, additional studies are needed. Our research indicates the potential applicability of GO-Ag as an antimicrobial agent.
Abreviações
- AFM:
-
Força atômica microscópica
- Ag-NPs:
-
Silver nanoparticles
- DLS:
-
Espalhamento de luz dinâmico
- GO:
-
Graphene oxide
- GO-Ag:
-
Graphene oxide decorated with silver nanoparticles
- LDE:
-
Laser Doppler electrophoresis
- LDH:
-
Lactate dehydrogenase
- ROS:
-
Espécies que reagem ao oxigênio
- SEM:
-
Microscopia eletrônica de varredura
- XRD:
-
Difração de raios X
Nanomateriais
- Nanofibras de polímero por eletrofiação decoradas com nanopartículas de metal nobre para detecção química
- Nanotubos de titanato Nanocompósitos de óxido de grafeno decorado:Preparação, Retardância de Chama e Fotodegradação
- Novos nanocompósitos de poliestireno com polianilina dopada com ácido lauril sulfúrico
- Células endoteliais de segmentação com nanopartículas de GaN / Fe multifuncionais
- Biossegurança e capacidade antibacteriana do grafeno e do óxido de grafeno in vitro e in vivo
- Efeitos sinérgicos de nanopartículas de Ag / BiV1-xMoxO4 com atividade fotocatalítica aprimorada
- Nanocompósitos de poli (N-isopropilacrilamida) magnético:efeito do método de preparação nas propriedades antibacterianas
- Promoção do crescimento celular SH-SY5Y por nanopartículas de ouro modificadas com 6-mercaptopurina e um peptídeo penetrador de neurônio
- Atividade antibacteriana de solução de nanopartículas de prata / quitosana preparada in situ contra cepas de Staphylococcus aureus resistentes à meticilina
- Avanços recentes em métodos sintéticos e aplicações de nanoestruturas de prata



