Síntese e propriedades de pontos quânticos de CdTe com liga de Mn com emissão de azul solúvel em água
Resumo
Neste trabalho, preparamos pontos quânticos de CdTe e séries de Cd 1-x Mn x Pontos quânticos com liga de Te com distribuição de tamanho estreita por uma reação de troca iônica em solução de água. Descobrimos que os picos de fotoluminescência são deslocados para energias mais altas com o aumento de Mn 2+ contente. Até agora, este é o primeiro relatório de pontos quânticos baseados em CdTe emissores de azul. Por meio da voltametria cíclica, detectamos características da atividade eletroquímica dos níveis de energia do manganês formados no interior do Cd 1-x Mn x Lacuna de banda de pontos quânticos com liga de Te. Isso nos permitiu estimar sua posição de energia. Também demonstramos comportamento paramagnético para Cd 1-x Mn x Pontos quânticos com liga de te que confirmaram o sucesso da reação de troca iônica.
Histórico
As propriedades ópticas dos pontos quânticos (QDs) podem ser manipuladas por dopagem / liga por meio do projeto da composição. Consequentemente, a possibilidade de controle sobre a incorporação de elementos de dopagem / liga em redes QDs desempenha um papel importante para um grande número de aplicações. Em particular, os QDs com liga de Mn são um dos materiais mais promissores para detecção de fluorescência e imagem por ressonância magnética. Consequentemente, técnicas de síntese já foram desenvolvidas para a obtenção de Mn 2+ -dopado / ligado ZnS, ZnSe, CdSe, CdS e núcleo / casca CdTe / CdS QDs [1,2,3,4,5,6]. Há também uma série de trabalhos que descrevem as capacidades do Mn 2+ - e Zn 2+ síntese de QDs de CdTe dopado / ligado [7,8,9,10]. A obtenção de tais composições em solução aquosa é fortemente dependente do pH, o que torna a dopagem difícil. Cheng et al. mostraram que o meio alcalino impediu a nucleação e o crescimento de CdTe QDs com liga de Zn [10]. Além disso, há uma alta probabilidade de aparecimento de Zn (OH) 2 na superfície dos QDs que inibe o crescimento dos QDs iniciais, formando uma camada de ZnO na superfície dos QDs. Processos semelhantes ocorrem na tentativa de preparar um CdSe QDs com liga de Mn em solução aquosa alcalina [11]. Neste caso, Mn 2+ a solvatação ocorre em vez da troca iônica de Cd 2+ por Mn 2+ . Por outro lado, a diferença da constante de solubilidade MnTe e CdTe indica reação de substituição ineficaz entre Mn 2+ e CdTe [12].
Neste trabalho, aplicamos o procedimento sintético descrito em nosso trabalho anterior [13] para a síntese de Cd 1 − x Mn x QDs com liga de te. Para garantir um processo de liga de Mn bem-sucedido, as condições ideais de pH neutro foram escolhidas. Tal abordagem eliminou a formação de hidróxido de manganês durante a síntese que nos permitiu obter Cd emissor de azul 1 − x Mn x QDs com liga de Te por uma reação de troca iônica. Os estudos sistemáticos de suas propriedades ópticas e eletroquímicas permitem um melhor entendimento das mudanças na estrutura de banda durante a transformação de CdTe QDs em Cd 1 − x Mn x QDs com liga de te.
Métodos
Síntese de CdTe e Cd 1-x Mn x QDs de te-liga
CdTe e Cd estabilizado com ácido tioglicólico solúvel em água 1-x Mn x QDs com te-liga foram sintetizados de acordo com nosso método de três etapas modificado relatado anteriormente [13]. Primeiramente, os nanoclusters de CdTe foram sintetizados usando um método fácil de temperatura ambiente [14] com ácido tioglicólico como estabilizador. Os nanoclusters de CdTe obtidos foram divididos em seis diferentes alíquotas de 50 ml. Em segundo lugar, as soluções coloidais obtidas de nanoclusters de CdTe foram submetidas a Mn 2+ liga devido ao processo de troca iônica com diferentes quantidades de MnSO 4 sal em alíquotas de 50 ml soluções sob sonicação. As concentrações de Mn 2+ os íons adicionados foram 1, 5, 10, 15 e 20% do Cd 2+ conteúdo nas misturas de reação (RM). Além disso, uma alíquota de nanoclusters de CdTe puro foi usada como controle. A etapa final foi um tratamento térmico possuído por aquecimento por micro-ondas no forno de micro-ondas a 700 W por 3 min.
Caracterização de materiais e procedimentos de medição
Os espectros de absorção e fotoluminescência (PL) foram medidos à temperatura ambiente pelo espectrofotômetro OceanOptics USB-2000. Os voltamogramas cíclicos (CV) foram registrados usando um Potenciostato / Galvanostato “ΠИ-50-1” controlado por computador. Um sistema de três eletrodos consistiu em um eletrodo de trabalho de platina, um contraeletrodo de carbono vítreo e um eletrodo de referência de Ag / AgCl. Os voltamogramas cíclicos foram obtidos pela varredura do potencial de - 2 a 2 V a uma taxa de varredura de 100 mV s -1 . Imagens de microscopia eletrônica de transmissão (TEM) obtidas com o microscópio Selmi TEM-125 K a uma tensão de aceleração de 80,00 kV. A análise elementar do Cd solúvel em água 1-x Mn x As amostras de QD com te-liga purificadas por múltiplas precipitações foram medidas por espectroscopia de emissão atômica С115М1 (AES). Os espectros de EPR foram registrados usando o espectrômetro EPR de banda Х “Radiopan” a 300 K. Modulação de cem quilohertz do campo magnético com amplitude de 0,1 mT. Programas visuais de EPR foram usados para o processamento (deconvolução, ajuste e modelagem) dos espectros obtidos [15]. Amostras de pó contendo QDs foram preparadas por precipitação de QDs da solução aquosa pelo método descrito em [16]. As amostras foram secas a 35 ° C durante 5 h. A composição de fase das amostras foi determinada por medições de XRD em pó usando o difratômetro Bruker D8 Advance. A identificação da fase cristalina do Cd 1-x Mn x Foi feito usando o cartão de banco de dados XRD:ICSD no. 040413 (versão do software Match! 3.6.0.111).
Resultados e discussão
Caracterização estrutural do CdTe e Cd 1-x Mn x QDs de te-liga
Análise TEM
As imagens TEM de Cd 0,91 Mn 0,09 QDs com te-liga indicaram que o diâmetro médio é consistente com o diâmetro do CdTe QDs calculado a partir das medidas espectroscópicas de acordo com o método descrito em [14]. A Figura 1 mostra uma imagem TEM para Cd 0,91 Mn 0,09 QDs com liga de te. A grande maioria dos QDs com tamanho médio de 2,3 ± 0,3 nm foi observada. Isso confirma nossa suposição de que o tamanho das partículas permanece inalterado durante a liga de Mn. Além disso, foram observados objetos maiores de forma irregular. Pode-se ver que esses objetos são compostos por vários QDs de diâmetro menor. Com base nesses dados, podemos concluir que objetos maiores são agregados formados durante a preparação das amostras para análise TEM.
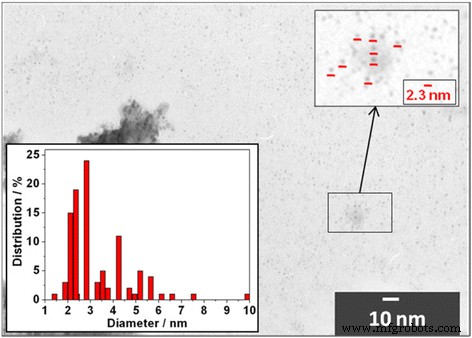
Imagem TEM de Cd 0,91 Mn 0,09 QDs com liga de te. Inserção:histograma ilustrando o Cd 0,91 Mn 0,09 Distribuição de diâmetro QD de te-liga
Análise de espectroscopia de emissão atômica
Foi mostrado anteriormente que apenas cerca de 20% do Cd 2+ Os íons da solução precursora participam da formação dos CdTe QDs por este método de síntese [13].
A composição elementar do CdTe e da série de Cd 1-x Mn x QDs com liga de te foram determinados por espectroscopia de emissão atômica (AES). O conteúdo de cádmio e manganês foi avaliado pela razão de Cd:Mn (mg / l) para a série de Cd 1-x Mn x QDs te-ligados com diferentes conteúdos de Mn 2+ íons (Tabela 1).
É interessante notar que a formação de liga de Mn ocorreu de forma desigual com o aumento de Mn 2+ concentração nas misturas de reação. É claramente visto que a adição em cerca de 1% Mn 2+ íons (em relação ao conteúdo de Cd 2+ íons na mistura de reação) para a solução coloidal recentemente preparada de nanoclusters de CdTe leva à formação de Cd 0,96 Mn 0,04 QDs com liga de te. Por outro lado, quando a concentração de Mn adicionado 2+ foi de 5%, a formação de Cd 0,97 Mn 0,03 Observou-se QDs com liga de te. Essa discordância pode sugerir que o processo de liga de Mn é mais eficiente na presença de um pequeno excesso do componente de liga. Uma adição adicional de 10, 15 e 20% Mn 2+ íons leva a uma liga consistente de Mn com CdTe QDs.
Caracterização espectroscópica
As propriedades ópticas do CdTe e Cd 1-x preparados Mn x QDs com liga de Te foram estudados por meio de absorção na região de Vis e espectros de fluorescência. A Figura 2 ilustra uma absorção típica (a) e espectros PL (b) de CdTe e série de Cd 1-x Mn x QDs com liga de te. Dependendo do Mn incorporado 2+ em CdTe, observamos um deslocamento hipsocrômico dos picos de absorção para o comprimento de onda mais curto. Além disso, o desvio para o azul dos picos de PL de 542 para 496 nm foi observado. Há uma certa incompatibilidade de deslocamento hipsocrômico de absorção e picos de PL para as amostras 2 (linha vermelha) e 3 (linha azul), que é provavelmente causada por liga irregular de Mn.
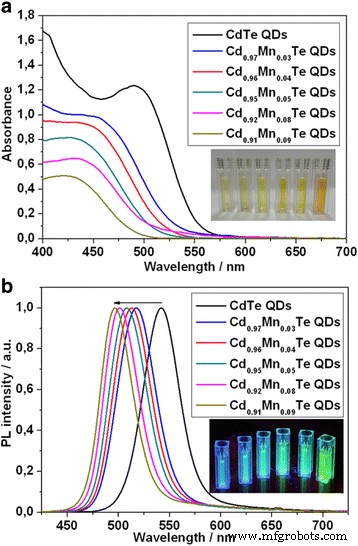
Absorção ( a ) espectros de CdTe e série de Cd 1-x Mn x QDs te-ligados com diferentes conteúdos de Mn 2+ íons. Detalhe:as imagens de CdTe e série de Cd 1-x Mn x QDs com liga de te sob a luz da lâmpada da luz do dia. PL normalizado ( b ) espectros de CdTe e série de Cd 1-x Mn x QDs te-ligados com diferentes conteúdos de Mn 2+ íons. Detalhe:as imagens de CdTe e série de Cd 1-x Mn x Te QDs sob luz ultravioleta
Deve-se notar que a intensidade de fluorescência do Cd 1-x Mn x QDs te-ligados diminuíram com o aumento de Mn 2+ conteúdo de íons (arquivo adicional 1:Figura S1). Isso pode ser explicado pela conjunção parcial de Mn 2+ íons que não participam do processo de liga e presença de um estabilizador (ácido tioglicólico), que pode extinguir a fluorescência dos QDs [17].
Caracterização voltamétrica cíclica
Um método de voltametria cíclica (CV) foi aplicado para entender as mudanças na estrutura de banda como resultado da transformação de CdTe QDs em Cd 1-x Mn x QDs te-ligados devido ao aumento de Mn 2+ contente.
No CV típico de QDs de CdTe coloidal, observamos (Fig. 3a) picos catódicos e anódicos em - 1,00 V (marcado como C1) e 1,48 V (marcado como A1), respectivamente. O valor da energia do bandgap de 2,48 eV, calculado de acordo com o método descrito em [18], concorda bem com o bandgap óptico de 2,50 eV obtido a partir dos máximos de pico de absorção.
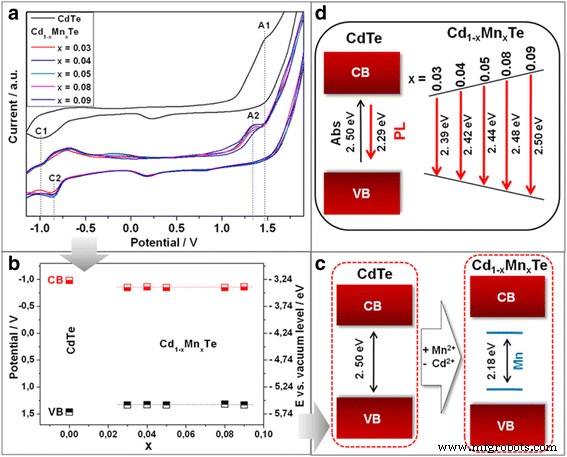
Voltamogramas cíclicos de CdTe coloidal e séries de Cd 1-x Mn x QDs te-ligados com diferentes Mn 2+ conteúdo de íons ( a ) Gráfico das posições das bordas da banda de valência (VB) e condução (CB) para CdTe e a série de Cd 1-x Mn x QDs com liga de Te, obtidos a partir das respectivas posições de pico anódico (A) e catódico (C) ( b ) Esquema da eletroquímica ( c ) e óptico ( d ) formação de sinal
Com base nas propriedades ópticas do Cd 1-x Mn x QDs com te-liga, esperávamos observar a oxidação em potenciais mais positivos e a redução em potenciais mais negativos para Cd 1-x Mn x QDs te-ligados, com aumento de Mn 2+ conteúdo em Cd 1-x Mn x QDs com liga de Te devido ao aumento da energia do gap. No entanto, a separação entre o pico de oxidação A2 e o pico de redução C2 é muito pequena para se correlacionar com a energia do intervalo de banda calculada a partir dos espectros de fotoluminescência. Curiosamente, a diferença de potencial de 2,18 V entre C2 e A2 é absolutamente idêntica para toda a série de Cd 1-x Mn x Amostras de QDs com liga de Te (Fig. 3a, b).
Como mostrado por Beaulac et al., Tempos de decaimento de PL excitônico de até 5 μs foram observados para Cd coloidal 1-x Mn x Se ( x =0,004 ± 0,002) QDs (d ≈ 2,2 nm) a 293 K, que surgem como resultado do equilíbrio térmico entre os estados excitônicos CdSe e o estado excitado do campo de ligante de vida muito longa do Mn 2 + dopantes. Portanto, o doping Mn não extingue o PL excitônico do Cd 1-x Mn x Se QDs. Em vez disso, os efeitos de extinção de si mesmo do Mn 2+ PL por transferência de energia de retorno assistida termicamente para o Cd 1-x Mn x Os estados excitônicos Se QDs ocorrem. [4].
Podemos assumir que no caso de Cd coloidal 1-x Mn x QDs com liga de Te (d ≈ 2,3 nm) à temperatura ambiente, ocorre um fenômeno muito semelhante. Usando o método CV, a atividade eletroquímica dos níveis de energia do manganês "escuro" dentro do Cd 1-x Mn x O gap de banda QDs com liga de Te foi detectado (Fig. 3b, c). Propriedades ópticas do Cd 1-x Mn x QDs com te-ligas mostram um aumento da energia do gap com aumento de Mn 2+ conteúdo como resultado de fenômenos de transferência de energia de retorno (Fig. 3d).
Análise de XRD
Arquivo adicional 1:A Figura S2 mostra os espectros de XRD para CdTe e série de Cd 1-x Mn x Amostras secas QD com liga de Te que foram precipitadas de uma solução aquosa usando álcool isopropílico.
O espectro de XRD para varredura de CdTe QDs ao longo da faixa de dois teta de 20 ° -60 ° mostra o pico de difração a 25 °, que é atribuído aos (111) planos de cristal de CdTe com estrutura cristalina cúbica [19]. Este pico é significativamente maior do que o dos materiais a granel devido ao tamanho pequeno dos QDs com distribuição de tamanho estreita. O sinal nos padrões de XRD de todas as séries de Cd 1-x Mn x Os QDs com liga de Te são deslocados para ângulos mais altos. O pico em 30 ° –35 ° pode ser deconvoluído em dois picos em 30 ° e 35 °, que são atribuídos aos planos (200) e (220) de Cd 1-x Mn x Liga de te. Esses resultados podem indicar a formação de Cd 1-x Mn x Te com estrutura cúbica. Esses dados de XRD confirmam que os CdTe QDs foram submetidos ao processo de liga de Mn com sucesso. Notavelmente, aquele pico centrado em 25 ° decai no padrão de XRD de Cd 0,97 Mn 0,03 Os QDs ligados e desaparecem nos padrões de XRD das amostras com Mn mais alto 2+ contente. No caso de Cd 0,97 Mn 0,03 Na amostra de QDs, concluímos a formação do núcleo / casca CdTe / Cd 1-x Mn x Te QDs onde o sinal de Cd 1-x Mn x O shell rastreia o sinal do núcleo de CdTe. Para todas as amostras subsequentes, um pico de difração amplo em 30 ° -35 ° pode testemunhar a liga de Mn adicional de QDs de CdTe e a formação de um Cd mais espesso 1-x Mn x Te shell. Geralmente, isso leva à formação de QDs com maiores teores de manganês.
Medições EPR
Os espectros EPR de Cd 0,97 Mn 0,03 Os QDs com liga de Te são mostrados na Fig. 4. O espectro consiste em seis linhas assimétricas que são sobrepostas no amplo sinal subjacente. A presença de seis linhas no espectro é típica para Mn 2+ íons nos sistemas desordenados [2, 20,21,22]. No entanto, a forma do espectro é mais complexa do que o trivial Mn 2+ -relacionado sinal. Uma análise detalhada mostrou que o espectro experimental de EPR pode ser descrito como uma superposição de três sinais:gaussiana ampla com largura de linha de 50 mT e dois sextetos com linhas espaçadas por 10 e 6 mT, respectivamente.
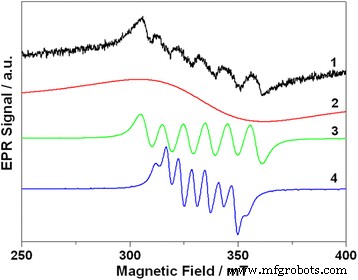
Espectro EPR de Cd 0,97 Mn 0,03 QDs com liga de Te e sua deconvolução:1 - espectro experimental; 2 — Curva gaussiana com largura de linha pico a pico 50 mT. 3 — sexteto com divisão de ~ 10 mT. 4 — sexteto com divisão de ~ 6 mT. Detalhes veja no texto
Sinal EPR de forma gaussiana centrado em g =2,0069 (sinal 2 ) pode ser atribuído a Mn 2+ íons interconectados por interação dipolo-dipolo. Esses íons estão localizados em regiões com alta concentração local de manganês e interagem entre si. Devido ao alargamento das linhas, uma forte interação dipolo-dipolo entre os íons de manganês mascara as características espectrais específicas que são características para os íons de manganês isolados e leva a um sinal EPR de linha única. Os dois outros sinais EPR (marcados como 3 e 4 ) deve ser atribuído a Mn isolado 2+ íons. Para determinar os parâmetros de Mn isolado 2+ íons e sua localização, o spin-hamiltoniano contendo eletrônica, interação Zeeman nuclear, interação hiperfina e a interação do spin do elétron com o campo cristalino (termo de divisão de campo zero) foi usado:
$$ \ widehat {H} =g \ beta \ mathbf {BS} - {g} _ {\ mathrm {N}} {\ beta} _ {\ mathrm {N}} \ mathbf {BI} + A \ mathbf { SI} + \ sum \ limits_ {n, m} {b} _m ^ m {O} _m ^ m $$
onde β e β N denotam o Bohr e os magnetos nucleares, respectivamente; B é o campo magnético externo; g e g N são os tensores g de elétron e nuclear, respectivamente; A é o tensor da interação hiperfina; S e eu são os operadores de spin mecânicos quânticos de elétrons e nucleares, respectivamente; e b n m e O n m são as constantes do campo cristalino e os operadores da mecânica quântica, respectivamente. Os valores de g , g N , β , β N e А são considerados isotrópicos (sendo isso característico para Mn 2+ iões em compostos II-VI). O conjunto de b n m os parâmetros são determinados pelos arredores de Mn 2+ e depende da simetria das posições dos íons.
O sinal 2 pode ser descrito pelos parâmetros g =2,0069 e A =- 94,5 × 10 −4 cm −4 que pode ser atribuído ao Mn isolado 2+ íons localizados na posição próxima à superfície dos QDs. Ao mesmo tempo, sinal 3 foi encontrado para ser caracterizado por parâmetros g =2,0069, A =- 57,5 × 10 −4 cm −4 e b 4 0 =27,7 × 10 −4 cm −4 . Este conjunto de parâmetros é típico para Mn 2+ na posição catiônica (Mn Cd ) de cristais de CdTe em massa.
Conclusões
A síntese do Cd emissor de azul 1-x Mn x Foram desenvolvidos QDs com liga de Te de pequeno tamanho. O estudo sistemático de suas propriedades ópticas e eletroquímicas foi fornecido. O desvio para o azul do PL atinge o pico de 542 para 496 nm durante o aumento do Mn 2+ conteúdo em Cd 1-x Mn x Observou-se QDs com liga de te. As análises de XRD e EPR confirmam a substituição bem-sucedida do cádmio por íons de manganês no processo de síntese. Cd coloidal 1-x Mn x QDs com te-ligas mostram um aumento da energia do gap com o aumento de Mn 2+ conteúdo à temperatura ambiente como resultado da transferência de energia de retorno assistida termicamente.
Abreviações
- CV:
-
Voltametria cíclica
- EPR:
-
Ressonância paramagnética de elétrons
- PL:
-
Fotoluminescência
- QDs:
-
Pontos quânticos
- TEM:
-
Microscopia eletrônica de transmissão
- TGA:
-
Ácido tioglicólico
- XRD:
-
Difração de raios X
Nanomateriais
- Síntese fácil e propriedades ópticas de pequenos nanocristais de selênio e nanorods
- Composto Híbrido de Sílica Nanoestruturada / Ouro-Celulose Ligado Amino-POSS via Processo Sol-Gel e Suas Propriedades
- Síntese de pontos quânticos do tipo II / tipo I suprimida por reabsorção / CdS / ZnS Core / Shell Quantum Dots e sua aplicação para ensaio de imunossorvente
- Síntese de pontos quânticos de carbono co-dopados com N, S ricos em piridínicos como imitações de enzimas eficazes
- O efeito do plasma sem equilíbrio de contato nas propriedades estruturais e magnéticas de Mn Х Fe3 - X О4 Spinels
- Propriedades de síntese e luminescência de nanopartículas α-NaGdF4 / β-NaYF4:Yb, Er Core – Shell solúveis em água
- Síntese verde de pontos quânticos InP / ZnS Core / Shell para aplicação em diodos emissores de luz livres de metais pesados
- Síntese de pontos quânticos de sulfeto de antimônio solúvel em água e suas propriedades fotoelétricas
- Síntese sonoquímica fácil de uma etapa e propriedades fotocatalíticas de compostos de pontos quânticos de grafeno / Ag3PO4
- Material e propriedades ópticas de pontos quânticos de carbono fluorescente fabricados a partir de suco de limão via reação hidrotérmica



