Nanopartículas de MnO2 modeladas por membrana de casca de ovo:síntese fácil e descontaminação do cloridrato de tetraciclina
Resumo
Aproveitando as vantagens das proteínas reticulares e grupos redutivos na superfície, a membrana da casca do ovo (ESM) foi selecionada para sintetizar MnO 2 nanopartículas de permanganato de potássio por meio de uma forma super simples em que o ESM atuou como molde e redutor. Este processo evitou condições de reação adversas ou pós-tratamentos complicados e, portanto, possuía os méritos da síntese verde, operação prática, baixo custo e purificação fácil. O modelo ESM MnO 2 nanopartículas (MnO 2 NPs / ESM) foram caracterizados e o conteúdo de nanomateriais no modelo foi testado. MnO 2 NPs / ESM mostraram uma boa capacidade de descontaminação do cloridrato de tetraciclina (TCH). Os materiais macroscópicos podem ser separados facilmente retirando a membrana para interromper a degradação em vez de centrifugação ou filtração. Foi estudado que 72,27% do TCH (50 mg / L) foi descontaminado em 20 min por 0,1920 g / L MnO 2 nanopartículas, e a eficiência de remoção pode chegar a 83,10% após 60 min em condição tamponada. A cinética foi estudada com ou sem tampão e concluiu-se que o processo de degradação seguia um modelo de pseudo-segunda ordem. A síntese fácil de materiais e a degradação efetiva facilitariam o nano-MnO 2 aplicações de descontaminação baseadas em
Histórico
Produtos farmacêuticos e de higiene pessoal (PPCPs) são um tipo de poluição da água emergente e são preocupados de perto pelos pesquisadores em consideração à ecologia e saúde humana [1,2,3,4,5]. Antibióticos como medicamento para tratar e prevenir infecções bacterianas são usados em todo o mundo, acompanhando os riscos preocupantes ao meio ambiente aos poucos surgindo [6]. Como representante, os medicamentos com tetraciclina (TC) têm sido usados na ciência veterinária e na aquicultura há anos [7]. No entanto, os CTs dificilmente podem ser degradados no meio ambiente e, portanto, persistem por muito tempo [8, 9], o que leva a várias influências negativas no ecossistema ou na saúde humana [10,11,12,13]. Portanto, a triagem de uma maneira fácil e eficaz de descontaminar a água contaminada com TC tornou-se um ponto importante de pesquisa. Uma técnica promissora pode ser a assistência de nanomateriais de dióxido de manganês.
Os nanomateriais de dióxido de manganês têm sido extensivamente estudados devido aos seus méritos únicos de alta área de superfície, estrutura ajustável, atividade de oxidação catalítica e eco-inofensivos [14, 15]. Portanto, nano-MnO 2 As aplicações baseadas em aplicações cobriram vários campos que vão desde catálise [16, 17], sensores [18, 19] e capacitores [20, 21] para entrega de drogas [22, 23] e terapia do câncer [24, 25]. Da mesma forma, MnO 2 nanomateriais com propriedades de adsorção e oxidação têm sido aplicados no tratamento de águas residuais. Poluentes da água, incluindo íons pesados [26], corantes orgânicos [27] e fenóis [28] tratados por MnO 2 nanomateriais foram relatados. Enquanto isso, antibióticos como levofloxacina [29], ciprofloxacina [30], norfloxacina [31], sulfametoxazol [32], sulfadiazina [33], cefazolina [34], lincosamida [35] e TCs [36, 37] foram bem-sucedidos descontaminado através de MnO 2 tratamento. Específico para antibióticos TC, MnO altamente poroso 2 nanofolhas foram utilizadas para degradar a tetraciclina, e o pH, a temperatura e a cinética com base na dose foram investigados [38]. A MnO 2 esquema baseado foi aplicado para remover o cloridrato de tetraciclina (TCH) e As (III) simultaneamente, e o efeito interativo sobre o arsênio e antibióticos durante MnO 2 o tratamento foi estudado [39]. Degradação de antibióticos de tetraciclina por MnO 2 foi realizada, e a cinética e as vias de transformação foram relatadas [40]. Embora alta eficiência de remoção de TCs tenha sido obtida nos trabalhos acima mencionados, entretanto, a operação de degradação normalmente envolvida na centrifugação ou filtração para separar o material das soluções de antibióticos, o que consumia muito tempo de tratamento e tornava o processo complicado.
A membrana da casca de ovo (ESM) como um biomaterial único com propriedades extraordinárias tem sido amplamente utilizada na ciência dos materiais [41]. A principal composição da fibra no ESM é uma proteína que confere ao ESM a capacidade de se ligar ao metal. Nanomateriais de metais nobres como Ag NPs e Au NPs foram sintetizados com sucesso usando ESM como um modelo [42,43,44]. Além disso, nanomateriais de óxido de metal, como ZnO [45], Co 3 O 4 [45], PbO [45], Mn 3 O 4 [46] e TiO 2 [47] também foram preparados por meio de modelos ESM, o que tornou a síntese fácil e sob controle e, portanto, forneceu um novo caminho para a síntese de nanopartículas de metal ou óxido de metal.
Neste trabalho, MnO 2 modelado por membrana de casca de ovo nanopartículas (MnO 2 NPs / ESM) foram sintetizados de forma simples e rápida por um método de bio-modelagem. A membrana da casca do ovo desempenhou funções duplas como molde e redutor, tornando as nanopartículas dispersas uniformemente nas membranas macroscópicas. Combinando o oxidante MnO 2 nanopartículas com a membrana fácil de manipular, MnO 2 NPs / ESM foram posteriormente aplicados à descontaminação do cloridrato de tetraciclina, em que os nanomateriais podiam ser separados facilmente simplesmente removendo as soluções.
Métodos
Materiais e aparelhos
Água desionizada com uma condutividade de 18,2 MΩ cm −1 foi usado neste experimento a partir de um sistema de purificação de água (ULUPURE, Chengdu, China). Permanganato de potássio (KMnO 4 , M w =158,03), MnO 2 pó e outros reagentes eram pelo menos de grau analítico e adquiridos de Kemiou Chemical Co. Ltd. (Tianjin, China). O cloridrato de tetraciclina (TCH, grau USP) e a glutationa (GSH, 98%) foram adquiridos da Aladdin Reagents Company (Shanghai, China). A membrana da casca de ovo (ESM) foi removida cuidadosamente de uma casca de ovo fresca obtida no refeitório de estudantes de Hongye do Instituto de Tecnologia de Taiyuan. Soluções tampão de PBS (0,2 M, pH =7,0) foram preparadas pela mistura de 39 mL de NaH 2 PO 4 solução (0,2 M) e 61 mL de Na 2 HPO 4 (0,2 M), e soluções de PBS com diferentes valores de pH foram preparadas titulando a solução acima mencionada com hidróxido de sódio ou solução de ácido clorídrico (ambas as concentrações foram 0,2 M) para os valores de pH requeridos.
Microscopia eletrônica de varredura (SEM) de MnO 2 NPs / ESM foi realizado em um microscópio eletrônico de varredura Quanta 200 FEG para a observação morfológica. Microscopia eletrônica de transmissão (TEM) e microscopia eletrônica de transmissão de alta resolução (HRTEM) de MnO 2 As NPs foram realizadas em um microscópio eletrônico de transmissão Tecnai-G20. A distribuição de tamanho de MnO 2 conforme preparado NPs foram obtidos em um medidor de partículas a laser (Malvern Nano-ZS90). A espectroscopia de fotoelétrons de raios X (XPS) foi coletada em um espectrômetro de elétrons AXIS ULTRA DLD (Kratos) com radiação monocromática Al Kα para a composição da superfície e teste do estado químico do produto. Análise de termogravimetria (TG) de ESM e MnO 2 NPs / ESM foi medido no ar a uma taxa de aquecimento de 10 ° C / min em um analisador térmico Rigaku TG (Rigaku Co. Japão). Espectroscopia de infravermelho com transformada de Fourier (FTIR) de 4000 a 400 cm −1 de ESM e MnO 2 NPs / ESM foram registrados em discos KBr em um espectrômetro Tensor II FTIR (Bruker, Alemanha), e os espectros foram processados por deconvolução. Os espectros de absorção ultravioleta-visível (UV-vis) de TCH foram registrados em um espectrofotômetro TU-1901 UV-vis (Puxi, China).
Síntese de ESM-Templated MnO 2 Nanopartículas
O modelo de membrana da casca de ovo MnO 2 nanopartículas (MnO 2 NPs / ESM) foram sintetizados por meio de um método direto e fácil. Em um processo típico, a membrana da casca do ovo foi primeiro retirada manualmente de uma casca de ovo fresca e lavada dez vezes com água desionizada para remover a clara do ovo desnecessária. Após secagem à temperatura ambiente, o ESM limpo foi então cortado em fatias com 5 mg de peso cada. Após a síntese, dez fatias de ESM foram embebidas em 20 mL de KMnO 4 (1 mmol / L) e o sistema aberto manteve a agitação à temperatura ambiente. Trinta e cinco minutos depois, as fatias de ESM foram retiradas e lavadas dez vezes com água deionizada para remover a solução redundante. Por fim, as membranas obtidas foram secas e estocadas em temperatura ambiente para posterior caracterização e uso.
Descontaminação do TCH
A descontaminação do TCH foi realizada adicionando MnO 2 NPs / ESM nas soluções de TCH de forma simples e agitada à temperatura ambiente. Vinte fatias de MnO 2 NPs / ESM foram colocados em soluções de TCH de 15 mL (50 mg / L) que foram diluídas por soluções tampão de PBS e mantidas em agitação por 60 min. Os espectros de UV-vis das soluções de TCH após o tratamento foram registrados imediatamente à temperatura ambiente. Todas as intensidades de absorção da medição de TCH foram fixadas em um comprimento de onda de 358 nm. A eficiência de remoção ( R ,%) foi calculado usando a equação abaixo:
$$ R =\ frac {C_0-C} {C_0} \ vezes 100 \% $$
onde C 0 e C (mg / L) representam as concentrações inicial e final de TCH nas soluções de tratamento, respectivamente.
Resultados e discussão
Mecanismo e monitoramento de MnO 2 Síntese de NPs / ESM
A síntese de MnO 2 NPs / ESM foi realizado em um sistema aberto com ESM como biotemplate. A membrana da casca do ovo era composta de muitas proteínas fibrosas nas quais muitos grupos redutores como –OH, –NH 2 , –SH, etc. foram intercalados. Uma reação redox in situ foi desencadeada assim que o KMnO 4 foi introduzido. Enquanto MnO 2 foi gerado, ele cresceu gradualmente em torno desses grupos ativos. Como consequência, foi disperso uniformemente na superfície de proteínas fibrosas para formar MnO 2 modelado por ESM NPs.
A Figura 1a exibiu as fotos do sistema de síntese em diferentes momentos, em que roxo KMnO 4 solução tornou-se marrom claro gradualmente e, enquanto isso, as fatias ESM brancas tornaram-se marrons (Fig. 1b, c). Para monitorar o processo sintético, a intensidade de absorção de KMnO 4 a 525 nm e o pH deste sistema foram investigados na Fig. 1d, e. Como mostrado, a intensidade de absorção de KMnO 4 diminuiu com o tempo prolongado, e o pH, ao contrário, melhorou gradualmente. Dois conjuntos de dados mostraram uma plataforma após 35 min e, portanto, o tempo de síntese foi selecionado. O aumento do pH foi atribuído à formação de –OH durante a reação e um curso de reação foi especulado abaixo:
ESM (vermelho) + KMnO 4 + H 2 O → MnO 2 / ESM (Ox) + OH¯ + K +
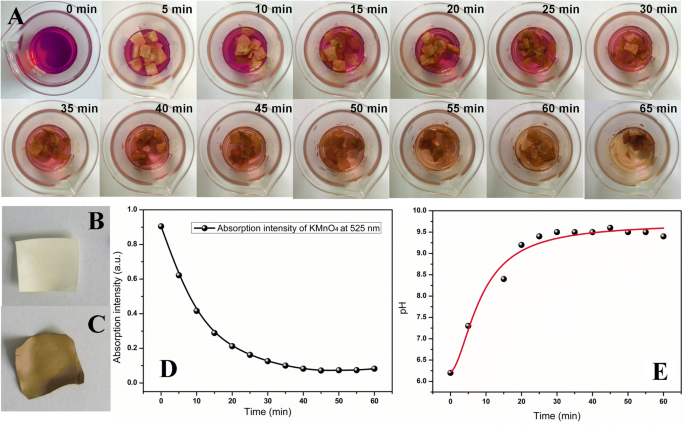
a As fotos do sistema sintético em momentos diferentes. b A imagem da fatia ESM antes da reação redox. c A imagem de MnO 2 NPs / ESM. d A intensidade de absorção de KMnO 4 a 525 nm. e pH do sistema sintético em momentos diferentes
Caracterização de MnO 2 NPs / ESM
A morfologia do MnO obtido 2 NPs / ESM foi investigado por microscopia eletrônica de varredura (SEM) na Fig. 2. Rede de fibrina multicamadas e de interseção foi observada na Fig. 2a, b. Após a amplificação, muitas partículas foram encontradas uniformemente revestidas na superfície das proteínas fibrosas. Portanto, concluiu-se que o ESM atuou não apenas como redutor, mas também como molde durante a síntese. Para investigar melhor o tamanho do MnO 2 partículas, foi realizado um teste de dimensionamento de partículas a laser. A fim de descartar a possibilidade de que as partículas com 4,8 nm fossem proteínas decompostas, MnO 2 NPs / ESM e quantidades iguais de ESM em branco (controle) foram primeiro colocados em soluções de NaOH (0,1 M) e fervidos por 30 min e, em seguida, filtrados para formar soluções para atender à condição de teste. Foi encontrado no arquivo adicional 1:Figura S1 que o tamanho médio de MnO 2 NPs era 4,8 nm. As fotos de MnO 2 NPs / ESM antes e depois do tratamento com NaOH foram exibidos no arquivo adicional 2:Figura S2A. Era óbvio que a cor marrom da membrana desbotou evidentemente, enquanto a membrana se manteve inalterada após o tratamento com NaOH, indicando que o MnO 2 NPs foram liberados do modelo. Ao pensar sobre o problema de que o tamanho da proteína da casca do ovo pode interferir nos resultados, as soluções filtradas após o tratamento com NaOH foram obtidas tanto do ESM em branco quanto do MnO 2 (Arquivo adicional 2:Figura S2B) para ser incolor e marrom, respectivamente. Além disso, os dados de distribuição de tamanho de ESM após o tratamento com NaOH exibiram um tamanho médio de 1,7 nm no arquivo adicional 2:Figura S2C. Portanto, a possibilidade de que as partículas com 4,8 nm fossem proteínas decompostas do próprio ESM foi descartada. Com base nisso, TEM foi capturado após o filtrado acima mencionado ter sido dialisado. Conforme mostrado na Fig. 2c, nanopartículas esféricas foram observadas e o tamanho era consistente com o do arquivo adicional 1:Figura S1. A imagem HRTEM na Fig. 2d indicou um espaçamento de rede de 2,5 Å que era bem coincidente com o plano de rede (400) de α-MnO 2 [48].

As imagens SEM de MnO 2 NPs / ESM com barras de escala diferentes (2 μm ( a ) e 200 nm ( b )). O TEM ( c ) e HRTEM ( d ) imagens de MnO 2 NPs, as barras de escala eram de 10 nm e 5 nm, respectivamente
Além disso, a técnica de espectroscopia de fotoelétrons de raios X (XPS) foi realizada para a composição da superfície e análise elementar do MnO obtido 2 NPs / ESM. O espectro de varredura completa (Fig. 3a) indicou que o material sintetizado era composto pelos elementos Mn 2p, O 1s, N 1s e C 1s. Elemento C 1s, N 1s e O 1s parciais vieram do modelo ESM. Os espectros XPS parciais de Mn 2p e O 1s foram medidos para estudar os detalhes. Conforme mostrado na Fig. 3b, dois picos em 653,8 e 642,0 eV podem ser atribuídos a Mn 2p 1/2 e Mn 2p 3/2 , respectivamente. O espectro de O 1s (Fig. 3c) pode ser dividido em três picos de componentes com energia de ligação em 532,6, 531,4 e 530,5 eV, que foram atribuídos a H – O – H, Mn – O – H e Mn – O – Mn , respectivamente. Os dados acima demonstraram que o material como preparado foi com modelo ESM MnO 2 NPs.
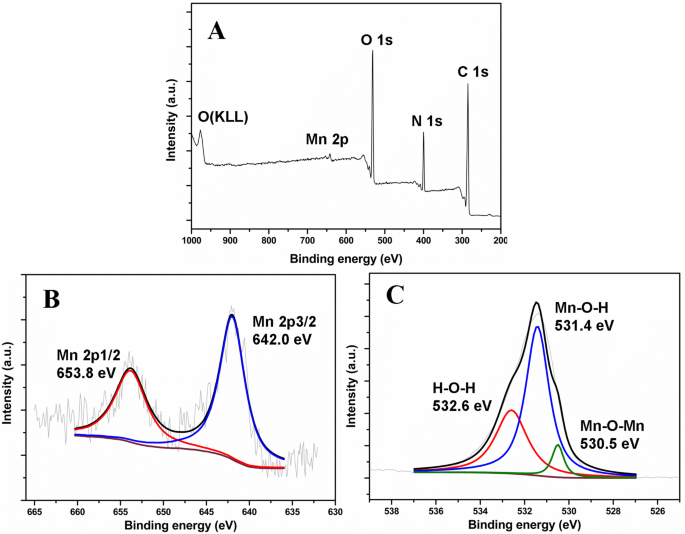
O XPS ( a ) verificação completa, ( b ) Mn 2p, ( c ) Espectros de O 1s de MnO conforme preparado 2 NPs / ESM
Para verificar ainda mais este resultado, a solução GSH foi aplicada ao material de teste assim obtido, inspirado por uma reação especial entre GSH e MnO 2 [49, 50]. Conforme mostrado no arquivo adicional 3:Figura S3, a cor marrom de MnO 2 desapareceu após imersão na solução de GSH por 1 min, indicando que os materiais revestidos no ESM eram MnO 2 . Além disso, a análise de termogravimetria (TG) foi realizada para medir o teor de massa de MnO 2 no ESM. As curvas pretas e vermelhas no arquivo adicional 4:Figura S4 representava as mudanças de massa de apenas ESM e MnO 2 NPs / ESM, respectivamente. A qualidade relativa do ESM era quase zero a 600 ° C, indicando que o ESM estava totalmente queimado. No entanto, a qualidade relativa do modelo ESM MnO 2 NPs permaneceram em 2,61% depois que o ESM foi queimado. Foi relatado que MnO 2 foi decomposto termicamente a 500 ° C e convertido em Mn 2 O 3 [51]. Além disso, posterior decomposição térmica de Mn 2 O 3 para Mn 3 O 4 ocorreu acima de 1000 ° C [52]. Portanto, o conteúdo de massa de 2,61% a 800 ° C obtido neste experimento refletiu o conteúdo de Mn 2 O 3 . De acordo com a conservação em massa de Mn, o MnO original 2 o carregamento de conteúdo no ESM foi calculado em 2,88%.
Espectros de FTIR (arquivo adicional 5:Figura S5) de ESM e MnO 2 NPs / ESM foram coletados após a moagem dos materiais em pó. As interações entre proteínas e nanopartículas envolvem principalmente mudanças na estrutura secundária, que são refletidas na banda da amida I ~ 1650 cm −1 (que pode mudar um pouco) ou amida II ~ 1550 cm −1 . No entanto, não houve mudanças óbvias na posição do pico em torno de 1650 ou 1550 cm −1 de ESM antes e depois de MnO 2 estava envolvido, o que era diferente dos resultados relatados anteriormente que poderiam demonstrar a mudança estrutural da proteína [53]. A fim de entrar em detalhes e evitar perder quaisquer pequenas alterações, a deconvolução foi aplicada a esses espectros. Mesmo que nenhum pico observável tenha sido mostrado por volta de 1650 ou 1550 cm −1 , um novo pico em 506 cm −1 apareceu após MnO 2 Carregamento de NPs, e foi associado ao modo vibracional característico de Mn – O [54].
Mn tem vários estados de oxidação, portanto, existem alguns tipos de óxidos, como Mn 2 O 3 , MnO e MnO 2 . A energia de ligação de Mn 2 O 3 é próximo ao de MnO 2 . A fim de examinar o estado de oxidação de Mn neste trabalho, o HRTEM de materiais como preparados foi fotografado e exibido na Fig. 2d. O espaçamento de rede de 2,5 Å detectado é bem coincidente com o plano de rede (400) de α-MnO 2 [48]. Além disso, nossos materiais Mn foram obtidos com base na reação redox entre KMnO 4 e ESM sob a condição neutra que favoreceu a formação de MnO 2 em vez de outros estados de oxidação [55]. É importante ressaltar que os materiais preparados possuem a atividade de reação com GSH (arquivo adicional 3:Figura S3), que também é um testemunho de que a nanopartícula é MnO 2 [49, 50]. Também foi relatado que MnO 2 pode ser termicamente decomposto a 500 ° C e convertido em Mn 2 O 3 [51]. A curva TG dos materiais preparados no arquivo adicional 4:Figura S4 mostra uma perda de peso óbvia em torno de 500 ° C, indicando a transformação de MnO 2 para Mn 2 O 3 , que é outro testemunho de que o estado de oxidação de Mn é MnO 2 .
Descontaminação TCH por MnO 2 NPs / ESM
Aproveitando as vantagens do MnO oxidativo 2 NPs e modelo macroscópico, MnO 2 NPs / ESM foram aplicados à descontaminação do cloridrato de tetraciclina (TCH) devido à sua remoção eficaz e fácil operação. A Figura 4a exibiu a intensidade de absorção dependente do tempo de TCH em 358 nm tratado apenas por ESM (preto) e MnO 2 NPs / ESM (vermelho). Foi demonstrado que a intensidade de absorção se manteve inalterada na presença de ESM apenas. No entanto, ele caiu abruptamente primeiro e se achatou gradualmente sob MnO 2 Tratamento NPs / ESM. Este contraste evidente demonstrou a capacidade de MnO 2 NPs / ESM para descontaminação TCH. Da mesma forma, os espectros de absorção de UV-vis de TCH após o tratamento com ESM dificilmente mudaram, mas o pico de absorção em 358 nm diminuiu obviamente após MnO 2 Descontaminação de NPs / ESM (Fig. 4b). A Figura 4c investigou a variação do espectro de absorção de TCH, em que o pico de absorção em 270 nm diminuiu nos primeiros 10 min, mas outro pico em 358 nm diminuiu com o tempo. A eficiência de remoção dependente do tempo por MnO 2 A descontaminação de NPs / ESM foi calculada na Fig. 4d, e verificou-se que a eficiência de remoção foi de 72,27% em 20 min e pode chegar a 83,10% em 60 min.
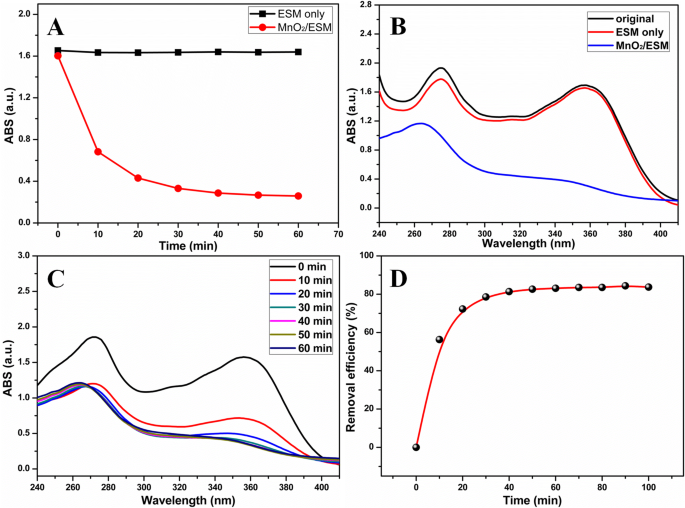
a A intensidade de absorção dependente do tempo de TCH por ESM e MnO 2 Tratamento NPs / ESM. b Os espectros de absorção de UV-vis de TCH antes e depois de ESM ou MnO 2 Tratamento NPs / ESM. c Os espectros de absorção de UV-vis dependentes do tempo de TCH e ( d ) eficiência de remoção tratada por MnO 2 NPs / ESM. (Condições:20 fatias de MnO 2 NPs / ESM ou ESM, a concentração inicial de TCH era de 50 mg / L, o pH controlado era de 3,0)
Efeito do pH e do tampão na descontaminação de TCH
O pH desempenhou um papel importante no MnO 2 com base na degradação oxidativa, e o efeito do pH na descontaminação do TCH neste trabalho foi investigado. A Figura 5a exibiu a intensidade de absorção de TCH antes e depois de MnO 2 Tratamento de NPs / ESM por 60 min sob diferentes pH, e a eficiência de remoção correspondente foi calculada na Fig. 5b. Foi demonstrado que a descontaminação ideal de TCH por MnO 2 NPs / ESM foi alcançado sob tampão PBS com um pH de 3,0. Além disso, a descontaminação TCH por MnO 2 NPs / ESM sem solução tampão foi investigado na Fig. 5c, em que a intensidade de absorção de TCH diminuiu gradualmente e o pH do sistema de degradação foi melhorado de forma constante. O mesmo fenômeno de aumento do pH durante o processo de descontaminação também foi relatado em trabalho anterior [38]. Vale a pena notar que a eficiência de remoção sem tampão aumentou mais rapidamente do que sob uma condição de tampão no início (primeiros 20 minutos). Então, com o passar do tempo, no entanto, a eficiência de remoção com tampão excedeu a sem tampão após 30 min (83,10% para a condição com tampão e 78,37% para a condição sem tampão em 60 min). As eficiências de remoção foram monitoradas por meio de variações de concentração de TCH que foram calculadas a partir do gráfico de calibração linear (arquivo adicional 6:Figura S6 e arquivo adicional 7:Figura S7). Sob a condição tamponada, os íons salinos do PBS impediram a difusão das moléculas de TCH na superfície de MnO 2 NPs para reação posterior e, portanto, a taxa de reação foi menor do que sem um tampão. No entanto, o aumento do pH do sistema de reação junto com o tempo sob condição sem tamponamento limitou a capacidade oxidativa de MnO 2 NPs e, portanto, a eficiência de remoção não pode atingir a obtida sob um pH ótimo controlado.
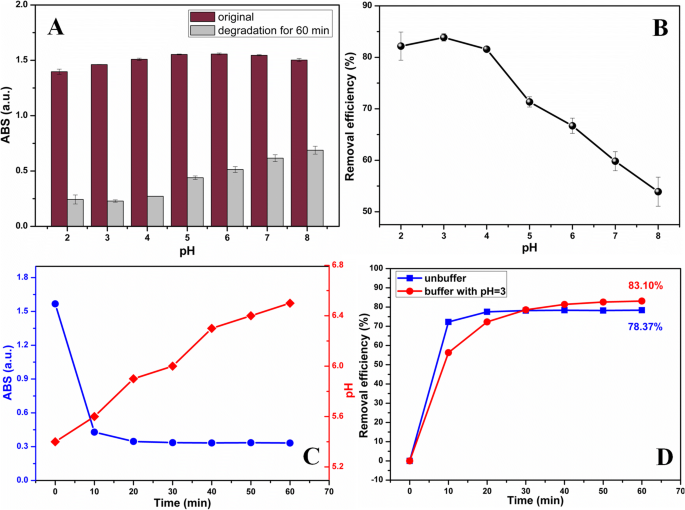
a A intensidade de absorção de TCH antes e depois da degradação e ( b ) eficiência de remoção em diferentes pH. c A intensidade de absorção dependente do tempo de TCH e variação de pH sob condição sem tamponamento. d Comparação da eficiência de remoção de TCH sob condições tamponadas e não tamponadas. (Condições:20 fatias de MnO 2 NPs / ESM, a concentração inicial de TCH era de 50 mg / L.)
Estudo cinético da descontaminação TCH
Para entender melhor a degradação do TCH por MnO 2 NPs / ESM, o estudo cinético foi realizado alterando a concentração inicial de TCH ou a dose de MnO 2 . Nós investigamos a cinética de degradação por diferentes quantidades de MnO 2 sob condições de buffer. A Figura 6a exibiu a intensidade de absorção dependente do tempo de TCH degradado por diferentes doses de MnO 2 (0,0960, 0,1440 e 0,1920 g / L), e as eficiências de remoção correspondentes foram calculadas na Fig. 6b. E os gráficos cinéticos lineares por pseudo-primeira ordem e pseudo-segunda ordem foram ajustados na Fig. 6c, d, respectivamente. Além disso, a degradação em diferentes concentrações iniciais de TCH (30, 50 e 70 mg / L) com tampão foi estudada por meio do monitoramento da intensidade de absorção (Fig. 7a) e da eficiência de remoção (Fig. 7b) em momentos diferentes. A Figura 7c, d ajustou os gráficos cinéticos lineares de primeira / segunda ordem para investigar a cinética. Da mesma forma, a cinética de degradação em diferentes quantidades de MnO 2 NPs e diferentes concentrações iniciais de TCH sob condições sem buffer foram estudados no arquivo Adicional 8:Figura S8 e Arquivo Adicional 9:Figura S9, respectivamente. A Tabela 1 exibiu os dados cinéticos obtidos em diferentes condições. Os coeficientes de correlação foram ajustados linearmente e calculados para demonstrar a cinética de degradação do TCH por MnO 2 NPs / ESM. Geralmente, os coeficientes de correlação calculados por meio do modelo de pseudo-segunda ordem foram superiores aos da pseudo-primeira ordem, indicando que esse processo foi mais consistente com o modelo de pseudo-segunda ordem. Em detalhes, este modelo de pseudo-segunda ordem tinha coeficientes de correlação mais altos com pequenas doses de MnO 2 ou altas concentrações iniciais de TCH. E de qualquer forma, os coeficientes de correlação foram mais próximos de 1 nas condições de buffer em comparação com a degradação sem um buffer.
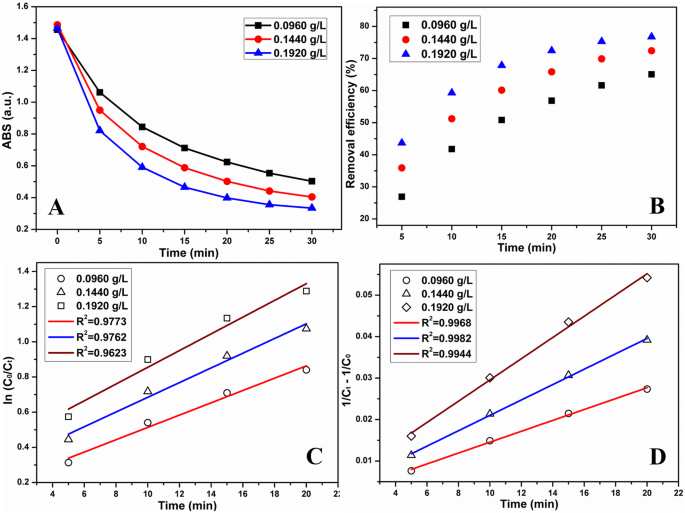
O dependente do tempo a intensidade de absorção de TCH e b eficiência de remoção por diferentes quantidades de MnO 2 Tratamento NPs / ESM. c Parcelas cinéticas lineares de primeira ordem e d gráficos cinéticos lineares de segunda ordem por diferentes quantidades de MnO 2 Tratamento NPs / ESM. (Condições:a concentração inicial de TCH era de 50 mg / L, o pH controlado era de 3,0)
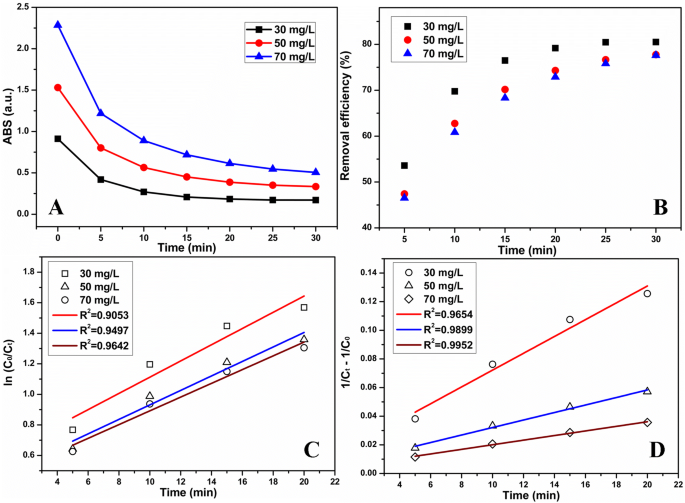
O dependente do tempo a intensidade de absorção de TCH e b eficiência de remoção para a degradação de diferentes concentrações iniciais de TCH. c Parcelas cinéticas lineares de primeira ordem e d gráficos cinéticos lineares de segunda ordem para degradação de diferentes concentrações iniciais de TCH. (Condições:uma dose de MnO 2 NPs / ESM era 0,1740 g / L, o pH controlado era 3,0)
Comparação de MnO comercial 2 Pó e outros materiais relatados
Para ilustrar a propriedade avançada do MnO conforme preparado 2 NPs / ESM, a mesma quantidade de MnO comercial 2 o pó foi testado de forma contrastante para a descontaminação de TCH nas mesmas condições. A Figura 8 mostrou a eficiência de remoção de MnO 2 conforme preparado NPs / ESM e MnO comercial 2 pó com ou sem tampão. Foi indicado que MnO 2 NPs / ESM mostraram uma vantagem proeminente sobre o MnO comercial 2 pó em ambas as condições. Embora a eficiência de remoção seja de cerca de 80% por meio de MnO 2 a descontaminação foi obtida em trabalho anterior [38, 39], podendo atingir até 98% sob pH =6,5 através de um MnO 2 e sistema de barreira reativa permeável (PRB) baseado em ferro zero valente (ZVI) [56], que foi atribuído aos múltiplos efeitos do acoplamento de ZVI com MnO 2 . Além disso, outros materiais também foram aplicados na descontaminação do TC. TiO imobilizado 2 nanobelts modificados por nanopartículas de Au e CuS (Au – CuS – TiO 2 RNs) apresentaram uma eficiência de remoção de 96% em relação à oxitetraciclina (OTC) devido à sua atividade fotocatalítica superior [57]. O óxido de grafeno (GO) como um adsorvente eficiente mostrou uma boa remoção para TC após 24 h ( R =96%) [58]. Carvão ativado em pó / Fe 3 O 4 nanopartículas magnéticas (PAC / Fe 3 O 4 MNPs) foram aplicados como um catalisador para H 2 O 2 -assistiu a degradação do TC, e eficiência de remoção de 94,5% foi obtida [59]. Percebeu-se que a eficiência da remoção poderia ser aumentada com o prolongamento do tempo de tratamento ou aumento das doses do material [39]. No entanto, todo o trabalho precisa de medições de degradação complicadas e processamento subsequente, o que aumenta o trabalho e o tempo de teste. A operação prática do nosso método, como nem centrifugação nem filtração, facilitaria o procedimento de descontaminação.
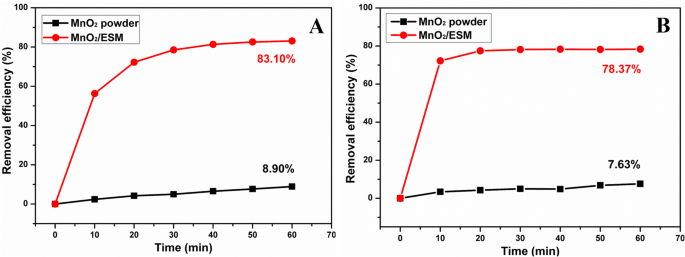
Comparação da eficiência de remoção de TCH por MnO comercial igual 2 pó e MnO 2 NPs / ESM sob a armazenado em buffer e b condições sem buffer
Conclusões
MnO 2 nanopartículas foram sintetizadas neste trabalho através de um procedimento super fácil, misturando a membrana da casca do ovo e soluções de permanganato de potássio. Essas condições de reação adversas ou método desnecessário de pós-tratamento complicado tornaram o processo de síntese e purificação rápido e prático. O MnO obtido 2 nanopartículas dispersas uniformemente na superfície de proteínas fibrosas para formar um modo de combinação microcósmico / macroscópico. Além disso, o modelo de membrana de casca de ovo MnO 2 nanopartículas foram aplicadas para descontaminação do cloridrato de tetraciclina. Foi obtida uma eficiência de remoção de 83,10% após 60 min sob a condição tamponada e um modelo de cinética de pseudo-segunda ordem. Mais notavelmente, MnO 2 NPs / ESM podem ser separados facilmente retirando-os das soluções, o que evitou operações complexas como centrifugação ou filtração, tornando-se uma vantagem na descontaminação de águas residuais com base em nanomateriais.
Abreviações
- ESM:
-
Membrana de casca de ovo
- GSH:
-
Glutationa
- HRTEM:
-
Microscopia eletrônica de transmissão de alta resolução
- NPs:
-
Nanopartículas
- OTC:
-
Oxitetraciclina
- PBS:
-
Solução salina tampão de fosfato
- PPCPs:
-
Produtos farmacêuticos e de cuidados pessoais
- SEM:
-
Microscopia eletrônica de varredura
- TCH:
-
Cloridrato de tetraciclina
- TCs:
-
Tetraciclinas
- TEM:
-
Microscopia eletrônica de transmissão
- TG:
-
Termogravimetria
- UV-vis:
-
Visível por ultravioleta
- XPS:
-
espectroscopia de fotoelétrons de raios-X
Nanomateriais
- Síntese biogênica, caracterização e avaliação do potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
- Síntese fácil e propriedades ópticas de pequenos nanocristais de selênio e nanorods
- Síntese fácil de nanopartículas de SiO2 @ C ancoradas em MWNT como materiais de ânodo de alto desempenho para baterias de íon-lítio
- Síntese fácil de compósito CuSCN colorido e condutor revestido com nanopartículas de CuS
- Síntese fácil de nanofios de prata com diferentes proporções de aspecto e usados como eletrodos transparentes flexíveis de alto desempenho
- Propriedades de formação e luminescência de Al2O3:Nanocompósitos de SiOC na base de nanopartículas de alumina modificados por feniltrimetoxisilano
- Propriedades de síntese e luminescência de nanopartículas α-NaGdF4 / β-NaYF4:Yb, Er Core – Shell solúveis em água
- Síntese e desempenho in vitro de nanopartículas de ferro-platina revestidas com polipirrole para terapia fototérmica e imagem fotoacústica
- Síntese fácil de óxido de estanho mesoporoso semelhante a buraco de minhoca via auto-montagem induzida por evaporação e propriedades aprimoradas de detecção de gás
- Adepto verde na síntese e estabilização de nanopartículas de cobre:atividades catalíticas, antibacterianas, citotoxicidade e antioxidantes



