Adsorção de tetraciclina com óxido de grafeno reduzido decorado com nanopartículas de MnFe2O4
Resumo
Nanomateriais foram amplamente utilizados como adsorventes eficientes para remediação ambiental da poluição por tetraciclina. No entanto, a separação dos adsorventes representou um desafio para suas aplicações práticas. Neste estudo, aumentamos o MnFe magnético 2 O 4 nanopartículas no óxido de grafeno reduzido (rGO) para formar MnFe 2 O 4 Nanocompósito / rGO com um método de uma etapa. Quando usado como absorvente de tetraciclina, apresentou capacidade de adsorção de 41 mg / g. A cinética de adsorção e a isotérmica foram bem ajustadas com o modelo de pseudo-segunda ordem e o modelo de Freundlich, respectivamente. O MnFe 2 O 4 O nanocompósito / rGO pode ser facilmente extraído da solução com o campo magnético externo e regenerado com lavagem ácida.
Introdução
Devido à sua baixa toxicidade com amplo espectro de atividade, a tetraciclina (TC) é um dos antibióticos mais utilizados no mundo [1]. No entanto, uma preocupação crescente tem sido levantada nos últimos anos porque o TC é pouco degradado pelo metabolismo. Como resultado, o TC residual é descarregado diretamente no meio ambiente através das fezes e se espalha em corpos d'água próximos e no solo com a água, causando a poluição difusa dessas áreas [1,2,3]. Depois que o resíduo TC é acumulado no corpo humano, ele exibe toxicidade crônica. Enquanto isso, pode influenciar os organismos fotossintéticos aquáticos e as populações microbianas indígenas [4, 5]. Para tratar água poluída com TC, a adsorção tem emergido como um método promissor por ser eficiente e com boa relação custo-benefício. Os adsorventes usados na adsorção incluem argila esmectita [6], montmorilonita [7], diatomita [8], carvão ativado [9], alumina [10] e nanotubo de carbono [11]. Mais recentemente, nanomateriais à base de grafeno têm sido usados como os adsorventes mais eficazes devido à existência de interação π-π, ligação H e ligação cátion-π entre TC e materiais à base de grafeno [12, 13]. Assim, esses nanomateriais exibem altas capacidades de adsorção de TC. Por exemplo, máximo teórico da capacidade de adsorção ( q m ) de óxido de grafeno e óxido de grafeno reduzido pode atingir 313 e 558 mg / g, respectivamente [14, 15]. O composto à base de grafeno exibe até mesmo capacidades de adsorção mais altas. TiO 2 / GO composto exibe um q m valor de 1805 mg / g [16]. No entanto, a separação de absorventes à base de nanomateriais da água poluída representa um desafio para suas aplicações práticas. Para facilitar a separação do absorvente, foram utilizados absorventes magnéticos. Nosso grupo demonstrou que o híbrido de magnetita / óxido de grafeno funcionalizado com tiol pode ser usado como um adsorvente reutilizável para Hg 2+ remoção [17]. Chandra et al. utilizou compósitos de óxido de grafeno com redução de magnetita dispersível em água para remoção de arsênio [18]. Neste estudo, utilizamos Mn na formação de GO para sintetizar MnFe magnético 2 O 4 / rGO composto com um método de um único recipiente. MnFe 2 O 4 / rGO como o adsorvente exibiu capacidade de adsorção relativamente alta de 41 mg / g com uma concentração inicial de TC de 10 mg / L. O adsorvente magnético pode ser extraído facilmente das soluções de água com a ajuda do campo magnético externo e reutilizado após ter sido regenerado por imersão em solução aquosa de HCl.
Materiais e métodos
Síntese de GO
GO foi preparado com um método modificado de Hummer. Resumidamente, H 2 SO 4 (75,0 ml, 98% em peso) foi adicionado lentamente em um frasco com 1,0 g de grafite em flocos e 0,75 g de NaNO 3 com agitação mecânica em banho de água gelada. Após 10 min, 4,5 g KMnO 4 foi adicionado gradualmente no frasco. Com agitação contínua e vigorosa, a mistura tornou-se pastosa e acastanhada, sendo então diluída com água desionizada. H 2 O 2 solução aquosa (20 ml, 30% em peso) foi então lentamente adicionada à mistura para formar a mistura GO com Mn 2+ íons.
Síntese de MnFe 2 O 4 / rGO Composite
Nós sintetizamos o MnFe 2 O 4 / rGO composto conforme relatado anteriormente [19]. Resumidamente, a mistura anterior foi ainda diluída para 3000 ml com água desionizada. FeCl 3 (9,237 g) foi dissolvido em 400 ml de água desionizada e, em seguida, adicionado à mistura. Solução aquosa de amônia (30% em peso) foi adicionada para ajustar seu pH a 10 em 2 h. Após a mistura ser aquecida a 90 ° C, hidrato de hidrazina (98% em peso, 30 mL) foi adicionado lentamente e agitado durante 4 h, resultando em uma suspensão preta. A suspensão foi arrefecida e separada com ímanes, lavada várias vezes com água desionizada e etanol e finalmente seca sob vácuo a 60 ° C.
Caracterização de MnFe 2 O 4 / rGO Composite
A análise de difração de raios X (XRD) foi conduzida com um difratômetro (Bruker D8 Discover) com radiação Cu Kα (40 kV, 40 mA). A morfologia das amostras foi observada por um microscópio eletrônico de transmissão (TEM, JEOL 2100F). Neste estudo, o magnetômetro de amostra vibrante (VSM 7410, o Lake Shore) foi usado para a análise da propriedade magnética do nanocompósito.
Determinação da concentração de TC
Um oscilador termostático (ZD-85A) foi usado para garantir um processo de adsorção estável e controlável. Um espectrofotômetro de absorção atômica (GTA 120, Agilent) foi usado para detectar o pico de absorção característica ultravioleta; e espectrofotômetro de UV (UV-1100, Shanghai mapada) foi usado para investigar a concentração de resíduo de TC em solução medindo a absorbância das soluções. Outros instrumentos envolvidos neste estudo incluíram medidor de pH (PHS-3C), forno de secagem (DHG-9240A), limpador ultrassônico (KQ5200E), balança eletrônica (TP-214) e assim por diante. A solução TC (10 mg / L) foi preparada para a curva de calibração linear. A Figura 1a mostra o espectro de UV de TC. Os picos de adsorção característicos de são 276 nm e 355 nm. Neste estudo, 355 nm foi escolhido como o comprimento de onda de varredura para a adsorção de TC. A curva de calibração foi apresentada na Fig. 1b. De acordo com a lei de Lambert-Beer [20], medindo a absorbância da solução, a concentração pode ser determinada. A capacidade de adsorção ( Q t , mg / g) e taxa de adsorção ( r ) são calculados pela Eq. (1) e Eq. (2)
$$ {Q} _t =\ frac {\ left ({C} _0- {C} _t \ right) \ vezes V} {m} $$ (1) $$ \ mathrm {r} =\ frac {\ left ({\ mathrm {C}} _ 0 - {\ mathrm {C}} _ {\ mathrm {t}} \ right)} {{\ mathrm {C}} _ 0} \ times 100 \% $$ (2)
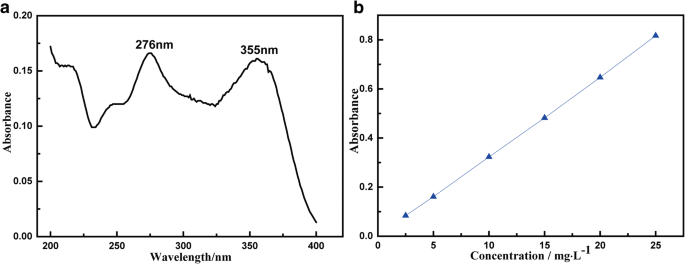
a Espectro UV e ( b ) curva calibrada para medição da concentração de TC
onde C 0 (mg / L) e C t (mg / L) são a concentração de resíduos de TC na solução no início e no tempo t, respectivamente. V (mL) representa o volume da solução e é de 30 mL neste estudo e m (g) é o peso do MnFe 2 O 4 / rGO amostra usada.
Resultados e discussão
Síntese e caracterização de MnFe 2 O 4 / rGO
MnFe 2 O 4 / rGO nanocompósito foi sintetizado com um método one-pot, conforme relatado. No processo, preparamos uma mistura contendo GO com um método Hummer modificado sem purificação. Mais tarde, chega de H 2 O 2 solução aquosa foi adicionada à mistura para reduzir íons Mn com alta valência para Mn 2+ na lama. Eles foram co-precipitados com Fe 3+ em um ambiente alcalino para formar MnFe 2 O 4 nanocristais em nanofolhas GO que foram reduzidas a grafeno com a aparência de N 2 H 4 . MnFe 2 O 4 O nanocompósito / rGO foi finalmente formado. A Figura 2a mostrou os padrões de difração de raios-X do nanocompósito. Os picos de difração são 29,9, 35,5, 42,9, 56,8 e 62,3 o correspondia ao plano de (220), (311), (400), (511) e (440) de MnFe 2 O 4 com a fase cúbica (cartão JCPDS nº 10-319). No espectro Raman (Fig. 2b) do composto, o pico em 600 cm - 1 estava relacionado à vibração de MnFe 2 O 4 enquanto o outro atinge o pico em 1351 e 1575 cm −1 foram as bandas D e G de rGO, respectivamente [21, 22]. A área de superfície específica de BET foi de 42,7 m 2 / g (arquivo adicional 1:Figura S1). A elevada área de superfície foi atribuída às seguintes razões. Durante o processo de síntese, nanofolhas GO foram usadas sem purificação ou secagem. Enquanto isso, MnFe 2 O 4 nanopartículas nuclearam e cresceram nelas, impedindo-as de se empilhar. As relações de peso das folhas rGO e MnFe 2 O 4 componentes no MnFe 2 O 4 –RGO nanocompósitos foram avaliados em aproximadamente 12% e 88%, por análise térmica gravimétrica (Arquivo adicional 1:Figura S2) no ar, respectivamente. Imagens TEM (Fig. 2c) do nanocompósito mostraram que MnFe 2 O 4 nanopartículas com tamanhos abaixo de 30 nm foram decoradas nas nanofolhas. Imagens TEM de alta resolução (Fig. 2d) do nanocompósito mostraram ainda as franjas de rede claras com distâncias interplanares de 0,29 nm, correspondendo a (220) planos de MnFe 2 O 4 com fase cúbica. As propriedades magnéticas do nanocompósito foram examinadas com um magnetômetro. Um ciclo de histerese de MnFe 2 O 4 / rGO a 25 ° C foi mostrado na Fig. 3a, a magnetização saturada e a magnetização de remanência foram medidas em 22,6 emu / ge 1,1 emu / g, respectivamente. A pequena magnetização saturada deveu-se ao pequeno tamanho da magnetita e ao aparecimento de GO no compósito. A coercividade do nanocompósito foi de 39,0 Oe. O adsorvente com pequena magnetização remanescente e coercividade à temperatura ambiente pode ser atraído e separado até mesmo por um pequeno campo magnético externo. Na verdade, MnFe 2 O 4 / rGO nanocompósito disperso em solução de água foi facilmente extraído da água com um ímã, como confirmado por na imagem óptica na Fig. 3b.
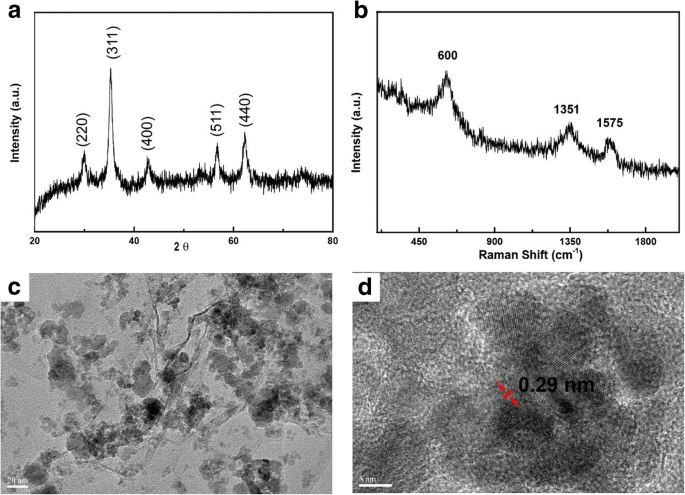
Caracterização do MnFe 2 O 4 Nanocompósito / rGO. a Padrões de XRD e ( b ) Análise Raman do nanocompósito; Imagem TEM ( c ) e imagem HRTEM ( d ) do nanocompósito
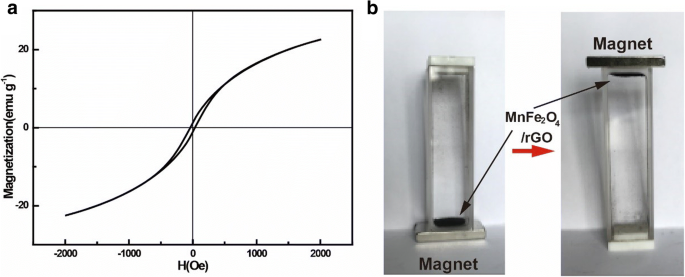
Propriedade magnética do nanocompósito MnFe2O4 / rGO. a Loop de histerese e ( b ) separação magnética do nanocompósito da água
Adsorção de TC em MnFe 2 O 4 / rGO
Para investigar a cinética de adsorção, MnFe 2 O 4 / rGO (5 mg) foi adicionado à solução de TC (10 mg / L) à temperatura de 25 ° C para adsorção. Em seguida, a solução foi colocada em um oscilador de temperatura constante para garantir mistura suficiente. As amostras foram coletadas em momentos diferentes, e a absorbância da amostra foi medida usando o espectrofotômetro. Comparando a curva de calibração, a concentração de TC na solução em diferentes momentos durante o processo de adsorção pode ser determinada. A Figura 4 mostra a influência do tempo na adsorção de TC e no equilíbrio de adsorção, respectivamente. O processo de adsorção de TC em MnFe 2 O 4 foi moderadamente rápido. Ele mostrou que a concentração de TC diminuiu drasticamente durante as primeiras 5 horas. Então, o processo de adsorção ficou mais lento. Após cerca de 8 horas de adsorção, a concentração da solução de TC estava estável, o que implica que a adsorção atinge o equilíbrio. A cinética de adsorção foi mais lenta do que a dispersão GO pura [14], mas mais rápida do que a esponja magnética de óxidos de grafeno [23]. Também é muito mais rápido do que a adsorção de ciprofloxacina no alginato de sódio / GO. A cinética de adsorção pode estar relacionada com a estrutura de empilhamento de GO e como o TC se difunde facilmente para o site de adsorção ativo. De acordo com a Fig. 4b, a capacidade de adsorção foi estimada em 41 mg / g com a concentração inicial de TC de 10 mg / L. Este valor foi um pouco maior do que (39 mg / g) das partículas magnéticas GO [24]. Dois modelos cinéticos, modelos de pseudo-primeira ordem e pseudo-segunda ordem, foram aplicados aqui para o estudo do mecanismo de adsorção. A equação dinâmica de pseudo-primeira ordem é freqüentemente usada para simular o sistema de adsorção sólido-líquido, com a expressão linear mostrada na Eq. (3) [25]:
$$ \ mathit {\ ln} \ left ({q} _e- {q} _t \ right) =\ mathit {\ ln} {q} _e- {K} _1t $$ (3)
onde q e ( mg / g) é a quantidade de adsorção em equilíbrio, e q t (mg / g) é a quantidade de adsorção no tempo t . K 1 é a constante de taxa da cinética de pseudo-primeira ordem. Ao mesmo tempo, o modelo cinético de pseudo-segunda ordem é mais amplamente aplicado à cinética de adsorção de íons. A expressão linear da equação da taxa pseudo-secundária é mostrada na Eq. (4) [26]:
$$ \ frac {t} {q_t} =\ frac {1} {K_2 {q} _e ^ 2} + \ frac {1} {q_e} t $$ (4)
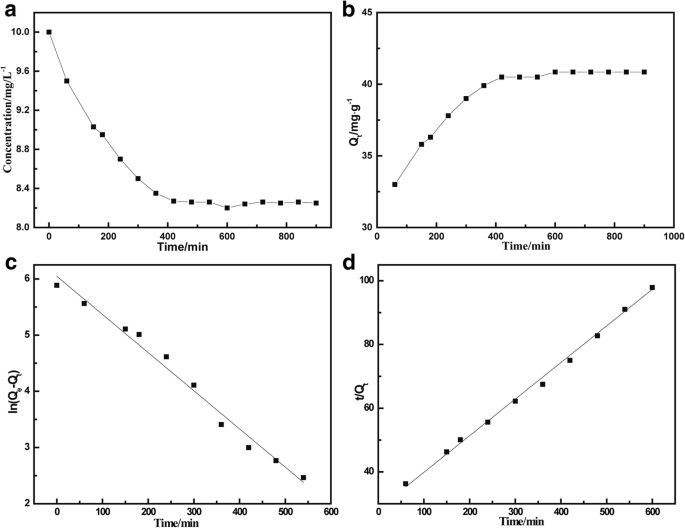
Cinética de adsorção de TC de MnFe 2 O 4 Nanocompósito / rGO. a Concentração de TC e ( b ) capacidade de adsorção versus tempo durante a adsorção e cinética de adsorção equipada com ( c ) modelo cinético de pseudo-primeira ordem e ( d ) modelo cinético de pseudo-segunda ordem
Onde K 2 nesta equação representa a constante de taxa da cinética de pseudo-segunda ordem.
Com base nos resultados experimentais deste estudo, a Fig. 4c, d mostrou a linha de ajuste da adsorção aplicando a cinética de adsorção de primeira ordem e a cinética de adsorção de segunda ordem, respectivamente. Os parâmetros detalhados dos dois modelos cinéticos estão listados na Tabela 1.
O coeficiente de correlação ( R 2 , 0,99) para o ajuste do modelo de pseudo-segunda ordem foi maior do que (0,98) do modelo de pseudo-primeira ordem. Indicou que o modelo cinético de pseudo-segunda ordem é adequado para descrever a cinética de adsorção de TC em MnFe 2 O 4 Nanocompósito / rGO. A constante cinética K 2 era 114,87 g mg min −1 . Para entender como TC interagiu com MnFe 2 O 4 / rGO nanocompósito, modelos de isoterma de Langmuir e Freundlich foram usados para ajustar os dados de adsorção. O modelo de Langmuir é comumente expresso como Eq. (5) [27]:
$$ \ frac {C_e} {q_e} =\ frac {1} {K_L {q} _m} + \ frac {C_e} {q_m} $$ (5)
onde C e (mg / L) é a concentração de equilíbrio, q e (mg / g) é a quantidade de adsorção em equilíbrio, q m (mg / g) é a capacidade máxima de adsorção de monocamada do adsorvente, K L , a constante de Langmuir está relacionada à afinidade entre o adsorvente e o adsorbato. Os valores de q m e K L pode ser obtido pela inclinação da equação e a interceptação. Enquanto isso, o modelo de isoterma de Freundlich é expresso como a seguinte equação [28]:
$$ \ mathit {\ ln} {q} _e =\ mathit {\ ln} {K} _F + \ frac {1} {n} \ mathit {\ ln} {C} _e $$ (6)
onde K F é constante de Freundlich e n é o índice de adsorção que descreve a intensidade.
Para se ter uma ideia do modelo isotérmico deste tipo de adsorção, o ajuste linear usando os modelos de Langmuir e Freundlich são mostrados na Fig. 5, e os parâmetros relevantes estão listados na Tabela 2. Como pode ser visto na Tabela 2, a adsorção de MnFe 2 O 4 / rGO para TC ajustou-se melhor com a isoterma de Freundlich do que a isoterma de Langmuir. O modelo de adsorção de Freundlich assume que a adsorção é baseada em superfície heterogênea, enquanto o modelo de Freundlich é freqüentemente usado para adsorção não ideal de superfícies diferentes e adsorção multicamadas. A adsorção da tetraciclina no rGO foi relacionada com a estrutura molecular da tetraciclina e do rGO. TC tinha quatro anéis aromáticos que podiam ser facilmente adsorvidos em rGO pela interação π-π. Essa interação tornou possível a adsorção em várias camadas. Ele poderia atrair moléculas de TC adicionais pela mesma interação entre as moléculas de TC. O índice de adsorção n neste modelo estava na faixa de 2-3, o que previu que este sistema de adsorção é "favorável". Quando a temperatura aumentou, a capacidade de adsorção do TC no nanocompósito também aumentou. Isso indicou que o processo de adsorção era endotérmico.
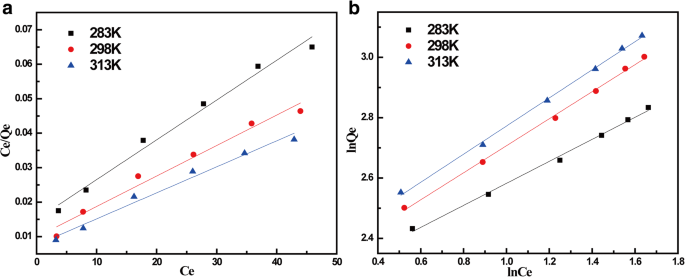
Isotermas de adsorção de TC de MnFe 2 O 4 Nanocompósito / rGO. Isotermas de adsorção equipadas com ( a ) Modelo Langmuir e ( b ) Isoterma de Freundlich a 283, 298 e 313 K, respectivamente
Para investigar os efeitos do pH na adsorção, 30 mL de solução de TC (10 mg / L) e 5 mg de MnFe 2 O 4 / rGO pó foram misturados e o pH da solução foi ajustado para 2,0, 3,3, 5,0, 7,7, 9,0, 9,7 e 10,5 em cada teste. A solução foi colocada no oscilador à temperatura de 25 ° C. As amostras foram retiradas no equilíbrio de adsorção para medir a concentração. O comportamento de adsorção sob diferentes pH foi investigado, e os resultados testados sob pH 2,0 a 10,5 foram mostrados na Fig. 6. A capacidade máxima de adsorção de MnFe 2 O 4 / rGO em TC ocorre quando o pH da solução era 3,3. Quando o pH foi menor que 3,3, a adsorção diminuiu com o aumento da acidez. Isso ocorreu principalmente por causa da competição nos sites de adsorção entre TCH 3+ e grandes quantidades de H + íons na solução. Quando o pH estava entre 3,3 e 7,7, o TC existia na forma de TCH 2 0 . A interação eletrostática foi semana. Com a solução se tornando mais alcalina, o aumento de OH - pode causar sedimentação com o íon metálico de MnFe 2 O 4 / rGO e, assim, reduzir a adsorção. Em pH =9,7, este foi exatamente o ponto de transição onde o TC dominante formado na solução muda de TCH - para TC 2− . Assim, assume-se que a existência do pico em pH =9,7 foi devido à mudança de formas de íons na solução. Neste estudo, solução de HCl (0,1 mol / L) foi usada como eluente para descobrir as características de adsorção-regeneração de MnFe 2 O 4 / rGO para TC. A adsorção foi realizada a 25 ° C, com 5 mg de MnFe 2 O 4 / rGO adicionado à solução de TC de 10 mg / L. Após o equilíbrio de adsorção, MnFe 2 O 4 / rGO foi eluído por solução de HCl. Então, o MnFe eluído 2 O 4 / rGO foi usado para adsorção novamente, e a capacidade de adsorção foi medida. A eluição foi realizada três vezes e, comparando a capacidade de adsorção após cada eluição, foi traçada a característica de adsorção-regeneração. Neste estudo, todos os testes foram executados pelo menos três vezes. O oscilador em todos os experimentos foi ajustado para uma velocidade fixa de 180 rpm. A Figura 6b mostrou o comportamento de adsorção-regeneração de MnFe 2 O 4 / rGO na adsorção de TC. A taxa de remoção inicial foi de 86%. Depois de ser eluído por HCl, a taxa de remoção de TC foi de 85%, 82%, 79% e 71% para os primeiros 4 ciclos. Isso indicou que os adsorventes podem ser facilmente regenerados e reutilizados.
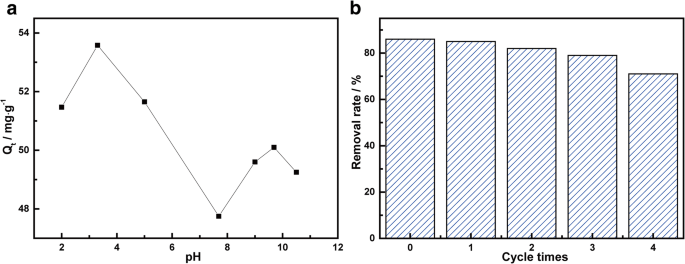
a Influência do pH na adsorção de TC em MnFe 2 O 4 / Nanocompósito rGO e ( b ) taxa de remoção em relação ao número de ciclo com a concentração inicial de TC de 10 mg / L
No geral, acreditamos que rGO contribuiu principalmente para a adsorção de TC. Em primeiro lugar, o tamanho de MnFe 2 O 4 atingiu várias dezenas de nanômetros; não poderia contribuir muito para a área de superfície geral. Em segundo lugar, a capacidade de adsorção geral foi de ~ 40 mg / g em TC com uma concentração inicial de ~ 10 mg / mL. Este valor foi quase o mesmo com as capacidades de adsorção relatadas de GO [14]. O aparecimento de MnFe magnético 2 O 4 fez a extração e reciclagem do adsorvente, rGO, facilmente.
Conclusões
MnFe 2 O 4 O nanocompósito / rGO foi sintetizado com sucesso com o método de um vaso. O nanocompósito poderia ser usado como adsorvente eficiente de TC com capacidade de adsorção de 41 mg / g quando a concentração inicial de TC era de 10 mg / L. A cinética e a isoterma do processo de adsorção foram descritas como o modelo de pseudo-segunda ordem e o modelo de Freundlich, respectivamente. Os adsorventes magnéticos podem ser separados e regenerados, indicando o MnFe 2 O 4 / rGO nanocompósito pode ser um adsorvente reutilizável promissor para remediação ambiental para poluição de TC.
Abreviações
- GO:
-
Óxido de grafeno
- rGO:
-
Óxido de grafeno reduzido
- TC:
-
Tetraciclina
- TEM:
-
Microscopia eletrônica de transmissão
Nanomateriais
- Nanofibras de polímero por eletrofiação decoradas com nanopartículas de metal nobre para detecção química
- Nanotubos de titanato Nanocompósitos de óxido de grafeno decorado:Preparação, Retardância de Chama e Fotodegradação
- Células endoteliais de segmentação com nanopartículas de GaN / Fe multifuncionais
- Biossegurança e capacidade antibacteriana do grafeno e do óxido de grafeno in vitro e in vivo
- Toxicidade de nanopartículas de CoFe2O4 revestidas com PEG com efeito de tratamento da curcumina
- Preparação de moagem de esferas em uma etapa de nanoescala CL-20 / óxido de grafeno para sensibilidade e tamanho de partícula significativamente reduzidos
- Nanocompósitos à base de óxido de grafeno decorados com nanopartículas de prata como agente antibacteriano
- Redução do óxido de grafeno a baixa temperatura:Condutância elétrica e microscopia de varredura de força de sonda Kelvin
- O Surfactante Aniônico / Líquidos Iônicos Óxido de Grafeno Reduzido Intercalado para Supercapacitores de Alto Desempenho
- Uma abordagem fácil para a preparação de óxido de zinco de tamanho nanométrico em água / glicerol com fontes de zinco extremamente concentradas



