Atividade de imitação da peroxidase ativada por elétrons quentes de nanozimas ultrafinas de Pd
Resumo
As nanozimas ativadas por luz podem fornecer uma grande variedade de novas oportunidades para a indústria química e biotecnologia. No entanto, os atuais sistemas catalíticos de controle remoto ainda estão longe de ser satisfatórios. Aqui, apresentamos um exemplo interessante de aplicação de nanofolhas ultrafinas de Pd (Pd NSs) como um mimetizador de peroxidase controlável por luz. Uma vez que a maioria dos átomos de Pd está exposta em sua superfície, Pd NSs com uma espessura de 1,1 nm possuem alta atividade semelhante à peroxidase. Mais importante ainda, sob excitação de luz, essa atividade intrínseca pode ser ainda mais ativada em cerca de 2,4 a 3,2 vezes. Tal fenômeno pode ser atribuído à propriedade ótica única de Pd NSs ultrafinos, que podem capturar fótons com eficiência para gerar elétrons quentes por meio do efeito de ressonância plasmônica de superfície e, assim, promover a decomposição in situ de H 2 O 2 em radicais de espécies reativas de oxigênio (O *). Esta catálise aprimorada também pode ser usada para detecção colorimétrica em tempo real e altamente sensível de H2O2. Esperamos que nosso trabalho possa fornecer informações valiosas sobre o design racional de nanozimas artificiais com atividade controlável e eficiente em diagnósticos biomédicos, administração de medicamentos e química ambiental.
Introdução
As enzimas naturais são biocatalisadores requintados que podem catalisar quase todas as transformações químicas da vida [1, 2]. No entanto, ainda existem defeitos inerentes, como baixa estabilidade e alto custo. Uma vez que nanopartículas de magnetita com atividade imitadora de peroxidase intrínseca foram relatadas pela primeira vez [3], o projeto e desenvolvimento de nanomateriais com atividades semelhantes a enzimas (nanozimas) têm atraído a atenção de pesquisas cada vez maiores [4]. Até agora, uma série de óxido- [5,6,7], metal- [8,9,10] e nanomateriais à base de carbono [11,12,13] foram usados para imitar a peroxidase de rábano (HRP). Entre estes, nanomateriais de metais nobres [8, 14,15,16,17,18,19], como prata (Ag) [15], ouro (Au) [16, 17], platina (Pt) [8], e paládio (Pd) [18, 19] et al., relataram possuir altas atividades miméticas de peroxidase. Por outro lado, a introdução de luz para ativar a atividade das nanozimas também tem sido relatada, o que oferece uma grande variedade de oportunidades para a biotecnologia e a indústria química [4, 20]. No entanto, os atuais sistemas catalíticos de controle remoto ainda estão longe de ser satisfatórios.
Os nanomateriais de metal plasmônico podem capturar ou responder à luz solar devido à propriedade ótica única de ressonância plasmônica de superfície (SPR). Esses nanomateriais metálicos, que podem capturar fótons para gerar elétrons quentes através do efeito SPR, tornaram-se os principais materiais para melhorar a taxa catalítica [21], promovendo um novo sensor óptico de biomoléculas [22], terapia fototérmica de engenharia e usando a luz solar como energia renovável [ 23, 24]. No entanto, nenhum deles se concentrou no efeito SPR das nanozimas à base de metal plasmônico em suas atividades de imitação de enzimas. Assim, seria atraente combinar nanozimas à base de metal plasmônico com efeito SPR para obter catálise enzimática altamente ativa e ajustável à luz.
Aqui, relatamos pela primeira vez que nanofolhas de Pd ultrafinas (Pd NSs) com uma espessura de cerca de 1,1 nm podem servir como um imitador de peroxidase excelente e controlável por luz. Foi relatado que os sistemas de nanozima à base de Pd e de nanozima controlada por luz exibem múltiplas atividades miméticas de enzimas, incluindo oxidase, peroxidase, catalase e superóxido dismutase [4, 18, 19]. No entanto, suas estruturas são geralmente partículas, volumes e hastes. Como todos sabemos, Pd NSs ultrafinos têm alta energia de superfície, tamanho lateral pequeno e alta mobilidade de elétrons, o que resulta em alta densidade de sítios ativos de superfície [25]. Além disso, a maioria dos átomos expostos a nanofolhas ultrafinas podem servir como uma plataforma ideal para projetar seu desempenho [26]. Inspirados pela estrutura única das nanofolhas ultrafinas, apresentamos uma estratégia que não apenas faz uso total dos sítios ativos dos átomos de Pd, mas também injeta elétrons quentes no processo de catálise enzimática. Conforme mostrado no Esquema 1, a interação de fótons com Pd NSs ultrafinos pode excitar a ressonância plasmônica de superfície que decai não radiativamente em elétrons quentes e lacunas, promovendo assim o H 2 O 2 decomposição in situ redutivamente para gerar radicais de espécies de oxigênio (O *) com TMB oxidante sob visível. Ao introduzir luz visível na reação enzimática, os Pd NSs exibem atividades catalíticas significativamente maiores do que os Pd NSs em condições de escuridão.
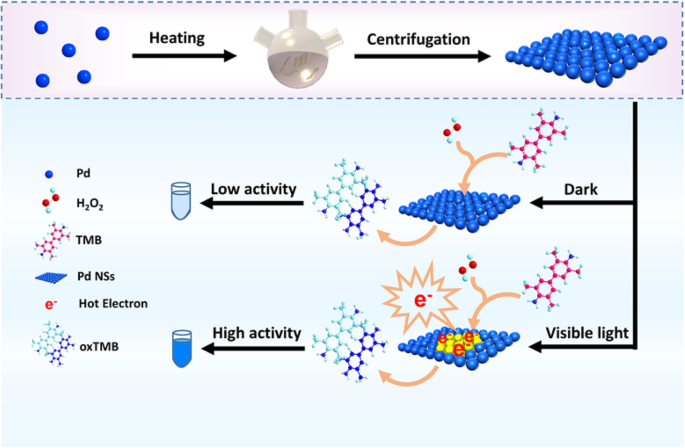
Ilustração esquemática da estrutura de Pd NSs e variação de atividade de Pd NSs sob luz escura e visível
Materiais e Experimental
Materiais e caracterizações
O ácido cítrico (CA); N, N-dimetilformamida (DMF); 3,3,5,5-tetrametilbenzidina (TMB); e o brometo de cetiltrimetilamónio (CTAB) foram adquiridos à Sigma Aldrich. Acetilacetonato de Pd (II), W (CO) 6 e a polivinilpirrolidona (PVP) foram obtidas na Macklin. Peróxido de hidrogênio (H 2 O 2 , 30% em peso) foi comprado na Beijing Chemicals (Pequim, China). Todos os produtos químicos foram utilizados sem purificação adicional. Água experimental purificada pelo sistema Millipore (18,2 MΩ; Millipore Co., EUA) foi usada ao longo do trabalho.
As estruturas de fase dos produtos foram caracterizadas por um difratômetro de raios-X PANalytical que utilizou radiação Cu Kα ( λ =1,5406 Å). E os espectros de refletância difusa de UV-vis (DRS) das amostras foram caracterizados à temperatura ambiente usando o Lambda 750, PerkinElmer. As concentrações dos catalisadores nas soluções foram determinadas pelo ICP-AES (720, Agilent). Imagens de microscopia eletrônica de transmissão (TEM) foram registradas no JEM1400 mais microscópio eletrônico de transmissão operado a 100 kV. As análises de TEM de alta resolução (HRTEM) foram realizadas em um microscópio eletrônico de transmissão de emissão de campo JEM-2100F (FE-TEM) a 200 kV.
Síntese de nanofolhas Pd
De acordo com o método relatado [27], Pd NSs foram sintetizados. Resumidamente, Pd (II) acetilacetonato (16 mg), PVP (MW =24.000, 30 mg), CA (150 mg) e CTAB (60 mg) foram misturados em DMF (10 mL) e agitados em uma atmosfera de nitrogênio por 1 h. Quando a cor da solução no frasco (25 mL) muda para uma solução laranja-vermelho uniforme, 100 mg de W (CO) 6 foi adicionado à solução sob um N 2 atmosfera. Em seguida, aqueça o frasco a 80 ° C por 1 h. Após a reação, o produto azul escuro foi separado por centrifugação (9000 rpm / min, 3 min) com uma quantidade suficiente de acetona e, em seguida, disperso em etanol. Este processo foi repetido três vezes. Finalmente, as nanofolhas de Pd foram dispersas em 10 mL de etanol para experimentos posteriores.
Medição fotocatalítica de imitação de peroxidase
A atividade mimetizadora da peroxidase das nanozimas Pd NSs foi avaliada medindo a oxidação de TMB. Uma lâmpada Xe 300-W (CEL-HXF300 / CEL-HXUV300, China Education Au-light Co., Ltd., Pequim) serviu como fonte de luz, e adicionar um filtro de vidro permite a luz visível ( λ ≥ 400 nm) para passar. Em um experimento típico, 12,6 μg mL −1 Nanozimas de Pd NSs (medidas por ICP-AES) foram adicionadas a 1 mL de solução tampão de ácido fosfórico (0,1 M, pH 4) contendo H 50 mM 2 O 2 e TMB 0,7 mM à temperatura ambiente. Durante os diferentes tempos de irradiação, a atividade mimetizadora da peroxidase foi determinada monitorando o pico de absorção característica a 652 nm após a centrifugação, que indica a concentração dos produtos de oxidação de TMB. O experimento controle teve as mesmas condições, exceto para a iluminação.
Resultados e discussão
Projeto e caracterização das nanozimas Pd NSs
Uma síntese típica de nanofolhas de paládio foi preparada através de um método clássico (Fig. 1a) para construir uma série de nanozimas ultrafinas de sítios atômicos altamente ativos que possuem substratos inerentes e captura de fótons e características miméticas de enzimas de peróxido eficientes. A Figura 1 b – d mostra uma imagem típica de microscopia eletrônica de transmissão de baixa ampliação (TEM) do Pd NSs sintetizado, no qual é composto por nanofolhas uniformes com dimensões laterais de cerca de 10,0 nm (Fig. 1b, inserção) e a espessura média de cerca de 1,1 nm (Fig. 1c, inserção). De acordo com o tamanho, a porcentagem de área da superfície plana superior e inferior é superior a 90%. A microscopia eletrônica de transmissão de alta resolução (HRTEM) é usada para confirmar a morfologia e a fase de Pd NSs. A Figura 1 g mostra os espaçamentos apropriados de ~ 0,22 e 0,256 nm para os planos de rede (111) e (200) do paládio [27]. Para atender às necessidades do experimento, o padrão de XRD de Pd NSs foi caracterizado por carregamento em carbono comercial. Como mostrado na Fig. 1e, os picos de difração em torno de 40.11, 46.65 e 68.12 correspondem a (111), (200) e (220) planos de Pd NSs cúbicos, o que é consistente com a observação de HRTEM. Além disso, nenhum pico indicativo de fases cristalinas além dos picos associados ao carbono comercial. O espectro Pd 3d exibe dois picos (Fig. 1f) Pd 3d 5/2 e Pd 3d 3/2 (resultante da divisão spin-órbita), localizado respectivamente em 335,5 e 339,2 eV [25], que revelou que existem dois ambientes químicos para o átomo de paládio.
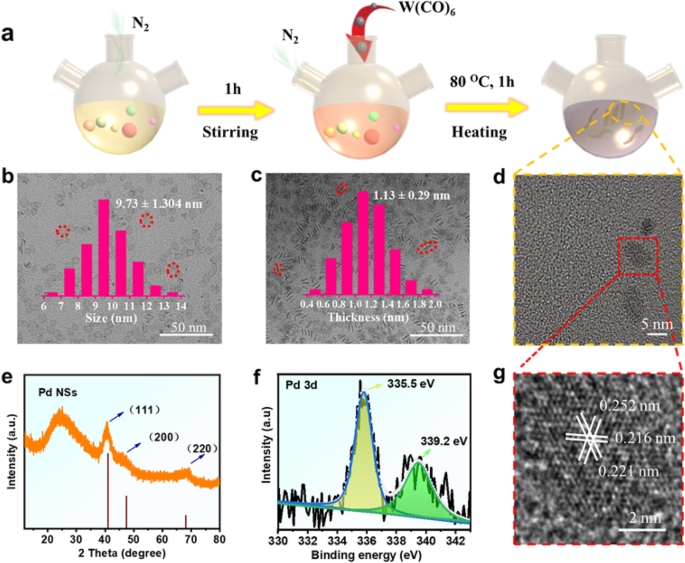
Caracterização das nanozimas. a Mecanismo de crescimento das nanozimas de Pd. b , c , e d TEM. e Padrões de XRD. f Espectro Pd 3d XPS de Pd NSs. g Imagem HRTEM de Pd NSs
Atividade de imitação da peroxidase fotocatalítica
A atividade semelhante à peroxidase do Pd NSs foi investigada usando TMB como um substrato de peroxidase típico. Uma vez que a maioria dos átomos de Pd foram expostos na superfície de nanofolhas ultrafinas, concluímos que Pd NSs ultrafinos possuem uma alta densidade de sítios de superfície ativos e, portanto, resultando em excelente atividade catalítica. Como esperado, na coexistência de H 2 O 2 , Pd NSs pode catalisar eficientemente a oxidação do substrato incolor TMB para o produto azul oxTMB, com a absorção característica em 652 nm (Fig. 2a, b). No entanto, sem a adição de H 2 O 2 , a atividade do Pd NSs pode ser desprezada sob as mesmas condições experimentais, o que revelou que a atividade semelhante à peroxidase desempenhou um papel importante durante a reação. Semelhante a enzimas naturais e outras nanozimas, as nanozimas de Pd têm uma atividade de peroxidase dependente de pH, temperatura e concentração (Fig. 2c e Fig. S1). Sob a condição de experimento, Pd NSs mostrou atividade catalítica otimizada na solução de ácido fraco, e o pico de absorbância característica da solução de reação foi maior a 35 ° C quando a temperatura variou de 25 a 75 ° C (Fig. 2c). Surpreendentemente, com ou sem irradiação de luz, foi observada uma diferença significativa na atividade mimetizadora da peroxidase (Fig. 2d e Fig. S2). De acordo com o valor de absorção da solução de reação por 60 min, a atividade de Pd NSs sob luz visível exibiu aproximadamente 2,4 ~ 3,2 vezes maior do que a de Pd NSs em condições de escuridão (Fig. 2d e Fig. S2). Da mesma forma, a introdução de luz no processo de catálise de outras nanopartículas de metal plasmônico também pode aumentar sua atividade semelhante à peroxidase (Fig. S3-S5). Por comparação dessas nanozimas, descobrimos que Pd NSs apresentou a maior faixa de regulação da atividade. Tal fenômeno se deve principalmente à estrutura única da nanofolha ultrafina. A partir dos resultados obtidos, podemos inferir que a luz visível tem um efeito direto na atividade semelhante à peroxidase de todos os nanomateriais de metal plasmônico (Fig. 2e), e o efeito SPR pode desempenhar um papel essencial no processo catalítico.
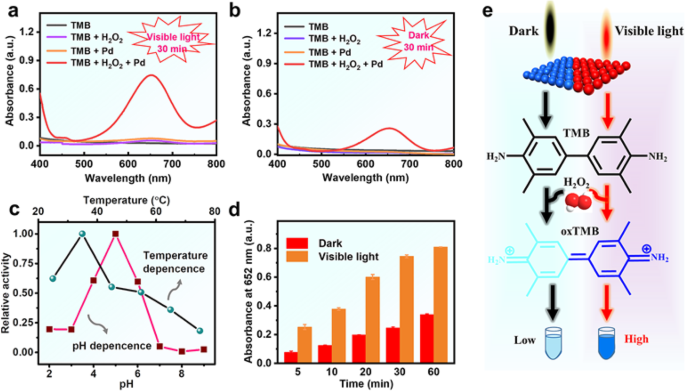
A atividade mimetizadora da peroxidase de Pd NSs. a-b Espectros de absorção de UV-visível típicos de diferentes amostras sob condições de luz visível e escuridão. c Efeito da temperatura e do pH na atividade mimetizadora da peroxidase. d Cursos de tempo para atividade mimetizadora de peroxidase. e O mecanismo semelhante à peroxidase de Pd NSs sob luz escura e visível. Condições experimentais:luz visível =λ ≥ 400 nm, TMB =0,7 mM, H 2 O 2 =50 mM, temperatura =25 ° C, Pd NSs =12,6 μg / mL e solução tampão de fosfato (0,1 M, pH 4)
Investigação cinética e de mecanismo de nanozimas de Pd
Para caracterizar o comportamento enzimático do Pd NSs, determinamos a teoria da cinética enzimática para a reação. No entanto, dentro da faixa de concentração adequada de TMB, Pd NSs apresentam uma curva de Michaelis-Menten típica (Fig. 3a). A constante de Michaelis (Km) e a velocidade máxima de reação (Vmax) foram obtidas usando a equação Lineweaver Burk, conforme mostrado na Tabela S1. Em comparação com a peroxidase de rábano (HRP), o valor de Km aparente do Pd NSs com TMB foi enfraquecido em 0,28 (Fig. 3a, be Tabela S1). Este resultado indica que a estrutura de folha ultrafina de Pd NSs como preparado exibe alta afinidade para TMB, ainda maior do que a da enzima natural HRP.
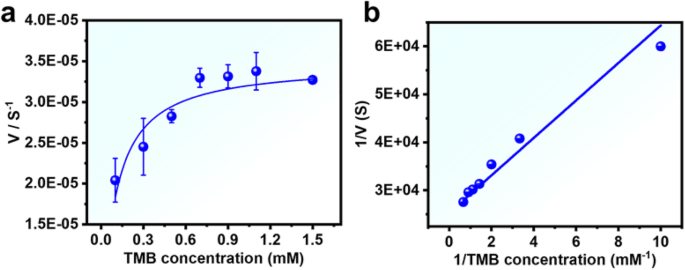
Ensaio cinético de estado estacionário e mecanismo catalítico de Pd NSs (12,6 μg / mL). a A concentração de H 2 O 2 foi de 50 mM e a concentração de TMB foi variada (0,1-1,5 mM). b Gráficos recíprocos duplos para TMB
Uma vez que está claro que H 2 O 2 pode ser decomposto para formar espécies reativas de oxigênio com Pd NSs, é crucial entender quais espécies são produzidas para fornecer uma função de oxidação. Em princípio, metais nobres podem catalisar a decomposição de H 2 O 2 para formar • OH, e intermediários de reação O * em condições de pH mais baixo [28], qualquer um dos quais pode ser a espécie que fornece a função de oxidação em reações enzimáticas miméticas. Para entender o possível mecanismo catalítico de Pd NSs, primeiro usamos ácido tereftálico (TA) / H 2 O 2 para testar se as características semelhantes à peroxidase de Pd NSs estão relacionadas à formação de radicais • OH (Fig. 4a). Usando TA como uma sonda fluorescente, um produto altamente fluorescente foi produzido pela reação do ácido 2-hidroxitereftálico com • OH [29]. Conforme mostrado na Fig. 4b, a intensidade de fluorescência da solução diminui significativamente após a adição de Pd NSs. Os resultados são consistentes com a intensidade de fluorescência diminuída com o aumento da concentração de Pd NSs (Fig. S6). Esses resultados indicam que Pd NSs podem consumir radicais • OH em vez de gerá-los. Portanto, semelhante ao comportamento catalítico relatado de nanopartículas de ferritina-platina [30], o desempenho catalítico de nossos Pd NSs foi independente da formação do radical • OH.
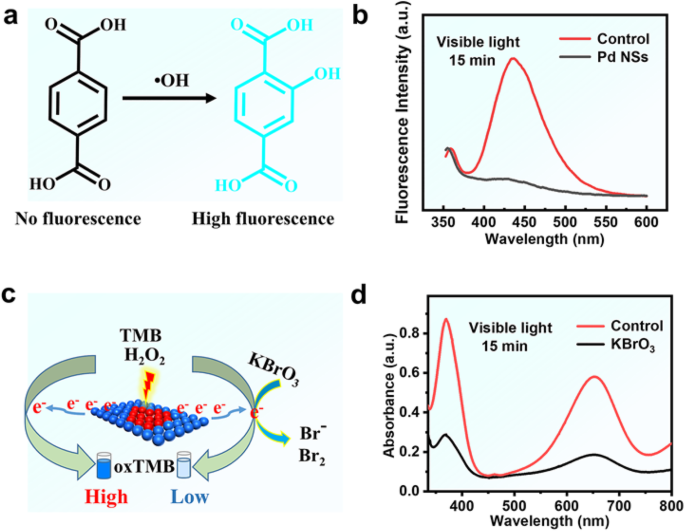
a Diagrama do mecanismo do ácido tereftálico (TA) capturando radicais hidroxila (• OH). Espectros de amostras contendo tampão fosfato (0,1 M, pH 4), H 2 O 2 (50 mM), e iluminação de luz visível ( λ ≥ 400 nm, 15 min). b Os espectros de emissão de fluorescência na presença de Pd NSs (12,6 μg / mL) e TA (66,7 μM). c Diagrama do mecanismo do KBrO 3 capturando eletrônicos quentes. d O espectro de absorção na presença de Pd NSs (12,6 μg / mL), KBrO 3 (0,3 mg / mL) e TMB (0,7 mM)
Para investigar se o mecanismo catalítico de Pd NSs se relaciona com a formação de elétrons quentes pela luz, também exploramos o experimento de captura de elétrons quentes de espécies ativas durante a reação fotocatalítica (Fig. 4c) [31]. Como pode ser visto na Fig. 4d, a capacidade catalítica de Pd NSs em relação à oxidação de TMB diminui significativamente em 15 min pela adição de 0,3 mg / mL de KBrO 3 (um supressor de e - ) Que diferença enorme entre o KBrO 3 / sistema de reação e sistema puro revelam que a presença de elétrons quentes pode ser crítica para a oxidação de TMB. Isso está de acordo com os resultados da Fig. S7 que os Pd NSs têm um amplo pico de absorção através do efeito SPR na faixa espectral de 500-1000 nm [25]. Além disso, uma vez que os elétrons quentes se afastaram da superfície dos Pd NSs, há buracos correspondentes deixados em sua superfície. Uma vez que esses orifícios podem oxidar o etanol para produzir acetaldeído, eles também podem ter uma poderosa capacidade de oxidação em direção ao TMB. Como esperado, sem a adição de H 2 O 2 , mais oxTMB foi criado sob a iluminação de luz visível.
Em seguida, testamos se as espécies reativas de oxigênio foram formadas pela ativação de O 2 sob luz visível, incluindo superóxido (O 2 - ) Diante disso, experimentos controlados foram realizados em diferentes ambientes. Para a Fig. S8, o desempenho catalítico de enzimas miméticas não muda significativamente quando somos introduzidos nitrogênio e oxigênio com saturação do sistema de reação, respectivamente, o que não é consideravelmente afetado pelo O 2 para a atividade fotocatalítica de Pd NSs. É essencial ressaltar que o desempenho final do Pd NSs, mesmo até 0,051 a.u./min por 5 min sob luz visível, foi 3,2 vezes maior do que o dos catalisadores Pd NSs no escuro (Fig. 2d). A atividade extremamente alta da nanozima Pd sob luz visível leva a uma hipótese de que a existência de elétrons quentes pelo efeito SPR de Pd NSs promovendo a formação de intermediários de reação O * em vez de radical livre é responsável por uma atividade semelhante à peroxidase (Fig. 5a ) [28]. Em resumo, o experimento de captura de espécies ativas e o experimento de ventilação fornecem um suporte robusto para o mecanismo enzimático mimético fotocatalítico de Pd NSs.
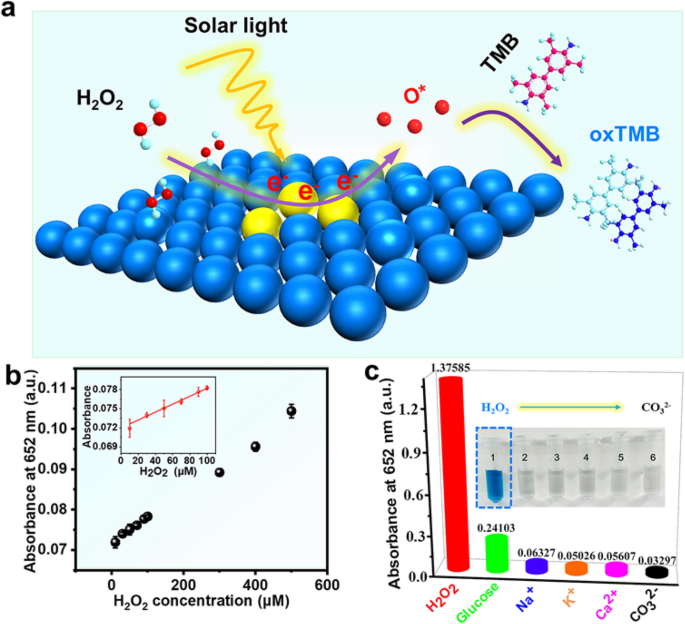
a Diagrama esquemático de um sensor para H 2 O 2 detecção. b Curva dose-resposta de diferentes concentrações de peróxido de hidrogênio. Condições experimentais:nanozima Pd (25,2 μg / mL), tampão de fosfato (0,1 M, pH 4) e iluminação de luz visível TMB (0,7 mM) ( λ ≥ 400 nm, 3 min). Inserção:gráficos de calibração linear. c Interferência de outras impurezas na absorção de H 2 O 2 sensor colorimétrico a 652 nm. Condições experimentais:nanozima Pd (25,2 μg / mL), tampão fosfato (0,1 M, pH 4), TMB (0,7 mM), iluminação de luz visível ( λ ≥ 400 nm, 15 min), e incluindo 50 mM H 2 O 2 , Glicose 200 mM, Na + , K + , Ca 2 + e CO 3 2− , e a inserção mostra as mudanças de cor das soluções de reação
Um novo sensor em tempo real e altamente sensível
Isso foi demonstrado em vários estudos que a introdução de luz no sensor como uma entrada de energia externa pode melhorar o desempenho do sensor [22, 32, 33]. Por exemplo, Ling et al. [32] descobriu que O 2 propriedades de detecção de 10 at. % LaOCl-SnO 2 sensor foi significativamente melhorado pela iluminação de luz ultravioleta. Considerando a influência significativa da luz no sensor e a excelente atividade mimetizadora da peroxidase de Pd NSs sob luz visível em nossos experimentos, um sensor colorimétrico sensível e eficaz H 2 O 2 foi construído. O mecanismo do sensor (Fig. 5a) mostra que Pd NSs pode fazer uso total de sua grande área de superfície específica para capturar fótons e gerar um grande número de elétrons quentes. Depois disso, o elétron quente promove a decomposição de H 2 O 2 para produzir intermediários de reação O *, que podem oxidar TMB a oxTMB azul. Finalmente, a detecção eficiente de H 2 O 2 foi realizado.
Como pode ser visto na inserção da Fig. 5b, o intervalo linear do H 2 construído O 2 sensor por nós foi de 10 a 100 μM, e o cálculo do limite de detecção foi de 13,40 μM (LOD =3 s / k , onde s e k representam os blocos de calibração linear do desvio padrão relativo e inclinação de oito medições de controle paralelo, respectivamente. Neste trabalho, s =2,97988 × 10 −4 , k =6,67 × 10 −5 ) Portanto, o sensor de peróxido de hidrogênio baseado em Pd NSs foi superior a outros nanomateriais relatados sob a condição de introdução de luz. Da Tabela S2, pode-se ver que com o mesmo método colorimétrico para detectar peróxido de hidrogênio, nosso sensor mostra uma ampla faixa de linearidade [34]. E o limite de detecção era menor do que muitos sensores baseados em miméticos de peroxidase baseados em Fe ou Co (Tabela S3) [35, 36]. Finalmente, realizamos H 2 O 2 e uma série de experimentos de controle (Fig. 5c) com potenciais interferências, como K + , glicose, Na + , CO 3 2− e Ca 2+ . Conforme mostrado na inserção da Fig. 5c, é óbvio que a absorvância dessas interferências é fraca a 652 nm e a cor não muda. Com base em nossos resultados, um sensor de peróxido de hidrogênio eficiente e altamente específico com base na luz visível foi realizado com sucesso. Este sensor não só faz uso total da luz visível para melhorar seu desempenho de detecção, mas também fornece um bom exemplo para outros metais plasmônicos no sensor.
Conclusões
Em resumo, demonstramos um exemplo emocionante de aplicação de nanofolhas de Pd ultrafinas (Pd NSs) como um mimetizador de peroxidase altamente eficiente e controlável por luz, devido a uma alta densidade de sítios ativos na superfície das nanofolhas e propriedade óptica única de SPR. Com a irradiação de luz visível, os elétrons quentes gerados a partir de nanofolhas de Pd via efeito SPR podem subsequentemente decompor H 2 O 2 para produzir intermediários O *. Sob irradiação de luz visível, tais nanozimas exibiram atividade semelhante à peroxidase muito maior do que no escuro. Esse sistema ativado por luz foi posteriormente usado para o biossensor aprimorado de H 2 O 2 . O conceito básico apresentado aqui, baseado na geração de eletricidade quente por meio do efeito SPR nas nanozimas Pd fotoativadas, pode contribuir para o projeto de sistemas de enzimas artificiais inteligentes ou mais eficientes e oferecer muitas novas oportunidades para a indústria química e biotecnologia.
Disponibilidade de dados e materiais
Todos os dados gerados ou analisados durante este estudo estão incluídos neste artigo publicado.
Abreviações
- Pd NSs:
-
Nanofolhas Pd
- Ag:
-
Prata
- Au:
-
Ouro
- Pt:
-
Platina
- Pd:
-
Paládio
- SPR:
-
Ressonância de plasmon de superfície
- TEM:
-
Microscopia eletrônica de transmissão
- HRTEM:
-
TEM de alta resolução
- XRD:
-
Difração de raios X
- HRP:
-
Peroxidase de rábano
- Km:
-
Michael é constante
- O 2 - :
-
Superóxido
Nanomateriais
- Atividade de elétrons em reações químicas
- Nanozimas
- Prevendo a toxicidade do desacoplamento de ácidos orgânicos
- Nanopartículas de FePO4 biocompatíveis:entrega de drogas, estabilização de RNA e atividade funcional
- Preparação e atividade de hidrogenação catalítica aprimorada de nanopartículas de Sb / Palygorskite (PAL)
- Efeitos sinérgicos de nanopartículas de Ag / BiV1-xMoxO4 com atividade fotocatalítica aprimorada
- Síntese e atividade de oxidação de CO de 1D óxido binário misto CeO2-LaO x catalisadores de ouro suportados
- Síntese de um vaso de nanoplacas Cu2ZnSnSe4 e sua atividade fotocatalítica orientada por luz visível
- Fabricação, Caracterização e Atividade Biológica de Sistemas de Nanotransmissão de Avermectina com Diferentes Tamanhos de Partículas
- Atividade fotocatalítica do nanocompósito ternário de atapulgita-TiO2-Ag3PO4 para degradação de Rodamina B sob irradiação solar simulada



